一种靶向脂质体药物递送系统及其制备方法和应用
1.本发明属于药物制剂领域,具体涉及一种靶向脂质体纳米药物递送系统,所述药物递送系统可用于淋巴管畸形的靶向缓释治疗。
背景技术:
2.淋巴管畸形是淋巴系统的先天性发育畸形,病变可压迫气道、食道等重要部位,严重影响患者的健康及生存质量。针对淋巴管畸形,目前临床一线疗法为硬化治疗,具有操作安全、适用范围广泛等优势。但单纯局部注射博来霉素等硬化剂,药物在病变部位滞留时间短、有效利用率低;若提高注射剂量,会造成肺纤维化等严重副作用。另外,儿童硬化治疗前需全身麻醉,多次重复治疗会对儿童的成长发育造成损伤。因此,亟需一种新型硬化剂药物递送系统以解决传统硬化治疗药效低、毒副作用大的问题。
3.纳米材料是药物传递系统研发的热点。纳米载体的粒径为10
‑
1000 nm,小分子治疗药物包裹在纳米粒子内部或吸附在其表面,通过主动靶向或被动运输到病变部分实现药物的靶向缓释。纳米载药系统的突出优势在于:通过靶向分子与细胞表面特异性受体结合,实现药物的靶向运输;实现药物缓释,延长药物在病变部位的作用时间,延长药物体内半衰期;有效降低小分子药物的毒副作用。
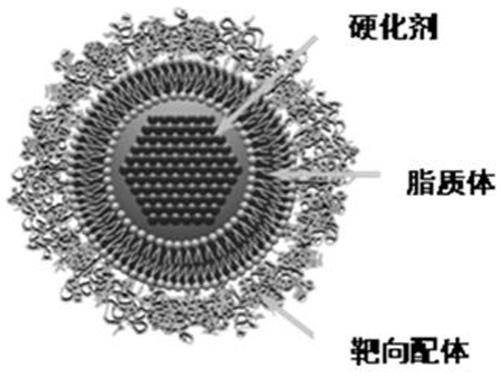
4.脂质体是磷脂依靠疏水缔合作用形成双分子层结构的球形囊泡,结构上类似生物膜双分子层,具有两亲性。脂质体结构上自我封闭,能够分别或者同时包载水溶性和脂溶性物质,脂溶性分子包载在脂质体双层膜中间,水溶性分子包载在脂质体最内部,并可防止药物降解。此外,在脂质体表面还可以进行靶向修饰,用于脂质体的靶向药物呈递。相比于其他载药系统,脂质体具有生物相容性好,体内可降解等优势,可以实现药物在病变组织的靶向缓释,有效提高药物利用率,降低毒副作用。
5.脂质体作为一种保护和递送药物的载体在临床诊疗方面得到了广泛的关注,目前主要集中应用于肿瘤治疗领域,在淋巴管畸形硬化治疗中的应用尚未见报道。相比于血液循环系统,淋巴系统液体流动速率较慢,淋巴管内皮细胞间隙较大,管壁具有很强的通透性,小分子药物更容易自由扩散到周围组织和血液循环系统中。基于纳米载体应用于淋巴系统中的尺寸优势和临床淋巴管畸形硬化治疗的迫切需求,本发明提供一种利用脂质体包载硬化剂得到药物递送系统,并将其应用于淋巴管畸形硬化治疗,有望解决目前临床硬化治疗药效低、毒副作用大等问题。
技术实现要素:
6.为解决淋巴管畸形传统硬化治疗药效低、毒副作用大的问题,本发明首次提出一种用于淋巴管畸形硬化治疗的脂质体药物递送系统。所述药物递送系统使用配体靶向脂质体包载活性药物,利用脂质体作为药物递送载体实现药物靶向释放。
7.本发明通过以下技术方案实现上述目的:第一方面,本发明提供一种靶向脂质体药物递送系统,其特征在于,所述药物递送
系统由靶向配体修饰的脂质体包载硬化剂组成,所述靶向配体为透明质酸。
8.所述硬化剂选自鱼肝油酸钠、明矾、平阳霉素(pym)、博来霉素(blm)、乙醇胺、泛影酸、喹啉、四环素、强力霉素、脲素中的一种或两种以上的组合。
9.优选的,所述硬化剂选自平阳霉素和/或博来霉素。
10.所述脂质体膜材为卵磷脂、胆固醇、二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
靶向配体。
11.优选的,所述卵磷脂、胆固醇、二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
靶向配体质量比为(30
‑
32):(7
‑
9):1。
12.所述硬化剂在药物递送系统中的质量百分比为3
‑
6%。
13.所述脂质体药物递送系统的平均粒径为50
‑
440 nm,优选的,所述脂质体药物递送系统的平均粒径为90
‑
200 nm。
14.优选的,在所述靶向脂质体药物递送系统中硬化剂药物包封率为75
‑
95%。
15.第二方面,本发明提供一种靶向脂质体药物递送系统的制备方法,所述方法包括如下步骤:(1)将靶向配体溶解,加入edc和nhs活化,滴加二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
nh2混悬液,反应过夜,透析,得到二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
靶向配体;(2)将卵磷脂、胆固醇和硬化剂溶于氯仿和/或甲醇溶液中,旋转蒸发去除溶剂,加入步骤(1)制备的二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
靶向配体和水化液,60
‑
62 ℃水化1
‑
2 h,超声处理,通过多孔聚碳酸酯滤膜挤压,得到脂质体药物递送系统。
16.优选的,所述步骤(1)中靶向配体为透明质酸,透明质酸与edc和nhs的质量比为1:2:(2.5
‑
3),透明质酸与二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
nh2的质量比为1: (2
‑
2.5)。
17.优选的,所述步骤(2)中脂质体膜材卵磷脂、胆固醇和二硬脂酰磷脂酰乙醇胺
‑
聚乙二醇
‑
靶向配体的质量比为(30
‑
32):(7
‑
9):1,硬化剂相对于脂质体膜材的占比为3
‑
6%。
18.优选的,所述步骤(2)中挤压方式为依次通过450
‑
50 nm孔径的滤膜进行梯度挤压。更优选的,所述挤压方式为依次通过450 nm、200 nm和100 nm孔径的滤膜,或者依次通过450 nm、200 nm孔径的滤膜。在本发明的最优选实施方式中,所述挤压方式为依次通过450 nm、200 nm和100 nm孔径的滤膜。
19.所述步骤(2)中的水化液为磷酸盐缓冲液或无水乙酸钠和无水氯化钙的混合液。
20.第三方面,本发明提供一种靶向脂质体药物递送系统在制备预防和/或治疗脉管畸形药物中的应用,所述脉管畸形选自静脉畸形、微静脉畸形、淋巴管畸形、动静脉畸形中的一种或两种以上的组合。
21.优选的,所述脉管畸形为淋巴管畸形。
22.本发明中靶向配体之所以选择透明质酸的原因在于:透明质酸(hyaluronic acid, ha)是一种组织相容性良好的高分子粘多糖。在生物体内,ha 是细胞外基质(extracellular matrixc,ecm)的重要组分,可以促进细胞的迁移和增殖等过程。有多个研究表明,淋巴管内皮细胞高表达淋巴管内皮透明质酸受体(lymphatic vessel endothelial hyaluronic acid receptor 1, lyve
‑
1)。在前期工作中,发明人收集临床淋巴管畸形患者组织样本,进行淋巴管内皮细胞原代培养,免疫荧光成像观测到lyve
‑
1在淋巴管内皮细胞和淋巴管畸形病变组织中大量表达。因此,利用ha对载药脂质体进行修饰,有望实现药物在淋巴管畸形病变组织中的靶向运输。发明人在试验中还发现,淋巴管内皮细
nps。
29.实施例4制备原料及方法同实施例1,区别仅在于脂质体挤出过程,具体是将探头超声处理后的混悬液依次通过450nm、200nm、100nm和50nm的聚碳酸酯膜各进行挤压20遍,得到ha
‑
blm
‑
lip nps。
30.blm
‑
lip nps的制备称取卵磷脂(spc)120 mg,胆固醇(cho)30 mg,博来霉素6 mg 于单口瓶中,加入氯仿溶剂 10 ml,超声使其充分溶解,置于旋转蒸发仪中将溶剂蒸出,加入 3 ml(ph=7.4)pbs缓冲溶液和 2 ml dspe
‑
peg的pbs溶液(2 mg/ml)后在 60 ℃水浴条件下水化 1 h,对悬液进行探头超声处理;并且依次通过孔径为450nm、200nm和100nm的聚碳酸酯膜各进行挤压20遍,得到ha
‑
blm
‑
lip nps。
31.效果实施例1、ha
‑
blm
‑
lip nps的表征将本发明实施例1
‑
4制备的ha
‑
blm
‑
lip nps和blm
‑
lip nps通过透射电子显微镜确定脂质体递药系统的形貌、尺寸和单分散性;并且通过动态光散射(dynamic light scattering, dls)方法确认其水合粒径。如图2所示,实施例1
‑
4制备得到的ha
‑
blm
‑
lip nps溶液呈乳白色,水合粒径分别为440.8
±ꢀ
50.13 nm 、187
±ꢀ
34.60 nm 、95.2
ꢀ±ꢀ
22.49 nm、50
±ꢀ
10.33 nm。如图3所示,透射电镜下实施例3制备得到的ha
‑
blm
‑
lip nps呈球状,粒径分布较为均一,分散性良好。其他实施例制备得到的脂质体递药系统形貌和分散性与实施例3相似,为了节省篇幅,说明书附图中不一一呈现。
32.、ha
‑
blm
‑
lip nps药物包封率检测博来霉素包封率=(w1/w2)
×
100%,其中w1为透析后脂质体悬浮液中博来霉素的测定量,w2为透析前脂质体悬浮液中博来霉素测定的量。
33.脂质体悬浮液中博来霉素含量测定方法:收集等体积的透析前后的脂质体,加入适量的甲醇充分破坏脂质体,使用hplc测定透析前后溶液中博来霉素的峰面积,用标准品所得线性回归曲线换算得到相应的含量值。博来霉素hplc检测条件:c18色谱柱,以乙腈:ddh2o=3:1为流动相,流速为1.0ml/min。
34.通过以上方法检测到本发明实施例1
‑
4制备得到的ha
‑
blm
‑
lip nps中博来霉素的包封率为75.8%、80.2%、93.7%、91.8%。
35.、ha
‑
blm
‑
lip nps体外细胞结合实验ha
‑
blm
‑
lip nps@cy5.5的制备:取3 ml上述制备的ha
‑
blm
‑
lip nps悬浊液加入50 μl cy5.5染料(5 mg/ml),在振荡器上振荡2 h。
36.blm
‑
lip nps@cy5.5的制备:取3 ml上述制备的blm
‑
lip nps悬浊液加入50 μl cy5.5染料(5 mg/ml),在振荡器上振荡2 h。
37.取对数生长期的淋巴管内皮细胞接种于直径为15 mm细胞共聚焦皿中,1
×
105细胞/皿,在培养箱中培养24小时。以博来霉素浓度计,用egm完全培养基稀释ha
‑
blm
‑
lip nps@cy5.5或blm
‑
lip nps@cy5.5至博来霉素浓度为1 μg/ml,并分别与淋巴管内皮细胞进行孵育。37℃孵育4 h后用pbs 冲洗3
‑
5次,在荧光显微镜下观测荧光脂质体与细胞结合情况。结果如图5所示,a图荧光强度明显高于b图(白色箭头所指),说明与blm
‑
lip nps相比,
ha
‑
blm
‑
lip nps与细胞结合率更高。主要因为淋巴管内皮细胞高表达的透明质酸受体(lyve
‑
1),使得ha对于淋巴管内皮细胞有特异性结合能力,淋巴管内皮细胞对ha
‑
blm
‑
lip nps的摄取量更高,说明ha
‑
blm
‑
lip nps具有主动靶向淋巴管内皮细胞的效果。
38.、不同粒径的ha
‑
blm
‑
lip nps体外细胞治疗实验将对数生长期的淋巴管内皮细胞接种于96孔细胞培养板中,1
×
104细胞/孔,置于培养箱中培养24小时。设置实验组和对照组共5组,以博来霉素浓度计,用egm完全培养基将实施例1
‑
4制备的ha
‑
blm
‑
lip nps配置成浓度为1μg/ml的溶液作为实验组药物;用egm完全培养基将博来霉素配置成浓度为1μg/ml的溶液作为对照组药物。待淋巴管内皮细胞于96孔板培养贴壁后实验组分别加相应粒径的ha
‑
blm
‑
lip nps溶液200μl,对照组加博来霉素溶液200μl进行孵育,4 h后弃掉培养基继续培养。分别在0、2、4、12、24 h检测细胞存活率。
39.结果如图6所示,整体来看,0
‑
4 h,博来霉素对照组(blm)细胞存活率低于ha
‑
blm
‑
lip nps实验组,说明此时对照组的治疗效果更好一些。4h 后ha
‑
blm
‑
lip nps组细胞存活率更低,细胞治疗效果更好。因为0
‑
4h内,游离博来霉素直接作用于淋巴管内皮细胞发挥治疗效果,而脂质体递药系统中博来霉素被包覆其中,需要一个释放过程,说明本发明制备的ha
‑
blm
‑
lip nps具有缓慢释放博来霉素的效果,才使得0
‑
4h内游离博来霉素的细胞治疗效果更好。4h后对照组的博来霉素被洗去,对照组基本失去治疗效果。而实验组的ha
‑
blm
‑
lip nps由于内吞作用进入细胞,随着博来霉素的缓慢释放,ha
‑
blm
‑
lip nps组细胞存活率显著下降。上述实验结果证明使用ha
‑
blm
‑
lip nps治疗效果优于单纯博来霉素治疗,ha
‑
blm
‑
lip nps对细胞治疗作用更持久,能有效提高细胞硬化治疗疗效。
40.对比ha
‑
blm
‑
lip nps实验组在24h的细胞存活率,实施例3制备的ha
‑
blm
‑
lip nps在24 h细胞存活率最低,说明实施例3制备的脂质体细胞治疗效果优于其他粒径。其次是实施例2,实施例1制备的脂质体在24h时细胞存活率最高。说明不同粒径的脂质体对细胞治疗效果存在差异,粒径过小或过大都不利于脂质体细胞治疗,实施例3中通过450nm、200nm和100nm的膜制备得到的脂质体细胞治疗效果最好。后续以此实施例进行在体治疗实验及体外细胞结合实验。
41.、ha
‑
blm
‑
lip nps对于淋巴管畸形小鼠体内治疗实验淋巴管畸形小鼠模型的构建:将弗氏不完全佐剂体积比1:1稀释于pbs溶液(ph7.3,0.1 m;1:1v/v),再向注射液中加入200 μl浓度为1 nm的vegf
‑
c蛋白,在balb/c雌性小鼠左侧颈部皮下注射200μl注射液;15天后在相同位置重复注射。随后观察8周,待颈部皮下有明显的透明或半透明囊性病变形成。如图7所示,a图表示在第6周时,小鼠颈部已经出现明显囊性病变,对病变区域进行组织切片,b图证明囊性病变为淋巴管畸形。如图8所示,在第8周时将小鼠病变区域暴露,可见小鼠颈部病变区域进一步增大。
42.以博来霉素浓度计,用生理盐水将实施例3制备的ha
‑
blm
‑
lip nps配置成浓度为1mg/ml的溶液作为实验组药物;用生理盐水将博来霉素配置成浓度为1mg/ml的溶液作为对照组药物。将淋巴管畸形小鼠分为2组,每组5只。实验组分别注射ha
‑
blm
‑
lip nps生理盐水溶液100 μl,对照组分别注射blm生理盐水溶液100 μl,10天后观察并记录病变部位尺寸变化。每10天进行一次治疗,直至病变消失。结果如图9所示,ha
‑
blm
‑
lip nps硬化治疗组的模型小鼠经3
‑
4次治疗后病变消失。单纯博来霉素治疗组则需要5
‑
6次重复治疗。相比于单纯博来霉素治疗,ha
‑
blm
‑
lip nps治疗可有效缩短治疗周期。
43.最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1