兼具开放大孔和全连通微通道的生物支架及其制备方法
1.本发明涉及生物支架技术领域,特别涉及兼具开放大孔和全连通微通道的生物支架及其制备方法。
背景技术:
2.兼具开放大孔和连通微通道的生物支架在组织工程和再生医学领域有着重要的应用,特别是对组织工程血管化、心肌修复和创面愈合等方面。但是制备一种结构可控兼具开放大孔和全连通的微通道生物支架目前依然是一个挑战。目前制备具有微通道的生物支架的方法主要是3d打印技术,且主要分为两类,一类是打印牺牲材料来造微通道结构;另一类是利用同轴喷头来直接打印微通道结构的生物支架。
3.在第一类方法中,通常是首先打印一种水溶性材料支架,然后在支架中灌入含有活细胞的水凝胶,待水凝胶交联后,将原打印的支架去除,形成了微通道(空心管)的结构。该方法虽然可以制备出具有全连通(层层之间微通道完全互连)的微通道结构。但是不足之处是该支架不具有开放的大孔结构和可控的外形结构,且该微通道的管壁对溶液的屏障功能比较差。
4.另外一类方法是利用同轴喷头直接3d打印出具有微通道(空心管)的支架。虽然同轴3d打印方法可以制备兼具微通道和开放大孔的孔隙率高的生物支架,但是该方法制备的微通道却是非全连通的,即层与层之间的微通道不是直接相连的,这样非全连通的微通道网络在用循环灌流细胞培养系统进行细胞培养时,很难达到单进单出的快速在整个体系进行灌注的目的。
技术实现要素:
5.本发明实施例提供了兼具开放大孔和全连通微通道的生物支架及其制备方法,旨在提供一种结构稳定、力学性能较好的兼具开放大孔和全连通微通道的生物支架,进而通过该生物支架提升体内的组织成血管能力。
6.本发明实施例提供了一种兼具开放大孔和全连通微通道的生物支架制备方法,包括:
7.将海藻酸钠溶于水基溶液中,制备得到可打印的生物材料;
8.利用3d打印的方式将所述可打印的生物材料打印为具有开放大孔的支架;
9.采用浓度为0.05mol/l~2mol/l的交联剂溶液,对所述支架浸泡1s~120s,以对所述支架进行部分交联;
10.将部分交联的支架浸泡于水基溶液中,以清除支架中未交联的生物材料,从而在支架中形成全连通的微通道结构;
11.将具备开放大孔和微通道结构的支架再次浸泡于交联剂溶液中,对支架进行完全交联,得到最终的生物支架。
12.进一步的,所述将海藻酸钠溶于水基溶液中,制备得到可打印的生物材料,包括:
13.按照重量比为20~100:80~0的比例称取海藻酸钠和配方材料并混合得到复合材料,然后按照复合材料与水基溶液重量比为6~35:94~65的比例将复合材料溶于水基溶液中,得到可打印的生物材料。
14.进一步的,所述配方材料为明胶、聚乙烯醇、甲基丙烯酸酐化明胶、胶原、透明质酸、聚乙二醇、丝素蛋白、羟甲基纤维素的一种或多种的组合;
15.所述水基溶液为去离子水、磷酸缓冲液、氯化钠水溶液、细胞培养液中的一种或多种的组合。
16.进一步的,所述制备得到可打印的生物材料之后,包括:
17.在可打印的生物材料中加入促进血管生产的生长因子。
18.进一步的,所述开放大孔的直径为0.1mm~2.5mm。
19.进一步的,所述部分交联的支架中,每根打印线表面被交联但内部未被交联。
20.进一步的,所述交联剂溶液为钙离子溶液、铜离子溶液、锰离子溶液、铁离子溶液、锶离子溶液或者锌离子溶液。
21.进一步的,所述全连通的微通道结构的直径范围为100μm~2500μm,孔壁厚度为40μm~1000μm。
22.进一步的,所述将具备开放大孔和微通道结构的支架再次浸泡于交联剂溶液中,对支架进行完全交联,得到最终的生物支架,包括:
23.利用二价阳离子交联剂溶液对支架中的海藻酸钠进行充分交联;
24.根据配方材料的成分,对支架进行紫外、edc盐酸盐和n
‑
羟基琥珀酰亚胺或者京尼平交联,得到最终的生物支架。
25.本发明实施例还提供了一种兼具开放大孔和全连通微通道的生物支架,其特征在于,采用如上任一项所述的制备方法制成。
26.本发明实施例提供了一种兼具开放大孔和全连通微通道的生物支架及其制备方法,该制备方法包括:将海藻酸钠溶于水基溶液中,制备得到可打印的生物材料;利用3d打印的方式将所述可打印的生物材料打印为具有开放大孔的支架;采用浓度为0.05mol/l~2mol/l的交联剂溶液,对所述支架浸泡1s~120s,以对所述支架进行部分交联;将部分交联的支架浸泡于水基溶液中,以清除支架中未交联的生物材料,从而在支架中形成全连通的微通道结构;将具备开放大孔和微通道结构的支架再次浸泡于交联剂溶液中,对支架进行完全交联,得到最终的生物支架。本发明实施例通过3d打印的方式为生物支架打印出开放大孔,然后对生物支架进行部分交联,以形成全连通的微通道结构,使生物支架同时具备开放大孔和全连通微通道。
附图说明
27.为了更清楚地说明本发明实施例技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
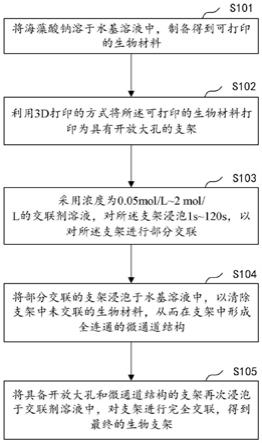
28.图1为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架制备方法流程示意图;
29.图2为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架制备方
法中铜离子的eds分布示意图;
30.图3为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架制备方法中钙离子的eds分布示意图;
31.图4为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架制备方法中铁离子的eds分布示意图;
32.图5为图2中铜离子的电子扫描图;
33.图6为图3中钙离子的电子扫描图;
34.图7为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架的结构示意图的正面电子扫描图;
35.图8为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架的结构示意图的侧面电子扫描图;
36.图7、图8中,1、微通道结构;2、开放大孔。
具体实施方式
37.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
38.应当理解,当在本说明书和所附权利要求书中使用时,术语“包括”和“包含”指示所描述特征、整体、步骤、操作、元素和/或组件的存在,但并不排除一个或多个其它特征、整体、步骤、操作、元素、组件和/或其集合的存在或添加。
39.还应当理解,在此本发明说明书中所使用的术语仅仅是出于描述特定实施例的目的而并不意在限制本发明。如在本发明说明书和所附权利要求书中所使用的那样,除非上下文清楚地指明其它情况,否则单数形式的“一”、“一个”及“该”意在包括复数形式。
40.还应当进一步理解,在本发明说明书和所附权利要求书中使用的术语“和/或”是指相关联列出的项中的一个或多个的任何组合以及所有可能组合,并且包括这些组合。
41.下面请参见图1,图1为本发明实施例提供的一种兼具开放大孔和全连通微通道的生物支架制备方法,具体包括:步骤s101~s105。
42.s101、将海藻酸钠溶于水基溶液中,制备得到可打印的生物材料;
43.s102、利用3d打印的方式将所述可打印的生物材料打印为具有开放大孔的支架;
44.s103、采用浓度为0.05mol/l~2mol/l的交联剂溶液,对所述支架浸泡1s~120s,以对所述支架进行部分交联;
45.s104、将部分交联的支架浸泡于水基溶液中,以清除支架中未交联的生物材料,从而在支架中形成全连通的微通道结构;
46.s105、将具备开放大孔和微通道结构的支架再次浸泡于交联剂溶液中,对支架进行完全交联,得到最终的生物支架。
47.本实施例中,首先利用海藻酸钠和水基溶液配置用于打印的生物材料,然后通过3d打印的方式(例如使用3d打印机)将生物材料打印为具备开放大孔的支架,接着对支架进行部分交联,即采用浓度为0.05mol/l~2mol/l的交联剂溶液,对所述支架浸泡1s~120s。
通过水基溶液将部分交联的支架中未交联的生物材料去除,形成全连通的微通道结构。再对已经具备开放大孔和全连通的微通道结构的支架进行完全交联,从而得到最终的生物支架。
48.本实施例的所述大孔的主要作用是利于体外细胞(比如成纤维细胞、成骨细胞以及干细胞等)的培养和体内新组织的长入。在形成全连通的微通道结构时,需要特别注意交联剂溶液的浓度和支架的浸泡时间,使支架处于每根打印线表面被交联但打印线内部未交联的不均匀交联状态。全连通的微通道可以是一种完全仿血管网络的结构,可以提高氧气、营养在微通道内的传输和交换。并且利用高浓度的海藻酸钠/水凝胶复合材料,可以提高微通道的管壁屏障功能,防止微通道内部的液体从管壁的泄漏。对于形成一个单进口单出口快速流体循环系统有较大的提升。同时,本实施例采用高浓度的水凝胶材料和充分的双交联对生物支架的力学性能(包括拉升强度、模量和压缩强度和模量)有较大的提升,故本实施例所述制备的生物支架能够显著的提升体内的组织成血管能力。
49.还需说明的的是,由本实施例所述的制备方法制备而成的生物支架特别适用于组织工程与再生医学血管化、创面愈合、心肌修复、骨
‑
软骨修复等方面。
50.在一实施例中,所述步骤s101包括:
51.按照重量比为20~100:80~0的比例称取海藻酸钠和配方材料并混合得到复合材料,然后按照复合材料与水基溶液重量比为6~35:94~65的比例将复合材料溶于水基溶液中,得到可打印的生物材料。
52.本实施例中,海藻酸钠与配方材料按照重量比为20~100:80~0的比例混合得到复合材料,然后将复合材料与水基溶液按照重量比为6~35:94~65的比例混合。
53.例如按照重量比为40:60的比例称取海藻酸钠和配方材料并混合得到复合材料,以及按照复合材料与水基溶液重量比为20:80的比例将复合材料溶于水基溶液中.
54.进一步的,所述配方材料为明胶、聚乙烯醇、甲基丙烯酸酐化明胶、胶原、透明质酸、聚乙二醇、丝素蛋白、羟甲基纤维素的一种或多种的组合;
55.所述水基溶液为去离子水、磷酸缓冲液、氯化钠水溶液、细胞培养液中的一种或多种的组合。
56.在一实施例中,所述制备得到可打印的生物材料混合物之后,包括:
57.在可打印的生物材料中加入促进血管生产的生长因子。
58.本实施例中,在可打印的生物材料中还可以添加一些促血管生成的生长因子,实现生长因子从支架中缓释的效果,达到更进一步的促进成血管的目的。所述生长因子可以使血小板衍生生长因子(pdgf)、血管内皮细胞生长因子(vegf)、成纤维细胞生长因子(fgf)、转化生长因子β(tgf
‑
β)、血管生成素和/或胰岛素样生长因子(igf)等。
59.在一实施例中,所述开放大孔的直径为0.1mm~2.5mm。
60.本实施例中,在打印开放大孔时,首先将生物材料装入3d打印机置的打印管中,燃装配打印喷头(型号范围32g
‑
12g),进行打印,得到具有开放大孔的支架,大孔的尺寸范围(即直径范围)可以通过3d打印机的电脑辅助(类如cad)设计在0.1mm~2.5mm。大孔的主要作用是利于体外细胞(比如成纤维细胞、成骨细胞以及干细胞等)的培养和体内新组织的长入。
61.在一实施例中,所述部分交联的支架中,每根打印线表面被交联但内部未被交联。
62.本实施例中,将支架浸泡在浓度范围为0.05mol/l~2mol/l的交联剂溶液中,浸泡时间为1s~120s,然后将支架取出,得到的支架上的每根打印线表面被交联,而打印线内部还没来得及被交联(交联剂来不及从表面扩散到内部)。此时的支架是一个每根打印线表面被交联,而内部没交联的一种不均匀交联状态。形成这种状态是制备整个完全连通微通道支架的关键所在。因此,需要精确控制交联剂溶液的浓度和浸泡时间。交联剂溶液的浓度要跟浸泡时间进行匹配,一般浓度越高,浸泡的时间要求越短。
63.如图2、图3和图4所示,交联剂元素(ca,cu,fe)在支架的打印线表面密度非常大,而在内部缺非常稀少。并且,结合图4和图5,扫描电子显微镜照片可以看出,支架的打印线的表面由于被交联,结构比较致密,但内部由于未交联而呈现多孔疏松状态。
64.在一实施例中,所述交联剂溶液为钙离子溶液、铜离子溶液、锰离子溶液、铁离子溶液、锶离子溶液或者锌离子溶液。其中,钙离子溶液可以使氯化钙、硝酸钙等溶液。另外,所述交联剂溶液也可以采用其他可交联海藻酸钠的二价阳离子溶液。
65.在一实施例中,所述全连通的微通道结构的直径范围为100μm~2500μm,孔壁厚度为40μm~1000μm。
66.本实施例中,将得到的部分交联的支架上的打印线的末端切除,然后浸泡在水基溶液中(例如去离子水或者其他水溶液),通过水基溶液将每根打印线内部未交联的材料去除,形成具有完全互联的微通道网络结构。形成的支架的微通道的孔径范围(即直径范围)在100μm
‑
2.5mm内。孔壁厚度在40μm
‑
1mm范围内。
67.需要说明的是,本实施例所述的全连通的微通道结构与所述的开放大孔的结构并不相同,所述全连通的微通道结构属于类似于一种血管网络的结构,有利于促进血管化的功能,主要用于体外内皮细胞的贴内壁培养(体外血管构建)及体内的促血管生成的目的。而所述的开放大孔主要是用于其他类型细胞(比如成纤维细胞、成骨细胞或者干细胞等)的培养和组织的长入。
68.在一实施例中,所述步骤s105包括:
69.利用二价阳离子交联剂溶液对支架中的海藻酸钠进行充分交联;
70.根据配方材料的成分,对支架进行紫外、edc盐酸盐和n
‑
羟基琥珀酰亚胺或者京尼平交联,得到最终的生物支架。
71.本实施例中,将具有大孔和全连通微通道的支架再次浸泡在二价阳离子交联剂溶液,对支架材料中的海藻酸钠进行充分交联,然后根据生物材料中的配方材料的成分,将支架进行紫外(混有gelma)、1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二亚胺/n
‑
羟基琥珀酰亚胺(edc/nhs)或者京尼平(混有明胶、胶原等)交联,最终形成结构稳定、力学性能较好的兼具开放大孔和全连通微通道的生物支架。其中,紫外交联混有gelma(甲基丙烯酸酐化明胶)、京尼平交联混有明胶、胶原等。
72.在一具体实施例中,将2g海藻酸钠溶于10g去离子水中,充分搅拌形成海藻酸钠浓度为16.7wt%(重量比)的打印水凝胶材料(即所述可打印的生物材料)。然后将可打印的生物材料装入装有18g点胶针头打印管中,利用3d打印机打印成具备开放大孔的支架,打印速度为8mm/s,打印压力为300
‑
500kpa,。将具备开放大孔的支架转移至0.1mol/l氯化铜(cucl2)溶液中进行10秒的交联,即部分交联。然后利用去离子水对部分交联的支架冲洗3次后,切除支架四边的最外列,然后将支架放于37℃去离子水中,以去除打印线条中间未交
联的部分,以形成全连通的微通道结构。当打印线内部未交联的部分去除干净后,再将支架浸泡在1mol/l的氯化钙(cacl2)溶液中,对支架进行完全交联,最终得到充分交联的兼具开放大孔和完全连通的微通道的生物支架。
73.通过光学显微镜、扫描电子显微镜、micro
‑
ct以及内部红墨水注射等手段可以证明该支架兼具开放大孔和完全连通的微通道结构。同时,微通道的尺寸(即微通道的直径)可以通过打印针头、交联时间、交联剂浓度等控制在100μm~2.5mm的范围。
74.在另一具体实施例中,将2g海藻酸钠溶于10g明胶溶液(9wt%)中,充分搅拌形成海藻酸钠浓度为16.7wt%的打印水凝胶材料(即所述可打印的生物材料)。然后将可打印的生物材料装入装有20g点胶针头打印管中,利用3d打印机打印成具备开放大孔的支架,打印速度为5mm/s,打印压力为300
‑
500kpa。然后将支架转移至0.5mol/l氯化铜(cucl2)溶液中进行5秒的部分交联,然后利用去离子水对部分交联的支架冲洗3次,切除支架四边的最外列,然后将支架放于37℃去离子水中,将打印线中间未交联的部分去除,形成全连通的微结构通道。当内部未交联的部分去除干净后,再将支架浸泡在edc/nhs中浸泡过夜,将支架中的明胶充分交联。然后再将支架浸泡在1mol/l的氯化钙(cacl2)溶液中,使支架的海藻酸钠部分充分交联,最终得到完全交联的兼具开放大孔和完全连通的微通道的海藻酸/明胶复合生物支架。
75.通过光学显微镜、扫描电子显微镜、micro
‑
ct以及内部红墨水注射等手段证明了该支架兼具开放大孔和完全连通的微通道结构。微通道的尺寸可以通过打印针头、交联时间、交联剂浓度等控制在100μm~2.5mm的范围。
76.如图7和图8所示,本发明实施例还提供了一种兼具开放大孔和全连通微通道的生物支架,采用如上所述的制备方法制成。结合图7和图8可知,该生物支架包括全连通的微通道结构1和开放大孔2,以此可以提升体内的组织成血管能力。
77.说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。对于实施例公开的系统而言,由于其与实施例公开的方法相对应,所以描述的比较简单,相关之处参见方法部分说明即可。应当指出,对于本技术领域的普通技术人员来说,在不脱离本技术原理的前提下,还可以对本技术进行若干改进和修饰,这些改进和修饰也落入本技术权利要求的保护范围内。
78.还需要说明的是,在本说明书中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的状况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1