具有消融电极和返回电极的球囊导管的制作方法
1.本发明整体涉及医疗装置,并且具体地涉及用于使用具有可膨胀框架的导管执行单极消融手术的方法和系统。
背景技术:
2.各种类型的诊断与治疗导管(诸如球囊导管)可用于标测和/或治疗应用中,诸如用于患者器官的单极消融中。
3.例如,美国专利申请公布2016/0199127描述了用于通过脾和/或颈动脉去神经来治疗全身性神经多动的工具和方法。本发明公开了用于执行消融并保护患者免于形成栓塞的装置,以及用于执行分支消融的消融单元。
4.美国专利9,925,001描述了一种肾神经消融装置,该肾神经消融装置包括具有远侧区域的细长管状构件。可膨胀构件可耦合到远侧区域。一个或多个有源电极可耦合到可膨胀构件。一个或多个接地电极可耦合到可膨胀构件。一个或多个有源电极和/或一个或多个接地电极可围绕可膨胀构件的长度螺旋地取向。
技术实现要素:
5.本文所述的本发明的实施方案提供了一种导管,该导管包括用于插入到患者的器官中的可膨胀框架、一个或多个第一电极以及第二电极。该一个或多个第一电极在一个或多个第一位置处设置在可膨胀框架上以用于放置成与器官的目标组织接触,并且被配置成执行以下操作中的一者或两者:(i)感测来自目标组织的一个或多个电信号,以及(ii)将一个或多个消融脉冲施加到目标组织。该第二电极在当一个或多个第一电极接触目标组织时不与目标组织接触的第二位置处设置在可膨胀框架的内部体积内,并且被配置成用作用于电信号的返回电极或公共电极。
6.在一些实施方案中,导管包括消融功率源,该消融功率源电连接到导管并且被配置成将一个或多个单极消融脉冲施加到一个或多个第一电极。在其他实施方案中,器官包括患者心脏,并且一个或多个电信号包括从心脏感测到的一个或多个单极心内电信号。在其他实施方案中,器官包括患者心脏,并且一个或多个消融脉冲包括施加到心脏的一个或多个单极射频(rf)消融脉冲。
7.在一个实施方案中,可膨胀框架包括可充胀球囊。在另一个实施方案中,可膨胀框架包括可膨胀篮状体。
8.根据本发明的一个实施方案,还提供了一种用于制造导管的方法,该方法包括接收用于插入到患者的器官中的可膨胀框架。用于放置成与器官的目标组织接触的一个或多个第一电极在一个或多个第一位置处设置在可膨胀框架上。用作用于电信号的返回电极或公共电极的第二电极在当一个或多个第一电极接触目标组织时不与目标组织接触的第二位置处设置在可膨胀框架的内部体积内。
9.在一些实施方案中,设置一个或多个第一电极包括在可膨胀框架中制造一个或多
个第一电极。在其他实施方案中,设置第二电极包括在处于可膨胀框架的内部体积内的第二位置处将第二电极耦合到导管轴。
10.在一个实施方案中,该方法包括在当一个或多个第一电极接触目标组织时在不与目标组织接触的第三位置处设置第三电极,该第三电极用作用于电信号的附加返回电极。在另一个实施方案中,在第三位置处设置第三电极包括将第三电极设置在可膨胀框架的内部体积之外的导管轴上。
11.结合附图,通过以下对本发明的实施方案的详细描述,将更全面地理解本发明,其中:
附图说明
12.图1为根据本发明的一个实施方案的基于导管的定位-跟踪和射频(rf)消融系统的示意性图解;
13.图2为根据本发明的实施方案的rf消融系统的导管末端的示意性图解;并且
14.图3为示意性地示出根据本发明的实施方案的用于制造包括球囊和多个电极的导管末端的流程图。
具体实施方式
15.概述
16.单极(也称为单电极)射频(rf)消融手术用于若干医疗应用中,诸如用于患者心脏的感测和消融中。大体上,医师可采集单极信号和/或使用一个或多个感测/消融电极连同可耦合到外部患者皮肤的返回电极贴片一起施加单极脉冲。然而,在该配置中,与患者心脏的目标组织接触的一个或多个感测/消融电极与返回电极之间的较大距离可(i)将噪声添加到从组织获取的单极信号,和/或(ii)对在rf消融手术期间施加到组织的单极信号具有增大的阻抗。
17.本文所述的本发明的实施方案提供了一种消融系统,该消融系统具有导管,该导管包括耦合到位于导管远侧端部处的导管末端的可膨胀框架,诸如可膨胀球囊或可膨胀篮状体,该可膨胀框架插入到患者心脏中。
18.在一些实施方案中,导管包括一个或多个感测和/或消融电极,该一个或多个感测和/或消融电极在一个或多个位置处设置在可膨胀框架上以用于放置成与心脏的目标组织接触(旨在被消融),并且被配置成执行以下操作中的一者或两者:(i)感测来自目标组织的一个或多个心内电信号,以及(ii)将一个或多个rf消融脉冲施加到目标组织。
19.在一些实施方案中,导管包括附加电极,该附加电极在当一个或多个感测和/或消融电极接触目标组织时不与目标组织接触的位置处设置在可膨胀框架的内部体积内。在此类实施方案中,附加电极被配置成用作用于电信号或所施加的脉冲的返回电极或公共电极,以便:(i)能够从心脏采集单极心内电信号,和/或(ii)使用消融电极将单极rf消融脉冲施加到目标组织。
20.在一些实施方案中,消融系统包括脉冲发生器,该脉冲发生器电连接到导管并且被配置成将rf消融脉冲施加到一个或多个消融电极。消融系统还包括处理器,该处理器被配置成接收由感测电极采集的采集的心内信号并且控制脉冲发生器以将rf消融脉冲施加
到消融电极。
21.在一些实施方案中,所公开的技术可以必要的变更用于其他应用中,例如用于肾神经的感测和消融手术或者患者的其他器官的感测和/或消融中。
22.所公开的技术,特别是设置在同一导管上的感测/消融电极和返回电极之间的接近度,通过减小消融手术中使用的消融电极和返回电极之间的阻抗来减小从患者组织采集的电信号中的噪声水平,并且改善组织消融的准确性。
23.系统描述
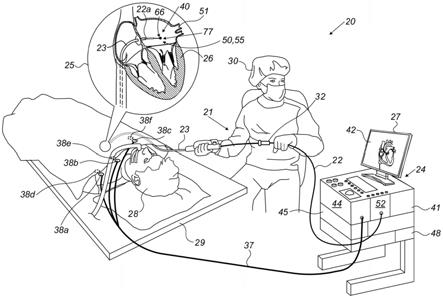
24.图1为根据本发明的一个实施方案的基于导管的定位-跟踪和射频(rf)消融系统20的示意性图解。
25.现在参考插图25。在一些实施方案中,系统20包括导管末端40,该导管末端装配在图1的全视图中所示的导管21的轴22的远侧端部22a处。
26.在一些实施方案中,导管末端40包括可膨胀框架,在本示例中,可充胀球囊66具有多个电极,诸如但不限于(i)多个感测和/或rf消融电极77,以及(ii)一个或多个电极50和55,其被配置成用作返回电极或公共电极,如将在下文详细描述的。在一些实施方案中,电极77以及电极50和55用作返回电极,以用于从心脏26中的肺静脉(pv)的口51采集单极信号,或者用于将一个或多个单极消融脉冲消融到心脏26中的口51。球囊66以及电极50、55和77在下图2中详细描述。
27.现在参见回到图1的全视图。在一些实施方案中,导管21的近侧端部连接到控制台24,该控制台包括rf发生器45以用于将单极消融脉冲施加到口51的组织。包括消融参数的消融方案存储在控制台24的存储器48中。
28.在一些实施方案中,医师30将轴22的远侧端部22a通过护套23插入到躺在工作台29上的患者28的心脏26中。医师30通过使用导管21的近侧端部附近的操纵器32操纵轴22来将轴22的远侧端部推进到心脏26中的口51(本文也称为目标位置)。在插入远侧端部22a期间,导管末端40被保持在护套23内部,以便最小化沿着到达目标位置的路径的血管创伤。
29.在一些实施方案中,系统20包括基于阻抗的有功电流定位(acl)系统,医师30可使用该系统来导航和跟踪导管末端30在心脏26中的位置。
30.在一个实施方案中,医师30通过跟踪导管末端40的位置来将轴22的远侧端部导航到目标位置。在心脏26中的远侧端部22a的导航期间,控制台24从线圈(未示出)或从被配置成用作acl系统的基于阻抗的位置传感器的任何其他元件(例如,电极50和55中的任一者)接收信号。
31.在一些实施方案中,acl系统包括多个电极38,这些电极例如经由贴附于患者28的皮肤的贴片29耦合到患者28的身体。在图1的示例中,系统10包括六个电极,其中电极38a、38b和38c耦合到患者28的前部(例如,胸部),并且电极38d、38e和38f耦合到患者28的背部。如图1所示,这些电极如下成对布置:电极38a和38d在患者28的右侧处面向彼此,电极38c和38f在患者28的左侧处面向彼此,并且电极38b和38e在患者28的胸部和背部的上部处面向彼此。
32.在其他实施方案中,系统20可包括任何合适数量的电极,这些电极以任何合适的布置耦合到患者皮肤。
33.在一些实施方案中,电极38a-38f通常经由缆线37连接到系统20的处理器41,该处
理器被配置成从电极38a-38f接收指示所测量的阻抗的电信号,并且基于所接收的信号,使用本文所述的技术来估计导管末端40在心脏26内的位置。
34.在一些实施方案中,电极38a-38f通常用于使用前述基于阻抗的acl系统和跟踪技术在患者28的体内对导管21进行导航,诸如例如在美国专利8,456,182和美国专利申请公布2015/0141798中所述的技术,这些专利的公开内容以引用方式并入本文。
35.在一些实施方案中,acl系统被配置成响应于在耦合到导管末端40的电极与电极38a-38f中的每个电极之间测量的不同阻抗来估计导管末端40的位置。
36.在一些实施方案中,处理器41被配置成估计导管末端40在心脏26中的位置,并且在控制台24的显示器27上显示覆盖在心脏26的解剖图像42(或合成模型)上的标记物(未示出)。医师30可使用该标记物来例如将导管末端40导航到口51中。
37.在一些实施方案中,一旦轴22的远侧端部22a已到达心脏26,医师30就缩回护套23,并且进一步操纵轴22以将导管末端40导航至肺静脉的口51或心脏26的任何其他目标位置。
38.在一些实施方案中,当导管末端40被放置成与组织接触时,医师30可控制系统20以用于从心脏26的目标组织采集单极心内电信号和/或用于将单极消融脉冲施加到目标组织。
39.原则上,医师30可使用耦合到患者28的皮肤外部的返回电极(在本文中也称为无关电极或中性电极)贴片来采集单极信号。类似地,医师30可使用返回电极来将一个或多个单极消融脉冲施加到心脏26的组织。返回电极可选自电极38a-38f中的任一者,或选自用于任何其他配置的电极中的电极贴片,诸如威尔逊中心电端(wilson central terminal)(wct)。基于该配置,医师30可控制rf发生器45以施加rf电流的脉冲,该rf电流要在导管末端40的电极77和耦合到患者28的皮肤外部的所选择的无关电极贴片之间传递。然而,在该配置中,电极77(与心脏26的目标组织接触)与所选择的无关电极之间的大距离可以(i)向从组织采集的单极信号添加噪声,和/或(ii)向在rf消融手术期间施加到组织的单极信号增加阻抗。
40.用以克服增加的噪声和/或增加的阻抗的技术在下文图2中详细描述。
41.处理器41通常为通用计算机,具有合适的前端部以及(a)ecg接口电路44,以用于接收来自电极38的ecg信号,和(b)电接口电路52,以用于接收来自导管21的信号,以及用于经由导管21将rf能量治疗施加于心脏26的左心房中,并用于控制系统20的其它部件。处理器41通常包括系统20的存储器48中的软件,该软件被编程为实施本文所述的功能。该软件可通过网络以电子形式被下载到计算机,例如或者其可另选地或另外地设置和/或存储在非临时性有形介质(诸如磁存储器、光存储器或电子存储器)上。
42.以举例的方式示出了系统20的该特定配置,以便示出通过本发明的实施方案解决的某些问题,并且展示这些实施方案在增强此类消融系统的性能方面的应用。然而,本发明的实施方案决不限于这种特定类别的示例性系统,并且本文所述的原理可类似地应用于其他类别的消融系统。
43.在其他实施方案中,代替球囊66,导管末端40可具有任何其他合适的部件,诸如可膨胀篮状体或任何其他合适类型的可膨胀框架。
44.使用整合在消融球囊导管中的返回电极执行单极消融
45.图2为根据本发明的实施方案的导管末端40的示意性图解。
46.在一些实施方案中,当医师30将导管末端40移动到目标位置时,耦合到导管21的导管末端40的球囊66或任何其他可膨胀框架通常处于塌缩位置,并且被配置成在目标位置处膨胀。
47.在本公开的上下文中,可膨胀框架具有塌缩位置和膨胀位置,并且特别地,球囊66具有塌缩位置和充胀位置,该充胀位置对应于可膨胀框架的膨胀位置。需注意,下文的描述涉及球囊66,但下文所述的技术可加上必要的变更应用于具有其他类型的可膨胀框架的任何导管,诸如但不限于篮形导管。
48.在一些实施方案中,球囊66具有约12mm的直径或任何其他合适的直径,并且包括设置在球囊66的表面上的电极77。在一些实施方案中,当被放置成与心脏26的组织接触时,电极77被配置成感测来自组织的心内电信号。在图2的示例中,球囊66具有多个电极77,以便获得组织中的电信号的高分辨率标测。在本示例中,导管末端40被配置成从组织采集单极心内电信号。
49.在本公开和权利要求的上下文中,针对任何数值或范围的术语“约”或“大致”指示合适的尺寸公差,该合适的尺寸公差允许部件的一部分或集合为本文所述的预期目的起作用。
50.在一些实施方案中,电极77进一步被配置成将一个或多个单极rf消融脉冲施加到组织,该一个或多个单极rf消融脉冲从rf发生器45接收并由处理器41和/或由医师30控制,如上文在图1中所述。在一些实施方案中,通过使用与组织接触的一个电极77,医师30可在经消融组织的期望位置处获得高分辨率消融(例如,形成窄消融灶)。
51.在一些实施方案中,医师30可通过控制特别是在目标位置处施加到组织的rf消融脉冲的能量和持续时间来确定消融灶的深度。
52.在一些实施方案中,导管末端40包括电极55,该电极在所选择的接近球囊66的位置处耦合到轴22,并且被配置成用作返回电极。需注意,当球囊66处于充胀位置时,一个或多个电极77被放置成与(例如,口51的)目标组织接触,但电极55被放置成与心脏26的血池接触,但不直接与目标组织接触。因此,电极55可用作返回电极,该返回电极用于感测来自目标组织的单极信号和/或用于将单极消融脉冲施加到目标组织。
53.在一些实施方案中,导管末端40可包括电极50,该电极在不被放置成与目标组织接触的位置处设置在球囊66的内部体积内,并且因此在图2中被示出为虚线元件。例如,电极50可以沿着导管末端40的轴线74耦合到轴22。在该配置中,当球囊66处于充胀位置时,一个或多个电极77被放置成与目标组织接触。然而,电极50位于球囊66的内部体积内,并且因此不被放置成与目标组织接触,而是与另一个组织(例如,心脏26的血池)或与用于使球囊66充胀的盐水溶液接触。需注意,血液和盐水溶液均为导电的,并且因此被配置成传导上述所感测的信号和/或所施加的脉冲,使得电极50以及电极55可用作如上所述的返回电极或公共电极。此外,在电极50或55与一个或多个电极77一起与目标组织接触的情况下,上述所感测的信号和/或所施加的脉冲可以是双极的,例如,在电极77和50之间或在电极77和55之间,这是不期望的,并且在一些情况下,可对心脏26造成损伤。
54.在一些实施方案中,球囊66可包括具有印刷的电互连件的柔性基板,诸如但不限于柔性印刷电路板(pcb)。在本示例中,电互连件包括与导管末端40的轴线74平行的电迹线
76和与轴线74正交的电迹线78。柔性pcb缠绕在球囊66的表面的周围,使得电迹线76和78被配置成在电极77和控制台24之间传导电信号和/或rf消融脉冲。
55.以举例的方式提供了球囊66的构型,以便示出通过本发明的实施方案解决的某些问题,并且展示这些实施方案在增强此类消融导管的导管末端的性能方面的应用。然而,本发明的实施方案决不限于这种特定类别的示例性导管末端,并且本文所述的原理可类似地应用于其他类别的消融导管。
56.在其他实施方案中,代替球囊66,导管末端40可具有任何其他合适的部件,诸如具有耦合到导管21的轴22的可膨胀框架的篮型远侧端部。在此类实施方案中,电极77可耦合到篮状体的可膨胀框架的花键,并且电极50可耦合到可膨胀框架的内部体积内的轴22。除此之外或另选地,电极55可例如在图2所示的位置处耦合到轴22。需注意,电极50和55被配置成用作用于由电极77感测的电信号的返回电极或公共电极,因此导管末端40可包括电极50和55中的仅一者。在该配置中,电极50或电极55与心脏26的血池接触,并且不被放置成与心脏26的目标组织接触。
57.制造具有返回电极的消融球囊导管
58.图3为根据本发明的实施方案的示意性地示出用于制造导管末端40的方法的流程图。该方法从基板接收步骤100开始,其中接收具有电互连件(诸如电迹线76和78)的柔性pcb。在消融电极设置步骤102处,将一个或多个消融电极77设置在柔性pcb上并且连接到电迹线76和78。在本公开的上下文和权利要求中,术语“设置”是指“形成”或“制造”(pcb中的电极77,例如使用任何合适的pcb制造工艺)或“耦合”或“附接”(使用任何合适的耦合技术,诸如但不限于焊接将电极77耦合到pcb)。
59.在返回电极耦合步骤104处,一个或多个返回电极50和55(但通常一个返回电极是足够的)在导管21的远侧端部22a处耦合到导管末端40。需注意,以举例的方式提供了电极50和55的位置,以便示出,当球囊66或任何其他合适类型的可膨胀框架处于充胀或膨胀位置时,一个或多个电极77被放置成与目标组织接触,但电极50和电极55均不被放置成与目标组织接触。在其他实施方案中,返回电极或公共电极可在任何合适的位置处耦合到可膨胀框架(例如,球囊66或前述篮状体)或在可膨胀框架中产生,使得当电极77被放置成与目标组织接触以用于感测心内电信号或用于将一个或多个消融脉冲施加到目标组织时,返回电极或公共电极不与目标组织接触,如上文图1和图2中详细描述。
60.在结束该方法的导管末端组装步骤106处,将柔性pcb缠绕在球囊66周围并耦合到该球囊(例如,使用粘结或焊接),并且将球囊66耦合到轴22的远侧端部22a,以便完成导管末端40的形成。注意,在使用上述篮状体代替球囊66的情况下,步骤106可包括将篮状体耦合到轴22的远侧端部22a,以便完成导管末端40的制造。
61.为了概念清晰起见,简化并描述了导管末端40的构造及其制造方法,以示出本发明所公开的关键特征。
62.虽然本文所述的实施方案主要涉及心脏组织的单极感测和消融,但本文所述的方法和系统也可用于其他应用中,诸如用于在患者身体的任何其他组织中执行单极感测和/或消融。
63.因此应当理解,上面描述的实施方案以举例的方式被引用,并且本发明不限于上文特定示出和描述的内容。相反,本发明的范围包括上文描述的各种特征的组合和子组合
以及它们的变型和修改,本领域的技术人员在阅读上述描述时将会想到该变型和修改,并且该变型和修改并未在现有技术中公开。以引用方式并入本专利申请的文献被视为本技术的整体部分,不同的是如果这些并入的文献中限定的任何术语与本说明书中明确或隐含地给出的定义相冲突,则应仅考虑本说明书中的定义。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1