一种细菌在制备免疫检查点抑制剂的增效剂中的应用
response in immunotherapy-refractory melanoma patients[j].science,371.以及davar d,dzutsev a k,mcc ulloch j a,et al.fecal microbiota transplant overcomes resistance to anti
–
pd-1therapy in melanoma patients[j].science,2021,371(6529):595-602.),且无毒副作用,力证了内源性肠道微生物对icis疗法的增效作用。粪菌移植成分复杂,在粪菌移植中发挥功效的是肠道微生物整体,且肠道菌群受环境,饮食及生活方式等的影响很大,无法获取持续稳定的供体粪菌来源限制了粪菌移植icis联合免疫疗法在临床中的应用。因此鉴定可标准化量化生产的成分单一的抗肿瘤肠道菌成为解决这一问题的关键。在一项最新研究中(mager lf,burkhard r,pett n,cooke nca,brown k,ramay h,paik s,stagg j,groves ra,gallo m,lewis ia,geuking mb,mccoy kd.microbiome-derived inosine modulates response to checkpoint inhibitor immunotherapy.science.2020sep 18;369(6510):1481-1489.),研究人员从icis治疗的肠癌小鼠模型中分离出三种细菌:假长双歧杆菌(bifidobacterium pseudolongum)、约氏乳杆菌(lactobacillus johnsonii)和欧陆森氏菌(olsenella species)。这3种特殊细菌分别联合免疫检查点抑制剂可在4种小鼠癌症模型中增强icis的疗效。进一步研究发现,其中假长双歧杆菌可通过其代谢产物肌苷来发挥icis的增效作用。
技术实现要素:
[0008]
本发明的目的是为了克服现有技术的上述不足,提供细菌在制备免疫检查点抑制剂的增效剂中的应用,本发明涉及一种增效免疫检查点抑制剂疗效的联合疗法,适用于一种或多种肿瘤,以及适用于所述方法的活性全细胞芬氏别样杆菌(alistipes finegoldii),其中癌症免疫治疗涉及免疫检查点抑制剂疗法,目的是增强癌症免疫治疗的抗肿瘤药效,延长癌症患者整体存活时间,提高癌症免疫治疗人群的响应率,扩大癌症免疫治疗的受益肿瘤患者人群。
[0009]
本发明给出的治疗方法,针对常规疗法的缺点:毒副作用大、易转移复发、持续时间短、生存期短、和生活质量差,有明显的改善;针对免疫检查点单药疗法的缺点:作用瘤种范围有限和药物响应人群少,有明显的改善;针对免疫检查点联合放化疗疗法的缺点:毒副作用大和药物响应人群少,有明显的改善。
[0010]
本发明给出的治疗方法针对以下患者都有很好的治疗效果:治疗不可手术,无可用靶向药物,放疗,化疗等无效的肿瘤患者;治疗单药免疫检查点抑制剂无效或耐药(原发性、适应性和获得性耐药)的肿瘤患者;治疗免疫检查点抑制剂联合放疗、化疗、靶向治疗无效或耐药(原发性、适应性和获得性耐药)的肿瘤患者。
[0011]
为了实现上述目的,本发明是通过以下方案予以实现的:
[0012]
一种细菌在肿瘤治疗上的应用。
[0013]
优选地,所述应用为作为活性成分在制备免疫检查点抑制剂的增效剂中的应用。
[0014]
优选地,所述应用为作为免疫检查点抑制剂的增效剂的应用,提高免疫检查点抑制剂治疗肿瘤的效果。
[0015]
优选地,所述细菌菌种属于别样杆菌属(alistipes),即,所述细菌菌种的16s rdna序列与别样杆菌属(alistipes)的16s rdna序列具有至少85%,至少90%,至少95%,至少96%,至少97%,至少98%,至少99%,至少99.5%或100%的一致性。
[0016]
优选地,所述属于别样杆菌属(alistipes)的细菌为一个或多个属于别样杆菌属(alistipes)的细菌的菌种或菌株的组合。
[0017]
更优选地,所述属于别样杆菌属(alistipes)细菌为芬氏别样杆菌(alistipes finegoldii)。
[0018]
进一步优选地,所述芬氏别样杆菌(alistipes finegoldii),其包含的16s rdna序列,其与芬氏别样杆菌菌种(alistipes finegoldii)的16s rdna序列具有至少99%的一致性。
[0019]
进一步优选地,所述芬氏别样杆菌(alistipes finegoldii),其包含的16s rdna序列,与芬氏别样杆菌菌株dsm17242(alistipes finegoldii dsm17242)的16s rdna序列具有至少99.5%或100%的一致性。
[0020]
再进一步优选地,所述芬氏别样杆菌(alistipes finegoldii)的一个或多个芬氏别样杆菌(alistipes finegoldii)菌株的组合。
[0021]
再进一步更优选地,所述芬氏别样杆菌(alistipes finegoldii)的菌株为美国国家生物技术中心(national center for biotechnology information,简称ncbi)基因组数据库(https://www.ncbi.nlm.nih.gov/genome/browse/#!/prokaryotes/11196/)中亚种分类的菌株名称(strain name of sub species classification)为:alistipes finegoldii dsm 17242、alistipes finegoldii d53t1_180928_d3、alistipes finegoldii 2789stdy5834947、alistipes finegoldii1001713b170207_170306_h2、alistipes finegoldii dfi.2.31、alistipes finegoldii bioml-a1、alistipes finegoldii dfi.2.16、alistipes finegoldii dfi.2.10、alistipes finegoldii aa_0143、alistipes finegoldii 2789stdy5608890、alistipes finegoldii mgbc116453、alistipes finegoldii copd076、或alistipes finegoldii ubg195中的一个或几个的组合。
[0022]
再进一步优选地,所述芬氏别样杆菌菌株为以下菌株的中的一个或几个的组合:
[0023]
保藏于德国dsm微生物和细胞培养物保藏中心,保藏号为dsm 17242的芬氏别样杆菌(ncbi:txid679935,https://www.ncbi.nlm.nih.gov/taxonomy/browser/wwwtax.cgi?id=679935);
[0024]
保藏于日本jcm菌种保藏中心(deutsche sammlung von mikroorganismen und zellkulturen=german collection of microorganisms and cell cultures),保藏号为jcm16770的芬氏别样杆菌;
[0025]
保藏于韩国kctc菌种保藏中心(korean collection for type cultures),保藏号为kctc 15236的芬氏别样杆菌;
[0026]
保藏于芬兰赫尔辛基厌氧菌参考实验室(anaerobe reference laboratory,helsinki collection,national public health institute,helsinki,finland),保藏号为ahn 2437的芬氏别样杆菌;
[0027]
保藏于瑞典ccug菌种保藏中心(culture collection university of gothenburg),保藏号为ccug46020的芬氏别样杆菌;
[0028]
保藏于法国cip菌种保藏中心(collection de l'institut pasteur of institut pasteur),保藏号为cip107999的芬氏别样杆菌。
[0029]
保藏于中国广东省微生物菌种保藏中心,保藏号为gdmcc 1.2324的芬氏别样杆菌。
[0030]
优选地,所述芬氏别样杆菌(alistipes finegoldii),其包含的16s rdna序列,其与芬氏别样杆菌菌种(alistipes finegoldii)的16s rdna序列具有至少99%的一致性,所述芬氏别样杆菌菌种(alistipes finegoldii)的16s rdna序列如seq id no:1所示。
[0031]
最优选地,所述芬氏别样杆菌细菌为保藏于dsm保藏号17242的芬氏别样杆菌(alistipes finegoldii)菌株。
[0032]
优选地,所述细菌,包括细菌活菌、细菌衍生物、或细菌代谢产物中的一种或几种。
[0033]
更优选地,同时或分别施用属于别样杆菌属(alistipes)的细菌和免疫检查点抑制剂。
[0034]
优选地,所述细菌代谢物包括细菌制备和储存过程中以及在哺乳动物胃肠道转运过程中作为细菌生长、生存、留滞、转运或存在的结果由所述细菌产生或修饰的所有分子。
[0035]
更优选地,所述细菌代谢物包括所有有机酸、无机酸、碱、蛋白质和肽、酶和辅酶、氨基酸和核酸、碳水化合物、脂质、糖蛋白、脂蛋白、糖脂、维生素、所有生物活性化合物、含有无机成分的代谢物以及所有小分子,例如含氮分子或含亚硫酸分子。
[0036]
优选地,所述细菌衍生物,包括细菌组成成分和遗传物质及其相关成分,其实例包括细菌细胞膜,菌毛,鞭毛,lps,核酸物质等来源于细菌的成分。
[0037]
优选地,所述细菌活菌为完整细菌。
[0038]
更优选地,所述细菌活菌为整活力菌。
[0039]
优选地,述治疗肿瘤为肿瘤缩小或稳定、总生存时间延长、无恶化生存期延长、生活质量改善。
[0040]
优选地,所述肿瘤为腺瘤、恶性肿瘤和腺癌,其中肿瘤按照组织来源或细胞名称分类,包括:肾上腺皮质癌、膀胱尿路上皮癌、乳腺癌、胰腺癌、宫颈癌、胆管癌、结肠癌、结直肠癌、弥漫性大b细胞淋巴瘤、多形成性胶质细胞瘤、胶质瘤、头颈癌、肾嫌色细胞癌、混合肾癌、肾癌、白血病、淋巴瘤、脑癌、肝癌、肺腺癌、肺鳞癌、间皮瘤、卵巢癌、胰腺癌、嗜铬细胞瘤、副神经节瘤、前列腺癌、直肠腺癌、肉瘤、皮肤黑色素瘤、胃癌、食管癌、睾丸癌、甲状腺癌、胸腺癌、子宫内膜癌、子宫肉瘤、葡萄膜黑色素瘤和软组织肉瘤中的一种或几种。
[0041]
在本发明的一个具体的实施例中,肿瘤为结直肠癌或黑色素瘤。
[0042]
优选地,所述肿瘤为恶性肿瘤、转移性肿瘤或非转移性肿瘤。
[0043]
优选地,在此所述肿瘤包括恶性、转移性和非转移性类型;包括癌症的任何阶段(临床分期i、ii、iii或iv,恶性肿瘤tnm分类t1-4,n0-4、或m0-1,组织学等级g1、g2、g3或g4等)
[0044]
更优选地,所述免疫检查点抑制剂为作用于t细胞负性共刺激(共抑制)分子和/或它们各自的配体的阻断剂的一种或多种的组合。
[0045]
进一步优选地,t细胞负性共刺激(共抑制)分子和/或它们各自的配体选自ctla-4、pd-1、pd-l1、pd-l2、b7-1、b7-2、b7-h3、b7-h4、b7-h6、a2ar、ido、tim-3、btla、vista、tigit、lag-3、cd40、kir、ceacam1、garp、ps、csf1r、cd94/nkg2a、tdo、tnfr、dcr3。
[0046]
再进一步优选地,所述t细胞负性共刺激(共抑制)分子的配体的阻断剂选自纳武利尤单抗(nivolumab,pd-1单抗)、伊匹单抗(ipilimumab,ctla-4单抗)、帕博利珠单抗
(pembrolizumab,pd-1单抗)、阿托珠单抗(azetolizumab,pd-l1单抗)、阿特朱单抗(atezolizumab,pd-l1单抗)、卡瑞珠丽单抗(camrelizumab,pd-l1单抗)、替雷丽珠单抗(tislelizumab,bgb-a317)、度伐利尤单抗(durvalumab,pd-l1单抗)、曲美木单抗(tremelimumab,ctla-4单抗)、斯巴达珠单抗(spartalizumab,pd-1单抗)、阿维鲁单抗(avelumab,pd-l1单抗)、信迪利单抗(sintilimab,pd-1单抗)、特瑞普利单抗(toripalimab,pd-1单抗)、西米普利单抗(cemiplimab,pd-1单抗)、mga012(retifanlimab,pd-1单抗)、mgd013(tebotelimab,pd-1/lag-3双抗)、mgd019(pd-1/ctla-4双抗)、恩比利珠单抗(enoblituzumab,b7-h3单抗)、mgd009(b7-h3单抗)、mgc018(b7-h3单抗)、medi0680(pd-1单抗)、pdr001(pd-1单抗)faz053(pd-l1单抗)、tsr022(tim-3单抗体)、mbg453(tim-3单抗)、relatlimab(bms986016,lag-3单抗)、lag525(lag-3单抗)、imp321(lag-3单抗)、regn3767(lag-3单抗)、培西达替尼(pexidartinib,csf-1r单抗)、ly3022855(csf-1r单抗)、fpa008(csf-1r单抗)、blz945(csf-1r单抗)、gdc0919(navoximod,ido单抗)、艾帕斯塔(epacadostat,ido单抗)、indoximid(ido单抗)、bms986205(ido单抗)、cpi-444(a2ar单抗)、medi9447(oleclumab,cd73单抗)、pbf509(a2ar单抗)、利瑞路单抗(lirilumab,kir单抗)或其中任意几种的组合;优选地,其中所述阻断剂选自纳武利尤单抗、帕博利珠单抗、特瑞普利单抗、信迪利单抗、西米普利单抗或其中任意几种的组合。
[0047]
更进一步优选地,所述免疫检查点抑制剂为作用于pd-1/pd-l1信号通路和/或pd-1/pd-l2信号通路的抑制剂,其中pd-1是指程序性细胞死亡蛋白1,又称cd279,pd-l1(b7-h1或cd274)和pd-l2(b7-dc或cd273)是pd-1的配体。
[0048]
再更进一步优选地,所述pd-1/pd-l1信号通路或pd-1/pd-l2信号通路的抑制剂选自纳武利尤单抗(nivolumab,pd-1单抗)、帕博利珠单抗(pembrolizumab,pd-1单抗)、阿托珠单抗(azetolizumab,pd-l1单抗)、阿特朱单抗(atezolizumab,pd-l1单抗)、卡瑞珠丽单抗(camrelizumab,pd-l1单抗)、替雷丽珠单抗(tislelizumab,bgb-a317)、度伐利尤单抗(durvalumab,pd-l1单抗)、斯巴达珠单抗(spartalizumab,pd-1单抗)、阿维鲁单抗(avelumab,pd-l1单抗)、信迪利单抗(sintilimab,pd-1单抗)、特瑞普利单抗(toripalimab,pd-1单抗)、西米普利单抗(cemiplimab,pd-1单抗)、mga012(retifanlimab,pd-1单抗)、mgd013(tebotelimab,pd-1/lag-3双抗)、mgd019(pd-1/ctla-4双抗)、medi0680(pd-1单抗)、pdr001(pd-1单抗)、faz053(pd-l1单抗)或其中任意几种的组合。
[0049]
更进一步优选地,所述免疫检查点抑制剂为作用于ctla-4/b7-1信号通路和/或ctla-4/b7-2信号通路的抑制剂,其中ctla-4是指胞毒性t淋巴细胞蛋白4,又称cd152,b7-1(cd80)和b7-2(cd86)是ctla-4的配体。
[0050]
再更进一步优选地,其可选自伊匹单抗(ipilimumab,ctla-4单抗)、曲美木单抗(tremelimumab,ctla-4单抗)、mgd019(pd-1和ctla-4双抗)或其中任意几种的组合。
[0051]
作为本发明的一个具体的实施例,所述免疫检查点抑制剂为作用于pd-1/pd-l1信号通路和/或pd-1/pd-l2信号通路的抑制剂和/或作用于ctla-4/b7-1信号通路和/或ctla-4/b7-2信号通路的抑制剂。
[0052]
具体地,所述免疫检查点抑制剂为pd-1单克隆抗体或ctla-4单克隆抗体。
[0053]
优选地,在与芬氏别样杆菌的施用同时、分别或顺序进行化学治疗,免疫治疗或放射治疗。
[0054]
优选地,所述应用的施用的对象是人类,所述人类是婴幼儿,儿童,青少年,成年人或老人。
[0055]
优选地,其中所述应用施用的对象是非人类灵长类动物,所述非人类灵长类动物是哺乳动物(例如狗、猫、雪貂、马、兔、豚鼠、沙鼠、仓鼠、灰鼠、大鼠、小鼠);鸟类;爬行动物;鱼;两栖动物;节肢动物或家畜动物(例如牛、猪、羊、山羊、羊驼、驴、骆驼、水牛或水貂)
[0056]
优选地,将所述细菌以包含所述细菌的105至10
12
个cfu(菌落形成单位)之间,或以107至10
11
cfu之间、或108至10
11
cfu之间、或109至10
11
cfu之间、或10
10
至10
11
cfu之间的剂量施用,更优选地,以包含所述细菌的109至10
11
cfu之间的剂量施用。
[0057]
本发明还要求保护以下内容:
[0058]
一种用于肿瘤治疗的试剂盒,其包含所述的免疫检查点抑制剂的一种或多种,以及权所述的细菌,并且任选地包含容器;
[0059]
或由所述的免疫检查点抑制剂的一种或多种,以及所述的细菌组成,并且任选地包含容器。
[0060]
一种细菌,其包含的16s rdna序列,与别样杆菌(alistipes)的16srdna序列具有至少85%,至少90%,至少95%,至少96%,至少97%,至少98%,至少99%,至少99.5%或100%的一致性。
[0061]
一种细菌,其特征在于,其包含的16s rdna序列,与芬氏别样杆菌(alistipes finegoldii)的16s rdna序列具有至少99%的一致性。
[0062]
一种细菌,其包含的16s rdna序列,其16s rdna序列与以下菌株的中的任意一个的16s rdna序列具有至少99.5%或100%的一致性:
[0063]
保藏于德国dsm微生物和细胞培养物保藏中心,保藏号为dsm 17242的芬氏别样杆菌(ncbi:txid679935,https://www.ncbi.nlm.nih.gov/taxonomy/browser/wwwtax.cgi?id=679935);
[0064]
保藏于日本jcm菌种保藏中心(deutsche sammlung von mikroorganismen und zellkulturen=german collection of microorganisms and cell cultures),保藏号为jcm16770的芬氏别样杆菌;
[0065]
保藏于韩国kctc菌种保藏中心(korean collection for type cultures),保藏号为kctc 15236的芬氏别样杆菌;
[0066]
保藏于芬兰赫尔辛基厌氧菌参考实验室(anaerobe reference laboratory,helsinki collection,national public health institute,helsinki,finland),保藏号为ahn 2437的芬氏别样杆菌;
[0067]
保藏于瑞典ccug菌种保藏中心(culture collection university of gothenburg),保藏号为ccug46020的芬氏别样杆菌;
[0068]
保藏于法国cip菌种保藏中心(collection de l'institut pasteur of institut pasteur),保藏号为cip107999的芬氏别样杆菌。
[0069]
保藏于中国广东省微生物菌种保藏中心,保藏号为gdmcc 1.2324的芬氏别样杆菌。
[0070]
其中保藏号为:dsm 17242的芬氏别样杆菌(alistipes finegoldii dsm17242)的16srdna序列如seq id no:1所示。
[0071]
一种制剂,其特征在于,将有效量的用于治疗肿瘤的权利要求32到33中任一项所述的细菌中的一种或多种的组合物,加入药学上可接受的载体和辅料制备成冻干粉,片剂、胶囊剂、颗粒剂或针剂。
[0072]
其中“药学上可接受的载体”是指对有机体不引起明显刺激性和不干扰所给予化合物的生物活性和性质的载体。其中“辅料”是指溶剂、稀释剂或其它赋形剂、分散剂、表面活性剂。
[0073]
一种组合物,其包含任一项中所述的细菌和药学上可接受的载体。
[0074]
一种组合物,其包含配制成用作药物的任一项中所述的细菌。
[0075]
一种组合物,其特征在于,其包含配制为用作医疗食品的任一项中所述的细菌。
[0076]
一种组合物,其特征在于,其包含两种或更多种任一项中所述的细菌菌株的混合物,并且任选地还包含药学上可接受的载体。
[0077]
一种组合物,其特征在于,其包含有效量的用于肿瘤治疗的两种或更多种任一项所述的细菌的混合物,并且还任选地包含药学上可接受的载体。
[0078]
一种组合物,其特征在于,其包含有效量的用于肿瘤治疗的两种或更多种任一项中所述的细菌的细菌活菌、细菌衍生物、或细菌代谢产物中的一种或几种组合物,并且还任选地包含药学上可接受的载体。
[0079]
一种食品、饮料、食品补充剂、益生菌或保健食品,其包含任一项中所述的细菌,被配制成制剂用于肠内营养
[0080]
一种食品、饮料、食品补充剂、益生菌或保健食品,其包含两种或更多种任一项中所述的细菌的混合物,被配制成制剂用于肠内营养。
[0081]
任一项细菌或组合物,其中所述细菌或组合物被制备成冻干粉,片剂、胶囊剂、颗粒剂或针剂。
[0082]
任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品,其特征在于,其施用对象为人类。
[0083]
优选地,其中所述人类是婴幼儿、儿童、青少年、成年人或老人。
[0084]
任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品,施用于非人类灵长类动物,所述非人类灵长类动物是哺乳动物(例如狗、猫、雪貂、马、兔、豚鼠、沙鼠、仓鼠、灰鼠、大鼠、小鼠);鸟类;爬行动物;鱼;两栖动物;节肢动物或家畜动物(例如牛、猪、羊、山羊、羊驼、驴、骆驼、水牛或水貂)。
[0085]
任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品,在肿瘤治疗中的应用。
[0086]
任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品,包含有效量的所述细菌,在肿瘤治疗中的应用。
[0087]
任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品,包含有效量的所述细菌,在肿瘤治疗中的应用,其特征在于,所述肿瘤治疗施用任一项所述的细菌、制剂、组合物、食品、饮料、食品补充剂、益生菌或保健食品。
[0088]
一种组合物,其包含用于治疗癌症的有效量的任一项细菌或组合物,并且任选地还包含药学上可接受的载体。
[0089]
一种组合物,其包含有效量的用于治疗癌症的两种或更多种中任一项细菌或组合
物,并且还任选地包含药学上可接受的载体。
[0090]
一种组合物,包括芬氏别样杆菌(alistipes finegoldii)和免疫检查点抑制剂。
[0091]
优选地,所述免疫检查点抑制剂为pd-1单克隆抗体(αpd-1)和/或ctla-4单克隆抗体(αctla4)。
[0092]
本发明还要求保护所述组合物在制备肿瘤治疗的药物中的应用。
[0093]
本发明还要求保护一种药物,包括所述的组合物,具体地,一种活性成分为芬氏别样杆菌(alistipes finegoldii)和免疫检查点抑制剂治疗肿瘤的药物组合物,
[0094]
属于别样杆菌属(alistipes)的细菌的细菌活菌、细菌衍生物、或细菌代谢产物中的一种或几种在制备免疫检查点抑制剂治疗肿瘤的增效剂中的应用。
[0095]
优选地,芬氏别样杆菌作为活性成分在制备免疫检查点抑制剂的增效剂中的应用,所述增效剂能够提高免疫检查点抑制剂治疗肿瘤的效果。
[0096]
更优选地,述芬氏别样杆菌菌株为以下菌株的中的一个或几个的组合:
[0097]
保藏于德国dsm微生物和细胞培养物保藏中心,保藏号为dsm 17242的芬氏别样杆菌(ncbi:txid679935,https://www.ncbi.nlm.nih.gov/taxonomy/browser/wwwtax.cgi?id=679935);
[0098]
保藏于日本jcm菌种保藏中心(deutsche sammlung von mikroorganismen und zellkulturen=german collection of microorganisms and cell cultures),保藏号为jcm16770的芬氏别样杆菌;
[0099]
保藏于韩国kctc菌种保藏中心(korean collection for type cultures),保藏号为kctc 15236的芬氏别样杆菌;
[0100]
保藏于芬兰赫尔辛基厌氧菌参考实验室(anaerobe reference laboratory,helsinki collection,national public health institute,helsinki,finland),保藏号为ahn 2437的芬氏别样杆菌;
[0101]
保藏于瑞典ccug菌种保藏中心(culture collection university of gothenburg),保藏号为ccug46020的芬氏别样杆菌;
[0102]
保藏于法国cip菌种保藏中心(collection de l'institut pasteur of institut pasteur),保藏号为cip107999的芬氏别样杆菌。
[0103]
保藏于中国广东省微生物菌种保藏中心,保藏号为gdmcc 1.2324的芬氏别样杆菌。
[0104]
本发明提出一种用于治疗肿瘤患者的活性全细胞芬氏别样杆菌(alistipes finegoldii),其增效免疫检查点抑制剂疗效。具体地,本发明提出一种联合疗法:将在与芬氏别样杆菌的施用同时、分别或顺序进行免疫检查点抑制治疗,从而增加免疫检查点抑制的治疗效果。
[0105]
施用芬氏别样杆菌(alistipes finegoldii)的给药方式为口服。
[0106]
施用联合疗法顺序为:在免疫检查点抑制治疗同时,之前和/或之后施用所述芬氏别样杆菌(alistipes finegoldii)。
[0107]
所述联合疗法中,根据个体患者对治疗的耐受性,根据需要执行剂量延迟和/或剂量减少以及时间调整。
[0108]
本发明中所述的芬氏别样杆菌(alistipes finegoldii)可包含有效量的通常分
散于药学上或药理学上可接受的载体中的芬氏别样杆菌(alistipes finegoldii)。
[0109]
术语“药学上或药理学上可接受的”是指当施用至动物(例如人,如果合适)时不产生不良反应、过敏反应或其他不利反应的分子实体和组合物。如本文所述的药理学上可接受的载体的具体实例是硼酸盐缓冲液或无菌盐水溶液。
[0110]
本发明中所述增效免疫检查点抑制剂,可用于免疫检查点抑制剂难治性患者,其中所述免疫检查点抑制剂难治性患者表现出对所述免疫检查点抑制剂治疗的先天性(原发性)抗性,表现为从第一剂开始持续至少约8周或12周对所述检查点抑制剂治疗的应答缺乏或应答不足。
[0111]
本发明中所述增效免疫检查点抑制剂,可用于免疫检查点抑制剂难治性患者,其中所述免疫检查点抑制剂难治性患者表现出对所述检查点抑制剂治疗的后天性(继发性)抗性,表现为对所述检查点治疗有初始应答,但一种或多种肿瘤随后复发和发展。
[0112]
本发明中所述的联合疗法的治疗效果评估,通过增加的总生存时间来测量增强的治疗效果。
[0113]
本发明中所述的联合疗法的治疗效果评估,通过增加的无进展生存期来测量增强的治疗效果。
[0114]
本发明中所述的联合疗法的治疗效果评估,其中如recist 1.1所定义,通过减少或稳定一个或多个所述肿瘤的肿瘤尺寸来测量所述增强的治疗效果,包括目标肿瘤的疾病稳定(sd)、完全缓解(cr)或部分缓解(pr);和/或一种或多种非目标肿瘤的疾病稳定(sd)或完全缓解(cr)。
[0115]
本发明中所述的联合疗法的治疗效果评估,通过改善的总缓解率和/或提升的生活质量来测量增强的治疗效果。
[0116]
本发明中所述的联合疗法的安全性评估,通过是否引发腹泻或肠炎来测量其安全性。
[0117]
与现有技术相比,本发明具有以下有益效果:
[0118]
本发明通过使用人体共生细菌单菌口服制剂,联合免疫检查点抑制剂,由细菌刺激产生的抗肿瘤免疫保护反应,显著增强免疫检查点抑制剂对多多种肿瘤的药效,且安全性更好,延长癌症患者整体存活时间,提高癌症免疫治疗人群的响应率,扩大癌症免疫治疗(免疫治疗检查点抑制剂)的受益肿瘤患者人群。
附图说明
[0119]
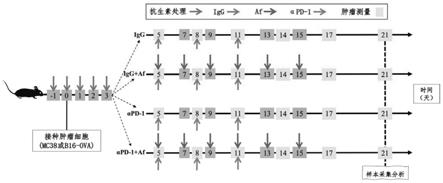
图1为实施例1的流程图。
[0120]
图2为肿瘤照片(第21天)。
[0121]
图3为肿瘤体积变化曲线。
[0122]
图4为肿瘤重量统计图。
[0123]
图5为小鼠肛门照片(第21天)
[0124]
图6为小鼠肠道组织he染色图(第21天)。
[0125]
图7为肿瘤组织免疫细胞浸润(第21天)。
[0126]
图8为小鼠的生存曲线图。
[0127]
图9为芬氏别样杆菌在不同人群中的分布及相对丰度。
具体实施方式
[0128]
下面结合说明书附图及具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
[0129]
实施例1芬氏别样杆菌联合免疫检查点抑制剂对肿瘤的治疗作用
[0130]
一、实验方法
[0131]
1、实验材料
[0132]
(1)小鼠品系:6周龄的雌性c57bl/6j小鼠
[0133]
(2)肿瘤细胞株:鼠黑色素瘤细胞系(b16-ova,atcc),鼠肠癌细胞系(mc38,atcc)
[0134]
(3)细菌制剂:芬氏别样杆菌(alistipes finegoldii,dsm no.:17242,type strain,其16s rdna序列如seq id no:1所示),简称为af,商购自dsmz德国国家培养物保藏中心,(dsmz的官方网址:http://www.dsmz.de)。
[0135]
(4)细菌培养基:液体dsmz104培养基,配方主要包括含蛋白胨,酵母提取物,牛肉提取物和葡萄糖等,商购自dsmz德国国家培养物保藏中心。
[0136]
(5)免疫检查点抑制剂:pd-1单抗(αpd-1),克隆号g4c2,试剂为上海君实生物医药科技股份有限公司赠送。
[0137]
(6)抗生素组合:甲硝唑100mg/kg,万古霉素50mg/kg,青霉素钠100mg/kg,硫酸新霉素100mg/kg
[0138]
2、实验分组
[0139]
实验分组如表1所示,
[0140]
表1:
[0141][0142]
3、实验步骤(流程如图1所示)
[0143]
(1)细菌培养:接种芬氏别样杆菌于dsmz104液体培养基,37℃厌氧箱培养18小时后离心浓度至1
×
10
10
cfu/ml。
[0144]
(2)皮下接种肿瘤细胞,mc38细胞系1
×
106/只,b16-ova细胞系5
×
105/只。
[0145]
(3)第1~3天:对各组小鼠灌胃抗生素组合清除肠道固有菌群。
[0146]
(4)分别在第5、8、11天腹腔注射igg或αpd-1,200μg/只。
[0147]
(5)分别在第5、7、9、11、13、15天,通过灌胃方式进行af活体菌液进行细菌制剂治
疗,100μl/只,1
×
109cfu/只。
[0148]
(6)分别在第5、8、11、14、17、21天测量肿瘤大小,并计算肿瘤体积。
[0149][0150]
(7)在第21天对小鼠实施安乐死,取出肿瘤组织拍照并称重,取肠道组织行he染色明确肠炎情况:
[0151]
小鼠肿瘤体积的测量,终末时间点肿瘤的重量测量,免疫组化评估肿瘤组织免疫细胞的浸润进行效果评估;
[0152]
采用小鼠肛门及肠道组织切片he染色观测评估芬氏别样杆菌是否会引发肠炎以进行安全性评估;
[0153]
二、实验结果
[0154]
图2为第21天的肿瘤。图3为肿瘤体积变化曲线及图4为肿瘤重量统计图,在mc38肠癌和b16-ova黑色素瘤小鼠模型中,相对于安慰剂治疗组(igg),单药免疫检查点抑制剂组(αpd-1)显示出明显而显著(p《0.01)的肿瘤缩减,而相对于单药免疫检查点抑制剂组(αpd-1),联合疗法组(αpd-1+af)均显示出明显而显著(p《0.01)的肿瘤缩减,证明芬氏别样杆菌具有增强αpd-1的抗肿瘤效应。芬氏别样杆菌单菌治疗组小鼠(igg+af)与安慰剂治疗组(igg)肿瘤无差别,说明芬氏别样杆菌发挥抗肿瘤作用依赖于αpd-1。
[0155]
图5小鼠的肛门照片及图6肠道组织切片he染色显示,芬氏别样杆菌单菌(igg+af)与联合疗法组(αpd-1+af)小鼠均未发现有肠炎现象,证明芬氏别样杆菌经肠胃给药的安全性。
[0156]
图7实验终点mc38小鼠模型肿瘤组织免疫组化显示,芬氏别样杆菌单菌治疗组(igg+af)能够显著增加肿瘤间质区cd4+辅助t细胞浸润,与单药免疫检查点抑制剂组(αpd-1)相比,联合疗法组(αpd-1+af)表现出增加的肿瘤间质区cd4+辅助t细胞浸润趋势,但是未达到统计学差异。与安慰剂组(igg)相比,单药免疫检查点抑制剂组(αpd-1)的小鼠实验终点的cd4+辅助t细胞浸润也只有增加的趋势,未达到统计学差异。这个结果说明,αpd-1单药治疗和联合疗法(αpd-1+af)对小鼠肿瘤组织免疫细胞浸润的影响可能是短时间的,在实验终点的肿瘤样本中无法检测出显著差异。芬氏别样杆菌单菌治疗(igg+af)对小鼠肿瘤组织免疫细胞浸润的影响持续时间较长,在治疗停止一周后仍然具有显著增高的cd4+辅助t细胞浸润,证实了芬氏别样杆菌单菌口服对系统免疫的调节作用。
[0157]
实施例2不同剂量芬氏别样杆菌联合不同免疫检查点抑制剂对总生存时间的延长
[0158]
一、实验方法
[0159]
1、实验材料
[0160]
(1)小鼠品系:6周龄的雌性c57bl/6j小鼠
[0161]
(2)肿瘤细胞株:鼠黑色素瘤细胞系(b16-ova,atcc),鼠肠癌细胞系(mc38,atcc)
[0162]
(3)细菌制剂:芬氏别样杆菌(alistipes finegoldii,dsm no.:17242,type strain,其16s rdna序列如seq id no:1所示),简称为af,商购自dsmz德国国家培养物保藏中心。
[0163]
(4)细菌培养基:液体dsmz104培养基,配方主要包括含蛋白胨,酵母提取物,牛肉
提取物和葡萄糖等,商购自dsmz德国国家培养物保藏中心。
[0164]
(5)免疫检查点抑制剂:pd-1单抗(αpd-1),克隆号g4c2,试剂为上海君实生物医药科技股份有限公司赠送。ctla4单抗(αctla4),克隆号9d9,商购自美国bioxcell。
[0165]
(6)抗生素组合:甲硝唑100mg/kg,万古霉素50mg/kg,青霉素钠100mg/kg,硫酸新霉素100mg/kg
[0166]
2、实验分组
[0167]
实验分组如表2所示,
[0168]
表2
[0169][0170]
3、实验步骤(流程如图1所示)
[0171]
(1)细菌培养:接种芬氏别样杆菌于dsmz104液体培养基,37℃厌氧箱培养18小时后离心浓度至1
×
10
10
cfu/ml。
[0172]
(2)皮下接种肿瘤细胞,mc38细胞系1
×
106/只,b16-ova细胞系5
×
105/只。
[0173]
(3)第1~3天:对各组小鼠灌胃抗生素组合清除肠道固有菌群。
[0174]
(4)从第5天开始,每3天腹腔注射igg或αpd-1或αctla4,200μg/只。
[0175]
(5)从第5天开始,每2天通过灌胃方式进行af活体菌液不同剂量的细菌制剂治疗,其中低剂量组(low)为100μl/只,1
×
109cfu/只,中等剂量组(medium)为200μl/只,2
×
109cfu/只,高剂量组(high)为400μl/只,4
×
109cfu/只。
[0176]
(6)从第5天开始,每3天测量肿瘤大小,并计算肿瘤体积。
[0177][0178]
(7)治疗周期直到小鼠肿瘤生长到伦理体积大小(2000mm3)实施安乐死或未达到肿瘤伦理体积大小而自然死亡。
[0179]
(8)记录每一只小鼠的死亡状态及时间,并绘制生存曲线图。
[0180]
二、实验结果
[0181]
图8为小鼠的生存曲线,在mc38肠癌和b16-ova黑色素瘤小鼠模型中,相对于单药免疫检查点抑制剂组(αpd-1),af高(high),中(medium)和低(low)剂量的联合疗法组(αpd-1+af)均能显著增加荷瘤小鼠的生存时间。在b16-ova黑色素瘤小鼠模型中,af还呈现出对αctla4免疫检查点抑制剂的疗效促进作用:αctla4联合高(high),中(medium)和低(low)剂量的af均能显著增加荷瘤小鼠的生存时间。而在mc38肠癌小鼠模型中,由于αctla4免疫检
查点抑制剂药效作用太强,未观察到af对αctla4的增效作用。
[0182]
实施例3芬氏别样杆菌(alistipes finegoldii)为人类的内源性肠道共生细菌
[0183]
一、实验方法
[0184]
分析了四个人类肠道宏基因组数据集,共包含1396个人类粪便样本,涉及9种不同类型的人群。宏基因组测序技术可达到人类肠道菌种水平鉴定的精度。
[0185]
9种不同类型的人群包括:1)健康成人;2)结直肠腺瘤患者;3)结直肠癌患者;4)结直肠癌术后患者;5)动脉粥样硬化性疾病患者;6)接受免疫检查点抑制剂(icis)前的非小细胞肺癌患者;7)接受免疫检查点抑制剂(icis)后的非小细胞肺癌患者;8)接受免疫检查点抑制剂(icis)前的肾癌患者的肠道菌群宏基因组学数据;9)接受免疫检查点抑制剂(icis)后的肾癌患者。
[0186]
数据集的具体情况如表3所示。
[0187]
表3人类肠道宏基因组公共数据集:
[0188][0189]
二、实验结果
[0190]
如图9和表4结果显示,芬氏别样杆菌(alistipes finegoldii)在不同的人群中均有存在,其相对丰度为0.001~0.07%,且在不同的人群芬氏别样杆菌的相对丰度存在差异,其中相对丰度是指某一个菌种占肠道全部细菌菌种的比例。按照人类肠道包含的全部细菌菌种数量约为10
14
cfu/ml的估算,芬氏别样杆菌在人类肠道的数量约为109cfu/ml~10
10
cfu/ml。
[0191]
表4芬氏别样杆菌在不同人群中的相对丰度
[0192][0193]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1