芦荟松在制备抗氧化应激损伤产品中应用
1.本发明涉及抗氧化剂领域,特别涉及芦荟松在制备抗氧化应激损伤产品中应用。
背景技术:
2.现代研究表明,人的生命活动中不断地产生自由基。一是机体内各种代谢反应产生的内源性自由基;二是由于高温、紫外线、光解、电离辐射、化学药物以及环境污染等导致生物体内有机分子共价键均裂产生的外源性自由基。自由基主要为氧自由基,氧自由基的含量约占95%,如超氧阴离子自由基(
·
o
2ˉ
)、烷氧基(ro
·
),氢过氧基(hoo
·
)、烷过氧基(roo
·
)等,另外,还存在许多虽然电子配对,但却易失去一个电子而变为自由基的含氧化合物,例如:单线态氧(激发态氧1o2)、过氧化氢(h2o2)、臭氧(o3)等这些活泼的氧自由基与具有氧自由基反应特性的其它含氧物质统称为活性氧(ros)。其次为非氧自由基,如氢自由基(h
·
)、有机自由基(r
·
)、活性氮(rns)和活性氯(rcs)等。
3.在正常的生理状况下,人体生成和消除氧自由基处在一个动态平衡,但是当机体的生成和消除自由基的动态平衡被打破,体内自由基水平增高的时候,因为自由基活泼,有极强的氧化能力,可以通过一系列的氧化反应,破坏细胞的结构与功能,使得机体产生不可逆转的氧化损伤,从而诱发多种病理损伤,如动脉粥样硬化,心血管疾病,糖尿病,肿瘤等。如果能够消除过多的氧化自由基,对于许多自由基引起的及衰老相关疾病都能够预防。所以从植物中寻找安全有效的抗氧化剂成为研究热点之一。
4.芦荟为药食两用性植物,来自百合科(liliaceae)芦荟属(aloe)多年生常绿肉质草本。芦荟具有抗炎、抗氧化、促进伤口愈合、保肝、降糖、止血、抗肿瘤和抗病毒等药理作用。传统认为蒽醌类化合物是芦荟的抗氧化活性成分。芦荟松(aloesone)是芦荟苦素的苷元,也是芦荟表皮中特有的化学成分。芦荟松在芦荟中的含量较低且相关药理活性的研究较少。
5.芦荟松结构3d图:
[0006][0007]
中文名:芦荟松,分子式c
13
h
12
o4;分子量:232.23198;英文名:aloesone;其它命名:2
‑
acetonyl
‑7‑
hydroxy
‑5‑
methylchromone(2
‑
丙酮基
‑7‑
羟基
‑5‑
甲基
‑
色酮)、2
‑
acetonyl
‑7‑
hydroxy
‑5‑
methyl
‑
chromen
‑4‑
one(2
‑
丙酮基
‑7‑
羟基
‑5‑
甲基
‑
色烯
‑4‑
酮)、2
‑
(2
‑
oxopropyl)
‑7‑
hydroxy
‑5‑
methyl
‑
4h
‑1‑
benzopyran
‑4‑
one(2
‑
(2
‑
氧丙基)
‑7‑
羟基
‑5‑
甲基
‑
4h
‑1‑
苯并吡喃
‑4‑
酮)、7
‑
hydroxy
‑5‑
methyl
‑2‑
(2
‑
oxopropyl)chromen
‑4‑
one(7
‑
羟基
‑5‑
甲基
‑2‑
(2
‑
氧丙基)色烯
‑4‑
酮)。
技术实现要素:
[0008]
鉴于此,本发明提出芦荟松在制备抗氧化应激损伤产品中应用。
[0009]
本发明的技术方案是这样实现的:
[0010]
芦荟松在制备抗氧化应激损伤产品中应用,所述芦荟松通过清除ros抑制巨噬细胞凋亡来抗氧化应激损伤。
[0011]
进一步的,所述抗氧化应激损伤产品应用于制备预防或治疗氧化应激损伤诱发疾病药物。
[0012]
进一步的,所述药物还包括药学上接受的辅料。
[0013]
与现有技术相比,本发明的有益效果是:
[0014]
本发明发现芦荟松具有直接清除活性氧的抗氧化活性,能够抑制脂多糖诱导的raw264.7细胞的活性氧(ros)生成及其介导的巨噬细胞凋亡,具有较好抗氧化应激损伤,因此可将芦荟松应用于制备抗氧化应激损伤产品,尤其是制备防治氧化应激损伤诱发疾病药物。而且相对于芦荟抗氧化活性成分蒽醌类化合物的肝毒性,色酮类化合物芦荟松具有更好的安全性,更利于制备安全性良好的抗氧化应激损伤产品。
附图说明
[0015]
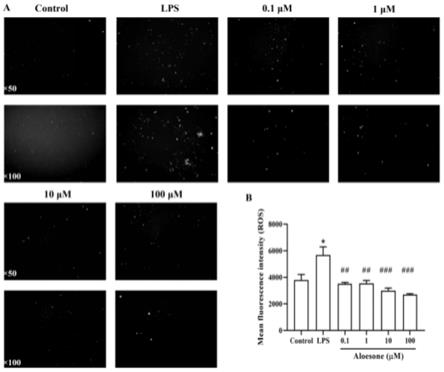
图1.芦荟松降低脂多糖诱发的巨噬细胞ros水平。
[0016]
a)各组不同物镜下dcf荧光图(
×
50,
×
100);
[0017]
b)平均荧光强度(流式细胞仪,*与正常对照组比,#与脂多糖处理组组比)
[0018]
图2.芦荟松抑制脂多糖诱发的巨噬细胞凋亡水平。
具体实施方式
[0019]
为了更好理解本发明技术内容,下面提供具体实施例,对本发明做进一步的说明。
[0020]
本发明实施例所用的实验方法如无特殊说明,均为常规方法。
[0021]
本发明实施例所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0022]
一、芦荟松合成
[0023]
1.1芦荟松合成路线
[0024][0025]
1.2芦荟松的合成方法:
[0026]
(1)3,5
‑
二羟基甲苯和乙酸和三氟化硼乙醚按摩尔比10:8:20混合,在80℃油浴下磁力搅拌反应12h。反应完毕后冷却至室温,用乙酸乙酯和水萃取,萃取三次,取乙酸乙酯层,加入到饱和nahco3溶液中,每摩尔3,5
‑
二羟基甲苯加入饱和nahco3溶液体积为1l,将混合物搅拌10min,使溶液中的乙酸反应完全。然后用乙酸乙酯和水萃取,萃取三次,取乙酸乙酯层,减压浓缩除去溶剂,得到浓缩物,加入乙酸乙酯使浓缩物溶解,再加入适量石油醚后静置重结晶,抽滤后得到化合物1
‑
1。
[0027]
(2)化合物1
‑
1、二氯甲烷和dipea(n,n
‑
二异丙基乙胺)混合,每摩尔化合物1
‑
1加入二氯甲烷体积为3.5l,化合物1
‑
1和dipea的摩尔比为1:6.5;冰浴磁力搅拌反应至0℃后,加入mem
‑
cl(2
‑
甲氧基乙氧基甲基氯),化合物1
‑
1和mem
‑
cl的摩尔比为1:1;室温下磁力搅拌反应12h。反应完毕后用乙酸乙酯和水萃取,萃取三次,取乙酸乙酯层,减压浓缩除去溶剂,得到浓缩物用柱层析(石油醚︰乙酸乙酯=6︰1,v/v)纯化得到化合物1
‑
2,即化合物c。
[0028]
(3)取化合物c、苹果酸、4
‑
二甲氨基吡啶和二氯甲烷混合,化合物c、苹果酸和4
‑
二甲氨基吡啶的摩尔比为1:1.0:1.0,化合物c和二氯甲烷的摩尔体积比mol/l为1:4.0;冰浴搅拌反应至0℃后,加入1
‑
乙基
‑
(3
‑
二甲基氨基丙基)碳二亚胺盐酸盐,25℃下搅拌反应6.0h;反应后用二氯甲烷和水萃取,取二氯甲烷层,减压浓缩除去溶剂,得到浓缩物,将浓缩物经柱层析纯化,所述柱层析的溶剂由体积比为6.0:1的石油醚和乙酸乙酯混合制得,得到化合物1
‑
3,即化合物b;
[0029]
(4)取化合物b、氢氧化钠和二甲基亚砜混合,化合物b和氢氧化钠的摩尔比为1:2.4,化合物b和二甲基亚砜的摩尔体积比mol/l为1:4.0,25℃下搅拌反应8.0h,反应后用乙酸乙酯和水萃取,取乙酸乙酯层,减压浓缩除去溶剂,得到浓缩物,将浓缩物经柱层析纯化,所述柱层析的溶剂由体积比为5.0:1的石油醚和乙酸乙酯混合制得,得到化合物1
‑
4,即化合物a;
[0030]
(5)将化合物a、氯化氢溶液和异丙醇混合,化合物a和氯化氢的摩尔比为1:4.0,异丙醇和化合物a的摩尔比为32.7:1,加热至45℃搅拌反应1.5h;反应后减压浓缩除去溶剂,得到浓缩物,将浓缩物用柱层析纯化,柱层析的溶剂由体积比为5:1的石油醚和乙酸乙酯混合制得;纯化、干燥后得到化合物1
‑
5,即目标产物芦荟松。
[0031]
芦荟松核磁数据:
[0032]
白色固体粉末,1h nmr(400mhz,d6)δ10.61(s,1h),6.62(s,1h),6.60(s,1h),6.03(s,1h),3.85(s,2h),2.65(s,3h),2.21(s,3h);
13
c nmr(100mhz,d6)δ202.87,178.22,161.09,160.62,159.27,141.65,116.70,114.39,112.92,100.58,47.58,29.89,22.48.
[0033]
二、应用试验
[0034]
1)试验方法
[0035]
1.dpph法测定芦荟松对自由基的清除率
[0036]
取dpph固体2mg溶于20ml无水乙醇中使其浓度为0.1mg/ml,超声5min,充分振摇,其吸光度在0.6
‑
1.0之间,避光保存。芦荟松用无水乙醇溶解,梯度稀释为5个浓度(2mg/ml、1mg/ml、0.5mg/ml、0.25mg/ml、0.125mg/ml)。于96孔板中每孔各加100ul不同浓度的芦荟松和dpph溶液,混匀后37℃避光孵育30min,517nm下测定孔板吸光度,同时应用抗坏血酸标准溶液作为阳性对照(0.05mg/ml)。分别以芦荟松浓度为横坐标,自由基清除率为纵坐标,绘制标准曲线并计算ic
50
。
[0037]
清除率%=[1
‑
(a1‑
a2)/a3]*100%
[0038]
a1=芦荟松与dpph的吸光度
[0039]
a2=芦荟松与乙醇的吸光度
[0040]
a3=dpph与乙醇的吸光度
[0041]
2.dcfh
‑
da法检测芦荟松对脂多糖诱导的巨噬细胞内活性氧(ros)清除作用
[0042]
巨噬细胞raw264.7采用含10%胎牛血清、100u/ml青霉素和100μg/ml链霉素高糖dmem培养基,于5%co2培养箱中37℃培养。raw264.7细胞以1.0~2.0
×
105个细胞/孔接种铺板(24孔板)24小时后应用芦荟松(0.1μm、1μm、10μm和100μm)处理2小时。随后应用lps(1μg/ml)处理24小时。实验结束后,收集细胞上清液,应用pbs清洗3次后加入1:1000稀释的dcfh
‑
da。避光并于37℃培养箱中孵育20分钟。随后pbs洗涤细胞3次,充分去除未进入细胞内的dcfh
‑
da。通过倒置荧光显微镜(zeiss x
‑
cite)进行镜下观察拍照,并应用具有fitc通道的流式细胞术测量平均荧光强度。
[0043]
3.annexin v
‑
fitc/pi检测芦荟松对脂多糖诱导的巨噬细胞凋亡的影响
[0044]
不同浓度芦荟松处理巨噬细胞后,pbs洗涤2次,应用胰酶裂解,离心收集细胞。加入500μl结合缓冲液,然后依次加入5μl annexin v
‑
fitc和pi染液,室温孵育5分钟,应用流式细胞仪(agilent novocyte)分析巨噬细胞中早期和晚期凋亡的细胞比例。
[0045]
2)试验结果
[0046]
1.芦荟松具有dpph清除活性
[0047]
dpph是一种稳定的有机自由基,在517nm处有一强吸收峰,抗氧化剂可与其单电子配对而使其吸收逐渐消失,吸光值的变化与其接受的电子数成定量关系,因而通过测定抗氧化剂对dpph的清除能力了即可表示其抗氧化性的强弱。实验结果显示,芦荟松能很好地清除dpph自由基,其ic
50
为0.73,与天然抗氧化剂茶多酚的抗氧化活性相当。
[0048]
表1.芦荟松体外dpph自由基清除活性
[0049][0050]
2.芦荟松降低脂多糖诱导的巨噬细胞ros水平
[0051]
dcfh
‑
da是一种通用的氧化应激指示剂。dcfh
‑
da本身没有荧光,可以自由穿过细胞膜,进入细胞后,可以被细胞内的酯酶水解生成dcfh(2',7'
‑
dichlorodihydrofluorescein,dcfh)。而dcfh不能通透细胞膜,从而使探针很容易被装载到细胞内。细胞内的活性氧可以氧化无荧光的dcfh生成有荧光的dcf。检测dcf的荧光以判定细胞内活性氧的水平。本研究通过dcfh
‑
da观察芦荟松对脂多糖诱导的巨噬细胞活性氧的影响。结果表明,如图1所示,与正常培养的巨噬细胞相比,脂多糖处理raw264.7细胞诱发ros积累。而芦荟松能显著降低由脂多糖诱发的raw264.7细胞ros水平,且抑制效果呈现剂量依赖性。
[0052]
3.芦荟松抑制脂多糖诱导的巨噬细胞凋亡
[0053]
细胞凋亡早期,细胞膜的不对称性消失,膜内磷脂酰丝氨酸转移到膜外,由fitc标
记的膜联蛋白(annexin v)能够与磷脂酰丝氨酸结合指示细胞凋亡早期;而另一种染色剂pi则能扩散至凋亡和坏死细胞的核内,并与dna结合,用于指示凋亡晚期。
[0054]
本研究结果表明,如图2所示,与正常巨噬细胞相比,脂多糖诱导的巨噬细胞出现较多早期和晚期凋亡细胞,而应用10μm和100μm芦荟松进行干预后能显著降低早期凋亡(43.5%和28.6%)和晚期凋亡(58.9%和47.4%)的巨噬细胞比例。
[0055]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1