一种黄体酮纳米晶注射液的制备的制作方法
1.本发明属于药物制剂领域,涉及一种黄体酮纳米晶注射液的制备的制备方法。
背景技术:
2.黄体酮(progesterone),别名孕酮、助孕素、孕烯二酮,化学名为右旋
‑
孕
‑4‑
烯
‑
3,20
‑
二酮,分子式为c
21
h3o2,其在三氯甲烷中极易溶解,在乙醇、乙醚或植物油中溶解,在水中不溶。黄体酮的熔点为128~131℃,比旋度为+186
°
~+198
°
,结构式如附图1所示。
3.随着我国全面开放三胎政策,预计未来平均每年新增的孕妈妈人数接近250万人。显然,这一政策势必涌现越来越多的高龄产妇,有研究表明,年龄是引起自然流产率增加的因素之一。高龄孕妇由于年龄较大,卵巢功能相应减退,因而妊娠流产率较高。如今市场上针对孕妇保胎、预防先兆流产、补充孕酮的普遍方法为注射黄体酮。未来,黄体酮的需求也会有增无减。
4.黄体酮在临床上有广泛应用,可用于自发性早产的预防、黄体功能不全、继发性闭经、经前期综合征的治疗,并且在赠卵、体外受精、激素替代治疗等中也发挥了重要作用。但是黄体酮溶解度和生物利用度较低,存在肝脏首过效应,用其制成的注射液刺激性大,患者顺应性差。要想制成高效、低毒的制剂产品无法通过常规的制剂技术解决。
5.近年来,学者们采用了各种方法来提高药物的溶解度,如环糊精包合、共溶剂增溶等,但均存在一定的局限性,如将药物制成环糊精包合物可能增加患者的肾脏负担,共溶剂在配伍时有药物析出和有机溶剂毒副作用等问题。黄体酮油注射剂为最常用的黄体酮制剂。肌内注射油剂,吸收完全,2
‑
8h就能达到有效的血药浓度,具有很高的生物利用度,不存在肝清除机制,是目前国内外应用最多、有效的黄体支持药物。但是上市的黄体酮注射剂采用油溶剂,由于油分子表面张力大,组织吸收慢,易造成药液在组织内堆积。长时间大剂量注射给药后易造成注射部位皮肤红肿、疼痛及产生硬结患者顺应性差。国家食品药品监督管理局(cfda)于2016年发布第178号文,要求所有黄体酮注射液生产企业对药品说明书进行修订。具体要求包括:一、【不良反应】项下增加“注射部位皮疹、瘙痒、疼痛、刺激、红肿,可形成局部硬结,严重者可发生局部无菌脓肿,也有人工性脂膜炎的病例报告”。二、【注意事项】项下増加“本品如长期大剂量应用增加局部硬结风险,偶有;发生局部无菌脓肿、人工性脂膜炎等严重的局部反应;通常形成的局部硬结、无菌脓月中的吸收恢复需较长时间”。
6.综上,研发一种以水为分散介质的黄体酮注射剂是临床所需,解决其溶解性的问题也是该领域面临的一个棘手问题。
7.纳米科学技术是20年代末崛起的一种新科技,广泛应用于药学、生物和材料合成等方面。近年来,纳米晶体技术发展迅猛,已成为药剂学领域的一个重要研究热点。纳米晶体药物即采用较少量的表面活性剂将纯的药物颗粒形成一种亚微米的胶体分散体系,不仅无需载体材料,还不受包封率的限制,药物剂量可调范围宽。纳米晶体的制备方法通常有两种,即bottom up法和top down法。纳米晶注射液可避免口服给药发生的肝脏首过作用及胃肠道灭活,减少胃肠给药的副作用;同时相比于油注射剂,又能减少给药后对注射部位造成
的不良反应,提高用药安全性,改善病人耐受性。
技术实现要素:
8.为了解决疏水性药物临床制剂的问题,本发明通过将采用top down法,即通过一定的机械力将大粒径的药物粉末粉碎成小的药物粒子,加入一些稳定剂以维持制剂的稳定,纳米晶体技术除了能增加药物的溶解度和溶出度,提高药物稳定性,还能提高药物疗效和生物利用度,同时降低毒副作用。
9.本发明的目的是通过以下方式实现的:
10.一种黄体酮纳米晶注射液,其特征是每20000ml注射液的组方为:黄体酮20g,氯化钠30g,稳定剂100
‑
300g,注射用水加至20000ml。
11.优选每20000ml注射液的组方为:黄体酮20g,氯化钠30g,稳定剂200
‑
300g,注射用水加至20000ml。
12.最优选每20000ml注射液的组方为:黄体酮20g,氯化钠30g,稳定剂200g,注射用水加至20000ml。
13.上述稳定剂为吐温80。
14.本发明黄体酮纳米结晶注射液的制备方法包括如下步骤:
15.将稳定剂加入氯化钠水溶液中于磁力搅拌器上搅拌过夜,加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
16.值得一提的是,本发明涉及的制备工艺所需设备均为业内注射液生产常用设备,实用性高。并且所用黄体酮、氯化钠和吐温80均市售可得。
17.下面就本发明的思路和稳定剂种类和用量的摸索过程,简要进行描述。
18.1、稳定剂种类的筛选
19.鉴于黄体酮api难溶于水的问题,发明人考虑大豆卵磷脂、蛋黄卵磷脂、吐温80、多库酯钠和泊洛沙姆188等作为稳定剂,同时从这些稳定剂中筛选出可用于肌肉注射的辅料,参考fda规定该辅料的使用量,进行处方的组合,比较所制得样品的粒径的分散系数。试验简述结果见表1。
20.表1五种稳定剂制得样品的粒径考察结果
21.稳定剂粒径(nm)pdirsd%大豆卵磷脂71250.884100蛋黄卵磷脂14020.98721.4吐温80284.20.2133.04多库酯钠65210.72115.8泊洛沙姆188745.10.4534.52
22.由表1可知,吐温80在相同条件下研磨时粒径可达纳米级,为284.2nm,且pdi为0.213,具有纳米混悬液的特征,其他辅料的研磨效果均不理想,很多都大于纳米级,因此处方中选择吐温80为稳定剂。
23.2、用量的筛选
24.确定稳定剂后,进一步对其用量进行优化,由于fda规定吐温80用于肌肉注射的最
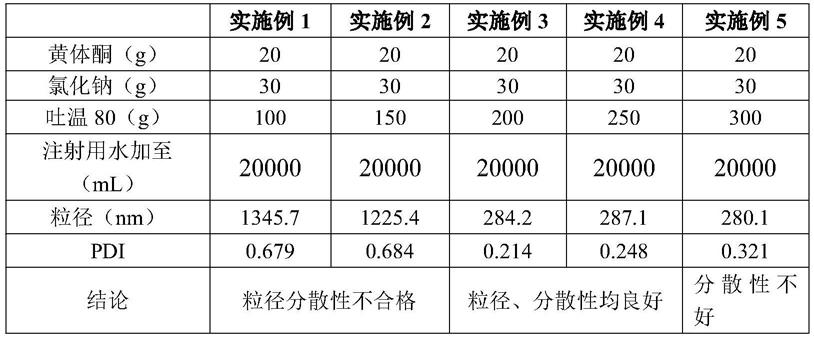
大使用量为12%(w/v),因此,先选取0.5%、0.75%、1%、1.25%和1.5%五个浓度分别质量考察,以判断合适浓度,结果如表2所示。
25.表2不同用量吐温80制备样品的质量考察结果
[0026][0027]
由表2可知,当吐温80含量增加,粒径会逐渐变小,而当含量为1%时粒径为300nm左右,继续增大吐温80的含量,粒径没有明显减小。由于吐温80有轻微溶血作用,根据注射液的特点,为尽可能减小其刺激性,应选择较低含量1%。
附图说明
[0028]
附图1黄体酮结构式。
具体实施方式
[0029]
通过下面给出的本发明的实施例,进一步阐述本发明的内容,但本发明并不受实施实例的限定。
[0030]
实施例1
[0031]
每20000ml黄体酮纳米晶注射液:
[0032]
黄体酮20g氯化钠30g吐温80200g注射用水20000ml
[0033]
将200g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0034]
实施例2
[0035]
每20000ml黄体酮纳米晶注射液:
[0036]
黄体酮20g氯化钠30g吐温80210g注射用水20000ml
[0037]
将210g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g
黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0038]
实施例3
[0039]
每20000ml黄体酮纳米晶注射液:
[0040]
黄体酮20g氯化钠30g吐温80220g注射用水20000ml
[0041]
将220g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0042]
实施例4
[0043]
每20000ml黄体酮纳米晶注射液:
[0044]
黄体酮20g氯化钠30g吐温80230g注射用水20000ml
[0045]
将230g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0046]
实施例5
[0047]
每20000ml黄体酮纳米晶注射液:
[0048]
黄体酮20g氯化钠30g吐温80240g注射用水20000ml
[0049]
将240g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0050]
实施例6
[0051]
每20000ml黄体酮纳米晶注射液:
[0052]
黄体酮20g氯化钠30g吐温80250g注射用水20000ml
[0053]
将250g吐温80,加入30g氯化钠水溶液中于磁力搅拌器上搅拌过夜,然后加入20g黄体酮搅拌成均匀的混悬液,并用c
25
分散乳化均质机搅拌,最后将药液倒入湿磨机的研磨腔(内含交联聚苯乙烯树脂)中研磨4000r 45min,注射用水加至20000ml制得。
[0054]
采用本发明的技术方案实施例1
‑
6的处方工艺,制备的产品,各项质量指标均符合规定,详细测定结果见表3。
[0055]
表3各实施例制备样品的质量考察结果
[0056][0057]
实施例6
[0058]
为了考察处方工艺的稳定性,对实施例1的三个批号进行了为期60天的粒径稳定性考察。实验结果见表4。
[0059]
表4黄体酮纳米晶注射液稳定性考察试验结果
[0060][0061][0062]
加入吐温80的实施例的3个批号,长期试验2个月,各项质量均符合规定,黄体酮粒径均可控制在300nm之间,pdi为0.2
‑
0.3左右,本发明技术方案制备的黄体酮纳米晶注射液质量稳定可控。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1