大过路黄药效物质在制备抗新冠病毒药物中的应用
1.本发明涉及药物技术领域,特别是涉及大过路黄不同溶剂提取物和单体化合物在制备抗新冠病毒药物中的应用。
技术背景
2.新冠病毒(sars-cov-2)属于单链rna正链包膜β冠状病毒,通过飞沫、接触、粪口侵入人体后,迅速攻击肺部、心脏、肾脏、肠道等多个器官,造成多器官衰竭,最后导致死亡。在sars-cov-2大流行期间,病毒基因组积累了多种突变,如voc b.1.617.2谱系(delta 变体)是高度融合并易形成合胞体的病毒株,由于p681r突变促进了弗林蛋白酶(furin)介导的刺突蛋白(s蛋白)的切割,加速了细胞
ꢀ‑
细胞的融合,促使b.1.617.对中和抗体产生抗性。
3.新冠病毒(sars-cov-2)的复制周期包括侵入、复制、组装与分泌等阶段,阻断病毒复制周期的任何阶段,都可以抑制病毒的复制,该病毒基因组包括28种编码蛋白,其中16种非结构蛋白,4种结构蛋白和8种辅助蛋白。目前已确立新冠病毒的7个药物筛选靶点分别是刺突糖蛋白(sars-cov s)、病毒受体ace2蛋白、木瓜样蛋白酶(plpro)、3-胰凝乳蛋白酶样蛋白酶(m
pro
)、介导病毒rna帽子的甲基化修饰的nsp16、病毒转录复制相关的rna聚合酶(rdrp)和潜在病毒用于干扰宿主免疫的x domain蛋白。据报道sars-cov s蛋白水解过程对病毒侵入和融合起着关键作用的肽链内切酶组织蛋白酶l(cathepsin l,catl pr)已被证明是sars-cov s蛋白酶酶解过程中关键裂解位点的相关外源基因蛋白酶,对病毒进入宿主细胞很重要的人类蛋白
‑‑‑
组织蛋白酶l(cathepsin l)是研究抗sars-cov-2 (2019-nconv)药物的有效靶点。
4.目前无抗新型冠状病毒特效药物,天然产物具有化学结构复杂性和生物活性多样性,是创新药物研究开发的重要物质来源之一。大过路黄为藤黄科金丝梅属植物,味苦、性寒,具有清热利湿解毒、疏肝通络、祛瘀止痛的功效,主治湿热淋病,肝炎,感冒,扁桃体炎,疝气偏坠,筋骨疼痛,跌打损伤,主要分布在中国陕西、贵州、四川、湖南、湖北、江苏等省。该属植物在民间具有2400年的药用历史,在欧洲民间草药治疗创伤,在德国用作抗抑郁药物已有百年的使用历史,目前未见有用于抗新冠病毒(sars-cov-2)的相关报道。
技术实现要素:
5.本发明所要解决的技术问题是提供一种大过路黄不同溶剂提取物和单体化合物在制备cathepsin l蛋白酶抑制剂抗新型冠状病毒药物中的应用,从而克服现有治疗新型冠状肺炎的有效药物稀少的缺陷,为患者提供新的药物选择。
6.为解决上述技术问题,本发明采用的技术方案如下:
7.大过路黄药效物质在制备抗新冠病毒药物中的应用。
8.上述应用中,包括大过路黄不同溶剂提取物在制备cathepsin l 蛋白酶抑制剂和治疗新型冠状病毒药物中的应用。
9.具体来说,大过路黄水提物、大过路黄30%醇提物、大过路黄60%醇提物和大过路
黄85%醇提物,具有抑制新型冠状病毒肺炎药物靶点 cathepsin l蛋白酶活性,其中大过路黄水提物、大过路黄30%醇提物、大过路黄60%醇提物和大过路黄85%醇提物抑制新型冠状病毒肺炎药物靶点cathepsin l蛋白酶活性ic
50
分别为0.21mg/ml、0.034 mg/ml、0.025mg/ml和0.03mg/ml。
10.上述应用中,还包括大过路黄中单体化合物金丝桃素、柚皮素、二氢槲皮素、槲皮苷、圣草酚、柚皮素查尔酮在制备cathepsin l蛋白酶抑制剂和治疗新型冠状病毒药物中的应用。
11.上述应用中,具体来说,大过路黄中单体化合物金丝桃素、柚皮素、二氢槲皮素、槲皮苷、圣草酚和柚皮素查尔酮在0.1mg/ml时抑制cathepsin l蛋白酶活性分别为79.4%、28.1%、18.1%、16.3%、 14.3%和22.2%。
12.有益效果:与现有技术相比,本技术的发明人经过研究发现大过路黄水提物、大过路黄30%醇提物、大过路黄60%醇提物和大过路黄 85%醇提物对新型冠状病毒肺炎药物靶点cathepsin l蛋白酶具有较好的抑制作用,大过路黄单体化合物中金丝桃素活性最强,柚皮素、二氢槲皮素、槲皮苷、圣草酚、柚皮素查尔酮对cathepsin l蛋白酶具有一定抑制性。上述所有药效物质(大过路黄不同溶剂提取物和大过路黄中单体化合物)可用于制备新型冠状病毒肺炎cathepsin l蛋白酶抑制剂和抗新型冠状病毒肺炎药物,以及用于制备预防和治疗新型冠状病毒肺炎药物,也可与其它组分复配用于制备预防和治疗新型冠状病毒肺炎的药物。
附图说明
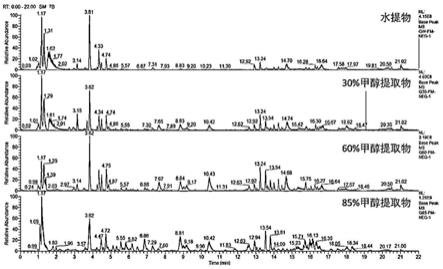
13.图1为大过路黄不同溶剂提取物uplc-hrms(negative)分析结果图;
14.图2为大过路黄不同溶剂提取物uplc-hrms(positive)分析结果图;
15.图3为rutin配体与cathpsin l蛋白的相互作用图;
16.图4为hypericin配体与cathpsin l蛋白的相互作用图;
17.图5为naringenin chalcone配体与cathpsin l蛋白的相互作用图。
具体实施方式
18.下面结合附图和实施例对本发明作进一步说明,但不作为对本发明的任何限制。
19.为了确认药物质量及验证其抗cathepsin l作用,本发明做了相关的实验如下:
20.1、大过路黄药材质量检测
21.1.1药材鉴定:实验药材于2020年08月购于贵阳花果园药材市场,经贵州中医药大学陈德媛教授鉴定为大过路黄(hypericumkouytchense l
é
vl.)和(hypericum acmosepalum n.robson)的瘤状物,样品编号:hk2020.08,实验样品存储于贵州中医药大学科研楼活性筛选实验室。
22.2、大过路黄不同溶剂提取物制备:取大过路黄粗粉200g各4份,分别加2倍体积不同溶剂(水、30%甲醇、60%甲醇和85%甲醇),回流提取三次,提取时间:1h,1h,30min。合并三次提取液,减压浓缩,低温真空干燥,制备出大过路黄水提取(hw)、大过路黄30%醇提物(h30)、大过路黄60%醇提物(h60)和大过路黄85%醇提物 (h85)。
23.3、药效评价:
24.检测仪器:synergy ii,十万分之一电子分析天平型号:ms205du (mettler totoledo瑞士)。
25.试剂盒:520cathepsin l试剂盒*fluorimetric* (cat#:as-72218,美国圣何塞anaspec);520renin试剂盒 *fluorimetric*(cat#:as-72040,美国圣何塞anaspec)。
26.受试药物:大过路黄水提取(hw)、大过路黄30%醇提物(h30)、大过路黄60%醇提物(h60)和大过路黄85%醇提物(h85)、金丝桃素、柚皮素、二氢槲皮素、槲皮苷、圣草酚等购于成都瑞芬思生物科技有限公司,经峰面积归一化,质量分数》99%,甲醇、乙腈和甲酸(色谱纯,美国fisher公司),水为超纯水。
27.阳性对照:cathpsin l inhibitor(cat#:as-72218,美国圣何塞anaspec),
28.renin inhibitor:ac-hpfv-(sta)-lf-nh2。
29.3.1.cathepsin l蛋白酶实验方法及结果:
30.测试溶液的配制(按试剂盒说明手册操作):
31.缓冲溶液:将2x实验缓冲液(component d)1m ddt(componentf)按124:1:进行混合,冰浴备用。
32.cathepsin l蛋白酶底物溶解:用2x实验缓冲液稀释底物 (component a)100倍,冰浴备用。
33.cathepsin l蛋白酶溶液:用2x实验缓冲液稀释酶(component c) 200倍,现配现用,冰浴备用。
34.cathepsin l抑制剂:用2x实验缓冲液稀释100μm的cathepsinl抑制剂(component e)100倍。
35.3.2.测定方法(按试剂盒说明手册操作):在384孔黑色平板(lot #.09818015,美国coring公司)中,先分别加入底物空白溶液 (substrate control,sc)、溶剂空白溶液(vehicle control,vc)、阳性对照(positive control,pc)、抑制剂对照(inhibitor control, ic)、测试化合物对照(test compound control,tcc),再加入 cathepsin l蛋白酶和底物。每个浓度均为3个复孔,震荡混匀后, 37℃下暖孵30分钟,经synergy ii在激发波长485nm和发射波长 535nm下测试荧光强度。
36.数据处理与分析:数据以均数标准差表示(x
±
s),通过微软 windows 2003excel软件完成统计学处理,计量资料采用stdev-t 检验计算抑制率。
37.抑制率计算公式:抑制率%=100
×
(f
vehicle-f
sample
)/f
vehicle
;式中的f为对照组和样品组荧光值。
38.3.3.renin蛋白酶活性测试:根据参考文献([wei y.,ma,c.m.,hattori, m.bioorg.med.chem.2009,17,3003.])方法,进行renin抑制剂筛选及评价。
[0039]
3.4.大过路黄不同溶剂提取物抗cathepsin l蛋白酶活性筛选结果
[0040]
大过路黄不同溶剂提取物对cathepsin l蛋白酶的抑制率(n=3)
[0041][0042][0043]
试验结果:大过路黄水提物、大过路黄30%醇提取、大过路黄60%醇提物和大过路黄85%醇提物,对病毒进入宿主细胞很重要的人类蛋白
‑‑‑‑
组织蛋白酶l(cathepsin l)抑制性ic
50
分别为0.21mg/ml, 0.034mg/ml,0.024mg/ml和0.03mg/ml,可用于制备抗新型冠状病毒的药物。
[0044]
3.5大过路黄不同溶剂提取物抗renin蛋白酶活性筛选(n=3)
[0045][0046]
3.6大过路黄不同溶剂提取物抗病毒蛋白酶选择性评价
[0047][0048]
由上表可知hk30对cathepsin l蛋白酶有较好的选择性抑制作用。
[0049]
4.活性部位化学成分定性分析
[0050]
4.1试剂:lc-ms级的乙腈、甲酸和hplc异丙醇和甲醇购于rhawnreagent co.ltd(shanghai,china,https://www.rhawn.cn/),mili-q系统超纯水(millipore,bedford,ma,
usa)。
[0051]
4.2样品预处理:大过路黄提取物(水提物,30%甲醇提取物,60%甲醇提取物,85%甲醇提取物),分别用水、50%甲醇、甲醇和异丙醇溶解,14000x g,离心10分钟,样品终浓度为10μg/μl。
[0052]
4.3检测分析:采用超高效液相色谱-高分辨质谱联用仪(uplc-hrms) 进行中药活性部位成分分析。
[0053]
仪器参数和方法设置:色谱柱为phenomenexc18 column (2.1
×
100mm,1.7μm),柱温为30℃,样品室温度为10℃,流动相a为含0.1%甲酸的超纯水,流动相b为含0.1%甲酸的乙腈。洗脱程序为0-2min,2-20%b;2-10min,20-31%b;10-13min,31-100% b;13-18min,100%b;18-19min,100-2%b;19-22min,2%b。进样量2μl,流速0.3ml/min。质谱检测采用电喷雾离子源(esi),分别采用正、负离子扫描,喷雾电压4kv,鞘气流速5arb,辅助气流速0arb。扫描模式为full mass/dd-ms2,分辨率为35,000,扫描离子范围为100-1500m/z。二级质谱分辨率为17,500,分离窗为 3.0m/z,碰撞能量为10、20、30。数据采集使用xcalibur 4.2软件。
[0054]
4.4数据分析:采用compound discoverer软件对检测所得总离子流图进行色谱峰识别,并以二维矩阵形式将结果列出。采用与mzcloud,chemspider,mass lists和mzvault数据库比对方式鉴定未知化合物。相似度结果为与mzcloud二级数据库比对而得。对与chemspider 和mass lists数据库比对结果采用mzlogic算法进行打分排序。
[0055]
4.5活性部位主要化合物(positive)
[0056][0057]
4.6活性部位主要化学成分定量分析
[0058]
4.6.1样品预处理:大过路黄提取物(水提物,30%甲醇提取物,50%甲醇提取物,100%甲醇提取物),分别用50%甲醇、50%甲醇、甲醇和甲醇溶解,14000xg,离心10分钟,样品终浓度为20μg/μl。
[0059]
4.6.2标准溶液配制:取待测标准品用甲醇配置成浓度为100、50、 25、12.5、6.25、3.12、1.56、0.78、0.39μg/ml的系列混标溶液。
[0060]
4.6.3检测分析:采用超高效液相色谱-高分辨质谱联用仪 (uplc-hrms)。仪器参数和方法设置:色谱柱为phenomenex c18 column(2.1
×
100mm,1.7μm),柱温为30℃,样品室温度为 10℃,流动相a为含0.1%甲酸的超纯水,流动相b为含0.1%甲酸的乙腈。洗脱程序为0-2min,2-20%b;2-10min,20-31%b;10-13min, 31-100%b;13-18min,100%b;18-19min,100-2%b;19-22min, 2%b。进样量为10μl,流速为0.3ml/min。锥孔电压4kv,屏蔽气流为40,保护气流为10。扫描模式为prm,碰撞能量为20、50、 80。数据采集使用xcalibur 4.2软件。
[0061]
4.6.4数据分析:使用根据已知浓度标准品构建标准曲线,获得方程 y=ax+b,其中y为峰面积,a为斜率,x为标准品浓度,b为背景常数。采用xcalibur4.2软件,对原始数据文件进行峰整合、校正,根据已知标准曲线以及活性部位中检测到的目标峰面积进行定量浓度计算。
[0062]
4.6.5酶标仪法测定金丝桃素含量
[0063]
据文献([西南国防医药,2010,20(7),720])报道,酶标仪对物质含量测定符合朗伯-比尔定律,即物质在一定波长处的吸光度与浓度之间存在线性关系,从而实现对化合物定量检测的目的。酶标仪测定具有简单,试剂用量小,速度快,耗时短,效率高的特点。酶标仪的样品池通常为聚苯乙烯制成的96孔板,该材料在400nm以上无紫外吸收,研究表明,在可见光区酶标仪是紫外分光光度计的理想替代工具。
[0064]
4.6.6仪器与试剂
[0065]
检测仪器:synergy ii,十万分之一电子分析天平型号:ms205du (mettler totoledo瑞士)。96孔板(康宁)。金丝桃素对照品(成都瑞芬思生物科技有限公司),mili-q系统超纯水(millipore,bedford,ma,usa),dmso(索莱宝,d8370),eppendorf移液器。
[0066]
4.6.7测定波长选择
[0067]
实验发现,金丝桃素在589nm处具有紫外吸收,而dmso、水和聚苯乙烯96孔板在该波长处无吸收,故选定589nm为检测波长。
[0068]
4.6.8.酶标仪方法学考察
[0069]
(1)标准曲线绘制:精密称取金丝桃素对照品,置于0.5ml离心管,精密量取dmso溶解稀释,配成0.01,0.02,0.03,0.05,0.09,0.1 和0.2mg/ml溶液,低温避光处理。在589nm处测定吸光度值,以浓度为横坐标,吸光度值为纵坐标,进行线性回归(n=3),得到回归方程为:y=4.5778x+0.004,r2=1.000。结果表明,金丝桃素在0.01
‑ꢀ
0.2mg/ml浓度范围内线性良好。
[0070]
(2)精密度实验:取同一金丝桃对照品,重复测定5次,得到的吸光度值分别为:0.285,0.291,0.285,0.287,0.301,rsd为2.74%。
[0071]
(3)重复性试验:取同一批大过路黄样品5份,按样品含量测定方法操作,结果金丝桃素平均含量为0.1%,rsd为1.86%。
[0072]
(4)加样回收率实验:精密量取9份大过路黄样品溶液(g85)25.00 μl,分别加入0.05mg/ml的金丝桃素对照品溶液25.00μl,27.00 μl,20.00μl(n=3),计算加样回收率分别为104.5%(rsd=3.21%), 98.7%(rsd=4.25%),98.4%(rsd=2.92%)。
[0073]
4.6.8酶标仪测定结果:见下表。
[0074]
nf:未发现
[0075]
[0076][0077]
※
:酶标法测定
[0078]
4.7活性部位主要化学成分定量分析结果
[0079]
研究发现,大过路黄水提物中主要含表儿茶素(82.19μg/mg)、柚皮素查尔酮(66.91μg/mg);大过路黄30%醇提物中主要含表儿茶素(124.26μg/mg)、柚皮素查尔酮(395.10μg/g)、金丝桃素(34.3μg/mg)、圣草酚(29.34μg/mg);大过路黄60%醇提物中主要含表儿茶素(114.07μg/mg)、金丝桃素(112.3μg/mg)、柚皮素查尔酮(479.23μg/mg)、圣草酚(58.86μg/mg);大过路黄 85%醇提物中主要含表儿茶素(89.54μg/mg)、柚皮素查尔酮(361.83 μg/mg)、圣草酚(51.51μg/mg)。
[0080]
5.大过路黄瘤状物不同溶剂提取物中主要化合物抗cathepsin l蛋白活性研究
[0081]
5.1大过路黄瘤状物不同溶剂提取物中主要化合物抗cathepsin l 蛋白活性筛选结果
[0082][0083]
*:在1%dmso-buffer溶液体系中,样品未完全溶解;-:未测定
[0084]
5.2大过路黄瘤状物不同溶剂提取物中主要化合物分子对接研究
[0085]
5.2.1配体的准备:使用maestro软件中ligprep模块 (release 2018-1:maestro version 11.5,l lc,new york,ny)准备化合物,opls3用来能量最小化;在 ph=7.0
±
2.0的条件下将分子离子化,并保持分子的手性。
[0086]
5.2.2蛋白的准备:从蛋白质数据库中检索到对应蛋白的晶体结构 (pdb id:3of9),利用protein preparation wizard模块准备蛋白后,设置蛋白质活性位点为对接位置
[0087]
5.2.3分子对接:采用软件中的配体对接(ligand docking)模块,在对接之后,额外的精度(xp)被用于再对接阶段,相关取舍阈值是默认的,ligand docking评分由默认的打分函数计算。
[0088]
大过路黄主要化合物计算机药物辅助设计计算结果
[0089]
5.3部分配体与cathpsin l蛋白的相互作用,见图3-5。
[0090]
下面给出本发明的几个实施例。
[0091]
实施例1:经实验验证,大过路黄水提物、大过路黄30%醇提取、大过路黄60%醇提物和大过路黄85%醇提物,对cathepsin l蛋白酶抑制性,ic
50
分别为0.21mg/ml、0.034mg/ml、0.024mg/ml和0.03 mg/ml,可用于制备抗新型冠状病毒的药物。
[0092]
实施例2:经实验验证,大过路黄中单体化合物金丝桃素、柚皮素、二氢槲皮素、槲皮苷、圣草酚和柚皮素查尔酮,在浓度为0.1mg/ml 时,对cathepsin l蛋白酶的抑制作用分别为79.4%、28.1%、18.1%、 16.3%、14.3%和22.2%,可作为潜在抗新型冠状病毒的药物
[0093]
实施例3:取上述大过路黄不同溶剂提取物和单体化合物制成颗粒剂、胶囊剂、片剂、注射剂、口服液、软胶囊剂、滴丸剂等药剂上可以接受的剂型。
[0094]
实施例4:取上述大过路黄不同溶剂提取物和单体化合物,加入其它抗病毒原料药复配,制成颗粒剂、胶囊剂、片剂、注射剂、口服液、软胶囊剂、滴丸剂等药剂上可以接受的剂型。
[0095]
以上只是本发明的具体应用范例,本发明还有其他的实施方式,凡采用等同替换或等效变换形成的技术方案,均落在本发明所要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1