一种缓释抗菌的敷料及其制备方法与流程
1.本发明属于医药技术领域,特别涉及一种缓释抗菌的敷料及其制备方法。
背景技术:
2.皮肤作为人体最大的器官,也是人体的第一道屏障,但人们在日常工作和生活中难免发生皮肤和黏膜损伤的情况。自上世纪60年代英国动物学家winter提出“湿性愈合”理念以来,传统的敷料让伤口自行结痂干燥的愈合理念因愈合周期长、易滋生细菌、不利于创面愈合,传统的敷料治疗效果已无法满足人们对皮肤损伤恢复的需求。因此许多湿性医用敷料应运而生。目前的敷料虽种类繁多,能适应大部分的创面愈合需求,但仍存抗菌效果不佳,特别是抗菌种类有限,需要频繁更换敷料,大面积深度创面应用外用药物和敷料后可并发真菌、耐药菌二重感染,需要频繁更换敷料。
3.因此,亟需一种抗菌效果佳,特别是能抗耐药菌的新型的敷料。
技术实现要素:
4.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种缓释抗菌的敷料及其制备方法,所述敷料具有缓释抗菌的效果,不仅广谱抗菌,抗菌效果好,而且对耐甲氧西林金黄色葡萄球菌(mrsa)具有很好的抗菌效果,使得皮肤伤口愈合快,愈合后伤口疤痕不明显。
5.本发明的发明构思:本发明提供的一种抗菌敷料,将抗菌物质包埋在穿心莲提取物和凝胶物质形成的凝胶状混合物中,形成的纳米级悬液渗入敷料的载体中,从而使得敷料中的抗菌物质具有缓释效果(该敷料的制备过程可称为采用纳米包埋技术制备敷料),可显著提高难溶的抗菌活性成分的水溶解度,促进抗菌活性成分透皮吸收,提高抗菌活性成分稳定性、降低抗菌活性成分的刺激性和毒副作用,显著提高抗菌活性成分的生物利用度,抗菌种类多。另外,本发明所述敷料降解性好,对耐甲氧西林金黄色葡萄球菌(mrsa)具有很好的抗菌效果。
6.本发明的第一方面提供一种缓释抗菌的敷料。
7.具体的,一种缓释抗菌的敷料,包括载体、抗菌物质、穿心莲提取物、凝胶物质。
8.优选的,所述抗菌物质包括澳洲茶树精油。澳洲茶树精油植物活性成分含4
‑
松油醇和1,8
‑
桉叶素,澳洲茶树精油是一种优良的天然抗菌剂,对人体皮肤表面的致病菌显示出了良好的杀灭作用,具有抗感染,增强机体免疫调节能力,加速创面愈合的功能。
9.优选的,所述敷料还包括乳化剂。澳洲茶树精油与乳化剂混合后,可提高抗菌物质中的抗菌活性成分的稳定性,从而可缓慢释放抗菌活性成分。
10.优选的,所述澳洲茶树精油中,按质量百分比计,4
‑
松油醇的含量为35
‑
48%,1,8
‑
桉叶素的含量不超过4.5%。
11.优选的,所述澳洲茶树精油还包括α
‑
蒎烯、桧烯、α
‑
松油烯、柠檬烯、对伞花烃、γ
‑
松油烯、异松油烯、香橙烯、喇叭烯、δ
‑
杜松烯、蓝桉醇、绿花白千层醇中的至少一种。
12.进一步优选的,所述乳化剂选自吐温80、司盘80、烷基糖苷、peg
‑
40氢化蓖麻油(聚氧乙烯醚
‑
40蓖麻油)、甘油硬脂磷酯、氢化卵磷脂、脂肪醇聚氧乙烯醚、聚山梨醇酯
‑
80中的至少一种。
13.优选的,所述凝胶物质中包括聚丙烯酰基二甲基牛磺酸铵、卡波姆、三乙醇胺、壳聚糖、壳聚糖衍生物、明胶、丙烯酸(酯)类/c10
‑
30烷醇丙烯酸酯交联聚合物中的至少一种。
14.优选的,所述载体选自棉布或老化/氧化的棉布、无纺布、纱布、涤纶、多孔有机高分子材料中的至少一种。载体规格长*宽可为10*15cm、20*25cm、40*50cm,载体需要有多孔的特点,使得敷料透气性好。
15.优选的,所述敷料还包括水。
16.优选的,所述敷料,按重量份数计,包括抗菌物质0.01
‑
25份、穿心莲提取物0.1
‑
30份、凝胶物质0.1
‑
10份。
17.优选的,所述敷料,按重量份数计,包括抗菌物质5
‑
17份、穿心莲提取物7.5
‑
20份、凝胶物质2.5
‑
7份。
18.优选的,所述敷料,按重量份数计,包括抗菌物质0.01
‑
25份、乳化剂0.1
‑
5份、穿心莲提取物0.1
‑
30份、凝胶物质0.1
‑
10份。
19.优选的,所述敷料,按重量份数计,包括抗菌物质5
‑
17份、乳化剂1
‑
3.5份、穿心莲提取物7.5
‑
20份、凝胶物质2.5
‑
7份。
20.更优选的,所述敷料,按重量份数计,由以下组分组成:抗菌物质5
‑
17份、乳化剂1
‑
3.5份、穿心莲提取物7.5
‑
20份、凝胶物质2.5
‑
7份、水余量。
21.本发明的第二方面提供一种缓释抗菌的敷料的制备方法。
22.具体的,一种缓释抗菌的敷料的制备方法,包括以下步骤:
23.(1)将穿心莲提取物、凝胶物质搅拌混合,制得凝胶状混合物;
24.(2)在搅拌凝胶状混合物的过程中,将抗菌物质滴入凝胶状混合物中,均质,制得纳米级悬液;
25.(3)将载体浸入纳米级悬液中,取出载体,制得所述敷料。
26.优选的,所述抗菌物质在滴入前先与乳化剂进行混合,优选采用超声处理进行混合。
27.优选的,步骤(1)中,将穿心莲提取物、凝胶物质和水进行搅拌混合。
28.优选的,步骤(1)中,所述搅拌混合的搅拌速度为500
‑
1200转/分钟;进一步优选的,所述搅拌混合的搅拌速度为500
‑
1100转/分钟。优选磁力搅拌器进行搅拌。
29.优选的,步骤(2)中,所述均质的过程采用高压均质机进行均质1.5
‑
5分钟,均质速度为8800
‑
9000转/分钟。
30.优选的,步骤(3)中,取出敷料时,纳米级悬液与载体之间形成饱和但不滴液状态。
31.本发明的第三方面提供含上述敷料的应用。
32.具体的,上述敷料在制备药物中的应用。
33.进一步优选的,上述敷料在制备抗菌药物中的应用。
34.更优选的,上述敷料在制备治疗皮肤损伤的药物中的应用。
35.所述敷料的缓释效果可长达24小时,在24小时以内具备良好抗菌效果。
36.相对于现有技术,本发明的有益效果如下:
37.(1)本发明提供的一种抗菌敷料,将抗菌物质包埋在穿心莲提取物和凝胶物质形成的凝胶状混合物中,形成的纳米级悬液渗入敷料的载体中,从而使得敷料中的抗菌物质具有缓释效果,在24小时以内具备良好抗菌效果,对人体安全无毒性,是一种理想的创面外用敷料。
38.(2)本发明所述敷料含澳洲茶树精油,作为抗菌物质,广谱抗菌,高渗透性。可同时抗细菌、真菌和病毒三大微生物,且对耐药菌株耐甲氧西林金黄色葡萄球菌(mrsa)有良好杀菌作用。
39.(3)本发明的敷料透气性好、生物相容性好、亲和力强、降解快,有利于皮肤创面组织细胞的更新代谢和愈合。
具体实施方式
40.为了让本领域技术人员更加清楚明白本发明所述技术方案,现列举以下实施例进行说明。需要指出的是,以下实施例对本发明要求的保护范围不构成限制作用。
41.以下实施例中所用的原料、试剂或装置如无特殊说明,均可从常规商业途径得到,或者可以通过现有已知方法得到。
42.以下实施例使用的澳洲茶树精油也称互生叶白千层(melaleuca alternifolia)叶油,可由南宁万家辉香料有限公司提供。
43.以下实施例使用的凝胶物质(卡波姆941)可由上海谱振生物科技有限公司提供,批号:zy210907。
44.实施例1:敷料的制备
45.一种缓释抗菌的敷料,按重量份数计,包括载体(棉布),澳洲茶树精油0.01份、乳化剂(吐温80)0.01份、穿心莲提取物30份、凝胶物质(聚丙烯酰基二甲基牛磺酸铵)0.1份、水69.88份。
46.上述缓释抗菌的敷料的制备方法,包括以下步骤:
47.(1)将穿心莲提取物、凝胶物质和水充分搅拌混合,搅拌速度为1000转/分钟,制得凝胶状混合物;
48.(2)在搅拌凝胶状混合物的过程中,将抗菌物质与乳化剂超声处理进行混合,得到的抗菌混合物滴入凝胶状混合物中,继续搅拌10分钟,用高压均质机进行均质3分钟,均质速度为9000转/分钟,制得纳米级悬液;
49.(3)将载体浸入纳米级悬液中,取出载体,取出敷料时,纳米级悬液与载体之间形成饱和但不滴液状态,制得敷料。
50.实施例2:敷料的制备
51.一种缓释抗菌的敷料,按重量份数计,包括载体(棉布),澳洲茶树精油5份、乳化剂(吐温80、司盘80,各0.5份)1份、穿心莲提取物20份、凝胶物质(卡波姆941和三乙醇胺,分别为9份和1份)10份、水64份。
52.上述缓释抗菌的敷料的制备方法,包括以下步骤:
53.(1)将穿心莲提取物、凝胶物质和水充分搅拌混合,搅拌速度为1000转/分钟,制得凝胶状混合物;
54.(2)在搅拌凝胶状混合物的过程中,将抗菌物质与乳化剂超声处理进行混合,得到
的抗菌混合物滴入凝胶状混合物中,继续搅拌10分钟,用高压均质机进行均质3分钟,均质速度为9000转/分钟,制得纳米级悬液;
55.(3)将载体浸入纳米级悬液中,取出载体,取出敷料时,纳米级悬液与载体之间形成饱和但不滴液状态,制得敷料。
56.实施例3:敷料的制备
57.一种缓释抗菌的敷料,按重量份数计,包括载体(棉布),澳洲茶树精油12.5份、乳化剂(聚山梨醇酯
‑
80)3.5份、穿心莲提取物15份、凝胶物质(聚丙烯酰基二甲基牛磺酸铵)5份、水64份。
58.上述缓释抗菌的敷料的制备方法,包括以下步骤:
59.(1)将穿心莲提取物、凝胶物质和水充分搅拌混合,搅拌速度为1000转/分钟,制得凝胶状混合物;
60.(2)在搅拌凝胶状混合物的过程中,将抗菌物质与乳化剂超声处理进行混合,得到的抗菌混合物滴入凝胶状混合物中,继续搅拌10分钟,用高压均质机进行均质3分钟,均质速度为9000转/分钟,制得纳米级悬液;
61.(3)将载体浸入纳米级悬液中,取出载体,取出敷料时,纳米级悬液与载体之间形成饱和但不滴液状态,制得敷料。
62.实施例4:敷料的制备
63.一种缓释抗菌的敷料,按重量份数计,包括载体(棉布),澳洲茶树精油17份、乳化剂(吐温80、司盘80,各1.25份)2.5份、穿心莲提取物10份、凝胶物质(聚丙烯酰基二甲基牛磺酸铵)2.5份、水68份。
64.上述缓释抗菌的敷料的制备方法,包括以下步骤:
65.(1)将穿心莲提取物、凝胶物质和水充分搅拌混合,搅拌速度为1000转/分钟,制得凝胶状混合物;
66.(2)在搅拌凝胶状混合物的过程中,将抗菌物质与乳化剂超声处理进行混合,得到的抗菌混合物滴入凝胶状混合物中,继续搅拌10分钟,用高压均质机进行均质3分钟,均质速度为9000转/分钟,制得纳米级悬液;
67.(3)将载体浸入纳米级悬液中,取出载体,取出敷料时,纳米级悬液与载体之间形成饱和但不滴液状态,制得敷料。
68.实施例5:敷料的制备
69.一种缓释抗菌的敷料,按重量份数计,包括载体(棉布),澳洲茶树精油25份、乳化剂(吐温80、司盘80,各2.5份)5份、穿心莲提取物0.1份、凝胶物质(聚丙烯酰基二甲基牛磺酸铵)7份、水62.9份。
70.上述缓释抗菌的敷料的制备方法,包括以下步骤:
71.(1)将穿心莲提取物、凝胶物质和水充分搅拌混合,搅拌速度为1000转/分钟,制得凝胶状混合物;
72.(2)在搅拌凝胶状混合物的过程中,将抗菌物质与乳化剂超声处理进行混合,得到的抗菌混合物滴入凝胶状混合物中,继续搅拌15分钟,用高压均质机进行均质5分钟,均质速度为9000转/分钟,制得纳米级悬液;
73.(3)将载体浸入纳米级悬液中,取出载体,取出敷料时,纳米级悬液与载体之间形
成饱和但不滴液状态,制得敷料。
74.对比例1
75.与实施例3相比,对比例1中的敷料不含凝胶物质,其余组成及制备过程与实施例3相同。即对比例1的敷料制备过程不加入凝胶物质。
76.对比例2
77.与实施例3相比,对比例2中的敷料不含穿心莲提取物,其余组成及制备过程与实施例3相同。即对比例2的敷料制备过程不加入穿心莲提取物。
78.产品效果测试(为了方便以下实验,采用本发明实施例的步骤(2)制得的纳米级悬液来代替敷料进行实验,本发明使用用于制备敷料的纳米级悬液的效果可代表敷料的效果)
79.1.抗耐甲氧西林金黄色葡萄球菌(mrsa)效果测试
80.根据《消毒技术规范2002年版》中载体浸泡定量杀菌试验操作步骤如下:
81.1)取无菌平皿若干,分别标明所注入的是实施例1
‑
5和对比例1
‑
2制得的用于制备敷料的纳米级悬液,按每平皿5.0ml的量,注入平皿中。
82.2)将盛有实施例3
‑
5和对比例1
‑
2制得的纳米级悬液的平皿置20℃
±
1℃水浴箱内5分钟后,用无菌镊子分别放入预先制备的耐甲氧西林金黄色葡萄球菌(mrsa)菌片3片,并使之浸透于实施例3
‑
5和对比例1
‑
2制得的纳米级悬液(作为试验组)中。
83.3)待耐甲氧西林金黄色葡萄球菌与纳米级悬液相互作用至预定时间1小时,用无菌镊子将菌片取出分别移入一含5.0ml中和剂(2%质量浓度的吐温
‑
80+0.5%质量浓度的卵磷脂+1%质量浓度的甘氨酸+0.03mol/l pbs磷酸盐缓冲盐溶液)试管中。用电动混合器混合20s,或将试管在手掌上振敲80次,使菌片上的细菌被洗脱进入中和液中,再放置5分钟以上,使中和作用充分。最终进一步混匀后,吸取1.0ml直接接种平皿,每管接种2个平皿,测定存活菌数。
84.4)另取一平皿,注入10.0ml无菌硬水,放入3片菌片,作为阳性对照组。其随后的试验步骤和活菌培养计数与上述试验组相同。
85.5)所有试验样本均在37℃温箱中培养,对细菌繁殖体培养48小时观察最终结果;对细菌芽孢需培养72小时观察最终结果。
86.6)上述试验组和对照组重复3次,计算各组的活菌量(cfu/片)。
87.7)计算杀灭率:
88.杀灭率(%)=n
t
=(v0‑
v
t
)/v0×
100%;
89.nt:实验中细菌的杀灭率;
90.v0与v
t
:分别为阳性对照组杀菌前和杀菌后(杀菌前为v0,杀菌后为v
t
)含菌量。
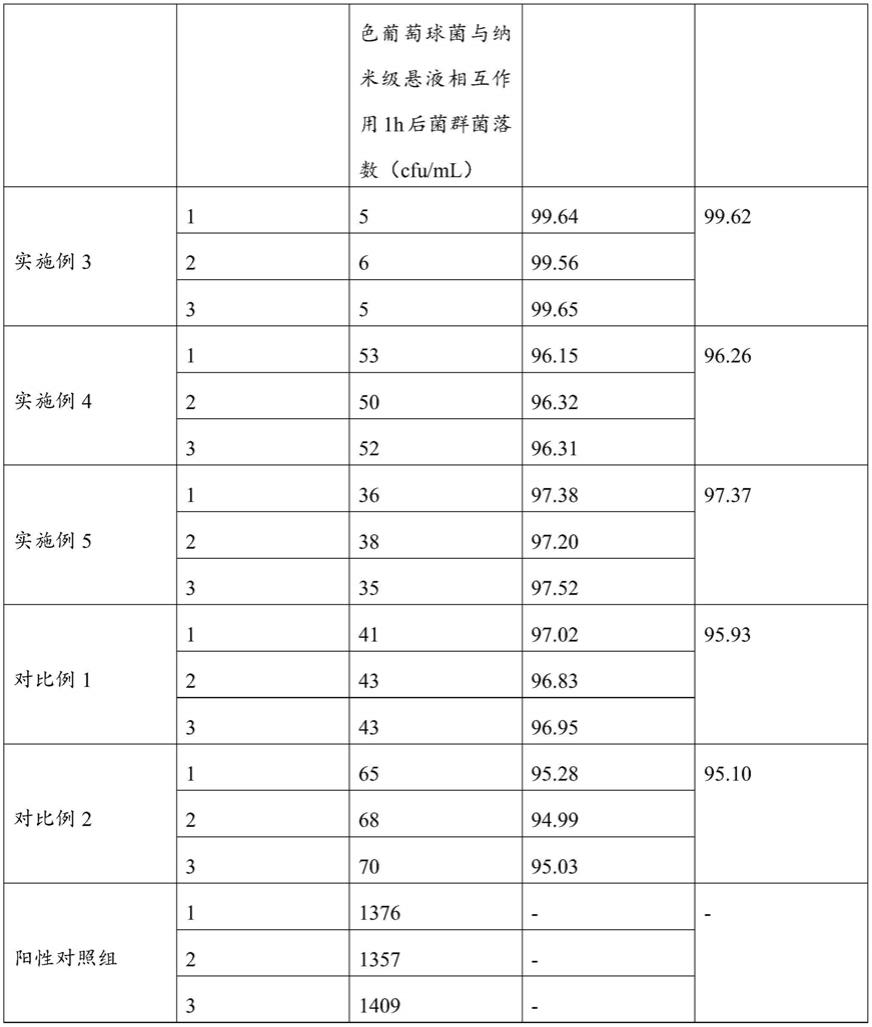
91.使用纳米级悬液前后抗菌实验结果如表1所示。
92.表1:抗菌结果
93.[0094][0095]
从表1可以看出,本发明实施例3
‑
5制得的敷料对耐甲氧西林金黄色葡萄球菌(mrsa)具有明显的抑制效果,对耐药菌有较好抗菌活性,其中实施例3制得的敷料对耐甲氧西林金黄色葡萄球菌(mrsa)最佳。
[0096]
2.广谱抗菌性测试
[0097]
取培养18
‑
24小时的大肠杆菌、金黄色葡萄球菌、绿脓杆菌、白色念珠菌菌落,分别采用直接菌落悬液配制法,制备成符合实验要求的菌悬液(称为试验菌悬液)。
[0098]
在无菌试管内加入1ml试验菌悬液和4ml实施例3制得的用于制备敷料的纳米级悬液,混匀,恒温至(20
±
1℃),作用5分钟、10分钟和20分钟。然后取无菌试管内的0.5ml样液加入到含4.5ml中和剂(2%质量浓度的吐温80+0.5%质量浓度的卵磷脂+1%质量浓度的甘氨酸+0.03mol/l pbs磷酸盐缓冲盐溶液)的试管内混匀,中和作用10分钟。分别吸取1.0ml样液,按活菌培养计数方法测定存活菌数,计算杀灭率。如平板上生长的菌落数较多时,可
进行系列10倍稀释后,再进行活菌培养计数。同时用稀释液(稀释液为本领域尝试试剂)代替实施例3混合液,进行平行试验,作为阳性对照组。结果如表2所示。
[0099]
表2:广谱抗菌性测试结果
[0100][0101]
从表2可以看出,实施例3制得的敷料对大肠杆菌、金黄色葡萄球菌、绿脓杆菌、白色念珠菌杀灭效果显著。
[0102]
3.破损皮肤刺激性实试验
[0103]
取24只大小、体重在160
‑
180g、年龄、健康状况、生长环境相近的sd大鼠(sd大鼠为大鼠的一个品系),雌雄不限,sd大鼠由南方医大实验动物科技发展公司提供。将sd大鼠随机分成8组,每组3只(3只sd大鼠编号1、2、3)。用电动剃刀将每只sd大鼠的背部毛发剃掉,背部毛发剃掉的面积大约为14cm2,制造1个大小、面积范围、深度及严重程度均一的烧伤创面,按照每2cm2皮肤500μl的剂量分别给予每组sd大鼠皮肤给药,每只sd大鼠画取12cm2的给药面积,也就是说每只sd大鼠给以3ml的药物(分别用实施例1
‑
5、对比例1
‑
2制得的用于制备敷料的纳米级悬液进行给药,另设一空白对照组用生理盐水给药),贴敷固定,24小时、48小时和72小时后进行观察。具体皮肤刺激的评价标准如表3、表4所示,观察的结果如表5所示。
[0104]
表3
[0105][0106]
表4
[0107][0108]
表5
[0109]
[0110][0111]
表5中红斑和水肿给出的小数点分值是参考表3给出的分值进行打分的。
[0112]
从表5可以看出,本发明实施例1
‑
5制得的用于制备敷料的纳米级悬液在24小时、48小时和72小时中都未出现红斑和水肿现象。其中本发明实施例3的用于制备敷料的纳米级悬液效果最好,则敷料刺激性低、缓释效果好。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1