一种治疗幽门螺杆菌的组合物及其制备方法和应用
1.本发明属于医药领域,具体涉及一种治疗幽门螺杆菌的组合物及其制备方法和应用。
背景技术:
2.幽门螺杆菌(helicobacterpylori,hp)是胃炎、消化性溃疡和胃癌等疾病的重要病因。现在hp感染了全球约半数以上的人口。目前,国内外根除hp方案的主要包括标准三联、非铋剂四联(ppi+3种抗菌药物)、铋剂四联(ppi+铋剂+2种抗菌药物)等,抗菌药物主要包括甲硝唑、克拉霉素、左氧氟沙星等。但随着广泛的使用抗生素进行治疗,hp耐药性越来越高,根除率也越来越低,严重威胁公众的健康安全。中药治疗hp具有疗效确切、不易产生耐药、毒性低、根除率高等优势。左金丸源自《丹溪心法》,由黄连和吴茱萸两味药组成,用量比例为6:1,具有清肝泄火,降逆止呕的功效,主要用于急慢性胃炎、幽门螺杆菌感染等,但是,经药物敏感性检测,左金丸水提物的最低抑菌浓度(mic)为50~100μg/ml,其对幽门螺杆菌的抑制作用并不明显,抑菌效果还有待提高。牛蒡子苷元和丹参酮ⅰ分别是牛蒡子和丹参等中药的活性成分,经我们实验证实其对幽门螺杆菌有良好的抑制作用,mic均能达到1μg/ml,而且作用机制不同,属于我国药典中的辅料,具有较好的安全性。因此,本专利将牛蒡子苷元和丹参酮ⅰ添加到左金丸中,既能通过不同的作用靶点协同增强对幽门螺杆菌的抑制作用,强化左金丸的抑菌效果,又不影响左金丸的作用机制,对治疗幽门螺杆菌感染相关疾病具有协同增效的作用。
3.本发明涉及的组合物制备方法,未见有报道;该组合物在体内体外对幽门螺杆菌具有特异性的抑制作用,且协同抑菌作用比左金丸增强10倍,能较好的促进小鼠胃粘膜炎症修复,不容易产生耐药、安全性高,可作为治疗幽门螺杆菌感染相关疾病的候选药物,其用途属于首次公开。
技术实现要素:
4.解决的技术问题:为了提升左金丸对幽门螺杆菌的抑制活性,又不改变其原有的作用机制,本发明提供了一种治疗幽门螺杆菌的组合物及其制备方法和应用,制备的组合物对耐药性和敏感性幽门螺杆菌均有较好的抑制作用,且抑菌作用和治疗效果明显优于左金丸。
5.技术方案:一种治疗幽门螺杆菌的组合物的制备方法,按如下比例,具体步骤为:第一步,水提物制备:黄连和吴茱萸按重量比6:1混合,加水分别浸泡20
‑
40min,煎煮3次,第一煮1h,第二次煮45min,第三次煮30min;其间加水补充蒸发的水分并搅拌,每次煎煮完成后,过滤,得滤液,再加水重新煎煮,合并三次滤液,浓缩,真空干燥,干燥完成后放置
‑
20℃冰箱保存备用;第二步,溶解药物:将牛蒡子苷元、丹参酮ⅰ分别称重后溶解于无水乙醇中,使得终浓度为4mg/ml,将制备的水提物称重溶解于无菌水中,使得终浓度为4mg/ml;第三步,组合药物:将水提物、牛蒡子苷元、丹参酮ⅰ按照不同的质量比100:(1
‑
16):(1
‑
16)混合
在一起,即得到组合物。
6.优选的,加水浸泡时间为30min。
7.优选的,水提物、牛蒡子苷元、丹参酮ⅰ配制相同母液浓度后按照100:8:8的比例混合。
8.上述制备方法制得的组合物。
9.上述组合物在制备治疗幽门螺杆菌感染相关疾病药物中的应用。
10.有益效果:首先,本发明成功制备组合物;第二,本发明制备的组合物作用于抑制幽门螺杆菌的生长,且效果优于左金丸,而且其作用特异性高、毒副作用小、不易产生耐药,能作为治疗幽门螺杆菌感染疾病的候选药物,有效缓解幽门螺杆菌严峻的耐药性问题。
附图说明
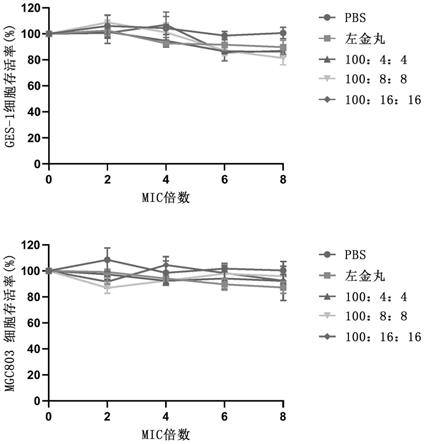
11.图1配制100:8:8组合物对细胞的毒性评价;
12.图2配制100:8:8组合物对小鼠胃、肝、脾和肾组织损伤;
13.图3配制100:8:8组合物耐药性评价;
14.图4配制100:8:8组合物治疗急性胃炎小鼠后hp159定植量;
15.图5配制100:8:8组合物治疗急性胃炎小鼠后胃粘膜组织修复情况;
16.图6配制100:8:8组合物治疗急性胃炎小鼠后炎症因子减少情况。
具体实施方式
17.实施例1
18.第一步,水提物制备:中药黄连、吴茱萸、牛蒡子和丹参按不同比例准确称量重量。加水没过中药浸泡30min,煎煮3次,第一煮1h,第二次煮45min,第三次煮30min。其间不断加水补充蒸发的水分,使用玻璃棒搅拌,避免糊底,每次煎煮完成后,过滤,得滤液,再加适量水重新煎煮。合并三次滤液,浓缩,真空干燥,干燥完成后放置
‑
20℃冰箱保存备用。
19.第二步,溶解药物:将第一步中干燥的水提物溶解于无菌水中,使得终浓度为4mg/ml,即得到组合物1。
20.实施例2
21.第一步,水提物制备:中药黄连和吴茱萸按6:1的比例准确称量重量。加水没过中药浸泡30min,煎煮3次,第一煮1h,第二次煮45min,第三次煮30min。其间不断加水补充蒸发的水分,使用玻璃棒搅拌,避免糊底,每次煎煮完成后,过滤,得滤液,再加适量水重新煎煮。合并三次滤液,浓缩,真空干燥,干燥完成后放置
‑
20℃冰箱保存备用。
22.第二步,溶解药物:将购买来的化合物牛蒡子苷元、丹参酮ⅰ称重溶解于无水乙醇中,使得终浓度为4mg/ml,将制备的水提物称重溶解于无菌水中,使得终浓度为4mg/ml。
23.第三步,组合药物:将水提物、牛蒡子苷元、丹参酮ⅰ按照分别按照100:1:1、100:2:2、100:4:4、100:8:8、100:16:16的比例混合在一起,即得到组合物2。
24.本发明对幽门螺杆菌的抑制作用通过如下实施例进一步详细的说明。
25.1.材料
26.1.1样品
27.用实施例1、2分别制备组合物。
28.1.2菌株
29.(1)幽门螺杆菌菌株:标准菌株26695、、nsh57、msd132及g27由南京医科大学毕洪凯老师赠送;临床甲硝唑耐药菌株、克拉霉素耐药菌株、左氧氟沙星耐药菌株、左氧氟沙星和甲硝唑耐药菌株、克拉霉素和甲硝唑耐药菌株、左氧氟沙星和克拉霉素及甲硝唑多重耐药菌株(hpbs001、hpbs002、hpbs003等)由右江民族医学院耐药微生物感染防治研究中心提供。
30.(2)非幽门螺杆菌:金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌、鲍曼不动杆菌、肺炎克雷伯氏菌、白色念珠菌、阴沟肠杆菌、空肠弯曲杆菌、枯草芽孢杆菌、奇异变形杆菌、弯曲乳杆菌、嗜麦芽寡养单胞菌、摩氏摩根菌、热带假丝酵母菌、溶血葡萄球菌、醋杆菌、酿酒酵母菌、霍氏肠杆菌由右江民族医学院耐药微生物感染防治研究中心提供。
31.1.3主要培养基和试剂:哥伦比亚培养基、脑心浸液培养基、营养琼脂培养基、营养肉汤培养基、mh培养基、沙氏培养基、标准小牛血清。
32.1.4主要仪器:三气培养箱、离心机、酶标仪、电子天平等。
33.1.5耗材:ep管、tip头、离心管等。
34.2.方法与结果
35.2.1微量稀释法检测实施例1制备的组合物对幽门螺杆菌的最低抑菌浓度(mic)
36.2.1.1微量稀释法检测组合物1对幽门螺杆菌的最低抑菌浓度(mic,100μl体系)
37.(1)配备不同比例组合物1(如:黄连(24g)+吴茱萸(4g)+牛蒡子(6g)+丹参(6g)、黄连(24g)+吴茱萸(4g)+牛蒡子(12g)+丹参(12g)等)4mg/ml,备用。
38.(2)琼脂板制备:将不同浓度的抗菌药物分别加入50ml烧瓶,使培养基和药物混合后含药量分别是1、0.8、0.6、0.4、0.2、0.1mg/ml,药物和培养基总量为20ml。
39.(3)菌液制备及接种:取固体平板上对数期生长的菌用对应培养基制作成菌悬液,hp调整菌液浓度为1
×
108cfu/ml(od600为0.3),备用。取1μl接种于琼脂表面,每点菌数约为105cfu。并取1μl菌液接种于菌株原培养基作阳性对照,含药液的琼脂板作阴性对照。接种好放置相应培养箱孵育。
40.(3)判断结果:当含药物未加菌的阴性对照板上细菌无生长和菌株原培养基阳性板上有菌生长实验才有意义。将平板置于暗色、无反光物体表面上判断试验终点,以抑制细菌生长的最低药物浓度为mic。在孔琼脂表面上可见轻微细菌生长,与生长对照比较抑制80%以上细菌生长的最低药物浓度作为终点浓度。如果出现有2个以上菌落生长于含药浓度高于终点水平的琼脂平板上,或低浓度药物琼脂平板上不长而高浓度药物琼脂平板上生长现象,则应检查培养物纯度或重复试验。
41.(6)结果:添加不同比例牛蒡子和丹参的组合物对幽门螺杆菌的抑制作用并未优于左金丸(黄连+吴茱萸),甚至降低了抑菌效果,因此左金丸添加其它中药可能很难提高其对幽门螺杆菌的抑菌效果,结果见表1、表2、表3。
42.表1左金丸添加牛蒡子和丹参后对159菌株mic检测(mg/ml)
[0043][0044]
表2左金丸添加牛蒡子和丹参后对26695菌株mic检测(mg/ml)
[0045][0046]
表3左金丸添加牛蒡子和丹参后对g27菌株mic检测(mg/ml)
[0047][0048]
2.1.2微量稀释法检测实施例2制备的组合物对幽门螺杆菌的最低抑菌浓度(mic)
[0049]
(1)配备左金丸水提物、牛蒡子苷元、丹参酮ⅰ4mg/ml,分别按100:1:1、100:2:2、100:4:4、100:8:8、100:16:16混合备用。
[0050]
(2)mic板制备第一孔先加培养基175μl,再加5μl抗菌药物,倍比稀释至第7孔;第8孔不加药,保留90μl培养基,作为加菌不加药对照。
[0051]
(3)菌液制备取固体平板上对数期生长的幽门螺杆菌用bhi培养基制作成菌悬液,调整浓度od
600
为0.3(1
×
108cfu/ml),稀释10倍,为1
×
107cfu/ml,备用。
[0052]
(4)接种菌液取10μl加至第1
‑
8孔(每孔菌液浓度约为1.0
×
106cfu/ml)。培养72h判断结果。
[0053]
(5)结果判断以在小孔内完全抑制细菌生长的最低药物浓度为mic。当阳性对照孔第8孔(即不含抗生素)内细菌明显生长和阴性对照孔(即无菌,仅含培养基)不生长试验才有意义。当在微量稀释法出现单一的跳孔时,应记录抑制细菌生长的最高药物浓度。如出现多处跳孔,则不应报告结果,需重复试验。每个药物重复3次试验。
[0054]
(6)结果:在实施例2制备的组合物中,左金丸水提物添加中药活性成分牛蒡子苷元、丹参酮ⅰ,100:8:8组合物抑菌效果最优,结果见表4;而且100:8:8组合物比原左金丸的最低抑菌浓度降低了约10~30倍,抑菌效果明显提高,结果见表5。
[0055]
表4不同配比组合物对幽门螺杆菌的mic(μg/ml)检测
[0056][0057]
表5配制100:8:8组合物对幽门螺杆菌不同菌株的mic(μg/ml)检测
[0058][0059]
2.2药物毒性检测
[0060]
2.2.1细胞毒性检测
[0061]
(1)制备ges
‑
1、mgc823细胞悬液,调浓度为1
×
105。
[0062]
(2)接种到96孔板中:每孔100μl,同样的样本做3个重复。
[0063]
(3)37℃培养箱中培养24小时。
[0064]
(4)加入不同配比组合物2,设加药不加细胞组。
[0065]
(5)37℃培养箱中培养24小时。
[0066]
(6)加入10μl cck8,轻敲混匀后培养4小时。
[0067]
(7)测定450nm吸光度,根据公式计算存活率:细胞存活率=[(as
‑
ab)]/[(ac
‑
ab)]
×
100%,as为含有细胞培养基、药物、cck
‑
8孔,ac为含有细胞培养基、cck
‑
8、没有药物孔,ab为不含细胞和药物、只有培养基和cck
‑
8孔。根据存活率建立生存曲线。
[0068]
(8)结果实施例2配制100:8:8组合物的8倍mic对ges
‑
1和bgc823细胞损伤不大,与左金丸无显著差异,毒性比较低,如图1所示。
[0069]
2.2.2动物毒性检测
[0070]
(1)准备小鼠:购买6
‑
8周龄的c57bl/6小鼠,随机分给药组和阴性对照组每组10只。
[0071]
(2)灌胃给药:10倍治疗量给药,组合物(100:8:8)治疗给药量为7mg/kg,即小鼠毒性检测给药量为70mg/kg,连续3天,每天给药1次;阴性对照组给pbs液,次数和量同给药组。
[0072]
(3)称量体重:从给药前1天开始称小鼠体重,连续称量7天。
[0073]
(4)药效检测:停药后第3天感染组的小鼠称重并计算平均体重,眼球采血,行脱臼断颈处死,取胃、肾、肝和脾组织,做病理切片并进行he染色。
[0074]
(5)结果:a~d为正常小鼠灌pbs组胃、肝、脾和肾损伤情况,e~h为灌胃实施例2配制的组合物(100:8:8)对胃、肝、脾和肾肾损伤情况,两组相比,实施例2配制的组合物(100:8:8)10倍治疗量给药,对小鼠胃、肝、脾和肾均无明显损伤,其毒性非常低,如图2所示。
[0075]
2.3微量稀释法检测实施例2配制的100:8:8组合物对非幽门螺杆菌的最低抑菌浓度(mic)
[0076]
(1)配备组合物(100:8:8)4mg/ml,混合备用。
[0077]
(2)mic板制备第一孔先加培养基175μl,再加5μl抗菌药物,倍比稀释至第7孔;第8孔不加药,保留90μl培养基,作为加菌不加药对照。
[0078]
(3)菌液制备取固体平板上对数期生长的菌用相应培养基制作成菌悬液,细菌调整浓度od600为0.3(1
×
108cfu/ml),稀释100倍,为1
×
106cfu/ml,真菌调整浓度od600为0.5(5
×
106cfu/ml),稀释1000倍,为5
×
103cfu/ml,备用。
[0079]
(4)接种菌液取10μl加至第1
‑
8孔(每孔菌液浓度约为1.0
×
106cfu/ml)。培养72h判断结果。第1孔至第6孔药物(左金丸+牛蒡子苷元+丹参酮ⅰ)浓度分别为86.21+6.9+6.9、43.1+3.45+3.45、21.55+1.72+1.72、10.78+0.86+0.86、5.39+0.43+0.43、2.69+0.22+0.22μg/ml。
[0080]
(5)结果判断以在小孔内完全抑制细菌生长的最低药物浓度为mic。当阳性对照孔第7孔(即不含抗生素)内细菌明显生长和第8孔(无菌)不生长试验才有意义。当在微量稀释法出现单一的跳孔时,应记录抑制细菌生长的最高药物浓度。如出现多处跳孔,则不应报告结果,需重复试验。每个药物重复3次试验。
[0081]
(6)结果:组合物2(100:8:8)对大多数非幽门螺杆菌抑制作用比较差,说明抗菌谱比较窄、专一性强,能特异性作用于幽门螺杆菌,结果见表6。
[0082]
表6配制100:8:8组合物对非幽门螺杆菌mic(μg/ml)检测
[0083][0084]
注:100:8:8组“>”指大于86.21+6.9+6.9;左金丸组“>”指大于100
[0085]
2.4实施例2配制的100:8:8组合物的耐药性检测
[0086]
(1)用幽门螺杆菌g27菌株进行检测连翘脂素衍生物的耐药性。首先检测甲硝唑和组合物2(100:8:8)的mic分别为2μg/ml、5.39+0.43+0.43μg/ml,用1/4mic浓度进行诱导,每3天检测一次,共诱导24天。诱导浓度随着mic变化而调整,如甲硝唑mic变为16μg/ml时,诱导的浓度则调为4μg/ml。
[0087]
(2)结果诱导24天后,甲硝唑耐药明显,mic增长了64倍;实施例2配制的100:8:8组合物mic无变化,不容易产生耐药,如图3所示。
[0088]
2.5构建动物模型体内检测组合物对h.pylori的抑制效果
[0089]
左金丸、牛蒡子苷元、丹参酮ⅰ、奥美拉唑、阿莫西林及克拉霉素均溶解稀释为10mg/ml。实验动物:c57bl/6。
[0090]
(1)动物分组:实验组将造模成功的感染组(bhk159)平均分成5组,分别为奥美拉唑+阿莫西林+克拉霉素组(三联疗法组)、奥美拉唑+左金丸(7mg/kg)、奥美拉唑+100:8:8组合物(7mg/kg)和pbs组,每组10只;未感染h.pylori的10只小鼠为阴性对照组。
[0091]
(2)动物给药:实验组灌胃给药,有奥美拉唑的组先给予奥美拉唑,30min后再给其它药物,给完药物后禁食禁水4小时;小鼠体重按照平均20g/只计算,给药量为奥美拉唑138.2mg/kg、阿莫西林28.5mg/kg、克拉霉素14.3mg/kg,每天给药1次,连续3次;阴性对照组给pbs溶液,容量、次数同上。
[0092]
(3)药效检测:停药后第2天感染组的小鼠称重并计算平均体重,眼球采血,行断颈处死,取胃组织,破碎,h.pylori的分离培养和鉴定及计算定植量,含100:8:8组合物组治疗效果明显优于三联疗法治疗和左金丸组,如图4所示。部分胃组织进行石蜡切片并做h&e染色和tunel免疫组化和荧光免疫检查,含100:8:8组合物组胃组织修复效果好,炎症因子明
显减少,如图5、图6所示。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1