一种注射用头孢噻肟钠的制备方法与流程
1.本发明涉及医药化工领域,具体涉及一种注射用头孢噻肟钠的制备方法。
背景技术:
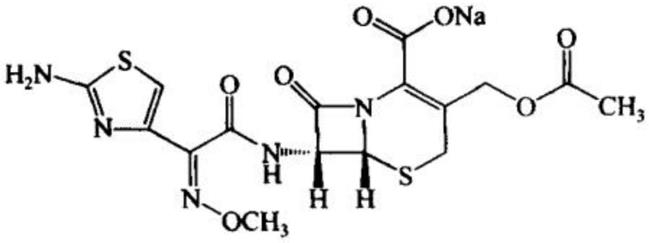
2.头孢噻肟钠(cefotaxime sodium)为第三代头孢类半合成广谱抗菌素,其产品为白色、类白色或淡黄白色结晶,无臭或微有特殊臭味。在水中易溶,在甲醇、乙醇、丙酮中微溶,在氯仿、正己烷、二氯甲烷、二乙醚及乙酸乙酯中不溶。分子式:c
16h16
n5o7s2na,分子量:477.44,分子结构式如下:
[0003][0004]
现有头孢噻肟钠结晶方法分为三水体系结晶法和含水体系结晶法。
[0005]
cn101486719a公开了一种选用丙酮水溶液作为溶媒体系的结晶方法,虽然解决了三水体系结晶方法制备产品溶液的澄清度较差的问题,但使用该方法所制备的产品的稳定性较差。这是因为头孢噻肟钠在有水分子存在的条件下稳定性差,其酰胺侧链、内酰胺环以及乙酰基三个部位都可能发生降解,在酸、碱和温度升高环境下均能促进其水解。
[0006]
注射用头孢噻肟钠由于头孢噻肟钠稳定性差,无法满足目前一致性评价需求,同时也给患者的用药带来了安全隐患。
技术实现要素:
[0007]
本发明需要解决的技术问题是提供一种注射用头孢噻肟钠的制备方法,可有效提升产品质量稳定性,同时易于粉针制剂分装,制备过程操作简单,适合工业化生产。
[0008]
为解决上述技术问题,本发明所采用的技术方案是:
[0009]
一种注射用头孢噻肟钠的制备方法,以头孢噻肟酸为起始原料,其特征在于,包括以下操作步骤:
[0010]
(a)将氯化钠溶液和头孢噻肟钠晶种混合溶液作为起始底料;
[0011]
(b)向醇类试剂中加入头孢噻肟酸,搅拌均匀得到第一混合液;
[0012]
(c)向醇类试剂中加入三水醋酸钠,搅拌均匀得到第二混合液;
[0013]
(d)向步骤(a)起始底料中同时流加步骤(b)、(c)所得第一混合液、第二混合液;
[0014]
(e)向步骤(d)结晶液中流加丙酮试剂,养晶;
[0015]
(f)流加完毕后,过滤,用醇类雾化试剂洗涤滤饼;
[0016]
(g)将步骤(e)滤饼用丙酮洗涤,干燥;
[0017]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0018]
本发明技术方案的进一步改进在于:步骤a中头孢噻肟钠晶种为头孢噻肟酸重量的0.5%~1%;氯化钠溶液中氯化钠质量分数为26.5%,氯化钠溶液与头孢噻肟酸的体积重量比(ml/g)为(2~3):4。
[0019]
本发明技术方案的进一步改进在于:步骤b、c和f中醇类试剂为甲醇、乙醇、异丙醇中的一种。
[0020]
本发明技术方案的进一步改进在于:步骤b醇类试剂与头孢噻肟酸的体积重量比(ml/g)为(2~3):4。
[0021]
本发明技术方案的进一步改进在于:步骤c中三水醋酸钠与头孢噻肟酸的摩尔比为(1.05~1.1):1;醇类试剂、水与三水醋酸钠的体积重量比(ml/g)为(10~15):(10~15):12。
[0022]
本发明技术方案的进一步改进在于:步骤d中第一混合液、第二混合液均在30min内匀速加完。
[0023]
本发明技术方案的进一步改进在于:步骤e中,所述丙酮与头孢噻肟酸的体积重量比(ml/g)为(10~15):1。
[0024]
本发明技术方案的进一步改进在于:步骤f中醇类雾化试剂采用高速气化喷头,形成雾化液滴直径为1~2μm,洗涤用量与头孢噻肟酸的体积重量比(ml/g)为(1~2):20。
[0025]
由于采用了上述技术方案,本发明取得的技术进步是:
[0026]
本发明方法制备注射用头孢噻肟钠工艺节能环保,所用溶剂可回收利用,结晶工艺操作简单,制备出的注射用头孢噻肟钠质量好、杂质含量低、产品稳定性好的优点,样品均一性和稳定性较好,尤其是吸光度质量指标较好。解决了头孢噻肟钠稳定性差的问题,制剂产品与原研产品质量稳定性一致,对产品的稳定性和安全性及均一性、一致性均有一定提升。
具体实施方式
[0027]
下面结合实施例对本发明做进一步详细说明:
[0028]
一种注射用头孢噻肟钠的制备方法,以头孢噻肟酸为起始原料,其特征在于,包括以下操作步骤:
[0029]
(a)将20-30ml质量分数为26.5%的氯化钠溶液和0.2-0.4g头孢噻肟钠晶种混合溶液作为起始底料;
[0030]
(b)将40g头孢噻肟酸加入甲醇、乙醇或异丙醇中,搅拌均匀20-30ml,得第一混合液;
[0031]
(c)将12.5-13.15g三水醋酸钠加入10-15ml甲醇、乙醇或异丙醇,10-15ml水中,搅拌均匀,得第二混合液;
[0032]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0033]
(e)向步骤(d)结晶液中流加400-600ml丙酮试剂。
[0034]
(f)流加完毕后,过滤,采用高速气化喷头将2~4ml甲醇、乙醇或异丙醇雾化试剂,形成雾化液滴直径为1~2μm,洗涤滤饼。
[0035]
(g)将步骤(e)滤饼用丙酮洗涤,干燥;
[0036]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0037]
实施例1
[0038]
(a)将20ml质量分数为26.5%的氯化钠溶液和0.2g头孢噻肟钠晶种混合溶液作为起始底料;
[0039]
(b)将40g头孢噻肟酸加入甲醇中,搅拌均匀20ml,得第一混合液;
[0040]
(c)将12.5g三水醋酸钠加入10ml甲醇10ml水中,搅拌均匀,得第二混合液;
[0041]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0042]
(e)向步骤(d)结晶液中流加400ml丙酮试剂。
[0043]
(f)流加完毕后,过滤,用甲醇雾化试剂;采用高速气化喷头将2ml甲醇雾化,形成雾化液滴直径为1μm,洗涤滤饼。
[0044]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠40.5g。
[0045]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0046]
实施例2
[0047]
(a)将30ml质量分数为26.5%的氯化钠溶液和0.4g头孢噻肟钠晶种混合溶液作为起始底料;
[0048]
(b)将40g头孢噻肟酸加入甲醇中,搅拌均匀30ml,得第一混合液;
[0049]
(c)将13.15g三水醋酸钠加入15ml甲醇15ml水中,搅拌均匀,得第二混合液;
[0050]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0051]
(e)向步骤(d)结晶液中流加600ml丙酮试剂。
[0052]
(f)流加完毕后,过滤,用甲醇雾化试剂;采用高速气化喷头将4ml甲醇雾化,形成雾化液滴直径为2μm,洗涤滤饼。
[0053]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠40.3g。
[0054]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0055]
实施例3
[0056]
(a)将25ml质量分数为26.5%的氯化钠溶液和0.3g头孢噻肟钠晶种混合溶液作为起始底料;
[0057]
(b)将40g头孢噻肟酸加入甲醇中,搅拌均匀25ml,得第一混合液;
[0058]
(c)将12.75g三水醋酸钠加入10-15ml甲醇12.5ml水中,搅拌均匀,得第二混合液;
[0059]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0060]
(e)向步骤(d)结晶液中流加500ml丙酮试剂。
[0061]
(f)流加完毕后,过滤,用甲醇雾化试剂;采用高速气化喷头将3ml甲醇雾化,形成雾化液滴直径为1μm,洗涤滤饼。
[0062]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠40.4g。
[0063]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0064]
实施例4
[0065]
(a)将25ml质量分数为26.5%的氯化钠溶液和0.3g头孢噻肟钠晶种混合溶液作为起始底料;
[0066]
(b)将40g头孢噻肟酸加入乙醇中,搅拌均匀25ml,得第一混合液;
[0067]
(c)将12.75g三水醋酸钠加入10-15ml乙醇12.5ml水中,搅拌均匀,得第二混合液;
[0068]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0069]
(e)向步骤(d)结晶液中流加500ml丙酮试剂。
[0070]
(f)流加完毕后,过滤,采用高速气化喷头将3ml乙醇雾化,形成雾化液滴直径为1μm,洗涤滤饼。
[0071]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠40.2g。
[0072]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0073]
实施例5
[0074]
(a)将25ml质量分数为26.5%的氯化钠溶液和0.3g头孢噻肟钠晶种混合溶液作为起始底料;
[0075]
(b)将40g头孢噻肟酸加入异丙醇中,搅拌均匀25ml,得第一混合液;
[0076]
(c)将12.75g三水醋酸钠加入12.5ml异丙醇12.5ml水中,搅拌均匀,得第二混合液;
[0077]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0078]
(e)向步骤(d)结晶液中流加500ml丙酮试剂。
[0079]
(f)流加完毕后,过滤,采用高速气化喷头将3ml异丙醇雾化,形成雾化液滴直径为1μm,洗涤滤饼。
[0080]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠40.2g。
[0081]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0082]
对比例1-3
[0083]
对比例1
[0084]
(a)将50ml质量分数为10%的氯化钠溶液和0.05g头孢噻肟钠晶种混合溶液作为起始底料;
[0085]
(b)将40g头孢噻肟酸加入甲醇中,搅拌均匀50ml,得第一混合液;
[0086]
(c)将14g三水醋酸钠加入20ml甲醇10ml水中,搅拌均匀,得第二混合液;
[0087]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0088]
(e)向步骤(d)结晶液中流加600ml丙酮试剂。
[0089]
(f)流加完毕后,过滤,用甲醇雾化试剂;采用高速气化喷头将5ml甲醇雾化,形成雾化液滴直径为5μm,洗涤滤饼。
[0090]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠39.1g。
[0091]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0092]
对比例2
[0093]
(a)将50ml质量分数为10%的氯化钠溶液和0.05g头孢噻肟钠晶种混合溶液作为起始底料;
[0094]
(b)将40g头孢噻肟酸加入乙二醇中,搅拌均匀50ml,得第一混合液;
[0095]
(c)将14g三水醋酸钠加入20ml乙二醇10ml水中,搅拌均匀,得第二混合液;
[0096]
(d)向起始底料中同时流加第一混合液、第二混合液,30min内匀速加完;
[0097]
(e)向步骤(d)结晶液中流加600ml丙酮试剂。
[0098]
(f)流加完毕后,过滤,用乙二醇雾化试剂;采用高速气化喷头将5ml乙二醇雾化,形成雾化液滴直径为5μm,洗涤滤饼。
[0099]
(g)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠38.5g。
[0100]
(h)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0101]
对比例3
[0102]
(a)将40g头孢噻肟酸加入乙二醇中,搅拌均匀20ml,得第一混合液;
[0103]
(b)将12.5g三水醋酸钠加入10ml甲醇和10ml水中,搅拌均匀,得第二混合液;
[0104]
(c)将第二混合液流加至第一混合液中,30min内匀速加完;
[0105]
(d)向步骤(c)结晶液中流加400ml丙酮试剂。
[0106]
(e)流加完毕后,过滤,用甲醇雾化试剂;采用高速气化喷头将2ml甲醇雾化,形成雾化液滴直径为1μm,洗涤滤饼。
[0107]
(f)将步骤(e)滤饼用丙酮洗涤,干燥,得到头孢噻肟钠39.5g。
[0108]
(g)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0109]
对比例4(cn101486719a)
[0110]
1)在500ml三颈瓶中,加入14.5ml水、60ml丙酮、4g无水醋酸钠,降温至10℃;
[0111]
2)在步骤1)的混合溶液中加入20g的头孢噻肟酸,搅拌至溶清;
[0112]
3)等澄清后,加入0.30g活性炭,10℃搅拌20分钟;
[0113]
4)过滤,用80%丙酮15ml洗涤;
[0114]
5)合并滤液,控制温度至18℃,滴加丙酮70ml,加入晶种,养晶搅拌0.5小时;
[0115]
6)缓慢滴加丙酮240ml;
[0116]
7)降温到5℃,养晶30分钟以上;
[0117]
8)过滤,用100ml丙酮分两次浸泡洗涤,
[0118]
9)真空干燥,得到头孢噻肟酸转钠盐晶体38.1g。
[0119]
10)经制剂分装得注射用盐酸头孢噻肟钠产品。
[0120]
以上步骤5)加入的晶种量,晶种量相对于投入的头孢噻肟酸的重量的0.03%;晶种大小挑拣80目。
[0121]
步骤6)中丙酮的滴加速度为每1小时240ml。
[0122]
所述步骤9)真空干燥条件为:夹套温度控制在0~20℃;真空在-0.05mpa;烘干时间2小时以上。
[0123]
所述步骤4)的过滤采用板框式压滤机;过滤介质的孔径在50μm;过滤介质为耐溶媒的介质材料。
[0124]
对比例1~3的制备方法与实施例1类似,区别仅在于:对比例1-2中和实施例1不同的是试验参数;对比例3和实施例1不同的是加料方式;对比例4为按照专利cn101486719a操作。
[0125]
表1:实施例和对比例的质量数据
[0126][0127]
根据表1数据可确定,本技术工艺产品质量稳定,吸光度及杂质水平相当,工艺可再现性好。与对比例1~3相比,按照本技术的方法制备的产品在含量及有关物质指标上存在明显优势;因此氯化钠加入量及本技术采用的加料方式对产品质量有明显提升。
[0128]
为了更好地验证本发明制备的注射用头孢噻肟钠质量稳定性的效果,取实施例1~3及对比例1~3得到的样品进行加速试验,条件为:温度40℃
±
2℃,相对湿度75%
±
5%,加速时间3个月,检查加速试验结束后各样品的质量。
[0129]
表2:实施例和对比例的样品加速实验数据
[0130][0131]
根据表2的实验数据可以看出,经过加速实验产品吸光度及杂质质量稳定,各项指标均符合ep10.0版药典质量要求,本发明制备方法对产品的稳定性起到良好的效果。上述各实施例和对比例的检测方法均按照ep10.0版药典规定的方法进行。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1