一种骨髓间充质干细胞/可降解水凝胶复合材料及其制备方法和用途
1.本发明涉及一种骨髓间充质干细胞/可降解水凝胶复合材料及其制备方法和用途,属于生物医用材料技术领域。
背景技术:
2.公众对自身的医疗健康愈发重视,对各种疾病的治疗与机体功能恢复或重建的需求日益增长。随着对各项疾病发病机制的不断深入研究,学界逐渐意识到,绝大多数疾病的发病与机体组织的过度炎症高度相关,并且随着炎症的产生和不受控发展,机体组织微环境发生剧烈改变,其中尤以氧化应激为最。具体地,在氧化应激过程中,由巨噬细胞、中性粒细胞等炎症细胞过量产生的活性氧物质(ros)会超出机体的抗氧化能力,从而对组织和细胞产生氧化损伤。在脊髓损伤中,过量的ros会对神经元、神经胶质细胞以及迁移到损伤部位或者外部植入的干细胞等造成包括dna、脂质、蛋白质等的氧化损伤,从而造成上述细胞的大量死亡。并且,目前直接将外部移植干细胞作为治疗手段条件并不十分成熟,直接局部注射干细胞后其原位留存率低下,且在原位因氧化应激所致存活率不高,体内的分化方向进一步受到氧化环境的限制。而单纯的生物材料,虽能在一定程度上消除氧化应激环境,却在长期的促进再生方面收效不大。因此,针对过量产生的ros的疾病微环境设计相应的体系方案,尤其是以生物材料为代表并与干细胞治疗进行联合应用的植入治疗方案,也即制备一种干细胞/生物材料的复合材料具有极高的重要性。
3.水凝胶材料在水中稳定溶胀并保有大量水分,其结构上与细胞外基质相近,且其与组织性能相近的力学模量可避免力学性能失配所致对机体组织的刺激伤害,因而具有对细胞和组织的亲和性。当前,对具有生物适配性(bio-adaptability)的材料研究方兴未艾。生物适配性,即在良好生物相容性的基础上,具有与体内失能或缺损组织再生速率相适配的降解速率。而水凝胶则可以通过调整成胶组分,采用可降解且降解产物对机体无害的高分子单体制备可降解的水凝胶。基于此,水凝胶材料是一类具有较高医用价值的高分子材料,同时其亦被广泛应用于细胞递送。然而,生物材料仅仅拥有生物适配性,对于复杂的组织修复和再生过程并不足够,生物材料还应具有自适应性(self-adaptability)。自适应性生物材料的特征表现在:材料的性能并不是静态和固定的,而是根据其所处的生理环境或病理微环境不同阶段的需求随时间和空间进行动态演化,并且具有一定的回馈调节能力。具体的,其涵盖了可以响应疾病微环境的刺激响应性并具有一定回馈机制的生物材料。而生物响应性可降解高分子材料因自身性能能够随生物体内微环境变化而作出响应,触发结构断裂,造成响应性降解而备受研究者青睐。作为响应生物体内无处不在且在机体损伤时大量产生活性氧的材料,活性氧(ros)响应性可降解生物材料也应运而生且不断崭露头角——其在原有可降解性的基础上,通过活性氧响应性进行过量产生活性氧消除、扭转氧化应激疾病微环境,进行组织保护;同时因为活性氧响应性,其在体内的降解速率进一步加速,与组织修复再生的速度进一步匹配。然而,迄今为止,仅有极其少量的骨髓间充质干细
胞/活性氧响应性可降解水凝胶复合材料,通过水凝胶材料的氧化响应降解对骨髓间充质干细胞的保护、通过骨髓间充质干细胞进一步强化活性氧响应性可降解水凝胶的后期促进修复再生功能。
4.酮缩硫醇化合物对活性氧高度敏感,且对酸、碱和蛋白酶催化的降解具有良好的耐受性。有报道利用巯基乙胺为原料合成了ros响应性的链接剂,再通过缩合反应得到活性氧响应性的聚合物作为dna的运输载体,该聚合物对酸碱具有良好的稳定性,用于高浓度活性氧环境的癌症细胞的靶向基因传递。然而,迄今为止报道的大部分基于酮缩硫醇化合物的材料都是以纳米粒子的形式存在且被广泛应用于药物传递载体,未曾有报道将其制备成骨髓间充质干细胞/活性氧响应性可降解水凝胶复合材料并用于神经修复再生。
技术实现要素:
5.本发明的目的是为了解决现有细胞包封型水凝胶较难以提供组织微环境响应性以保护所负载细胞及降解速率与体内组织再生速率较难匹配的问题,提供一种骨髓间充质干细胞/可降解水凝胶复合材料及其制备方法和用途。该材料具有与机体组织力学性能相适配及良好的生物相容性,且具有活性氧响应性强等优点,可以通过对活性氧响应断裂降解的方式消耗活性氧以保护负载细胞的特点。
6.本发明将酮缩硫醇小分子二胺化合物通过氨基与双端双键的聚乙二醇二丙烯酸酯间的加成反应将其制得含有活性氧响应性的可降解超支化聚合物,会同具有良好生物相容性的透明质酸组分及前述其它利于细胞活动的生物活性分子,在负载重悬细胞后并经由紫外光照成胶制得能够提供干预生物体内ros变化响应位点且具有良好的生物响应性和生物可降解性的骨髓间充质干细胞/可降解水凝胶复合材料。该活性氧响应性的可降解水凝胶材料不仅能够保留水凝胶材料与机体组织适配的力学性能和良好的生物相容性,也具备自身可降解性能及由活性氧响应出发的加速降解性能,同时该材料因制备简单可行而具有良好的应用价值,因此在中枢神经系统损伤,尤其是脊髓损伤等动物实验模型中的神经再生等方面的具有重要的应用。
7.本发明的目的是通过以下技术方案实现的。
8.本发明的骨髓间充质干细胞/可降解水凝胶复合材料,包括透明质酸生物相容性组分、由双端带双键结构的聚乙二醇衍生物及小分子二胺组成的活性氧响应性可降解超支化聚合物组分、以及改善细胞粘附性和促进细胞增殖生长的组分,以及骨髓间充质干细胞。
9.所述的小分子二胺为酮缩硫醇二胺,其合成路线如下:
[0010][0011]
所述的透明质酸生物相容性组分为甲基丙烯酸酯修饰的透明质酸(ha-ma),其合成路线如下:
[0012]
[0013]
其中,改性前的透明质酸的数均分子量为90~120kda。
[0014]
所述的双端带双键结构的聚乙二醇衍生物为聚乙二醇二丙烯酸酯。
[0015]
更进一步地,所述的聚乙二醇二丙烯酸酯的分子量为575~700da。
[0016]
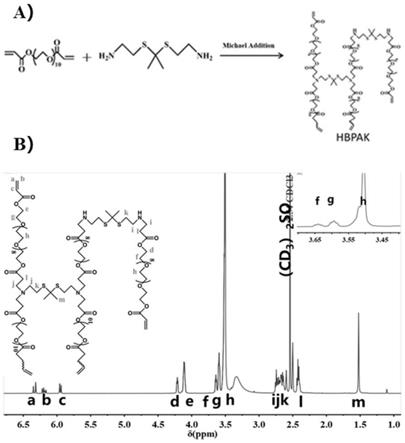
进一步地,所述的活性氧响应性可降解超支化聚合物为带有酮缩硫醇结构的超支化聚合物,其合成路线如下:
[0017][0018]
合成所得的活性氧响应性可降解超支化聚合物hbpak其数均分子量为5~8kda。
[0019]
进一步地,所述的改善细胞粘附性的组分为细胞粘附肽ikvav,所述的促进细胞增殖生长的组分为碱性成纤维生长因子bfgf和表皮生长因子egf。
[0020]
进一步地,所述的骨髓间充质干细胞/可降解水凝胶复合材料是以甲基丙烯酸酯修饰的透明质酸和带有酮缩硫醇结构的活性氧响应性超支化聚合物为组分,以细胞粘附肽ikvav、碱性成纤维生长因子、表皮生长因子为添加生物活性成分,通过重悬骨髓间充质干细胞,并以苯基-2,4,6-三甲基苯甲酰基亚磷酸锂为光引发剂,采用紫外光引发交联制备得到。
[0021]
所述的骨髓间充质干细胞/可降解水凝胶复合材料的制备方法,包括以下步骤:
[0022]
1)将透明质酸加入到反应容器a中,然后加入n,n-二甲基甲酰胺和水按体积比以体积比1:1~1:2混合所得的混合溶剂充分溶解,再以逐滴滴加的方式加入甲基丙烯酸酐,在4℃冰水浴及控制ph为8.0-9.0的条件下反应10~15h,经过7~10倍体积的无水乙醇溶液进行沉降后转移至超纯水中溶解并继续透析除去残余的乙醇及未反应的反应物,经过后续冷冻干燥得到甲基丙烯酸酯改性的透明质酸;其中甲基丙烯酸酐与透明质酸的质量比为7.5:1;
[0023]
2)将活性氧响应性可降解小分子二胺与聚乙二醇二丙烯酸酯加入到反应容器b中,然后加入二甲基亚砜充分溶解后于80℃反应6~8h,经过4~6倍于混合溶液体积的甲基叔丁基醚3~5次沉降后,经旋转蒸发除去甲基叔丁基醚溶剂,得到活性氧响应性可降解超支化聚合物,聚乙二醇二丙烯酸酯的物质的量与活性氧响应性小分子二胺的物质的量的比值为2.1~2.2:1,二甲基亚砜与活性氧响应性小分子二胺的质量比为10~15:1;
[0024]
3)将步骤1)制备的甲基丙烯酸酯改性的透明质酸的pbs溶液与步骤2)制备的活性氧响应性可降解超支化聚合物的pbs溶液混合,然后加入细胞粘附肽ikvav的pbs溶液、碱性成纤维生长因子的pbs溶液、表皮细胞生长因子的pbs溶液及光引发剂的pbs溶液进行混合得到水凝胶预聚液;将纯化的骨髓间充质干细胞消化离心,采用所述的水凝胶预聚液进行30~50次吹打重悬,后移入聚四氟乙烯模板中,经紫外光固化,得到骨髓间充质干细胞/可降解水凝胶复合材料。
[0025]
其中,所述光引发剂为苯基-2,4,6-三甲基苯甲酰基亚磷酸锂lap;所述水凝胶预聚液中,甲基丙烯酸酯改性的透明质酸的终浓度为0.005~0.015g/ml,活性氧响应性可降
解超支化聚合物的终浓度为0.05~0.15g/ml,细胞粘附肽ikvav的终浓度为400~600mg/ml,碱性成纤维生长因子及表皮生长因子的终浓度为5~10μg/ml,光引发剂的终浓度为0.5g/l,骨髓间充质干细胞的负载量为5
×
106~8
×
106/ml;光固化条件为:紫外光的功率为50mw/cm2,照射时间为30s。最终得到可负载骨髓间充质干细胞的活性氧响应性可降解水凝胶材料;
[0026]
所述的聚四氟乙烯模板优选直径为2~2.5mm、高度为2.5~3mm的圆柱形凹槽的聚四氟乙烯模板;
[0027]
进一步地,所述的骨髓间充质干细胞/可降解水凝胶复合材料适用于制备修复中枢神经系统损伤的包载物,尤其是用于脊髓损伤或脑梗中修复治疗和神经再生的包载物。
[0028]
与现有的细胞负载型水凝胶材料及活性氧响应性水凝胶相比,本发明制备的骨髓间充质干细胞/活性氧响应性可降解水凝胶复合材料具有以下优点:
[0029]
1)本发明中,通过引入ros响应性高分子组分,赋予骨髓间充质干细胞/活性氧响应性可降解水凝胶材料活性氧响应性触发的加速可降解性能;
[0030]
2)本发明中,通过引入ros响应性高分子组分,构建具有本体活性氧响应性的骨髓间充质干细胞/可降解水凝胶材料,通过活性氧响应性位点断裂用于体内组织环境过度产生的活性氧的消除,使其可以消除炎症过程中过度产生的活性氧,保护机体内的神经细胞及组织免受氧化应激损伤,同时可以避免所负载的骨髓间充质干细胞受到氧化损伤,为其在脊髓损伤后期发挥作用提供了保护。
[0031]
3)本发明中,可以通过改变hbpak组分的浓度及多肽ikvav添加与否,来影响骨髓间充质干细胞/可降解水凝胶复合材料的力学强度,使其与脊髓组织的力学模量相匹配,从而具有生物适配性和自适应性。
[0032]
4)本发明中,制得的骨髓间充质干细胞/可降解水凝胶复合材料,可以通过活性氧响应性水凝胶组分和干细胞组分协同消除炎症;
[0033]
5)本发明中,骨髓间充质干细胞/可降解水凝胶复合材料的降解产物无致癌及细胞急毒性等毒副作用。
附图说明
[0034]
图1为酮缩硫醇小分子二胺的分子式及1h nmr(cdcl3)谱图;
[0035]
图2为该水凝胶组分生物相容性组分的合成线路图及1h nmr(d2o)谱图;
[0036]
图3为该ros响应性可降解超支化聚合物组分的合成线路图及1h nmr(dmso)谱图;
[0037]
图4为实施例1中该可降解水凝胶组分中ikvav多肽与其它含双键组分之间键连方式的比较;
[0038]
图5为实施例1中该可降解水凝胶组分的力学性能表征;
[0039]
图6为实施例1中该可降解水凝胶组分的可降解性能表征,包括其在过氧化氢存在(即活性氧存在)条件下和单纯pbs溶液(模拟生理环境)条件下的情况;
[0040]
图7为实施例1中该ros响应性水凝胶组分的浸提液细胞毒性表征;
[0041]
图8为实施例1中该骨髓间充质干细胞/可降解水凝胶复合材料在1d和3d时的生物相容性;
[0042]
图9为实施例1中骨髓间充质干细胞/可降解水凝胶复合材料在体外模拟氧化应激
和炎症条件下干细胞组分存活情况对比;
[0043]
图10为实施例1中骨髓间充质干细胞/可降解水凝胶复合材料在体外模拟氧化应激和炎症条件下对炎症和活性氧消除的情况说明
[0044]
图11为实施例2中脊髓损伤模型的实图;
[0045]
图12为实施例2中该骨髓间充质干细胞/可降解水凝胶复合材料用于脊髓损伤治疗后在减少活性氧产生和减轻氧化损伤上的效果;
[0046]
图13为实施例2中该骨髓间充质干细胞/可降解水凝胶复合材料用于脊髓损伤治疗后的行为恢复和神经再生效果。
具体实施方式
[0047]
以下结合实例进一步说明本发明的技术方案,但这些实例并不用来限制本发明。本发明的活性氧响应性可降解水凝胶材料各组分的合成路线如图2,3。
[0048]
实施例1
[0049]
为验证本发明水凝胶的存在形式、力学强度与毒性,本实施例制备一种活性氧响应性的可降解水凝胶材料,是本发明提供的骨髓间充质干细胞/可降解水凝胶复合材料在不负载骨髓间充质干细胞时的情况。包括生物相容性透明质酸组分和活性氧响应性超支化聚合物组分,所述的透明质酸组分是数均分子量为100000的透明质酸经甲基丙烯酸酯改性而成,所述的活性氧响应性超支化聚合物是以聚乙二醇二丙烯酸酯及ros响应性酮缩硫醇二胺经迈克尔加成反应制得。其中,聚乙二醇二丙烯酸酯的分子量为575。合成所得的活性氧响应性超支化聚合物hbpak的数均分子量为6000da;合成所得的甲基丙烯酸酯改性的透明质酸分子量约为115kda。
[0050]
其制备包括以下步骤:
[0051]
取合成的分子量约为115kda的纯净ha-ma10mg加入到1.5ml离心管中,加入由新合成hbpak所配制的含有100mg hbpak溶质的pbs溶液900μl进行充分溶解后,加入50μl新配制的10mg/ml ikvav的pbs溶液和50μl新配制的含1.0wt%lap的pbs溶液进行充分混匀,得到1ml水凝胶预聚液。取500μl预聚液并将其转移到2ml一次性注射器中后送入紫外光固化箱,以50mw/cm2的辐射强度进行紫外光照30s即可得到1ml体积的水凝胶。经计算得,该水凝胶中ha-ma的终浓度为1.0%w/v,hbpak的终含量为500μg。与此作为对照的,在其它组分浓度相同、紫外光照相同的条件下,采用终浓度为0.6%w/v的pegda替代10%w/v hbpak构建不具备ros响应性的水凝胶。
[0052]
为考察实施例1中水凝胶组分中ikvav的存在形式,将500μl水凝胶浸泡于500μl pbs溶液中于37℃条件下静置24h得到浸提液后行高效液相色谱(hplc),同时分别配制ikvav浓度为7.5、15.5、31、62.5、125、250和500μg/ml的标准液并行hplc获得ikvav的标准曲线。如图4所示,经过比对,无论是本发明中的ros响应性的thi水凝胶、或者是作为对照组的不具备ros响应性的phi水凝胶,其浸提液中都几乎不含ikvav,证明ikvav多肽因其单端巯基成功键连到含有双键的水凝胶组分中。
[0053]
为考察实施例1制备的水凝胶组分的力学性能,取700μl水凝胶预聚液制成直径2cm,高约为1.5mm的水凝胶圆片,置于含20mm平行板转子的旋转流变仪上以1%应变,6.28rad/s转速和37℃条件下测定其储能模量g'和耗散模量g"。如图5所示,含有不同含量
的hbpak所制备的水凝胶、以及添加或不添加ikvav多肽的水凝胶(thi gel和th gel),其力学模量各不相同。结果表明,本发明中所述的ros响应性水凝胶可以通过调节hbpak组分含量、添加或不添加ikvav多肽的方式进行力学性能的调控。
[0054]
为考察实施例1制备的水凝胶组分的可降解性能,将其分别置于纯pbs溶液中或含有250mm h2o2的pbs溶液后放置于37℃恒温水浴锅中,并在相应时间点进行水凝胶的质量分析。与此相对应的,以终含量为0.6%w/v的pegda575替代终含量为10%w/v的hbpak,在其余组分及成胶条件不改变的条件下,制作不具备活性氧响应性的可降解水凝胶,同样将其置于上述两种溶液中和37℃温度下,作为可降解性能比对的对照组。如图6所示,不具备ros响应性的对照水凝胶无论是在含或不含过氧化氢的pbs溶液中均缓慢降解且二者几乎没有差异,这是由于ha-ma和pegda均具备一定缓慢降解的性质;而由于hbpak和水凝胶其它组分形成了β-氨基酯,其在pbs环境中降解性能优于对照组;而由于活性氧响应性触发交联结构断裂等,所制备的水凝胶组分在含有过氧化氢的pbs溶液中进一步降解加速。
[0055]
为考察实施例1制备的水凝胶组分对细胞的急毒性,制备500μl水凝胶并将其浸泡在2ml含有10%胎牛血清的α-mem培养基或高糖dmem培养基中,于37℃条件下浸泡24h,将得到的浸提液用0.22μm的微孔滤膜过滤灭菌。将骨髓间充质干细胞或施万细胞分别以每孔5
×
103的密度接种于96孔的细胞培养板中,用正常的培养基培养24h(骨髓间充质干细胞用含10%fbs的α-mem培养基,施万细胞用含10%fbs的高糖dmem培养基)进行种板,然后换水凝胶材料的浸提液继续进行细胞培养,培养1天后,用cck-8法进行细胞活性的检测。如图7所示,骨髓间充质干细胞和schwann细胞的存活率均高于85%,表明本实施例制得的水凝胶材料对细胞的毒性可以忽略。
[0056]
为考察实施例1制备的骨髓间充质干细胞/可降解水凝胶复合材料的生物相容性,制备包含有240万骨髓间充质干细胞的300μl水凝胶并将每块水凝胶均分成2小块置于48孔板中,同时添加1ml含有10%胎牛血清的α-mem培养基进行培养,于37℃条件下浸泡24h或72h后行死活染色。如图8所示,结果表明该骨髓间充质干细胞/可降解水凝胶复合材料中的细胞组分可以在较长时间内保持存活并具有一定的增殖效果,该复合材料的生物相容性较好。
[0057]
为考察实施例1制备的髓间充质干细胞/可降解水凝胶复合材料中活性氧响应性可降解水凝胶组分与骨髓间充质干细胞组分在氧化应激条件下的相互作用,制备了包含有240万骨髓间充质干细胞的骨髓间充质干细胞/可降解水凝胶复合材料共计300μl,将其置于transwell培养小室的上层;同时,将已预先经由lps和ifn-γ共同刺激过的小鼠源性的单核巨噬细胞白血病细胞raw264.7种板于transwell培养小室下层并与上层材料共孵育,用于体外模拟氧化应激和炎症刺激条件。与此同时,按先前所述的组分浓度和步骤制备骨髓间充质干细胞/不可活性氧响应触发降解加速水凝胶复合材料作为对照,并按上述相同条件置于transwell小室中培养。经培养1天后,行死活染色观察骨髓间充质干细胞的死活情况。如图9所示,本发明中的骨髓间充质干细胞/可降解水凝胶复合材料中,活性氧响应性可降解水凝胶组分比之无法进行活性氧响应性的可降解水凝胶组分能更好的在氧化应激条件下保护骨髓间充质干细胞组分,实现更好、更多的骨髓间充质干细胞存活。
[0058]
为考察实施例1制备的髓间充质干细胞/可降解水凝胶复合材料在炎症环境下对巨噬细胞调控的独到优势,制备了包含有240万细胞的骨髓间充质干细胞/可降解水凝胶复
合材料共计300μl,将其置于transwell培养小室的上层,同时,将已预先经由200ng/ml ifn-γ和1μg/ml lps共同刺激过的小鼠源性的单核巨噬细胞白血病细胞raw264.7种板于transwell培养小室下层并与上层材料共孵育。作为对照的,transwell培养小室上层不防止任何细胞或材料、放置单独的骨髓间充质干细胞、单独的可降解水凝胶(同时包括具有和不具有活性氧响应性的)、以及骨髓间充质干细胞/无活性氧响应性可降解水凝胶复合材料。在共同培育1天后,分别将各组别的transwell培养小室下层的巨噬细胞消化收集后行dcfh-da活性氧探针孵育染色,经漂洗后行流式细胞术进行活性氧荧光分析。如图10所示,结果表明,单独的可降解水凝胶组分以及单独的骨髓间充质干细胞均可减少巨噬细胞中活性氧的产生,其中具有活性氧响应性的可降解水凝胶组分效果明显优于不具备活性氧响应的可降解水凝胶组分。并且,骨髓间充质干细胞/活性氧响应性可降解水凝胶复合材料具有最好的降低巨噬细胞体内活性氧产生的效果。
[0059]
实施例2
[0060]
本实施例制备一种骨髓间充质干细胞/可降解水凝胶复合材料,其包括生物相容性透明质酸组分、活性氧响应性可降解超支化聚合物组分,以及细胞粘附肽ikvav、细胞增殖生长因子碱性成纤维生长因子bfgf和表皮生长因子egf,以及骨髓间充质干细胞。其中,所述的透明质酸组分是数均分子量为120,000的透明质酸经甲基丙烯酸酯改性而成,所述的活性氧响应性超支化聚合物是以聚乙二醇二丙烯酸酯及ros响应性酮缩硫醇二胺经迈克尔加成反应制得。其中,聚乙二醇二丙烯酸酯的分子量为575da。合成所得的活性氧响应性可降解超支化聚合物hbpak的数均分子量为6000da;合成所得的甲基丙烯酸酯改性的透明质酸分子量约为115kda。
[0061]
其制备包括以下步骤:
[0062]
取合成的分子量约为115kda的纯净ha-ma 6mg加入到1.5ml离心管中,加入由新合成hbpak所配制的含有60mg hbpak溶质的pbs溶液490μl进行充分溶解后,加入30μl新配制的10mg/ml ikvav的pbs溶液、30μl新配制的含1.0wt%lap的pbs溶液、含500μg/mlbfgf或egf的pbs溶液各25μl进行充分混匀,得到600μl水凝胶预聚液。同时,将100~120g雄性sd大鼠胫骨和腓骨处提取,并培养三代或以上的骨髓间充质干细胞采用胰蛋白酶消化并以1000rpm转速离心5min,去除上清液后用培养基重悬,计数,稀释后获得600万细胞,离心去上清后用预聚液重新吹打重悬,得到含有8
×
106/ml细胞密度的水凝胶预聚液。随后,分别取30μl负载有bmscs的水凝胶预聚液转移并依次填充入带有多个尺寸为长约2mm、宽度为2.5mm、深度为2mm圆柱形凹槽的聚四氟乙烯模板中,并将模板送入紫外光固化箱进行紫外光固化,以50mw/cm2的光照强度进行紫外光照30s即可得到骨髓间充质干细胞/可降解水凝胶复合材料(具有活性氧响应性)。
[0063]
经计算得,该骨髓间充质干细胞/可降解水凝胶复合材料(具有活性氧响应性)中ha-ma的终浓度为1.0%w/v,hbpak的终浓度为10%w/v,ikvav细胞粘附肽的终浓度为500μg/ml;生长因子的浓度约为20μg/ml。作为对照,在保持其它组分和光照条件不变的情况下,将终浓度为10%w/v的hbpak替换为终浓度为0.6%w/v的pegda575,以此构建不具有活性氧响应性的骨髓间充质干细胞/可降解水凝胶复合材料。
[0064]
为考察实施例2制备的骨髓间充质干细胞/可降解水凝胶复合生物材料对脊髓损伤的修复和促进神经再生作用,按上述条件系列制备尺寸为长2mm、宽2mm、高2.5mm的,具有
或不具备ros响应性的骨髓间充质干细胞/可降解水凝胶复合生物材料。随后,采用紫外线灯对工作间和操作台进行充分消毒灭菌,并采用75%乙醇对相应手术器械进行浸泡以实现灭菌。随后,采用1%戊巴比妥钠按4.5ml/1kg体重的用量进行腹腔注射麻醉术前1天已禁食禁水的sd大鼠,用电动剃毛刀剔除大鼠背部被毛,固定大鼠四肢,使其俯卧位固定于手术台架上。用浸泡在聚维酮碘溶液中的棉球消毒大鼠手术部位后,打开椎板t9-t11上方背侧线中间皮肤,切口长度约2cm。分离t10水平的肌肉,充分暴露椎骨后去除椎板,并充分暴露t10水平脊髓。采用显微手术剪切除t9-10水平约2mm长度的脊髓,该过程中尽量避免损伤脊髓的脉管系统。用干燥的无菌棉球充分止血后,移植本发明所提及的具有活性氧响应性和消除能力的骨髓间充质干细胞/可降解水凝胶复合生物材料thief-cells作为治疗组,移植具有活性氧响应性和消除能力的骨髓间充质干细胞/可降解水凝胶复合生物材料phief-cells、有活性氧响应性和消除能力的可降解水凝胶单一材料thi gel以及不治疗组作为对照组,同时,将不采取任何治疗的组别作为脊髓损伤对照组,并进行筋膜、肌肉、皮肤等的缝合;并且,将皮肤、肌肉、筋膜等分离并充分暴露椎骨后不进行椎板咬合及脊髓切除而立即重新缝合的组别作为假手术组。在术前、术中和术后分别给予2ml生理盐水腹腔注射。待大鼠苏醒后进行耳钉标记,悉数记录后放回笼舍。术后毎天按摩膀胱两次促进其排尿,直至大鼠可以自主排尿;连续14天每天给予20万单位青霉素钠注射,以防止血尿。若大鼠在术后第一天即可用后肢支撑身体行走,则认为脊髓全切模型制作失败,应当予以排除。图11(a)和(b)分别展示了脊髓损伤造模和取材时的图片。
[0065]
为考察实施例2所移植本发明所述复合材料对脊髓损伤后炎症改善的评定,在术后7天取材进行石蜡包埋和切片后行8-ohdg和dhe荧光染色用于表征dna氧化损伤和超氧阴离子自由基产生情况;如图12显示,在移植了具有ros响应性的可降解水凝胶后(无论是否负载bmscs),损伤部位周围超氧阴离子自由基产生显著下降,且dna氧化损伤明显减轻,这表明本实施例中的骨髓间充质干细胞/可降解水凝胶复合材料后可通过消除ros来减轻机体组织的炎症反应。
[0066]
为考察实施例2所移植材料对脊髓损伤后长期神经修复再生效果,在术后56天取材后进行石蜡包埋和切片后行行nf200和gfap免疫荧光染色用于表征神经纤维的再生情况,以及星形胶质细胞活化及产生胶质瘢痕情况;同时,在治疗期间,每7天行一次行为学评分。如图13显示,在移植了本发明所述骨髓间充质干细胞/可降解水凝胶复合材料后,损伤大鼠的行为学评分明显高于缺损模型组和其它两组对照组,且在损伤区域,再生神经纤维的荧光密度和强度明显高于其它组别,而胶质瘢痕活化情况明显改善。这表明,本实施例所制备的骨髓间充质干细胞/可降解水凝胶复合材料后可促神经进修复再生。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1