一种面向手术机器人的基于红外光控制的给药机构
1.本实用新型涉及微创手术机器人辅助领域,具体是一种面向手术机器人的基于红外光控制的给药机构。
背景技术:
2.微创手术是对普通外科手术的一个重大革新,是指利用腹腔镜、胸腔镜现在医疗器械以及相关设备在体腔内部进行的手术。与传统手术相比,微创手术最明显的优势是创口小、疼痛轻、恢复快。
3.随着微创手术的发展,微创手术机器人也被广泛的关注。微创手术机器人包括外科手术控制台、机械臂系统、成像系统。外科手术控制台只要是接收外科医生的命令,将需要执行的操作通过计算机程序传达给机械臂系统和成像系统。机械臂系统包括机械臂、动力机构、手术器械。机械臂控制手术器械的运动,调整器械的位置;手术器械伸入体内,用于手术操作;动力机构驱动手术器械的末端执行器进行相应的操作。
4.传统的手术器械尺寸大、刚度高、结构复杂,不利于手术的顺利开展,对执行手术操作的医生要求较高。所以有必要进一步的简化手术器械的结构、缩小尺寸、解决高刚度问题。
技术实现要素:
5.为了解决上述问题,本实用新型提出一种面向手术机器人的基于红外光控制的给药机构。
6.一种面向手术机器人的基于红外光控制的给药机构,包括能够控制机器人经自然腔道通过直线运动进入体内的直线电机、设置在直线电机上具有夹持、旋转功能并且夹持位置可调的旋转电机、设置在旋转电机上通过红外光控制刚度可变的给药机构、通过3d打印的支架固定在旋转电机中空轴上用于改变夹持给药机构位置的夹持开关。
7.所述的旋转电机的中空轴与夹持开关处于一条直线上。
8.所述的给药机构包括用于携带所需要投放的药物的熔融相变尖端、与熔融相变尖端配合用于控制机构整体刚度变化的红外控制模变段。
9.所述的熔融相变尖端由sma和其表面包裹的多功能保护层组成,所述的多功能保护层采用便于保护人体组织免受机构尖端伤害、载药和熔融状态下释药的静电纺丝结构。
10.所述的静电纺丝结构中能够掺杂用于拓展熔融相变尖端的工作空间并实现熔融相变尖端位置的微调磁性颗粒。
11.所述的多功能保护层的主要材料为具有低熔点特性的聚己内酯。
12.所述的sma为具有形状记忆功能的镍钛合金丝构成。
13.所述的红外控制模变段由sma和其表面的pda涂层组成,在有红外光的控制下,sma在表面pda涂层的辅助下,将红外光的光能转化为热能,使sma的温度升高,当温度达到a
f
以上时,sma会完成奥氏体相变,此时sma的弹性模量增加,其他零件的刚度提升。
14.所述的夹持开关夹持功能的实现主要是依靠具有单出轴的中空轴步进电机结合继电器构成,将继电器的封装的塑料外壳去除,暴露出其内部的电磁系统,电磁系统主要包括铁芯、线圈、衔铁、触点簧片。
15.本实用新型的有益效果是:本实用新型采用红外光控制机构,是一种安全的、无线的控制方式,红外控制首先是红外给机构提供升温的条件,在有需要时利用红外的高能量提高机构的工作温度,切换工作模式,实现不同功能;给药机构尖端包裹的低熔点聚合物材料,即lmpm,通过静电纺丝的方式结合在sma上,纺丝结构的疏松多孔的特性,便于药物的存放和运输;红外控制另一个作用就是可以熔融尖端的lmpm,熔融后的lmpm容易与机构剥离,可以实现在定点释放药物,再者,尖端的lmpm在机构与活体组织之间起到缓冲作用,进一步提高了机构的安全性。
附图说明
16.下面结合附图和实施例对本实用新型进一步说明。
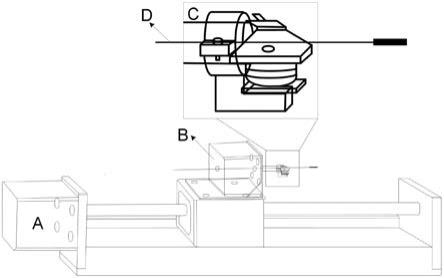
17.图1为本实用新型的立体结构示意图;
18.图2为本实用新型的给药机构结构示意图;
19.图3为本实用新型的给药机构局部剖视结构示意图。
具体实施方式
20.为了使本实用新型实现的技术手段、创作特征、达成目的与功效易于明白了解,下面对本实用新型进一步阐述。
21.如图1至图3所示,一种面向手术机器人的基于红外光控制的给药机构,包括能够控制机器人经自然腔道通过直线运动进入体内的直线电机a、设置在直线电机a上具有夹持、旋转功能并且夹持位置可调的旋转电机b、设置在旋转电机b上通过红外光控制刚度可变的给药机构d、通过3d打印的支架固定在旋转电机b中空轴上用于改变夹持给药机构d位置的夹持开关c。
22.本实用新型采用红外光控制机构,是一种安全的、无线的控制方式,红外控制首先是红外给机构提供升温的条件,在有需要时利用红外的高能量提高机构的工作温度,切换工作模式,实现不同功能:1.低刚度、顺应性、可在自然腔道内无创的被动顺应的运动模式,例如,利用顺应性可以预定义机器人的曲率,实现复杂弯曲管道内的运动;2.高刚度、可注射、可给药的精准操作的手术模式。
23.本实用新型利用红外光控制实现手术器械的变刚度,该机构具有两种工作
24.模式
25.1、在无红外光控制的情况下,机构是处于低刚度、顺应性、可在自然腔道内无创的被动顺应的运动模式,例如,利用顺应性可以预定义末端执行器的曲率,实现复杂弯曲管道内的运动。
26.2、有红外光控制的情况下,处于高刚度、可注射、可给药的精准操作的手术模式,该机构的尺寸可以达到亚毫米级别,结构简单,红外光控制既可以调节该机构的工作模式,另一方面,红外光可以控制机构尖端载药结构熔融脱落,实现定点给药。
27.在尺寸上,给药机构的直径可以控制在亚毫米级别,本实用新型中使用的是sma
丝,单根丝的直径在0.3mm,是目前比较先进的内窥镜手术机器人的末端执行器都难以达到的尺寸。适用于血管、消化道、气管等结构复杂、空间狭窄的腔道内。
28.本实用新型中使用的材料均为生物相容性材料,安全性高。机构的结构简单、成本低廉。
29.所述的旋转电机b的中空轴与夹持开关c处于一条直线上。
30.所述的给药机构d包括用于携带所需要投放的药物的熔融相变尖端1、与熔融相变尖端1配合用于控制机构整体刚度变化的红外控制模变段2。
31.所述的熔融相变尖端1由sma22和其表面包裹的多功能保护层11组成,所述的多功能保护层11采用便于保护人体组织免受机构尖端伤害、载药和熔融状态下释药的静电纺丝结构。
32.所述的多功能保护层11是为了充分发挥机构载药释药的能力,另一方面起到缓冲保护作用,可以理解的是,在材料和长度相同的情况下,棒材的刚度k与横截面积正相关,横截面积越小,k越小,柔度就越大,但是,另一方面横截面积越小,sma尖端的压强越大,在机构在体内运动时容易对周围软组织产生伤害。
33.所述的多功能保护层11的主要材料为具有低熔点特性的聚己内酯,即pcl,pcl是一种生物相容性良好的有机高分子聚合物,在可控释药载体、细胞和组织培养基架类方面具有重要应用,pcl应用于体内完全可降解,具有良好的生物降解性,降解产物为co2和h2o;另一方面pcl也非常柔软,易溶于多种极性有机溶剂。
34.所述多功能保护层11的结构为静电纺丝结构,pcl静电纺丝是疏松多孔的结构,疏松多孔结构具有较大的比表面积,可以增加pcl与sm,22表面的粘附性,使得pcl纺丝可以包裹吸附在sma22表面;另一方面,多孔结构便于装载和运载药物;pcl静电纺丝结构包裹sma22具体的操作为:静电纺丝过程中,在静电场中加一根匀速旋转的sma22丝,由于高压静电场的作用,暴露在静电场中的sma22就会包裹上一层纺丝结构,使用的纺丝液是丙酮溶解的pcl溶液,在纺丝过程中丙酮随着纺丝液流出针管,大面积的暴露在空气中而挥发,最终包裹在sma表面的物质就只剩下pcl。
35.所述的sma22为具有形状记忆功能的镍钛合金丝构成。
36.红外光可以控制红外控制模变段2弹性模量的变化,这也是本实用新型中可变刚度的主要原因,熔融相变尖端1同样受到红外光的控制,红外光对于尖端来说,有两方面的作用:1.控制多功能保护层下的sma22产生相变,进入手术模式;2.控制多功能保护层11的熔融,便于保护层脱落,将药物定点释放。
37.所述的静电纺丝结构中能够掺杂用于拓展熔融相变尖端1的工作空间并实现熔融相变尖端1位置的微调磁性颗粒。
38.所述的红外控制模变段2由sma22和其表面的pda涂层21组成,在有红外光的控制下,sma22在表面pda涂层21的辅助下,将红外光的光能转化为热能,使sma22的温度升高,当温度达到a
f
以上时,sma22会完成奥氏体相变,此时sma22的弹性模量增加,其他部件的刚度提升。
39.所述的sma22的丝直径为0.3mm,属于温控型sma,可以理解的是,sma22丝的刚度与其横截面积成正比,横截面积越大,同样长度的sma22的刚度越高,所以,sma22直径对于本实用新型是一个重要的参数,sma22的直径直接决定了该机构的尺寸范围;将机构整体尺寸
控制在亚毫米级别,另一方面,确定了机构的刚度范围,购买了市面上的各种直径的sma22丝进行刚度测试,水凝胶具有与人体组织相似的刚度,利用水凝胶模拟人体组织,利用sma对人造组织进行穿刺实验,最后,优选出直径为0.3mm的sma22丝,因为选用0.3mm的sma22丝作为本实用新型的主体,在红外灯关闭时,该机构无法刺破人造组织,表明机构运动时不会对人体组织产生威胁,具有良好的被动顺应性,打开红外灯后,该机构在几十秒内完成工作模式的切换,精准的对人造组织进行穿刺操作。
40.所述的sma22其马氏体结束温度m
f
为30℃左右,奥氏体结束温度a
f
为50℃。所述的多功能保护层11使用的pcl为低熔点聚合物材料lmpm,熔点在60℃,可以知道的是,人体正常体温在37.5℃,介于m
f
与a
f
之间,说明在正常人体内给药机构可以保持低刚度、被动顺应性。只有当外部条件改变时,给药机构升温至a
f
以上,才会发生工作模式的改变。给药机构工作模式的切换主要依靠红外光控制,体内环境的影响较小,另一方面lmpm的熔点高于a
f
,但是又与a
f
相近,说明给药机构可以在手术模式下将多功能保护层熔融,实现在手术模式下同时进行给药操作。多功能保护层熔融后,纺丝结构中的大量的孔隙会随之消失,促进孔隙中装载的药物释放。
41.采用红外光控制机构工作模式的切换,相较于其他控制方式,光控制是一种无约束的控制方式,红外光源能量较高,对人体来说也是一种较为安全的光源,给药机构将红外光的能量转化为热能,给机构升温,大大提高了机构的刚度,实现工作模式切换,另一方面帮助多功能保护层与sma22剥离,实现定点给药。
42.为了提高sma22的光热响应,将sma表面包覆上聚多巴胺pda纳米颗粒。pda是一种常用的光热填充剂,可以将光能转化为热能,具有良好的光热效应,pda的优势在于其合成的原料天然,成本低,制备方法简单,而且pda涂层21几乎可以应用于任何材料表面,不受材料的化学性质影响,因此pda涂层21被广泛的应用于各个领域,具体的操作步骤为:对购买的sma材料表面进行处理,将sma22用1000目砂纸进行打磨和酒精擦拭。在250ml的圆底烧杯中加入90ml去离子水和20ml乙醇,将两者混合。继续加入5ml28%
‑
30%氨水,常温搅拌均匀;然后配制10ml的质量浓度为50mg/ml盐酸多巴胺水溶液,将盐酸多巴胺水溶液快速加入上述溶液中,继续搅拌。最后将打磨擦拭处理后的sma加入,使sma完全浸泡在溶液中,让烧杯内溶液充分接触空气氧化,持续搅拌24h。
43.当给药机构d的熔融相变尖端1到达指定点或者指定点附近,需要在这一片区域操作时,这种情况下,不断从机构末端调整熔融相变尖端1的位置较为繁琐,目标点每改变一次,就需要从末端位置开始调整,运动从末端传递到尖端需要的时间也较长,而且这种方式不利于末端执行器位置细微的调整。并且机构整体的运动会给病人带来不必要的和过多的负担,造成病人的不适感加重,所以对熔融相变尖端1进行了进一步的调整,让尖端具有灵活的运动能力,在末端执行器包裹的pcl多功能保护层11中加入了fe3o4磁性颗粒,具体的步骤与上述的静电纺丝过程类似:将10%的pcl纺丝液换成等量的pcl与fe3o41:1混合的纺丝液;再按照pcl静电纺丝同样的方法将sma尖端包裹上pcl/fe3o4纺丝薄膜;在加入了fe3o4颗粒之后,尖端的多功能保护层就具有磁性。可以利用磁场控制尖端小幅度的摆动。
44.fe3o4作为光热剂常用于光热治疗,四氧化三铁颗粒具有一定的光热效应,掺杂了fe3o4颗粒的多功能保护层更容易达到熔融的条件,降低了保护层熔融的难度,便于药物释放。
45.给药机构d通过红外光控制变形,但是自身无法运动,需要依靠外部驱动来控制给药机构d整体运动,电机a可以控制机器人通过自然腔道进入体内,控制直线运动的电机a带动上面的旋转电机b运动,使得给药机构d具有直线和旋转方向的自由度。
46.所述的夹持开关c夹持功能的实现主要是依靠具有单出轴的中空轴步进电机b结合继电器构成,将继电器的封装的塑料外壳去除,暴露出其内部的电磁系统,电磁系统主要包括铁芯、线圈、衔铁、触点簧片,当线圈两端加上一定的电压,线圈中会流过一定的电流,线圈附近会产生电磁效应,衔铁就会受到电磁力的吸引克服弹簧的拉力吸向铁芯,衔铁和铁芯的吸附力足以将给药机构d固定不发生相对位置的偏移。
47.将夹持开关c通过3d打印的支架与电机b的中空轴固定,使得夹持开关c和中空轴在一条直线上。给药机构d穿过中空轴在衔铁和铁芯中间,具有夹持功能是希望给药机构d可以拥有旋转自由度,电机b的转轴是中空的,中空部分可以用于放置给药机构d,使得电机b与给药机构d处于接近同轴状态,但是同时它们在直线上的相对位置可以移动,实现了夹持位置可调的功能。
48.以上显示和描述了本实用新型的基本原理、主要特征和本实用新型的优点。本行业的技术人员应该了解,本实用新型不受上述实施例的限制,上述实施例和说明书中描述的只是本实用新型的原理,在不脱离本实用新型精神和范围的前提下,本实用新型还会有各种变化和改进,这些变化和改进都落入要求保护的本实用新型范围内。本实用新型要求保护范围由所附的权利要求书及其等效物界定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1