真空辅助电穿孔装置以及相关系统和方法与流程
真空辅助电穿孔装置以及相关系统和方法
1.相关申请的交叉引用
2.本技术要求于2020年3月20日提交的美国临时申请第62/992,513号的权益,所述美国临时申请的全部内容通过此引用并入本文。
技术领域
3.本发明涉及用于利用真空压力夹持组织和使组织变形、将流体注入组织中以及用电极对组织进行电穿孔的装置,以及涉及将流体注入或以其它方式递送到组织中和对组织进行电穿孔的系统和方法。
背景技术:
4.在20世纪70年代,发现电场可以用于在细胞中产生孔,而不会对细胞造成永久性损伤。这种被称为电穿孔(ep)的发现使大分子、小分子、离子和水能够通过细胞壁引入到细胞的细胞质中。在一些情况下,电穿孔可以用于如头颈癌等局部治疗,以将化学品和其它化合物引入到肿瘤中。在这些手术中,患者可能或可能不经受全身麻醉,因此必须使疼痛和不自主的肌肉运动最小化。
5.皮肤是ep的受欢迎的靶标,因为其很容易进入并且含有多种适于递送dna疫苗的免疫细胞。皮肤的天然免疫功能以及其高细胞更新速率通常会产生对ep增强的dna疫苗递送的快速、强烈的体液应答。在ep增强的dna疫苗递送后,皮肤也能够产生细胞免疫应答。由于皮肤的浅表性性质,因此皮肤适于微创或无创ep。
6.骨骼肌也是体内电穿孔介导(ep)递送dna的充分表征的靶标。肌细胞能够产生和分泌蛋白质持续长时间段,并且已经反复证明,将ep增强的dna疫苗接种到肌肉中能够产生免疫应答。然而,肌肉ep dna递送的应用因皮下脂肪的厚度变化而变得复杂,从而阻止了“一刀切”方法,因为不同的脂肪厚度会导致针穿透肌肉组织的深度不同。由于隔离皮下脂肪层和产生电场所需的深度,骨骼肌,特别是大型动物和人类的骨骼肌,通常不适于微创或无创ep技术。因此,穿透针电极最常用于在肌肉中进行ep。
7.历史上,脂肪组织(脂肪)一直被视为是一种主要用于以脂滴的形式储存能量的惰性组织。如此,直到最近ep增强的dna手术才针对组织的脂肪层进行。然而,最近的研究表明,皮下脂肪实际上起到许多动态作用。脂肪组织含有许多干细胞和免疫细胞,通过分泌大量激素作为内分泌器官,分泌许多局部信号,并且含有精细的毛细血管网络。实现脂肪组织的体内转染的尝试主要限于需要施用者切开并物理去除患者皮肤的样品以允许直接接触脂肪组织的外科手术技术。这些治疗极具侵入性,并且不适于临床装置。
技术实现要素:
8.根据本公开的一个实施例,一种用于组织的真空辅助体内电穿孔的装置包含壳体,所述壳体限定室和通向所述室的至少一个开口。端口延伸穿过所述壳体并远离所述至少一个开口并可与真空源连接。所述端口被配置成将真空压力从所述真空源传送到所述
室。多个电极定位在所述室内,并且被配置成将一个或多个电穿孔脉冲递送到组织的靶向部分,响应于所述真空压力,所述靶向部分延伸穿过所述开口并至少暂时保持在所述室中。
9.根据本公开的另一个实施例,一种对受试者的组织进行电穿孔的方法包含将室放置在所述组织附近,向所述室施加真空压力,从而通过所述室的开口抽吸所述组织,以及与沿所述室的内表面延伸的多个电极接触,并且通过所述多个电极将一个或多个电穿孔脉冲递送到所述组织,从而在所述组织内产生电穿孔场。
10.根据本公开的另外的实施例,一种用于组织的真空辅助处理的装置包含壳体,所述壳体限定室和通向所述室的至少一个开口。第一端口延伸穿过所述壳体并远离所述至少一个开口。所述第一端口可与真空源连接,使得所述第一端口被配置成将真空压力从所述真空源传送到所述室。所述装置包含穿过第二端口延伸到所述室中的射流注射装置。所述第二端口与至少一个开口相对。所述射流注射装置被配置成将流体的射流注射递送到组织的靶向部分,响应于所述真空压力,所述组织的靶向部分延伸穿过所述至少一个开口并至少暂时保持在所述室中。
附图说明
11.本专利申请含有至少一幅彩色附图。在请求并支付必要的费用后,官方将会提供带有彩色附图的本专利申请的副本。当结合附图阅读时,将更好地理解前述发明内容以及以下本技术的说明性实施例的具体实施方式。出于说明本技术的结构的目的,在附图中示出了说明性实施例。然而,应当理解,本技术不限于所示的精确布置和手段。在附图中:
12.图1是根据本公开的实施例的使用真空辅助电穿孔杯(或“真空杯”)与针注射装置的组合的电穿孔系统的示意视图;
13.图2a是根据本公开的实施例的图1中所展示的真空杯的透视图,示出了杯的真空室和位于所述室内的电极的阵列;
14.图2b是图2a中所展示的真空杯的底部平面视图,示出了电极排成阵列的图案;
15.图2c是图2a-2b中所展示的电极之一的平面正视图;
16.图2d是图2a中所展示的真空杯的沿杯的中心轴线截取的截面侧视图;
17.图2e是图2d中所展示的区域2e-2e的放大截面视图;
18.图2f是图2d中所展示的区域2f-2f的放大截面视图;
19.图3a是承载电极并可插入图2a中所展示的真空室内的套筒的透视图;
20.图3b是图3a中所展示的套筒的底部平面视图;
21.图3c-3d、3e-3f、3g-3h、3i-3j和3l-3m是根据本公开的另外的实施例的具有替代性电极阵列图案的套筒的相应的底部平面视图和截面侧视图;
22.图4a-4e是图2a中所展示的邻近组织的真空杯截面侧视图,示出了在真空辅助电穿孔处理中使用真空杯的代表性阶段;
23.图4f是图2a中所展示的真空杯的截面侧视图,示出了真空杯可以将组织抽吸到真空室中的不同程度;
24.图5a是根据本公开的实施例的具有柔性电极的真空杯的透视图;
25.图5b是图5a中所展示的真空杯的沿杯的中心轴线截取的截面侧视图;
26.图5c是图5b中所展示的区域5c-5c的放大截面视图,示出了处于中性状态的电极;
27.图5d是图5b中所展示的区域5d-5d的放大截面视图,示出了处于弯曲状态的电极;
28.图6a和6b是根据本公开的实施例的具有限定突起的接触表面的电极的相应的透视图和侧正视图;
29.图6c和6d是根据本公开的另一个实施例的具有限定侧向伸长突起的接触表面的电极的相应的透视图和侧正视图;
30.图7a是根据本公开的实施例的具有三角形远侧开口和真空室几何形状的真空杯的透视图;
31.图7b是图7a中所展示的真空杯的底部平面视图;
32.图7c是图7a中所展示的真空杯的沿杯的中心轴线截取的截面透视图;
33.图7d是定位在图7a中所展示的真空杯内的电极阵列的正视平面图;
34.图7e是图7d中所展示的电极阵列的侧视图;
35.图8a是根据本公开的实施例的具有矩形远侧开口和真空室几何形状的真空杯的透视图;
36.图8b是图8a中所展示的真空杯的底部平面视图;
37.图8c是图8a中所展示的真空杯的沿杯的中心轴线截取的截面透视图;
38.图9a是根据本公开的实施例的包含真空杯的电穿孔组合件的截面侧视图,所述真空杯具有收纳无针注射装置的收纳器;
39.图9b是放大截面侧视图,示出了使用图9a中所展示的电穿孔组合件将药剂注射到抽吸到真空室中的组织中的代表性阶段;
40.图10a是具有收纳无针注射装置的收纳器的真空杯的另一个实施例的截面透视图,其中所述真空杯具有限定歧管的杯壳体,所述歧管包含多个端口,所述多个端口通过限定在所述电极中的对应的多个孔与所述真空室流体连通;
41.图10b是图10a中所展示的对应的端口和孔的放大透视、局部截面视图;
42.图10c是根据本公开的另一个实施例的对应的端口和孔的替代性布置的透视、局部截面视图;
43.图10d是图10a中所展示的真空杯的一部分在用于向脂肪组织提供电穿孔治疗期间的放大截面侧视图;
44.图11a是通过与图2a中所展示的杯类似配置的真空杯在没有施加真空压力(左)和施加真空压力(右)的情况下猪皮下组织中亚甲蓝分布的视觉表示;
45.图11b和11c示出了注射亚甲蓝后豚鼠脂肪组织中的流体分布的并排比较;图11b中的注射是用与图9a中所示的无针真空杯类似的无针真空杯进行的;图11c中的注射是用皮下针技术进行的;
46.图12是示出用pgx 2013(一种针对流感病毒核蛋白(np)的dna疫苗)在脂肪组织中电穿孔处理后豚鼠中12周体液免疫原性elisa数据的图,尤其示出了用以下进行电穿孔处理后的比较体液免疫应答;图2a中所展示的真空杯;以及卡尺电极电穿孔装置;
47.图13是示出豚鼠在用pgx 2303(一种针对人呼吸道合胞病毒融合乙二醇蛋白(rsv-f)的dna疫苗)处理后的8周体液免疫原性elisa数据的图,尤其示出了以下的比较体液免疫应答:用图2a中所展示的真空杯对脂肪组织进行电穿孔处理;以及使用现有技术的针阵列电穿孔装置在皮肤中进行电穿孔处理;
48.图14a是示出豚鼠在pgx 2013(一种针对流感病毒核蛋白(np)的dna疫苗)处理后6周体液免疫原性elisa数据的图,尤其示出了在涉及以下的处理后的比较体液免疫应答:(1)使用现有技术的针阵列电穿孔装置对皮内组织进行电穿孔;(2)用图9a中所展示的无针真空杯对脂肪组织进行电穿孔,其中施加了电穿孔后真空压力;(3)用图2a中所展示的针注射真空杯注射到脂肪组织中,其中施加了注射后真空压力,但未进行电穿孔;(4)以及用图2a中所展示的针注射真空杯对脂肪组织进行电穿孔,其中施加了电穿孔后真空压力;
49.图14b是示出来自图14a中所展示的相同研究的细胞免疫应答的图表;
50.图15a是根据本公开的实施例的配置用于皮内组织的真空辅助电穿孔的真空杯的透视图;
51.图15b是图15a所示的真空杯的横截面侧视图;
52.图15c是图15a所示的杯的真空室使用期间的放大横截面视图;
53.图16a-16b是根据本公开的实施例的真空电穿孔组合件的横截面侧视图,其中电极安置在相应的真空室内的与真空室的相应的远侧开口相对的端表面上;
54.图17a-17b是根据本公开的实施例的限定在相应的电极支撑构件上的电极阵列图案和真空端口图案的底部平面视图,用于与图16a-16b所示的组合件一起使用;
55.图18a是具有多个远侧真空室的真空电穿孔装置的透视图;
56.图18b是图18a所示的真空电穿孔装置的横截面透视图;
57.图18c是图18a所示的真空电穿孔装置的侧视横截面视图;
58.图18d是图18c所示的区域18d-18d的放大横截面视图;
59.图18e是图18a所示的真空电穿孔装置的底部平面视图;
60.图19a是根据本公开的实施例的真空电穿孔装置的横截面侧视图,所述真空电穿孔装置具有远侧阵列的电极,所述电极其中具有真空端口;
61.图19b是根据本公开的实施例的图19a所示的真空电穿孔装置的底部平面视图,示出了电极阵列图案的平面视图;
62.图20是具有正方形电极阵列的电极支撑构件的平面视图,所述正方形电极阵列被配置成与类似于图19a所示的真空电穿孔装置一起使用;
63.图21a是具有矩形电极阵列的电极支撑构件的平面视图,所述矩形电极阵列在其它方面类似于图20所示的电极支撑构件;
64.图21b是图21a所示的电极支撑构件的侧视横截面视图;
65.图22是示出皮内注射各种体积的编码绿色荧光蛋白(gfp)基因的质粒,然后用各种技术和装置处理后豚鼠皮肤中的基因表达的图;
66.图23是示出豚鼠在hpv dna疫苗处理后8周体液免疫原性elisa数据的图,尤其示出了在使用以下在皮肤中进行相应的电穿孔处理后的比较体液免疫应答:现有技术的针阵列电穿孔装置;图2a所示的真空杯;以及图2a所示的真空杯,其剂量是其它处理的三倍(3x);
67.图24a是示出非人灵长类动物模型在hpv dna疫苗(pgx 3001和3002)处理后11周体液免疫原性elisa数据的图,尤其示出了在使用以下在皮肤中进行相应的电穿孔处理后的比较体液免疫应答:现有技术的针阵列电穿孔装置;图2a所示的真空杯;以及图2a所示的真空杯,其剂量是其它处理的三倍(3x);
68.图24b-24c是示出来自图24a所示的相同研究的细胞免疫应答的图;
69.图25是示出由现有技术的芒图注射(mantoux injection)产生的一对泡的透视图的断层扫描图像;左侧示出的泡含有与透明质酸酶调配物预混合的药剂;并且右侧示出的泡是在没有透明质酸酶调配物的情况下注射的;
70.图26是示出图25所示的泡的顶部视图和透视图的合成图像;
71.图27是示出在用针对mers(pgx 9101)的dna疫苗进行皮内处理后豚鼠中4周体液免疫应答数据的终点滴度的图,尤其示出了使用以下在皮肤中进行相应的电穿孔处理后的比较体液免疫应答:现有技术的针阵列电穿孔装置,具有和不具有透明质酸酶调配物;以及图2a所示的真空杯的一种形式,其具有15mm的室直径,具有和不具有透明质酸酶调配物;
72.图28是示出在用mers dna疫苗(pgx 9101)皮内处理后豚鼠中以终点滴度表示的6周体液免疫原性数据的图,尤其示出了使用以下在皮肤中进行相应的电穿孔处理后的比较体液免疫应答:现有技术的针阵列电穿孔装置;以及图2a所示的真空杯的一种形式,其具有15mm和10mm的室直径;
73.图29a是示出在皮内注射针对流感核蛋白的dna疫苗(pgx 2013)后豚鼠中以平均终点滴度表示的6周体液免疫原性数据的图,尤其示出了使用以下在皮肤中进行相应的电穿孔处理后的比较体液免疫应答:现有技术的针阵列电穿孔装置;以及图2a所示的真空杯的一种形式,其具有15mm的室直径;
74.图29b和29c是示出来自图29a所示的相同研究的第2周(图29b)和第4周(图29c)的细胞免疫应答的图,以斑点形成单位表示;
75.图30a示出了圆形电极阵列的透视图,所述圆形电极阵列具有围绕中心轴线以90度间隔隔开的四(4)个电极,用于与本公开的圆形开口真空杯一起使用以对脂肪组织进行电穿孔;图30b-30f展示了根据各种电极大小在脂肪组织中产生的各种模拟电场强度;
76.图31a示出了图30a所示的圆形电极阵列的透视图,用于对皮肤组织进行电穿孔;图31b-31f展示了根据各种电极大小在皮肤组织中产生的各种模拟电场强度;
77.图32a示出了矩形电极阵列的透视图,所述圆形电极阵列具有围绕中心轴线以90度间隔隔开的四(4)个平面电极,用于与本公开的矩形开口真空杯一起使用以对脂肪组织进行电穿孔;图32b-32f展示了根据各种电极大小在脂肪组织中产生的各种模拟电场强度;
78.图33a示出了图32a所示的矩形电极阵列的透视图,用于对皮肤组织进行电穿孔;图33b-33f展示了根据各种电极大小在皮肤组织中产生的各种模拟电场强度;
79.图34a-34b示出了真空辅助处理后豚鼠脂肪组织中细胞浸润(蓝色)的并排比较;图34a中的处理是使用类似于图2a中示出的真空杯的仅真空处理(即,无电穿孔);图35b中的处理是使用真空杯的真空辅助电穿孔处理(即,真空压力+电穿孔);
80.图35a是示出用针对mers的dna疫苗处理后豚鼠中6周体液免疫原性数据的图,尤其示出了在使用类似于图2a所示的,并且具有各种室直径和相同的电穿孔参数的真空杯在皮肤中进行相应的电穿孔处理后的比较体液免疫应答;
81.图35b是示出来自图35a所示的相同研究的细胞免疫应答的图;
82.图36a是示出在皮内注射编码绿色荧光蛋白(gfp)基因的质粒,然后使用真空杯在各种真空压力和电穿孔电压下处理后豚鼠皮肤中的基因表达的图;
83.图36b是示出来自图36a所示的gdf表达结果的皮肤荧光信号的测量的图;
84.图37a是示出在用针对mers的dna疫苗处理后豚鼠中6周体液免疫原性elisa数据的图,尤其示出了使用以下在皮肤中进行电穿孔处理后的比较体液免疫应答:(1)现有技术的针阵列电穿孔装置;以及(2)类似于图2a所示的真空杯;
85.图37b是示出来自图37a所示的相同研究的细胞免疫应答的图;
86.图38是示出在用针对复发性呼吸道乳头瘤病(rrp)的疫苗处理后第6周以斑点形成单位表示的细胞免疫应答的图,尤其示出了使用以下在皮肤中进行电穿孔处理后的比较应答:(1)现有技术的针阵列电穿孔装置;以及(2)类似于图2a所示的真空杯;
87.图39a是示出用针对mers的dna疫苗处理后豚鼠中4周体液免疫原性数据的图,尤其是比较仅使用芒图注射、芒图注射后真空压力以及芒图注射后真空压力和使用类似于图2a所示的真空杯的电穿孔在皮肤中进行处理后的体液免疫应答;
88.图39b是示出来自图39a所示的相同研究的细胞免疫应答的图;
89.图40a示出了由具有一对相对电极的电极阵列产生的模拟电场的横截面侧视图,所述电极阵列在被抽吸到与图2a中示出的真空杯配置类似的真空杯的组织堆中产生;
90.图40b示出了由具有一对圆环电极和中心同心电极的电极阵列产生的模拟电场的横截面侧视图,所述电极阵列在被抽吸到与图15a中示出的真空杯配置类似的真空杯的组织堆中产生;
91.图41a是示出用针对mers的dna疫苗处理后豚鼠中8周体液免疫原性数据的图,尤其是基于使用图40a-40b中示出的电极阵列的电极脉冲图案比较在皮肤中进行真空辅助电穿孔处理后的体液免疫应答;
92.图41b是示出来自图41a所示的相同研究的细胞免疫应答的图;
93.图42a是示出在芒图注射之后的对比注射剂流体分散体的图,并且:(1)不施加真空压力;(2)使用具有图40a中示出的电极阵列的真空杯施加真空压力;以及(3)使用具有图40b中示出的电极阵列的真空杯施加真空压力;
94.图42b-42d是示出图42a中绘制的流体分散体的照片;
95.图43a和4b是示出了安置在豚鼠皮肤中的注射剂的荧光镜图像,所述豚鼠皮肤定位在具有图40b中示出的电极阵列的真空杯下方;图43a示出了在室中施加真空压力之前的注射剂;图43b示出了在室中施加真空压力期间的注射剂;
96.图43c是示出比较分泌的碱性磷酸酶(seap)表达的图,如下:(1)单次高注射剂体积,使用如图43a-b所示的真空杯进行真空辅助电穿孔处理;以及(2)使用现有技术的针阵列电穿孔装置进行六次注射、六次电穿孔事件处理;
97.图44是示出在用pgx 2013在皮肤组织中进行电穿孔处理后豚鼠中8周体液免疫原性elisa数据的图,尤其示出了在用以下进行电穿孔处理后的比较体液免疫应答:(1)类似于图9a所示的射流注射真空杯;以及(2)现有技术的针阵列电穿孔装置;并且
98.图45a-47c是示出在各种真空压力设置和喷嘴到皮肤偏移距离设置下用类似于图9a所示的射流注射真空杯进行射流注射期间和之后豚鼠中的组织偏转的荧光镜图像。
具体实施方式
99.通过参考结合形成此公开的一部分的附图和实例的以下具体实施方式,可以更容易地理解本公开。应当理解,本公开不限于本文描述和/或示出的具体装置、方法、应用、条
件或参数,并且本文使用的术语仅出于通过实例描述特定实施例的目的,并不旨在限制本公开的范围。此外,如在包含所附权利要求的说明书中所使用的,单数形式“一”,“一个”和“所述”包含复数,并且除非上下文另有明确规定,否则对特定数值的引用至少包含那个特定值。
100.如本文所用,术语“多个”意指超过一个。当表达一系列值时,另一个实施例包含从一个特定值和/或到其它特定值。类似地,当通过使用先行词“约”将值表达为近似值时,将理解特定值形成另一个实施例。所有范围都是包含性的且可组合的。
101.如本文所用关于尺寸、角度和其它几何形状的术语“大约”和“基本上”考虑了制造公差。进一步地,术语“大约”和“基本上”可以包含大于或小于所述尺寸或角度的10%。进一步地,术语“大约”和“基本上”可以同样适用于所述的具体值。
102.如本文所使用的,术语“药剂”意指多肽、多核苷酸、小分子或其任何组合。所述药剂可以是编码抗体、其片段、其变体或其组合的重组核酸序列。作为非限制性实例,可以将药剂在水中或缓冲剂中调配,如盐水-柠檬酸钠(ssc)或磷酸盐缓冲盐水(pbs)。
103.如本文所使用的,术语“皮内”是指在包含表皮(即,表皮层,从角质层到基底层)和真皮(即,真皮层)的皮肤层内。
104.如本文所使用的,术语“脂肪”意指含有位于皮下层中的脂肪细胞(即,脂肪细胞)的层。
105.如本文所使用的,术语“电穿孔”意指在组织内使用电场,所述电场暂时且可逆地增加组织中细胞的细胞膜的渗透性和/或孔隙率,从而允许例如将药剂引入细胞。
106.如本文所使用的,术语“电穿孔场”意指能够对细胞进行电穿孔的电场。在电场包含能够对细胞进行电穿孔的部分和不能对细胞进行电穿孔的另一部分的情况下,“电穿孔场”特指电场的能够对细胞进行电穿孔的部分。因此,电穿孔场可以是电场的子集。
107.如本文所使用的,术语“区域”意指空间的体积,如组织内空间的体积。
108.如本文所使用的,术语“转染区域”意指发生转染的组织的体积,并且可以与术语“转染体积”同义地使用。
109.如本文所使用的,术语“细胞浸润”意指细胞迁移到一定体积的组织中。
110.如本文所使用的,术语“皮内针电极电穿孔装置”和“id针电极ep”各自是指现有技术的电穿孔装置,所述装置使用排列成三角形图案的三(3)个针电极的电极阵列以对皮内组织进行电穿孔。
111.下面描述的实施例涉及对组织进行真空辅助电穿孔的系统和装置,尤其是组织的靶向层,如皮内组织或脂肪组织。这些实施例使组织的靶向体积(或“组织体积”)经受真空压力(即,负压)以使组织以有利于在组织层中的靶标区域内对细胞进行电穿孔的方式变形。具体地,将如真空杯等真空装置的开口端放置为与覆盖组织体积的组织(例如,“皮肤”)的外表面接触,并且将真空压力施加到杯的内部,从而将组织体积抽吸到真空杯中,这将组织体积定位地固定到杯,允许定位在真空杯内的电极在组织体积内产生可预测的、基本均匀的电穿孔场,从而在组织体积内产生可预测的、基本均匀的转染区域。还观察到由下文描述的实施例提供的真空压力在组织体积内提供有利的流体再分布,包含注射剂在组织体积内有利的体内分散,以及流体进出靶标区域的有利体内进入和排出。换言之,真空压力增强了注射剂在整个组织中的分散,从而扩大了转染区域,也将更多的体内流体抽吸到靶标区
域中,从而增加了暴露于转染的细胞的细胞量。本发明人已经观察到,贯穿本公开描述的真空辅助电穿孔处理已经导致受试者对注射剂的应答增加。
112.本发明人还惊讶地和出乎意料地观察到,即使没有电穿孔,真空压力的施加也会导致组织体积内的转染。尽管不希望受任何特定理论的束缚,但本发明人认为由真空杯给予的真空压力在组织体积内的细胞膜上给予机械应力,这增加了细胞膜渗透性并因此增加了在组织体积内观察到的转染。本发明人还认为,上述流体再分布也可能至少部分地对观察到的没有电穿孔的转染负责。本发明人进一步认为,上述流体再分布和机械应力可能相互作用以在组织体积内产生有利的环境,用于将外部药剂转染到细胞中。
113.此外,下面描述的实施例也可以在使用之间和/或在使用期间进行适配,而无需机械重新配置。例如,在使用期间和/或使用之间,可以根据需要调节电极的电参数以操纵组织体积中的电穿孔场以实现有利的处理结果。另外或可替代地,可以在使用期间和/或使用之间根据需要调节真空压力,以物理地操纵组织体积以实现有利的处理结果。例如,可以施加较高的真空压力以将较大的组织体积抽吸到真空杯中,并且可以施加较低的真空压力以将较小的组织体积抽吸到真空杯中。以此方式,通过将不同的组织层选择性地暴露于电穿孔场,可以使用相同的真空杯来靶向不同的组织层进行电穿孔处理。另外,真空压力可以在使用期间脉冲,以操纵靶向的组织的机械行为,如增强组织内的流体再分布。
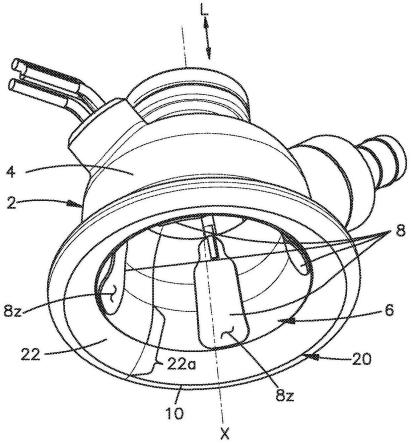
114.现在参考图1,根据本公开的用于治疗患者的电穿孔系统100包含真空辅助电穿孔装置2,所述装置包含限定内部真空室6和定位在室6内的多个电极8的壳体4(参见例如,图2a-2c)。多个电极8排列成电极8的阵列9,所述阵列也可以称为电极阵列9。装置2也可以称为“真空杯”或简称为“杯”。壳体4可以称为“杯壳体”。真空杯2被配置成使得医师可以将真空杯2的远侧端10放置在靶向的组织102的外表面101上以进行电穿孔处理,并且可以向真空室6施加真空压力以抽吸、拉动或以其它方式将组织102引入真空室6并与其中的电极8接触。电极8被配置成将一个或多个电穿孔脉冲递送到被抽吸到室6中并通过真空压力保持在其中的组织102。组织102包含靶向用于处理的层,如脂肪组织103(在本文中也称为“脂肪层”103)或皮内组织104(在本文中也称为“皮肤层”104)。
115.真空杯2包含如端口等一个或多个耦接器,用于与一个或多个外部组件连接。例如,真空杯2具有用于在真空室6和如真空泵等真空源106之间提供流体连通的第一端口12。真空杯2还可以具有第二端口14,用于提供到电路系统108的通路,所述电路系统提供电极8和如发电机等能源110之间的电通信。真空杯2可以进一步包含第三端口16,用于提供外部工具,如携带注射剂,特别是包括药剂的注射剂等的注射装置18,所述外部工具具有到真空室6的通路。如所示的,注射装置18可以是皮下注射针,但是真空杯2可以适用于其它类型的注射装置18,包含射流注射装置,如下文更详细描述的。还应当理解,在将药剂注射到组织102中之后可以任选地使用真空杯2。
116.能源110可以与如波形发生器等信号发生器112电通信,用于产生一个或多个具有特定电参数的电脉冲形式的电信号并将其传输到电极8,用于在真空室6中的组织102内对细胞进行电穿孔。此类电参数包含电势(电压)、电流类型(交流(ac)或直流(dc))、电流量值(安培数)、脉冲持续时间、脉冲量(即,递送的脉冲数量)和脉冲之间的时间间隔或“延迟”(在多脉冲递送中)。信号发生器112可以包含用于记录所递送的脉冲的电参数的波形记录器。信号发生器112可以与控制单元114(在本文中也称为“控制器”)电通信,所述控制单元
可以包含被配置成控制电穿孔系统100的操作的处理器116,包含信号发生器112的操作。处理器116可以与计算机存储器118进行电子通信,并且可以被配置成执行软件和/或固件,包含用于控制系统100的操作的一种或多种算法。处理器116可以与用户界面120电通信,所述用户界面可以包含用于呈现与系统100的操作相关的信息的显示器122和允许如医师等操作者输入如命令等与系统100的操作相关的信息的小键盘124。应当理解,显示器122可以是允许操作者直接在显示器122处输入信息的触摸屏显示器。还应当理解,界面120可以是计算机界面,如台式计算机或膝上型计算机,或手持电子装置,如智能手机等。
117.现在参考图2a-2b,真空杯2的远侧端10限定通向真空室6的至少一个开口20。如图所示,开口20可以是圆形的,但是其它开口形状也在本公开的范围内,如下文更详细描述的。真空杯2的远侧端10(以及因此开口20)可以由壳体4限定,所述壳体可以限定从壳体的远侧端10延伸到室6的近侧端24的内表面22。因此,室6也从远侧端10延伸到近侧端24。内表面22至少部分地限定了真空室6的边界。内表面22优选地具有钟形或“钟形曲线”几何形状。从远侧端10通向室6的内表面22的远侧部分22a可以具有锥形、辐射式轮廓,用于在使用真空杯2期间减少或减轻对远侧端10周围的组织的损伤,如擦伤。远侧部分22a可以被称为内表面22的“导入”部分22a。内表面22的近侧部分,如在真空室6的近侧端24处,可以被称为真空室6的“近侧端表面”或简称为“端表面”。
118.至少一个和至多所有电极8沿内表面22延伸。如所示的,电极8可以相对于沿壳体4的中心轴线x定向的纵向方向l在远侧端10与近侧端24之间沿内表面22延伸。本实施例的电极8优选地基本上是刚性的,但是在其它实施例中电极8可以具有一定程度的柔性。电极8可以包括导电材料薄层,所述导电材料薄层耦接到(例如,通过涂层、沉积、键合和/或粘附)相关联的基本上刚性的非导电支撑体,所述支撑体可以由塑料或其它合适的非导电材料构成。电极8可以具有与内表面22基本上共形的表面几何形状。电极8可以沿具有沿纵向方向l的方向分量的方向伸长。电极8还可以沿围绕中心轴线x的圆周方向c沿内表面22延伸。如图2b-2c所示,电极8可以各自限定沿圆周方向c测量的圆周尺寸c1(或“宽度”c1)。电极8可以围绕中心轴线x以规则的角间隔a1定位。角间隔a1可以从电极8的相应的中心轴线8x测量。如图2b所示,电极8可以例如围绕中心轴线x以九十度角间隔a1定位。因此,可以说电极8围绕中心轴线x对称地间隔开。应当理解,电极8之间的其它角间隔a1也在本公开的范围内,如下文更详细描述的。此外,在一些实施例中,电极8之间的角间隔a1可以沿内表面22变化。也就是说,电极8可以围绕中心轴线x以不规则的间隔间隔开。此外,电极8不需要围绕中心轴线x对称地间隔开。
119.如图2c所示,每个电极8可以限定从电极8的第一端8a到第二端8b沿中心电极轴8x彼此间隔测量的电极长度l1。电极8还可以具有彼此间隔开的第一侧和第二侧8c、d以限定沿圆周方向c的电极宽度c1。每个电极8可以具有内部电极表面8z,所述内部电极表面被配置成与组织表面101接触以递送一个或多个电穿孔脉冲。内部电极表面8z可以从电极8的第一端8a延伸到第二端8b并且从第一侧8c延伸到第二侧8d。每个电极8可以限定主要或“接触”部分8e,所述主要或“接触”部分从电极8的第二电极端8b向第一电极端8a延伸,并且还从第一侧向第二侧8a、b延伸。如所示的,电极宽度c1可以在第一电极侧与第二电极侧8a、b之间测量,并且不需要沿接触部分8e是均匀的。电极长度l1和宽度c1可以各自在约1.0mm至约30mm的范围内,更具体地在约2mm至约25mm的范围内,并且更具体地在约4mm至约20mm的
范围内。电极8可以限定在约0.0005mm至约2.000mm的范围内的厚度t1(参见图2f)。应当理解,电极长度l1可以大于、小于或等于电极宽度c1。
120.接触部分8e内的内部电极表面8z部分可以被称为电极的“接触表面”8z。接触表面8z可以在与中心轴线x正交的参考平面中与壳体4的内表面22弧形地和同心地(即,可以共享相同的中心点)延伸。接触表面8z也可以具有曲线轮廓,所述曲线轮廓在沿中心电极轴8x的方向上基本上与内表面22共形。接触表面8z可以是光滑的,如所示的,但是在其它实施例中,接触表面8z可以具有纹理以增强对组织102的夹持,如具有突起、凹坑、滚花、微针和/或粗糙表面,作为非限制性实例。在另外的实施例中,可以将涂层或粘合剂施加到接触表面8z以改善电极8与组织102之间的夹持和/或导电性。电极8还可以限定从接触部分8e延伸到第一端8a的次要部分8f,并且可以配置成与电路系统108的相应的引线连接以将电穿孔脉冲传输到电极8。
121.现在参考图2d,壳体4可以包含壳体主体26,所述壳体主体可以由优选具有一定柔性的材料形成,如聚合材料,包含聚醚醚酮(peek)、聚邻苯二甲酰胺(ppa)、聚乙烯、聚碳酸酯、聚醚酰亚胺(pei)、聚氯乙烯(pvc)、聚四氟乙烯(ptfe)、聚酰胺、聚酰亚胺、聚硅氧烷(硅酮)、聚对苯二甲酸乙二醇酯、聚氨酯、交联橡胶或非交联橡胶(弹性体)、聚酯,作为非限制性实例。应当理解,其它生物相容性和/或医用级材料可以用于壳体主体26。壳体主体26可以任选地是限定壳体4的整体结构,但是壳体主体26不需要是整体结构并且可以替代地包含耦接在一起以限定壳体4的两个或更多个主体组件。壳体主体26沿纵向方向l从近侧端28延伸到远侧端10。壳体主体26还限定了从壳体4的内表面22延伸到外表面32的壁30。壁30围绕真空室6的整个周边周向延伸。
122.壳体主体26限定端口12、14、16。如所示的,第一、第二和第三端口12、14、16中的每一个可以邻近壳体主体26的近侧端28并且远离远侧端10。换言之,端口12、14、16可以位于更靠近壳体4的近侧端28的位置,而不是更靠近远侧端10的位置。第一端口12,也可称为“真空端口”,从真空室6延伸,穿过壳体主体26,并且到达用于与配合构件36连接的端口耦接器34,所述配合构件将真空端口12与真空源106互连。端口耦接器34可包含座部38和管状延伸部40,所述管状延伸部从座部38向外延伸并限定收纳器,使得座部38限定收纳器的内端。配合构件36可以包含配合构件耦接器42和从其延伸的空心杆44。配合构件耦接器42可以是与端口耦接器34的管状延伸部40互连的管状延伸部,如通过在由管状延伸部40以配合方式限定的收纳器内延伸。单向阀构件46可以定位在座部38(所述座部可称为“阀座部”)上。阀构件46可以从阀座部38延伸并且在配合构件耦接器42的内部空间内,从而插入在真空端口12与配合构件36的空心杆44之间的流体通路中。如所示的,阀构件46可以是鸭嘴阀,但是在其它实施例中,阀46可以是球阀或伞形阀,作为非限制性实例。
123.第二端口14可与第一端口12相对地延伸并且可被配置成允许如电线等电路系统108穿过壳体4并与真空室6中的电极8接触。第二端口14还可以被配置成允许一个或多个另外的组件,如一个或多个工具和/或一个或多个传感器穿过壳体4并进入真空室6。当定位在真空室6内时,此类工具和/或传感器可以通过提供给室6的真空压力相对于组织定位地固定。第三端口16可以从室6的近侧端24沿中心轴线x延伸。壳体4可以在第三端口16的外端限定安装构造48。安装构造48可以被配置成将如穿刺塞等盖50安装在第三端口16上。安装构造48和穿刺塞50可以具有互补的配合几何形状,所述几何形状在穿刺塞50与第三端口16之
间提供气密密封。穿刺塞50可以由可以被皮下注射针18刺穿的材料形成,从而允许针18将药剂注射到被抽吸到真空室6中的组织102中。
124.继续参考图2d,电极阵列9可以安置在如套筒等插入物52上,所述插入物位于室6中并且沿壳体4的内表面22延伸。套筒52或至少其外表面53可以具有与壳体4的内表面22基本相同的轮廓几何形状。作为非限制性实例,套筒52可以由如橡胶、硅酮和热塑性弹性体等柔性材料构成。如图2e所示,套筒52的外表面53可以通过摩擦配合直接粘附到壳体4的内表面22,但是可以任选地使用一种或多种粘合剂将套筒52与内表面22连接。套筒52可以从与真空室6的近侧端24相邻的第一端或近侧端54延伸到与壳体4的远侧端10相邻的第二端或远侧端56。套筒52的远侧端56可以在壳体4的内表面22的导入部分22a内延伸。第一端54可以限定套筒52的近侧开口52a,所述近侧开口可以与中心轴线x同心,并且可以限定套筒52的远侧开口52b。如图2f中更清楚地示出的,套筒52的第一端54可以部分地堵塞第一端口12,并且还可以部分地堵塞第三端口16,同时允许电路系统206进入真空室6。因此,套筒52可以用作控制或至少影响室6内的真空压力的机构。
125.真空室6限定室体积v,所述室体积沿纵向方向l限定在室6的近侧端24与开口10之间,并且也可以至少部分地由壳体主体26的内表面22限定,如沿基本上垂直于纵向方向l的方向。在所展示的实例中,垂直于纵向方向l的方向是与中心轴线x相交的径向方向r。室体积v也可以至少部分地由套筒52限定,如沿径向方向r。室6可以具有从室6的近侧端24到环绕壳体4的远侧端10的参考平面测量的深度l2。室深度l2可以在约1.0mm至约50.0mm的范围内,更具体地在约3mm至约20mm的范围内,并且更具体地在约5mm至约17mm的范围内。室6还具有基座宽度,如基座直径d1,所述基座直径可以在套筒52的远侧端56处沿径向方向r测量。室直径d1可以在约1.0mm至约50.0mm的范围内,具体地在约3.0mm至约20.0mm的范围内,并且更具体地在约6.0mm至约17.0mm的范围内。在本实施例中,室直径d1可以在套筒52的内表面55在其远侧端56处的相对部分之间测量。在其它实施例中,可以省略套筒52并且电极8可以直接与壳体4的内表面22连接,例如通过嵌入或至少部分嵌入壳体壁30内。在此类实施例中,真空室6以及因此的室体积v可以至少部分地由壳体4的内表面22和电极8的内表面8z限定。因此,在此类实施例中,可以在电极8的远侧端8b处的壳体4的内表面22的相对部分之间测量室直径d1。
126.现在参考图3a-3b,套筒52可以承载电极8中的每个电极,并且因此承载电极阵列9。因此,套筒52也可以称为电极阵列基座、支撑件或基板。在所展示的实施例中,电极阵列9限定了包含第一电极8-1、第二电极8-2、第三电极8-3和第四电极8-4的电极图案,使得第一电极至第四电极8-1、8-2、8-3、8-4围绕套筒52的中心轴线x2以九十度间隔a1定位(当套筒52插入杯壳体4中时,所述中心轴线基本上与所述杯壳体的中心轴线x共同延伸)。本发明的实施例的电极阵列9可以被表征为具有电极8n的总数,即四(4)个电极8。电极8n的总数在本文中也可以称为“总数”8n或简称为“总”8n。套筒52还可以与具有不同电极阵列9图案和配置的其它套筒52互换,如用于在抽吸到真空室6中的组织102内产生具有不同特性的电场。例如,如图3c-3d所示,套筒52可以具有电极阵列9,所述电极阵列包含四个电极8,如上所述,所述电极围绕套筒52的中心轴线x2以九十度间隔间隔开;然而,与上述实施例中的电极8相比,电极8可以各自具有更窄的圆周尺寸c1,并且因此也可以具有更小的累积表面积。如图3e-3f所示,套筒52可以具有电极阵列9,所述电极阵列包含围绕中心轴线x2以六十度间
隔间隔开的六(6)个电极8。如图3g-3h所示,电极阵列9可以包含围绕中心轴线x2以三十六度间隔间隔开的十(10)个电极8。
127.如图3i-3j所示,电极阵列9可以包含七(7)个电极8,所述电极沿纵向方向l彼此间隔开,并且每个电极都围绕套筒52的整个圆周延伸。此类阵列9设计可以允许电极8按顺序被施加脉冲或“发射”,从而驱动所产生的电穿孔场“向上”和/或“向下”穿过由真空杯2夹持的组织体积。
128.如图3k-3l所示,电极阵列9可以包含多个周向细长电极8,包含四(4)个周向细长电极8的子集9a-d。每个子集9a-d内的电极8可以彼此基本上纵向对齐,并且每个子集9a-d可以与电极8的每个相邻子集9a-d周向间隔开。在本实例中,电极8的每个子集9a-d可以包含五(5)个纵向间隔开的电极8。因此,套筒52可包含总共二十(20)个周向细长电极8。在本实施例中,每个子集9a-d内的电极8可以具有围绕中心轴线x2在约1度到约90度范围内的角跨度a2,相邻子集8a-d之间的电极间跨度a3在约1度至约90度的范围内。使子集9a-d彼此沿周向隔开允许子集9a-d彼此独立地被发射(或以其它方式由电流源或电压源驱动)。这可以帮助确保组织体积内与子集9a-d相邻和相关联的每个区域(在此实施例中,此类组织区域可以被表征为组织体积的“象限”)接收电穿孔场覆盖,这导致处于更对称的电穿孔场中,并且可以避免组织体积中组织电导率的局部差异使电穿孔场偏离组织体积内的一个或多个区域的情况。
129.此外,图3k-3l中所示的周向间隔的子集9a-d还可以允许在组织体积内产生独特的定向电穿孔场,如用于在随后的脉冲中从多个角度对细胞进行电脉冲(即,将细胞暴露于沿不同方向的电穿孔场梯度),这可以比从单个方向对细胞进行电脉冲更有效地使细胞电透化。应当理解,此类多向电穿孔场也可以由图3a-3h的各种阵列设计产生。然而,图3k-3l的周向间隔的子集9a-d还允许电极8不仅横向和/或周向地发射穿过组织体积,还允许“向上”和/或“向下”穿过组织体积。通过增加阵列9中电极8的数量,可能的独特脉冲图案的数量也可以增加,考虑到电穿孔场集中在电极8的接触表面8z处,还允许更均匀的电穿孔场覆盖。
130.应当理解,上述各种电极阵列9图案是作为非限制性实例提供的,并且其它电极阵列9配置也在本公开的范围内。例如,上述电极阵列9的一个或多个参数可以根据需要进行定制,包含但不限于:每个阵列9中电极8的数量;电极长度l1和宽度c1;以及电极间距。这些参数可以影响电场的三维(3d)形状(并且因此也影响电穿孔场的3d形状)。换言之,电极8的尺寸、形状和布置可以根据需要进行定制,以便以提供增强的电穿孔处理的方式聚焦组织102内的电场分布。
131.参考图4a-4f,现在将描述使用真空杯2向脂肪组织103提供电穿孔处理的示例方法。
132.如图4a所示,医师可以在覆盖脂肪组织103的靶标区域105的位置处将真空杯2的远侧端10放置在患者皮肤104的外表面101上。靶标区域105可以是预先选择的或者可以是真空杯2放置的结果。优选地,医师将远侧端10的整个圆周与皮肤104接触。
133.如图4b所示,医师可以向真空室6施加真空压力脉冲(本文也称为“真空脉冲”),特别是通过激活真空源以产生范围为约-0.1psi至约-14.7psi,更优选地范围为约-3psi至约-14.7psi的真空压力,在真空室6内足以将组织102的体积或“堆”140抽吸到室6中并与电
极8的接触表面8z接触。应当理解,贯穿本公开的真空压力量值是指相对于在海平面处测量的大气压力的此类压力。组织堆140(特别是其皮肤层104)和杯2的内表面22之间的接触压力可以在约0.1psi至约200psi的范围内。以此方式,真空杯2将靶标区域105的至少一部分抽吸到由真空杯2限定的处理区域107中。在本实例中,组织堆140包含皮肤104和脂肪组织103。出于本公开的目的,处理区域107被定义为在电极8之间延伸的组织体积(如组织堆140)的一部分。如所示的,处理区域107的底部边界107a可以由沿电极8的第二端8b和在所述电极的第二端之间延伸的假想路径限定。因此,在组织堆140被抽吸到真空室6中之后,本实施例的处理区域107将含有组织堆140的至少一部分和其中的注射部位109的至少一部分(参见图4c)。在所展示的实施例中,在处理期间定位在处理区域107内的组织限于皮肤层104和脂肪层103。在其它实施例中,处理区域107可以包含平滑肌层111。优选地,处理区域107不包含其中的任何骨骼肌。如上文所描述的,真空压力优选地足以为真空杯2提供对组织堆140的牢固夹持,从而保持真空杯2与组织堆140之间的相对位置。尽管所展示的实施例展示了组织堆140的皮肤104被放置成与电极8的接触表面8z直接接触,应当理解,可以使用如导电凝胶等另外的物质来改善电极8与皮肤104之间的电通信。
134.如图4c所示,医师可以将药剂注射到堆140的脂肪组织103中。为了进行注射,医师可以将皮下注射针18穿过穿刺塞50,沿第三端口16,穿过皮肤104,并且进入室体积v内的脂肪组织103。然后医师可以将药剂注射到脂肪组织103内的注射部位,随后将皮下注射针18从真空杯2中取出。本发明人惊讶地和出乎意料地观察到,响应于真空压力,从皮下注射针18排出到脂肪组织103中的注射剂142向皮肤104分散,而不是保留在脂肪组织103中的汇集的团注142a中。因此,医师可以在处理区域107的附近或底部,或甚至在处理区域107稍下方注射注射剂142,并允许真空压力有效地将注射剂142向上拉入处理区域107中,甚至允许注射剂142在处理区域107中集中。发明人还认为,基于测试期间的观察,可以操纵真空压力以帮助将注射剂142与体内流体、细胞外组分和细胞混合,并且以增强其中注射剂142潜伏期的方式将注射剂142保留在处理区域107中,从而增加转染。
135.应当理解,在一些实施例中,针18可以在注射后保持插入组织102中,并且针18的至少一部分可以包括用于在电穿孔期间或之后检测组织102的参数(如电参数)的传感器152,如下文更详细描述的。
136.如图4d所示,医师可以将一个或多个电穿孔脉冲递送到组织堆140。具体地,医师可以使信号发生器112以一个或多个电穿孔脉冲的形式将电穿孔信号递送到电极8,这又将一个或多个电穿孔脉冲递送到与电极8接触的组织102,从而在所展示的实施例中在处理区域107中的脂肪组织103内产生电穿孔场144。电穿孔场144在处理区域107中的细胞(例如,脂肪细胞)的细胞膜中基本上引起可逆部分,从而引起注射剂转染到暂时穿孔的细胞中。以此方式,电穿孔场144在处理区域107内产生转染区域。由本实施例的电极8产生的电穿孔场144具有基本上球形的形状。应当理解,电穿孔场144是由电极8在脉冲递送期间产生的电场145的子区域。
137.由电极8递送的一个或多个电穿孔脉冲可具有约5v至约1000v(1kv)范围内的电势(电压)。
138.一个或多个电穿孔脉冲可以具有约0.01安培至约2.0安培范围内的电流(安培数)。
139.一个或多个电穿孔脉冲可以各自具有约100微秒至约500毫秒范围内的持续时间。
140.电穿孔脉冲的量可以在1个脉冲至约10个脉冲的范围内。
141.对于多脉冲递送,每个电穿孔脉冲可以通过约1毫秒至约1秒范围内的脉冲延迟在时间上与相邻脉冲间隔开。
142.在一些实施例中,电穿孔信号可以包含持续时间约100毫秒的约200v的3个脉冲,脉冲之间有200毫秒的延迟。在其它实施例中,电穿孔信号可以包含持续时间约100毫秒的约50v的3个脉冲,脉冲之间有200毫秒的延迟。在仍其它实施例中,电穿孔信号可以包含持续时间100毫秒的约50v的10个脉冲,脉冲之间有1秒的延迟。在仍其它实施例中,电穿孔信号可以包含持续时间约100毫秒的75v的8个脉冲,脉冲之间有约100毫秒的延迟。在仍其它实施例中,电穿孔信号可以包含约10微秒和约100微秒持续时间的约500v与约1000v之间的3个脉冲,脉冲之间有约100毫秒至约1秒的延迟。应当理解,提供前述电穿孔信号作为非限制性实例,特别是用于将dna递送到细胞中的可逆孔形成。还应当理解,本文公开的实施例可以适用于提供其它类型的处理,包含将其它类型的药剂递送到细胞中,如用于将小分子递送到细胞中、电化学疗法和不可逆电穿孔,作为非限制性实例。
143.在涉及多个电穿孔脉冲的处理中,脉冲可以通过电极8以脉冲序列或图案递送,其中:第一电穿孔脉冲由电极8的第一正子集通过组织102递送到电极8的第一负子集;第二电穿孔脉冲由电极8的第二正子集通过组织102递送到电极8的第二负子集;直到并包含处理的最终电穿孔脉冲。在每个电穿孔脉冲期间,电极8的每个正子集和负子集的范围可以从单个电极8到电极8的任何组合,所述组合比阵列9的电极8n的总数少至少一个(即8n-1
)。电穿孔脉冲图案可以根据编程的序列来递送,所述编程的序列可以由用户输入到控制器114(如通过用户界面120)。此外,电穿孔脉冲的序列可以任选地以分散的图案递送。在此类分散的图案序列中,多个电穿孔脉冲中的每个脉冲可以在一组至少两个电极8之间递送,并且多个电穿孔脉冲中的每个后续脉冲由不同组的至少两个电极8递送。分散的电穿孔脉冲图案可以最小化或优选地消除在被电穿孔的组织102上出现的与电穿孔相关的热应力,并且可以增强在组织102内产生的电场的均匀性。
144.真空杯2可以被配置成在电穿孔脉冲递送期间感测、测量或以其它方式检测组织102的一个或多个电参数,并且将检测到的信息中继回控制器114用于诊断和反馈。作为非限制性实例,在组织102中检测到的电参数可以包含电压、电流、阻抗和/或电阻。用于在电穿孔脉冲递送期间检测此类参数的一种技术是使电极8中的至少一个在脉冲期间测量期望的电参数。此类电极8可以表征为感测电极8或简称为“传感器”。感测电极8在脉冲期间可以是中性的。作为分散的电穿孔脉冲图案序列的非限制性实例,多个电穿孔脉冲中的每个脉冲可以在一组至少两个电极8之间传递,而至少一个其它电极8是感测电极8,所述感测电极是中性的并且测量组织102的电参数(如阻抗),并且其中多个电穿孔脉冲中的每个后续脉冲由不同组的至少两个电极8递送,而至少一个电极8是感测电极8,所述感测电极是中性的并且测量电参数。至少一个中性电极8可以在脉冲与脉冲之间交替,但是同一电极8(或电极8的组)可以在连续脉冲中保持中性。可替代地,在电穿孔脉冲期间,阵列9的至少一个电极8可以主动递送脉冲,同时还测量组织102的电参数。
145.用于在电穿孔脉冲递送期间检测电参数的另一种任选的技术是使用至少一个单独的传感器来检测参数。单独的传感器可以是非侵入性传感器150,如接触式传感器150,例
如,如图4d所示。接触式传感器150被配置成测量参数并将关于所测得的参数的信息传送到控制器114。接触式传感器150可以通过如第二端口14等端口插入到真空室6中。医师可以将接触式传感器150放置成与组织102接触,如在皮肤104处,其中接触式传感器150可以测量参数。在其它实施例中,单独的传感器可以是侵入性传感器152,如探针型传感器152。在探针型传感器152的一个此类实例中,传感器152可以是注射针18的一部分,如其远侧尖端区域(参见图4c),所述注射针可以与控制器114电通信以使关于所测得的参数的信息与控制器114相关。应当理解,在处理期间,可以使用多个传感器,包含一个或多个非侵入性传感器150和一个或多个探针型传感器152,以将关于组织102的单个电参数或多个电参数的信息中继到控制器114。
146.由控制器114接收到的电参数信息可以用于性能诊断目的和/或用于对电穿孔信号进行主动反馈控制,所述电穿孔信号递送到电极8并且因此递送到组织102。例如,为了提供主动反馈控制,所述一个或多个传感器8、150、152可以测量组织102中的一个或多个相应的电参数并将关于参数的信息传送到控制器114。处理器116可以运行结合参数信息的软件,如通过执行结合参数信息的一种或多种算法以处理或以其它方式获得输出,如用于控制电穿孔脉冲的控制命令。算法还可以使用从计算机存储器118检索到的参数数据。应当理解,基于来自传感器8、150、152的参数信息,从算法得出的控制命令可以实时调节电穿孔脉冲,如出于电穿孔目的基本上瞬时地调节电穿孔脉冲。以此方式,电穿孔系统100可以在主动反馈环路中使用传感器8、150、152以根据需要对电穿孔脉冲进行持续控制和调节,以便在所靶向的组织102中实现期望的电穿孔治疗结果。可以使用用于执行此类反馈控制的技术和/或电子组件,如在于2016年9月27日发布的题为“电穿孔装置以及其用于哺乳动物细胞的电穿孔的方法(electroporation devices and methods of using same for electroporation of cells in mammals)”的美国专利9,452,285('285参考文献)和于2011年1月13日公开的题为“可变电流密度单针电穿孔系统和方法(variable current density single needle electroporation system and method)”的美国专利公开第2011/0009807 a1号('807参考文献)中更完整地公开的,所述美国专利中的每个美国专利的全部公开内容特此通过引用并入本文。
147.如图4e所示,在所述一个或多个电穿孔脉冲之后,医师可以将真空室6内的压力恢复到大气压,从而允许真空杯2释放组织102,所述组织可以恢复到其解剖形状。经转染的脂肪细胞可以在脂肪层103中限定转染区域105z。
148.现在参考图4f,本文公开的真空杯2的显著优点之一是所述真空杯与真空源106相结合,允许医师控制组织102被抽吸到处理区域107中以进行电穿孔处理的体积(即,堆140的大小)。因此,如果靶标区域105仅位于皮肤层104中,则医师可以向真空室6施加真空压力,以将皮肤层104抽吸到室体积v中并与电极8接触,如在其远侧端8b处。如果靶标区域105位于脂肪层103中,则医师可以施加增加的真空压力以将脂肪层103抽吸到处理区域107中。如果靶标区域105位于如平滑肌层等肌肉层中,则医师可以施加进一步增加的真空压力,并且如果靶标区域105位于骨骼肌层中,则可以施加甚至进一步增加的真空压力。应当理解,靶标区域105可以存在于单层组织(例如,皮肤层104或脂肪层103)中,或者可以存在于多个组织层中,包含皮肤层104、脂肪层103和任选地平滑肌层。可以根据靶标区域105的深度,按照需要控制真空压力。
149.本公开的真空杯2的另一个显著益处是真空杯2与真空源106相结合,允许医师向组织102施加多个真空脉冲以增强组织与注射剂之间的相互作用,包含上述有利的体内流体分散机制。真空脉冲可以在注射之前、期间和/或之后施加,也可以在电穿孔之前、期间和/或之后施加。可以给予1个脉冲至20个脉冲范围内的量的真空脉冲,并且每个脉冲可以具有约0.1秒至约30秒范围内的持续时间。真空脉冲也可以以不同的真空压力和/或持续时间(和/或脉冲之间的不同时间)施加以实现期望的结果。
150.本发明人已经对本公开的真空杯2做出了许多令人惊讶和出乎意料的观察。例如,本发明人观察到使用真空杯2进行真空辅助电穿孔处理的测试受试者的免疫应答出乎意料且令人惊讶的增加。此结果令人惊讶且出乎意料,因为本发明人的初始目标是将真空杯2用于主要目的,所述主要目的是相对于现有技术的卡尺型电穿孔装置提供的夹持,实现对受试者组织的更牢固的夹持。本发明人无法将其在用真空杯2处理的测试受试者中测量到的增加的免疫应答解释为仅仅是真空杯电极8与组织之间的位置稳定性增强的结果。值得注意的是,本发明人还在用真空杯2处理的处理部位观察到出乎意料且令人惊讶的细胞浸润量。在使用真空杯2进行一些处理后,发明人观察到皮肤上的瘀伤和变色,具有红斑和/或血肿的特征,后者涉及通过破裂毛细血管的血液分散。
151.尽管不想受任何特定理论的束缚,但本发明人认为免疫应答和细胞浸润的令人惊讶的增加可能是相关的。此外,本发明人认为,增加的细胞浸润至少部分是由来自处理区域中破裂的毛细血管和附近白细胞的化学信号的自然分泌驱动的,所述化学信号吸引另外的细胞,如另外的白细胞,以应答性地迁移到处理区域。本发明人还认为,观察到的细胞浸润可能至少部分是由炎性应答驱动的。发明人进一步认为,基于观察到的通过响应于真空压力的组织的注射剂的分散,处理区域107外部的体内流体被机械地拉入响应于真空压力的处理区域107中。
152.现在参考图5a-5d,现在将描述使用柔性电极508的真空杯502的实施例。本实施例的真空杯502与上述真空杯2类似。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本实施例的真空杯502与上述真空杯2之间的差异。
153.如图5a-5b所示,真空杯502具有壳体主体526,所述壳体主体限定内表面522,所述内表面部分限定真空室506。壳体主体526还限定多个泄压端口560,所述泄压端口从壳体主体526的外表面532延伸到限定在壳体主体526的内表面522中的多个通道562。通道562可以包含沿纵向方向l彼此间隔开的近侧通道562和远侧通道562。通道562可以各自沿围绕中心轴线x的整圈环状地延伸,但是在其它实施例中,一个或多个通道562可以围绕中心轴线x环状地延伸小于整圈。
154.真空杯502包含柔性套筒552,所述柔性套筒位于真空室506内并承载布置在电极阵列509中的多个电极508。柔性套筒552具有与壳体主体526的内表面522连接的外表面553。柔性套筒552以在通道562与真空室6之间提供柔性屏障或膜的方式覆盖在通道562上。电极508安置在套筒552的内表面555上。套筒552还可以承载电路系统,如有线电路系统或印刷电路系统,例如用于在电极508与控制器114之间提供电通信。本实施例的电极508可以是周向细长的,类似于上文参考图3k-3l描述的电极8。一个或多个以及至多每个电极508覆盖至少一个通道562并且由柔性材料构成。作为非限制性实例,电极材料可以是金属,如铜、
不锈钢和金。可替代地或另外,作为非限制性实例,电极材料可以包含导电聚合物或如石墨烯等碳同素异形体,所述碳同素异形体可以包含碳纳米管。在其它实施例中,电极508可以具有涂有导电材料的非导电芯,如上文描述的那些。
155.电极阵列509可以包含电极508的四(4)个子集509a-d。每个子集509a-d内的电极508可以基本上沿纵向方向l对齐,并且每个子集509a-d可以沿着圆周方向c与每个相邻子集509a-d间隔开。子集509a-d可以彼此规则地间隔开,如围绕中心轴线x以九十度间隔。在所展示的实例中,每个子集9a-d包含彼此纵向间隔开的近侧电极508和远侧电极508,从而为阵列509提供总共八(8)个电极508。阵列509的电极508还可以表征为布置在覆盖近侧通道562的电极508的近侧环形行和覆盖远侧通道562的电极508的远侧环形行中。如上文所描述的,电极508与在电极508与控制器114之间提供电通信的电路系统连接。应当理解,电极阵列509的电路系统可以被配置成使得控制器114可以单独控制电极508的每个子集509a-d的电穿孔脉冲的参数,并且可以进一步单独控制每个子集509a-d内的每个电极508的电穿孔脉冲的参数。
156.现在参考图5c-5d,柔性套筒552和电极508被配置成在室6内施加真空压力时向内弯曲进入真空室6(朝向中心轴线x)中,增加电极508的接触表面508z与被抽吸到室6中的组织间的接触。泄压端口560提供通道562与真空杯502的外部之间的流体连通,从而允许通道562内的压力基本保持在大气压。以此方式,室内的真空压力在室6与通道562之间的套筒552壁中提供压力梯度,允许套筒552和其上的电极508向内弯曲进入室6。
157.现在参考图6a-6d,用于定位在真空杯2、502的真空室6内的电极608可以包含多个突起664,所述突起可以由电极608的接触表面608z限定。与上述方式类似,电极608沿电极608的中心轴线608x从第一端608a延伸到第二端608。电极608可以沿着沿中心轴线608x定向的方向伸长。电极608还可以沿电极608的横轴608y从第一侧608c延伸到第二侧608d。接触表面608z可以包含基本上光滑的基座部分665,并且突起664可以从基座部分665向外延伸(即,向内进入室6)。如所示的,基座部分665可以基本上是平面的,但是在其它实施例中,基座部分665可以具有与杯壳体4的内表面22基本上共形的曲线轮廓。通过从基座部分665向外延伸,突起664可以增加电极608的接触表面608z与被抽吸到室6中的组织间的接触面积。在使用期间,突起664可以以破坏和改变皮肤104的顶层的方式压入组织102中,从而改善靶标组织内的电场分布。更具体地,突起664对于给定的输入电压增加在组织102内形成的电场的量值,如在2018年3月29日公开的题为“使用电穿孔对脂肪组织进行微创体内转染的方法和装置(method and device for minimally invasive in vivo transfection of adipose tissue using electroporation)”的国际(pct)专利公开第wo 2018/057900 a1号('900参考文献)中更完整地公开的,所述专利公开的全部公开内容特此通过引用并入本文。
158.如图6a-6b所示,突起664可以具有凸形、弧形、圆顶状几何形状。突起664可以排列成列和行的突起664。如图6c所示,突起可以沿着沿横轴608y定向的方向伸长。如图6b和6d所示,图6a和6c中的突起608可以具有相似的侧面轮廓。应当理解,其它突出几何形状,包含尖的、圆锥形的、截头圆锥形的、金字塔形的等都在本公开的范围内。还应理解,电极608可以被配置成与室6一起定位,从而沿真空杯2的纵向方向l伸长,沿真空杯2的圆周方向c伸长,或沿与纵向方向和圆周方向l、c倾斜的方向伸长。
159.本文所描述的真空杯2、502的各种参数,如室深度l2、室直径d1和杯几何形状,如与中心轴线x正交的参考平面中的横截面形状,和/或开口20的形状可以根据需要进行定制,以实现期望的电穿孔处理,如在广泛的哺乳动物和皮肤解剖学上。例如,作为非限制性实例,本公开的真空杯可以具有非圆形开口和/或室几何形状,如多边形开口和/或室几何形状。参考图7a-7e,将描述具有三角形开口和室几何形状的真空杯702。参考图8a-8c,将描述具有矩形开口和室几何形状的真空杯802。在此类实施例中,室尺寸d1可以被称为“室宽度”d1。
160.现在参考图7a-7c,示出了具有远侧端710的真空杯702,所述远侧端限定三角形开口720。本实施例的真空杯702与上述真空杯2、502类似。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本实施例的真空杯702与上述真空杯2、502之间的差异。
161.真空杯702包含壳体主体726,所述壳体主体限定布置成三角形图案的三(3)个侧壁730,如在与真空杯702的中心轴线x正交的参考平面中所见的。因此,壳体主体726限定真空室706,所述真空室在正交参考平面中也具有三角形形状。侧壁730在壳体主体726的三(3)个角735处彼此相交,所述角735优选地是辐射式的。如所示的,三角形图案可以是等边的,但是其它三角形图案也在本实施例的范围内,包含直角、等腰和不等边。
162.侧壁730的内表面722可以限定主要部分722b,所述主要部分从远侧导入部分722a朝向室706的近侧端724延伸。主要部分722b可以是平面的,从而限定线性表面轮廓,并且可以限定在约1mm至约20mm范围内的长度l4,如沿线性表面轮廓测量的。应当理解,主要部分722b可以可替代地是非平面的并且可以具有非线性轮廓。主要部分722b优选地朝向中心轴线x朝向室706的近侧端724向内逐渐变细。主要部分722b可以限定锥角a4,所述锥角相对于平行于中心轴线x的轴测量,在约0度至约80度的范围内,更具体地在约0.25度至约10度的范围内,并且更具体地在约0.5度至约5度的范围内。
163.真空杯702包含布置在电极阵列709中的多个电极708,所述电极阵列可以包含电极708的三(3)个子集709a-c。电极708的第一子集709a可以安置在第一侧壁730的内表面722上,电极708的第二子集709b可以安置在第二侧壁730的内表面722上,并且电极708的第三子集709c可以安置在第三侧壁730的内表面722上。电极708的子集709a-c可以由相应的基底或“焊盘”752承载,所述焊盘可以由电绝缘材料构成,如硅、聚醚醚酮(peek)、聚邻苯二甲酰胺(ppa)、聚乙烯;聚碳酸酯;以及聚醚酰亚胺(pei),作为非限制性实例。基底752可以是柔性的或刚性的。基底752还可以承载电路系统,如有线电路系统或印刷电路系统,例如用于在电极708与控制器114之间提供电通信。因此,基底752可以是电路板,如印刷电路板(pcb)。如上所述,电路系统可以被配置成使得控制器114可以单独控制电极708的每个子集709a-d的电穿孔脉冲的参数,并且还单独控制每个子集709a-c中的每个电极708的脉冲参数。基底752的外表面753可以通过粘合剂与相应的侧壁730的内表面722连接,但是其它紧固技术也在本公开的范围内。
164.电极708的每个子集709a-c可以包含单个电极708或优选地多个电极708。在所展示的实施例中,每个子集709a-c具有四(4)个电极708。应当理解,每个子集709a-c可以具有少于或多于四(4)个电极708,如单(1)个电极、两(2)个、三(3)个、五(5)个、六(6)个、七(7)个、八(8)个、九(9)个、十(10)个、十一(11)个、十二(12)个或多于十二个电极708,如一百
(100)个电极708或更多。由于微机电系统(mems)技术和纳米技术的进步,每个分立电极708的大小可以减小到使每个子集709a-c可以实际上具有无限数量的分立电极708的程度。
165.电极708限定接触表面708z,所述接触表面可以是光滑的,如所示的。接触表面708z的主要部分可以是平面的,如覆盖内表面722的主要部分722b的相应的部分。然而应当理解,与上述方式类似,至少一个和至多所有电极708的接触表面708z可以被纹理化和/或限定突起。此外,基底752和电极708可以是柔性的,并且可以覆盖限定在壳体主体726中的通道和泄压端口,以在向室706施加真空压力时允许电极708向内弯曲,类似于上文参考图5a-5d描述的方式。
166.现在参考图7d,每个子集709a-c中的电极708可以彼此平行。电极708可以限定电极长度l1,如沿其中心轴线708x在电极708的第一端708a与第二端708b之间测量的。电极长度l1可以在上述范围内。电极708还可以限定电极宽度w1,如在电极708的第一侧708c与第二侧708d之间测量的。电极宽度w1可以在上述c1的范围内。每个子集709a-c的电极708还可以限定电极间间隙w2,所述电极间间隙可以在约1.0mm至约30mm的范围内。
167.现在参考图7e,电极708可以从基底752向内(进入真空室706)延伸。电极708可以限定从基底752的内表面755到接触表面708z测量的电极厚度t1。电极厚度t1可以在约0.001mm至约2.000mm的范围内。如所示的,电极708的外表面708w可以固定到基底752的内表面755上。在其它实施例中,电极708的外表面708w可以部分地嵌入基底752中。也就是说,电极708的外表面708w可以驻留在基底752的外表面753与内表面755之间的深度处。在另外的实施例中,电极708的外表面708w可以完全嵌入基底752中。也就是说,电极708的外表面708w可以与基底752的外表面753共同延伸。
168.本实施例的电极阵列709a-c被配置成当真空压力将组织102抽吸到真空室中时,组织102被拉入与接触表面708z接触并且还被拉入电极间间隙w2中,从而也接触电极的侧面708c、708d,从而增加组织102与电极708之间的总接触界面面积。
169.本实施例的真空室706的几何形状和电极阵列709a-c的配置允许沿真空杯702的侧壁730的基本上平面的电极708,这在组织102中相对于上述真空杯2、502提供了更柱状的电穿孔场(即,沿中心轴线x更伸长)。与现有技术的电穿孔装置相比,本实施例的三角形形状还可以在由三角形脉冲图案限定的电穿孔场的边界内将组织有利地约束到更大的程度。另外,与包含圆形设计在内的其它阵列设计相比,包含本实施例的三角形阵列在内的多边形阵列几何形状可以由于拐角735相对侧上的相邻电极之间的锐角或“尖锐”角度而产生更不均匀的电穿孔场。例如,可能期望在靶标组织内产生增加的电场幅度(导致电流增加)的区域,并且具有“尖锐”或锐角的相邻电极边缘是在组织中产生此类增加的电场/电流区域的一种方式。
170.现在参考图8a-8c,示出了具有远侧端810的真空杯802,所述远侧端限定了矩形开口820。本实施例的真空杯802与上述真空杯2,502、702类似。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本实施例的真空杯802与上述真空杯2、502、708之间的差异,特别是与上文参考图7a-7e描述的真空杯702的差异。
171.真空杯802包含壳体主体826,所述壳体主体限定四(4)个壁,特别是在一对相对端壁831之间延伸的一对相对侧壁830,布置成矩形图案,从而提供真空室806,所述真空室也
具有正交参考平面中的矩形形状。在所展示的实施例中,侧壁830比端壁831长,但是在其它实施例中侧壁830和端壁831可以具有相同的长度,使得矩形是正方形。还应当理解,壳体主体826的壁可以限定其它四边形几何形状(即,非矩形)。
172.壁830、321的内表面822可以限定主要部分822b,所述主要部分从远侧导入部分822a朝向室806的近侧端824延伸。侧壁830和/或端壁831的主要部分822bs可以以锥角a4向内和向近端逐渐变细,所述锥角可以在上述范围内。真空杯802包含布置在电极阵列809中的多个电极808,所述电极阵列可以包含安置在侧壁830的内表面822上的电极808的两(2)个相对子集809a、809b。如所示的,端壁831可以没有电极808,但是在其它实施例中,端壁831中的一个或两个可以具有电极808的另外的子集。在又其它实施例中,端壁831可以具有电极并且侧壁839可以没有电极。在又另外的实施例中,壁830、831中的一个或多个并且至多每个可以具有单个电极,所述单个电极可以根据各种尺寸和形状进行配置。
173.如上所述,电极808的子集809a、809b可以由与内表面822连接的相应的非导电基底852承载。每个子集809a、809b可以具有四(4)个电极808,但是每个子集809a、809b可以具有多于或少于四(4)个电极808。如上所述,电极阵列809可以包含电路系统,所述电路系统被配置成使得控制器114可以单独控制电极808的每个子集809a、809b的电穿孔脉冲的参数,并且还单独控制每个子集809a、809b内的每个电极808的脉冲参数。
174.如所示的,电极808的接触表面808z可以是光滑的,并且其主要部分可以是平面的。然而,在其它实施例中,接触表面808z可以是纹理化的和/或限定突起,如上所述。壳体主体826、基底852和电极808也可以协作地被配置成允许电极808响应于真空压力向内弯曲,类似于上文参考图5a-5d描述的方式。电极808可以具有与上文参考图7d-7e描述的那些类似的长度l1、宽度w1和厚度t1,并且可以如上所述类似地操作。
175.本实施例的真空室806的矩形几何形状和电极阵列809a、809b的配置提供了球形电穿孔场,所述球形电穿孔场相对于上述真空杯2、502、702沿横向于中心轴线x的方向(特别是沿与端壁831正交的方向)更伸长。此外,本实施例的矩形阵列允许彼此直接相对并且能够发射直接相对的电脉冲的基本上平面的电极。在此方面,本实施例的阵列可以以类似于本领域已知的相对板或卡尺型电穿孔装置的方式使用。例如,本实施例的矩形阵列设计可以允许医师“捏”组织的伸长部分,类似于卡尺型电极配置。主要沿一个轴“抓取”组织并将其捏住以在组织中形成伸长的处理区域可能是有利的。例如,随着纵横比的增加,矩形杯802可以处理更大的整体组织区域而不增加电极之间的间隙。例如,与在相同电压下操作的圆形阵列设计相比,这可以允许使用更低的电压并处理更大的组织区域。
176.另外,与上述类似,多边形阵列几何形状,包含本实施例的阵列,由于在杯802的相对侧壁830上的相邻电极之间(在此实施例中,几乎平行)的锐角,可以产生更不均匀的电穿孔场。此外,如上所述,所述阵列可用于在组织内产生电场幅度增加的区域,如上所述。
177.应当理解,其它实施例的真空杯可以具有其它多边形形状的开口和/或室几何形状,如五边形、六边形、七边形、八边形等直至圆形几何形状。此外,此类多边形形状不需要具有等边配置。在又其它实施例中,作为非限制性实例,真空杯可以具有其它形状的开口和/或室几何形状,如椭圆形、长方形或不规则形状。应当理解,椭圆杯形状可以提供类似于上述矩形杯802的优点,包含主要沿一个轴“抓取”组织并将其捏住以在组织中形成伸长的处理区的能力,从而允许以较低的电压处理更大的组织区域。
178.现在参考图30a-33f,现在将描述脂肪组织103和皮肤104上的各种四电极阵列9的模拟测试结果。在图30a-33f中的每个中,相对电极8彼此间隔15mm的距离(所述距离类似于室直径d1),并且在电极两端施加的电压相同。因此,图30a-33f展示了电极形状、大小和间距对电场产生的影响。
179.图30a-31f示出了圆形阵列9,其中电极的接触表面沿大致圆形的周边延伸。图30a-31f中示出的电极宽度由室直径的分数定义;因此,朝顶部向内逐渐变细的室将在顶部附近具有较薄的电极宽度,而在底部附近具有较厚的电极宽度,同时在沿室的内表面的任何位置处始终占据室圆周的相同百分比。图30b和31b中的电极各自具有15度的角跨度a2;图30c和31c中的电极各自具有30度的角跨度a2;图30d和31d中的电极各自具有45度的角跨度a2;图30e和31e中的电极各自具有60度的角跨度a2;并且图30f和31f中的电极各自具有75度的角跨度a2。
180.图32a-33f示出了矩形(具体地正方形)阵列9,其中电极的接触表面限定了矩形的侧边。图32b和33b中的电极各自具有2.5mm的宽度;图32c和33c中的电极各自具有5.0mm的宽度;图32d和33d中的电极各自具有7.5mm的宽度;图32e和33e中的电极各自具有10.0mm的宽度;图32f和33f中的电极各自具有12.5mm的宽度。图32a-33f中示出的电极的宽度从上到下是恒定的。因此,朝顶部向内逐渐变细的室将使以此方式构造的相邻电极在顶部处比在底部处更靠近彼此。根据杯尺寸和壁的锥角,这可能使相邻电极彼此非常靠近或甚至在室的顶部处相互接触,这不是优选的。
181.从这些图中可以看出,正方形阵列(图32a-33f)在脂肪组织103和皮肤104两者中产生比其圆形阵列对应物(图30a-31f)更不均匀的电场。因此,也可以说圆形阵列在脂肪组织103和皮肤104两者中产生比其矩形阵列对应物更均匀的电场。可以根据期望的处理根据需要有利地使用由圆形和矩形阵列产生的场异质性/均质性的这些差异。例如,当特定的电穿孔处理受益于更均匀的电场时,医师可以选择圆形真空杯(以及电极阵列)。当特定的电穿孔处理受益于更不均匀的电场时,医师可以选择多边形真空杯(以及电极阵列)。应当理解,关于电极设计,优选的是在相邻电极之间保持足够的间距,特别是当真空室在顶部处向内逐渐变细时,如通过图30a-31f中示出的设计所展示的。
182.现在参考图9a,示出了示例真空电穿孔组合件900,所述组合件包含真空杯902,所述真空杯被配置成用于无针注射药剂,特别是通过射流注射。因此,真空杯902可以被称为“无针”真空杯902或“射流注射”真空杯902。本发明的实施例的真空杯902类似于上文描述的真空杯2、502、702、802,特别是上文参考图1-4f描述的真空杯2。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本发明的实施例的真空杯902与上文参考图1-4f描述的真空杯2之间的差异。
183.如上所述,真空杯902具有壳体主体926,所述壳体主体限定真空室906,所述真空室其中安置有电极908以及第一端口912、第二端口914和第三端口916,每个端口与真空室906连通。如上所述,第一端口912被配置成与真空源106连接,第二端口914被配置成用于电路系统等进入真空室906。然而,本实施例的第三端口916被配置成接收射流注射装置970,用于将注射剂142的小流或“射流”注射到抽吸到真空室906中的组织902中。另外,壳体主体926在第三端口916的外端处限定安装构造948,所述安装构造被配置成提供与注射装置970的密封耦接器。安装构造948可以承载一个或多个密封构件,如密封o形环951,所述密封构
件可以位于安装构造948中限定的收纳器953中并且被配置成提供与注射装置970的外部的密封接合。
184.射流注射970装置包含注射壳体972,所述注射壳体限定了流体室或储器974,其中储存了包含药剂的注射剂142。注射壳体972的外表面975与第三端口916以及与密封o形环951尺寸协作,以提供注射壳体972与真空室906之间的密封连接。注射壳体972的远侧部分976限定了与储器974流体连通的喷嘴978。喷嘴978被配置成将注射剂142从储器974排出到真空室906中。远侧部分976还可以包含至少部分地围绕喷嘴978的护罩980。护罩980可以充当物理屏障,所述物理屏障遏制在射流注射期间产生的注射剂142的任何潜在的后溅或反弹。护罩980还可以保护杯902的电路系统免于暴露于注射剂142。
185.喷嘴978的远侧端979优选地向远侧延伸超过护罩980的远侧端981。射流注射装置970包含柱塞982,所述柱塞在其远侧端处承载活塞984。活塞984的远侧尖端986和在其远侧端990处的储器974的内表面988具有互补几何形状,使得活塞984向远侧端990的推进将注射剂142的射流从喷嘴978排出并进入组织102。应当理解,储器974可以被配置成承载预先测量的体积或剂量的注射剂。此外,可以控制柱塞982,如通过发射机构或致动器,以通过喷嘴978排出预定剂量的注射剂并进入患者的组织102。作为非限制性实例,此类发射机构可以包含预装载的或可装载的弹簧或多个弹簧、压缩气体罐等。
186.射流注射装置970可以如2018年8月14日发布的题为“皮内注射装置(intradermal injection device)”的美国专利10,045,911(“'911参考文献”);2019年1月3日公开的题为“皮内射流注射电穿孔装置(intradermal jet injection electroporation device)”的美国专利公开第2019/0000489a1号;以及2009年5月28日公开的题为“带喷嘴自动禁用的无针注射装置(needle-free injection device with nozzle auto-disable)”的美国专利公开第2009/0137949a1号(“'949参考文献”)的任一项中更完整地公开的那样构造,所述美国专利中的每个美国专利的全部公开内容特此通过引用并入本文。
187.无针真空杯902和射流注射装置970具有互补特征,所述特征增强了由此提供的电穿孔处理。例如,参考图9b,当真空压力将组织102的堆140抽吸到真空室6中时,堆140上的皮肤层104收紧,暂时降低皮肤层104的弹性,这允许射流或注射剂流离开喷嘴978以更有效地刺穿皮肤层104,同时注射剂反弹更少。为了帮助收紧皮肤层104,医师可以使用足够的真空压力将皮肤层104抽吸到与喷嘴978的远侧端979接触,使得皮肤层104围绕喷嘴978的远侧端979变形,从而在与远侧端979的接触界面处的皮肤层104中形成凹陷104a并且进一步拉伸凹陷104a处的皮肤层104。皮肤层104处的此类紧绷与射流注射装置970的使用相结合,允许排出的注射剂142在注射时刺穿皮肤层104并穿透整个组织堆140,其程度大于针注射(与图4c比较),并且比没有真空压力辅助的射流注射装置更大。
188.整个组织堆140的注射剂渗透可以表征为加压注射剂在组织102内形成数千个微观切口或路径,因为注射剂被强制通过组织102,特别是脂肪组织103,有效地渗透组织。此外,通过此后使组织102经受真空压力(即,如在将组织堆140抽吸到室906中的真空脉冲的延续和任选地一个或多个后续真空脉冲中),根据上述流体分散机制,响应于真空压力,已经更广泛地分散的注射剂142可以进一步分散在整个组织堆140中。
189.现在参考图10a-10d,将描述无针真空杯1002的另一个实施例,其中真空杯1002具有真空室1006,所述真空室被配置成使得抽吸在其中的组织102被至少部分地拉入限定在
真空室1006内的电极1008中的多个孔1063中。本实施例的真空杯1002类似于上文描述的真空杯,特别是上文参考图9a-9b描述的真空杯902。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本实施例的真空杯1002与上述真空杯902之间的差异。
190.现在参考图10a-10b,本实施例的真空杯1002具有壳体主体1026,如上所述,所述壳体主体限定用于与真空源106连接的第一端口1012、用于为电路系统提供到真空室1006的通道的第二端口(未示出),以及用于提供与射流注射装置970的密封连接的第三端口1016。在本实施例中,第三端口1016不是直接延伸到真空室1006,而是第三端口1016向内延伸到由壳体主体1026限定的环形通道1062。环形通道1062至少部分地围绕真空室1006并沿径向方向r与其向外间隔开。壳体主体1026进一步限定多个壳体端口1060,所述壳体端口从环形通道1062向内朝向真空室1006延伸。因此,壳体主体1026可以限定歧管,所述歧管限定多个壳体端口1060。如上所述,电极1008可以由固定到壳体主体1026的内表面1022的套筒1052承载。套筒1052限定套筒端口1057,所述套筒端口提供壳体端口1060与孔1063之间的流体连通。因此,套筒端口1057还提供环形通道1062与真空室1006之间的流体连通。真空压力依次通过第三端口1016、环形通道1062、壳体端口1060、套筒端口1057和电极孔1063提供给真空室1006。在电极1008直接耦接到壳体主体1026的内表面1022的实施例中,电极孔1063可以直接与壳体端口1060邻接。环形通道1062可以沿围绕中心轴线的整圈环状地延伸,但是在其它实施例中,通道1062可以围绕中心轴线x延伸小于一整圈。
191.如图10a所示,每个电极1008可以限定单列孔1063,所述单列孔可以沿圆周方向c伸长。每列可以包含五(5)个孔1063,如所示的,所述孔可以表征为“5x1”(即,5行
×
1列)孔阵列1063或“孔阵列”。其它孔阵列也在本公开的范围内。例如,如图10c所示,每个电极1008的孔1063可以排列成具有多行和多列孔1063的孔阵列,所述孔与对应的套筒端口1057的行和列以及对应的壳体端口1060的行和列对齐。孔阵列可以是4x5阵列,但其它孔径阵列配置也在本公开的范围内。
192.如图10d所示,孔1008被配置成使得被抽吸到真空室1006中的组织102可以至少部分地在孔1063中的一个或多个内延伸,如突出显示的区域104a所示。这增加了皮肤层104与电极1008之间的粘附力,并且还增加了组织102与电极1006之间的接触表面积。此外,通过将如皮肤层104等的组织102拉入一个或多个孔1063,将真空压力传送到室1006中,本实施例的真空杯1002可以有效地拉动和拉伸堆140的皮肤层104,如远离中心轴线x,从而允许注射剂142的射流注射流比其它实施例更有效地穿透组织102。例如,通过将真空端口1060分布在整个室1006中,室1006中的真空压力不太可能将注射剂拉出注射部位处的组织。此外,皮肤层104的延伸到孔1063中的部分可以破坏和改变皮肤层104的顶部,从而改善组织堆140内的电场分布,类似于上文参考图6a-6d的突起664描述的方式。
193.继续参考图10a-10d,应当理解,真空杯1002可以被配置成感测单独的孔1063内、单独的套筒端口1057内和/或单独的壳体端口1060内存在和/或不存在组织。例如,每个电极1008中的一个或多个以及至多所有单独的孔1063可以包含可以感测相关联的孔1063内存在和/或不存在组织的单独的传感器。作为非限制性实例,此类组织传感器可以包含单独的电极,所述电极可以被配置成感测指示组织存在/不存在的电参数,如阻抗。前述实例的单独的组织感测电极可以与电穿孔电极1008电隔离,或者可替代地在与电穿孔电极1008分
离的通道上。在其它实施例中,组织传感器可以是另一种类型,如可以检测直接组织接触的力型传感器或可以检测单独的孔1063、套筒端口1057和/或壳体端口1060何时被密封的压力传感器,作为非限制性实例。
194.组织传感器可以与如有线电路系统或印刷电路系统等电路系统连接,所述电路系统与控制器114电通信。例如,此类电路系统可以是与用于控制电极1008的电路系统相同的印刷电路板(pcb)上的印刷电路系统。组织传感器可用于映射整个室1006的组织粘附。此类组织粘附映射信息可以用于数据收集目的,并且可以另外或可替代地用于主动压力反馈机制中,用于基于每个孔中的传感器读数向上或向下调节真空压力的水平。在此类组织粘附映射实施例中,组织传感器电路系统优选地包含用于每个组织传感器的单独的电路。作为组织粘附映射的替代方案,组织传感器可以共同位于共享电路上,并且控制器114可以计算与初始基线测量相比的集体传感器测量(即,总体“δ”)的变化,以提供对室壁发生了多少组织粘附的总体测量。
195.在射流注射真空杯的另外的实施例中,如上述杯902、1002,喷嘴978的远侧端979可以适于限定阵列的电极。作为此类实施例的非限制性实例,喷嘴978的远侧端979可以涂有导电材料或由导电材料制成,如导电涂料、金属或聚合物,并且可以与控制器114电通信。以此方式,喷嘴978的远侧端979可用于将电穿孔脉冲递送到真空室的内表面上的其它电极和/或从真空室的内表面上的其它电极递送电穿孔脉冲。在此类实施例中,其它电极可以是圆环型电极或半环状电极,如上文参考图3i-3l,和/或下文参考图15a-15c描述的那些电极。此类实施例将允许同心电穿孔脉冲图案(“发射图案”),包含下文更详细讨论的那些图案。本发明人成功地使用真空杯中的此类同心电极阵列来向兔和豚鼠进行流体的皮内射流注射,然后在注射部位进行皮内组织的电穿孔。
196.如上所述,本发明人已经从使用上述真空杯的真空辅助电穿孔处理中发现了许多有益结果。此类有益结果包含增加注射剂在皮下组织和皮肤组织中的流体分散,以及增加体内流体在处理部位处的渗透。
197.现在参考图11a,可以看到真空压力对注射部位的影响。在此实例中,使用相同的注射技术在相同的皮下深度处将等效体积的亚甲蓝注射剂在两个部位处注射到猪组织中。左侧示出的注射部位没有受到真空压力。使用上文参考图2a-2f所述的真空杯2,使右侧所示的注射部位经受约-10.6psi的真空压力15秒,所述真空杯具有约15mm的基座直径d1,室深度l2约为15mm,内壁锥角约为4度。两个部位都没有用电穿孔处理。在此实例中,真空压力有效地重新分配了流体并随后将注射剂保持在杯下方的区域内。如果进行了电穿孔,这将在杯的处理区域内提供更高的注射剂浓度。
198.现在参考图11b-11c,对豚鼠进行了对流体分散的真空压力的比较研究。受试者都施用了注射到脂肪组织中的亚甲蓝。图11b中的注射是使用类似于图9a所示的无针真空杯进行的。具体地,组织在射流注射期间位于响应于真空压力的真空室中。图11c中的注射是通过皮下针技术进行的并且没有施加真空压力。此研究中的两个受试者均未用电穿孔处理。如展示的,与不施加真空压力的皮下针注射(图11c)相比,真空辅助射流注射(图11b)在脂肪层中引起的注射剂分散明显更多。
199.现在参考图34a-34b,对豚鼠进行了电穿孔和真空压力对脂肪组织中细胞浸润的累积效应的比较研究。使用29号胰岛素注射器将编码绿色荧光蛋白(gfp)基因的质粒通过
皮下注射注射到肩胛间脂肪垫中的脂肪组织中。两名受试者的注射部位均用相同的真空压力处理。图34b中的受试者使用类似于图2a所示的真空杯在注射部位通过电穿孔进一步处理。图34a中的受试者没有通过电穿孔进行处理。在处理部位取组织学切片用于比较gfp表达(可见绿色荧光)和细胞浸润(4',6-二脒基-2-苯基吲哚(dapi)染色后可见蓝色荧光)。如所示的,在两名受试者的真空压力后(即,无论处理部位是否电穿孔)都可检测到gfp表达(绿色)。然而,与仅施加真空压力(图34a)相比,进一步施加电穿孔与真空压力(图34b)相结合增加了细胞浸润(蓝色)。这些研究表明,真空压力与电穿孔相结合的施加可以增强免疫原性。
200.现在参考图12,测试数据显示,在比较受试者豚鼠的体液免疫应答的为期12周的elisa研究中,使用图2a所示的真空杯2(蓝色图
‑“
真空”)处理的受试者与使用卡尺型电穿孔装置(红色图
‑“
卡尺”)处理的受试者相比,在为期12周的研究中体液免疫原性增加。通过在脂肪层中的针注射给两组中的受试者注射等效体积的pgx 2013(一种针对流感病毒核蛋白(np)的dna疫苗)并用电穿孔进行处理。
201.现在参考图13,在比较受试者豚鼠的体液免疫应答的为期8周的elisa研究中,用pgx 2303(一种针对人呼吸道合胞病毒融合乙二醇蛋白(rsv-f)的dna疫苗)在脂肪组织中注射,并且使用图2a所示的真空杯2进行电穿孔(蓝色图
‑“
真空”)处理的受试者与皮内注射疫苗和使用皮内针电极电穿孔装置进行电穿孔处理的受试者(红色图
‑“
id针电极ep”)相比,显示出相当的体液免疫原性。注射是等效剂量的(20ug)。皮内注射为100ul,脂肪注射为300ul。真空杯2的室直径d1为15mm,具有4个电极。
202.现在参考图14a-14b,一项为期6周的研究比较了用针对流感核蛋白的dna疫苗(pgx 2013)处理后(第0周、第2周和第4周)豚鼠的体液免疫原性数据。图14a示出了elisa数据,而图14b示出了来自同一研究的elispot数据。图中表示了以下组:(1)“id针电极ep”(红色图)
–
8ug芒图注射,然后使用皮内针电极电穿孔装置进行皮内电穿孔;(2)“真空射流+ep”(蓝色图)
–
将40ug射流注射到脂肪组织中,然后使用类似于图9a所示的装置进行真空辅助电穿孔;(3)“真空针”(绿色图)
–
使用图2a所示的装置,
–
将40ug皮下针注射到脂肪组织中,然后施加负真空压力,无电穿孔;(4)“真空针+ep”(紫色图)
–
将40ug皮下针注射到脂肪组织中,然后使用图2a所示的装置进行真空辅助电穿孔。
203.这些研究表明,本文所述的针注射真空电穿孔装置2和射流注射真空电穿孔装置902在处理脂肪组织时产生与用皮内针电极电穿孔装置处理产生的体液应答相当的体液免疫应答。
204.参考图15a-22,现在将描述被配置成靶向皮肤层104中的电穿孔的真空杯。
205.现在参考图15a-15b,示出了示例真空杯1502,所述真空杯包含电极阵列1509,所述电极阵列具有一个或多个圆环电极1508和沿真空杯1502的中心轴线x延伸的中心电极1511。本实施例的真空杯1502类似于上文描述的真空杯2、502、702、802、902、1002,特别是上文参考图9a-9b描述的真空杯902。因此,如上文使用的相似的附图标记表示本发明的实施例中的共同特征。为简洁起见,以下描述集中于本实施例的真空杯1502与上述真空杯902之间的差异。
206.本实施例的真空杯1502具有壳体主体1526,所述壳体主体限定内表面1522,所述内表面至少部分地限定真空室1506。壳体主体1526还限定第三端口1516,所述第三端口从
真空室1506沿中心轴线x向近侧延伸。中心电极1511延伸穿过第三端口1516并从内表面1522的端表面部分进入真空室1506。第三端口1516还延伸穿过安装构造1548,用于提供与中心电极1511的密封接合。与上述方式类似,安装构造1548可以承载一个或多个密封构件,如密封o形环1551,所述密封构件密封接合中心电极1511的外表面1513。中心电极1511的外表面1513的远侧部分1513z被配置成与被抽吸到真空室1506中的组织102接触。因此,远侧部分1513z可以被称为中心电极1511的“接触表面”1513z。接触表面1513z可以具有圆形轮廓,如半球形轮廓,所述轮廓的半径r1在0.5mm至约10mm的范围内,更具体地在约1mm至约7mm的范围内,更具体地在约1mm至约4mm的范围内。真空杯1502的中心轴线x优选地延伸穿过接触表面1513z的顶点。中心电极1511具有近侧部分1518,所述近侧部分可以比中心电极1511的与密封o形环1551接触的部分窄。因此,近侧部分1518可以被称为中心电极1511的“茎”。
207.现在参考图15c,电极阵列1509被配置成使得在电穿孔脉冲递送期间,中心电极1511充当正电极或负电极,而圆环电极1508中的一个或两个充当正电极或负电极中的另一个(即,中心电极1511的相反极性)。以此方式,中心电极1511在脉冲期间有效地向上移动电场145,将电穿孔场144聚焦在皮肤层104中。本实施例的真空杯1502可以在药剂被注射到皮肤层104中之后,如通过例如芒图注射或皮内射流注射等的针注射放置在靶标区域处的组织102上。应当理解,在其它实施例中,真空杯1502可以使用特征或“柱”来代替中心电极1511。柱可以呈现形状类似于真空室1506内的表面1513z的表面。柱表面被配置成与通过真空压力抽吸到室1506中的皮肤接触。例如,柱可以被配置成在施加真空压力期间使组织顺应或以其它方式围绕柱表面的一部分弯曲。此类组织-柱接触已显示出在施加真空压力期间有利地增强组织中的流体分散,如下文参考图42a和42d更详细讨论的。
208.现在参考图16a,示出了真空电穿孔组合件1600的版本,每个版本都包含真空杯1602,所述真空杯具有定位在真空室1606内的端表面1624上的电极阵列1609,与其远侧开口1620相对。端表面1624可以是基本上平坦的,并且可以由定位在室1606内的电极支撑构件1652限定。支撑构件1652可以被称为“插入物”并且可以承载阵列1609的电极1608。例如,支撑构件1652可以是电路板,如印刷电路板(pcb),所述支撑构件具有与如上述控制器114等控制单元电通信的电路系统。支撑构件1652还限定了多个延伸穿过其中的端口1660,提供真空室1606与用于与真空源连接的外部端口1616之间的流体连通。以此方式,支撑构件1652中的端口1660将真空压力传送到室1606中,将组织102抽吸到其中并与电极1608接触。电极1608可以具有突出和/或倾斜的几何形状,如圆锥形、金字塔形等,用于压入抽吸到室1606中的组织堆140的皮肤层104中,从而破坏和改变皮肤104的顶层,改善其中的电场分布,如上文所描述的。
209.真空电穿孔组合件1600可以被配置成接收注射装置,如无针注射装置,如上述射流注射装置970。因此,真空杯1602具有壳体主体1626,所述壳体主体可以限定用于接收射流注射装置970的至少远侧部分的收纳器1616,使得其喷嘴978与限定在支撑构件1652中的注射孔1617对齐。如所示的,喷嘴978和注射孔可以与真空杯1602的中心轴线同心对齐。
210.壳体主体1626还可以限定从真空室1606偏移的辅助或“隔离”室1607,使得支撑构件1652分离或插入在真空室1606与隔离室1607之间。为了注射剂142的皮内分散的目的,隔离室1607被配置成在喷嘴978的远侧端与端表面1624之间提供隔离距离l5,以允许在喷嘴
978与组织102之间有利地形成注射剂142流。具体地,隔离距离l5可以允许在液体流接近皮肤104时在所述液体流中形成不规则性。例如,此类不规则性可以包含数百、数千或甚至更多数量的微米和/或纳米大小的液滴,每个液滴以足以有效地允许流在皮肤104的外表面101中形成数百或数千微米和/或纳米大小的切口的速度接近皮肤104,从而提供在皮肤层104中定位的增强的注射剂分散。隔离距离l5连同其它因素,如射流注射器喷嘴几何形状和注射器力,也可以用作控制注射剂的最大穿透深度的手段。应当理解,隔离距离l5也可以表征为在使用期间喷嘴978的远侧端与皮肤104的外表面101之间的最小隔离距离。隔离距离l5可以在约1.0mm至约20mm的范围内。
211.如图16b所示,壳体主体1626可以任选地限定空心护罩1685,所述空心护罩延伸穿过隔离室1607并且可以邻接支撑构件1652的后表面1625,使得护罩1685的空心与支撑构件1652的注射孔1617流体连通。以此方式,空心护罩1685可以提供从喷嘴978的远侧端到真空室1606的直的、对齐的、受防护的通道,从而保护支撑构件1652(以及其电路系统)免于无意地暴露于注射剂流。
212.现在参考图17a-17b,示出了支撑构件1652的不同实施例,其中电极1608和端口1660围绕注射孔1617以不同的图案布置。如图17a所示,电极1608可以沿与中心轴线x同心的圆周轴c2排列成圆形或环形图案。电极1608可以排列成单个同心环,或者如图17b所示,可以排列成多个环,所述环可以与中心轴线x同心,或可替代地相对于中心轴线x偏心。继续参考图17b,端口1660也可以围绕中心轴线x布置成一个或多个环。此外,电极1608和/或端口1660还可以(或可替代地)沿相应的轴r4、r5布置成辐条图案,从中心轴线x径向向外延伸。相邻电极1608“辐条”和相邻端口1660辐条的相应的轴r4、r5可以围绕中心轴线以相应的角度间隔a5、a6彼此偏移,所述角度间隔可以在约5度至约180度的范围内,更具体地,约15度至约120度。如所示的,轴r4、r5可以是线性的,但在其它实施例中,轴r4、r5可以是弧形的。应当理解,示例电极1608和端口1660图案作为非限制性实例提供,并且包含不对称和/或不规则图案在内的其它图案也在本公开的范围内。
213.现在参考图18a-18b,在另外的实施例中,真空电穿孔装置1802可以包含多个远侧真空室1807,用于在其中诱导组织,特别是皮肤。电极1808由电极支撑构件1852承载,所述电极支撑构件可以与限定主真空室1806的真空壳体主体1826的远侧端1810连接。以此方式,支撑构件1852的远侧端表面1824限定了装置1802的远侧端。壳体主体1826限定了用于向主真空室1806提供真空压力的主真空端口1812,并且可以限定第二端口1814,如用于为在主真空室1806内延伸的电路系统和到支撑构件1852提供通路。
214.现在参考图18b,本实施例的电极1808被布置成对,每个包含相对于彼此同心定位的外环电极1808a和内环电极1808b。外环电极1808a和内环电极1808b可以是沿纵向方向l伸长的管状构件,并且通过支撑构件1852延伸到其后表面1825,并且任选地进一步延伸到主真空室1806中。每对的外环电极1808a和内环电极1808b通过电绝缘的环形材料层1894彼此径向隔开,从而将内环电极1808a和外环电极1808b彼此电隔离。在每个同心电极对中,外环电极1808a延伸到支撑构件1852的远侧端表面1824,而内环电极1808b从远侧端表面1824向近端凹陷。以此方式,远侧端真空室1807由外环电极1808a的内表面1808z、内环电极1808b的远侧端和绝缘层1894的远侧端表面共同限定,并且任选地还任选的是外环电极1808a的远侧端导入表面在表面1808y。
215.如图18c-18d所示,内环电极1808b的远侧端(以及任选地还有绝缘层1894的远侧端)可以从远侧端表面1824以偏移距离l6凹陷,所述偏移距离可以在约0.05mm至约5.0mm的范围内,并且更具体地在约0.5mm至约2.0mm的范围内,并且优选地在约0.8mm至约1.2mm的范围内。所述装置可以限定沿纵向方向l从近侧端1828到远侧端表面1824测量的装置长度l7。装置长度l7可以在约15.0mm至约200mm的范围内,并且更具体地在约20mm至约40mm的范围内,但是小于15.0mm和大于200mm的长度l7也在本实施例的范围内。
216.如以上所提及的,内环电极1808b可以是管状的,特别是以限定提供与主真空室1806流体连通的端口1860的方式。以此方式,施加到主真空室1806的真空压力通过内环电极1808b传送到远侧真空室1807,从而允许装置1802将皮肤层104的部分抽吸到远侧真空室1807中并与内环电极1808a和外环电极1808b接触。皮肤层104的此类变形可以破坏和改变其顶部,从而改善皮肤层104内的电场分布,类似于上述方式。
217.每对的内环电极1808a和外环电极1808b优选地具有相反的极性,使得电穿孔脉冲从环电极1808a、1808b中的一个通过组织递送到对的环电极1808a、1808b中的另一个。
218.如图18所示,电极阵列1809可以是圆形阵列,所述圆形阵列包含中心电极对1808a、1808b和外围电极对1808a、1808b的圆形图案,所述外围电极对沿围绕中心电极对1808a、1808b同心的圆周轴c2布置。应当理解,其它阵列图案也在本实施例的范围内。外围的相邻电极对1808a、1808b可以以相应的角间隔a5彼此间隔开,类似于上述方式。
219.现在参考图19a-19b,在另外的实施例中,真空电穿孔装置1902可以包含在壳体主体1926的远侧端1910处的电极支撑构件1952,类似于上述实施例的装置1802。在本实施例中,每个电极1908是管状的并且从支撑构件的远侧端表面1924延伸穿过支撑构件1924到其后表面1925,从而限定与壳体主体1926的真空室1906流体连通的端口1960。电极1908的端口1960的大小设定成使得皮肤层104的外部可以响应于真空室1906中的真空压力而延伸到端口1960中。本实施例的每个电极1908在电脉冲期间为单极性(正或负)。电极1908与可以递送电穿孔信号的电路系统连接,使得在电脉冲期间,一个或多个电极1908为一种极性(正或负),而一个或多个其它电极1908为相反极性。例如,继续参考图19a-19b,电极1908可以布置成圆形电极阵列1908,所述圆形电极阵列包含中心电极1908和围绕中心电极1908同心布置的外围电极1908的圆形图案。可以在中心电极1908与外围电极1908中的至少一个外围电极之间递送一个或多个以及至多每个电穿孔脉冲。电穿孔信号可以包含多个电穿孔脉冲,所述多个电穿孔脉冲以采用电极1908的分散图案的顺序递送,类似于上述方式。
220.现在参考图20和21a-21b,电极支撑构件2052、2152可以承载具有非圆形图案的电极阵列2009、2109。如图20所示,支撑构件2052可以具有正方形电极阵列2009,所述正方形电极阵列沿彼此基本上垂直的第一阵列方向ad1和第二阵列方向ad2基本上等距。在所展示的实施例中,阵列2009具有4x4阵列图案,但是其它正方形阵列图案也在本公开的范围内,作为非限制性实例,包含2x2、3x3、5x5、6x6、7x7、8x8、9x9、10x10等。
221.如图21a-21b所示,支撑构件2152可以具有沿第一阵列方向ad1比沿第二阵列方向ad2更长的矩形电极阵列2109。阵列2109可以包含例如第一行电极和对应的第二行电极,如在2x6(即,2行
×
6列)阵列2109中,但是其它矩形阵列2109图案也在本公开的范围内,作为非限制性实例,包含1x2、1x3、1x4、2x3、2x4、2x5、2x7、2x8、2x9、2x10、3x4、3x5、3x6、3x7、3x8、3x9、3x10、4x5、4x6、4x7、4,8、4x9、4x10、5x6、5x7、5,8、5x9、5x10电极阵列2109。
222.应当理解,上述正方形和矩形电极阵列2009、2109实际上可以具有以其相应的图案布置的任何数量的电极2008、2108。此类正方形和矩形电极阵列2009、2109可以产生可以以行或列方式激活的大致矩形电场,从而允许沿给定轴线的高度有序的电场。例如,如果注射剂被有意注射或碰巧沿着组织的一个轴向方向累积,那么可以容易地激活电极2008、2108的另外的行或列以处理期望的组织体积。在此方面,这些电极阵列2009、2109可以被表征为提供模块化激活功能。另外,矩形电极阵列2109可以放置在靶标区域上方的皮肤104上,使得第一阵列方向ad1(阵列沿所述第一阵列方向伸长)基本上与被有意注射的流体所沿的轴线对准,或者其中流体由于存在如纤维组织等各向异性特征而自然分布,由此在注射剂分散通过组织时将注射剂封装在电穿孔场内持续更长的持续时间。此外,由于阵列2109还限定了真空端口的阵列,所述真空端口在施加真空压力期间破坏皮肤104的顶层,矩形阵列2109还可以有效地在皮内组织中形成破坏通路,所述破坏通路进一步引导注射剂沿电穿孔场分散。
223.现在参考图22,示出了在皮内注射各种体积的编码绿色荧光蛋白(gfp)基因的质粒,然后用各种装置进行电穿孔处理后,豚鼠皮肤中的基因表达。在此研究中,在100ul、300ul、500ul和900ul的注射体积下,使用本文所描述的真空杯2、902对皮内组织进行真空辅助电穿孔以与注射体积成比例的方式显著增加了基因表达。在一项类似的研究中,本发明人发现gfp的基因表达也随着真空压力的增加而增加。相比之下,使用皮内针电极电穿孔装置的基因表达并未随着注射体积的增加而增强。进一步地,在没有真空施加或电穿孔的情况下单独增加注射体积不会增强基因表达。这些研究表明真空压力和注射体积影响基因表达。
224.现在参考图35a-35b,一项为期6周的研究使用真空辅助电穿孔装置在给定的电穿孔电压和电流下评估了室直径d1对豚鼠皮肤中免疫原性的影响。图35a比较了使用具有8mm、10mm、12mm和15mm室直径d1的真空杯的皮内真空辅助电穿孔处理后的体液免疫原性elisa数据。每个真空杯的皮内处理包含芒图注射50ug的mers dna疫苗,然后使用相同的电压和电流进行电穿孔。图35b示出了在图35a所展示的同一研究中第2周和第4周的细胞免疫应答elispot数据。此研究表明,在给定的电穿孔电压和电流限制下,体液免疫应答和真空杯直径之间存在直接的负相关。在细胞免疫应答方面,此研究还表明,室直径d1为8mm至12mm的真空杯产生了类似的结果,当直径d1从12mm增加到15mm时,细胞应答会发生降低。
225.现在参考图36a-36b,一项研究评估了真空压力和电穿孔电压参数对豚鼠皮肤中基因表达的有利组合。这些研究采用皮内注射(特别是芒图注射)编码绿色荧光蛋白(gfp)基因的质粒,然后使用类似于上述杯2的真空杯在各种真空压力和电压下进行电穿孔处理。对皮肤施加0kpa(无真空)、40kpa和70kpa的真空压力和0v(无电压)、50v、100v和200v的电压。在处理后3天观察处理部位反应和gfp表达。图36a示出了在各种真空压力和电压下对处理部位的视觉观察。在图36b中,针对各种电压和真空压力绘制了皮肤荧光信号的测量。这些研究表明真空压力和电压独立地增加gfp表达。这些研究还表明,在每个测试的电压下,较高的真空压力增强了gfp表达。
226.现在参考图23,一项为期8周的研究比较了豚鼠在hpv dna疫苗的皮内处理和电穿孔后的体液免疫原性elisa数据。表示了以下组:(1)“id针电极ep”(黑色图)
–
在100ul芒图注射66.7ug质粒后使用皮内针电极电穿孔装置进行处理;(2)“真空杯”(红色图)
–
在注射
1ml等效剂量的66.7ug质粒后,使用15mm真空杯电穿孔装置进行处理,所述装置由4个壁电极组成(参见例如,图2a),所述质粒也用139u/m的hylenex调配;(3)“真空杯3x剂量”(栗色图)
–
使用与“真空杯”组相同的装置和方法进行处理,但剂量增加到先前提到的组的3倍,所述组为200ug的质粒。所有组均在第0周、第4周和第7周进行处理。
227.现在参考图24a,一项为期11周的研究比较了非人灵长类动物在hpv dna疫苗(pgx 3001和3002)的皮内处理和电穿孔后的体液免疫原性elisa数据。表示了以下组:(1)“id针电极ep”(黑色图)
–
使用皮内针电极电穿孔装置的处理;(2)“真空杯”(红色图)
–
在注射与“id针电极ep”相同剂量后使用图2a所示的真空杯进行处理;(3)“真空杯6x剂量”(栗色图)
–
使用与“真空杯”组相同的装置和方法进行处理,但剂量增加到先前提到的组的6倍。所有组均在第0周、第4周和第9周进行处理。现在参考图24b-24d,在图24a所示的相同研究的第2周、第6周和第11周,分别示出了每组的细胞免疫应答elispot数据。这些研究表明,高剂量真空辅助电穿孔处理(第3组)比id针电极ep装置(第1组)产生更快的体液和细胞应答,而在等效剂量下,真空辅助电穿孔处理(第2组)的进行通常类似于id针电极ep装置(第1组)。此外,高剂量真空辅助电穿孔处理(第3组)在第十一(11)周时产生的细胞应答大约是id针电极ep装置(第1组)的十倍(10
×
)。
228.现在参考图37a-37b,一项为期6周的研究比较了真空辅助电穿孔装置与皮内针电极电穿孔装置在免疫原性方面的性能。图37a比较了豚鼠在用50ug的mers dna疫苗通过芒图注射然后电穿孔进行皮内处理后的体液免疫原性elisa数据。图中表示的组是:(1)“id-vep
”–
使用与图2a所示类似的真空杯进行处理;以及(2)使用皮内针电极电穿孔装置进行“id-ep”处理。两组均在第0周、第2周和第4周进行处理。此研究表明,与皮内针电极电穿孔装置相比,真空杯产生更快速但更强的体液应答。图37b示出了在图37a所展示的同一研究中第2周和第4周的细胞免疫应答数据。
229.图38显示了一项为期6周的研究,比较了用100ug复发性呼吸道乳头瘤病(rrp)dna疫苗通过芒图注射然后电穿孔皮内处理后豚鼠中的细胞免疫应答数据。图38中表示的组包含:(1)使用皮内针电极电穿孔装置进行“id-ep”处理;(2)“id-vep
”–
使用类似于图2a所示的真空杯进行处理。
230.图37b和38所示的研究表明,与皮内针电极电穿孔装置相比,真空杯产生基本等效的细胞免疫应答。另外,在图37a-38所示的研究期间,观察到处理后7天至10天内在真空杯处理部位处没有可见的组织损伤。
231.现在参考图39a-39b,一项为期4周的研究评估了真空压力和电穿孔对皮肤中免疫原性的累积效应。此研究比较了通过芒图注射50ug mers dna疫苗进行皮内处理后豚鼠的体液和细胞免疫应答。图39a示出以下组在第0周、第2周和第4周的体液免疫原性elisa数据:(1)“id-vep
”–
使用类似于图2a所示真空杯的真空辅助电穿孔处理;(2)“id-真空
”–
使用真空杯的真空脉冲、非电穿孔处理;(3)“id
”–
仅芒图注射。图39b示出了图39a所示相同研究的第4周的细胞免疫应答elispot数据。这些研究表明,在芒图注射后,单独的真空压力(即,没有电穿孔)可以产生至少部分体液应答,但是电穿孔对于真空压力引起免疫原性是必需的。本发明人认为,这些研究还表明前述免疫应答仅部分地由dna疫苗的表面转染解释。进一步的研究证实,电穿孔电压是比真空压力更强的免疫原性驱动力。
232.现在参考图40a-40b,比较电场的横截面视图显示为由被抽吸到真空室中的组织
堆中的两个不同示例电极阵列产生。图40a示出了由电极阵列产生的电场,所述电极阵列具有与图2a中所示的真空杯2的电极类似地配置的一对相对电极。相对电极8之间的电穿孔脉冲递送图案(也称为“发射图案”)导致电流在电极之间横向穿过组织堆140行进。图40b示出了由电极阵列产生的电场,所述电极阵列具有与图15a中所示的真空杯1502类似地配置的两个圆环电极和一个中心电极。此实例中的电穿孔脉冲发射图案使电流在圆环电极与中心电极之间同心地行进,从而将电场集中在与中心电极相邻的皮肤层104中。因此,图40a-40b展示了相对电极之间的电穿孔脉冲发射图案(图40a)产生了与圆环电极与中心电极之间产生的电场(图40b)相比更均匀地穿过皮肤层104的电场。基于所期望的特定电穿孔处理,可以有利地使用电场产生中的这些差异。
233.现在参考图41a-41b,一项为期8周的研究评估了电穿孔脉冲发射图案对免疫原性的影响。在此研究中,在通过芒图注射mers dna疫苗并随后使用具有图40a-40b所示的电极阵列的真空杯进行真空辅助电穿孔进行皮内处理后,对豚鼠的体液和细胞免疫应答进行了测试。图41a示出了两种阵列配置在第0周、第2周、第4周和第8周的体液免疫原性elisa数据。两组均在第0周、第2周和第4周进行处理。图41b示出了在图41a所示的相同研究期间在第4周和第4周之后的细胞免疫应答elispot数据。此研究表明,阵列配置在体液应答方面表现相似,而同心阵列在细胞应答方面显著优于相对阵列。
234.现在参考图42a-42d,一项研究评估了中心电极对豚鼠皮肤中液体分散的比较影响。测量了三组有色注射剂的流体分散:(1)仅芒图注射(即,无真空压力);(2)具有相对电极而没有中心电极的阵列(参见图40a);(3)具有中心电极的阵列(参见图40b)。通过芒图注射将等效体积的注射剂注射到每组。对第2组和第3组施加真空压力。此研究未进行电穿孔。图42b、42c和42d分别示出了第1组、第2组和第3组的组织中的流体分散。根据有色注射剂的视觉纵横比,将结果在图42a中示出。结果表明,在施加真空压力时,中心电极或特征的存在会影响注射剂的流体分散。这些结果进一步表明,真空室的内部几何形状可以影响施加真空压力时的流体分散。
235.应当理解,上述皮内真空电穿孔组件、装置和杯可以与各种调配物一起使用以增强真空辅助电穿孔处理。例如,注射剂142可以包含药剂与调配物的混合物,用于以有利的方式影响药剂的特性。此类调配物的非限制性实例包含透明质酸酶和hylenex(人重组透明质酸酶),所述调配物可以暂时分解药剂基质,从而允许以更高的药剂体积注射,而皮肤中的肿块或泡更小、疼痛更小。如图25-26所示,与不包含透明质酸酶的注射剂相比,包含透明质酸酶的芒图注射产生的泡(如左图所示)在高度和直径上都更小。透明质酸酶调配物在2019年9月19日公开的题为“体内使用软骨素酶和/或透明质酸酶以增强药剂的递送(in vivo use of chondroitinase and/or hyaluronidase to enhance delivery of an agent)”的美国专利公开第2019/0284263 a1号(“'263参考文献”)中有更完整的描述,所述美国专利公开的全部公开内容通过引用并入本文。通过在使用本文公开的真空电穿孔装置进行的注射中使用透明质酸酶,可以将更大体积的药剂注射到皮内组织中,从而允许医师使用本文具有更大处理区域107的装置处理更大的组织体积。例如,本发明人通过多次测试,使用具有各种室直径d1(例如,8mm、10mm和12mm)的真空杯与注射剂结合142,所述注射剂具有包含透明质酸酶(即,50%欧乃派克350(omnipaque 350)+50%150u/ml透明质酸酶(最终75u/ml透明质酸酶)),8mm直径真空杯可以容纳0.2ml的注射剂体积,基本将所有注射
剂拉入真空室中;10mm直径真空杯可以容纳约0.4ml的注射剂体积,基本将所有注射剂拉入真空室中;并且12mm直径真空杯可以容纳0.8ml的注射剂体积,基本将所有注射剂拉入真空室中。观察到注射剂调配物中透明质酸酶的存在显著增强了注射剂在皮肤层内的流体分散。来自这些测试的数据强烈表明,更高的注射剂体积应该在注射剂调配物中使用透明质酸酶,否则注射泡更大并且不会有利地横向扩散通过皮肤。
236.现在参考图27,一项为期4周的研究比较了在用针对mer的dna疫苗(pgx 9101)进行皮内处理,随后进行电穿孔后豚鼠在终点滴度方面的体液免疫应答。在第0周和第2周,所有组在胁腹以100ul芒图注射接受50ug的质粒。图中表示的组是:(1)“id针电极ep”(黑色图)-使用皮内针电极电穿孔装置进行处理;(2)“id针电极ep+hya”(灰色图)-与先前的组一样,使用皮内针电极电穿孔装置进行处理,但调配物包含270u/ml的intropharma透明质酸酶;(3)“15mm真空杯”(红色图)-使用图2a中所示的真空杯2进行处理,其中室直径d1为15mm;(4)“15mm真空杯”图中的同一真空杯,使用包含270u/ml的intropharma透明质酸酶的调配物。
237.现在参考图28,一项为期6周的研究比较了在用针对mer的dna疫苗(pgx 9101)进行皮内处理,随后在第0周、第2周和第4周进行电穿孔后豚鼠在终点滴度方面的体液免疫应答。图中表示的组是:(1)“id针电极ep”(蓝色图)-100ul注射50ug的质粒,随后用皮内针电极电穿孔装置进行处理;(2)“15mm真空-500ug”(红色图)-1ml芒图注射500ug的质粒,其中调配物包含270u/ml intropharma透明质酸酶。电穿孔由图2a中所示的真空杯递送,其中室直径l1为15mm;(4)“15mm真空-id输注500ug”(绿色图)-1ml深皮注射500ug的质粒,但在至少2分钟的过程中输注,其中调配物包含270u/ml的intropharma透明质酸酶。电穿孔由与前一组相同的真空杯2递送;(4)“10mm真空-50ug”(紫色图)-100ul芒图注射50ug的质粒,随后用图2a中所示的真空杯2进行处理,其中室直径l为10mm。
238.现在参考图29a,一项为期6周的研究比较了在皮内注射针对流感核蛋白的dna疫苗(pgx 2013),随后在第0周、第3周和第6周进行电穿孔后豚鼠在平均终点滴度方面的体液免疫应答。图中表示的组是:(1)“id针电极ep 1ug”(红色图)-通过芒图注射1ug的质粒并且然后使用皮内针电极电穿孔装置进行电穿孔来处理;(2)“真空,使用hya 10ug”(蓝色图)-1ml芒图注射调配物中的10ug的质粒,所述调配物包含用图2a中所示的真空杯2处理的139.5u/ml hylenex,其中室直径d1为15mm;(3)“真空,使用hya 1ug”(绿色图)-100ul芒图注射1ug的质粒,所述质粒包含139.5u/ml的hylenex,然后使用与前一组中的真空杯相同的真空杯2进行电穿孔;(4)“真空,不使用hya 1ug”(紫色图)-100ul芒图注射1ug的质粒,然后使用与组(2)和(3)中的真空杯相同的真空杯2进行电穿孔。图29b和29c示出了在图29a中的研究的第2周(图29b)和第4周(图29c)以斑点形成单位表示的细胞免疫应答。
239.现在参考图43a-43c,一项为期7天的研究评估了在豚鼠中单次高体积注射和真空辅助电穿孔处理与使用皮内针电极电穿孔装置的多次注射、多次电穿孔处理的比较效果。单次高体积真空辅助电穿孔处理使用15mm直径的真空杯进行,所述真空杯具有一对圆环电极和一个中心(同心)电极,类似于图15a所示的真空杯。单次注射是0.8ml芒图注射与135u/ml透明质酸酶共同调配的编码分泌型碱性磷酸酶(seap)的质粒,然后进行真空辅助电穿孔。多次注射、多次电穿孔处理包括六(6)次单独的0.1ml芒图注射,每次随后使用皮内针电极进行电穿孔(总共0.6ml注射剂和六(6)次应用电穿孔)。图43a示出了在施加真空压力之
前定位在注射剂上方的真空杯。图43b示出了在施加真空压力期间真空杯内的注射剂,其中可以看出组织内的注射剂已经围绕中心电极变形,从而将注射剂集中在电穿孔场处(参见图40b)。图43c示出了在第0天、第1天、第2天、第6天和第7天两种处理的seap表达(作为受试者系统性蛋白质产生的读数)。此研究表明,使用真空杯的单次、高体积、真空辅助电穿孔处理与使用针电极装置的六次注射、六次电穿孔处理基本等效。
240.这些研究表明,使用本公开的装置和组合件的真空辅助电穿孔能够将dna高体积递送到皮肤中。此外,透明质酸酶调配物(例如,hylenex)增强了皮肤真空辅助电穿孔后的免疫原性。此外,本文所描述的真空杯适于利用由透明质酸酶调配物提供的皮内组织中显著更高的注射剂体积,包含1000ul(1ml)或更高的注射剂体积。换言之,通过将透明质酸酶调配物与本公开的真空杯一起使用,真空杯可以处理显著更大体积的皮内组织。另外,本公开的装置和组合件产生比皮内针电极电穿孔装置更快的体液应答和与皮内针电极电穿孔装置相当的整体体液免疫应答。此外,这些研究表明,通过皮内组织的真空辅助电穿孔可以增强细胞应答动力学和量值。本发明人还发现,使用具有皮内组织真空辅助电穿孔的透明质酸酶调配物有效地允许转染表层以下的真皮层。
241.现在参考图44,一项为期8周的研究比较了电穿孔脉冲发射图案对免疫原性的体液免疫应答数据影响。在此研究中,在通过芒图注射mers dna疫苗并随后使用具有图40a-40b所示的电极阵列的真空杯进行真空辅助电穿孔进行皮内处理后,对豚鼠的体液和细胞免疫应答进行了测试。图41a示出了两种阵列配置在第0周、第2周、第4周和第8周的体液免疫原性elisa数据。两组均在第0周、第2周和第4周进行处理。图41b示出了在图41a所示的相同研究期间在第4周和第4周之后的细胞免疫应答elispot数据。此研究表明,阵列配置在体液应答方面表现相似,而同心阵列在细胞应答方面显著优于相对阵列。
242.现在参考图45a-47c,荧光镜图像示出了使用与图9所示的真空杯902类似的射流注射真空杯在各种真空压力和喷嘴到皮肤偏移距离下射流注射期间豚鼠中的比较组织偏转。这些图像中使用的注射剂是50%欧乃派克350溶液,以允许放射照相成像。在这些图像中的每一个中,叠加的横向参考线表示真空杯的远侧端(并且因此真空室的远侧端和真空施加之前的初始皮肤-室界面)。图45a-45c示出了在室内没有施加真空压力的情况下进行的射流注射。图46a-46c示出了在室内施加真空压力并且没有喷嘴到皮肤偏移距离的情况下进行的射流注射。图47a-47c示出了在室内施加真空压力并且具有3mm的喷嘴到皮肤偏移距离的情况下进行的射流注射。应当注意的是,图45a、46a和47a示出了组织预注射;图45b、46b和47b示出了射流注射期间的组织;并且图45c、46c和47c示出了注射后的组织。
243.如图45a-45c所示,在室中不施加真空压力的情况下,射流会导致显著的组织偏转(图45b),之后组织在注射后弹回喷嘴(图45c),但是注射剂通常停留在真空室下方。
244.如图46a-46c所示,当在注射期间在室内施加真空压力时(图46b),组织偏转消除。然而,如图46c所示,缺少喷嘴到皮肤偏移距离会导致注射剂在注射后停留在真空室下方。
245.现在参考图47a-47c,当以3mm的喷嘴到皮肤偏移距离进行射流注射并且在室内施加真空压力时,在注射期间组织偏转基本消除(图47b)。当皮肤在注射前被拉入真空室中时,如此研究所示,注射期间射流喷嘴与皮肤之间存在密切接触,并且真空压力足以防止组织偏转。此外,在注射后(图47c),与图46c中示出的非偏移设置相比,注射剂停留在室内并具有更大的垂直分布,其中注射剂被压缩到较小的垂直空间中。这些测试表明了本文所公
开的射流注射真空杯在注射剂流体分布方面提供的显著益处。
246.应当理解,尽管本文描述的实施例被配置成靶向皮内和/或皮下组织中的电穿孔,但是真空杯2、502、702、802、902、1002、1502、1602和真空装置1802、1902的任何设计参数的尺寸可以向上或向下缩放以靶向更具体和/或不同的组织层,如皮肤或甚至肌肉层内的特定组织层,如平滑肌和骨骼肌层。此外,本文的真空杯2、502、702、802、902、1002、1502、1602和真空装置1802、1902的设计参数可以根据需要调整以靶向其它类型组织的电穿孔,包含粘膜、器官等。
247.尽管已经对本公开进行详细说明,但是应当理解的是,在不背离由所附权利要求定义的本发明的精神和范围的前提下,本文可以作出各种改变、替换和替代。例如,本文描述的各种实施例的特征可以并入本文所描述的一个或多个以及至多所有其它实施例中。此外,本公开的范围并不旨在限于本说明书中描述的具体实施例。如本领域的普通技术人员将从中容易理解的,可以利用执行与本文所述的对应实施例中的功能基本上相同的功能或实现与本公开所述的对应实施例中的结果基本上相同的结果的当前存在或稍后待开发的过程、机器、制造、物质组合物、构件、方法或步骤。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1