离体γδT细胞群体的制作方法
离体
γδ
t细胞群体
技术领域
1.本发明涉及与抗tcrγ可变4(抗vγ4)抗体接触的γδt细胞群体。
背景技术:
2.对癌症的t细胞免疫疗法日益增长的兴趣集中在cd8+和cd4+alpha beta(αβ)t细胞亚群识别癌细胞和介导宿主保护性功能潜力的明显能力上,特别是当pd-1、ctla-4和其他受体所施加的抑制途径受到临床介导的拮抗作用去抑制时。然而,αβt细胞受mhc限制,这可导致移植物抗宿主病。
3.gamma delta t细胞(γδt细胞)代表在其表面表达独特的、定义γδt细胞受体(tcr)的t细胞的亚群。该tcr由一条gamma(γ)链和一条delta(δ)链组成,每条链都经历链重排,但与αβt细胞相比,具有有限数量的v基因。编码vγ的主要trvg基因区段是trgv2、trgv3、trgv4、trgv5、trgv8、trgv9和非功能基因trgv10、trgv11、trgva和trgvb。最常见的trdv基因区段编码vδ1、vδ2和vδ3,外加几个同时具有vδ和vα名称的v区段(adams等人,296:30-40(2015)cell immunol.)。人γδt细胞可以根据它们的tcr链进行广泛分类,因为某些γ和δ类型在细胞上更普遍地(但不完全地)在一种或多种组织类型中被发现。例如,大多数血液驻留γδt细胞表达vδ2 tcr,通常是vγ9vδ2,而这在组织驻留γδt细胞(诸如皮肤中的那些)中不太常见,组织驻留γδt细胞更频繁地使用与γ链配对,例如常常与肠道中的vγ4配对的vδ1 tcr。
4.然而,迄今为止,由于vγ4 tcr与其它trgv家族成员(诸如vγ2 tcr)之间的高度同源性,能够仅靶向vγ4 tcr的形式尚不可能。因此,对于对vγ4具有特异性的抗体(包括此类特异性地结合或调节vγ4 tcr的特异性抗体)的需要未得到满足。
技术实现要素:
5.根据本发明的第一方面,提供了一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4 t细胞的细胞群体施用抗体或其片段,所述抗体或其片段与γδt细胞受体(tcr)的vγ4链特异性地结合而不与γδtcr的γ可变2(vγ2)链特异性地结合。应当理解,这是参考来自同一物种的vγ4链和vγ2。优选地,根据本文描述的所有方面和实施方案,该物种是智人(homo sapiens)(人)并且因此本发明还提供了一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括施用抗体或其片段,所述抗体或其片段与γδt细胞受体(tcr)的人γ可变4(vγ4)链特异性地结合而不与γδtcr的人γ可变2(vγ2)链特异性地结合。例如,人vγ4链可以具有根据seq id no.1的氨基酸1-99的序列并且/或者人vγ2链可以具有根据seq id no.335的序列。在其它物种中,该抗体或其片段与γδt细胞受体(tcr)的人γ可变4(vγ4)链的物种特异性直系同源物特异性地结合,而不与γδtcr的人γ可变2(vγ2)链的物种特异性直系同源物特异性地结合。因此,该抗体或其片段可以与具有对应于seq id no.1的氨基酸1-99的序列的γδt细胞受体(tcr)的人γ可变4(vγ4)链或其非人直系同源物特异性地结合,而不与具有对应于seq id no.335的序列的γδtcr的人γ可变2
(vγ2)链或其非人直系同源物特异性地结合。这种背景下的直系同源物可以意指与参考序列具有最高序列相似性的γ链序列,或者优选具有相同功能(例如与体内直系同源配体具有相互作用)的γ链序列。例如,在小鼠中,依据heilig和tonegave命名法指定为vγ7的蛋白质与人vγ4在功能上最密切相关(barros等人(2016)cell,167:203-218.e17)。
6.这是该领域的重大进步。例如,在人中,vγ4链和vγ2链高度同源(序列同一性为91%),仅9个氨基酸存在差异。这九个变化中的三个变化映射跨越cdr1和cdr2,而这九个变化中的四个变化映射到框架区3(fr3)的亚区-seq id no:1的氨基酸67-82。由于vγ4链与vγ2链之间的序列相似性非常高,先前认为不可能开发出能够特异性地区分γδtcr的人vγ4链和vγ2链的抗体或其片段。令人惊讶地并且与本领域的普遍观点相反,发明人已经能够使用本文更详细描述的方法开发出此类抗体。因此,本发明提供了使用能够特异性地调节含vγ4的γδtcr的抗体及其片段的离体方法。
7.本文描述的抗体或其片段可以与γδtcr的人vγ4链的包含seq id no:1的氨基酸区域67-82内的一个或多个氨基酸残基的表位结合。
8.根据本发明的再一个方面,提供了一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗vγ4抗体或其片段,所述抗vγ4抗体或其片段包含以下的一者或多者:
9.cdr3,其包含与seq id no:2-47中的任一个,优选与seq id no:10和/或33具有至少80%序列同一性的序列;
10.cdr2,其包含与seq id no:48-70和序列:a1-a23(图1)中的任一个序列,优选与seq id no:56和/或a9具有至少80%序列同一性的序列;和/或
11.cdr1,其包含与seq id no:71-116中的任一个,优选与seq id no:79和/或102具有至少80%序列同一性的序列。
12.在一些实施方案中,抗vγ4抗体或其片段可以包含以下的一者或多者:
13.重链cdr3(hcdr3),其包含与seq id no:2-24中的任一个,优选与seq id no:10具有至少80%序列同一性的序列;
14.重链cdr2(hcdr2),其包含与seq id no:48-70中的任一个,优选与seq id no:56具有至少80%序列同一性的序列;和/或
15.重链cdr1(hcdr1),其包含与seq id no:71-93中的任一个,优选与seq id no:79具有至少80%序列同一性的序列。
16.可替代地或除此之外,抗vγ4抗体或其片段可以包含以下的一者或多者:
17.轻链cdr3(lcdr3),其包含与seq id no:25-47中的任一个,优选与seq id no:33具有至少80%序列同一性的序列;
18.轻链cdr2(lcdr2),其包含与序列:a1-a23(图1)中的任一个,优选与seq id no:a9具有至少80%序列同一性的序列;和/或
19.轻链cdr1(lcdr1),其包含与seq id no:94-116中的任一个,优选与seq id no:102具有至少80%序列同一性的序列。
20.在一些实施方案中,抗vγ4抗体或其片段包含与seq id no:117-162中的任一个具有至少80%序列同一性的氨基酸序列。在一些实施方案中,抗vγ4抗体或其片段可以包含与seq id no:117-139中的任一个,优选与seq id no:125具有至少80%序列同一性的重
no:26的lcdr3,任选地其中所述vl包含seq id no:141;
40.(j)vh,其包含具有seq id no:74的hcdr1、具有seq id no:51的hcdr2和具有seq id no:5的hcdr3,任选地其中所述vh包含seq id no:120;和
41.vl,其包含具有seq id no:97的lcdr1、具有序列a4(图1)的lcdr2和具有seq id no:28的lcdr3,任选地其中所述vl包含seq id no:143;
42.(k)vh,其包含具有seq id no:75的hcdr1、具有seq id no:52的hcdr2和具有seq id no:6的hcdr3,任选地其中所述vh包含seq id no:121;和
43.vl,其包含具有seq id no:98的lcdr1、具有序列a5(图1)的lcdr2和具有seq id no:29的lcdr3,任选地其中所述vl包含seq id no:144;
44.(1)vh,其包含具有seq id no:76的hcdr1、具有seq id no:53的hcdr2和具有seq id no:7的hcdr3,任选地其中所述vh包含seq id no:122;和
45.vl,其包含具有seq id no:99的lcdr1、具有序列a6(图1)的lcdr2和具有seq id no:30的lcdr3,任选地其中所述vl包含seq id no:145;
46.(m)vh,其包含具有seq id no:77的hcdr1、具有seq id no:54的hcdr2和具有seq id no:8的hcdr3,任选地其中所述vh包含seq id no:123;和
47.vl,其包含具有seq id no:100的lcdr1、具有序列a7(图1)的lcdr2和具有seq id no:31的lcdr3,任选地其中所述vl包含seq id no:146;
48.(n)vh,其包含具有seq id no:78的hcdr1、具有seq id no:55的hcdr2和具有seq id no:9的hcdr3,任选地其中所述vh包含seq id no:124;和
49.vl,其包含具有seq id no:101的lcdr1、具有序列a8(图1)的lcdr2和具有seq id no:32的lcdr3,任选地其中所述vl包含seq id no:147;
50.(o)vh,其包含具有seq id no:80的hcdr1、具有seq id no:57的hcdr2和具有seq id no:11的hcdr3,任选地其中所述vh包含seq id no:126;和
51.vl,其包含具有seq id no:103的lcdr1、具有序列a10(图1)的lcdr2和具有seq id no:34的lcdr3,任选地其中所述vl包含seq id no:149;
52.(p)vh,其包含具有seq id no:81的hcdr1、具有seq id no:58的hcdr2和具有seq id no:12的hcdr3,任选地其中所述vh包含seq id no:127;和
53.vl,其包含具有seq id no:104的lcdr1、具有序列a11(图1)的lcdr2和具有seq id no:35的lcdr3,任选地其中所述vl包含seq id no:150;
54.(q)vh,其包含具有seq id no:82的hcdr1、具有seq id no:59的hcdr2和具有seq id no:13的hcdr3,任选地其中所述vh包含seq id no:128;和
55.vl,其包含具有seq id no:105的lcdr1、具有序列a12(图1)的lcdr2和具有seq id no:36的lcdr3,任选地其中所述vl包含seq id no:151;
56.(r)vh,其包含具有seq id no:85的hcdr1、具有seq id no:62的hcdr2和具有seq id no:16的hcdr3,任选地其中所述vh包含seq id no:131;和
57.vl,其包含具有seq id no:108的lcdr1、具有序列a15(图1)的lcdr2和具有seq id no:39的lcdr3,任选地其中所述vl包含seq id no:154;
58.(s)vh,其包含具有seq id no:87的hcdr1、具有seq id no:64的hcdr2和具有seq id no:18的hcdr3,任选地其中所述vh包含seq id no:133;和
59.vl,其包含具有seq id no:110的lcdr1、具有序列a17(图1)的lcdr2和具有seq id no:41的lcdr3,任选地其中所述vl包含seq id no:156;
60.(t)vh,其包含具有seq id no:89的hcdr1、具有seq id no:66的hcdr2和具有seq id no:20的hcdr3,任选地其中所述vh包含seq id no:135;和
61.vl,其包含具有seq id no:112的lcdr1、具有序列a19(图1)的lcdr2和具有seq id no:43的lcdr3,任选地其中所述vl包含seq id no:158;
62.(u)vh,其包含具有seq id no:90的hcdr1、具有seq id no:67的hcdr2和具有seq id no:21的hcdr3,任选地其中所述vh包含seq id no:136;和
63.vl,其包含具有seq id no:113的lcdr1、具有序列a20(图1)的lcdr2和具有seq id no:44的lcdr3,任选地其中所述vl包含seq id no:159;
64.(v)vh,其包含具有seq id no:91的hcdr1、具有seq id no:68的hcdr2和具有seq id no:22的hcdr3,任选地其中所述vh包含seq id no:137;和
65.vl,其包含具有seq id no:114的lcdr1、具有序列a21(图1)的lcdr2和具有seq id no:45的lcdr3,任选地其中所述vl包含seq id no:160;
66.和/或
67.(w)vh,其包含具有seq id no:93的hcdr1、具有seq id no:70的hcdr2和具有seq id no:24的hcdr3,任选地其中所述vh包含seq id no:139;和
68.vl,其包含具有seq id no:116的lcdr1、具有序列a23(图1)的lcdr2和具有seq id no:47的lcdr3,任选地其中所述vl包含seq id no:162。
69.在一些实施方案中,抗vγ4抗体或其片段包含与seq id no:163-185中的任一个具有至少80%序列同一性的氨基酸序列。
70.在一些实施方案中,抗vγ4抗体包含与seq id no:233-255中的任一个具有至少80%序列同一性的氨基酸序列。在一个相关的实施方案中,抗vγ4抗体包含与seq id no:284-306中的任一个具有至少80%序列同一性的重链氨基酸序列和/或与seq id no:307-329中的任一个具有至少80%序列同一性的轻链氨基酸序列,或者由与seq id no:284-306中的任一个具有至少80%序列同一性的重链氨基酸序列和/或与seq id no:307-329中的任一个具有至少80%序列同一性的轻链氨基酸序列组成。
71.在一些实施方案中,抗vγ4抗体或其片段与γδt细胞受体(tcr)的vγ4链特异性地结合并且与如本文所限定的抗体或其片段竞争与γδt细胞受体(tcr)的vγ4链的结合。
72.根据本发明的进一步方面,提供了通过如本文所限定的离体方法获得的vγ4 t细胞群体。
73.根据本发明的进一步方面,提供了一种包含如本文所限定的vγ4 t细胞群体的组合物。
74.根据本发明的进一步方面,提供了一种包含如本文所限定的vγ4 t细胞群体,任选地连同药学上可接受的稀释剂或载剂的药物组合物。
75.根据本发明的进一步方面,提供了如本文所限定的本发明的药物组合物,其用作药物。类似地,提供了一种治疗有需要的受试者的疾病或病症(例如癌症、传染性疾病或炎性疾病)的方法,其包括向受试者施用治疗有效量的如本文所限定的本发明的vγ4 t细胞群体或本发明的药物组合物。
附图说明
76.图1:示例性抗vγ4抗体的互补决定区(cdr)序列。示出了本文描述的示例性抗vγ4抗体的cdr序列。相应的seq id no.示于每个序列的右侧。
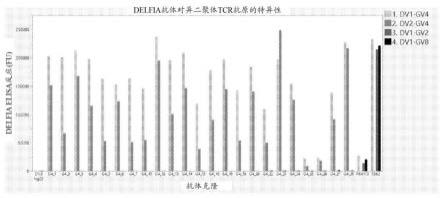
77.图2:经由delfia elisa测定获得的针对异二聚体tcr抗原的抗体特异性。(a)呈现了所有通过qc评估(分析sec-hplc)并且还对人vγ4链表现出特异性的抗体的结果。测试了这些抗体(x轴)分别对四种不同的重组异二聚体人tcr(dv1-gv4;dv2-gv4;dv1-gv2;dv1-gv8)的结合。对照包括同种型对照的抗鸡溶菌酶d1.3抗体(内部,最左侧)加上抗vδ1抗体rea173(miltenyi)和ts8.2(fisher)-最右侧。(b)数据的量化示于(a)中并且进一步显示每个示例克隆与人vγ4链的结合对比该克隆与人vγ2链的结合的倍数变化增加。
78.图3:抗体与作为重组抗原或作为重组细胞表面受体呈现的vγ4vδ1 tcr的结合的比较。(a)经由delfia elisa测定的抗体与dv1-gv4抗原的结合(y轴)或与jrt3-hu17细胞的结合(x轴)的经归一化和经对数转换的x/y图。垂直灰色虚线指示本研究中被认为对于jrt3-hu17结合为阴性(左)和阳性(右)的mab的截止值。将x轴gmfi信号针对cd3作归一化,以解释每个构建体之间tcr表达的变化。(b)进一步例示阴性/阳性截止值的流数据图。抗体g4_26(左中图)表现出在阴性组中最高的归一化gmfi值,并表现出与阴性同种型对照(d1.3;最左侧图)相似的图。g4_15(中图)具有在阳性组中最低的归一化gmfi值并且与d1.3同种型对照相比,表现出明显但较弱的染色增强。还提供了中间信号(g4_16;中右)和强信号(g4_18;最右侧)用于参考。
79.图4:抗体与一组含有不同cdr3序列并且/或者与不同的δ链配对的重组表达的γ4 tcr的结合。(a)针对在jurkat细胞上表达的重组tcr生成的抗体结合信号的直方图表示。序列分析如下呈现:针对vγ4vδ1-hu17的抗体结合信号(黑色柱);针对vγ4vδ1-hu20的抗体结合信号(水平条纹柱);针对vγ4vδ2 hu20γ-pbδ的抗体结合信号(斜条纹柱);针对vγ4vδ5-les的抗体结合信号(白色柱)。将所有结合信号针对cd3作归一化,以解释jrt3中不同tcr构建体之间tcr表达的变化。(b)本研究中主要抗体中的两种主要抗体的示例流数据,其用于进一步例示对所有vγ4 tcr显示为阳性的一个示例性抗体(g43)与仅对一些vγ4 tcr显示为阳性的另一主要抗体(g44)之间的差异。
80.图5:针对jrt3细胞上表达的嵌合hu17 tcr的抗体结合和表位作图。(a)呈现了所指示的嵌合hu17构建体的种系编码的可变γ区的比对。注意,由于空间限制,成熟vγ2/3/4序列的前10个氨基酸(seq id no:256的氨基酸1-10[ssnlegrtks])被省略,但在所有结构中都是相同的。指示出了不同于参考hu17序列(野生型vγ4 tcr)的氨基酸。(b)每种抗体与所指示的嵌合tcr构建体的反应性的汇总表。结果强调了每种指示的抗体与在jrt3细胞上表达的单个tcr的相对结合特异性。(c)用于例示本研究中观察到的差异性结合信号的表位作图的示例流数据。
[0081]
图6:表达vγ4 tcr(hu17)的细胞上的示例抗体结合和赋予的功能。(a)抗体与jrt3-hu17的结合的滴定,其显示所有示例抗体均与jrt3-hu17细胞结合。用作阴性对照的非转导的jrt3细胞(无tcr)证明hu17的表达对于抗体结合是必需的。(b)经滴定的抗体赋予的tcr下调对比阳性对照抗体:抗cd3ε(ucht-1,biolegend)或抗泛-tcrγδ(anti-pan-tcrγδ)(b1,biolegend)赋予的下调。(c)经滴定的抗体赋予的cd69上调对比通过比较器抗体:抗cd3ε(ucht-1,biolegend)或抗泛-tcrγδ(b1,biolegend)观察到的上调。
[0082]
图7:原代vγ4阳性细胞的示例抗体靶向和调节。(a)抗vγ4抗体与从两个个体供体的皮肤扩增的原代vγ4+t细胞的结合的滴定,其表明所有示例抗体都可以以剂量依赖性方式与皮肤来源的vγ4+t细胞结合。采用同种型对照作为阴性对照,证明示例抗体对vγ4的特异性。(b)抗vγ4抗体与源自外周血单核细胞(pbmc)的vy4+t细胞的结合,其表明实质上所有示例抗体都可以与血液来源的原代vγ4+t细胞结合。采用rsv同种型对照作为阴性对照。(c)抗vγ4抗体g4_3、g4_12和g4_18与来自于结直肠癌(crc)患者的肠源性上皮内淋巴细胞(iel)的结合,其表明所有三种示例抗体均与该细胞群体结合。细胞被门控为单个活的γδ
+
、igg1
+
(vγ4)
+
。(d)用抗vγ4抗体刺激前肠道消化物中vγ4+γδ t细胞的表型分析,其表明示例抗体g4_18可被用于鉴定vγ4+细胞。1.4%的活的单细胞为vδ1+。在这些中,44.2%与vγ4配对,并且这些展示出组织驻留标志物(cd69+cd103+)。(e)分别由示例抗体g4_12和g4_18赋予的tcr下调对比同种型阴性对照赋予的下调,其随附有代表性facs图。
[0083]
图8:vγ4特异性抗体增加入原代vγ4 t细胞的数目的用途。(a)用于说明在il-2或il-2+il-15的存在下在pbmc与板结合的抗vγ4克隆g4_12一起培养14天后vγ4 t细胞与同种型对照相比的增加(如通过用克隆g4_18染色来确定)的示例流数据。(b)在il-2或il-2+il-15的存在下来自两个供体的pbmc与板结合的抗vγ4克隆g4_12一起培养7天(上一行)和14天(下一行)后vγ4t细胞与同种型对照相比的增加(如通过用克隆g4_18染色来确定)的汇总。
具体实施方式
[0084]
定义
[0085]
除非另外定义,否则本文使用的所有技术和科学术语均具有与本发明所属领域中技术人员通常所理解的含义。如本文中所用,以下术语具有下面归于它们的含义。
[0086]
gamma delta(γδ)t细胞代表在其表面表达独特的、定义的t细胞受体(tcr)的t细胞的小亚群。该tcr由一条gamma(γ)链和一条delta(δ)链组成。每条链含有可变(v)区、恒定(c)区、跨膜区和胞质尾。v区含有抗原结合位点。人γδt细胞有两种主要亚型:一种在外周血中占优势的亚型和一种在非造血组织中占优势的亚型。这两个亚型可以由细胞上存在的δ和/或γ的类型来定义。例如,大多数血液驻留γδt细胞表达vδ2 tcr,例如vγ9vδ2,而这在组织驻留γδt细胞中不太常见,组织驻留γδt细胞更频繁地使用例如皮肤中的vδ1和肠道中的vγ4。对“vγ4 t细胞”的提及是指具有vγ4链的γδt细胞,即vγ4+细胞。
[0087]
对“γ可变4”的提及也可以称为vγ4或vg4。γ可变4多肽,或编码含有该区域的tcr链的核苷酸,或包含该区域的tcr蛋白复合物可称为“trgv4”。与γδtcr的vγ4链相互作用的抗体或其片段实际上全部是与vγ4结合的抗体或其片段并且可称为“抗tcrγ可变4抗体或其片段”或“抗vγ4抗体或其片段”。对人vγ4多肽的提及可以意指具有对应于seq id no.1的氨基酸1-99的氨基酸序列的多肽。该99个氨基酸的序列也对应于seq id no:334。因此,应理解根据本发明的所有方面和实施方案,本文对seq id no.1的氨基酸1-99的提及可以与对seq id no:334的提及互换使用。例如,本文对seq id no:1的氨基酸区域67-82的提及等同于对seq id no:334的氨基酸区域67-82的提及并且可以在本文中互换使用。
[0088]
对“δ可变1”的提及也可以称为vδ1或vd1。δ可变1多肽,或编码含有该区域的tcr链的核苷酸,或包含该区域的tcr蛋白复合物,可称为“trdv1”。与γδtcr的vδ1链相互作用的
抗体或其片段实际上全部是与vδ1结合的抗体或其片段并且可称为“抗tcrδ可变1抗体或其片段”或“抗vδ1抗体或其片段”。对人vδ1多肽的提及可以意指具有对应于seq id no.337的氨基酸序列的多肽。
[0089]
对“γ可变2”的提及也可以称为vγ2或vg2。γ可变2多肽,或编码含有该区域的tcr链的核苷酸,或包含该区域的tcr蛋白复合物可称为“trgv2”。与γδtcr的vγ2链相互作用的抗体或其片段实际上全部是与vγ2结合的抗体或其片段并且可称为“抗tcrγ可变2抗体或其片段”或“抗vγ2抗体或其片段”。对人vγ2多肽的提及可以意指具有对应于seq id no.335的氨基酸序列的多肽。
[0090]
对“γ可变8”的提及也可以称为vγ8或vg8。γ可变8多肽,或编码含有该区域的tcr链的核苷酸,或包含该区域的tcr蛋白复合物可称为“trgv8”。与γδtcr的vγ8链相互作用的抗体或其片段实际上全部是与vγ8结合的抗体或其片段并且可称为“抗tcrγ可变8抗体或其片段”或“抗vγ8抗体或其片段”。对人vγ8多肽的提及可以意指具有对应于seq id no.336的氨基酸序列的多肽。
[0091]
术语“抗体”包括任何包含至少一个抗体可变结构域的抗体蛋白质构建体,该抗体可变结构域包含至少一个抗原结合位点(abs)。抗体包括但不限于iga、igg、ige、igd、igm型(及其亚型)的免疫球蛋白。由两条同一的重(h)链和两条相同的轻(l)链多肽组装而成的免疫球蛋白g(igg)抗体的整体结构在哺乳动物中已得到充分确立并且高度保守(padlan(1994)mol.immunol.31:169-217)。
[0092]
常规抗体或免疫球蛋白(ig)是包含以下四条多肽链的蛋白质:两条重(h)链和两条轻(l)链。每条链分为恒定区和可变结构域。重(h)链可变结构域在本文中缩写为vh,轻(l)链可变结构域在本文中缩写为vl。这些结构域、与这些结构域相关的结构域和源自这些结构域的结构域在本文中可称为免疫球蛋白链可变结构域。vh和vl结构域(也称为vh和vl区)可以进一步细分为称为“互补决定区”(“cdr”)的区域,其中散布着更保守的区域(称为“框架区”(“fr”))。框架区和互补决定区已经被精确定义(kabat等人sequences of proteins of immunological interest,第5版u.s.department of health and human services,(1991)nih公开号91-3242)。还存在cdr序列的替代编号惯例,例如chothia等人(1989)nature 342:877-883中列出的那些。在常规抗体中,每个vh和vl均由从氨基端到羧基端按以下顺序排列的三个cdr和四个fr组成:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。两条重免疫球蛋白链和两条轻免疫球蛋白链的常规抗体四聚体是由通过例如二硫键相互连接的重免疫球蛋白链和轻免疫球蛋白链形成,并且重链被类似地连接。重链恒定区包括三个结构域ch1、ch2和ch3。轻链恒定区由一个结构域即cl构成。重链的可变结构域和轻链的可变结构域是与抗原相互作用的结合结构域。抗体恒定区通常介导抗体与宿主组织或因子的结合,所述因子包括免疫系统的各种细胞(例如效应细胞)和经典补体系统的第一组分(c1q)。
[0093]
如本文所用的抗体片段(其也可称为“抗体片段”、“免疫球蛋白片段”、“抗原结合片段”或“抗原结合多肽”)是指抗体的这样的部分(或含有该部分的构建体),该部分与靶标,即γδt细胞受体的γ可变4(vγ4)链(例如其中一条或多条免疫球蛋白链不是全长的但与靶标特异性地结合的分子)特异性地结合。涵盖在术语抗体片段内的结合片段的实例包括:
[0094]
(i)fab片段(由vl、vh、cl和ch1结构域组成的单价片段);
[0095]
(ii)f(ab
′
)2片段(由在铰链区处通过二硫键连接的两个fab片段组成的二价片段);
[0096]
(iii)fd片段(由vh和ch1结构域组成);
[0097]
(iv)fv片段(由抗体单臂的vl和vh结构域组成);
[0098]
(v)单链可变片段scfv(由使用重组方法通过合成接头来联接的vl结构域和vh结构域组成,该合成接头使该vl结构域和vh结构域能够被制成单个蛋白链,在该单个蛋白链中,vl区和vh区配对从而形成单价分子);
[0099]
(vi)vh(由vh结构域组成的免疫球蛋白链可变结构域);
[0100]
(vii)vl(由vl结构域组成的免疫球蛋白链可变结构域);
[0101]
(viii)结构域抗体(dab,由vh或vl结构域组成);
[0102]
(ix)微型抗体(由一对经由ch3结构域连接的scfv片段组成);知
[0103]
(x)双抗体(由scfv片段的非共价二聚体组成,该scfv片段由来自一种抗体的vh结构域组成,该vh结构域由小肽接头连接到来自另一种抗体的vl结构域)。
[0104]“人抗体”是指具有源自人种系免疫球蛋白序列的可变区和恒定区的抗体。施用了所述人抗体的人受试者不会对所述抗体内所含主要氨基酸产生跨物种抗体反应(例如,称为hama反应-人抗小鼠抗体)。所述人抗体可以例如在cdr中且尤其是在cdr3中包括不是由人种系免疫球蛋白序列编码的氨基酸残基(例如,通过随机或位点特异性突变或通过体细胞突变引入的突变)。然而,该术语并非旨在包括其中源自另一哺乳动物物种(诸如小鼠)的种系的cdr序列已经被移植到人框架序列上的抗体。通过重组方式制备、表达、产生或分离的人抗体,诸如使用转染到宿主细胞中的重组表达载体表达的抗体、从重组的组合人抗体文库中分离的抗体、从对于人免疫球蛋白基因而言是转基因的动物(例如,小鼠)中分离的抗体,或通过任何其它涉及将人免疫球蛋白基因序列剪接至其它dna序列的方式制备、表达、产生或分离的抗体也可以称为“重组人抗体”。
[0105]
用来自人可变结构域的相应残基取代非人免疫球蛋白可变结构域的框架区中的至少一个氨基酸残基称为“人源化”。可变结构域的人源化可以降低在人类中的免疫原性。
[0106]“特异性”是指特定抗体或其片段可以结合的不同类型的抗原或抗原决定簇的数量。抗体的特异性是抗体将特定抗原识别为独特分子实体并将它与其它抗原区分开来的能力。与抗原或表位“特异性地结合”的抗体是本领域熟知的术语。如果分子与特定靶抗原或表位的反应比它与替代靶标的反应更频繁、更迅速、时间更长持续和/或亲和力更高,则称该分子表现出“特异性结合”。如果抗体以比其与其它物质的结合亲和力更大地、亲合力更高地、更容易地和/或持续时间更长地结合靶抗原或表位,则所述抗体与靶抗原或表位“特异性地结合”。如果抗体(或其片段)与靶标的结合与非相关结合物相比在统计学上显著,则可以认为该抗体(或其片段)与靶标特异性地结合。
[0107]
由抗原与抗原结合多肽解离的平衡常数(kd)表示的“亲合力”,是抗原决定簇与抗体(或其片段)上的抗原结合位点之间的结合强度的量度:kd值越小,抗原决定簇与抗原结合多肽之间的结合强度越强。可替代地,亲和力也可以表示为亲和常数(ka),即1/kd。亲和力可以通过已知方法根据目标特定抗原确定。例如,kd可以通过表面等离子体共振来确定。
[0108]
任何小于10-6
的kd值都被认为指示结合。抗体或其片段与抗原或抗原决定簇的特异性结合可以任何合适的已知方式确定,该方式包括例如scatchard分析和/或竞争性结合
测定,诸如放射免疫测定(ria)、酶免疫测定(eia)和夹心竞争测定、平衡透析、平衡结合、凝胶过滤、elisa、表面等离子体共振或光谱法(例如使用荧光测定)以及它们的本领域已知的不同变型。
[0109]“亲合力”是抗体或其片段与相关抗原之间的结合强度的量度。亲合力与抗原决定簇和抗体上的其抗原结合位点之间的亲和力及抗体上存在的相关结合位点的数量有关。
[0110]“人组织vγ4+细胞”和“造血和血液vγ4+细胞”和“肿瘤浸润淋巴细胞(til)vγ4+细胞”分别被定义为人组织或造血血液系统或人肿瘤中所含的或源自其中的vγ4+细胞。所有所述细胞类型都可以通过(i)它们的位置或它们所源自的位置和(ii)它们的vγ4+tcr表达来鉴定。
[0111]
适当地,该抗体或其片段(即多肽)是经分离的。“分离的”多肽是从其原始环境中取出的多肽。术语“经分离的”可用于指实质上不含具有不同抗原特异性的其它抗体的抗体(例如,特异性地结合vγ4或其片段、实质上不含特异性地结合除vγ4以外的抗原的抗体的分离的抗体)。术语“分离的”也可用于指这样的制品,其中分离的抗体足够纯从而能够在被配制为药物组合物的活性成分时进行治疗性施用,或为至少70-80%(w/w)纯的,更优选地,为至少80-90%(w/w)纯的,甚至更优选地为90-95%纯的;并且,最优选地,为至少95%、96%、97%、98%、99%或100%(w/w)纯的。
[0112]
适当地,用于本发明的多核苷酸是经分离的。“分离的”多核苷酸是从其原始环境中取出的多核苷酸。例如,如果将天然存在的多核苷酸与自然系统中的一些或所有共存材料分开,则天然存在的多核苷酸是经分离的。例如,如果将多核苷酸克隆到不是其自然环境的一部分的载体中或者如果多核苷酸包含在cdna内,则认为该多核苷酸是经分离的。
[0113]
抗体或其片段可以是“功能活性变体”,该功能活性变体还包括天然存在的等位基因变体,以及突变体或任何其它非天然存在的变体。如本领域已知的,等位基因变体是(多)肽的替代形式,该替代形式的特征在于具有基本上不改变多肽生物学功能的一个或多个氨基酸的取代、缺失或添加。作为非限制性实例,当含有cdr的框架被修饰时,当cdr本身被修饰时,当所述cdr被移植到替代框架上时,或者当并入n端或c端延伸时,所述功能活性变体仍然可以发挥功能。进一步地,含cdr的结合结构域可以与不同的伴侣链(诸如与另一种抗体共享的伴侣链)配对。在与所谓的“普通”轻链或“普通”重链共享后,所述结合结构域仍然可以发挥功能。进一步地,所述结合结构域可以在多聚化时发挥功能。进一步地,“抗体或其片段”还可以包含功能变体,其中vh或vl或恒定结构域已远离或朝向不同的规范序列(例如,如imgt.org中所列的)进行修饰并且仍然发挥功能。
[0114]
为了比较两个密切相关的多肽序列,可以使用ncbi blast v2.0,使用多肽序列的标准设置(blastp)计算第一多肽序列与第二多肽序列之间的“序列同一性%”。为了比较两个密切相关的多核苷酸序列,可以使用ncbi blast v2.0,使用核苷酸序列的标准设置(blastn)计算第一核苷酸序列与第二核苷酸序列之间的“序列同一性%”。
[0115]
如果多肽或多核苷酸序列与其他多肽或多核苷酸序列在它们的整个长度上共享100%的序列同一性,则称该多肽或多核苷酸序列与该其他多肽或多核苷酸序列相同或“同一”。序列中的残基从左到右进行编号,即对于多肽而言从n端到c端进行编号;对于多核苷酸而言从5
′
到3
′
端进行编号。
[0116]
在一些实施方案中,序列的任何指定的序列同一性%是在抗体的所有6个cdr的序
列不存在的情况下计算的。例如,抗vγ4抗体或其抗原结合片段可以包含:可变重链区序列,其与指定的可变重链区序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性;和/或可变轻链区序列,其与指定的可变轻链区序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性,其中任何氨基酸变异仅发生在可变重链和轻链区序列的框架区中。在此类实施方案中,具有某些序列同一性的抗vγ4抗体或其片段保留了相应抗vγ4抗体或其片段的完整重链和轻链cdr1、cdr2和cdr3序列。
[0117]
序列之间的“差异”是指与第一序列相比,在第二序列的某个位置中的单个氨基酸残基的插入、缺失或取代。两个多肽序列可以含有一个、两个或更多个此类氨基酸差异。在其它方面与第一序列同一(100%序列同一性)的第二序列中的插入、缺失或取代导致%序列同一性降低。例如,如果同一序列为9个氨基酸残基长,则第二序列中的一个取代导致序列同一性为88.9%。如果第一多肽序列和第二多肽序列为9个氨基酸残基长并且共享6个同一残基,则第一多肽序列和第二多肽序列共享大于66%的同一性(第一多肽序列和第二多肽序列共享66.7%的同一性)。
[0118]
可替代地,为了比较第一参考多肽序列与第二比较多肽序列的目的,可以确定为产生第二序列而对第一序列制作的添加、取代和/或缺失的数目。“添加”是将一个氨基酸残基添加到第一多肽的序列中(包括在第一多肽的任一端处添加)。“取代”是用一个不同的氨基酸残基取代第一多肽的序列中的一个氨基酸残基。所述取代可以是保守性的或非保守性的。“缺失”是使第一多肽的序列中缺失一个氨基酸残基(包括在第一多肽的任一端处缺失)。
[0119]
使用三字母代码和一字母代码,天然存在的氨基酸可称为如下:甘氨酸(g或gly)、丙氨酸(a或ala)、缬氨酸(v或val)、亮氨酸(l或leu)、异亮氨酸(i或ile)、脯氨酸(p或pro)、苯丙氨酸(f或phe)、酪氨酸(y或tyr)、色氨酸(w或trp)、赖氨酸(k或lys)、精氨酸(r或arg)、组氨酸(h或his)、天冬氨酸(d或asp)、谷氨酸(e或glu)、天冬酰胺(n或asn)、谷氨酰胺(q或gln)、半胱氨酸(c或cys)、甲硫氨酸(m或met)、丝氨酸(s或ser)和苏氨酸(t或thr)。在残基可以是天冬氨酸或天冬酰胺的情况下,可以使用符号asx或b。在残基可以是谷氨酸或谷氨酰胺的情况下,可以使用符号glx或z。除非上下文另有说明,否则对天冬氨酸的提及包括天冬氨酸盐,且谷氨酸包括谷氨酸盐。
[0120]“保守性”氨基酸取代是其中一个氨基酸残基被另一个具有相似化学结构的氨基酸残基置换的预期对多肽的功能、活性或其它生物学特性几乎没有影响的氨基酸取代。此类保守性取代适当地是以下组中的一个氨基酸被同一组中的另一个氨基酸残基取代的取代:
[0121][0122]
适当地,疏水性氨基酸残基是非极性氨基酸。更适当地,疏水性氨基酸残基选自v、i、l、m、f、w或c。在一些实施方案中,疏水性氨基酸残基选自甘氨酸、丙氨酸、缬氨酸、甲硫氨酸、亮氨酸、异亮氨酸、苯丙氨酸、酪氨酸或色氨酸。
[0123]
如本文所用,多肽序列的编号以及cdr和fr的定义如根据kabat系统所定义(kabat等人,1991,通过引用整体并入本文)。第一多肽序列与第二多肽序列之间的“对应”氨基酸残基是第一序列中与第二序列中的氨基酸残基共享根据kabat系统的相同位置的氨基酸残基,同时第二序列中的氨基酸残基的身份可能与第一序列中的氨基酸残基的身份不同。适当地,如果根据kabat定义,框架和cdr的长度相同,则对应残基将共享相同的数字(和字母)。可以手动或通过使用例如用于序列比对的已知计算机算法,诸如ncbi blast v2.0(blastp或blastn),使用标准设置来实现比对。
[0124]
本文对“表位”的提及是指靶标的被抗体或其片段特异性结合的部分。表位也可称为“抗原决定簇”。当一种抗体与另一种抗体都识别同一的或空间上重叠的表位时,该两种抗体结合“基本上相同的表位”。确定两种抗体是否与同一或重叠表位结合的常用方法是竞争测定法,该竞争测定法可以使用标记的抗原或标记的抗体以多种不同的格式进行配置(例如,使用放射性或酶标记的孔板,或对抗原表达细胞进行流式细胞术)。当一种抗体与另一种抗体都识别同一的表位时(即抗原与抗体之间的所有接触点相同),该两种抗体结合“相同的表位”。例如,当借助表征方法(诸如抗体/抗原交联-联合ms、hdx、x-射线晶体学、冷冻-em或诱变)鉴定抗原指定区域上的所有接触点都相同时,一种抗体可与另一种抗体结合相同表位。
[0125]
进一步地,借助此类表征方法,还可以通过识别一些但不是全部同一的接触点来表征结合基本上相同的表位的抗体。具体地,此类抗体可以在指定抗原区域共享足够数目的同一接触点,以提供广泛等效的技术效果和/或等效的抗原相互作用选择性。另外,在由此抗体识别基本上相同的表位并赋予广泛等效的技术效果和/或相互作用选择性的一些情况下,根据包括最n端的抗原接触点到最c端的抗原接触点的抗原接触的总数来界定表位结合足迹可能会有用。
[0126]
在蛋白质靶标上发现的表位可以被界定为“线性表位”或“构象表位”。线性表位由蛋白质抗原中连续的氨基酸序列形成。构象表位由蛋白质序列中不连续的,但在蛋白质被折叠成其三维结构后聚集在一起的氨基酸形成。
[0127]
如本文所用的术语“载体”意指能够转运已经与之连接的另一核酸的核酸分子。一种类型的载体为“质粒”,其意指额外的dna区段可被连结到其中的环状双链dna环。另一种类型的载体为病毒载体,其中额外的dna区段可以被连结到病毒基因组中。某些载体能够在将其引入其中的宿主细胞中自主复制(例如,具有细菌复制起点的细菌载体和附加型哺乳动物和酵母载体)。其它载体(例如,非附加型哺乳动物载体)可以在被引入到宿主细胞中后整合到宿主细胞的基因组中,从而连同宿主基因组一起被复制。而且,某些载体能够指导与之操作性地连接的基因的表达。此类载体在本文中称为“重组表达载体”(或简称为“表达载体”)。一般而言,在重组dna技术中有实用性的表达载体常常呈质粒形式。在本说明书中,“质粒”和“载体”可互换使用,因为质粒是最常用的载体形式。然而,还包括具有等效功能的其它形式的表达载体,诸如病毒载体(例如,复制缺陷型逆转录病毒、腺病毒和腺相关病毒),并且还包括噬菌体和噬菌粒系统。如本文中所用的术语“重组宿主细胞”(或简称“宿主细胞”)意在指已引入了重组表达载体的细胞。此类术语旨在不仅指特定的受试者细胞,而且指此类细胞的后代,例如,当采用所述后代制备然后任选地被储存、提供、出售、转移或用于制造如本文所述的抗体或其片段的细胞系或细胞库时。
[0128]
对“受试者”、“患者”或“个体”的提及是指待治疗的受试者,尤其是哺乳动物受试者。哺乳动物受试者包括人、非人灵长类动物、农场动物(诸如奶牛)、运动动物或宠物动物(诸如狗、猫、豚鼠、兔子、大鼠或小鼠)。在一些实施方案中,受试者是人患者。在替代性实施方案中,受试者是非人哺乳动物,诸如小鼠。
[0129]
术语“足够量”意指足以产生所需效果的量。术语“治疗有效量”是有效改善疾病或病症的症状的量。治疗有效量可以是“防治有效量”,因为防治可以被认为是治疗。
[0130]
如果疾病或病症的体征或症状的严重程度、受试者经历此类体征或症状的频率,或两者都降低,则该疾病或病症得到“改善”。
[0131]
如本文所用,“治疗疾病或病症”意指降低受试者所经历的该疾病或病症的至少一种体征或症状的频率和/或严重程度。
[0132]
如本文所用,“癌症”是指细胞的异常生长或分裂。一般来说,癌细胞的生长和/或寿命超过正常细胞及其周围的组织的的生长和/或寿命并且与之不协调。癌症可以是良性的、恶化前的或恶性的。癌症发生在多种细胞和组织中。
[0133]“炎症”是指产生发炎的细胞、细胞类型、组织或器官的免疫系统的慢性或急性触发。
[0134]
如本文所用,术语“约”包括比指定的值高至多10%(并包括10%)和低至多10%(并包括10%),适当地比指定的值高至多5%(并包括5%)和低至多5%(并包括5%),特别是指定的值。术语“(在)
……
之间”包括指定边界的值。
[0135]
调节γδt细胞的方法
[0136]
根据本发明的第一方面,提供了一种调节γ可变4链(vγ4)t细胞的离体方法,所述方法包括向包含vγ4 t细胞的细胞群体施用如本文所限定的抗vγ4抗体或其片段。应当理解,“施用”抗体或其片段包括“接触”vγ4 t细胞。
[0137]
vγ4 t细胞的调节可包括:
[0138]-例如通过选择性地增加vγ4 t细胞的数目或促进vγ4 t细胞的存活来扩增vγ4 t细胞;
[0139]-例如通过增加vγ4 t细胞效力(即增加靶细胞杀伤)来刺激vγ4 t细胞;
[0140]-例如通过增加vγ4 t细胞的持久性来防止vγ4 t细胞耗竭;
[0141]-使vγ4 t细胞脱粒;
[0142]-例如通过下调vγ4 tcr细胞表面表达(即通过引起vγ4 tcr内化或降低vγ4 tcr蛋白的表达,或阻断vγ4 tcr结合)来对vγ4 t细胞进行免疫阻抑;
[0143]-例如通过抑制vγ4 t细胞增殖或通过诱导vγ4 t细胞死亡(即杀伤vγ4 t细胞)来减少vγ4 t细胞数目。
[0144]
vγ4 t细胞的此类调节可以包括,例如,vγ4 t细胞激活或vγ4 t细胞抑制。在一个实施方案中,通过施用如本文限定的抗vγ4抗体或其片段来激活vγ4 t细胞。在一个替代实施方案中,通过施用如本文限定的抗vγ4抗体或其片段来抑制vγ4 t细胞。在一个替代实施方案中,在施用如本文限定的抗vγ4抗体或其片段后,vγ4 t细胞未受到抑制。
[0145]
在一个实施方案中,vγ4 t细胞的调节包括将抗tcr γ4可变抗体或其片段施用于培养物中(即体外或离体)的vγ4 t细胞。vγ4 t细胞可以存在于混合细胞群体中,例如存在于包含其它淋巴细胞细胞类型(例如αβt细胞或nk细胞)的细胞群体中。
[0146]
在一个实施方案中,在施用抗vγ4抗体或其片段之前分离包含vγ4 t细胞的细胞群体(即从如本文所述的样品中分离)。在进一步的实施方案中,在施用抗vγ4抗体或其片段之前,使该细胞群体富集t细胞。在再进一步的实施方案中,在施用抗vγ4抗体或其片段之前,使该细胞群体富集γδt细胞。
[0147]
该方法也可以对包含经纯化的γδt细胞级分的细胞群体执行。在此类实施方案中,在施用抗vγ4抗体或其片段之前,使细胞群体耗尽样品中存在的除γδt细胞以外的细胞类型,诸如αβt细胞和/或nk细胞。可另外或可替代地在施用抗vγ4抗体或其片段之前使该细胞群体富集可含有vγ4的细胞类型,诸如t细胞和/或γδ细胞。例如,在培养样品之前,可使样品富集t细胞,或富集γδt细胞,或耗尽αβt细胞或耗尽非γδt细胞。在一个实施方案中,首先使该样品耗尽αβt细胞,然后使该样品富集cd3+细胞。富集或耗尽可以使用本领域已知的技术来实现,诸如使用涂有结合至细胞表面上与待富集/耗尽的表型相关的分子的抗体的磁珠来实现。
[0148]
细胞培养物中除淋巴细胞以外的细胞类型的存在可能会抑制vγ4细胞扩增。此类
细胞,例如基质细胞、上皮细胞、肿瘤细胞和/或饲养细胞可在培养前被去除。因此,在一个实施方案中,细胞群体在培养期间不与基质细胞直接接触。基质细胞的实例包括成纤维细胞、周细胞、间充质细胞、角化细胞、内皮细胞和非血液肿瘤细胞。优选地,淋巴细胞在培养期间不与成纤维细胞直接接触。在一个实施方案中,细胞群体在培养期间不与上皮细胞直接接触。在一个实施方案中,细胞群体在培养期间不与肿瘤细胞和/或饲养细胞直接接触。
[0149]
在一个实施方案中,该方法包括在不存在实质性的基质细胞接触的情况下培养vγ4 t细胞。在再一个实施方案中,该方法包括在不存在实质性的成纤维细胞接触的情况下培养vγ4 t细胞。
[0150]
在一个实施方案中,该方法包括在实质上不含血清的培养基(例如无血清培养基或含有血清替代物(sr)的培养基)中培养vγ4 t细胞。因此,在一个实施方案中,该方法包括在无血清培养基中培养。此类无血清培养基还可以包括血清替代物培养基,其中血清替代物是基于化学确定的组分从而避免使用人或动物来源的血清。在一个替代实施方案中,该方法包括在含有血清(例如人ab血清或胎牛血清(fbs))的培养基中培养。在一个实施方案中,该培养基含有血清替代物。在一个实施方案中,该培养基不含动物来源的产品。
[0151]
应当理解,在无血清培养基中培养的样品具有避免过滤、沉淀、污染和血清供给问题的优点。此外,动物来源的产品不适合用于临床级人类治疗剂的制造。
[0152]
在一个实施方案中,抗vγ4抗体或其片段呈可溶形式或固定化形式。例如,抗体或其片段可以以可溶形式施用于vγ4 t细胞。可替代地,当抗体或其片段结合或共价连接至表面,诸如珠粒或板(即,呈固定化形式)时,可将该抗体或其片段施用于vγ4 t细胞。在一个实施方案中,抗体被固定在表面,诸如fc包被的孔上。可替代地,抗体或其片段结合至细胞表面(例如,固定在抗原呈递细胞(apc)的表面上)。在另一个实施方案中,当细胞群体与抗体接触时,该抗体未被固定在表面上。
[0153]
与抗vγ4抗体或其片段接触的细胞群体可以从多种样品类型获得(分离方法在下文进一步描述)。在一个实施方案中,样品是非造血组织样品。本文对“非造血组织”或“非造血组织样品”的提及包括皮肤(例如人皮肤)和肠道(例如人肠道)。非造血组织是除血液、骨髓、淋巴样组织、淋巴结组织或胸腺组织以外的组织。在一个实施方案中,非造血组织样品是皮肤(例如人皮肤)。在一些实施方案中,细胞群体(例如,γδt细胞)不是从特定类型的生物流体样品(诸如血液或滑液)获得的。在一些实施方案中,细胞群体(例如γδt细胞)是从皮肤(例如人皮肤)获得的,该皮肤可以通过本领域已知的方法获得。例如,可以通过在被构造为利于细胞从非造血组织样品中排出的合成支架上培养非造血组织样品而从非造血组织样品中获得细胞群体。可替代地,所述方法可以应用于从胃肠道(例如结肠或肠道)、乳腺、肺、前列腺、肝脏、脾脏、胰腺、子宫、阴道和其它皮肤、黏膜或浆膜获得的细胞群体(例如γδt细胞)。
[0154]
在一个替代实施方案中,样品是造血样品或其级分(即,细胞群体是从造血样品或其级分获得的)。本文对“造血样品”或“造血组织样品”的提及包括血液(诸如外周血或脐带血)、骨髓、淋巴样组织、淋巴结组织、胸腺组织,以及它们的级分或经富集部分。该样品优选是血液,该血液包括外周血或脐带血或其级分,包括血沉棕黄层细胞、白细胞分离产物、外周血单核细胞(pbmc)和低密度单核细胞(ldmc)。在一些实施方案中,该样品是人血或其级分。可以使用本领域已知的技术诸如密度梯度离心从血液样品中获得细胞。例如,可以将全
血分层到等体积的ficoll-hypaque上,接着在室温下以400xg离心15-30分钟。界面材料将含有低密度单核细胞,可将低密度单核细胞收集并在培养基中洗涤,并在室温下以200xg离心10分钟。
[0155]
细胞群体可以从癌组织样品(即,γδt细胞也可以驻留于癌组织样品中),例如肠道、乳腺或前列腺肿瘤中获得。在一些实施方案中,细胞群体可以来自人癌组织样品(例如,实体瘤组织)。在其它实施方案中,细胞群体可以来自除人癌组织以外的样品(例如,没有大量肿瘤细胞的组织)。例如,细胞群体可以来自与附近或相邻癌组织分开的皮肤区域(例如健康皮肤)。因此,在一些实施方案中,细胞群体不是从癌组织(例如人癌组织)中获得的。
[0156]
细胞群体可以从人或非人动物组织获得。因此,该方法可以另外包括从人或非人动物组织获得细胞群体的步骤。在一个实施方案中,样品已经从人中获得。在一个替代实施方案中,样品已经从非人动物受试者中获得。
[0157]
γδt细胞的扩增
[0158]
在一个实施方案中,调节包括vγ4 t细胞的活化,特别是vγ4 t细胞的扩增。因此,根据本发明的一个方面,提供了一种扩增vγ4 t细胞的离体方法,所述方法包括向包含vγ4 t细胞的细胞群体施用如本文所限定的抗vγ4抗体或其片段。vγ4 t细胞的此种扩增可以通过选择性增加vγ4 t细胞的数目和/或通过促进vγ4 t细胞的存活来实现。在一个实施方案中,vγ4 t细胞的扩增包括将抗tcrγ4可变抗体或其片段施用于培养物中(即体外或离体)的vγ4 t细胞。vγ4 t细胞可以存在于混合细胞群体中,例如存在于包含其它淋巴细胞细胞类型(例如αβt细胞或nk细胞)的细胞群体中。
[0159]
因此本发明提供了用于产生经富集γδt细胞(例如vγ4 t细胞)群体的离体方法。经富集的群体可以从经分离的混合细胞群体产生(例如,从取自患者/供体的样品获得),这通过包括使混合细胞群体或其经纯化级分与抗体或其片段接触的方法来实现。所述抗体(或其片段)通过结合至对γδtcr的vγ4链具有特异性的表位来选择性地扩增vγ4 t细胞。
[0160]
还提供了根据如本文所限定的方法获得的扩增的vγ4 t细胞群体。根据本发明的这个方面,应当理解,此类扩增的vγ4 t细胞群体可以是在体外或离体获得和/或扩增的。在一个方面,提供了根据如本文所限定的方法获得的扩增的vγ4群体,其中将vγ4群体分离并且在体外或离体扩增。
[0161]
如本文所述的抗体或其片段可被用于扩增γδt细胞(例如vγ4 t细胞)的方法。这些方法可以在体外进行。如果该扩增方法在体外进行,则可以将抗体(或其片段)施加于如上所述的那样获得的经分离的γδt细胞(例如vγ4 t细胞)。在一些实施方案中,γδt细胞是从已经从非造血组织样品中分离的细胞群体扩增的。在一个替代实施方案中,γδt细胞是从已经从造血组织样品诸如血液样品中分离的细胞群体扩增的。
[0162]
γδt细胞(例如vγ4 t细胞)的扩增可以包括在如本文所述的抗体或其片段和细胞因子的存在下培养样品。细胞因子可包括白细胞介素、淋巴因子、干扰素、集落刺激因子和趋化因子。在一个实施方案中,细胞因子选自由以下组成的组:白细胞介素-2(il-2)、白细胞介素-4(il-4)、白细胞介素-6(il-6)、白细胞介素-7(il-7)、白细胞介素-8(il-8)、白细胞介素-9(il-9)、白细胞介素-12(il-12)、白细胞介素-18(il-18)、白细胞介素-21(il-21)、白细胞介素-33(il-33)、胰岛素样生长因子1(igf-1)、白细胞介素-1β(il-1β)、干扰素-γ(ifn-γ)和基质细胞衍生因子-1(sdf-1)。应当理解,对如本文所述的细胞因子的提
及可以包括与所述细胞因子具有相同的活性(就促进对培养物中的vγ4 t细胞的类似生理作用的能力而言)的任何化合物,并且包括但不限于其模拟物或任何功能等效物。
[0163]
在一个实施方案中,所述细胞因子是细胞因子的常见细胞因子受体γ链(γc)家族。在进一步的实施方案中,γc-细胞因子选自:il-2、il4、il-7、il-9、il-12、il-15、il-21或它们的混合物。
[0164]
使用的细胞因子(例如白细胞介素)可以是人或动物来源的,优选是人来源的。它可以是野生型蛋白质或任何生物活性片段或变体,也就是说,能够与其受体结合。此类结合可以在根据本发明的方法的条件下诱导γδt细胞的活化。更优选地,该细胞因子可以是可溶形式,与另一种分子,诸如肽、多肽或生物活性蛋白融合或复合。优选地,使用人重组细胞因子。更优选地,白细胞介素浓度的范围可以在1-10000u/ml之间变化,甚至更优选地在100-1000u/ml之间变化。
[0165]
在进一步的实施方案中,细胞因子是趋化因子。应进一步理解,趋化因子将根据用于获得γδt细胞的样品而变化和选择。
[0166]
在一个实施方案中,该方法包括在il-2、il-9和/或il-15的存在下培养细胞群体。在进一步的实施方案中,该方法包括在il-2的存在下培养细胞群体。在进一步的实施方案中,该方法包括在il-2和/或il-15(即il2、il-15或它们的组合)的存在下培养细胞群体。在一个替代实施方案中,该方法包括在il-9和/或il-15(即il9、il-15或它们的组合)的存在下培养细胞群体。在一个实施方案中,该方法包括在il-2、il-9和/或il-15和附加生长因子(例如il-21)的存在下的细胞群体。在其它实施方案中,该方法包括在没有除il-2和/或il-15以外的生长因子的培养基中培养细胞群体。在替代实施方案中,该方法包括在没有除il-9和/或il-15以外的生长因子的培养基中培养细胞群体。在进一步的实施方案中,该方法包括在由补充有il-2、il-9和/或il-15的基础培养基组成的培养基中培养细胞群体。在进一步的实施方案中,该方法包括在由补充有il-2和/或il-15的基础培养基组成的培养基中培养细胞群体。
[0167]
在一个实施方案中,该方法包括在il-15和选自由il-2、il-4、il-21、il-6、il-7、il-8、il-9、il-12、il-18、il-33、igf-1、il-1β、ifn-γ、人血小板裂解物(hpl)和基质细胞衍生因子-1(sdf-1)组成的组的因子的存在下培养细胞群体。
[0168]
γδt细胞的扩增可以包括在至少一种进一步的t细胞有丝分裂原的存在下培养样品。术语“t细胞有丝分裂原”(也可称为“γδtcr激动剂”)意指任何可通过tcr信号传导刺激t细胞的剂,包括但不限于植物凝集素,诸如植物血凝素(pha)和伴刀豆球蛋白a(cona)和非植物来源的凝集素。在一个实施方案中,t细胞有丝分裂原是抗cd3单克隆抗体(mab)。其它有丝分裂原包括佛波醇12-肉豆蔻酸酯-13-乙酸酯(tpa)及其相关化合物,诸如瑞香素(mezerein),或细菌化合物(例如葡萄球菌肠毒素a(sea)和链球菌蛋白a)。t细胞有丝分裂原可以是可溶的或固定的,并且在扩增方法中可以使用超过一种t细胞有丝分裂原。
[0169]
如本文所用,对“扩增的”或“扩增的γδt细胞群体”的提及包括比未扩增的群体更大或含有更多数目的细胞的细胞群体。此类群体可以在数目上多、在数目上小,或者是其中群体内的一定比例或特定细胞类型扩增混合的群体。应当理解,术语“扩增方法”是指引起扩展或扩增的群体的过程。因此,与尚未进行扩增步骤或在任何扩增步骤之前的群体相比,扩增或扩增的群体在数目上可能更大或含有更大数目的细胞。应进一步理解,本文中指示
1640。在一个替代实施方案中,aim-v培养基可以补充有cts免疫血清替代物和两性霉素b。在某些实施方案中,该培养基可以进一步补充有如本文所述的il-2、il-4、il-9和/或il 15。方便地,在分离和/或扩增期间将细胞在37℃下在含有5%co2的加湿气氛中在合适的培养基中培养。
[0177]
也可以采用在γδt细胞的扩增培养物中添加其它因子。在一个实施方案中,此类因子被用于选择性地促进γδt细胞扩增的扩增中。例如,扩增可以另外包括向扩增培养物中添加外源细胞因子,诸如白细胞介素。此类扩增可以包括在il-2和il-15的存在下培养γδt细胞。可替代地,扩增可以包括在il-9和il-15的存在下培养γδt细胞。应当理解,任何扩增步骤都被执行对于产生扩增的γδt细胞群体有效的持续时间。
[0178]
扩增γδt细胞的方法可以包括小于5天(例如小于4.5天、小于4.0天、小于3.9天、小于3.8天、小于3.7天、小于3.6天、小于3.5天、小于3.4天、小于3.3天、小于3.2天、小于3.1天、小于3.0天、小于2.9天、小于2.8天、小于2.7天、小于2.6天、小于2.5天、小于2.4天、小于2.3天、小于2.2天、小于2.1天、小于2.0天、小于46小时、小于42小时、小于38小时、小于35小时、小于32小时)的群体倍增时间。
[0179]
分离γδt细胞的方法
[0180]
如本文所述,可将抗体(或其片段)施加到培养物中的γδt细胞,即已从样品中获得的γδt细胞。在一个实施方案中,在施用抗vγ4抗体或其片段之前从样品中分离细胞群体。因此,提供了调节(尤其是扩增)vγ4t细胞的方法,该方法包括将如本文所限定的抗vγ4抗体或其片段施用于从样品分离的γδt细胞群体(例如,包含vγ4t细胞的细胞群体)。
[0181]
本文对细胞(尤其是γδt细胞)的“分离”或“分离”细胞(尤其是γδt细胞)的提及是指从组织或细胞库中移出、分开、纯化、富集或以其它方式取出细胞的方法或过程。应当理解,此类提及包括术语“分开的”、“移出的”、“纯化的”、“富集的”等。γδt细胞的分离包括将细胞从完好的非造血组织样品或从非造血组织的基质细胞(例如,成纤维细胞或上皮细胞)中分离或分开。此种分离可替代地或另外包括将γδt细胞与其它造血细胞(例如αβt细胞或其它淋巴细胞)分离或分开。分离可以持续限定的时间段,例如从将组织外植体或活检物置于分离培养物中的时间开始到诸如通过离心或其它用于将分离的细胞群体转移到扩增培养物中或用于其它目的的手段从培养物中收集细胞,或从培养物中移出原组织外植体或活检物时结束。分离步骤可以持续至少约3天至约45天。在一个实施方案中,分离步骤持续至少约10天到至少28天。在进一步的实施方案中,分离步骤持续至少14天到至少21天。因此分离步骤可以持续至少3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天、15天、16天、17天、18天、19天、20天、21天、22天、23天、24天、25天、26天、27天、28天、29天、30天、31天、32天、约35天、约40天或约45天。可以理解的是,尽管细胞增殖在这个分离步骤中可能不是实质性的,但不一定不存在。实际上,对于本领域技术人员而言,已认识到分离的细胞也可以开始分裂以在含有样品的分离容器内生成多个此类细胞。
[0182]
因此,本文对“经分离的γδ t细胞”、“经分离的γδ t细胞群体”或“γδt细胞的经分离群体”应被理解为是指这样的γδ细胞,该γδ细胞已从样品(诸如来源非造血组织样品)中分离、分开、移出、纯化或富集,从而使得该细胞与完好(非造血组织)样品内所含的细胞没有实质性的接触。本文对“经分离的vγ4 t细胞”、“经分离的vγ4 t细胞群体”、“vγ4 t细胞的经分离群体”、“经分开的vγ4 t细胞”、“经分开的vγ4 t细胞群体”或“vγ4 t细胞
的经分开群体”的提及应被理解为这样的vγ4 t细胞,该vγ4 t细胞是指已从样品(诸如来源非造血组织样品)中分离、分开、移出、纯化或富集,从而使得该细胞与完好(非造血组织)样品内所含的细胞没有实质性的接触。
[0183]
可以收获非造血组织驻留淋巴细胞并且例如通过稳固的移液将该非造血组织驻留淋巴细胞与基质细胞(诸如真皮成纤维细胞)分开。可将淋巴细胞收获物进一步通过40μm尼龙网进行洗涤,以便截留在该过程中可能已经变得松散的成纤维细胞聚集体。淋巴细胞也可以使用例如cd45抗体利用荧光或磁相关细胞分选来分离。
[0184]
γδt细胞的分离可以包括在至少一种细胞因子的存在下培养样品。例如,该方法可以包括在至少一种剂(诸如趋化因子)的存在下培养样品。应进一步理解,将根据正在分离的γδt细胞来选择趋化因子。此外,趋化因子将根据用于分离γδt细胞的样品而变化和选择。
[0185]
γδt细胞的分离可以包括在至少一种细胞因子的存在下进一步培养样品。所述细胞因子可以不同于初始培养中使用的细胞因子。
[0186]
分离方法可以包括培养样品。本文对“培养”的提及包括将样品(包括从样品中分离、分开、移出、纯化或富集的细胞)添加到包含细胞和/或样品所需和/或偏好的生长因子和/或必需营养素的培养基中。应当理解,此类培养条件可以根据要从样品中分离的细胞或细胞群体进行调适,或者可以根据要从样品中分离和扩增的细胞或细胞群体进行调适。
[0187]
在某些实施方案中,样品的培养持续了足以从样品中分离γδt细胞的持续时间。在某些实施方案中,培养持续时间为至少14天。在某些实施方案中,培养持续时间小于45天,诸如小于30天,诸如小于25天。在进一步的实施方案中,培养持续时间在14天至35天之间,诸如在14天至21天之间。在再进一步的实施方案中,培养持续时间为约21天。
[0188]
在特定实施方案中,在培养样品后从培养物中收集γδt。γδt细胞的收集可以包括从培养物中物理收集γδt细胞,从其它淋巴细胞(例如αβt细胞和/或nk细胞)中分离γδt细胞或者将γδt细胞与样品中存在的其它细胞(例如基质细胞,诸如成纤维细胞)分离和/或分开。在一个实施方案中,γδt细胞通过机械手段(例如移液)来收集。在进一步的实施方案中,γδt细胞通过磁力分开(magnetic separation)和/或标记来收集。在再进一步的实施方案中,γδt细胞通过流式细胞技术诸如facs来收集。因此,在某些实施方案中,γδt细胞通过特异性标记γδt细胞的手段来收集。应当理解,此类γδt细胞的收集可以包括从样品的培养物中物理去除、转移到单独的培养容器或转移到单独的或不同的培养条件。
[0189]
应当理解,γδt细胞的此种收集是在足以从样品中获得分离的γδt细胞群体的持续时间之后执行的。在某些实施方案中,在培养样品至少一周、至少10天、至少11天、至少12天、至少13天或至少14天后收集γδt细胞。适当地,在40天或更短时间,诸如38天或更短时间、36天或更短时间、34天或更短时间、32天或更短时间、30天或更短时间、28天或更短时间、26天或更短时间或24天或更短时间后收集γδt细胞。在一个实施方案中,在培养样品至少14天后收集γδt细胞。在进一步的实施方案中,在培养样品14至21天后收集γδt细胞。
[0190]
在一个实施方案中,在实质上不含血清的培养基(例如无血清培养基或含有血清替代物(sr)的培养基)中培养所述样品。因此,在一个实施方案中,在无血清培养基中培养样品。此类无血清培养基还可以包括血清替代物培养基,其中血清替代物是基于化学确定的组分从而避免使用人或动物来源的血清。在一个实施方案中,该培养基不含动物来源的
产品。在一个替代实施方案中,在含有血清(例如人ab血清或胎牛血清(fbs))的培养基中培养样品。
[0191]
培养基可以另外包括可以帮助γδt细胞生长和扩增的其它成分。可被添加的其它成分的实例包括但不限于血浆或血清、经纯化的蛋白质(诸如白蛋白)、脂质来源(诸如低密度脂蛋白(ldl))、维生素、氨基酸、类固醇和任何其它支持或促进细胞生长和/或存活的补充物。
[0192]
抗体或其片段
[0193]
本文提供了一种抗体或其片段,该抗体或其片段与γδt细胞受体(tcr)的可变γ4(vγ4)链特异性地结合。具体而言,该抗体或其片段不与γδtcr的可变γ2(vγ2)链结合(或交叉反应)。应当理解,这是参考来自同一物种的vγ4链和vγ2。优选地,该物种是智人(人)并且因此该抗体或其片段可以与γδt细胞受体(tcr)的人γ可变4(vγ4)链特异性地结合而不与γδtcr的人γ可变2(vγ2)链特异性地结合。例如,人vγ4链可以具有根据seq id no.1的氨基酸1-99的序列并且/或者人vγ2链可以具有根据seq id no.335的序列。在其它物种中,该抗体或其片段与γδt细胞受体(tcr)的人γ可变4(vγ4)链的物种特异性直系同源物特异性地结合,而不与γδtcr的人γ可变2(vγ2)链的物种特异性直系同源物特异性地结合。因此,该抗体或其片段可以与具有对应于seq id no.1的氨基酸1-99的序列的γδt细胞受体(tcr)的人γ可变4(vγ4)链或其非人直系同源物特异性地结合,而不与具有对应于seq id no.335的序列的γδtcr的人γ可变2(vγ2)链或其非人直系同源物特异性地结合。这种背景下的直系同源物可以意指与参考序列具有最高序列相似性的γ链序列,或者优选具有相同功能(例如与体内直系同源配体具有相互作用)的γ链序列。例如,在小鼠中,依据heilig和tonegave命名法指定为vγ7的蛋白质与人vγ4在功能上最密切相关(barros等人(2016)cell,167:203-218.e17)。
[0194]
这种开发是意义深远的。在人中,例如,vγ4和vγ2链共享91%的序列同一性(它们仅相差9个氨基酸)。因此,这使得难以获得与(人)vγ4结合而不与(人)vγ2结合的抗体并且在本领域中预计不可能产生此类抗体。
[0195]
当提及与γδtcr的vγ4链特异性地结合的抗体或其片段时,这通常意指该抗体或其片段与vγ4链的结合相对于阴性对照抗体和/或阴性对照抗原在统计学上显著增加(例如如在elisa测定、任选delfia elisa测定或spr中经由结合测量的)。关于阴性对照抗体和/或阴性对照抗原所检测到的水平可以被认为是所用测定的背景水平,代表测定系统中的“噪声”,如本领域技术人员所熟知的。在特定实施方案中,高于相对于背景水平的预定阈值的信号水平可以被认为代表结合检测量(例如,高于背景水平的约1倍、2倍、3倍、4倍、5倍或更高)。例如,在delfia elisa测定中,是背景水平5倍或更高的信号水平可以被认为指示抗体与抗原的结合。技术人员能够很好地基于所使用的测定系统确定合适的阈值。相反,当提及不与γδtcr的vγ2链结合(或交叉反应)的抗体或其片段时,这通常意指该抗体或其片段与vγ2链的结合相对于阴性对照抗体和/或阴性对照抗原在统计学上没有显著增加(例如如在elisa测定、任选delfiaelisa测定或spr中经由结合测量的)。例如,这在图2a中进行了证明并且在实施例4中进行了讨论。根据本文公开的本发明的所有方面和实施方案,该特性也可以表示为所述抗体或其片段与vγ4链之间的检测到的结合水平(例如,如在elisa测定、任选delfia elisa测定或spr中经由结合测量的)与所述抗体或其片段与vγ2链之间的
检测到的结合水平相比的倍数变化差异。例如,所述抗体或其片段可以显示出与其与vγ2链的结合相比增加了至少约50倍、60倍、70倍、80倍、90倍、100倍、150倍、200倍、300倍、400倍、500倍、600倍、700倍、800倍、900倍、1000倍、2000倍、3000倍、4000倍、5000倍、6000倍、7000倍、8000倍、9000倍、10000倍、15000倍、25000倍、50000倍、75000倍、95000倍或更高倍数的与vγ4链的结合。例如,这在图2b中进行了证明并且在实施例4中进行了讨论。然而,这些倍数增加被视为是保守性的,因为在计算它们时假设所有高于对照的vγ2信号都不是背景噪声。然而,如先前所讨论的,技术人员可以替代地将此类delfia elisa测定中高于背景的低信号作为测定噪声(例如背景水平的约1倍、2倍、3倍、4倍、5倍或更多)排除,因此将低于这些阈值的信号视为非特异性背景结合。
[0196]
在一个实施方案中,所述抗体或其片段是scfv、fab、fab
′
、f(ab
′
)2、fv、可变结构域(例如vh或vl)、双抗体、微型抗体或单克隆抗体。在一个特定实施方案中,所述抗体或其片段是scfv。在另一个特定实施方案中,所述抗体是单克隆抗体。
[0197]
本文所述的抗体可以属于任何类别,例如igg、iga、igm、ige、igd或其同种型,并且可以包含κ或λ轻链。在一个实施方案中,所述抗体是igg抗体,例如同种型igg1、igg2、igg3或igg4中的至少一种。在一个实施方案中,所述抗体是igg1。在进一步的实施方案中,所述抗体可以是已经被修饰成赋予所需特性(诸如fc被突变成降低效应子功能、延长半衰期、改变adcc或提高铰链稳定性)的格式,诸如igg格式。此类修饰是本领域中熟知的并且本文描述了示例性实施方案。例如,抗体或其片段可以包含igg1恒定结构域,该igg1恒定结构域包含根据seq id no:332或333的氨基酸序列。
[0198]
在一个实施方案中,该抗体或其片段是人的。因此,所述抗体或其片段可以源自人免疫球蛋白(ig)序列。所述抗体(或其片段)的cdr、框架和/或恒定区可以源自人ig序列,尤其是人igg序列。所述cdr、框架和/或恒定区对于人ig序列,尤其人igg序列而言是实质上同一的。使用人抗体的优点在于它们在人类中具有低免疫原性或没有免疫原性。
[0199]
所述抗体或其片段也可以是嵌合的,例如小鼠-人抗体嵌合体。
[0200]
可替代地,所述抗体或其片段源自非人物种,诸如小鼠。此类非人抗体可以被修饰以增加它们与在人中天然产生的抗体变体的相似性,因此所述抗体或其片段可以部分或完全人源化。因此,在一个实施方案中,所述抗体或其片段是人源化的。
[0201]
靶向表位的抗体
[0202]
本文提供了与γδtcr的vγ4链的表位结合的抗体(或其片段)。vγ4链上表位的结合可以任选地对γδtcr活性产生诸如激活或抑制的影响。该抗体(或其片段)可通过阻止另一抗体或分子的结合或相互作用而具有阻断作用。该抗体对γδtcr的vγ4链具有特异性,并且不结合其它抗原的表位,诸如如本文限定的γδtcr的vγ2链或γδtcr的vγ8链。
[0203]
在一个实施方案中,该表位可以是γδt细胞的激活性表位。“激活性”表位可以包括,例如,tcr相关功能的调节,诸如tcr下调、细胞脱粒、细胞毒性、增殖、动员、存活或对衰竭的抵抗力的增加、细胞内信号传导、细胞因子或生长因子分泌、表型变化或基因表达的变化。例如,激活性表位的结合可以刺激γδt细胞群体,优选vγ4+t细胞群体的扩增(即增殖)。因此,这些抗体可用于调节γδt细胞激活,从而调节免疫反应。因此,在一个实施方案中,激活性表位的结合使γδtcr下调。在额外的或可替代的实施方案中,激活性表位的结合激活γδt细胞的脱粒。在进一步的另外的或可替代的实施方案中,激活性表位的结合激活
γδt细胞以杀伤靶细胞(例如癌细胞)。
[0204]
在一个实施方案中,该抗体或其片段阻断vγ4并阻止tcr结合(例如通过空间位阻)。通过阻断vγ4,该抗体可以阻止tcr激活和/或信号传导。因此该表位可以是γδt细胞的抑制性表位。“抑制性”表位可以包括例如阻断tcr功能,从而抑制tcr激活。
[0205]
该表位优选由γδtcr的vγ4链的至少一个胞外、可溶性、亲水性、外部或胞质部分组成。
[0206]
在特定实施方案中,该表位不包括在γδtcr的vγ4链的非种系编码区,尤其是vγ4链的cdr3中发现的表位。在一个优选实施方案中,该表位处于γδtcr的vγ4链的框架区内,该框架区可以是框架区3的高变4区。应当理解,此类结合允许vγ4链的独特识别,一般不受在vγ4链之间高度可变的tcr序列(尤其是cdr3)的限制。因此,应当理解,任何包含vγ4链的γδtcr都可以使用如本文所限定的抗体或其片段来识别,而不管γδtcr的特异性如何。
[0207]
γδ受体独立地经由空间上不同的结构域来结合多种调节配体是可能的。与此类多模式配体结合一致,melandri等人(2018)nat.immunol.19:1352-1365最近的研究显示,人tcr与内源性btnl3配体的结合是经由位于γ4链上cdr3的n端的离散结构域进行的。作者强调,因为btnl3结合是经由tcr的这个特定种系区介导的,所以离c端越近,体细胞重组的cdr3环仍然可以独立地自由结合其它配体。此外,框架区3(fr3)的这个亚区(也可称为“高变区4”(hv4))与人γ2链相差四个氨基酸。然而,melandri等人没有公开特定的抗vγ4抗体,也没有建议如何得到此类抗体。事实上,普遍的观点是,这是不可能的,因为人vγ4与vγ2链之间共享显著的序列同源性(91%的序列同一性)。
[0208]
结合在hv4区内的抗体可以允许γ4链的cdr3区仍然结合,另外的优点是提供对γ4比对γ2特异性更高的结合物。此外,由于hv4是种系编码的,一些靶向该区域的抗体可识别所有vγ4链,而识别vγ4的其它抗体可对某些vγ4链具有特异性。
[0209]
本公开现在提供了可以与vγ4链的hv4区特异性地结合的抗体及其片段。因此,在一个实施方案中,所述抗体或其片段与vγ4链的hv4区的表位结合。hv4区包含seq id no:1的氨基酸67-82。因此,在一个实施方案中,该表位包含在seq id no:1的氨基酸区67-82内的一个或多个氨基酸残基,例如不是cdr1、cdr2和/或cdr3序列的一部分的vγ4链部分。这样做时,所述抗体或其片段可以调节vγ4+tcr与btnl3/8之间的相互作用。在一个实施方案中,该表位不包含在seq id no:1的氨基酸区域96-106(cdr3)内的氨基酸残基。在一个实施方案中,该表位不包含在seq id no:1的氨基酸区域50-57(cdr2)内的氨基酸残基。在一个实施方案中,该表位不包含在seq id no:1的氨基酸区域27-32(cdr1)内的氨基酸残基。
[0210]
在特定实施方案中,该抗体或其片段可在与seq id no:1的氨基酸67至82中的一个或多个结合后激活vγ4+tcr。
[0211]
以与充分表征的αβt细胞类似的方式,γδt细胞利用一组不同的体细胞重排变量(v)、多样性(d)(仅对于β和δ)、联接(j)和恒定(c)基因,但是γδt细胞含有比αβt细胞更少的v、d和j区段。在一个实施方案中,由抗体(或其片段)结合的表位不包含在vγ4链的j区中发现的表位。因此该抗体或片段可以仅结合在vγ4链的v区中。因此,在一个实施方案中,该表位由γδtcr的v区中的表位(例如seq id no:1的氨基酸残基1-99)组成。
[0212]
对该表位的提及是针对luoma等人(2013)immunity 39:1032-1042,和rcsb蛋白质
数据库条目:4mnh中描述的vγ4序列作出的,该vγ4序列示为seq id no:1:
[0213][0214][0215]
seq id no:1表示包含v区(也称为可变结构域)和j区的可溶性tcr。v区包含氨基酸残基1-99,j区包含氨基酸残基102-116并且来自tcrβ的恒定区包含氨基酸残基117-256。在v区内,cdr1定义为seq id no:1的氨基酸残基27至32,cdr2定义为seq id no:1的氨基酸残基50至57,且cdr3定义为seq id no:1的氨基酸残基96至106。
[0216]
发明人已经鉴定,seq id no:1的氨基酸k76(即位置76处的赖氨酸)和m80(即位置80处的甲硫氨酸)可能对于与(人)vγ4链的hv4区的结合特别重要(实施例6)。因此,该表位可以包含seq id no:1的k76和/或m80或者由该k76和/或m80组成。
[0217]
发明人已经进一步鉴定,seq id no:1的氨基酸区域71-79内的氨基酸可能对于与(人)vγ4链的hv4区的结合特别重要。因此,在进一步的实施方案中,该表位包含在seq id no:1的氨基酸区域71-79内的一个或多个氨基酸残基。
[0218]
在一个实施方案中,该表位包含在所述区域内的一个或多个,诸如两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个氨基酸残基。
[0219]
在一个实施方案中,该表位包含在seq id no:1的氨基酸区域67-82内的一个或多个(诸如5个或更多,诸如10个或更多)氨基酸残基。在进一步的实施方案中,该表位包含在seq id no:1的氨基酸区域71-79内的一个或多个(诸如3个或更多个,诸如5个或更多个)氨基酸残基。
[0220]
将进一步理解,所述抗体(或其片段)不需要与限定范围内的所有氨基酸结合。此类表位可以称为线性表位。例如,与包含位于seq id no:1的氨基酸区域67-82内的氨基酸残基的表位结合的抗体可以仅与所述范围内的一个或多个氨基酸残基(例如位于该范围的每个末端处的氨基酸残基(即氨基酸67和82),任选地包括位于该范围内的氨基酸(即氨基酸71、73、75、76和79))结合。
[0221]
例如,发明人已经发现seq id no:1的氨基酸残基71、73、75、76和79可以形成抗vγ4抗体或其片段结合的表位(实施例8)。因此,在一个实施方案中,该表位包含seq id no:1的氨基酸残基71、73、75、76和79中的至少一个。在更多的实施方案中,该表位包含一个、两个、三个、四个或五个(尤其是四个或五个)选自seq id no:1的氨基酸残基71、73、75、76和79的氨基酸。
[0222]
在进一步的实施方案中,该表位由位于seq id no:1的氨基酸区域:67-82内的一个或多个氨基酸残基组成。在进一步的实施方案中,该表位由位于seq id no:1的氨基酸区域:71-79内的一个或多个氨基酸残基组成。
[0223]
在进一步的实施方案中,该表位包含seq id no:1的氨基酸残基:71-79,或适当地
由seq id no:1的氨基酸残基:71-79组成。在再进一步的实施方案中,该表位包含seq id no:1的氨基酸残基:71、73、75、76和79,或适当地由seq id no:1的氨基酸残基:71、73、75、76和79组成。
[0224]
本领域已知用于确定抗体所结合的表位的各种技术。示例性技术包括例如常规交叉阻断测定、丙氨酸扫描突变分析、肽印迹分析、肽切割分析晶体学研究和nmr分析。另外,还可以采用诸如表位切除、表位提取和抗原化学修饰的方法。另一种可用于鉴定多肽内与抗体相互作用的氨基酸的方法是通过质谱法检测的氢/氘交换(如实施例8中所述)。一般而言,氢/氘交换法涉及用氘标记目标蛋白质,然后使抗体与氘标记的蛋白质结合。接下来,将蛋白质/抗体复合物转移到水中,并且使受抗体复合物保护的氨基酸内的可交换质子以比不属于界面的一部分的氨基酸内的可交换质子更慢的速率经历氘到氢的反向交换。因此,形成蛋白质/抗体界面的一部分的氨基酸可以保留氘,因此与未包括在界面中的氨基酸相比,表现出相对较高的质量。抗体解离后,使靶蛋白经受蛋白酶切割和质谱分析,从而揭示与抗体相互作用的特定氨基酸相对应的氘标记残基。
[0225]
另外,或作为替代,可以使用抗原嵌合和诱变研究鉴定多肽内与抗体相互作用的氨基酸(如实施例6中所述)。一般地说,该方法涉及产生一系列的一种或多种嵌合抗原,其中第一参考抗原的氨基酸序列可以基于第二参考抗原的氨基酸序列系统地改变,以便用来自第二参考抗原的相应氨基酸取代第一参考抗原中的一个或多个氨基酸。该上下文中的“相应氨基酸”意指在对第一参考抗原和第二参考抗原进行序列比对时在该第一参考抗原和第二参考抗原的序列内的等效位置处的氨基酸。然后测量试验抗体与第一参考抗原、第二参考抗原和/或一系列的一种或多种嵌合抗原中的每一者的结合。然后可以将与每种抗原的结合的丧失/获得归因于相对于第一参考序列和/或第二参考序列所产生的特定氨基酸变化。可能已经知道抗体是否能够与第一参考抗原结合和/或第二参考抗原结合。例如,如实施例6中所述,第一参考抗原可以是人vγ4链并且第二参考抗原可以是人vγ2链,通过用vγ2链序列中相应的一个或多个氨基酸取代vγ4链序列中的一个或多个氨基酸来制成一系列嵌合抗原。
[0226]
抗体序列
[0227]
抗vγ4抗体或其片段可以参考它们的cdr序列进行描述。
[0228]
因此,在一个实施方案中,抗vγ4抗体或其片段包含以下的一者或多者:
[0229]
cdr3,其包含与seq id no:2-47中的任一个,优选与seq id no:10和/或33具有至少80%序列同一性的序列;
[0230]
cdr2,其包含与seq id no:48-70和序列:a1-a23(图1)中的任一个序列,优选与seq id no:56和/或a9具有至少80%序列同一性的序列;和/或
[0231]
cdr1,其包含与seq id no:71-116中的任一个,优选与seq id no:79和/或102具有至少80%序列同一性的序列。
[0232]
在一个实施方案中,抗vγ4抗体或其片段包含包含与seq id no:2-47中的任一个具有至少80%序列同一性的序列的cdr3。在一个实施方案中,该抗体或其片段包含包含与seq id no:48-70和序列:a1-a23(图1)中的任一个序列具有至少80%序列同一性的序列的cdr2。在一个实施方案中,该抗体或其片段包含包含与seq id no:71-116中的任一个具有至少80%序列同一性的序列的cdr1。
24中的任一个具有至少95%序列同一性的序列的cdr3;和/或vl区,该vl区包含包含与seq id no:25-47中的任一个具有至少95%序列同一性的序列的cdr3。在一个实施方案中,该抗体或其片段包含:vh区,该vh区包含由与seq id no:2-24中的任一个具有至少95%序列同一性的序列组成的cdr3;和/或vl区,该vl区包含由与seq id no:25-47中的任一个具有至少95%序列同一性的序列组成的cdr3。
[0246]
在一个实施方案中,该抗体或其片段包含:vh区,该vh区包含包含与seq id no:2-24中的任一个具有至少80%序列同一性的序列的cdr3;和vl区,该vl区包含包含与seq id no:25-47中的任一个具有至少80%序列同一性的序列的cdr3。在一个实施方案中,该抗体或其片段包含:vh区,该vh区包含由与seq id no:2-24中的任一个具有至少80%序列同一性的序列组成的cdr3;和vl区,该vl区包含由与seq id no:25-47中的任一个具有至少80%序列同一性的序列组成的cdr3。
[0247]
本文提及“至少80%”或“80%或更高”的实施方案将被理解为包括等于或高于80%的所有值,诸如85%、90%、95%、97%、98%、99%或100%的序列同一性。在一个实施方案中,该抗体或片段与指定序列具有至少85%,诸如至少90%、至少95%、至少97%、至少98%或至少99%的序列同一性。
[0248]
代替序列同一性百分比,实施方案也可以用一个或多个氨基酸变化,例如一个或多个添加、取代和/或缺失来限定。在一个实施方案中,该序列可以包含最多五个氨基酸变化,诸如最多三个氨基酸变化,尤其是最多两个氨基酸变化。例如,该序列可以包含最多五个氨基酸取代,诸如最多三个氨基酸取代,尤其是最多一个或两个氨基酸取代。例如,该抗体或其片段的cdr3可以包含与seq id no:2-47中的任一个相比具有不超过2个,更适当地不超过1个取代的序列或更适当地由该序列组成。
[0249]
适当地,cdr1、cdr2或cdr3中的不同于它们在seq id no:2-116和序列:a1-a23中的对应残基的任何残基是相对于它们的对应残基的保守性取代。例如,cdr3中的不同于它们在seq id no:2-47中的对应残基的任何残基是相对于它们的对应残基的保守性取代。
[0250]
在一个实施方案中,该抗体或其片段包含:
[0251]
(i)vh区,其包含包含与seq id no:2-24中的任一个具有至少80%序列同一性的序列的cdr3;
[0252]
(ii)vh区,其包含包含与seq id no:48-70中的任一个具有至少80%序列同一性的序列的cdr2;
[0253]
(iii)vh区,其包含包含与seq id no:71-93中的任一个具有至少80%序列同一性的序列的cdr1;
[0254]
(iv)vl区,其包含包含与seq id no:25-47中的任一个具有至少80%序列同一性的序列的cdr3;
[0255]
(v)vl区,其包含包含与序列:a1-a23(图1)中的任一个具有至少80%序列同一性的序列的cdr2;和/或
[0256]
(vi)vl区,其包含包含与seq id no:94-116中的任一个具有至少80%序列同一性的序列的cdr1。
[0257]
在一个实施方案中,该抗体或其片段包含重链,该重链具有:
[0258]
(i)vh区,其包含包含与seq id no:2-24中的任一个具有至少80%序列同一性的
no:23的序列组成,cdr2由seq id no:69的序列组成,且cdr1由seq id no:92的序列组成。
[0273]
在一个实施方案中,该抗体或其片段包含vl区(或由vl区组成),该vl区包含包含与seq id no:25-47中的任一个,诸如seq id no:33、27、37、38、40、42或46具有至少80%序列同一性的序列的cdr3。在一个实施方案中,该抗体或其片段包含vl区(或由vl区组成),该vl区包含包含与序列:a1-a23(图1)中的任一个,诸如序列:a9、a3、a13、a14、a16、a18或a22具有至少80%序列同一性的序列的cdr2。在一个实施方案中,该抗体或其片段包含vl区(或由vl区组成),该vl区包含包含与seq id no:94-116中的任一个,诸如seq id no:102、96、106、107、109、111或115具有至少80%序列同一性的序列的cdr1。
[0274]
在一个实施方案中,该vl区包含:包含seq id no:33的序列的cdr3、包含序列:a9的序列的cdr2和包含seq id no:102的序列的cdr1。在一个实施方案中,该cdr3由seq id no:33的序列组成,该cdr2由序列:a9的序列组成,且该cdr1由seq id no:102的序列组成。
[0275]
在一个实施方案中,该vl区包含:包含seq id no:27的序列的cdr3、包含序列:a3的序列的cdr2和包含seq id no:96的序列的cdr1。在一个实施方案中,该cdr3由seq id no:27的序列组成,该cdr2由序列:a3的序列组成,且该cdr1由seq id no:96的序列组成。
[0276]
在一个实施方案中,该vl区包含:包含seq id no:37的序列的cdr3、包含序列:a13的序列的cdr2和包含seq id no:106的序列的cdr1。在一个实施方案中,该cdr3由seq id no:37的序列组成,该cdr2由序列:a13的序列组成,且该cdr1由seq id no:106的序列组成。
[0277]
在一个实施方案中,该vl区包含:包含seq id no:38的序列的cdr3、包含序列:a14的序列的cdr2和包含seq id no:107的序列的cdr1。在一个实施方案中,该cdr3由seq id no:38的序列组成,该cdr2由序列:a14的序列组成,且该cdr1由seq id no:107的序列组成。
[0278]
在一个实施方案中,该vl区包含:包含seq id no:40的序列的cdr3、包含序列:a16的序列的cdr2和包含seq id no:109的序列的cdr1。在一个实施方案中,该cdr3由seq id no:40的序列组成,该cdr2由序列:a16的序列组成,且该cdr1由seq id no:109的序列组成。
[0279]
在一个实施方案中,该vl区包含:包含seq id no:42的序列的cdr3、包含序列:a18的序列的cdr2和包含seq id no:111的序列的cdr1。在一个实施方案中,该cdr3由seq id no:42的序列组成,该cdr2由序列:a18的序列组成,且该cdr1由seq id no:111的序列组成。
[0280]
在一个实施方案中,该vl区包含:包含seq id no:46的序列的cdr3、包含序列:a22的序列的cdr2和包含seq id no:115的序列的cdr1。在一个实施方案中,该cdr3由seq id no:46的序列组成,该cdr2由序列:a22的序列组成,且该cdr1由seq id no:115的序列组成。
[0281]
在一个实施方案中,该抗体或其片段包含一个或多个如图1中所述的cdr序列。在进一步的实施方案中,该抗体或其片段包含如图1中所描述的克隆1140_p01_g08[g4_12]或克隆1139_p01_a04[g4_03]的一个或多个(诸如所有)cdr序列。
[0282]
因此,抗vγ4抗体或其片段可以包含以下的一者或多者:
[0283]
(a)vh,其包含具有seq id no:79的hcdr1、具有seq id no:56的hcdr2和具有seq id no:10的hcdr3,任选地其中所述vh包含seq id no:125或由seq id no:125组成;和
[0284]
vl,其包含具有seq id no:102的lcdr1、具有序列a9(图1)的lcdr2和具有seq id no:33的lcdr3,任选地其中所述vl包含seq id no:148或由seq id no:148组成;
[0285]
(b)vh,其包含具有seq id no:86的hcdr1、具有seq id no:63的hcdr2和具有seq id no:17的hcdr3,任选地其中所述vh包含seq id no:132或由seq id no:132组成;和
id no:7的hcdr3,任选地其中所述vh包含seq id no:122或由seq id no:122组成;和
[0306]
vl,其包含具有seq id no:99的lcdr1、具有序列a6(图1)的lcdr2和具有seq id no:30的lcdr3,任选地其中所述vl包含seq id no:145或由seq id no:145组成;
[0307]
(m)vh,其包含具有seq id no:77的hcdr1、具有seq id no:54的hcdr2和具有seq id no:8的hcdr3,任选地其中所述vh包含seq id no:123或由seq id no:123组成;和
[0308]
vl,其包含具有seq id no:100的lcdr1、具有序列a7(图1)的lcdr2和具有seq id no:31的lcdr3,任选地其中所述vl包含seq id no:146或由seq id no:146组成;
[0309]
(n)vh,其包含具有seq id no:78的hcdr1、具有seq id no:55的hcdr2和具有seq id no:9的hcdr3,任选地其中所述vh包含seq id no:124或由seq id no:124组成;和
[0310]
vl,其包含具有seq id no:101的lcdr1、具有序列a8(图1)的lcdr2和具有seq id no:32的lcdr3,任选地其中所述vl包含seq id no:147或由seq id no:147组成;
[0311]
(o)vh,其包含具有seq id no:80的hcdr1、具有seq id no:57的hcdr2和具有seq id no:11的hcdr3,任选地其中所述vh包含seq id no:126或由seq id no:126组成;和
[0312]
vl,其包含具有seq id no:103的lcdr1、具有序列a10(图1)的lcdr2和具有seq id no:34的lcdr3,任选地其中所述vl包含seq id no:149或由seq id no:149组成;
[0313]
(p)vh,其包含具有seq id no:81的hcdr1、具有seq id no:58的hcdr2和具有seq id no:12的hcdr3,任选地其中所述vh包含seq id no:127或由seq id no:127组成;和
[0314]
vl,其包含具有seq id no:104的lcdr1、具有序列a11(图1)的lcdr2和具有seq id no:35的lcdr3,任选地其中所述vl包含seq id no:150或由seq id no:150组成;
[0315]
(q)vh,其包含具有seq id no:82的hcdr1、具有seq id no:59的hcdr2和具有seq id no:13的hcdr3,任选地其中所述vh包含seq id no:128或由seq id no:128组成;和
[0316]
vl,其包含具有seq id no:105的lcdr1、具有序列a12(图1)的lcdr2和具有seq id no:36的lcdr3,任选地其中所述vl包含seq id no:151或由seq id no:151组成;
[0317]
(r)vh,其包含具有seq id no:85的hcdr1、具有seq id no:62的hcdr2和具有seq id no:16的hcdr3,任选地其中所述vh包含seq id no:131或由seq id no:131组成;和
[0318]
vl,其包含具有seq id no:108的lcdr1、具有序列a15(图1)的lcdr2和具有seq id no:39的lcdr3,任选地其中所述vl包含seq id no:154或由seq id no:154组成;
[0319]
(s)vh,其包含具有seq id no:87的hcdr1、具有seq id no:64的hcdr2和具有seq id no:18的hcdr3,任选地其中所述vh包含seq id no:133或由seq id no:133组成;和
[0320]
vl,其包含具有seq id no:110的lcdr1、具有序列a17(图1)的lcdr2和具有seq id no:41的lcdr3,任选地其中所述vl包含seq id no:156或由seq id no:156组成;
[0321]
(t)vh,其包含具有seq id no:89的hcdr1、具有seq id no:66的hcdr2和具有seq id no:20的hcdr3,任选地其中所述vh包含seq id no:135或由seq id no:135组成;和
[0322]
vl,其包含具有seq id no:112的lcdr1、具有序列a19(图1)的lcdr2和具有seq id no:43的lcdr3,任选地其中所述vl包含seq id no:158或由seq id nq:158组成;
[0323]
(u)vh,其包含具有seq id no:90的hcdr1、具有seq id no:67的hcdr2和具有seq id no:21的hcdr3,任选地其中所述vh包含seq id no:136或由seq id no:136组成;和
[0324]
vl,其包含具有seq id no:113的lcdr1、具有序列a20(图1)的lcdr2和具有seq id no:44的lcdr3,任选地其中所述vl包含seq id no:159或由seq id no:159组成;
[0325]
(v)vh,其包含具有seq id no:91的hcdr1、具有seq id no:68的hcdr2和具有seq id no:22的hcdr3,任选地其中所述vh包含seq id no:137或由seq id no:137组成;和
[0326]
vl,其包含具有seq id no:114的lcdr1、具有序列a21(图1)的lcdr2和具有seq id no:45的lcdr3,任选地其中所述vl包含seq id no:160或由seq id no:160组成;
[0327]
和/或
[0328]
(w)vh,其包含具有seq id no:93的hcdr1、具有seq id no:70的hcdr2和具有seq id no:24的hcdr3,任选地其中所述vh包含seq id no:139或由seq id no:139组成;和
[0329]
vl,其包含具有seq id no:116的lcdr1、具有序列a23(图1)的lcdr2和具有seq id no:47的lcdr3,任选地其中所述vl包含seq id no:162或由seq id no:162组成。
[0330]
适当地,上面列举的vh区和vl区各自包含四个框架区(fr1-fr4)。在一个实施方案中,该抗体或其片段包含框架区(例如,fr1、fr2、fr3和/或fr4),该框架区包含与seq id no:117-162中的任一个中的框架区具有至少80%序列同一性的序列。在一个实施方案中,该抗体或其片段包含框架区(例如,fr1、fr2、fr3和/或fr4),该框架区包含与seq id no:117-162中的任一个中的框架区具有至少90%,诸如至少95%、97%或99%序列同一性的序列。在一个实施方案中,该抗体或其片段包含框架区(例如,fr1、fr2、fr3和/或fr4),该框架区包含seq id no:117-162中的任一个中的序列。在一个实施方案中,该抗体或其片段包含框架区(例如,fr1、fr2、fr3和/或fr4),该框架区由seq id no:117-162中的任一个中的序列组成。
[0331]
本文所述的抗体可以由它们的完整轻链和/或重链可变序列来限定。因此,在一个实施方案中,抗vγ4抗体或其片段包含与seq id no:117-162中的任一个具有至少80%序列同一性的氨基酸序列。在一个实施方案中,抗vγ4抗体或其片段由与seq id no:117-162中的任一个具有至少80%序列同一性的氨基酸序列组成。
[0332]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含与seq id no:117-139中的任一个具有至少80%序列同一性的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由与seq id no:117-139中的任一个具有至少80%序列同一性的氨基酸序列组成。在进一步的实施方案中,该vh区包含与seq id no:125、119、129、130、132、134或138中的任一个具有至少80%序列同一性的氨基酸序列。在进一步的实施方案中,该vh区由与seq id no:125、119、129、130、132、134或138中的任一个具有至少80%序列同一性的氨基酸序列组成。
[0333]
在一个实施方案中,该抗体或其片段包含vl区,该vl区包含与seq id no:140-162中的任一个具有至少80%序列同一性的氨基酸序列。在一个实施方案中,该抗体或其片段包含vl区,该vl区由与seq id no:140-162中的任一个具有至少80%序列同一性的氨基酸序列组成。在进一步的实施方案中,该vl区包含与seq id no:148、142、152、153、155、157或161中的任一个具有至少80%序列同一性的氨基酸序列。在进一步的实施方案中,该vl区由与seq id no:148、142、152、153、155、157或161中的任一个具有至少80%序列同一性的氨基酸序列组成。
[0334]
在进一步的实施方案中,该抗体或其片段包含:vh区,该vh区包含与seq id no:117-139中的任一个具有至少80%序列同一性的氨基酸序列;和vl区,该vl区包含与seq id no:140-162中的任一个具有至少80%序列同一性的氨基酸序列。在进一步的实施方案中,
该抗体或其片段包含vh区,该vh区由与seq id no:117-139中的任一个具有至少80%序列同一性的氨基酸序列组成;和vl区,该vl区由与seq id no:140-162中的任一个具有至少80%序列同一性的氨基酸序列组成。
[0335]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:125的氨基酸序列(1140_p0i_g08)[g4_12]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:125的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:148的氨基酸序列(1140_p01_g08)[g4_12]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:148的氨基酸序列组成。
[0336]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:125的氨基酸序列;和vl区,该vl区包含seq id no:148的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:125的氨基酸序列组成;和vl区,该vl区由seq id no:148的氨基酸序列组成。
[0337]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:119的氨基酸序列(1139_p01_a04)[g4_3]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:119的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:142的氨基酸序列(1139_p01_a04)[g4_3]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:142的氨基酸序列组成。
[0338]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:119的氨基酸序列;和vl区,该vl区包含seq id no:142的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:119的氨基酸序列组成;和vl区,该vl区由seq id no:142的氨基酸序列组成。
[0339]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:129的氨基酸序列(1248_p02_d10)[g4_16]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:129的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:152的氨基酸序列(1248_p02_d10)[g4_16]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:152的氨基酸序列组成。
[0340]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:129的氨基酸序列;和vl区,该vl区包含seq id no:152的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:129的氨基酸序列组成;和vl区,该vl区由seq id no:152的氨基酸序列组成。
[0341]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:130的氨基酸序列(1254_p01_h04)[g4_18]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:130的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:153的氨基酸序列(1254_p01_h04)[g4_18]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:153的氨基酸序列组成。
[0342]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:130的氨基酸序列;和vl区,该vl区包含seq id no:153的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:130的氨基酸序列组成;和vl区,该vl区由seq id no:153的氨基酸序列组成。
[0343]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:132的氨基酸序列(1254_p02_g02)[g4_20]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:132的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:155的氨基酸序列(1254_p02_g02)[g4_20]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:155的氨基酸序列组成。
[0344]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:132的氨基酸序列;和vl区,该vl区包含seq id no:155的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:132的氨基酸序列组成;和vl区,该vl区由seq id no:155的氨基酸序列组成。
[0345]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:134的氨基酸序列(1253_p03_h05)[g4_23]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:134的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:157的氨基酸序列(1253_p03_h05)[g4_23]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:157的氨基酸序列组成。
[0346]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:134的氨基酸序列;和vl区,该vl区包含seq id no:157的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:134的氨基酸序列组成;和vl区,该vl区由seq id no:157的氨基酸序列组成。
[0347]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:138的氨基酸序列(1248_p02_c10)[g4_27]。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:138的氨基酸序列组成。在一个实施方案中,该抗体或其片段包含vl区,该vl区包含seq id no:161的氨基酸序列(1248_p02_c10)[g4_27]。在一个实施方案中,该抗体或其片段包含vl区,该vl区由seq id no:161的氨基酸序列组成。
[0348]
在一个实施方案中,该抗体或其片段包含vh区,该vh区包含seq id no:138的氨基酸序列;和vl区,该vl区包含seq id no:161的氨基酸序列。在一个实施方案中,该抗体或其片段包含vh区,该vh区由seq id no:138的氨基酸序列组成;和vl区,该vl区由seq id no:161的氨基酸序列组成。
[0349]
对于同时包含vh区和vl区的片段,这些vh区和vl区可以共价缔合(例如经由二硫键或接头)或非共价缔合。本文所述的抗体片段可包含scfv,即包含通过接头联接的vh区和vl区的片段。在一个实施方案中,vh区和vl区通过(例如合成的)多肽接头联接。该多肽接头可以包含(gly4ser)n接头,其中n=1至8,例如2、3、4、5或7。该多肽接头可包含[(gly4ser)n(gly3alaser)m]
p
接头,其中n=1至8,例如2、3、4、5或7,m=0至8,例如0、1、2或3,以及p=1至8,例如1、2或3。在进一步的实施方案中,该接头包含seq id no:186。在进一步的实施方案中,该接头由seq id no:186组成。
[0350]
在一个实施方案中,该抗体或其片段包含与seq id no:163-185中的任一个具有至少80%序列同一性的氨基酸序列。在进一步的实施方案中,该抗体或其片段包含seq id no:163-185中的任一个的氨基酸序列。在再进一步的实施方案中,该抗体或其片段包含seq id no:171、165、175、176、178、180或184的氨基酸序列。
[0351]
在一个实施方案中,该抗体或其片段由与seq id no:163-185中的任一个具有至
少80%序列同一性的氨基酸序列组成。在进一步的实施方案中,该抗体或其片段由seq id no:163-185中的任一个的氨基酸序列组成。再进一步的实施方案中,该抗体或其片段由seq id no:171、165、175、176、178、180或184的氨基酸序列组成。
[0352]
如本文所述,该抗体可以呈任何格式。在一个优选实施方案中,该抗体呈igg1格式。因此,在一个实施方案中,该抗体或其片段包含与seq id no:233-255中的任一个具有至少80%序列同一性的氨基酸序列。在进一步的实施方案中,该抗体或其片段包含seq id no:233-255中的任一个的氨基酸序列。再进一步的实施方案中,该抗体或其片段包含seq id no:235、241、245、246或254的氨基酸序列。
[0353]
在一个实施方案中,该抗体或其片段由与seq id no:233-255中的任一个具有至少80%序列同一性的氨基酸序列组成。在进一步的实施方案中,该抗体或其片段由seq id no:233-255中的任一个的氨基酸序列组成。在再进一步的实施方案中,该抗体或其片段由seq id no:235、241、245、246或254的氨基酸序列组成。
[0354]
可替代地,提供了一种抗体或其片段,该抗体或其片段包含与seq id no:284-306中的任一个具有至少80%序列同一性的重链氨基酸序列和/或与seq id no:307-329中的任一个具有至少80%序列同一性的轻链氨基酸序列,或者由与seq id no:284-306中的任一个具有至少80%序列同一性的重链氨基酸序列和/或与seq id no:307-329中的任一个具有至少80%序列同一性的轻链氨基酸序列组成。因此,提供了一种抗体或其片段,该抗体或其片段包含根据seq id no:284-306中的任一个的重链氨基酸序列和/或根据seq id no:307-329中的任一个的轻链氨基酸序列,或者由根据seq id no:284-306中的任一个的重链氨基酸序列和/或根据seq id no:307-329中的任一个的轻链氨基酸序列组成。在一个特定实施方案中,该抗体或其片段包含根据seq id no:292的重链氨基酸序列和根据seq id no:315的轻链氨基酸序列,或者由根据seq id no:292的重链氨基酸序列和根据seq id no:315的轻链氨基酸序列组成(克隆g4_12)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:286的重链氨基酸序列和根据seq id no:309的轻链氨基酸序列,或者由根据seq id no:286的重链氨基酸序列和根据seq id no:309的轻链氨基酸序列组成(克隆g4_3)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:296的重链氨基酸序列和根据seq id no:319的轻链氨基酸序列,或者由根据seq id no:296的重链氨基酸序列和根据seq id no:319的轻链氨基酸序列组成(克隆g4_16)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:297的重链氨基酸序列和根据seq id no:320的轻链氨基酸序列,或者由根据seq id no:297的重链氨基酸序列和根据seq id no:320的轻链氨基酸序列组成(克隆g4_18)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:299的重链氨基酸序列和根据seq id no:322的轻链氨基酸序列,或者由根据seq id no:299的重链氨基酸序列和根据seq id no:322的轻链氨基酸序列组成(克隆g4_20)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:301的重链氨基酸序列和根据seq id no:324的轻链氨基酸序列,或者由根据seq id no:301的重链氨基酸序列和根据seq id no:324的轻链氨基酸序列组成(克隆g4_23)。在进一步的实施方案中,该抗体或其片段包含根据seq id no:305的重链氨基酸序列和根据seq id no:328的轻链氨基酸序列,或者由根据seq id no:305的重链氨基酸序列和根据seq id no:328的轻链氨基酸序列组成(克隆g4_27)。在其它实施方案中,该抗体或其片段包含以下或由以下组成:
[0355]
(a)根据seq id no:284的重链氨基酸序列和根据seq id no:307的轻链氨基酸序列(克隆g4_1);
[0356]
(b)根据seq id no:285的重链氨基酸序列和根据seq id no:308的轻链氨基酸序列(克隆g4_2);
[0357]
(c)根据seq id no:287的重链氨基酸序列和根据seq id no:310的轻链氨基酸序列(克隆g4_4);
[0358]
(d)根据seq id no:288的重链氨基酸序列和根据seq id no:311的轻链氨基酸序列(克隆g4_5);
[0359]
(e)根据seq id no:289的重链氨基酸序列和根据seq id no:312的轻链氨基酸序列(克隆g4_6);
[0360]
(f)根据seq id no:290的重链氨基酸序列和根据seq id no:313的轻链氨基酸序列(克隆g4_7);
[0361]
(g)根据seq id no:291的重链氨基酸序列和根据seq id no:314的轻链氨基酸序列(克隆g4_10);
[0362]
(h)根据seq id no:293的重链氨基酸序列和根据seq id no:316的轻链氨基酸序列(克隆g4_13);
[0363]
(i)根据seq id no:294的重链氨基酸序列和根据seq id no:317的轻链氨基酸序列(克隆g4_14);
[0364]
(j)根据seq id no:295的重链氨基酸序列和根据seq id no:318的轻链氨基酸序列(克隆g4_15);
[0365]
(k)根据seq id no:298的重链氨基酸序列和根据seq id no:321的轻链氨基酸序列(克隆g4_19);
[0366]
(1)根据seq id no:300的重链氨基酸序列和根据seq id no:323的轻链氨基酸序列(克隆g4_22);
[0367]
(m)根据seq id no:302的重链氨基酸序列和根据seq id no:325的轻链氨基酸序列(克隆g4_24);
[0368]
(n)根据seq id no:303的重链氨基酸序列和根据seq id no:326的轻链氨基酸序列(克隆g4_25);
[0369]
(o)根据seq id no:304的重链氨基酸序列和根据seq id no:327的轻链氨基酸序列(克隆g4_26);
[0370]
或者
[0371]
(p)根据seq id no:306的重链氨基酸序列和根据seq id no:329的轻链氨基酸序列(克隆g4_28)。
[0372]
竞争抗体
[0373]
在一个实施方案中,与γδ tcr的vγ4链特异性地结合而不与γδtcr的vγ2链特异性地结合的抗体或其片段与如本文定义或举例说明的抗体或其片段结合相同或基本上相同的表位,或者与如本文定义或举例说明的抗体或其片段竞争。通过使用本领域已知的常规方法,可以容易地确定抗体是否与参考抗vγ4抗体结合相同的表位,或者与参考抗vγ4抗体竞争结合。例如,为了确定试验抗体是否与本文所述的参考抗vγ4抗体结合相同的表
位,让该参考抗体在饱和条件下与vγ4蛋白或肽结合。接下来,评估试验抗体与vγ4链结合的能力。如果试验抗体在与参考抗vγ4抗体饱和结合后能够与vγ4结合,则可以断定试验抗体与参考抗vγ4抗体结合不同的表位。另一方面,如果试验抗体在与参考抗vγ4抗体饱和结合后不能与vγ4链结合,则试验抗体可以与和参考抗vγ4抗体所结合的表位相同的表位结合。
[0374]
本公开还包括与如本文限定的抗体或其片段或具有本文所述的任何示例性抗体的cdr序列的抗体竞争与vγ4的结合的抗vγ4抗体或其片段。例如,可以用本文所述的抗体执行竞争性测定以确定哪些蛋白质、抗体和其它拮抗剂与所述抗体竞争与vγ4链的结合以及/或者共享表位。这些测定是本领域技术人员容易知道的;它们评价拮抗剂或配体之间对蛋白质上有限数目的结合位点(例如vγ4)的竞争。使该抗体(或其片段)在竞争之前或之后固定或不溶解,并且例如通过倾析(在使抗体预先不溶解的情况下)或通过离心(在竞争反应后抗体沉淀的情况下)将与vγ4链结合的样品与未结合的样品分开。此外,竞争性结合可以通过功能是否因抗体与蛋白质的结合或不结合而改变,例如,抗体分子是否抑制或加强例如标记的酶活性来确定。如本领域已知和本文所述,可以使用elisa和其它功能测定。
[0375]
如果两种抗体中每一种抗体均竞争性地抑制(阻断)另一种抗体与靶抗原的结合,则这两种抗体与相同或重叠表位结合。也就是说,一种抗体的1、5、10、20或100倍或更多倍过量将另一种抗体的结合抑制了至少50%,但优选75%、90%或甚至99%,如在竞争性结合测定中测量的。可替代地,如果靶抗原中降低或消除一种抗体的结合的基本上所有的氨基酸突变也降低或消除另一种抗体的结合,则该两种抗体具有相同的表位。
[0376]
然后可以进行额外的常规实验(例如,肽突变和结合分析)以确认观察到的试验抗体结合的缺乏事实上是否是由于与参考抗体结合相同的表位,或者空间阻断(或另一种现象)是否是造成缺乏观察到的结合的原因。可以使用elisa、ria、表面等离子体共振、流式细胞术或本领域可用的任何其它定量或定性抗体结合测定来进行此类实验。
[0377]
抗体序列修饰
[0378]
可以使用已知方法修饰抗体及其片段。本领域技术人员可以容易地掺入对本文所述的抗体分子的序列修饰。以下实例是非限制性的。
[0379]
在从噬菌体文库中发现抗体和恢复序列期间,可以通过亚克隆将所需的抗体可变结构域重新格式化为全长igg。为了加速该过程,常常使用限制性酶转移可变结构域。这些限制位点可以引入额外的/替代性氨基酸且远离规范序列(此类规范序列可以在例如国际免疫遗传学[imgt]信息系统(参见http://www.imgt.org)中找到)。这些可以作为κ或λ轻链序列修饰引入。
[0380]
κ轻链修饰
[0381]
κ轻链可变序列可以使用限制位点(例如nhe1-not1)在重新格式化为全长igg期间克隆。更具体地说,在κ轻链n端,引入额外的ala-ser序列以支持克隆。优选地,然后在进一步开发期间去除此额外的as序列以生成规范的n端序列。因此,在一个实施方案中,本文所述的含κ轻链的抗体在它们的n-端不含as序列,即seq id no:140-147和156-158不包含初始as序列。应当理解,该实施方案也适用于本文中包含的含有这个序列的其它序列。
[0382]
可以制作额外的氨基酸变化以支持克隆。例如,对于本文所述的抗体,在制备全长序列时在κ轻链可变结构域/恒定结构域边界处引入了缬氨酸到丙氨酸的变化以支持克隆。
这导致了κ恒定结构域修饰。具体地,这导致以rtaaaps(从noti限制位点)开始的恒定结构域。优选地,该序列可以在进一步开发期间进行修饰,以生成以rtvaaps开始的规范κ轻链恒定区。此类修饰不会改变抗体的功能特性。因此,在一个实施方案中,本文所述的含κ轻链的抗体含有以序列rtv开始的恒定结构域。因此,在一个实施方案中,seq id no:233-240、249-251、307-314和323-325的序列rtaaaps被序列rtvaaps置换。在包含优选的κ轻链恒定结构域同种异型的优选实施方案中,κ轻链恒定结构域具有根据seq id no:330的氨基酸序列并且可以与本文公开的任何轻链可变结构域组合。
[0383]
λ轻链修饰
[0384]
与上面的κ实例类似,λ轻链可变结构域也可以通过引入限制位点(例如nhe1-not1)在重新格式化为全长igg期间克隆。更具体地说,在λ轻链n端,可以引入额外的ala-ser序列以支持克隆。优选地,然后在进一步开发期间去除此额外的as序列以生成规范的n端序列。因此,在一个实施方案中,本文所述的含λ轻链的抗体在它们的n-端不含as序列,即seq id no:148-155和159-162不包含初始as序列。应当理解,该实施方案也适用于本文中包含的含有这个序列的其它序列。
[0385]
作为另一个实例,对于本文所述的抗体,在制备全长序列时在λ轻链可变结构域/恒定结构域边界处引入了赖氨酸到丙氨酸的变化以支持克隆。这导致了λ恒定结构域修饰。具体地,这导致以gqpaaaps(从noti限制位点)开始的恒定结构域。优选地,该序列可以在进一步开发期间进行修饰,以生成以gqpkaaps开始的规范λ轻链恒定区。此类修饰不会改变抗体的功能特性。因此,在一个实施方案中,本文所述的含λ轻链的抗体含有以序列gqpk开始的恒定结构域。因此,在一个实施方案中,seq id no:241-248、252-255、315-322和326-329的序列gqpaaaps被序列gqpkaaps置换。在包含优选的λ轻链恒定结构域同种异型的优选实施方案中,λ轻链恒定结构域具有根据seq id no:331的氨基酸序列并且可以与本文公开的任何轻链可变结构域组合。
[0386]
λ和κ轻链修饰
[0387]
鉴于以上关于从本文公开为seq id no:140-162的λ和/或κ轻链可变结构域中去除n端as残基的公开内容,抗vγ4抗体或片段可包含根据seq id no:261-283(其对应于缺乏n端as残基的seq id no:140-162)中的任一个的轻链可变(vl)氨基酸序列。因此,本说明书中对根据seq id no:140-162中的一个或多个的vl氨基酸序列的任何提及可以分别用根据seq id no:261-283的vl氨基酸序列代替,并且所有此类实施方案特此被公开。通过举例说明的方式,本文对根据seq id no:148的轻链可变结构域(源自克隆g4_12)的提及可以用对seq id no:269的提及代替。
[0388]
重链修饰
[0389]
通常,人可变重链序列以碱性谷氨酰胺(q)或酸性谷氨酸(e)开始。然而,已知这两种序列都转化为酸性氨基酸残基焦谷氨酸(pe)。q到pe的转化导致抗体的电荷变化,而e到pe的转化不改变抗体的电荷。因此,为了避免随时间推移的可变电荷变化,一种选择是首先将起始重链序列从q修饰为e。因此,在一个实施方案中,在重链的n端具有q残基的本文所述的抗体的重链可以在n端含有q到e的修饰。具体而言,seq id no:118、120、124、126、132、133、135、137、138和/或139中任一个的起始残基可以从q修饰为e。应当理解,该实施方案也适用于本文包括的含有该序列的其它序列(即,将这些序列掺入到例如全长抗体或其片段
中的任何实施方案)。在一些实施方案中,将重链n端的e残基取代为q残基可能是有利的。因此,在一些实施方案中,seq id no:117、119、121-123、125、127-131、134和/或136中任一个的n端处的e残基可以被q残基取代。
[0390]
此外,igg1恒定结构域的c端以pgk结束。然而,端碱性赖氨酸(k)常常然后在表达期间被切割(例如,在cho细胞中)。这转而通过c端赖氨酸残基的不同损失导致抗体的电荷变化。因此,一种选择是首先去除赖氨酸,从而产生以pg结束的统一且一致的重链c端序列。因此,在一个实施方案中,本文所述的抗体的重链的端k从该重链的c端被去除。具体而言,该抗体可以包含seq id no:233-255或284-306中的任一个,其中端赖氨酸残基已被去除。
[0391]
任选的同种异型修饰
[0392]
在抗体发现期间,可以采用特定的人同种异型。任选地,抗体可以在开发期间转换为不同的人同种异型。作为非限制性实例,对于κ链,存在命名为km1、km1,2和km3的三种人同种异型,它们限定了三个km等位基因(使用同种异型编号):km1与缬氨酸153(imgt v45.1)和亮氨酸191(imgt l101)相关;km1,2与丙氨酸153(imgt a45.1)和亮氨酸191(imgt l101)相关;且km3与丙氨酸153(imgt a45.1)和缬氨酸191(imgt v101)相关。任选地,因此可以通过标准克隆方法将序列从一种同种异型修饰为另一种同种异型。例如,l191v(imgt l101v)变化会将km1,2同种异型转换为km3同种异型。对于有关此类同种异型的进一步参考,参见jefferis和lefranc(2009)mabs1(4):332-8,其通过引用并入本文。
[0393]
因此在一个实施方案中,本文所述的抗体含有源自相同基因的另一种人同种异型的氨基酸取代。在进一步的实施方案中,抗体含有对κ链的l191v(imgt l101v)取代以将c-结构域从km1,2转化为km3同种异型。
[0394]
在包含优选的κ轻链恒定结构域同种异型的优选实施方案中,κ轻链恒定结构域具有根据seq id no:330的氨基酸序列并且可以与本文公开的任何轻链可变结构域组合。在包含优选的λ轻链恒定结构域同种异型的替代性优选实施方案中,λ轻链恒定结构域具有根据seq id no:331的氨基酸序列并且可以与本文公开的任何轻链可变结构域组合。
[0395]
抗体结合
[0396]
所述抗体或其片段可以以如通过表面等离子体共振测量的小于3.0x10-7
m(即300nm)或小于1.5x10-7
m(即150nm)的结合亲和力(kd)与γδtcr的vγ4链结合。在进一步的实施方案中,kd为1.3x10-7
m(即130nm)或更小,诸如1.0x10-7
m(即100nm)或更小。在再进一步的实施方案中,kd小于6.0x10-8
m(即60nm),诸如小于5.0x10-8
m(即50nm)、小于4.0x10-8
m(即40nm)、小于3.0x10-8
m(即30nm)或小于2.0x10-8
m(即20nm)。在进一步的实施方案中,kd可以是1.0x10-8
m(即10nm)或更小,诸如5.0x10-9
m(即5nm)或更小,4.0x10-9
m(即4nm)或更小,3.0x10-9
m(即3nm)或更小,2.0x10-9
m(即2nm)或更小,或1.0x10-9
m(即1nm)或更小。例如,在一个实施方案中,(例如人)抗vγ4抗体以如通过表面等离子体共振测量的小于1.5x10-7
m(即150nm)的结合亲和力(kd)与γδtcr的vγ4链结合。
[0397]
在一个实施方案中,该抗体或其片段以如通过表面等离子体共振测量的小于4.0x10-8
m(即40nm),小于3.0x10-8
m(即30nm)或小于2.0x10-8
m(即20nm)的结合亲和力(kd)与γδtcr的vγ4链结合。
[0398]
在一个实施方案中,该抗体或其片段的结合亲和力是通过将该抗体或其片段直接或间接(例如通过用抗人iggfc捕获)包被到传感器(例如胺高容量芯片或等效物)的表面上
来确定的,其中使被该抗体或其片段结合的靶标(即,γδtcr的vγ4链)流过芯片以检测结合。在可替代的实施方案中,可以将抗原直接或间接地包被到传感器的表面上,然后使试验抗体或其片段流过该表面。技术人员将能够很好地确定合适的试验条件。例如,适当地,mass-2仪器(其也可以称为sierraspr-32)可以在25℃下在30μl/min的pbs+0.02%吐温20运行缓冲液中使用。在其它合适的实施方案中,reichert4spr仪器可以在室温(例如25℃)下在流速为25μl/min的pbs+0.05%吐温20中使用。
[0399]
抗体功能表征
[0400]
本文描述了可用于界定抗体功能的测定。例如,本文所述的抗体或其片段可以通过例如测量抗体结合后γδtcr的下调和/或抗体结合后cd69表面表达的上调的γδtcr接合(engagement)来评估。可以例如通过流式细胞术测量在施加抗体或其片段(任选地被呈递在细胞表面上)后的γδtcr或cd69的表面表达。
[0401]
本文所述的抗体或其片段也可以通过测量γδt细胞脱粒来评估。例如,可以在将抗体或其片段(任选地被呈递在细胞表面上)施加于γδt细胞后通过流式细胞术测量cd107a(细胞脱粒的标志物)的表达。本文所述的抗体或其片段也可以通过测量γδt细胞介导的杀伤活性(以测试该抗体是否对γδt细胞的杀伤活性有影响,即该抗体诱导γδt细胞直接或间接杀伤靶细胞的能力)来评估。例如,可以将靶细胞在存在该抗体或其片段(任选地被呈递在细胞表面上)的情况下与γδt细胞一起孵育。孵育后,可以用细胞活力染料对培养物进行染色,以区分活靶细胞和死靶细胞。然后可以例如通过流式细胞术测量死细胞的比例。
[0402]
如本文所述,测定中使用的抗体或其片段可以被呈递在表面,例如细胞(诸如包含fc受体的细胞)的表面上。例如,该抗体或其片段可以被呈递在thp-1细胞,诸如tib-202
tm
细胞(可从美国模式培养物保藏中心(atcc)获得)的表面上。可替代地,该抗体或其片段可以在测定中直接使用。
[0403]
在此类功能测定中,可以通过计算半数最大浓度(也称为“ec50”或“50%时的有效浓度”)来测量输出。术语“ic50”是指抑制浓度。ec50和ic50都可以使用本领域已知的方法,诸如流式细胞术方法测量。为免生疑问,本技术中的ec50值是使用呈igg1格式的抗体提供的。此类值可以很容易地如下基于该抗体格式的分子量转换为等效值:
[0404]
(μg/ml)/(mw(以kda计))=μm
[0405]
毫升在本文中可表示为“ml”或“ml”并且可互换使用。
[0406]
抗体(或片段)结合后γδtcr下调的ec50可小于0.5μg/ml,诸如小于0.4μg/ml、0.3μg/ml、0.2μg/ml、0.15μg/ml、0.1μg/ml或0.05μg/ml。具体而言,所述ec50值是当抗体以igg1格式被测量时的值。例如,可以使用流式细胞术测量ec50γδtcr下调值。
[0407]
抗体(或片段)结合后γδt细胞脱粒的ec50可小于0.05μg/ml,诸如小于0.04μg/ml、0.03μg/ml、0.02μg/ml、0.015μg/ml、0.01μg/ml或0.008μg/ml。具体而言,所述ec50值是当抗体以igg1格式被测量时的值。例如,γδt细胞脱粒ec50值可以通过使用流式细胞术检测cd107a表达(即细胞脱粒的标志物)来测量。在一个实施方案中,cd107a表达是使用抗cd107a抗体,诸如抗人cd107a bv421(克隆h4a3)(bd biosciences)测量的。
[0408]
该抗体(或片段)结合后γδt细胞介导的杀伤的ec50可小于0.5μg/ml,诸如小于0.4μg/ml、0.3μg/ml、0.2μg/ml、0.15μg/ml、0.1μg/ml或0.07μg/ml。具体而言,所述ec50值
是当抗体以igg1格式被测量时的值。例如,ec50γδt细胞介导的杀伤值可以通过在抗体、γδt细胞和靶细胞孵育后使用流式细胞术检测死细胞的比例(即使用细胞活力染料)来测量。在一个实施方案中,使用细胞活力染料,即活力染料efluor
tm
520(thermofisher)测量靶细胞的死亡。
[0409]
在这些方面中描述的测定中,该抗体或其片段可以被呈递在细胞,诸如thp-1细胞(例如tib-202
tm
(atcc))的表面上。thp-1细胞任选地用染料,诸如celltracker
tm
orange cmtmr(thermofisher)标记。
[0410]
多核苷酸和表达载体
[0411]
还提供了编码本文所述的抗vγ4抗体或片段的多核苷酸。在一个实施方案中,抗vγ4抗体或其片段由多核苷酸编码,该多核苷酸包含与seq id no:187-232具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列或由该序列组成。在一个实施方案中,抗vγ4抗体或其片段由包含seq id no:187-209的vh区的表达载体编码。在另一个实施方案中,抗vγ4抗体或其片段由包含seq id no:210-232的vl区的表达载体编码。在进一步的实施方案中,抗vγ4抗体或其片段由多核苷酸编码,该多核苷酸包含seq id no:187-232或由seq id no:187-232组成。在进一步的实施方案中,提供了包含该多核苷酸的cdna。
[0412]
在一个实施方案中,该多核苷酸包含与seq id no:195、189、199、200、202、204、208、218、212、222、223、225、227或231具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列或由该序列组成。在一个实施方案中,该表达载体包含seq id no:195、189、199、200、202、204或208的vh区。在另一个实施方案中,该表达载体包含seq id no:218、212、222、223、225、227或231的vl区。在进一步的实施方案中,该多核苷酸包含以下或由以下组成:seq id no:195、189、199、200、202、204、208、218、212、222、223、225、227或231,尤其是seq id no:195和/或218;或seq id no:189和/或212。在进一步的实施方案中,提供了包含该多核苷酸的cdna。
[0413]
在一个实施方案中,该多核苷酸包含以下或由以下组成:与编码所编码的免疫球蛋白链可变结构域的cdr1、cdr2和/或cdr3的seq id no:187-232的任一部分具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列。在一个实施方案中,该多核苷酸包含以下或由以下组成:与编码所编码的免疫球蛋白链可变结构域的cdr1、cdr2和/或cdr3的seq id no:195、189、199、200、202、204、208、218、212、222、223、225、227或231的任一部分具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列。
[0414]
在一个实施方案中,该多核苷酸包含以下或由以下组成:与编码所编码的免疫球蛋白链可变结构域的fr1、fr2、fr3和/或fr4的seq id no:187-232的任一部分具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列。在一个实施方案中,该多核苷酸包含以下或由以下组成:与编码所编码的免疫球蛋白链可变结构域的fr1、fr2、fr3和/或fr4的seq id no:195、189、199、200、202、204、208、218、212、222、223、225、227或231的任一部分具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性的序列。
[0415]
为了使抗体或其片段表达,将如本文所述的编码部分或全长轻链和重链的多核苷
酸插入到表达载体中,以使得基因操作性地连接到转录和翻译控制序列(其可称为如本领域所熟知的“表达盒”)。因此,还描述了包含如本文所限定的多核苷酸序列的表达载体。在一个实施方案中,该表达载体包含seq id no:187-209中的任一个,诸如seq id no:195、189、199、200、202、204或208中的任一个的vh序列。在另一个实施方案中,该表达载体包含seq id no:210-232中的任一个,诸如seq id no:218、212、222、223、225、227或231中的任一个的vl区。此类表达载体或表达盒可以成对使用,从而适当地根据提供本文公开的抗体的各种氨基酸序列的配对对重链和轻链可变序列进行配对。在一些实施方案中,表达载体包含与seq id no:187-209中的任一个具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性或100%的同一性的序列(编码可变重区)并且进一步包含与seq id no:210-232中的任一个具有至少70%,诸如至少80%,诸如至少90%,诸如至少95%,诸如至少99%的序列同一性或100%的同一性的序列(编码可变轻区)。同样,该序列可以如本文所述以特定对的形式提供以编码本文公开的抗体。
[0416]
多核苷酸和表达载体也可以参考所编码的氨基酸序列进行描述。因此,在一个实施方案中,该多核苷酸包含编码seq id no:1至186、233-260中的任一个的氨基酸序列的序列或者由编码seq id no:1至186、233-260中的任一个的氨基酸序列的序列组成。
[0417]
可以给编码多肽的dna或cdna制作这样的突变,该突变对于该多肽的氨基酸序列沉默的,但是为在特定宿主中的翻译提供了优选密码子。用于在例如大肠杆菌(e.coli)和酿酒酵母(s.cerevisiae),以及哺乳动物,特别是人中翻译核酸的优选密码子是已知的。
[0418]
多肽的突变可以例如通过对编码该多肽的核酸的取代、添加或缺失来实现。对编码该多肽的核酸的取代、添加或缺失可以通过许多方法引入,该方法包括例如易错pcr、改组、寡核苷酸定向诱变、组装pcr、pcr诱变、体内诱变、盒式诱变、递归整体诱变、指数整体诱变、位点特异性诱变、基因重组装、人工基因合成、基因位点饱和诱变(gssm)、合成连结重组装(slr)或这些方法的组合。对核酸的修饰、添加或缺失也可以通过包括以下的方法来引入:重组、递归序列重组、硫代磷酸酯修饰的dna诱变、含尿嘧啶的模板诱变、缺口双重诱变、点错配修复诱变、修复缺陷型宿主菌株诱变、化学诱变、放射引起的诱变、缺失诱变、限制选择诱变、限制纯化诱变、整体诱变、嵌合核酸多聚体创建和/或它们的组合。
[0419]
具体而言,可以使用人工基因合成。编码多肽的基因可以通过例如固相dna合成法合成产生。整个基因可以从头合成,不需要前体模板dna。为了获得所需的寡核苷酸,将构建块(building block)按产物序列所需的顺序依序偶联到不断增长的寡核苷酸链上。在链组装完成后,将产物从固相释放到溶液中,进行脱保护并进行收集。产物可以通过高效液相色谱法(hplc)分离,以获得高纯度的所需寡核苷酸。
[0420]
表达载体包括例如质粒、逆转录病毒、粘粒、酵母人工染色体(yac)和爱泼斯坦-巴尔病毒(ebv)来源的附加体。将多核苷酸连结到载体中,以使得该载体中的转录和翻译控制序列发挥它们的调控多核苷酸的转录和翻译的预期功能。表达和/或控制序列可以包括启动子、增强子、转录终止子、编码序列5
′
的起始密码子(即atg)、内含子的剪接信号和终止密码子。该表达载体和表达控制序列被选择为与所用表达宿主细胞相容。因此,还描述了编码根据seq id no:163-185中的任一个的单链可变片段的核苷酸序列,其包含通过合成接头(编码seq id no:186)联接的vh区和vl区。应当理解,本文所述的多核苷酸或表达载体可以包含vh区、vl区或两者(任选地包括接头)。因此,可以将编码vh区和vl区的多核苷酸插入到
单独的载体中,可替代地将编码这两个区的序列插入到同一表达载体中。通过标准方法将一种或多种多核苷酸插入到表达载体中(例如,连结多核苷酸和载体上的互补限制性位点,或者如果不存在限制性位点,则进行平端连接)。
[0421]
方便的载体是编码功能完全的人ch或cl免疫球蛋白序列的载体,其中的适当限制性位点被工程改造成使得任何vh或vl序列都可以容易地插入和表达,如本文所述。表达载体还可以编码促进抗体(或其片段)从宿主细胞分泌的信号肽。可以将多核苷酸克隆到该载体中,以使得信号肽与抗体的氨基端框内连接。信号肽可以是免疫球蛋白信号肽或异源信号肽(即,来自非免疫球蛋白的信号肽)。
[0422]
宿主细胞可以包含编码抗体或其片段的轻链的第一载体,和编码抗体或其片段的重链的第二载体。可替代地,该重链和轻链都可以在被引入到宿主细胞中的同一表达载体上被编码。
[0423]
在一个实施方案中,该多核苷酸或表达载体编码与抗体或其片段融合的膜锚或跨膜结构域,其中抗体或其片段被呈递在宿主细胞的细胞外表面上。
[0424]
可以通过任何已知的用于将多核苷酸引入到宿主细胞中的方法进行转化。用于将异源多核苷酸引入到哺乳动物细胞中的方法是本领域熟知的,并且包括葡聚糖介导的转染、磷酸钙沉淀、聚凝胺介导的转染、原生质体融合、电穿孔、转导、一种或多种多核苷酸在脂质体中的包封、基因枪注射和dna直接显微注射到细胞核中。另外,核酸分子可以通过病毒载体引入到哺乳动物细胞中。
[0425]
可用作宿主进行表达的哺乳动物细胞系在本领域中是熟知的,并且包括许多可从美国模式培养物保藏中心(atcc)获得的永生化细胞系。这些细胞系尤其包括中国仓鼠卵巢(cho)细胞、nso、sp2细胞、hela细胞、幼仓鼠肾(bhk)细胞、猴肾细胞(cos)、人肝细胞癌细胞(例如,hep g2)、a549细胞、3t3细胞和许多其它细胞系。哺乳动物宿主细胞包括人、小鼠、大鼠、狗、猴、猪、山羊、牛、马和仓鼠细胞。通过确定哪些细胞系具有高表达水平来选择特别优选的细胞系。可以使用的其它细胞系是昆虫细胞系(诸如sf9细胞)、两栖动物细胞、细菌细胞、植物细胞和真菌细胞。可以使用本领域已知的方法在大肠杆菌中分离和表达抗体的抗原结合片段,诸如scfv和fv片段。
[0426]
通过培养宿主细胞一段足以允许抗体在宿主细胞中表达,或更优选地抗体分泌到宿主细胞在其中生长的培养基中的时间来产生抗体。可以使用标准的蛋白质纯化方法从培养基中回收抗体。
[0427]
本文所述的抗体(或片段)可以使用例如green和sambrook,molecular cloning:a laboratory manual(2012)第4版cold spring harbour laboratory press中公开的技术获得和操纵。
[0428]
可以使用杂交瘤技术通过将产生抗体的特定b细胞与骨髓瘤(b细胞癌)细胞融合来产生单克隆抗体,该骨髓瘤细胞是因其在组织培养中生长的能力和不存在抗体链合成而被选择。
[0429]
针对确定的抗原的单克隆抗体可以例如通过如下方式获得:
[0430]
a)用永生细胞且优选用骨髓瘤细胞使从先前用确定的抗原免疫的动物的外周血中获得的淋巴细胞永生化,以便形成杂交瘤,
[0431]
b)培养形成的永生化细胞(杂交瘤)并回收产生具有所需特异性的抗体的细胞。
[0432]
可替代地,不需要使用杂交瘤细胞。可以经由常规实践,例如使用本领域已知的噬菌体展示、酵母展示、核糖体展示或哺乳动物展示技术,从合适的抗体文库中分离出能够与如本文所述的靶抗原结合的抗体。因此,单克隆抗体可以例如通过包括以下步骤的工艺获得:
[0433]
a)将从淋巴细胞,尤其是动物(适当地先前用确定的抗原免疫)的外周血淋巴细胞获得的dna或cdna序列克隆到载体,尤其是噬菌体且更特别是丝状噬菌体中,
[0434]
b)在允许抗体产生的条件下用上述载体转化原核细胞,
[0435]
c)通过使抗体经受抗原亲和力选择来对抗体进行选择,
[0436]
d)回收具有所需特异性的抗体。
[0437]
药物组合物
[0438]
根据本发明的进一步方面,提供了一种包含通过如本文所限定的方法获得的vγ4t细胞群体的组合物。在一个实施方案中,vγ4t细胞群体是扩增的vγ4t细胞群体。在此类实施方案中,该组合物可以包含任选地与其它赋形剂组合的细胞。还包括包含一种或多种额外的活性剂(例如适用于治疗本文提及的疾病的活性剂)的组合物。
[0439]
药物组合物可以包含与一种或多种药学上或生理上可接受的载剂、稀释剂或赋形剂组合的如本文所述的vγ4t细胞,尤其是扩增的vγ4t细胞。此类组合物可以包含缓冲剂,诸如中性缓冲盐水、磷酸盐缓冲盐水等;碳水化合物,诸如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇;蛋白质;多肽或氨基酸,诸如甘氨酸;抗氧化剂;螯合剂,诸如edta或谷胱甘肽;佐剂(例如,氢氧化铝);和防腐剂。可用于本发明的药物组合物中的冷冻保存溶液包括例如dmso。可以配制组合物,例如用于静脉内施用。
[0440]
在一个实施方案中,药物组合物实质上不含,例如,没有可检测水平的污染物,例如,内毒素或支原体。
[0441]
优选的施用模式是肠胃外(例如,静脉内、皮下、腹膜内、肌肉内、鞘内)。在一个优选实施方案中,该组合物通过静脉输注或注射施用。在另一个优选实施方案中,该组合物通过肌肉内或皮下注射施用。
[0442]
将本发明的药物组合物作为通常用于治疗如本文所述的疾病的其它确立的疗法的辅助或者与该其它确立的疗法联合用于治疗此类疾病的治疗方法中是在本发明的范围内。
[0443]
在本发明的进一步方面,该细胞群体、组合物或药物组合物与至少一种活性剂依序、同时或单独施用。
[0444]
使用细胞群体的治疗方法
[0445]
根据本发明的进一步方面,提供了通过如本文所限定的方法获得的细胞群体,其用作药物。根据本发明的进一步方面,提供了如本文所限定的扩增的细胞群体,其用作药物。本文对细胞群体“用”作药物或用于疗法中的提及限于将细胞群体施用于受试者。此类用途不包括将抗体或其片段直接施用于患者,即其中所述抗体被用作治疗剂。
[0446]
在一个实施方案中,该细胞群体用于治疗癌症、传染性疾病或炎性疾病。在进一步的实施方案中,该细胞群体用于治疗癌症。
[0447]
在一个实施方案中,用作药物的细胞群体包含超过50%的vγ4t细胞,诸如超过60%、超过70%、超过80%、超过90%、超过95%或超过99%的vγ4t细胞。在进一步的实施
方案中,用作药物的细胞群体由vγ4t细胞组成。
[0448]
根据本发明的进一步方面,提供了包含如本文所限定的细胞群体的药物组合物,其用作药物。在一个实施方案中,包含细胞群体的药物组合物用于疗法中,特别是用于治疗癌症、传染性疾病或炎性疾病。在进一步的实施方案中,包含细胞群体的药物组合物用于治疗癌症。
[0449]
根据本发明的进一步方面,提供了调节有需要的受试者中的免疫反应的方法,其包括施用治疗有效量的如本文限定的细胞群体。
[0450]
根据本发明的进一步方面,提供了治疗有需要的受试者中的癌症、传染性疾病或炎性疾病的方法,其包括施用治疗有效量的如本文所限定的细胞群体。可替代地,施用治疗有效量的包含细胞群体的药物组合物。
[0451]
根据本发明的进一步方面,提供了如本文限定的细胞群体用于制造药物,例如用于治疗癌症、传染性疾病或炎性疾病的药物的用途。
[0452]
过继性t细胞疗法
[0453]
通过本发明的扩增方法获得的γδt细胞可以用作药物,例如用作用于过继性t细胞疗法的药物。这涉及将γδt细胞转移到患者体内。该疗法可以是自体的,即γδt细胞可以被转移回它们所获自的同一患者体内,或者该疗法可以是同种异体的,即来自一个人的γδt细胞可以被转移到不同的患者体内。在涉及同种异体转移的情况下,γδt细胞可以实质上不含αβt细胞。例如,可例如在扩增之后使用本领域已知的任何合适的手段(例如,通过负选择,例如使用磁珠)来使αβt细胞从γδt细胞群体中耗尽。一种治疗方法可以包括:提供从供体个体获得的样品(例如非造血组织样品);培养从如本文所述的样品中获得的γδt细胞,例如以产生扩增的群体;以及将γδt细胞群体施用给受者个体。
[0454]
待治疗的患者或受试者优选为人类癌症患者(例如,正在治疗实体瘤的人类癌症患者)或病毒感染患者(例如,cmv感染患者或hiv感染患者)。在一些情况下,患者患有和/或正在治疗实体瘤。因为它们通常驻留在非造血组织中,所以组织驻留的vγ4t细胞也比其全身血液驻留的对应物更有可能归巢并保留在肿瘤块内,并且这些细胞的过继转移可能更有效地靶向实体瘤和潜在的其它非造血组织相关免疫病理。
[0455]
由于γδt细胞是非mhc限制的,它们不能将它们所转移到的宿主识别为外来的,这意味着它们不太可能引起移植物抗宿主疾病。这意味着它们可以“现成(off the shelf)”使用并转移到任何受者中,例如,用于同种异体过继性t细胞疗法。
[0456]
通过本文所述的方法获得的γδt细胞可以表达nkg2d并对nkg2d配体(例如mica)作出反应,该配体与恶性肿瘤密切相关。它们还可以在不存在任何激活的情况下表达细胞毒性谱,并且因此可能有效地杀伤肿瘤细胞。例如,如本文所述获得的γδt细胞可以在不存在任何激活的情况下表达ifn-γ、tnf-α、gm-csf、ccl4、il-13、粒溶素、颗粒酶a和b以及穿孔素中的一种或多种,优选全部。il-17a可能不被表达。
[0457]
在一些实施方案中,患有肿瘤的个体的治疗方法可以包括:提供从供体个体获得的所述肿瘤的样品,培养从如上所述的样品获得的γδt细胞;以及将γδt细胞群体施用给患有肿瘤的个体。在进一步的实施方案中,非造血组织中具有肿瘤的个体的治疗方法可以包括:提供从供体个体获得的所述非造血组织的样品,培养从如上所述的样品获得的γδt细胞;以及将γδt细胞群体施用给患有肿瘤的个体。
[0458]
在一些情况下,可以将治疗有效量的通过上述任何方法获得的γδt细胞以治疗有效量施用给受试者(例如,用于治疗癌症,例如用于治疗实体瘤)。在一些情况下,γδt细胞(例如,vγ4t细胞)的治疗有效量小于10x10
12
个细胞/剂(例如,小于9x10
12
个细胞/剂、小于8x10
12
个细胞/剂、小于7x10
12
个细胞/剂、小于6x10
12
个细胞/剂、小于5x10
12
个细胞/剂、小于4x10
12
个细胞/剂、小于3x10
12
个细胞/剂、小于2x10
12
个细胞/剂、小于1x10
12
个细胞/剂、小于9x10
11
个细胞/剂、小于8x10
11
个细胞/剂、小于7x10
11
个细胞/剂、小于6x10
11
个细胞/剂、小于5x10
11
个细胞/剂、小于4x10
11
个细胞/剂、小于3x10
11
个细胞/剂、小于2x10
11
个细胞/剂、小于1x10
11
个细胞/剂、小于9x10
10
个细胞/剂、小于7.5x10
10
个细胞/剂、小于5x10
10
个细胞/剂、小于2.5x10
10
个细胞/剂、小于1x10
10
个细胞/剂、小于7.5x109个细胞/剂、小于5x109个细胞/剂、小于2.5x109个细胞/剂、小于1x109个细胞/剂、小于7.5x108个细胞/剂、小于5x108个细胞/剂、小于2,5x108个细胞/剂、小于1x108个细胞/剂、小于7.5x107个细胞/剂、小于5x107个细胞/剂、小于2,5x107个细胞/剂、小于1x107个细胞/剂、小于7.5x106个细胞/剂、小于5x106个细胞/剂、小于2,5x106个细胞/剂、小于1x106个细胞/剂、小于7.5x105个细胞/剂、小于5x105个细胞/剂、小于2,5x105个细胞/剂或小于1x105个细胞/剂)。
[0459]
在一些实施方案中,γδt细胞(例如vγ4t细胞)的治疗有效量在治疗过程中小于10x10
12
个细胞(例如,在治疗过程中小于9x10
12
个细胞、小于8x10
12
个细胞、小于7x10
12
个细胞、小于6x10
12
个细胞、小于5x10
12
个细胞、小于4x10
12
个细胞、小于3x10
12
个细胞、小于2x10
12
个细胞、小于1x10
12
个细胞、小于9x10
11
个细胞、小于8x10
11
个细胞、小于7x10
11
个细胞、小于6x10
11
个细胞、小于5x10
11
个细胞、小于4x10
11
个细胞、小于3x10
11
个细胞、小于2x10
11
个细胞、小于1x10
11
个细胞、小于9x10
10
个细胞、小于7.5x10
10
个细胞、小于5x10
10
个细胞、小于2.5x10
10
个细胞、小于1x10
10
个细胞、小于7.5x109个细胞、小于5x109个细胞、小于2.5x109个细胞、小于1x109个细胞、小于7.5x108个细胞、小于5x108个细胞、小于2.5x108个细胞、小于1x108个细胞、小于7.5x107个细胞、小于5x107个细胞、小于2.5x107个细胞、小于1x107个细胞、小于7.5x106个细胞、小于5x106个细胞、小于2.5x106个细胞、小于1x106个细胞、小于7.5x105个细胞、小于5x105个细胞、小于2.5x105个细胞或小于1x105个细胞)。
[0460]
在一些实施方案中,如本文所述的γδt细胞(例如,vγ4t细胞)的剂量包括约1x106、1.1x106、2x106、3.6x106、5x106、1x107、1.8x107、2x107、5x107、1x108、2x108或5x108个细胞/千克。在一些实施方案中,γδt细胞(例如,vγ4t细胞)的剂量包括最多约1x106、1.1x106、2x106、3.6x106、5x106、1x107、1.8x107、2x107、5x107、1x108、2x108或5x108个细胞/千克。在一些实施方案中,γδt细胞(例如,vγ4t细胞)的剂量包括约1.1x10
6-1.8x107个细胞/千克。在一些实施方案中,γδt细胞(例如,vγ4t细胞)的剂量包括约1x107、2x107、5x107、1x108、2x108、5x108,1x109、2x109或5x109个细胞。在一些实施方案中,γδt细胞(例如,vγ4t细胞)的剂量包括至少约1x107、2x107、5x107、1x108、2x108、5x108、1x109、2x109或5x109个细胞。在一些实施方案中,γδt细胞(例如,vγ4t细胞)的剂量包括最多约1x107、2x107、5x107、1x108、2x108、5x108、1x109、2x109或5x109个细胞。
[0461]
在一个实施方案中,向受试者施用104至106个γδt细胞(例如,vγ4t细胞)/kg受试者体重。在一个实施方案中,受试者接受初始施用γδt细胞群体(例如,初始施用104至106个γδt细胞/千克受试者体重,例如,104至105个γδt细胞/千克受试者体重),以及一次或多次(例如2、3、4或5次)后续施用γδt细胞(例如,一次或多次后续施用104至106个γδt细胞/千
克受试者体重,例如,104至105个γδt细胞/千克受试者体重)。在一个实施方案中,该一次或多次后续施用在前一次施用后少于15天,例如14、13、12、11、10、9、8、7、6、5、4、3或2天,例如在前一次施用后少于4、3或2天施用。在一个实施方案中,受试者在至少三次γδt细胞群体施用的过程中接受总共约106个γδt细胞/千克受试者体重,例如,受试者接受1x105个γδt细胞的初始剂量,3x105个γδt细胞的第二次施用和6x105个γδt细胞的第三次施用,并且例如,每次施用在前一次施用后少于4、3或2天施用。
[0462]
在一些实施方案中,向受试者施用一种或多种额外的治疗剂。额外的治疗剂可以选自由免疫治疗剂、细胞毒剂、生长抑制剂、放射治疗剂、抗血管生成剂或这些中的两种或更多种剂的组合组成的组。额外的治疗剂可以在施用γδt细胞同时、之前或之后施用。额外的治疗剂可以是可作用于受试者身体内的靶标(例如,受试者自身的免疫系统)和/或作用于转移的γδt细胞的免疫治疗剂。
[0463]
组合物的施用可以任何方便的方式进行。本文所述的组合物可以经动脉、皮下地、皮内地、瘤内地、结节内地、髓内地、肌内地、通过静脉内注射或腹膜内地,例如通过皮内或皮下注射施用于患者。γδt细胞的组合物可以直接注射到肿瘤、淋巴结或感染部位中。
[0464]
基因工程改造
[0465]
通过本发明的方法获得的γδt细胞也可以被基因工程改造以获得增强的治疗特性,诸如用于嵌合抗原受体t细胞(car-t)疗法的增强的治疗特性。这涉及生成经工程改造的t细胞受体(tcr),以重新编程具有新特异性,例如单克隆抗体的特异性的t细胞。经工程改造的tcr可以使t细胞对恶性细胞具有特异性,并且因此可用于癌症免疫疗法。例如,t细胞可以识别表达肿瘤抗原,诸如不被来自受试者组织的正常体细胞表达的肿瘤相关抗原的癌细胞。因此,car修饰的t细胞可被用于例如癌症患者的过继性t细胞疗法。
[0466]
抗体或其片段的其它用途
[0467]
根据本发明的进一步方面,提供了如本文所述的抗vγ4抗体或其片段用于研究γδt细胞(尤其是vγ4t细胞)的抗原识别、激活、信号转导或功能的用途。如本文所述,该抗体已被证明在可用于探究γδt细胞功能的测定中具有活性。此类抗体还可用于诱导γδt细胞的增殖,因此可被用于扩增γδt细胞(诸如vγ4t细胞)的方法中。
[0468]
与vγ4链结合的抗体可被用于检测γδt细胞。例如,可将该抗体用可检测标记或报告分子标记或用作捕获配体,以选择性地检测和/或分离样品中的vγ4t细胞。标记的抗体可用于本领域已知的许多方法,例如免疫组织化学和elisa。
[0469]
可检测标记或报告分子可以是放射性同位素,诸如3h、
14
c、
32
p、
35
s或
125
l;荧光或化学发光部分诸如异硫氰酸荧光素或罗丹明;或酶诸如碱性磷酸酶、β-半乳糖苷酶、辣根过氧化物酶或萤光素酶。施加于本发明抗体的荧光标记然后可被用于荧光激活细胞分选(facs)方法中。
[0470]
应当理解,本文描述的所有实施方案都可以适用于本发明的所有方面。
[0471]
条款
[0472]
定义本发明及其优选方面的一组条款如下:
[0473]
1.一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗体或其片段,所述抗体或其片段与γδt细胞受体(tcr)的vγ4链特异性地结合而不与γδtcr的γ可变2(vγ2)链特异性地结合。
no:107的序列的cdr1。
[0505]
30.如条款12至25中任一项所限定的方法,其中所述抗体或其片段包含vl区,所述vl区包含:包含seq id no:40的序列的cdr3、包含序列:a16的序列的cdr2和包含seq id no:109的序列的cdr1。
[0506]
31.如条款12至25中任一项所限定的方法,其中所述抗体或其片段包含vl区,所述vl区包含:包含seq id no:42的序列的cdr3、包含序列:a18的序列的cdr2和包含seq id no:111的序列的cdr1。
[0507]
32.如条款12至25中任一项所限定的方法,其中所述抗体或其片段包含vl区,所述vl区包含:包含seq id no:46的序列的cdr3、包含序列:a23的序列的cdr2和包含seq id no:115的序列的cdr1。
[0508]
33.一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗vγ4抗体或其片段,所述抗vγ4抗体或其片段包含与seq id no:117-162或261-283中的任一个具有至少80%序列同一性的氨基酸序列。
[0509]
34.如条款33所限定的方法,其中所述抗体或其片段包含vh区,该vh区包含与seq id no:117-139中的任一个具有至少80%序列同一性的氨基酸序列。
[0510]
35.如条款34所限定的方法,其中所述vh区包含与seq id no:125、119、129、130、132、134或138中的任一个具有至少80%序列同一性的氨基酸序列。
[0511]
36.如条款33至35中任一项所限定的方法,其中所述抗体或其片段包含vl区,所述vh区包含与seq id no:140-162或261-283中的任一个具有至少80%序列同一性的氨基酸序列。
[0512]
37.如条款36所限定的方法,其中所述vl区包含与以下的任一者具有至少80%序列同一性的氨基酸序列:
[0513]
(a)seq id no:148、142、152、153、155、157或161;或
[0514]
(b)seq id no:269、263、273、274、276、278或282。
[0515]
38.如条款33至37中任一项所限定的方法,其中所述抗体或其片段包含vh区,所述vh区包含seq id no:125的氨基酸序列;和vl区,所述vl区包含seq id no:148或269的氨基酸序列。
[0516]
39.如条款33至37中任一项所限定的方法,其中所述抗体或其片段包含vh区,所述vh区包含seq id no:119的氨基酸序列;和vl区,所述vl区包含seq id no:142或263的氨基酸序列。
[0517]
40.如条款33至37中任一项所限定的方法,其中所述抗体或其片段包含vh区,所述vh区包含seq id no:129的氨基酸序列;和vl区,所述vl区包含seq id no:152或273的氨基酸序列。
[0518]
41.如条款33至37中任一项所限定的方法,其中所述抗体或其片段包含vh区,所述vh区包含seq id no:130的氨基酸序列;和vl区,所述vl区包含seq id no:153或274的氨基酸序列。
[0519]
42.如条款33至37中任一项所限定的方法,其中所述抗体或其片段包含vh区,所述vh区包含seq id no:132的氨基酸序列;和vl区,所述vl区包含seq id no:155或276的氨基酸序列。
no:25的lcdr3,任选地其中所述vl包含seq id no:140或261;
[0539]
(i)vh,其包含具有seq id no:72的hcdr1、具有seq id no:49的hcdr2和具有seq id no:3的hcdr3,任选地其中所述vh包含seq id no:118;和
[0540]
vl,其包含具有seq id no:95的lcdr1、具有序列a2(图1)的lcdr2和具有seq id no:26的lcdr3,任选地其中所述vl包含seq id no:141或262;
[0541]
(j)vh,其包含具有seq id no:74的hcdr1、具有seq id no:51的hcdr2和具有seq id no:5的hcdr3,任选地其中所述vh包含seq id no:120;和
[0542]
vl,其包含具有seq id no:97的lcdr1、具有序列a4(图1)的lcdr2和具有seq id no:28的lcdr3,任选地其中所述vl包含seq id no:143或264;
[0543]
(k)vh,其包含具有seq id no:75的hcdr1、具有seq id no:52的hcdr2和具有seq id no:6的hcdr3,任选地其中所述vh包含seq id no:121;和
[0544]
vl,其包含具有seq id no:98的lcdr1、具有序列a5(图1)的lcdr2和具有seq id no:29的lcdr3,任选地其中所述vl包含seq id no:144或265;
[0545]
(l)vh,其包含具有seq id no:76的hcdr1、具有seq id no:53的hcdr2和具有seq id no:7的hcdr3,任选地其中所述vh包含seq id no:122;和
[0546]
vl,其包含具有seq id no:99的lcdr1、具有序列a6(图1)的lcdr2和具有seq id no:30的lcdr3,任选地其中所述vl包含seq id no:145或266;
[0547]
(m)vh,其包含具有seq id no:77的hcdr1、具有seq idno:54的hcdr2和具有seq id no:8的hcdr3,任选地其中所述vh包含seq id no:123;和
[0548]
vl,其包含具有seq id no:100的lcdr1、具有序列a7(图1)的lcdr2和具有seq id no:31的lcdr3,任选地其中所述vl包含seq id no:146或267;
[0549]
(n)vh,其包含具有seq id no:78的hcdr1、具有seq id no:55的hcdr2和具有seq id no:9的hcdr3,任选地其中所述vh包含seq id no:124;和
[0550]
vl,其包含具有seq id no:101的lcdr1、具有序列a8(图1)的lcdr2和具有seq id no:32的lcdr3,任选地其中所述vl包含seq id no:147或268;
[0551]
(o)vh,其包含具有seq id no:80的hcdr1、具有seq id no:57的hcdr2和具有seq id no:11的hcdr3,任选地其中所述vh包含seq id no:126;和
[0552]
vl,其包含具有seq id no:103的lcdr1、具有序列a10(图1)的lcdr2和具有seq id no:34的lcdr3,任选地其中所述vl包含seq id no:149或270;
[0553]
(p)vh,其包含具有seq id no:81的hcdr1、具有seq id no:58的hcdr2和具有seq id no:12的hcdr3,任选地其中所述vh包含seq id no:127;和
[0554]
vl,其包含具有seq id no:104的lcdr1、具有序列a11(图1)的lcdr2和具有seq id no:35的lcdr3,任选地其中所述vl包含seq id no:150或271;
[0555]
(q)vh,其包含具有seq id no:82的hcdr1、具有seq id no:59的hcdr2和具有seq id no:13的hcdr3,任选地其中所述vh包含seq id no:128;和
[0556]
vl,其包含具有seq id no:105的lcdr1、具有序列a12(图1)的lcdr2和具有seq id no:36的lcdr3,任选地其中所述vl包含seq id no:151或272;
[0557]
(r)vh,其包含具有seq id no:85的hcdr1、具有seq id no:62的hcdr2和具有seq id no:16的hcdr3,任选地其中所述vh包含seq id no:131;和
[0558]
vl,其包含具有seq id no:108的lcdr1、具有序列a15(图1)的lcdr2和具有seq id no:39的lcdr3,任选地其中所述vl包含seq id no:154或275;
[0559]
(s)vh,其包含具有seq id no:87的hcdr1、具有seq id no:64的hcdr2和具有seq id no:18的hcdr3,任选地其中所述vh包含seq id no:133;和
[0560]
vl,其包含具有seq id no:110的lcdr1、具有序列a17(图1)的lcdr2和具有seq id no:41的lcdr3,任选地其中所述vl包含seq id no:156或277;
[0561]
(t)vh,其包含具有seq id no:89的hcdr1、具有seq id no:66的hcdr2和具有seq id no:20的hcdr3,任选地其中所述vh包含seq id no:135;和
[0562]
vl,其包含具有seq id no:112的lcdr1、具有序列a19(图1)的lcdr2和具有seq id no:43的lcdr3,任选地其中所述vl包含seq id no:158或279;
[0563]
(u)vh,其包含具有seq id no:90的hcdr1、具有seq id no:67的hcdr2和具有seq id no:21的hcdr3,任选地其中所述vh包含seq id no:136;和
[0564]
vl,其包含具有seq id no:113的lcdr1、具有序列a20(图1)的lcdr2和具有seq id no:44的lcdr3,任选地其中所述vl包含seq id no:159或280;
[0565]
(v)vh,其包含具有seq id no:91的hcdr1、具有seq id no:68的hcdr2和具有seq id no:22的hcdr3,任选地其中所述vh包含seq id no:137;和
[0566]
vl,其包含具有seq id no:114的lcdr1、具有序列a21(图1)的lcdr2和具有seq id no:45的lcdr3,任选地其中所述vl包含seq id no:160或281;
[0567]
和/或
[0568]
(w)vh,其包含具有seq id no:93的hcdr1、具有seq id no:70的hcdr2和具有seq id no:24的hcdr3,任选地其中所述vh包含seq id no:139;和
[0569]
vl,其包含具有seq id no:116的lcdr1、具有序列a23(图1)的lcdr2和具有seq id no:47的lcdr3,任选地其中所述vl包含seq id no:162或283。
[0570]
46.如条款33至45中任一项所限定的方法,其中所述vh区和vl区通过接头诸如多肽接头联接。
[0571]
47.如条款46所限定的方法,其中所述接头包含(gly4ser)n格式,其中n=1至8。
[0572]
48.如条款46或47所限定的方法,其中所述接头包含seq id no:186。
[0573]
49.如条款48所限定的方法,其中所述接头由seq id no:186组成。
[0574]
50.一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗vγ4抗体或其片段,所述抗vγ4抗体或其片段包含与seq id no:163-185中的任一个具有至少80%序列同一性的氨基酸序列。
[0575]
51.如条款50所限定的方法,其中所述抗体或其片段包含seq id no:163-185中的任一个的氨基酸序列。
[0576]
52.如条款50或条款51所限定的方法,其中所述抗体或其片段包含seq id no:171、165、175、176、178、180或184。
[0577]
53.一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗vγ4抗体或其片段,所述抗vγ4抗体或其片段包含与seq id no:233-255中的任一个具有至少80%序列同一性的氨基酸序列。
[0578]
54.如条款53所限定的方法,其包含seq id no:233-255中的任一个的氨基酸序
列。
[0579]
55.如条款53或条款54所限定的方法,其包含seq id no:235、241、245、246或254。
[0580]
56.一种调节γ可变4(vγ4)t细胞的离体方法,所述方法包括向包含vγ4t细胞的细胞群体施用抗vγ4抗体或其片段,所述抗vγ4抗体或其片段包含与seq id no:284-306中的任一个具有至少80%序列同一性的重链氨基酸序列和/或与seq id no:307-329中的任一个具有至少80%序列同一性的轻链氨基酸序列。
[0581]
57.如条款56所限定的方法,其包括包含seq id no:284-306中的任一个的重链氨基酸序列和/或包含seq id no:307-329中的任一个的轻链氨基酸序列。
[0582]
58.如条款1-11中任一项所限定的方法,其中所述抗vγ4抗体或其片段与如条款12-57中任一项所限定的抗体或其片段结合相同或基本上相同的表位,或者与如条款12-57中任一项所限定的抗体或其片段竞争。
[0583]
59.如条款1-58中任一项所限定的方法,其中所述抗体或其片段是scfv、fab、fab
′
、f(ab
′
)2、fv、可变结构域(例如vh或vl)、双抗体、微型抗体或全长抗体。
[0584]
60.如条款59所限定的方法,其中所述抗体或其片段是scfv或全长抗体。
[0585]
61.如条款60所限定的方法,其中所述抗体或其片段是全长抗体,诸如igg1抗体。
[0586]
62.如条款1-61中任一项所限定的方法,其中所述抗体或其片段是人的。
[0587]
63.如权利要求1至62中任一项所限定的方法,其中所述调节包括扩增vγ4t细胞。
[0588]
64.如权利要求63所限定的方法,其中所述方法提供vγ4t细胞的扩增群体,所述扩增群体含有大于约60%的vγ4t细胞,诸如大于约70%的vγ4t细胞。
[0589]
65.如权利要求1至64中任一项所限定的方法,其中所述方法包括培养所述细胞群体至少5天。
[0590]
66.如权利要求1至65中任一项所限定的方法,其中所述方法包括在至少一种细胞因子的存在下培养所述细胞群体。
[0591]
67.如权利要求66所限定的方法,其中所述细胞因子选自:白细胞介素2(il-2)、白细胞介素4(il-4)、白细胞介素7(il-7)、白细胞介素9(il-9)、白细胞介素12(il-12)、白细胞介素15(il-15)、白细胞介素21(il-21)或它们的混合物。
[0592]
68.如权利要求1至67中任一项所限定的方法,其中所述方法包括在il-2和/或il-15的存在下培养所述细胞群体。
[0593]
69.如权利要求65至68中任一项所限定的方法,其中所述细胞群体在培养期间不与基质细胞和/或上皮细胞直接接触。
[0594]
70.如权利要求69所限定的方法,其中所述细胞群体在培养期间不与成纤维细胞直接接触。
[0595]
71.如权利要求65至70中任一项所限定的方法,其中所述细胞群体在培养期间不与肿瘤细胞和/或饲养细胞直接接触。
[0596]
72.如权利要求1至71中任一项所限定的方法,其中所述方法包括在无血清培养基中培养所述细胞群体。
[0597]
73.如权利要求1至72中任一项所限定的方法,其中在施用所述抗体或其片段之前使所述细胞群体富集t细胞。
[0598]
74.如权利要求1至73中任一项所限定的方法,其中在施用所述抗体或其片段之前
使所述细胞群体富集γδt细胞。
[0599]
75.如权利要求1至74中任一项所限定的方法,其中在施用所述抗体或其片段之前使所述细胞群体耗尽αβt细胞或nk细胞。
[0600]
76.如权利要求1至75中任一项所限定的方法,其中所述细胞群体是从造血样品或其级分中获得的。
[0601]
77.如权利要求76所限定的方法,其中所述造血样品选自外周血、脐带血、淋巴组织、胸腺、骨髓、淋巴结组织或其级分。
[0602]
78.如权利要求76或权利要求77所限定的方法,其中所述造血样品由外周血单核细胞(pbmc)或低密度单核细胞(ldmc)组成。
[0603]
79.如权利要求1至75中任一项所限定的方法,其中所述细胞群体是从非造血组织样品,诸如皮肤、结肠、肠道、乳腺、肺、前列腺、肝脏、脾脏、胰腺、子宫、阴道或其它皮肤、粘膜或浆膜样品获得的。
[0604]
80.如权利要求1至75中任一项所限定的方法,其中所述细胞群体是从癌组织样品获得的。
[0605]
81.如权利要求1至80中任一项所限定的方法,其中所述细胞群体是从人或非人动物组织获得的。
[0606]
82.如权利要求1至81中任一项所限定的方法,其中在施用所述抗vγ4抗体或其片段之前从样品中分离所述细胞群体。
[0607]
83.一种通过如权利要求1至82中任一项所限定的离体方法获得的vγ4t细胞群体。
[0608]
84.一种组合物,所述组合物包含如条款83所限定的vγ4t细胞群体。
[0609]
85.一种药物组合物,所述药物组合物包含如条款83所限定的vγ4t细胞群体连同药学上可接受的稀释剂或载剂。
[0610]
86.如条款85所限定的药物组合物,所述药物组合物用作药物。
[0611]
87.如条款86所限定的药物组合物,所述药物组合物用于治疗癌症、传染性疾病或炎性疾病。
[0612]
88.一种治疗有需要的受试者中的癌症、传染性疾病或炎性疾病的方法,所述方法包括施用治疗有效量的如条款83所限定的vγ4t细胞群体或如条款85所限定的药物组合物。
[0613]
本发明的其它特征和优点将从本文提供的描述中显而易见。然而应该理解,虽然描述和具体实施例示出本发明的优选实施方案,但它们仅通过举例说明的方式给出,因为各种变化和修改对于本领域的技术人员将变得显而易见。现在将使用以下非限制性实施例来描述本发明:
[0614]
实施例
[0615]
实施例1.材料和方法
[0616]
抗原制备
[0617]
下面实施例中使用的包含tcrα和tcrβ恒定区的可溶性yδtcr异二聚体的设计是根据xu等人(2011)pnas 108:2414-2419生成的。使vγ或vδ结构域与缺乏跨膜结构域的tcrα或tcrβ恒定区,随后是亮氨酸拉链序列或fc序列和组氨酸标签/接头框内融合。
[0618]
将表达构建体瞬时转染到哺乳动物expi hek293悬浮细胞中(作为用于异二聚体的单一转染或共转染)。通过亲和色谱法从培养物上清液中回收分泌的重组蛋白并且对其进行纯化。为了确保单体抗原的良好回收,使用制备型尺寸排阻色谱法(sec)进一步纯化样品。通过sds-page分析经纯化的抗原的纯度并通过分析型sec分析该抗原的聚集状态。
[0619]
使用可商购获得的质粒将选择的scfv亚克隆到igg1框架中。用所述质粒转染expi293f悬浮细胞以进行抗体表达。为方便起见,除非另有说明,否则这些实施例中表征的抗体是指作为scfv从噬菌体展示中选择的呈igg1格式的抗体。然而,所述抗体可以是如前所讨论的任何抗体格式。
[0620]
抗体纯化
[0621]
使用蛋白a色谱法从上清液中批量纯化igg抗体。使用elisa、sds-page和sec-hplc分析经纯化的igg的质量。
[0622]
抗原结合
[0623]
将噬菌体展示选择输出物亚克隆到scfv表达载体psang10(martin等人(2006)bmc biotechnol.6∶46)中。使可溶性scfv表达并且针对在解离增强的镧系荧光免疫测定(delfia)中在直接固定化靶标上的结合对该可溶性scfv进行筛选。命中物被定义为高于3000个荧光单位的delfia信号。
[0624]
还采用delfia elisa结合方法来评估抗体上清液或进一步的蛋白a纯化的抗体的结合。简言之,给maxisorp板涂覆3μg/ml的抗原bsa或l1(dv1-gv4)、l2(dv1-gv2)、l3(dv1-gv8)或l4(dv2-gv4)重组tcr抗原。然后将板用pbs洗涤,用pbs/脱脂乳封闭,然后添加试验品并在室温下孵育1小时。此后,将板用pbs-吐温洗涤并添加delfia eu-n1抗人igg(perkin elmer#1244-330)并在室温下保持1小时,然后进一步洗涤,添加delfia增强溶液(perkin elmer#4001-0010),并在pherastar酶标仪上读数。
[0625]
d1.3higg1(描述于england等人(1999)j.immunol.162:2129-2136)用作阴性对照,rea173(miltenyi)和ts8.2(thermofisher,编号tcr1730)用作比较器抗体。
[0626]
用重组jrt3-tcr细胞进行的抗体研究
[0627]
在抗体结合、tcr下调和cd69上调研究中采用的重组jrt3-tcr细胞先前有描述(参见melandri等人(2018)nature immunology 19(12):1352-1365,和willcox等人(2019)immunity 51(5):813-825.e4)。
[0628]
对于抗体结合研究,对100,000个未转导的jrt3对照或jrt3-tcr细胞的初步染色在4℃下在pbs 5%fcs中用标准的1.0μg/ml(如果在图6中未指示出量)或图6中指示的量(诸如0.08、0.4、2或10μg/m1)的每种主要抗体来进行,持续30分钟。然后用a647抗人igg(biolegend)进行二次染色。另外,如指示的那样/在指示的情况下进行bv421抗cd3ε(biolegend)或pe-cy7 immu510抗γδtcr(beckman coulter)染色。然后将细胞在pbs 5%fcs中洗涤两次并在facs canto ii 3l上进行流式分析。
[0629]
对于tcr下调/cd69上调研究,首先通过向每个孔中添加20μg/ml二抗,特别是抗人igg-fc(对于人d1.3和vγ4抗体而言)或抗小鼠igg(对于鼠抗cd3e或抗pan tcrgd而言)来预包被96孔板,然后将该板在37℃下孵育2小时。首先将如所指示的试验抗体稀释到0.01、0.1、1和10μg/ml的最终浓度。然后将每种浓度各50μl添加到预包被的板的孔中,之后在4℃下孵育过夜。然后用pbs洗涤未结合的抗体两次,之后添加饱和pbs 5%fcs并在37℃下保持
1小时。然后通过400g旋转接种100,000个细胞/孔。然后将细胞在37℃、5%co2下孵育5小时,然后转移到96孔圆底板上以进行染色。采用的染色抗体包括1:400稀释的bv421抗cd3ε(克隆okt-3biolegend);1:200稀释的pe-cy7抗γδtcr(克隆immu510beckman coulter);和1∶200稀释的a647抗cd69(克隆fn50 biolegend)。所有染色均在pbs5%fcs中在4℃下进行30分钟。
[0630]
用原代细胞(pbmc)进行的抗体研究
[0631]
首先通过向每个孔中添加20μg/ml(每孔250μl)抗人igg-fc(biolegend)来预先包被24孔板,然后将其在37℃下孵育2小时。用pbs洗涤未结合的二抗两次,并且将同种型对照(人igg1,biolegend)或抗vγ4(克隆g4_12)首先稀释到0.1、1和10μg/ml的最终浓度。然后将每种浓度250μl添加到预先包被的板的孔中,之后在4℃下孵育过夜。然后用pbs洗涤未结合的抗体两次,之后添加饱和pbs 5%fcs,在37℃下保持1小时。然后向每个孔中添加以106个细胞/ml重悬于完全培养基(补充有5%热灭活人ab血清[paa实验室]、丙酮酸钠[1mm]和青霉素/链霉素[thermofisher]的rpmi)中的500,000个pbmc。然后将细胞在37℃、5%co2下孵育。24小时后添加il-2或il-2+il-15(最终浓度分别为100u/ml和10ng/ml)并且每2-3天添加补充有il-2或il-2+il-15的新鲜完全培养基。在培养的第7天和第14天,将细胞转移到96孔圆底板中进行染色。采用的染色抗体包括稀释到1μg/ml的生物素抗tcrvγ2/3/4(克隆23d12)、1:100稀释的pe链霉亲和素(biolegend);1∶400稀释的bv421抗cd3ε(克隆okt-3biolegend);1∶200稀释的pe-cy7抗tcrγδ(克隆immu510 beckman coulter);fitc抗vδ2(克隆b6 biolegend);和稀释到1μg/ml的a647抗vγ4(克隆g4_18)。所有染色均在pbs 5%fcs中在4℃下进行30分钟。
[0632]
基于ms的表位作图
[0633]
采用covalx
‘
超快构象/线性表位作图’方法。首先使用高质量maldi分析蛋白质抗原l1(dv1-gv4)加抗体g4_3(1139_p01_a04)的蛋白质完整性和聚集水平。为了以高分辨率确定l1(dv1-gv4)/g4_3复合物的结合表位,将该复合物与氘代交联剂一起孵育,并使该复合物经受使用胰蛋白酶、糜蛋白酶、asp-n、弹性蛋白酶和嗜热菌蛋白酶进行的多酶蛋白水解。交联肽富集后,通过高分辨率质谱法(nlc-ltq-orbitrap ms)分析样品,并使用xquest和stavrox软件分析生成的数据。
[0634]
γδt细胞结合测定
[0635]
抗体与γδt细胞的结合可以通过将固定浓度的经纯化抗体与250000个γδt细胞一起孵育来测试。这种孵育可以在封闭条件下,诸如通过添加hufc片段或ig以阻止抗体经由fc受体的非特异性结合来执行。可以通过添加针对人igg1的荧光染料缀合的二抗来进行检测。对于阴性对照,可以用以下制备细胞:a)仅同种型抗体(重组人igg)、b)仅荧光染料缀合的抗人igg抗体和c)a)和b)的组合。还可以制备和分析完全未染色细胞的对照孔。作为阳性对照,可将经纯化的鼠单克隆igg2抗人cd3抗体以两种不同的浓度使用并用荧光染料缀合的山羊抗小鼠二抗染色。如果较低浓度的阳性对照在fitc通道中的平均荧光强度是最高阴性对照的至少10倍,则该测定可被接受。
[0636]
spr分析
[0637]
带有胺高容量芯片的mass-2仪器(均来自sierra sensors,germany)可被用于执行spr分析。15nm igg可经由蛋白g被捕获到胺高容量芯片(对于ts8.2而言为100nm)。可以
使l1(dv1-gv4)抗原以2000nm至15.625nm的1:2稀释系列以下列参数流过细胞:180秒缔合,600秒解离,流速30μl/min,运行缓冲液pbs+0.02%吐温20。所有实验均在室温下在mass-2仪器上执行。稳态拟合可根据langmuir 1∶1结合使用软件sierra analyzer 3.2进行确定。
[0638]
γδtcr下调和脱粒测定
[0639]
可将负载或未负载试验抗体的thp-1(tib-202
tm
,atcc)靶细胞用celltracker
tm
orange cmtmr(thermofisher,c2927)标记并与γδt细胞一起以2:1的比率在cd107a抗体(抗人cd107a bv421(克隆h4a3)bd biosciences 562623)的存在下孵育。孵育2小时后,可以使用流式细胞术评价γδt细胞上γδtcr的表面表达(以测量tcr下调)和cd107a的表达(以测量脱粒)。
[0640]
杀伤测定
[0641]
可以通过流式细胞术评估γδt细胞介导的杀伤活性和试验抗体对γδt细胞杀伤活性的影响。在体外共培养4小时后,可将20∶1比率的γδt细胞和celltracker
tm
orange cmtmr(thermofisher,c2927)标记的thp-1细胞(负载或未负载抗体)用活力染料efluor
tm
520(thermofisher,520 65-0867-14)染色以区分活的和死的靶thp-1细胞。在样品采集期间,可以根据celltracker
tm
orange cmtmr阳性对靶细胞进行门控,并基于活力染料的摄取情况检查该靶细胞的细胞死亡。cmtmr和efluor
tm
520双阳性细胞可被识别为死的靶细胞。γδt细胞的杀伤活性可作为死的靶细胞的%呈现。
[0642]
实施例2.抗原设计
[0643]
gamma delta(γδ)t细胞是具有cdr3多克隆性的多克隆细胞。为了避免针对cdr3序列来选择所生成的抗体的情形(因为cdr3序列将在tcr克隆与tcr克隆之间不同),抗原设计涉及以不同格式维持一致的cdr3。该设计旨在生成识别被种系编码并且因此在所有克隆中都相同的可变结构域内序列的抗体,从而提供识别更广泛的γδt细胞亚群的抗体。
[0644]
抗原制备过程的另一个重要方面是设计适合作为蛋白质表达的抗原。γδtcr是一种涉及具有链间和链内二硫键的异二聚体的复杂蛋白质。使用亮氨酸拉链(lz)格式和fc格式来生成待用于噬菌体展示选择的可溶性tcr抗原。lz和fc格式都表达良好并成功展示tcr(特别是异二聚体tcr,例如vδ1vγ4)。
[0645]
发现来自γδtcr的公共数据库条目的cdr3序列与蛋白质(rscb蛋白质数据库条目:4mnh)一样表达良好。因此选择这用于抗原制备。
[0646]
含有γ可变4链的抗原以lz格式表达为异二聚体(即与不同的δ可变链组合-例如dv1-gv4,其是一种由δ可变1链和γ可变4链组成的异二聚体,[称为“l1”];和dv2-gv4,由δ可变2链和γ可变4链组成的异二聚体,[称为“l4”]),并且以fc格式表达为异二聚体或表达为同型二聚体(即,与另一γ可变4链组合-gv4-gv4,其是一种由两条γ可变4链组成的同型二聚体,[称为“fc4/4”])。抗原的所有γ可变4链都含有4mnh cdr3。另一系列使用类似格式的γδtcr抗原被设计为含有不同的γ可变链(诸如γ可变2和γ可变8),并且被用于取消选择具有非特异性或脱靶结合的抗体(例如dv1-gv2,其是一种由δ可变1链和γ可变2链组成的异二聚体,[称为“l2”];或dv1-gv8,其是一种由δ可变1链和γ可变8链组成的异二聚体,[称为“l3”])。这些抗原还被设计为包括4mnh cdr3,以确保在cdr3区域结合中的抗体也被取消选择。
[0647]
实施例3.噬菌体展示
[0648]
在第1轮和第2轮中使用任一异二聚体lz tcr格式对人scfv文库执行噬菌体展示选择,在两轮中均取消选择异二聚体lz tcr。或者,使用同型二聚体fc融合tcr执行第1轮,并对人igg1 fc执行取消选择,接着对异二聚体lz tcr执行第2轮并对异二聚体lz tcr执行取消选择(参见表1)。
[0649]
表1.噬菌体展示选择综述
[0650][0651]
bt=生物素。
[0652]
选择在溶液相中使用100nm生物素化蛋白质执行。取消选择使用1μm非生物素化蛋白质执行。
[0653]
实施例4.抗体选择
[0654]
对实施例3中获得的命中物进行测序(使用本领域已知的标准方法)。鉴定了130个独特的克隆,其显示出vh和vl cdr3的独特组合。在这130个独特的克隆中,129个显示出独特的vh cdr3且116个显示出独特的vl cdr3。
[0655]
重新排列独特的克隆,并通过elisa(delfia)分析特异性。从该选择中鉴定出一组结合trgv4但不结合trgv2或trgv8的42种独特的人scfv结合物。
[0656]
纳入所选择的结合物的亲和力排名以帮助克隆的选择向前推进。大量结合物显示出纳摩尔范围的亲和力,从而与25至100nm的生物素化抗原(l1)反应。少量结合物显示出与5nm抗原的强烈反应,表明可能存在个位数的纳摩尔的亲和力。一些结合物没有显示出与100nm抗原的反应,表明亲和力在微摩尔范围中。
[0657]
对于对用于继续进行到igg转化的克隆的选择,目的是纳入尽可能多的种系谱系和尽可能多的不同cdr3。进一步地,避免了序列倾向,如糖基化、整联蛋白结合位点、cd11c/cd18结合位点、未配对的半胱氨酸。另外,还纳入了各种亲和力。所选择的待转化为igg的克隆在图1中示出。elisa结合的结果(值以荧光单位(fu)计)在图2a中示出。结果表明,所有23种抗体都表现出所需的γ4链特异性谱,而与伴侣δ链无关。相同的数据也表示在图2b中并且进一步显示每个克隆与人vγ4链的结合对比该克隆与人vγ2链的结合的倍数变化增加。与人vγ4链的结合对比与人vγ2链的结合的倍数变化增加在从80倍(克隆g4_26)到增加98387倍(克隆g4_18)的范围内。
[0658]
还使用重组urkat(jrt3-hu17)细胞进行抗体结合研究。elisa数据和流式细胞术数据的结果比较在图3a中示出。选择经由delfia elisa被鉴定为与dv1-gv4抗原(y轴)且与jrt3-hu17细胞(x轴)结合的抗体克隆用于进一步探究。
[0659]
实施例5.vγ4抗体结合的探究
[0660]
探究了实施例4中选择的抗体对带有不同cdr3序列(hu17对比hu20,均为vγ4vδ1)或δ链(hu20γ/hupbδ,vγ4vδ2;les,vγ4vδ5)的vγ4tcr染色的能力。结果如图4a所示并且表明所有测试的抗体显示出与研究中使用的一种或多种vγ4 tcr的结合相对于d1.3同种
型对照显著增加。具体而言,五种示例性抗体(g4_3、g4_12、g4_16、g4_18和g4_27)结合本研究中表达的所有vγ4tcr而与cdr3序列或伴侣δ链无关,表现出超越d1.3同种型对照的明显增强的结合信号。通过举例说明的方式,本研究中抗体中的两种抗体的示例流数据示于图4b中并且例示了g4_3结合(对于所有vγ4tcr而言染色呈阳性)与g4_4结合(对于hu17和les而言染色呈阳性,而针对hu20[与hu17相比不同的cdr3序列]和hu20g/hupbd[vγ4vδ2]的染色减少)之间的差异。
[0661]
实施例6.使用嵌合hu17 tcr的表位作图
[0662]
hu17是一种vγ4/vδ1tcr,其配对的cdr3序列是通过单细胞pcr从btnl3+8反应性人结肠上皮内淋巴细胞克隆的(如melandri等人(2018)nat.immunol.19:1352-1365中所述)。如图5a中汇总的那样制备不同的嵌合hu17 tcr构建体。这些构建体源自hu17并且全部在melandri等人(2018)nat.immunol.19:1352-1365和willcox等人(2019)immunity 51:813-825中有描述(两者均通过引用并入本文)。
[0663]
然后通过流式细胞术针对在jrt3细胞上表达的嵌合hu17 tcr探究抗体结合。每种抗体与所指示的嵌合tcr构建体的反应性的汇总表示于图5b中。结果强调了单个抗体对jrt3细胞上表达的单个tcr的相对结合特异性。抗体g43、g412、g416、g418和g427全部被指示为在hv4区域内或周围特异性地结合,因为当使用在hv4区域中含有vγ2序列的hu17 tcr构建体时未观察到染色或观察到染色减少。
[0664]
用于例示本研究中观察到的差异性结合信号的表位作图的示例流数据示于图5c中。在这种情况下,并且作为这种表位作图方法的实例,示出了g4_12与各种重组嵌合tcr的结合。首先,g4_12表现出与起始hu17 tcr的强烈结合(最左侧图)。当cdr1+2序列框内交换为vγ2等效cdr时(左中图)或当hu17经hv4修饰为vγ2序列dg>ya时(右中图),也观察到针对hu17的强烈结合。然而,在可替代的vγ4到vγ2的氨基酸取代(dgkm>yanl;中图)或km>nl(最右侧图)的情况下,分别观察到g4_12结合明显下降。因此在这种情况下,被g4_12识别的表位位于hv4区(seq id no.1的氨基酸67-82[kydtygstrknlrmil]),并且受到将带下划线的k和m残基修饰为在vγ2hv4区的该位置处发现的等效残基的严重影响。
[0665]
实施例7.染色和功能测定中对所探究抗体的滴定
[0666]
用于通过流式细胞术对jrt3-hu17细胞进行染色和分析的所探究抗体的滴定结果(浓度范围为0.08至10μg/ml,5倍稀释步骤)示于图6a中。未转导的jrt3细胞(无tcr)用作阴性对照。结果显示所有抗体都能够与表达vγ4tcr的jrt3细胞结合。
[0667]
然后通过探究经滴定的抗体引起的tcr转换和cd69上调与抗cd3ε结合或抗泛-tcrγδ抗体赋予的转换来进行功能测定。图6b和图6c中示出了其中五种抗体的结果并且表2中汇总了原始队列内更广泛的抗体选择的结果。
[0668]
表2.选定抗体的tcr下调和激活
[0669][0670]
表2中列出的所有抗体均已被证明与γδtcr的vγ4链结合。然而,如表中所示,这些抗体中的一些能够激活vγ4tcr,如经由vγ4tcr下调和/或cd69表达增加所度量的(指示为
‘
+’、
‘
++’或者
‘
+++’,其中
‘
+++’意指最高的相对激活水平),而其它抗体没有显示出激活vγ4tcr的明显能力(指示为
“‑”
)。
[0671]
实施例8.基于ms的表位作图
[0672]
为了以高分辨率确定抗原/抗体复合物的表位,将蛋白质复合物与氘代交联剂一起孵育并进行多酶切割。交联肽富集后,通过高分辨率质谱法(nlc-ltq-orbitrap ms)分析样品,并使用xquest(2.0版本)和stavrox(3.6版本)软件分析生成的数据。
[0673]
在用氘代d0d12对蛋白质复合物l1(dv1-gv4)/1139_p01_a04进行胰蛋白酶、糜蛋白酶、asp-n、弹性蛋白酶和嗜热菌蛋白酶蛋白水解之后,nlc-orbitrap ms/ms分析检测到l1(dv1-gv4)与抗体1139_p01_a04(g4_3)之间的11个交联肽。表位作图结果呈现于表3中。
[0674]
表3.抗原/抗体复合物的表位作图结果
[0675]
克隆物idseq id no:1的表位作图氨基酸编号1139_p01_a04(g4_3)71、73、75、76、79
[0676]
该表位作图数据与上述实验相关,表明这种抗体结合在γ4链的hv4区内。
[0677]
实施例9.原代vγ4阳性细胞的抗vγ4抗体靶向和调节。
[0678]
进行进一步的研究以证明抗vγ4抗体靶向源自皮肤、血液和肠道的原代vγ4
+
细胞,包括源自健康和患病患者样品的细胞。
[0679]
与源自皮肤的原代vγ4
+
细胞的结合
[0680]
首先,测试抗vγ4抗体与从两个个体供体的皮肤中扩增的原代vγ4
+
t细胞的结合。通过去除皮下脂肪来制备皮肤样品并使用3mm活检穿孔器制作多个穿孔。将穿孔器放置在碳矩阵网格上并放置在g-rex6(wilson wolf)的孔中。每个孔都装有含aim-v培养基(gibco,life technologies)、cts免疫血清替代物(life technologies)、il-2和il-15的完全分离培养基。在培养的前7天,使用含有两性霉素b(life technologies)的完全分离培养基(“+amp”)。每7天更换一次培养基,方法是轻轻吸出上部培养基并更换为2x完全分离培养基(不含amp),尽量不要干扰板或生物反应器底部的细胞。培养超过三周后,然后将所得的排出细胞传代到新鲜的组织培养容器和新鲜培养基(例如aim-v培养基或texmax培养基(miltenyi))加上重组il-2、il-4、il-15和il-21中,然后进行收获。然后借助于αβt细胞耗竭试剂盒和相关方案(诸如miltenyi提供的那些)来去除培养物内也存在的αβt细胞。对于
进一步的参考,参见wo2020/095059。
[0681]
分离后,首先将γδt细胞用活力染料在fc块的存在下在4℃下染色20分钟。然后将γδt细胞与固定浓度的示例性抗vγ4抗体(0.046-100μg/ml)或同种型对照(igg1抗呼吸道合胞病毒(rsv)抗体)一起在4℃下孵育30分钟。通过添加针对人igg1(is11-12e4.23.20)的荧光染料缀合的二抗进行检测。然后将细胞固定并且在macsquant16流式细胞仪上采集。将细胞门控为单个活的igg1(vγ4)
+
。所示数据是检测到与vγ4
+
细胞结合的检测二抗的中值荧光强度(mfi)。
[0682]
结果示于图7a中。这些数据证实,所有测试的抗vγ4抗体都能够以剂量依赖方式与皮肤来源的原代vγ4
+
t细胞结合。在同种型对照的情况下没有观察到结合。
[0683]
与源自外周血单核细胞(pbmc)的原代vγ4
+
细胞的结合
[0684]
简言之,首先将人pbmc(lonza,产品代码cc-2702)用活力染料在4℃下在fc块的存在下染色20分钟。然后将细胞与10μg/ml抗vγ4抗体或同种型对照(rsv)一起在4℃下孵育30分钟,然后洗涤并用抗vδ1(rea173)、抗vδ2(rea771)、抗γδ(rea591)和抗人igg1(is11-12e4.23.20)在4℃下进行细胞外染色20分钟。然后将细胞固定并且在macsquant16流式细胞仪上采集。将细胞门控为单个活的γδ
+
vδ2-igg1(vγ4)
+
。
[0685]
结果示于图7b中。所示数据是使用被缀合的抗人igg1二抗结合的每种单独抗体检测到的γδ
+
vδ2-细胞中的vγ4
+
细胞%。这些数据强调了实质上所有抗vγ4抗体结合血液来源的原代vγ4
+
t细胞的能力。使用抗体g4_23、g4_3、g4_12、g4_18或g4_20检测到最强的信号。
[0686]
与来自于从结直肠癌(crc)患者获得的肠源性上皮内淋巴细胞(iel)的原代vγ4
+
细胞的结合
[0687]
对于本研究,人crc肿瘤活检物是新鲜运输的并且在收到后进行加工。将活检物切成测量为~2mm2的小块并使用对最初由kupper和clarke描述的方法(til)(clarke等人,2006,j.invest.dermatol.126,1059-1070)的改编获得肿瘤浸润淋巴细胞(til)。具体地,将多达四个2mm2活检物置于9mm x 9mm x 1.5mm cellfoam矩阵上,在24孔板的每孔放置一个矩阵。然后将活检物在2ml伊斯科夫改良杜尔贝科培养基(iscove’s modified dulbecco’s medium,imdm)中培养,该培养基补充有4%人血浆、β-巯基乙醇(50μm)、青霉素(100u/ml)、链霉素(100μg/ml)、庆大霉素(20μg/ml)、甲硝哒唑(1μg/ml)、两性霉素b(2.5μg/ml)、hepes(10mm)、丙酮酸钠(1mm)、mem非必需氨基酸溶液(1x)和il-15(20ng/ml,miltenyi biotech)。每3天吸出1ml培养基并用1ml含有2倍浓缩的il-15的完全培养基替换。10天后收获til,使其通过70μm尼龙细胞过滤器,以300x g离心5分钟并重悬于完全培养基中以进行表型分析。首先将til用活/死活力染料在fc块的存在下在4℃下染色20分钟。然后将细胞与10μg/ml抗vγ4抗体或同种型对照(rsv)一起在4℃下孵育30分钟,然后洗涤并用抗vδ1(rea173)、抗γδ(rea591)和抗人igg1(is11-12e4.23.20)在4℃下进行细胞外染色20分钟。然后将细胞固定并且在macsquant16流式细胞仪上采集。将细胞门控为单个活的γδ
+
、igg1
+
(vγ4)
+
。
[0688]
结果示于图7c中。所示数据是例示出经由缀合的抗人igg1二抗检测到的抗vγ4抗体g4_3、g4_12和g4_18与原代肠源性vγ4
+
细胞的结合的facs图。数据证明了本发明的抗体与从crc肿瘤组织中获得的vγ4
+
细胞结合的能力。
[0689]
抗vγ4抗体赋予的人肠源性γδt细胞的检测和tcr下调
[0690]
进行了进一步的研究以探索抗vγ4抗体对人肠源性γδt细胞的调节作用。对于这些研究,来自crc患者结肠的正常邻近组织(nat)活检物是新鲜运输的并且在收到后进行加工以获得单细胞悬浮液。具体地,将组织切成测量为~2mm2的小块并且将至多1g组织连同4.7ml rpmi一起放入miltenyi c管中,其中除了酶r以外还具有来自miltenyi肿瘤解离试剂盒的酶,其浓度为制造商推荐的浓度,酶r以0.2x浓度使用以阻止相关的细胞表面分子裂解。将c管放置在附接有加热块的gentlemacs
tm
octo离解器上。选择程序37c_h_tdk_1用于解离软肿瘤。1小时后,通过70μm过滤器过滤消化物并添加含有4%人血浆的完全imdm以淬灭酶活性。然后将细胞洗涤两次并重悬于完全imdm中以进行计数。此时,将细胞接种以用抗vγ4抗体进行刺激,或用于表型分析。
[0691]
在一系列实验中,确定了在用抗vγ4抗体刺激之前肠道消化物中vγ4
+
γδt细胞的表型。简言之,将细胞用活/死活力染料在fc块的存在下在4℃下染色20分钟。然后将细胞与10μg/ml g4_18克隆一起在4℃下孵育30分钟,然后进行洗涤并用抗vδ1(rea173)、抗γδ(rea591)、抗cd69(rea824)、抗cd103(ber-act8)和抗人igg1(is11-12e4.23.20)在4℃下进行细胞外染色20分钟。然后将细胞固定并且在macsquant16流式细胞仪上采集。如图7d所示,1.4%活的单细胞为vδ1
+
。其中,44.2%与vγ4配对并且这些全部展示出肠道组织驻留标志物(cd69
+
cd103
+
),正如对于来自肠道的γδt细胞所预期的那样。这些结果证实本文所述的抗体(在这种情况下为示例抗体g4_18)可用于特异性地检测从人肠道组织中分离的vγ4
+
γδt细胞。
[0692]
下一系列实验测量了用抗vγ4抗体刺激细胞的影响。在48孔板中每孔接种2x106个细胞,并用g4_12、g4_18或rsv igg1同种型对照抗体在2ng/ml浓度的il-15的存在下对该细胞进行刺激。在mab刺激后24小时,通过流式细胞术分析通过酶消化分离的上皮内淋巴细胞(iel)。刺激24小时后,将细胞用活力染料在fc块的存在下在4℃下染色20分钟。然后将细胞针对γδtcr(rea591)进行细胞外染色,固定并在macsquant16流式细胞仪上采集。将活的单细胞门控为γδtcr
+
。图7e示出了与rsv同种型对照相比,用g4_12或者g4_18克隆刺激24小时后赋予的γδtcr下调,其随附有代表性facs图。这两种抗vγ4抗体g4_12和g4_18相对于rsv同种型对照都诱导了γδtcr下调,其中在g4_12情况下观察到最大的下调。
[0693]
实施例10.测量如通过本发明的示例抗vγ4抗体的表面等离子体共振(spr)所测量的对人vγ4的结合亲和力(kd)的进一步研究
[0694]
此外,对于实施例4中描述的关于scfv结合物的spr结合研究(实施例1中描述的方法),进行了额外的研究以测量当克隆被表达为全igg1单克隆抗体时选择的示例克隆与人vγ4链的结合亲和力。
[0695]
简言之,使用reichert 4spr仪器(reichert technologies)通过spr分析确立抗体与靶标(即γδtcr的人vγ4链)的结合亲和力。使抗原(l1(dv1-gv4))以10ug/ml偶联到羧甲基葡聚糖芯片(reichert technologies)上,这导致分别从基线增加大约750uriu。使抗体以从500nm至31.25nm的1:2稀释系列以下列参数流过细胞:180秒缔合,300秒解离,流速25μl/min,运行缓冲液pbs+0.05%吐温20。所有实验均在室温下进行,样品在流过芯片之前保持在4℃。根据langmuir 1∶1结合使用软件tracedrawer(reichert technologies)确定稳态拟合。
[0696]
结果示于表4中并且代表每种抗体2次实验的平均值(除非另有说明)。
[0697]
表4.示例抗体对人vγ4的结合亲和力
[0698][0699][0700]
*nd-未测定
[0701]
正如预期的那样,测定了一系列结合亲和力,从而使得能够根据需要的结合亲和力为特定情形选择特定抗体。具体而言,结合亲和力范围为大约260nm-2.8nm,如图所示。这与实施例4中描述的scfv研究一致。
[0702]
实施例11.vγ4特异性抗体增加人原代vγ4 t细胞的数目的用途。
[0703]
进一步测试对jrt3-hu17细胞展示出最高刺激活性的抗体(克隆g4_12,图5b、图5c)刺激原代vγ4+t细胞的能力。使用包括a647缀合的抗vγ4克隆g4_18在内的一组抗体通过流式细胞术分析用g4_12进行板结合刺激之后pbmc培养物中vγ4t细胞百分比与同种型对照相比的增加,其在图8中示出。在第7天和第14天,在g4_12抗体存在下的vg4阳性细胞的比例高于存在同种型对照的培养物。
[0704]
序列
[0705]
[0706]
[0707]
[0708]
[0709]
[0710]
[0711]
[0712]
[0713]
[0714]
[0715]
[0716]
[0717]
[0718]
[0719]
[0720]
[0721]
[0722]
[0723]
[0724]
[0725]
[0726]
[0727]
[0728]
[0729]
[0730]
[0731]
[0732]
[0733]
[0734]
[0735]
[0736]
[0737]
[0738]
[0739]
[0740]
[0741]
[0742]
[0743]
[0744]
[0745]
[0746]
[0747]
[0748]
[0749]
[0750]
[0751]
[0752]
[0753]
[0754]
[0755]
[0756]
[0757]
[0758]
[0759]
[0760]
[0761]
[0762]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1