用于测试安得塞奈效力的方法与流程
用于测试安得塞奈效力的方法
1.相关申请的交叉引用本技术要求2020年6月16日提交的美国申请号63/039,795的优先权权益,将该文献通过引用并入本文以用于所有目的。
背景技术:
2.安得塞奈α(凝血因子xa[重组]灭活的zhzo)是一种修饰的重组灭活形式的因子xa,经特别设计用于结合并隔离因子xa抑制剂。因子xa抑制剂(例如阿哌沙班、利伐沙班、依度沙班、贝曲西班和依诺肝素)是常用的抗凝剂。然而,这样的抗凝剂的使用与急性大出血发作相关。安得塞奈α或安得塞奈是预防和阻止这样的出血的有效解毒剂。
[0003]
重要的是在使用前对每一批次的安得塞奈的活性和效力进行评价。
技术实现要素:
[0004]
本披露提供了用于测量测试样品中安得塞奈α的效力(活性)的组合物、试剂盒和方法。可以基于测试样品在与fxa抑制剂一起的混合物中恢复人野生型fxa活性的能力来定量效力。人fxa的活性可以用例如来自已经建立了国际参考标准品的牛或人的fxa蛋白进一步校准。
[0005]
本披露的一个实施例提供了一种用于确定安得塞奈样品的活性的方法,该方法包括将包含安得塞奈的测试样品与包含人因子xa(hfxa)和直接因子xa(fxa)抑制剂的混合物混合,其中该fxa与该xa抑制剂的摩尔比是0.2 : 1至0.3 : 1;向该混合物中添加显色fxa底物,其中该显色fxa底物能够在与该hfxa反应时释放生色团;检测释放的生色团的量;以及从释放的生色团的量计算安得塞奈样品在从直接fxa抑制剂释放hfxa中的活性。
[0006]
另一实施例提供了一种用于确定安得塞奈样品的活性的方法,该方法包括:将包含安得塞奈的测试样品与包含牛因子xa(bfxa)和直接因子xa(fxa)抑制剂的混合物混合,其中该bfxa与该fxa抑制剂的摩尔比是0.15 : 1至0.25 : 1;向该混合物中添加显色fxa底物,其中该显色fxa底物能够在与该bfxa反应时释放生色团;检测释放的生色团的量;以及从释放的生色团的量计算安得塞奈样品在从直接fxa抑制剂释放bfxa中的活性。
附图说明
[0007]
作为本披露的实施例,提供了仅通过示例而非限制说明的附图,其中:图1比较了人fxa相比于牛fxa(hyphen bfxa)切割spectrozyme-fxa底物的酶活性。按250、125、62.5、31.25、15.625、7.8125、3.90625、0 ng/ml将人fxa()或bfxa()连续稀释于1xtbs(ph7.4,0.1% bsa)中。将连续稀释的fxa(100 μl)与50 μl spectrozyme-fxa(2 mm)混合。在室温下孵育10 min后,通过添加50 μl乙酸淬灭反应。基于斜率(od405 nm相比于浓度),牛fxa的活性比hfxa低大约31%。
[0008]
图2a-2c通过在直接效力测定中匹配酶浓度来比较牛fxa和人fxa。2a. bfxa(1x)/贝曲西班(1x);2b. bfxa(1x)/贝曲西班(1.5x);2c. bfxa(1x)/贝曲西班(2x)。首先分别制
备hfxa、bfxa和贝曲西班的储备溶液。通过以下制备fxa/贝曲西班混合物:混合不同体积的fxa和贝曲西班的储备溶液,得到hfxa/贝曲西班或bfxa/贝曲西班。如直接效力测定中所述,将fxa/贝曲西班混合物(50 μl)添加到反应混合物中。使用hfxa(1x)/贝曲西班(1x)混合物()作为对照。在保持相同浓度的bfxa(1x)的同时,在不同浓度的贝曲西班下测试bfxa/贝曲西班混合物()。小图a):bfxa(1x)/贝曲西班(1x);小图b:bfxa(1x)/贝曲西班(1.5x);小图c):bfxa(1x)/贝曲西班(2x)。
[0009]
图3a-3b示出了通过匹配酶活性得到的牛fxa和贝曲西班浓度的优化结果。3a. bfxa(1.64x)/贝曲西班(2x);3b. bfxa(1.45x)/贝曲西班(2x)。首先分别制备hfxa、bfxa和贝曲西班的储备溶液。通过以下制备fxa/贝曲西班混合物:混合不同体积的fxa和贝曲西班的储备溶液,得到hfxa/贝曲西班或bfxa/贝曲西班。如直接效力测定中所述,将fxa/贝曲西班混合物(50 μl)添加到反应混合物中。使用hfxa(1x)/贝曲西班(1x)混合物()作为对照。在保持相同浓度的贝曲西班(2x)的同时,在不同浓度的bfxa下测试bfxa/贝曲西班混合物()。小图a):bfxa(1.64x)/贝曲西班(2x);小图b:bfxa(1.45x)/贝曲西班(2x)。
具体实施方式
[0010]
i.定义所有数字表达,例如ph、温度、时间、浓度和分子量(包括范围)都是近似值,其以0.1的增量变化(+)或(-)。应当理解的是,尽管不总是明确陈述,在所有数字表达前面加上术语“约”。还应当理解的是,尽管不总是明确陈述,本文所述的试剂仅是示例性的并且这样的试剂的等同物在本领域中是已知的。
[0011]“组合物”旨在意指活性剂和另一惰性化合物或组合物(例如,可检测的药剂或标签)或活性化合物或组合物的组合。
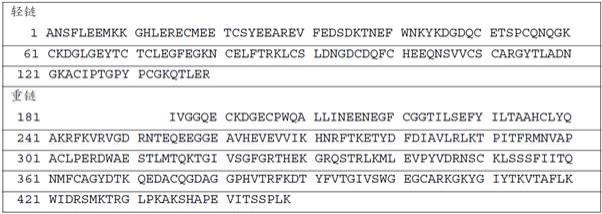
[0012]“因子xa”或“fxa”或“fxa蛋白”是凝血途径中的丝氨酸蛋白酶,其由灭活的因子x(fx)产生。编码人因子x(“fx”)的核苷酸序列可以在genbank登录号“nm_000504”中找到。在重链的前52个残基的催化裂解后,fx被活化为fxa(seq id no: 1,表1)。fxa含有轻链和重链(如表1中所示)。该轻链的前45个氨基酸残基(seq id no: 1的残基1-45)称为gla结构域,因为它含有11个翻译后修饰的γ-羧基谷氨酸残基(gla)。它还含有短的(6个氨基酸残基)芳香堆叠序列(seq id no: 1的残基40-45)。胰凝乳蛋白酶消化选择性地去除1-44残基,导致无gla结构域fxa。fxa的丝氨酸蛋白酶催化结构域位于c-末端重链上。fxa的重链与其他丝氨酸蛋白酶(如凝血酶、胰蛋白酶、和激活的蛋白c)高度同源。
[0013]“天然fxa”或“野生型fxa”是指天然存在于血浆中或以其原始的未修饰形式分离的fxa,其具有激活凝血酶原的生物活性,因此促进血液凝块的形成。该术语包括从组织样品中分离的天然存在的多肽以及重组产生的fxa。“活性fxa”是指具有激活凝血酶原的生物学活性的fxa。“活性fxa”可以是保留促凝血活性的天然fxa或经修饰的fxa。
[0014]
如本文所用,“fxa衍生物”是指修饰的fxa蛋白,其具有gla结构域的修饰或大量缺失(例如,至少50%、60%、70%、80%或90%的轻链氨基酸残基6-39的缺失)和活性位点的修饰,使得与野生型蛋白相比,fxa衍生物在组装到凝血酶原酶复合物方面的能力降低,并且催化活性降低或没有催化活性。与野生型蛋白类似,fxa衍生物仍然可以结合并且/或者基本上
中和fxa抑制剂。美国专利号8153590和8268783中提供了fxa衍生物及其生物等同物的实例。
[0015]
术语“活性位点”是指酶或抗体中发生化学反应的部分。“修饰的活性位点”是已经在结构上修饰以提供具有增加或降低的化学反应性或特异性的活性位点的活性位点。活性位点的实例包括但不限于包含235-488氨基酸残基的人因子x的催化结构域、和包含195-448氨基酸残基的人因子xa的催化结构域。修饰的活性位点的实例包括但不限于人因子xa的催化结构域,其包含seq id no: 2中的195-448氨基酸残基,其中在位置arg306、glu310、arg347、lys351、lys414或arg424处具有至少一个氨基酸取代。
[0016]
fxa衍生物的实例是“无gla结构域fxa”或“去gla fxa”,其是指不具有gla结构的fxa或fxa衍生物,并且涵盖除了去除gla结构域之外还具有其他一个或多个修饰的fxa衍生物。本发明中无gla结构域fxa的实例包括但不限于缺少seq id no: 1的1-39(或6-39)氨基酸残基的全部或一部分的fxa衍生物。
[0017]
fxa衍生物的另一实例是“gla缺陷型fxa”,gla缺陷型fxa是指其gla结构域中游离侧链γ-羧基基团的数量减少的fxa或fxa衍生物。就像无gla结构域fxa一样,gla缺陷型fxa也可以具有其他修饰。gla缺陷型fxa包括未羧基化的、羧基化不足的和脱羧基化的fxa。“未羧基化的fxa”或“脱羧基化的fxa”是指不具有gla结构域的γ-羧基谷氨酸残基的γ-羧基基团的fxa衍生物,例如所有gla结构域γ-羧基谷氨酸被不同的氨基酸替换的fxa,或通过例如胺化、酯化等手段去除或掩蔽其所有侧链γ-羧基的fxa。对于重组表达的蛋白质,未羧基化的fxa有时也称为非羧基化的fxa。“羧基化不足的fxa”是指与野生型fxa相比,gla结构域中的γ-羧基基团的数量减少的fxa衍生物,例如一个或多个但不是所有的gla结构域γ-羧基谷氨酸被一个或多个不同的氨基酸替换的fxa,或通过例如胺化和酯化等手段去除或掩蔽至少一个但不是所有侧链γ-羧基的fxa。
[0018]
在一些实施例中,fxa衍生物至少缺失野生型fxa的轻链(参见seq id no: 1中的轻链)的氨基酸残基6-39。在一些实施例中,fxa衍生物还缺失egf1结构域(氨基酸46-84)和/或egf2结构域(轻链的氨基酸85-128)。在一些实施例中,fxa衍生物的轻链至少包括野生型轻链的氨基酸129-139(或seq id no: 3的95-105)。
[0019]
seq id no: 2(表2)也称为“安得塞奈α”或简称为“安得塞奈”,其相对于野生型fxa含有两个突变。第一个突变是fx的gla结构域中氨基酸残基6-39的缺失。第二个突变是活性位点残基s379突变为ala残基。此氨基酸取代分别对应于seq id no: 1的氨基酸296。安得塞奈包括两条链,分别称为seq id no: 3(轻链)和seq id no: 4(重链)。
[0020]
fxa衍生物还涵盖在制造过程期间含有突变、翻译后修饰、和/或蛋白变化的那些。例如,在另一方面,具有或不具有ser379修饰的fxa衍生物可以含有催化三联体中his(至ala)和/或asp(至ala/asn)残基上的修饰,以及缺失的或修饰的gla结构域。这些修饰提供了具有降低的酶活性但是在组装到凝血酶原酶复合物中时不与fxa竞争的fxa衍生物。
[0021]
在一些实施例中,fxa衍生物具有重链,该重链具有一个或两个o-连接的糖基化。在一些实施例中,重链可以具有氨基酸残基或多达13、14或15个氨基酸残基的c-末端截短。在一些实施例中,轻链可以具有n-末端截短。
[0022]
本披露提供了披露的fxa衍生物序列的多种生物等同物,或者可替代地,提供了与这些fxa衍生物具有一定序列同一性的多肽。在一个方面,这样的生物等同物保留了这些
fxa衍生物的结构特征,即修饰的活性位点或重链以及缺失的或修饰的gla结构域。在另一方面,这样的生物等同物保留了这些fxa衍生物的功能特征,即在组装到凝血酶原酶复合物中时不与fxa竞争并且具有降低的催化活性。在另一方面,这样的生物等同物可以结合并且/或者基本上中和fxa抑制剂。
[0023]
表1. 激活的人因子x(fxa)的多肽序列(seq id no: 1)表2. 安得塞奈的多肽序列(seq id no: 2)术语“因子xa抑制剂”或“因子xa的抑制剂”是指可以直接或间接地抑制凝血因子xa在体外和/或体内催化凝血酶原转化为凝血酶的活性的化合物。
[0024]“直接因子xa抑制剂”或“直接fxa抑制剂”直接结合fxa并且抑制其活性。非限制性实例包括利伐沙班(xarelto)、阿哌沙班(eliquis)、贝曲西班(bevyxxa)、达瑞沙班(ym150)、依度沙班(lixiana)、奥米沙班、利他沙班(tak-442)、艾立沙班(pd0348292)、及其药学上可接受的盐、及其组合。
[0025]“间接因子xa抑制剂”或“间接fxa抑制剂”经由一种或多种其他因子抑制fxa活性。间接因子xa抑制剂的非限制性实例包括依诺肝素、磺达肝素、艾屈肝素、生物素化艾屈肝素、替地肝素、亭扎肝素、低分子量肝素(“lmwh”)、及其组合。
[0026]
ii.效力测定抗凝剂在治疗或预防具有形成血液凝块倾向的患者(例如像患有凝血障碍、受限于不动时间段或正在接受医学手术的那些患者)的不希望的血栓形成方面满足了市场的需求。然而,抗凝剂疗法的主要限制之一是与治疗相关的出血风险,以及在过度给药的情况下或如果需要紧急手术程序时对快速逆转抗凝剂活性的能力有限制。
[0027]
安得塞奈α(安得塞奈)是一种重组修饰的人因子xa诱饵蛋白,其可以逆转对因子xa的抑制,并且因此是基于因子xa的抗凝剂治疗的有效解毒剂。安得塞奈制成为由培养的
细胞产生的重组蛋白。使用前,重要的是测量每个生产批次的效力。
[0028]
效力测量测定需要将安得塞奈样品添加至fxa/抑制剂混合物中,在该混合物中,fxa已经至少部分地被抑制剂抑制。添加安得塞奈样品后,抑制剂被隔离,释放全部或部分结合的fxa,这可以通过其切割fxa特异性显色底物并释放生色团的能力来测量。
[0029]
有趣的是,发现适合的fxa/抑制剂混合物需要比fxa远高得多的抑制剂。例如,当将人fxa与特定fxa抑制剂贝曲西班马来酸盐一起使用时,适合的摩尔比是0.25 : 1。
[0030]
在某些情况下,优选的是用已经用国际标准品校准的fxa表示测量的安得塞奈效力。遗憾的是,人fxa直到最近才有适合的国际标准品。为此,实例2探索了牛fxa的使用。
[0031]
有趣的是,牛fxa表现出相当低的显色活性。这提出了挑战。如果牛fxa按质量或浓度计与人fxa匹配,则牛fxa将具有降低的活性。另一方面,如果牛fxa具有匹配的活性,则牛fxa将具有相对于人fxa的摩尔过量,从而影响测定中的fxa/抑制剂比率和抑制程度。仍另一令人惊讶的发现是,贝曲西班对牛fxa的抑制效力小于对人fxa的抑制效力。
[0032]
基于这些观察,在保持bfxa的相同浓度(1x)的同时,增加(1.5x、2.0x)混合物中的贝曲西班浓度,以便在不存在安得塞奈的情况下降低背景bfxa的活性。如图2(b-c) 中所示。在不存在安得塞奈的情况下,贝曲西班浓度的2倍增加将bfxa背景降低至与hfxa类似的水平。然而,在存在最高安得塞奈浓度时,使用bfxa(1x)的最大吸光度比使用hfxa(1x)/贝曲西班(1x)的对照低。
[0033]
本披露的一个令人惊讶的发现是,尽管显色活性和被fxa抑制剂抑制的能力存在差异,但是通过调节混合物中的牛fxa浓度,可以实现牛和人fxa对照之间在最大和最小吸光度、ec
50
、和测定范围方面相当的特性。在一些实施例中,牛fxa/抑制剂摩尔比可以是0.18: 1左右。在一些实施例中,牛fxa浓度可以是16.2 nm左右。
[0034]
因此,根据本披露的一个实施例,提供了一种用于确定安得塞奈样品的活性的方法。在一些实施例中,该方法需要将包含安得塞奈的测试样品与包含人因子xa(hfxa)和直接因子xa(fxa)抑制剂的混合物混合。然后向该混合物中添加显色fxa底物,其中该显色fxa底物能够在与该hfxa反应时释放生色团。一旦检测到释放的生色团的量,就可以计算与从直接fxa抑制剂释放hfxa有关的安得塞奈样品的活性。
[0035]
如本文所用,“安得塞奈样品”是指包括一个或多个安得塞奈分子的样品。安得塞奈样品可以是例如通过药物制造、或在临床使用之前取自已经制备的较大体积或质量的特定体积或质量的样品。
[0036]
在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.2 : 1至0.3 : 1。在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.1 : 1至0.5 : 1、0.12 : 1至0.5: 1、0.14 : 1至0.5 : 1、0.15 : 1至0.5 : 1、0.16 : 1至0.5 : 1、0.18 : 1至0.5 : 1、0.2 : 1至0.5 : 1、0.22 : 1至0.5 : 1、0.24 : 1至0.5 : 1、0.25 : 1至0.5 : 1、0.26: 1至0.5 : 1、0.28 : 1至0.5 : 1、0.3 : 1至0.5 : 1、0.1 : 1至0.48 : 1、0.12 : 1至0.48 : 1、0.14 : 1至0.48 : 1、0.15 : 1至0.48 : 1、0.16 : 1至0.48 : 1、0.18 : 1至0.48 : 1、0.2 : 1至0.48 : 1、0.22 : 1至0.48 : 1、0.24 : 1至0.48 : 1、0.25 : 1至0.48 : 1、0.26 : 1至0.48 : 1、0.28 : 1至0.48 : 1、0.3 : 1至0.48 : 1、0.1 : 1至0.46 : 1、0.12 : 1至0.46 : 1、0.14 : 1至0.46 : 1、0.15 : 1至0.46 : 1、0.16 : 1至0.46 : 1、0.18 : 1至0.46 : 1、0.2 : 1至0.46 : 1、0.22 : 1至0.46 : 1、0.24 : 1至
0.46 : 1、0.25 : 1至0.46 : 1、0.26 : 1至0.46 : 1、0.28 : 1至0.46 : 1、0.3 : 1至0.46 : 1、0.1 : 1至0.45 : 1、0.12 : 1至0.45 : 1、0.14 : 1至0.45 : 1、0.15 : 1至0.45 : 1、0.16 : 1至0.45 : 1、0.18 : 1至0.45 : 1、0.2 : 1至0.45 : 1、0.22 : 1至0.45 : 1、0.24 : 1至0.45 : 1、0.25 : 1至0.45 : 1、0.26 : 1至0.45 : 1、0.28 : 1至0.45 : 1、或0.3 : 1至0.45 : 1。
[0037]
在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.1 : 1至0.44 : 1、0.12 : 1至0.44 : 1、0.14 : 1至0.44 : 1、0.15 : 1至0.44 : 1、0.16 : 1至0.44 : 1、0.18 : 1至0.44 : 1、0.2 : 1至0.44 : 1、0.22 : 1至0.44 : 1、0.24 : 1至0.44 : 1、0.25 : 1至0.44 : 1、0.26 : 1至0.44 : 1、0.28 : 1至0.44 : 1、0.3 : 1至0.44 : 1、0.1 : 1至0.42 : 1、0.12 : 1至0.42 : 1、0.14 : 1至0.42 : 1、0.15 : 1至0.42 : 1、0.16 : 1至0.42 : 1、0.18 : 1至0.42 : 1、0.2 : 1至0.42 : 1、0.22 : 1至0.42 : 1、0.24 : 1至0.42 : 1、0.25 : 1至0.42 : 1、0.26 : 1至0.42 : 1、0.28 : 1至0.42 : 1、0.3 : 1至0.42 : 1、0.1 : 1至0.4 : 1、0.12 : 1至0.4 : 1、0.14 : 1至0.4 : 1、0.15 : 1至0.4 : 1、0.16 : 1至0.4 : 1、0.18 : 1至0.4 : 1、0.2 : 1至0.4 : 1、0.22 : 1至0.4: 1、0.24 : 1至0.4 : 1、0.25 : 1至0.4 : 1、0.26 : 1至0.4 : 1、0.28 : 1至0.4 : 1、0.3 : 1至0.4 : 1、0.1 : 1至0.38 : 1、0.12 : 1至0.38 : 1、0.14 : 1至0.38 : 1、0.15 : 1至0.38 : 1、0.16 : 1至0.38 : 1、0.18 : 1至0.38 : 1、0.2 : 1至0.38 : 1、0.22 : 1至0.38 : 1、0.24 : 1至0.38 : 1、0.25 : 1至0.38 : 1、0.26 : 1至0.38 : 1、0.28 : 1至0.38 : 1、或0.3 : 1至0.38 : 1。
[0038]
在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.1 : 1至0.36 : 1、0.12 : 1至0.36 : 1、0.14 : 1至0.36 : 1、0.15 : 1至0.36 : 1、0.16 : 1至0.36 : 1、0.18 : 1至0.36 : 1、0.2 : 1至0.36 : 1、0.22 : 1至0.36 : 1、0.24 : 1至0.36 : 1、0.25 : 1至0.36 : 1、0.26 : 1至0.36 : 1、0.28 : 1至0.36 : 1、0.3 : 1至0.36 : 1、0.1 : 1至0.35 : 1、0.12 : 1至0.35 : 1、0.14 : 1至0.35 : 1、0.15 : 1至0.35 : 1、0.16 : 1至0.35 : 1、0.18 : 1至0.35 : 1、0.2 : 1至0.35 : 1、0.22 : 1至0.35 : 1、0.24 : 1至0.35 : 1、0.25 : 1至0.35 : 1、0.26 : 1至0.35 : 1、0.28 : 1至0.35 : 1、0.3 : 1至0.35 : 1、0.1 : 1至0.34 : 1、0.12 : 1至0.34 : 1、0.14 : 1至0.34 : 1、0.15 : 1至0.34 : 1、0.16 : 1至0.34 : 1、0.18 : 1至0.34 : 1、0.2 : 1至0.34 : 1、0.22 : 1至0.34 : 1、0.24 : 1至0.34 : 1、0.25 : 1至0.34 : 1、0.26 : 1至0.34 : 1、0.28 : 1至0.34 : 1、0.3 : 1至0.34 : 1、0.1 : 1至0.32 : 1、0.12 : 1至0.32 : 1、0.14 : 1至0.32 : 1、0.15 : 1至0.32 : 1、0.16 : 1至0.32 : 1、0.18 : 1至0.32 : 1、0.2 : 1至0.32 : 1、0.22 : 1至0.32 : 1、0.24 : 1至0.32 : 1、0.25 : 1至0.32 : 1、0.26 : 1至0.32 : 1、0.28 : 1至0.32 : 1、或0.3 : 1至0.32 : 1。
[0039]
在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.1 : 1至0.3 : 1、0.12 : 1至0.3 : 1、0.14 : 1至0.3 : 1、0.15 : 1至0.3 : 1、0.16 : 1至0.3 : 1、0.18: 1至0.3 : 1、0.2 : 1至0.3 : 1、0.22 : 1至0.3 : 1、0.24 : 1至0.3 : 1、0.25 : 1至0.3: 1、0.26 : 1至0.3 : 1、0.28 : 1至0.3 : 1、0.1 : 1至0.28 : 1、0.12 : 1至0.28 : 1、0.14 : 1至0.28 : 1、0.15 : 1至0.28 : 1、0.16 : 1至0.28 : 1、0.18 : 1至0.28 : 1、0.2 : 1至0.28 : 1、0.22 : 1至0.28 : 1、0.24 : 1至0.28 : 1、0.25 : 1至0.28 : 1、
0.26 : 1至0.28 : 1、0.1 : 1至0.26 : 1、0.12 : 1至0.26 : 1、0.14 : 1至0.26 : 1、0.15 : 1至0.26 : 1、0.16 : 1至0.26 : 1、0.18 : 1至0.26 : 1、0.2 : 1至0.26 : 1、0.22 : 1至0.26 : 1、0.24 : 1至0.26 : 1、0.25 : 1至0.26 : 1、0.1 : 1至0.25 : 1、0.12 : 1至0.25 : 1、0.14 : 1至0.25 : 1、0.15 : 1至0.25 : 1、0.16 : 1至0.25 : 1、0.18 : 1至0.25 : 1、0.2 : 1至0.25 : 1、0.22 : 1至0.25 : 1、0.24 : 1至0.25 : 1、0.1 : 1至0.24 : 1、0.12 : 1至0.24 : 1、0.14 : 1至0.24 : 1、0.15 : 1至0.24 : 1、0.16 : 1至0.24 : 1、0.18 : 1至0.24 : 1、0.2 : 1至0.24 : 1、0.22 : 1至0.24 : 1、0.1 : 1至0.22 : 1、0.12 : 1至0.22 : 1、0.14 : 1至0.22 : 1、0.15 : 1至0.22 : 1、0.16 : 1至0.22 : 1、0.18 : 1至0.22 : 1、0.2 : 1至0.22 : 1、0.1 : 1至0.2 : 1、0.12: 1至0.2 : 1、0.14 : 1至0.2 : 1、0.15 : 1至0.2 : 1、0.16 : 1至0.2 : 1、或0.18: 1至0.2 : 1。
[0040]
在一些实施例中,混合物中fxa与fxa抑制剂的摩尔比是从0.21至0.29、0.22至0.28、0.23至0.27、0.24至0.26、0.245至0.255、0.248至0.252、或约0.25,但是不限于此。
[0041]
在一些实施例中,在添加测试样品后,hfxa的浓度是约8至14 nm。在一些实施例中,浓度是从5至20 nm、6至20 nm、7至20 nm、8至20 nm、9至20 nm、10至20 nm、11至20 nm、12至20 nm、5至19 nm、6至19 nm、7至19 nm、8至19 nm、9至19 nm、10至19 nm、11至19 nm、12至19 nm、5至18 nm、6至18 nm、7至18 nm、8至18 nm、9至18 nm、10至18 nm、11至18 nm、12至18 nm、5至17 nm、6至17 nm、7至17 nm、8至17 nm、9至17 nm、10至17 nm、11至17 nm、12至17 nm、5至16 nm、6至16 nm、7至16 nm、8至16 nm、9至16 nm、10至16 nm、11至16 nm、12至16 nm、5至15 nm、6至15 nm、7至15 nm、8至15 nm、9至15 nm、10至15 nm、11至15 nm、12至15 nm、5至14 nm、6至14 nm、7至14 nm、8至14 nm、9至14 nm、10至14 nm、11至14 nm、12至14 nm、5至13 nm、6至13 nm、7至13 nm、8至13 nm、9至13 nm、10至13 nm、11至13 nm、12至13 nm、5至12 nm、6至12 nm、7至12 nm、8至12 nm、9至12 nm、10至12 nm、11至12 nm、5至11 nm、6至11 nm、7至11 nm、8至11 nm、9至11 nm、10至11 nm、5至10 nm、6至10 nm、7至10 nm、8至10 nm、或9至10 nm。
[0042]
预期任何直接fxa抑制剂均可以用于该测定。在一些实施例中,直接fxa抑制剂选自由以下组成的组:贝曲西班、阿哌沙班、利伐沙班、依度沙班、奥米沙班、利他沙班和艾立沙班。在一些实施例中,直接fxa抑制剂是贝曲西班。在一些实施例中,直接fxa抑制剂是阿哌沙班。在一些实施例中,直接fxa抑制剂是利伐沙班。
[0043]
在一些实施例中,可以有帮助的是,该方法进一步需要使用参考安得塞奈样品生成的标准曲线来验证安得塞奈样品的活性。
[0044]
本披露的另一实施例提供了一种用于使用具有建立的国际标准品的fxa蛋白来确定安得塞奈样品的活性的方法。在一些实施例中,这样的fxa是牛fxa(bfxa)。在一些实施例中,这样的fxa是人fxa(hfxa)。已知人fxa(hfxa)具有约46 kda的分子量,并且牛fxa(bfxa)具有约45.3 kda的分子量。
[0045]
因此,在一些实施例中,该方法需要将包含安得塞奈的测试样品与包含牛因子xa(bfxa)和直接因子xa(fxa)抑制剂的混合物混合。随后向该混合物中添加显色fxa底物,其中该显色fxa底物能够在与该bfxa反应时释放生色团。检测释放的生色团的量,其可以用于计算安得塞奈样品在从直接fxa抑制剂释放bfxa中的活性。
[0046]
在一些实施例中,bfxa与fxa抑制剂的摩尔比是从约0.15 : 1至0.25 : 1。在一些实施例中,bfxa与fxa抑制剂的摩尔比是从约0.1 : 1至0.5 : 1、0.12 : 1至0.5 : 1、0.14: 1至0.5 : 1、0.15 : 1至0.5 : 1、0.16 : 1至0.5 : 1、0.18 : 1至0.5 : 1、0.2 : 1至0.5 : 1、0.22 : 1至0.5 : 1、0.24 : 1至0.5 : 1、0.25 : 1至0.5 : 1、0.1 : 1至0.48 : 1、0.12 : 1至0.48 : 1、0.14 : 1至0.48 : 1、0.15 : 1至0.48 : 1、0.16 : 1至0.48 : 1、0.18 : 1至0.48 : 1、0.2 : 1至0.48 : 1、0.22 : 1至0.48 : 1、0.24 : 1至0.48 : 1、0.25 : 1至0.48 : 1、0.1 : 1至0.46 : 1、0.12 : 1至0.46 : 1、0.14 : 1至0.46 : 1、0.15 : 1至0.46 : 1、0.16 : 1至0.46 : 1、0.18 : 1至0.46 : 1、0.2 : 1至0.46 : 1、0.22 : 1至0.46 : 1、0.24 : 1至0.46 : 1、0.25 : 1至0.46 : 1、0.1 : 1至0.45 : 1、0.12 : 1至0.45 : 1、0.14 : 1至0.45 : 1、0.15 : 1至0.45 : 1、0.16 : 1至0.45 : 1、0.18 : 1至0.45 : 1、0.2 : 1至0.45 : 1、0.22 : 1至0.45 : 1、0.24 : 1至0.45 : 1、0.25 : 1至0.45 : 1、0.1 : 1至0.44 : 1、0.12 : 1至0.44 : 1、0.14 : 1至0.44 : 1、0.15 : 1至0.44 : 1、0.16 : 1至0.44 : 1、0.18 : 1至0.44 : 1、0.2 : 1至0.44 : 1、0.22 : 1至0.44 : 1、0.24 : 1至0.44 : 1、或0.25 : 1至0.44 : 1。
[0047]
在一些实施例中,bfxa与fxa抑制剂的摩尔比是从约0.1 : 1至0.42 : 1、0.12 : 1至0.42 : 1、0.14 : 1至0.42 : 1、0.15 : 1至0.42 : 1、0.16 : 1至0.42 : 1、0.18 : 1至0.42 : 1、0.2 : 1至0.42 : 1、0.22 : 1至0.42 : 1、0.24 : 1至0.42 : 1、0.25 : 1至0.42 : 1、0.1 : 1至0.4 : 1、0.12 : 1至0.4 : 1、0.14 : 1至0.4 : 1、0.15 : 1至0.4 : 1、0.16 : 1至0.4 : 1、0.18 : 1至0.4 : 1、0.2 : 1至0.4 : 1、0.22 : 1至0.4 : 1、0.24: 1至0.4 : 1、0.25 : 1至0.4 : 1、0.1 : 1至0.38 : 1、0.12 : 1至0.38 : 1、0.14: 1至0.38 : 1、0.15 : 1至0.38 : 1、0.16 : 1至0.38 : 1、0.18 : 1至0.38 : 1、0.2 : 1至0.38 : 1、0.22 : 1至0.38 : 1、0.24 : 1至0.38 : 1、0.25 : 1至0.38 : 1、0.1 : 1至0.36 : 1、0.12 : 1至0.36 : 1、0.14 : 1至0.36 : 1、0.15 : 1至0.36 : 1、0.16 : 1至0.36 : 1、0.18 : 1至0.36 : 1、0.2 : 1至0.36 : 1、0.22 : 1至0.36 : 1、0.24 : 1至0.36 : 1、0.25 : 1至0.36 : 1、0.1 : 1至0.35 : 1、0.12 : 1至0.35 : 1、0.14 : 1至0.35 : 1、0.15 : 1至0.35 : 1、0.16 : 1至0.35 : 1、0.18 : 1至0.35 : 1、0.2 : 1至0.35 : 1、0.22 : 1至0.35 : 1、0.24 : 1至0.35 : 1、0.25 : 1至0.35 : 1、0.1 : 1至0.34 : 1、0.12 : 1至0.34 : 1、0.14 : 1至0.34 : 1、0.15 : 1至0.34 : 1、0.16 : 1至0.34 : 1、0.18 : 1至0.34 : 1、0.2 : 1至0.34 : 1、0.22 : 1至0.34 : 1、0.24 : 1至0.34 : 1、0.25 : 1至0.34 : 1、0.1 : 1至0.32 : 1、0.12 : 1至0.32 : 1、0.14 : 1至0.32 : 1、0.15 : 1至0.32 : 1、0.16 : 1至0.32 : 1、0.18 : 1至0.32 : 1、0.2 : 1至0.32 : 1、0.22 : 1至0.32 : 1、0.24 : 1至0.32 : 1、或0.25 : 1至0.32 : 1、0.1 : 1至0.3 : 1、0.12 : 1至0.3 : 1、0.14 : 1至0.3 : 1、0.15 : 1至0.3 : 1、0.16 : 1至0.3 : 1、0.18 : 1至0.3 : 1、0.2 : 1至0.3 : 1、0.22 : 1至0.3 : 1、0.24 : 1至0.3 : 1、0.25: 1至0.3 : 1、0.1 : 1至0.28 : 1、0.12 : 1至0.28 : 1、0.14 : 1至0.28 : 1、0.15: 1至0.28 : 1、0.16 : 1至0.28 : 1、0.18 : 1至0.28 : 1、0.2 : 1至0.28 : 1、0.22 : 1至0.28 : 1、0.24 : 1至0.28 : 1、0.25 : 1至0.28 : 1、0.1 : 1至0.26 : 1、0.12 : 1至0.26 : 1、0.14 : 1至0.26 : 1、0.15 : 1至0.26 : 1、0.16 : 1至0.26 : 1、0.18 : 1至0.26 : 1、0.2 : 1至0.26 : 1、0.22 : 1至0.26 : 1、0.24 : 1至0.26 : 1、
0.25 : 1至0.26 : 1、0.1 : 1至0.25 : 1、0.12 : 1至0.25 : 1、0.14 : 1至0.25 : 1、0.15 : 1至0.25 : 1、0.16 : 1至0.25 : 1、0.18 : 1至0.25 : 1、0.2 : 1至0.25 : 1、0.22 : 1至0.25 : 1、0.24 : 1至0.25 : 1、0.1 : 1至0.24 : 1、0.12 : 1至0.24 : 1、0.14 : 1至0.24 : 1、0.15 : 1至0.24 : 1、0.16 : 1至0.24 : 1、0.18 : 1至0.24 : 1、0.2 : 1至0.24 : 1、0.22 : 1至0.24 : 1、0.1 : 1至0.22 : 1、0.12 : 1至0.22 : 1、0.14 : 1至0.22 : 1、0.15 : 1至0.22 : 1、0.16 : 1至0.22 : 1、0.18 : 1至0.22 : 1、0.2 : 1至0.22 : 1、0.1 : 1至0.2 : 1、0.12 : 1至0.2 : 1、0.14 : 1至0.2 : 1、0.15 : 1至0.2 : 1、0.16 : 1至0.2 : 1、0.18 : 1至0.2 : 1。
[0048]
在一些实施例中,bfxa与fxa抑制剂的摩尔比是从约0.15 : 1至0.25 : 1、0.16 : 1至0.23 : 1、0.16 : 1至0.23 : 1、0.16 : 1至0.20 : 1、0.16 : 1至0.19 : 1、017 : 1至0.19 : 1、或约0.18 : 1。
[0049]
在一些实施例中,在添加测试样品后,bfxa的浓度是约10至20 nm。在一些实施例中,在添加测试样品后,bfxa的浓度是约10至20 nm、11至20 nm、12至20 nm、13至20 nm、14至20 nm、15至20 nm、16至20 nm、17至20 nm、10至19 nm、11至19 nm、12至19 nm、13至19 nm、14至19 nm、15至19 nm、16至19 nm、17至19 nm、10至18 nm、11至18 nm、12至18 nm、13至18 nm、14至18 nm、15至18 nm、16至18 nm、17至18 nm、10至17 nm、11至17 nm、12至17 nm、13至17 nm、14至17 nm、15至17 nm、16至17 nm、10至16 nm、11至16 nm、12至16 nm、13至16 nm、14至16 nm、15至16 nm、10至15 nm、11至15 nm、12至15 nm、13至15 nm、或14至15 nm。
[0050]
在一些实施例中,在添加测试样品后,bfxa的浓度是约14至18 nm、15至17 nm、或15.5至16.5 nm。
[0051]
预期任何直接fxa抑制剂均可以用于该测定。在一些实施例中,直接fxa抑制剂选自由以下组成的组:贝曲西班、阿哌沙班、利伐沙班、依度沙班、奥米沙班、利他沙班和艾立沙班。在一些实施例中,直接fxa抑制剂是贝曲西班。在一些实施例中,直接fxa抑制剂是阿哌沙班。在一些实施例中,直接fxa抑制剂是利伐沙班。
[0052]
在一些实施例中,可以有帮助的是,该方法进一步需要使用参考安得塞奈样品生成的标准曲线来验证安得塞奈样品的活性。
[0053]
本披露的另一实施例提供了一种用于使用具有建立的国际标准品的fxa蛋白来确定安得塞奈样品的活性的方法。在一些实施例中,这样的fxa是牛fxa(bfxa)。已知人fxa(hfxa)具有约46 kda的分子量,并且牛fxa(bfxa)具有约45.3 kda的分子量。
[0054]
因此,在一些实施例中,该方法需要将包含安得塞奈的测试样品与包含牛因子xa(bfxa)和直接因子xa(fxa)抑制剂的混合物混合。随后向该混合物中添加显色fxa底物,其中该显色fxa底物能够在与该bfxa反应时释放生色团。检测释放的生色团的量,其可以用于计算安得塞奈样品在从直接fxa抑制剂释放bfxa中的活性。
[0055]
在一些实施例中,显色fxa底物是spectrozyme-xa。
[0056]
在一些实施例中,提供了一种用于通过用人fxa(hfxa)和牛fxa(bfxa)两者测试参考安得塞奈来校准hfxa蛋白的活性的方法。然后,测试结果可以用于用bfxa活性表示hfxa活性。
[0057]
实例通过参考以下实例来进一步理解本披露,这些实例仅仅旨在示例本披露。本披露
的范围不受示例性实施例限制,这些示例性实施例仅仅旨在是本披露的单个方面的说明。任何功能等同的方法均在本披露的范围内。除了在本文描述的那些之外,从上文描述和附图,本披露的不同修改对本领域的技术人员而言将是显而易见的。这样的修改落入所附权利要求的范围内。
[0058]
实例1. 安得塞奈样品效力的测试该实例描述了一种确定安得塞奈α样品在中和因子xa抑制剂中的效力的测定。
[0059]
该测定基于安得塞奈α在由人fxa和贝曲西班组成的测定混合物中结合直接fxa抑制剂(贝曲西班马来酸盐)、并逆转对人fxa的抑制的能力来测量安得塞奈α的身份和效力。用fxa特异性显色底物测量恢复的人fxa活性,该显色底物在被fxa裂解时释放生色团。通过在软件程序中使用以4参数曲线拟合的斜率差进行的等效性检验对测试样品的响应与针对参考标准品获得的响应进行比较,以确定测试样品的效力。通过样品相比于参考品的ec50比率来计算效力。
[0060]
过程如下:1. 取出人fxa和fxa抑制剂(例如,贝曲西班,储备溶液226
ꢀµ
g/ml)的等分试样,并且在室温下解冻2. fxa参考标准品(rs)、测定对照和测试样品(ts)的制备a) 在测定缓冲液中制备0.6 mg/ml的参考标准品和每个测试样品的一式两份稀释液。除非另外说明,否则对于参考标准品使用释放时的实际测量浓度,并且使用所有测试样品的标示(靶)浓度。10.0 mg/ml时的最终体积参见以下实例示例稀释所需ts的量 = (0.6 mg/ml x 1000 μl)/10.0 mg/ml = 60.0 μl所需测定缓冲液的量 = 1000 μl
ꢀ‑ꢀ
60 μl = 940 μlb) 通过进行2.4倍的连续稀释,在稀释微孔板中制备参考标准品(rs)、测定对照(ctrl)、和测试样品(ts)的连续稀释液。示例稀释方案参见下文:示例连续稀释液:
稀释液编号样品的体积(
µ
l)测定缓冲液的体积(
µ
l)靶浓度(
µ
g/ml)最终浓度(
µ
g/ml)10.6mg/ml稀释液中30006003002稀释液1中1251752501253稀释液2中12517510452.14稀释液3中12517543.421.75稀释液4中12517518.19.046稀释液5中1251757.543.777稀释液6中1251753.141.578稀释液7中1251751.310.65419稀释液8中1251750.s450.27310稀释液9中1251750.2270.11411稀释液10中1251750.0950.047
3. fxa和贝曲西班(fxa抑制剂)的制备a) 在测定缓冲液中将fxa稀释至50 μg/ml,然后进一步稀释至1.0 μg/ml。
[0061]
b) 如下表所述,在测定缓冲液中将fxa抑制剂(226 μg/ml贝曲西班储备液)稀释
至40 ng/ml。
[0062]
c) 通过合并6 ml的1.0 μg/ml fxa和6 ml的40 ng/ml fxa抑制剂,将等体积的稀释的fxa和fxa抑制剂(贝曲西班)添加到适当的容器中。充分混合。
[0063]
4. fxa和fxa抑制剂对照的制备a) 通过将100 μl的稀释的fxa与300 μl的测定缓冲液混合,制备fxa对照。
[0064]
b) 通过混合200 μl的fxa抑制剂混合物和200 μl的测定缓冲液,制备fxa抑制物(贝曲西班)对照。
[0065]
5. 将50 μl/孔的参考标准品(rs)、测定对照(ctrl)和测试样品(ts)转移到测定板上。
[0066]
6. 向所有rs、ctrl、ts-1、ts-2孔中添加50 μl的人fxa/抑制剂混合物(其在步骤3(c) 中制备)。
[0067]
7. 将100 μl/孔的fxa对照和fxa/抑制剂对照转移到测定板上。向每个空白孔中添加100 μl的测定缓冲液。
[0068]
8. 在设置为在约300 rpm下混合的轨道板振动器上摇动板大约1分钟。
[0069]
9. 用粘性封板物覆盖板,并且在黑暗中孵育60
ꢀ±ꢀ
5分钟。
[0070]
10. 当样品正在孵育时,解冻并且制备浓度为2.0 mm的spectrozyme fxa底物。将4.5 ml的测定缓冲液添加到解冻的spectrozyme fxa底物的3.0 ml一次性等分试样中,并且充分混合。使用前立即制备该试剂。该体积足够用于1个测定板。
[0071]
11. 向所有孔中添加50 μl的制备的spectrozyme fxa底物,立即将板转移到设置为约300 rpm的板振动器上摇动大约1分钟。
[0072]
12. 在黑暗中孵育板10
ꢀ±ꢀ
1分钟,然后添加50 μl的终止溶液终止反应。
[0073]
13. 以405 nm作为测试波长,并且以490 nm作为参考波长,读取微孔板。
[0074]
14. 计算测试安得塞奈样品的效力实例2. 效力单位的校准实例1中检查的效力测定是基于在由安得塞奈、hfxa和贝曲西班组成的测定混合物中,安得塞奈结合直接fxa抑制剂(贝曲西班)并逆转其对人fxa(hfxa)活性的抑制的能力而开发的。用fxa特异性显色底物测量恢复的hfxa活性,该显色底物在被fxa裂解时释放生色团。将测试样品的逆转活性与安得塞奈参考标准品进行比较以获得比活性(以%或mg/mg表示)。实例1中使用的参考标准品是hfxa,其效力无法追溯到独立的国际参考标准品,这是因为直到最近才建立了hfxa国际参考标准品(例如who)。
[0075]
该实例描述了使用牛bfxa(hyphen-biomed公司)替换hfxa的直接效力单位测定的开发。已经针对英国国家生物制品检定所(national institute for biological standard and control)(nibsc)(英国)的国际参考标准品[nibsc代码:75/595]校准了bfxa活性。
[0076]
材料和方法人fxa(hfxa)购自血液技术公司(haematologic technologies, inc.)(埃塞克斯章克申,弗吉尼亚州(essex junction, vt))(目录号hcxa-0060)。在tris缓冲盐水(1xtbs,ph 7.4,0.1% bsa)中新鲜制备1.0 μg/ml的2x工作储备液。
[0077]
bfxa参考标准品购自hyphen biomed公司(法国)(目录号:be1010/be101k)。每一
小瓶的hyphen bfxa含有50 μg纯化牛fxa,或111单位/小瓶(即2.2单位/μg或0.45 μg/单位),针对非who国际参考标准品nibsc bfxa(75/595)进行校准。按照建议,用1 ml h2o将每个小瓶重构,得到50 μg/ml或111单位/ml。在1xtbs(ph 7.4,0.1% bsa)中制备0.9 μg/ml(2.0 u/ml)的工作储备液。
[0078]
将fxa抑制剂(贝曲西班)提供为1 mm(452 μg/ml,mw:425游离碱基)dmso储备溶液。在1xtbs(ph 7.4,0.1% bsa)中制备40 ng/ml的2x工作储备液,以与hfxa混合。当改变混合物中的贝曲西班浓度时,使400、300、200、40 ng/ml的可替代工作储备液与bfxa混合。
[0079]
fxa底物spectrozyme-xa底物购自sekisui diagnostics公司(列克星敦,马萨诸塞州(lexington, ma))(目录号222l)。将一小瓶的spectrozyme-fxa(50 μmol/小瓶)用10 ml h2o重构,得到5 mm储备溶液。在1xtbs(ph 7.4,0.1% bsa)中制备2 mm工作储备液。
[0080]
按照建议,用4.7 ml h2o将安得塞奈α(50 mg/小瓶)重构,得到9.7 mg/ml蛋白浓度(通过吸光度(a
280
))。将小等分试样储存在-80
°
c下。在1xtbs(ph 7.4,0.1% bsa)中制备0.6 mg/ml的工作储备液,并且将其用于制备0-600 μg/ml的标准品。
[0081]
结果目前用于安得塞奈样品的释放和稳定性测试的直接效力测定是通过混合等体积(50 μl)的每种试剂的终点方法。首先将人fxa和贝曲西班(抑制剂)制备为1.0 μg/ml(hfxa)和40 ng/ml(贝曲西班)的2x储备液,并且等体积(1 : 1混合)组合,分别得到混合物中的0.5 μg/ml的hfxa、20 ng/ml的贝曲西班。然后将hfxa/抑制剂混合物(50 μl)添加到反应混合物中。
[0082]
由制造商针对nibsc bfxa(75/595)参考标准品对hyphen bfxa的比活性进行校准。将重构的储备液浓度(50 μg/ml,111单位/ml,0.45 μg/单位)用作直接效力单位测定开发中的工作参考标准品。
[0083]
hfxa与hyphen bfxa之间的显色活性的比较在相同条件下,基于
µ
g/ml浓度,hyphen bfxa的显色活性比hfxa低约31%(图1)。观察结表明,需要优化直接效力测定的bfxa,因为通过匹配hfxa的质量或浓度,bfxa将具有较低的活性;而通过匹配活性,bfxa与hfxa相比将具有摩尔过量,并从而影响测定中的fxa/抑制剂比率和抑制程度。此外,发现贝曲西班对bfxa的抑制效力较弱。因此,关于bfxa和贝曲西班(抑制剂)两者的浓度,需要进一步优化测定条件。
[0084]
直接效力测定中hfxa与hyphen bfxa之间的比较直接效力单位测定的初始设置使用与直接效力测定中类似浓度的bfxa和hfxa(图2)。对于hfxa混合物,制备2x储备溶液,hfxa为1.0 μg/ml并且贝曲西班为40 ng/ml。通过等体积(1 : 1)混合制备hfxa(1x)/贝曲西班(1x)对照混合物,得到0.5 μg/ml hfxa和20 ng/ml贝曲西班。在直接效力测定中,向反应中添加50 μl的fxa/贝曲西班混合物。
[0085]
对于bfxa混合物,分别以0.9 μg/ml bfxa(2.0单位/ml)和200-400 ng/ml贝曲西班制备储备溶液。为了满足用于制备bfxa/贝曲西班混合物的体积要求,制备了较高的贝曲西班储备液浓度。通过混合适当体积的bfxa和贝曲西班制备bfxa(1x)/贝曲西班(1x)混合物,得到混合物中的0.5 μg/ml bfxa和20 ng/ml贝曲西班。在直接效力测定中,向反应中添加50 μl的fxa/贝曲西班混合物。
[0086]
如图2(a) 所示,与hfxa相比,bfxa在最高安得塞奈浓度下具有更低的吸光度,这
与观察到的bfxa更低的显色活性一致。然而,在贝曲西班的存在下,bfxa在不存在安得塞奈的情况下具有更高的背景,表明对bfxa活性的抑制更小。
[0087]
基于这些观察,在保持bfxa的相同浓度(1x)的同时,增加(1.5x、2.0x)混合物中的贝曲西班浓度,以便在不存在安得塞奈的情况下降低背景bfxa的活性。如图2(b-c) 中所示。在不存在安得塞奈的情况下,贝曲西班浓度的2倍增加将bfxa背景降低至与hfxa类似的水平。然而,在存在最高安得塞奈浓度时,使用bfxa(1x)的最大吸光度比使用hfxa(1x)/贝曲西班(1x)的对照低。
[0088]
直接效力测定中bfxa浓度的优化图3显示了在保持贝曲西班的相同浓度(2x)的同时改变bfxa浓度对最大吸光度的影响。具有bfxa(1.64x)/贝曲西班(2x)的混合物显示出可接受的最大吸光度,但是略高于hfxa对照(图3a)。用bfxa(1.45x)/贝曲西班(2x)进一步调节bfxa浓度,得到最终的优化条件,bfxa与hfxa对照之间具有相当的特性(图3b)。
[0089]
图3b中所示的优化条件满足在原始直接效力测定中用bfxa替换hfxa的预定测定设置,其中在最大和最小吸光度、ec
50
、和测定范围方面,bfxa与hfxa对照之间具有相当的特性。直接效力测定中使用的类似测定程序和标准可用于直接效力单位测定。
[0090]
因此,需要改变bfxa/贝曲西班混合物的制备,从而适应混合物中bfxa和贝曲西班浓度造成的变化。样品方案如下所示:1) bfxa(2.0 u/ml)的制备
‑ꢀ
通过向hyphen bfxa的小瓶中添加1.0 ml纯化水,重构bfxa(hyphen be101k,50
ꢀµ
g/小瓶)。这将产生50
ꢀµ
g/ml的bfxa(111单位/ml)。混合小瓶的内容物,并且将小瓶保持在冰上。
[0091]
‑ꢀ
在测定缓冲液中将重构的bfxa稀释至0.92
ꢀµ
g/ml(2.0单位/ml)。
[0092]
2) 贝曲西班储备溶液(200 ng/ml)的制备
‑ꢀ
在测定缓冲液中,将贝曲西班储备液稀释至200 ng/ml。
[0093]
3) bfxa/贝曲西班混合物的制备
‑ꢀ
将8体积的bfxa与2体积的贝曲西班混合,例如通过将8.0 ml的bfxa(0.92
ꢀµ
g/ml)与2.0 ml的贝曲西班(200 ng/ml)混合。
[0094]
‑ꢀ
将bfxa/贝曲西班混合物(50
ꢀµ
l)添加至直接效力单位测定混合物中。
[0095]
50
ꢀµ
l混合物中的bfxa浓度/质量分别是1.6单位/ml和0.08单位。50
ꢀµ
l混合物中的贝曲西班浓度/质量分别是40 ng/ml和2 ng。
[0096]
由于测定中使用的hyphen bfxa已经针对nibsc bfxa(75/595)进行了校准,用于安得塞奈α参考标准品的直接效力单位可追溯到独立的国际参考标准品。另外,hyphen bfxa可以用于校准hfxa参考样品。
[0097]
最近可获得的hfxa国际参考标准品[nibsc代码:15/102]可以与bfxa参考标准品类似地用于hfxa校准,或直接用于可追溯至独立国际参考标准品的效力单位测定。*
ꢀꢀꢀꢀꢀ
*
ꢀꢀꢀꢀꢀ
*
[0098]
本文中提及或引用的文章、专利和专利申请、以及所有其他文件和电子可用信息的内容特此通过引用以其全文并入,其程度如同特别地且单独地指示将每个单独出版物通过引用并入一样。
[0099]
申请人保留将任何这样的文章、专利、专利申请、或其他物理和电子文件中的任何和所有材料和信息实际并入本技术的权利。
[0100]
本文已经对本披露进行了广泛和一般性的描述。落入一般性披露之内的每个较窄种类和亚属分组也构成本披露的一部分。这包括具有从该类中去除任何主题的附带条件或否定限制的本披露的一般性描述,无论本文是否特别列举了去除的材料。其他实施例在以下权利要求内。此外,本披露的特征或方面以马库什组的形式描述时,本领域技术人员将认识到,本披露由此也以马库什组中任何单独成员或成员亚组的形式描述。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1