T细胞双特异性抗体相关不良反应的预防或减轻的制作方法
本发明涉及预防或减轻与t细胞双特异性抗体有关的不良反应,例如细胞因子释放综合征。具体地,本发明涉及预防或减轻因使用例如达沙替尼等酪氨酸激酶抑制剂而产生的副作用。
背景技术:
1、t细胞结合子或t细胞双特异性抗体(tcb)是通过一个结合部分识别靶细胞抗原(例如在肿瘤细胞上表达的肿瘤抗原)的双特异性抗体,以及通过另一个结合部分识别t细胞受体。tcb作为癌症免疫治疗剂有着广阔的前景。cd3与靶细胞抗原的交联触发t细胞活化、增殖和细胞因子释放,导致靶细胞杀伤(bacac等人,clin cancer res(2016)22,3286-97;bacac等人,oncoimmunology(2016)5,e1203498)。然而,因为中靶在瘤(on-target ontumor)、中靶脱瘤(on target off tumor)细胞毒性活性和细胞因子释放,tcb治疗有时与安全责任相关。据报道,tcb最常见的不良反应之一是细胞因子释放综合征(crs)。这种复杂的临床综合征以发热、低血压和呼吸不足为特征,并与促炎细胞因子诸如il-6、tnf-α、ifn-γ和il-1β的释放有关(参见例如shimabukuro-vornhagen等人,j immunother cancer(2018)6,56)。如果靶抗原在健康细胞中表达,则可能会发生肿瘤外毒性,这可能会导致组织损伤并危及患者的安全。非常需要减轻这些危及生命的毒性的方法,例如对tcb诱导的t细胞活化和增殖的药理学阻断。酪氨酸激酶抑制剂达沙替尼被认定为关闭car-t细胞功能的有效候选药物(weber等人,blood advances(2019)3,711-7;mestermann等人,scitransl med(2019)11,eaau5907)。另一方面,达沙替尼与t细胞结合子blinatumomab的同时施用似乎不会损害后者的活性(chiaretti等人,blood(2019)134(supplement 1),740;foà等人,n engl j med(2020)383,1613-1623)。
技术实现思路
1、本发明人已经发现,酪氨酸激酶抑制剂,特别是达沙替尼,可以用作药理学开/关的开关以通过t细胞参与疗法减轻肿瘤外毒性或crs。
2、使用人外周血单核细胞的靶细胞杀伤的体外模型,发明人评估了达沙替尼与四种示例性tcb(cea-tcb、cd20-tcb和cd19-tcb,作为肿瘤表面靶向tcb的实例,以及hla-a2 wt-1-tcb,作为tcr样-tcb的实例)组合对t细胞活化和增殖、靶细胞杀伤和细胞因子释放的可逆作用。使用达沙替尼的剂量反应进行杀伤测定,以确定完全抑制tcb诱导的t细胞活化的阈值。此外,发明人提出低于该阈值的达沙替尼浓度可用于控制tcb诱导的细胞因子释放。这些抵消作用可以在临床相关剂量的达沙替尼浓度下获得,并且可用于在crs症状无法通过标准干预控制的情况下诱导阻断tcb诱导的t细胞活化或用于减少细胞因子释放作为tnf的替代品或il-6r阻断。本实例中的数据表明,达沙替尼可以作为tcb介导的t细胞活化的可逆开/关的开关,该可逆开/关的开关可用于减轻tcb诱导的肿瘤内和肿瘤外毒性,包括crs。
3、因此,在第一方面,本发明提供t细胞双特异性抗体,其用于治疗个体中的疾病,其中该治疗包括
4、(a)对该个体施用该t细胞双特异性抗体,以及
5、(b)对该个体施用酪氨酸激酶抑制剂(tki)以预防或减轻与施用该t细胞双特异性抗体有关的不良反应。
6、本发明进一步提供了t细胞双特异性抗体在制备用于治疗个体中的疾病的药物中的用途,其中该治疗包括
7、(a)对该个体施用该t细胞双特异性抗体,以及
8、(b)对该个体施用酪氨酸激酶抑制剂(tki)以预防或减轻与施用该t细胞双特异性抗体有关的不良反应。
9、本发明还提供了治疗个体中的疾病的方法,其中该方法包括
10、(a)对该个体施用t细胞双特异性抗体,以及
11、(b)对该个体施用酪氨酸激酶抑制剂(tki)以预防或减轻与施用该t细胞双特异性抗体有关的不良反应。
12、在另一方面,本发明提供了酪氨酸激酶抑制剂(tki),其用于预防或减轻与向个体施用t细胞双特异性抗体有关的不良反应。
13、本发明进一步提供了酪氨酸激酶抑制剂(tki)在制备用于预防或减轻与向个体施用t细胞双特异性抗体有关的不良反应的药物中的用途。
14、本发明还提供了预防或减轻与向个体施用t细胞双特异性抗体有关的不良反应的方法,该方法包括向个体施用酪氨酸激酶抑制剂(tki)。
15、供使用的t细胞双特异性抗体、供使用的tki、以上和本文所述的用途或方法可以单独或组合地并入以下描述的任何特征(除非上下文另有说明)。
16、除非本文另外定义,否则本文所用的术语为本技术领域中的一般使用。
17、在一些方面,tki是lck和/或src激酶抑制剂。在更具体的方面,tki是达沙替尼。
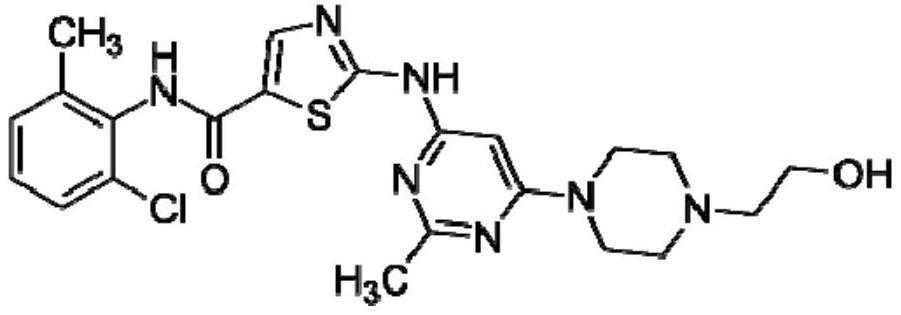
18、“达沙替尼”是一种酪氨酸激酶抑制剂(tki)。它以(除其他外)品牌出售,用于治疗某些慢性骨髓性白血病(cml)和急性淋巴细胞性白血病(all)的病例。其cas号、iupac名称和化学结构如下所示。
19、cas号:302962-49-8
20、iupac名称:n-(2-氯-6-甲基苯基)-2-[[6-[4-(2-羟乙基)-1-哌嗪基]-2-甲基-4-嘧啶基]氨基]-5-噻唑甲酰胺一水合物
21、化学结构:
22、
23、在一些方面,(施用)tki引起t细胞双特异性抗体活性的抑制。
24、t细胞双特异性抗体的“活性”是指由t细胞双特异性抗体在个体体内引起的反应。这种活性可以包括t细胞,特别是cd4+和/或cd8+ t细胞的细胞反应,诸如增殖、分化、细胞因子分泌、细胞毒性效应分子释放、细胞毒性活性和活化标志物的表达,和/或对靶细胞的效应,特别是表达t细胞双特异性抗体的靶细胞抗原的靶细胞(例如肿瘤细胞),诸如靶细胞的裂解。
25、在一些方面,(施用)tki引起(由t细胞双特异性抗体诱导的)t细胞活化的抑制。
26、如本文中所使用的“t细胞活化”(activation of t cells或t cellactivation),是指t淋巴细胞(特定是cd4+或cd8+ t细胞)的一种或多种细胞反应,选自:增殖、分化、细胞因子分泌、细胞毒性效应分子释放、细胞毒性活性和活化标志物的表达。测定t细胞活化的合适分析是本技术中已知的并在本文中描述。在特定方面,t细胞活化通过测量t细胞上cd25和/或cd69的表达来确定,例如通过流式细胞术。
27、在一些方面,(施用)tki引起(由t细胞双特异性抗体诱导的)t细胞增殖的抑制。在一些方面,(施用)tki引起(由t细胞双特异性抗体诱导的)t细胞的细胞毒性活性的抑制。
28、t细胞的“细胞毒性活性”是指t淋巴细胞,特别是cd4+或cd8+ t细胞对靶细胞的裂解(即杀伤)的诱导。细胞毒性活性通常涉及t淋巴细胞的脱粒,这与t淋巴细胞释放细胞毒性效应分子诸如颗粒酶b和/或穿孔素有关。
29、在一些方面,(施用)tki引起(由t细胞双特异性抗体诱导的)t细胞中的t细胞受体信号传导的抑制。
30、“t细胞受体信号传导”是指t淋巴细胞中t细胞受体(tcr)下游信号传导通路在tcr接合后的活性(诸如t细胞双特异性抗体接合tcr的cd3ε亚单位),涉及信号传导分子,包括酪氨酸激酶,诸如lck激酶。
31、在一些方面,(施用)tki引起(由t细胞双特异性抗体诱导的)t细胞细胞因子分泌的抑制。在一些方面,该细胞因子是选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组中的一种或多种细胞因子。在一些方面,该t细胞是cd8+ t细胞或cd4+细胞。
32、在一些方面,该抑制是可逆的(即,该抑制可以被解除,使得被抑制参数的水平恢复到接近其在抑制之前的水平)。在一些方面,在给定时间段内(即在停止施用tki之后)tki没有被施用(向个体)后,该抑制被逆转。在一些方面,该时间段是约1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、20小时、24小时、36小时、48小时、72小时或96小时。
33、该抑制可以是部分的或完全的。在一些方面,该抑制具有临床意义和/或统计学意义。
34、在一些方面,(施用)tki引起个体中一种或多种细胞因子的血清水平减少。在一些方面,该一种或多种细胞因子选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组。在一些方面,在给定的时间量未(向个体)施用tki之后,该减少持续。在一些方面,该时间量是约1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、20小时、24小时、36小时、48小时、72小时或96小时。在一些方面,该减少在后续施用t细胞双特异性抗体之后持续。特别地,即使在停止施用tki/没有进一步施用tki之后,该减少仍持续。该血清水平的减少特别是与未施用tki的个体(包括同一个体)中的血清水平相比(即在这种情况下,与未施用/施用tki之前相比,血清水平减少)。该血清水平的减少特别是与施用(特别是第一次施用)t细胞双特异性抗体但不施用tki的个体(包括同一个体)中的血清水平相比(即在这种情况下,与施用t细胞双特异性抗体/施用t细胞双特异性抗体之后但未施用tki/施用tki之前相比,血清水平减少)。在没有该减少的情况下,血清水平和/或细胞因子分泌特别地可能相对于(施用)t细胞双特异性抗体而升高/增加。在一些方面,该减少具有临床意义和/或统计学意义。
35、在一些方面,该不良反应是细胞因子释放综合征(crs)。
36、有时也称为“副作用”或“不良事件”(特别是在临床研究中)的“不良反应”是药物治疗个体(在本文中特别是使用t细胞双特异性抗体)导致的有害和不希望的影响。
37、“细胞因子释放综合征”(简称“crs”)是指在施用治疗剂(例如t细胞双特异性抗体)期间或之后不久(例如,在1天内)在受试者的血液中细胞因子水平升高,诸如肿瘤坏死因子α(tnf-α)、干扰素γ(ifn-γ)、白细胞介素6(il-6)、白细胞介素2(il-2)及其他,导致不良症状。crs是对治疗剂的不良反应,并且与施用治疗剂及时相关。它通常发生在施用治疗剂期间或之后不久,即通常在施用(通常是输注)之后24小时内,主要是在第一次施用时。在一些情况下,例如在施用car-t细胞后,crs也可能会在稍后发生,例如在car-t细胞扩增施用之后几天。发生率和严重程度通常随着后续施用而降低。症状可能从症状性不适到致命事件,并且可能包括发烧、发冷、头晕、高血压、低血压、缺氧、呼吸困难、烦躁、出汗、潮红、皮疹、心动过速、呼吸急促、头痛、肿瘤痛、恶心、呕吐和/或器官衰竭。
38、在一些方面,该不良反应是发烧、低血压和/或缺氧。在一些方面,该不良反应是一种或多种细胞因子的血清水平升高。该升高的血清水平特别是与健康个体的血清水平和/或未施用t细胞双特异性抗体的个体(包括同一个体)中的血清水平相比(即在这种情况下血清水平与未施用t细胞双特异性抗体的血清水平相比升高)。在一些方面,该一种或多种细胞因子选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组。
39、在一些方面,该不良反应是与t细胞双特异性抗体与表达t细胞双特异性抗体的靶细胞抗原的非癌细胞结合相关的不良反应(即,在靶/脱肿瘤效应)。非癌细胞可以是正常(即非癌性)细胞和/或健康组织中(即肿瘤外)的细胞。在一些方面,该不良反应是与t细胞双特异性抗体与其靶细胞抗原的结合无关的不良反应(即脱靶效应)。
40、在一些方面,tki的施用是在(个体的)不良反应的(临床上)显现时进行的。该施用可以是,例如,在不良反应显现(即出现副作用的临床症状,如发热)后约1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、20小时或24小时内。在一些方面,tki的施用是响应(个体的)不良反应的(临床上)显现。
41、在一些方面,tki的施用是在t细胞双特异性抗体的施用之前。在一些方面,tki的施用与t细胞双特异性抗体的施用同时进行。在一些方面,tki的施用是在t细胞双特异性抗体的施用之后。当tki的施用是在t细胞双特异性抗体的施用之前或之后,tki的这种施用可以是例如分别在施用t细胞双特异性抗体之前或之后的约1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、20小时或24小时内。tki的施用可以是间歇性或连续性地。在一些方面,tki的施用为口服。
42、在一些方面,tki的施用剂量足以引起t细胞双特异性抗体活性的抑制。在一些方面,tki的施用剂量足以引起(由t细胞双特异性抗体诱导的)t细胞活化的抑制。在一些方面,tki的施用剂量足以引起(由t细胞双特异性抗体诱导的)t细胞增殖的抑制。在一些方面,tki的施用剂量足以引起(由t细胞双特异性抗体诱导的)t细胞的细胞毒性活性的抑制。在一些方面,tki的施用剂量足以引起(由t细胞双特异性抗体诱导的)t细胞中t细胞受体信号传导的抑制。在一些方面,tki的施用剂量足以引起(由t细胞双特异性抗体诱导的)t细胞分泌细胞因子的抑制。在一些方面,该细胞因子是选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组中的一种或多种细胞因子。在一些方面,该t细胞是cd8+ t细胞或cd4+细胞。该抑制可以是部分的或完全的。在一些方面,该抑制具有临床意义和/或统计学意义。
43、在一些方面,tki的施用剂量足以引起个体中一种或多种细胞因子的血清水平的减少。在一些方面,tki的施用剂量足以引起个体中一种或多种细胞因子的血清水平的减少但不足以引起t细胞双特异性抗体活性的抑制。在一些方面,施用tki的剂量足以造成个体中的免疫细胞的一种或多种细胞因子的分泌减少,但不足以抑制t细胞活化和/或抑制由t细胞双特异性抗体所诱导的t细胞的细胞毒性活性。在一些方面,该一种或多种细胞因子选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组。在一些方面,该t细胞是cd8+ t细胞或cd4+细胞。免疫细胞可包括各种免疫细胞类型,诸如t细胞、巨噬细胞、nk细胞等。
44、该血清水平或细胞因子分泌的降低特别是与未施用tki的个体(包括同一个体)中的血清水平或细胞因子分泌相比(即在这种情况下,与未施用/施用tki之前相比,血清水平降低)。该血清水平或细胞因子分泌的降低特别是与施用(特别是第一次施用)t细胞双特异性抗体但不施用tki的个体(包括同一个体)中的血清水平或细胞因子分泌相比(即在这种情况下,与施用t细胞双特异性抗体/施用t细胞双特异性抗体之后但未施用tki/施用tki之前相比,血清水平降低)。在没有该减少的情况下,血清水平和/或细胞因子分泌特别地可能相对于(施用)t细胞双特异性抗体而升高/增加。在一些方面,该减少具有临床意义和/或统计学意义。该抑制可以是部分的或完全的。在一些方面,该抑制具有临床意义和/或统计学意义。
45、在一些方面,以有效剂量施用tki。
46、药剂例如tki或t细胞双特异性抗体的“有效量”或“有效剂量”是指在必要的剂量和时间段达到预期的治疗或预防效果所需的有效量。
47、在一些方面,tki的施用剂量为约10mg、20mg、30mg、40mg、50mg、60mg、70mg、80mg、90mg、100mg、110mg、120mg、130mg、140mg、150mg、160mg、170mg、180mg、190mg或200mg。在一些方面,tki的施用剂量为约20mg。在一些方面,tki的施用剂量为约70mg。在一些方面,tki的施用剂量为约80mg。在一些方面,tki的施用剂量为约100mg。在一些方面,tki的施用剂量为约140mg。
48、在一些方面,tki的施用剂量为约100mg或更低。在一些方面,tki的施用剂量为约20mg。在一些方面,tki的施用剂量为约70mg。在一些方面,tki的施用剂量为约80mg。在一些方面,tki的施用剂量为约100mg。在此类方面,tki的剂量可能足以引起个体中一种或多种细胞因子的血清水平降低但不足以抑制t细胞双特异性抗体的活性,或足以引起个体中免疫细胞对一种或多种细胞因子的分泌减少,但不足以抑制由t细胞双特异性抗体诱导的t细胞的活化和/或t细胞的细胞毒性活性。
49、在一些方面,tki为每天施用。在一些方面,tki每天施用一次。在一些方面,tki以约100mg的剂量每天施用一次。在一些方面,tki的施用是在不良反应持续的时间段期间(即tki的施用是从不良反应的显现到不良反应的减轻或消失)。在一些方面,在防止或减轻不良反应后停止施用tki。在一些方面,在不良反应减轻或消失后停止施用tki。该减少特别具有临床意义和/或统计学意义。在一些方面,tki的施用是一次、两次、三次、四次、五次、六次、七次、八次、九次或十次,特别是在用t细胞双特异性抗体治疗个体的过程中的一次、两次、三次、四次、五次,六次、七次、八次、九次或十次。在一些方面,tki的施用持续1天、2天、3天、4天、5天、6天、7天、8天、9天或10天。在一些方面,tki的施用为每日一次持续1天、2天、3天、4天、5天、6天、7天、8天、9天或10天。在一些方面,tki的施用与t细胞双特异性抗体的第一次施用相关。该第一次施用特别是在用t细胞双特异性抗体治疗个体的过程中第一次施用t细胞双特异性抗体。在一些方面,tki的施用与t细胞双特异性抗体的第一次施用同时进行。在一些方面,tki的施用是在t细胞双特异性抗体的第一次施用之前。在一些方面,tki的施用是在t细胞双特异性抗体的第一次施用之后。在一些方面,tki的施用是在t细胞双特异性抗体的第一次施用之后并且在t细胞双特异性抗体的第二次施用之前。当tki的施用是在t细胞双特异性抗体的(第一次)施用之前或之后,tki的这种施用可以是例如分别在施用t细胞双特异性抗体之前或之后的约1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、20小时或24小时内。
50、在一些方面,t细胞双特异性抗体的施用比tki的施用持续更长的时间段。在一些方面,在停止施用tki后继续施用t细胞双特异性抗体。在一些方面,t细胞双特异性抗体的施用是单次施用或重复施用。在用t细胞双特异性抗体治疗个体的过程中,t细胞双特异性抗体可以施用一次或多次。例如,用t细胞双特异性抗体治疗个体可包括多个治疗周期,每个治疗周期包括t细胞双特异性抗体的一次或多次施用。在一些方面,t细胞双特异性抗体的施用包括第一次和第二次施用。
51、为了在本发明中使用,t细胞双特异性抗体将以符合良好医疗实践的方式予以配制、给药和施用。在这种情况下,考虑的因素包括所治疗的特定疾患、所治疗的特定哺乳动物、个体患者的临床病症、疾患的原因、药剂的递送部位、施用方法、施用的时间安排以以及执业医师已知的其他因素。
52、在一些方面,以有效剂量施用t细胞双特异性抗体。对于全身施用,最初可以从诸如细胞培养物测定的体外测定估计有效剂量。然后可以在动物模型中制定剂量,以达到包括细胞培养物中确定的ic50在内的循环浓度范围。此类信息可用于更准确地确定对人体有用的剂量。也可以使用本技术领域中熟知的技术,根据体内数据(例如动物模型)估计初始剂量。可以单独调节剂量和间隔来提供足以维持治疗效果的t细胞双特异性抗体的血浆水平。通过注射施用的常见患者剂量在约0.1-50mg/kg/天的范围内,通常范围为0.5-1mg/kg/天。可以通过每天施用多种剂量来实现治疗有效的血浆浓度。血浆中的浓度可以例如通过hplc来测量。
53、可以施用有效量的t细胞双特异性抗体来预防或治疗疾病。t细胞双特异性抗体的适当施用途径和剂量可基于所治疗的疾病类型、t细胞双特异性抗体的类型、疾病的严重程度和病程、个体的临床状况、个体的临床病史和对治疗的反应,以及主治医生的判断力来确定。给药可通过任何合适的途径进行,例如通过注射,诸如静脉内或皮下注射,部分取决于短暂施用还是长期施用。本文中考虑各种给药方案,其包括但不限于在多种时间点单次或多次给药、快速注射给药和脉冲输注。
54、t细胞双特异性抗体和tki可以通过任何合适的途径施用,并且可以通过相同的施用途径或通过不同的施用途径来施用。在一些方面,t细胞双特异性抗体的施用是肠胃外的,特别是静脉内的。
55、在一些方面,t细胞双特异性抗体的施用是t细胞双特异性抗体对个体的第一次施用,特别是在用t细胞双特异性抗体治疗个体的过程中第一次施用t细胞双特异性抗体。
56、在一些方面,(施用)t细胞双特异性抗体诱发(即引起或增加)t细胞的活化。在一些方面,(施用)t细胞双特异性抗体诱发t细胞的增殖。在一些方面,(施用)t细胞双特异性抗体诱发t细胞的细胞毒性活性。在一些方面,(施用)t细胞双特异性抗体诱发t细胞中的t细胞受体信号传导。在一些方面,(施用)t细胞双特异性抗体诱发t细胞分泌细胞因子。在一些方面,细胞因子是选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组中的一种或多种细胞因子。在一些方面,该t细胞是cd8+ t细胞或cd4+细胞。
57、在一些方面,t细胞双特异性抗体的施用导致t细胞,特别是细胞毒性t细胞的活化,特别是在癌症部位(例如在实体瘤癌症内)。该活化可包含t细胞增殖、t细胞分化、t细胞分泌细胞因子、t细胞释放细胞毒性效应分子、t细胞的细胞毒性活性和t细胞活化标志物的表达。在一些方面,t细胞双特异性抗体的施用导致癌症部位(例如实体瘤癌症内)的t细胞,特别是细胞毒性t细胞的数量增加。
58、下面描述可用于本发明的t细胞双特异性抗体。
59、“t细胞双特异性抗体”是指能够结合,包括同时结合t细胞(通常经由在t细胞上表达的抗原决定簇,诸如cd3)和靶细胞(通常经由在靶细胞上表现的抗原决定簇,诸如cea、cd19、cd20或hla-a2/wt1)的抗体。
60、在根据本发明的优选方面,t细胞双特异性抗体能够同时结合t细胞上的抗原决定簇(即第一抗原,例如cd3)和靶细胞上的抗原决定簇(即第二抗原,例如cea、cd19、cd20或hla-a2/wt1)。在一些方面,t细胞双特异性抗体能够通过同时结合cd3和靶细胞抗原而交联t细胞和靶细胞。在甚至更优选的方面,这种同时结合导致靶细胞,特定是表达肿瘤细胞的靶细胞抗原(例如cea、cd19、cd20或hla-a2/wt1)裂解。在一些方面,这种同时结合导致t细胞活化。在一些方面,这种同时结合导致t细胞的细胞反应,该细胞反应选自以下项的组:增殖、分化、细胞因子分泌、细胞毒性效应分子释放、细胞毒性活性和活化标志物的表达。在一些方面,t细胞双特异性抗体与cd3结合而不同时与靶细胞抗原结合,不导致t细胞活化。在一些方面,t细胞双特异性抗体能够将t细胞的细胞毒性活性重定向至靶细胞。在优选方面,该重定向不依赖于靶细胞的mhc介导的肽抗原呈递和/或t细胞的特异性。
61、术语“双特异性”是指抗体能够与至少二个不同的抗原决定簇结合。通常,双特异性抗体包含两个抗原结合位点,其中每个抗原结合位点对不同抗原决定簇具有特异性。在某些方面,双特异性抗体能够同时结合两个抗原决定簇,特定是在两种不同细胞上表达的两个抗原决定簇。
62、如本文所使用,术语“抗原决定簇”与“抗原”和“表位”同义,并且是指多肽大分子上与抗原结合部分结合,形成抗原结合部分-抗原复合物的位点(例如,一段连续的氨基酸或由非连续氨基酸的不同区域组成的构象构型)。例如,可用的抗原决定簇可存在于肿瘤细胞的表面上、受病毒感染的细胞的表面上、其他患病细胞的表面上、免疫细胞的表面上,不存在于血清中,和/或存在于细胞外基质(ecm)中。
63、如本文所使用,术语“抗原结合部分”,是指结合,包括特异性结合抗原决定簇的多肽分子。在一些方面,抗原结合部分能够将其所附接的实体(例如第二抗原结合部分)引导至靶位点,例如引导至携带抗原决定簇的特定类型的肿瘤细胞。在另外的方面,抗原结合部分能够通过其靶抗原(例如t细胞受体复合物抗原)活化信号传导。抗原结合部分包括如本文进一步定义的抗体及其片段。特定抗原结合部分包括抗体的抗原结合结构域,其包含抗体重链可变区和抗体轻链可变区。在某些方面,抗原结合部分可包括如本文进一步定义和本技术中已知的抗体恒定区。可用的重链恒定区包括五种同种型(isotype)中的任一者:α、δ、ε、γ或μ。可用的轻链恒定区包括二种同种型中的任一者:κ和λ。
64、“特异性结合”是指结合对抗原具有选择性并且可区分出不想要或非特定的相互作用。本文中的术语“结合”(bind/binding)一般是指“特异性结合”。抗原结合部分结合特异性抗原决定簇的能力可通过酶联免疫吸附测定(elisa)或本领域技术人员熟悉的其他技术,例如表面等离子体共振(spr)技术(例如于biacore仪器上分析)(liljeblad等人,glycoj17,323-329(2000))和传统的结合测定(heeley,endocr res 28,217-229(2002))来测定。在一些方面,抗原结合部分结合不相关的蛋白质的程度小于抗原结合部分结合抗原的约10%,例如通过spr。在某些方面,与抗原结合的抗原结合部分或包含该抗原结合部分的抗体具有≤1μm、≤100nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm或≤0.001nm(例如10-8m或更小,例如10-8m至10-13m,例如,10-9m至10-13m)的解离常数(kd)。
65、“亲和力”指分子(例如受体)的单个结合位点与其结合配偶体(例如配体)之间的非共价相互作用总和的强度。除非另有说明,否则如本文中所使用的“结合亲和力”,是指反映结合对成员(例如,抗原结合部分和抗原或受体及其配体)之间1:1相互作用的内在结合亲和力。分子x对其搭配物y的亲和力通常可以用解离常数(kd)表示,其是解离速率常数与缔合速率常数(分别为koff和kon)的比。因此,等效亲和力可包括不同速率常数,只要速率常数比保持相同即可。可通过本领域已知的成熟的方法测量亲和力,该方法包括那些本文所述的方法。用于测定亲和力的特定方法为表面等离子体共振(spr)。
66、除非另有说明,否则“cd3”是指源自任何脊椎动物的任何天然cd3,该脊椎动物包括哺乳动物,诸如灵长类动物(例如人)、非人灵长类动物(例如食蟹猴)和啮齿动物(例如小鼠和大鼠)。该术语涵盖“全长”、未处理的cd3以及在细胞处理中得到的任何形式的cd3。该术语还涵盖天然生成的cd3变体,例如,剪接变体或等位基因变体。在一些方面,cd3是人cd3,特定是人cd3的ε亚基(cd3ε)。人cd3ε的氨基酸序列显示于uniprot(www.uniprot.org)登录号p07766(版本144)或ncbi(www.ncbi.nlm.nih.gov/)refseq np_000724.1。也可参见seq id no:25。食蟹猴[macaca fascicularis]cd3ε的氨基酸序列显示于ncbi genbank号bab71849.1。也可参见seq id no:26。
67、如本文中所使用的“靶细胞抗原”是指存在于靶细胞表面上的抗原决定簇,该靶细胞例如肿瘤中的细胞,诸如癌细胞或肿瘤基质的细胞(在此情况下为“肿瘤细胞抗原”)。优选地,靶细胞抗原不是cd3,和/或与cd3在不同的细胞上表达。在一些方面,靶细胞抗原为cea,特别是人cea。在其他方面,靶细胞抗原为hla-a2/wt1,特别是人hla-a2/wt1。在一些方面,靶细胞抗原为cd20,特别是人cd20。在一些方面,靶细胞抗原为cd19,特别是人cd19。
68、如本文所使用,关于抗原结合部分的术语“第一”、“第二”或“第三”,是用于方便区分每一类型的部分何时存在多于一个。除非明确说明,否则使用这些术语并非旨在赋予双特异性抗体特定的顺序或方向。
69、如本文中所使用的术语“价”,表示抗体中存在指定数量的抗原结合位点。因此,术语“与抗原单价结合”表示在抗原结合分子中存在对抗原具有特异性的一个(并且不超过一个)抗原结合位点。
70、本文中的术语“抗体”以最广义使用且涵盖各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(例如双特异性抗体)和抗体片段,只要它们展示出预期抗原-结合活性即可。
71、术语“全长抗体”、“完整抗体”和“全抗体”在本文中可互换使用,是指具有与天然抗体结构基本类似的结构的抗体。
72、“抗体片段”是指除完整抗体以外的分子,其包含结合完整抗体所结合的抗原的完整抗体的一部分。抗体片段的实例包括(但不限于)fv、fab、fab'、fab’-sh、f(ab')2、双体抗体、线性抗体、单链抗体分子(例如scfv)和单结构域抗体。关于某些抗体片段的综述,参见hudson等人,nat med 9,129-134(2003)。关于scfv片段的综述,请参见pluckthün,thepharmacology of monoclonal antibodies,第113卷,rosenburg和moore编,springer-verlag,new york,第269-315页(1994);也可参见wo 93/16185;以及美国专利第5,571,894号和第5,587,458号。关于包含补救受体结合抗原决定簇残基并且具有增加的体内半衰期的fab和f(ab')2片段的论述,参见美国第5,869,046号专利。双体抗体为具有两个抗原结合位点(其可以是二价或双特异性的)的抗体片段。参见例如ep 404,097;wo 1993/01161;hudson等人,nat med 9,129-134(2003);以及hollinger等人,proc natl acad sci usa90,6444-6448(1993)。hudson等人,nat med9,129-134(2003)中也描述了三体抗体和四体抗体。单结构域抗体为包含抗体的全部或部分重链可变结构域或抗体的全部或部分轻链可变结构域的抗体片段。在某些方面,单结构域抗体为人单结构域抗体(domantis,inc.,waltham,ma;参见例如美国专利第6,248,516b1号)。抗体片段可通过各种技术制造,包括但不限于如本文所述的完整抗体的蛋白水解消化以及重组宿主细胞(例如大肠杆菌或噬菌体)的产生。
73、术语“可变区”或“可变结构域”是指参与抗体与抗原结合的抗体重链或轻链的结构域。天然抗体的重链和轻链(分别为vh和vl)的可变结构域通常具有类似的结构,且每个结构域均包含四个保守框架区(fr)和三个高变区(hvr)。请参见kindt等人,kubyimmunology,第6版,w.h.freeman和co.,第91页(2007)。单个vh或vl结构域可能足以赋予抗原结合特异性。如在本文中结合可变区序列所使用的“kabat编号”,是指kabat等人,sequences of proteins of immunological interest,第5版public health service,national institutes of health,bethesda,md(1991)描述的编号系统。
74、如本文中所使用的重链和轻链的所有恒定区和结构域的氨基酸位置,根据描述于kabat等人,sequences of proteins of immunological interest,第5版,public healthservice,national institutes of health,bethesda,md(1991)的kabat编号系统(在本文中称为“根据kabat编号”或“kabat编号”)编号。具体地,kabat编号系统(参见kabat等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,md(1991)的第647-660页)用于卡帕和兰姆达同种型的轻链恒定结构域cl和kabat eu索引编号系统(参见第661-723页)用于重链恒定结构域(ch1、铰链、ch2和ch3),在此情况中,其于本文中通过参考“根据kabat eu索引编号”进一步阐明。
75、如本文所用,术语“高变区”或“hvr”是指抗体可变结构域中序列高度可变并确定抗原结合特异性的各个区,例如“互补决定区”(“cdr”)。通常,抗体包括六个cdr:三个在vh中(hcdr1、hcdr2、hcdr3),以及三个在vl中(lcdr1、lcdr2、lcdr3)。在本文中,例示性cdr包括:
76、(a)高变环存在于氨基酸残基26-32(l1)、50-52(l2)、91-96(l3)、26-32(h1)、53-55(h2)、和96-101(h3)处(chothia和lesk,j.mol.biol.196:901-917(1987));
77、(b)cdr存在于氨基酸残基24-34(l1)、50-56(l2)、89-97(l3)、31-35b(h1)、50-65(h2)、和95-102(h3)处(kabat et al.,sequencesof proteins of immunologicalinterest,第5版public health service,national institutes of health,bethesda,md(1991));以及
78、(c)抗原接触存在于氨基酸残基27c-36(l1)、46-55(l2)、89-96(l3)、30-35b(h1)、47-58(h2)、和93-101(h3)处(maccallum等人j.mol.biol.262:732-745(1996))。
79、除非另有说明,否则cdr根据kabat等人在上述文献中所述的方法来确定。本领域的技术人员将理解,也可以根据chothia在上述文献、mccallum在上述文献中所述的方法或任何其他科学上接受的命名系统来确定cdr名称。
80、“骨架”或“fr”是指除高变区(hvr)残基之外的可变结构域残基。可变结构域的fr通常由四个fr结构域组成:fr1、fr2、fr3、和fr4。因此,hvr和fr序列通常以如下顺序出现在vh(或vl)中:fr1-h1(l1)-fr2-h2(l2)-fr3-h3(l3)-fr4。
81、抗体或免疫球蛋白的“类别(class)”是指为其重链所具有的恒定结构域或恒定区的类型。有五大类抗体:iga、igd、ige、igg和igm,且其中的几种可进一步分为亚类(同种型),例如igg1、igg2、igg3、igg4、iga1和iga2。对应于不同类别的免疫球蛋白的重链恒定结构域分别称为α、δ、ε、γ和μ。
82、“fab分子”是指由免疫球蛋白的重链(“fab重链”)的vh和ch1结构域和轻链(“fab轻链”)的vl和cl结构域组成的蛋白质。
83、“交叉(crossover)”fab分子(也称为“crossfab”)是指这样的fab分子,其中fab重链和fab轻链的可变结构域或恒定结构域被交换(即彼此替换),即,交叉fab分子包含由轻链可变结构域vl和重链恒定结构域1ch1组成的肽链(vl-ch1,在n末端至c末端方向上),以及由重链可变结构域vh和轻链恒定结构域cl组成的肽链(vh-cl,在n末端至c末端方向上)。为清楚起见,在fab轻链和fab重链的可变结构域被交换的交叉fab分子中,包含重链恒定结构域1ch1的肽链在本文中称为(交叉)fab分子的“重链”。相反地,在fab轻链和fab重链的恒定结构域被交换的交叉fab分子中,包含重链可变结构域vh的肽链在本文中称为(交叉)fab分子的“重链”。
84、与此相反,“常规”fab分子是指其天然形式(即包含由重链可变结构域和恒定结构域组成的重链(vh-ch1,在n末端至c末端方向中)和由轻链可变结构域和恒定结构域组成的轻链(vl-cl,在n末端至c末端方向中))的fab分子。
85、术语“免疫球蛋白分子(immunoglobulin molecule)”是指具有天然生成的抗体的结构的蛋白质。例如,igg类的免疫球蛋白为约150,000道耳顿、由两条轻链和两条重链经二硫键键合所组成的异四聚体糖蛋白。从n末端至c末端,每条重链具有可变结构域(vh),也称为可变重链结构域或重链可变区,其后是三个恒定结构域(ch1、ch2和ch3),也称为重链恒定区。类似地,从n末端至c末端,每条轻链具有可变结构域(vl),也称为轻链可变结构域或轻链可变区,接着为轻链恒定(cl)结构域,也称为轻链恒定区。免疫球蛋白的重链可被归类为五种类型中的一种,称为α(iga)、δ(igd)、ε(ige)、γ(igg)或μ(igm),其中一些可进一步分为亚型,例如γ1(igg1)、γ2(igg2)、γ3(igg3)、γ4(igg4)、α1(iga1)和α2(iga2)。基于其恒定结构域的氨基酸序列,免疫球蛋白的轻链可被归类为两种类型中的一种,称为卡帕(kappa,κ)和兰姆达(lambda,λ)。免疫球蛋白基本上由经由免疫球蛋白铰链区连接的两个fab分子和一个fc结构域组成。
86、本文中的术语“fc结构域”或“fc区”,用于定义包含至少一部分恒定区的免疫球蛋白重链的c末端区。该术语包括天然序列fc区域和变体fc区域。尽管igg重链的fc区的边界可能略有变化,但通常将人igg重链的fc区定义为从cys226或pro230延伸至该重链的羧基末端。但是,由宿主细胞产生的抗体可能经历重链c末端的一种或多种,特别是一种或两种氨基酸的翻译后切割。因此,由宿主细胞通过表达编码全长重链的特定核酸分子而产生的抗体可包括全长重链,或者可包括全长重链的切割变体。可能是这种情况,其中重链的最后两个c末端氨基酸为甘氨酸(g446)和赖氨酸(k447,根据kabat eu索引编号)。因此,可以存在或可以不存在fc区域的c末端赖氨酸(lys447)或c末端甘氨酸(gly446)和赖氨酸(k447)。除非本文另有说明,否则fc区或恒定区中氨基酸残基的编号根据eu编号系统(也称为eu指数)进行,如kabat等人所述(sequences of proteins of immunological interest,第5版public health service,national institutes of health,bethesda,md,1991)(另见上文)。如本文中所使用的fc结构域的“亚基”,是指形成二聚体fc结构域的两个多肽之一,即包含能够稳定自缔合的免疫球蛋白重链的c末端恒定区的多肽。例如,igg fc结构域的亚基包含igg ch2和igg ch3恒定结构域。
87、“促进fc结构域的第一亚基和第二亚基的缔合的修饰”是对肽骨架的操纵或对fc结构域亚基的翻译后修饰,该操纵或翻译后修饰减少或阻止包含fc结构域亚基的多肽与相同多肽的缔合形成同型二聚体。本文所用的促进缔合的修饰,特别包括对期望缔合的两个fc结构域亚基(即fc结构域的第一亚基和第二亚基)中的每一个所进行的单独修饰,其中,该修饰彼此互补,以便促进两个fc结构域亚基的缔合。例如,促进缔合的修饰可改变一个或两个fc结构域亚基的结构或电荷,以分别使其在空间或静电上有利。因此,(异)二聚化发生在包含第一fc结构域亚基的多肽与包含第二fc结构域亚基的多肽之间,其就进一步融合到每个亚基(例如,抗原结合部分)的组分而言可能有所不同。在一些方面,促进缔合的修饰包含fc结构域中的氨基酸突变,特别是氨基酸取代。在特定方面,促进缔合的修饰包含fc结构域的两个亚基的每一个中的单独的氨基酸突变,特别是氨基酸取代。
88、术语“效应子功能”,是指归因于抗体的fc区的那些生物活性,其随抗体同种型而变化。抗体效应子功能的实例包括:c1q结合和补体依赖性细胞毒性(cdc)、fc受体结合、抗体依赖型细胞介导的细胞毒性(adcc)、抗体依赖性细胞吞噬作用(adcp)、细胞因子分泌、抗原呈现细胞摄取的免疫复合物介导抗原、细胞表面受体(例如,b细胞受体)降调和b细胞活化。
89、相对于参考多肽序列所述的“百分比(%)氨基酸序列同一性”,是指候选序列中氨基酸残基与参考多肽序列中的氨基酸残基相同的百分比,在比对序列并引入差异后(如有必要),可实现最大的序列同一性百分比,并且不考虑将任何保守取代作为序列同一性的一部分。为确定氨基酸序列同一性百分比的目的而进行的比对可通过本领域中技术范围内的各种方式实现,例如,使用公开可用的计算机软件诸如blast、blast-2、clustal w、megalign(dnastar)软件或fasta程序包实现。本领域的技术人员可确定用于比对序列的合适参数,包括在所比较的序列全长上实现最大比对所需的任何算法。但是,出于本文的目的,使用fasta包36.3.8c版或更高版本的ggsearch程序和blosum50比较矩阵来生成%氨基酸序列同一性值。fasta程序包由以下作者开发:w.r.pearson和d.j.lipman(1988)(“improved tools for biological sequence analysis”,pnas 85:2444-2448);w.r.pearson(1996)(“effective protein sequence comparison”meth.enzymol.266:227-258);以及pearson等人(1997)(genomics 46:24-36),并可从以下网址公开获得:http://fasta.bioch.virginia.edu/fasta_www2/fasta_down.shtml。可替代地,可使用通过http://fasta.bioch.virginia.edu/fasta_www2/index.cgi获得的公共服务器,使用ggsearch(global protein:protein)程序和默认选项(blosum50;open:-10;ext:-2;ktup=2)比较序列,以确保执行全局而不是局部比对。氨基酸同一性百分比在输出比对标题中给出。
90、“活化fc受体”为在抗体的fc结构域参与之后引起刺激受体携带细胞执行效应子功能的信号转导事件的fc受体。人活化fc受体包括fcγriiia(cd16a)、fcγri(cd64)、fcγriia(cd32)和fcαri(cd89)。
91、“减少结合”,例如减少结合fc受体,是指(例如)通过spr测得各自相互作用的亲和力降低。为清楚起见,该术语还包括将亲和力降低至零(或低于分析方法的检测极限),即相互作用完全消除。相反,“增加结合”是指各自相互作用的结合亲和性增加。
92、“融合”是指组分(例如fab分子和fc结构域亚基)经肽键直接或经由一或多个肽接头连接。
93、在特定方面,t细胞双特异性抗体结合cd3和靶细胞抗原。因此,在一些方面,t细胞双特异性抗体包含结合cd3的抗原结合部分和结合靶细胞抗原的抗原结合部分。
94、在一些方面,第一抗原结合部分和/或第二抗原结合部分为fab分子。在一些方面,第一抗原结合部分是交叉fab分子,其中fab轻链和fab重链的可变区或恒定区被交换。在这些方面,第二抗原结合部分优选是常规fab分子。
95、在一些方面,其中t细胞双特异性抗体的第一抗原结合部分和第二抗原结合部分两者均为fab分子,并且在抗原结合部分的一(特别是第一抗原结合部分)中,fab轻链和fab重链的可变结构域vl和vh彼此取代,
96、i)在第一抗原结合部分的恒定结构域cl中,124位的氨基酸被带正电荷的氨基酸(根据kabat编号)取代,并且其中,在第一抗原结合部分的恒定结构域ch1中,147位的氨基酸或213位的氨基酸被带负电荷的氨基酸(根据kabat eu索引编号)取代;或
97、ii)在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被带正电荷的氨基酸(根据kabat编号)取代,并且其中,在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸或213位的氨基酸被带负电荷的氨基酸(根据kabat eu索引编号)取代。
98、t细胞双特异性抗体不包含i)和ii)两者所提及的修饰。具有vh/vl交换的抗原结合部分的恒定结构域cl和ch1未彼此取代(即保持未交换状态)。
99、在更具体的方面,
100、i)在第一抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)独立取代,并且在第一抗原结合部分的恒定结构域ch1中,147位的氨基酸或213位的氨基酸被谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)独立取代;或
101、ii)在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)独立取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸或213位的氨基酸被谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)独立取代。
102、在一些方面,在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)独立取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸或213位的氨基酸被谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)独立取代。
103、在另外的方面,在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)独立取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸被谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)独立取代。
104、在优选的方面,在第二抗原结合部分的恒定结构域cl中,124位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,且123位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代,并且213位的氨基酸独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代。
105、在一些方面,在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)(根据kabat编号)取代,并且123位的氨基酸被赖氨酸(k)(根据kabat编号)取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸被谷氨酸(e)(根据kabat eu索引编号)取代,并且213位的氨基酸被谷氨酸(e)(根据kabat eu索引编号)取代。
106、在一些方面,在第二抗原结合部分的恒定结构域cl中,124位的氨基酸被赖氨酸(k)(根据kabat编号)取代,并且123位的氨基酸被精氨酸(r)(根据kabat编号)取代,并且在第二抗原结合部分的恒定结构域ch1中,147位的氨基酸被谷氨酸(e)(根据kabat eu索引编号)取代,并且213位的氨基酸被谷氨酸(e)(根据kabat eu索引编号)取代。
107、在特定的方面,如果根据上述方面的氨基酸取代发生在第二抗原结合部分的恒定结构域cl和恒定结构域ch1中,则第二抗原结合部分的恒定结构域cl为κ同种型。
108、在一些方面,第一抗原结合部分与第二抗原结合部分彼此融合,任选地经由肽接头彼此融合。
109、在一些方面,第一抗原结合部分和第二抗原结合部分各自为fab分子,并且(i)第二抗原结合部分在fab重链的c末端与第一抗原结合部分的fab重链的n末端融合,或(ii)第一抗原结合部分在fab重链的c末端与第二抗原结合部分的fab重链的n末端融合。
110、在一些方面,t细胞双特异性抗体提供与cd3的单价结合。
111、在特定方面,t细胞双特异性抗体包含结合cd3的单个抗原结合部分和结合靶细胞抗原的两个抗原结合部分。因此,在一些方面,t细胞双特异性抗体包含结合靶抗原的第三抗原结合部分,特别是fab分子,更特别是常规fab分子。第三抗原结合部分可以单独或组合地并入本文描述的与第二抗原结合部分相关的所有特征(例如cdr序列、可变区序列和/或恒定区中的氨基酸取代)。在一些方面,第三抗原部分与第一抗原结合部分相同(例如也是常规fab分子并包含相同的氨基酸序列)。
112、在特定的方面,t细胞双特异性抗体另外包含fc结构域,该fc结构域由第一亚基和第二亚基构成。在一些方面,fc结构域为igg fc结构域。在特定的方面,fc结构域为igg1fc结构域。在其他方面,fc结构域为igg4fc结构域。在更具体的方面,fc结构域为igg4fc结构域,其包含在位置s228(根据kabat eu索引编号)的氨基酸取代,特别是氨基酸取代s228p。该氨基酸取代减少体内igg4抗体的fab臂交换(参见stubenrauch等人,drug metabolismand disposition 38,84-91(2010))。在进一步特定方面,fc结构域为人fc结构域。在特定优选的方面,fc结构域为人igg1fc结构域。人igg1fc区的一个示例性序列在seq id no:27中给出。
113、在一些方面,其中该第一抗原结合部分、该第二抗原结合部分和(在存在时的)第三抗原结合部分各自为fab分子,(a)该第二抗原结合部分在该fab重链的c末端与该第一抗原结合部分的该fab重链的n末端融合,并且该第一抗原结合部分在该fab重链的c末端与该fc结构域的该第一亚基的n末端融合,或是(ii)该第一抗原结合部分在该fab重链的c末端与该第二抗原结合部分的该fab重链的n末端融合,并且该第二抗原结合部分在该fab重链的c末端与该fc结构域的该第一亚基的n末端融合;并且(b)该第三抗原结合部分(在存在时的)在该fab重链的c末端与该fc结构域的该第二亚基的n末端融合。
114、在一些方面,t细胞双特异性抗体基本上由第一、第二和第三抗原结合部分(特别是fab分子)、由第一和第二亚基组成的fc结构域以及任选地一个或多个肽接头组成。
115、t细胞双特异性抗体的成分可直接彼此融合或优选地经由一个或多个合适的肽接头融合。在fab分子与fc结构域的亚基的n末端融合的情况下,其通常通过免疫球蛋白铰链区融合。
116、抗原结合部分可与fc结构域直接融合或彼此融合,或者通过胜肽接头与fc融合或彼此融合,该胜肽接头包含一个或多个氨基酸,通常约2-20个氨基酸。胜肽接头为本领域中所公知的并且如本文所述。合适的非免疫肽接头包括例如(g4s)n、(sg4)n、(g4s)n、g4(sg4)n或(g4s)ng5肽接头。“n”通常为1至10的整数,特别为2至4。在一些方面,该肽接头的长度为至少5个氨基酸;在一些方面,长度为5至100个氨基酸;在另外的方面,长度为10至50个氨基酸。在一些方面,该肽接头为(gxs)n或(gxs)ngm,其中g=甘氨酸,s=丝氨酸,并且(x=3,n=3、4、5或6,并且m=0、1、2或3)或(x=4,n=1、2、3、4或5,并且m=0、1、2、3、4或5);在一些方面,x=4并且n=2或3;在另外的方面,x=4并且n=2;在又另外的方面,x=4,n=1,并且m=5。在一些方面,该肽接头为(g4s)2。在其他方面,该肽接头为g4sg5。另外,连接子可包含免疫球蛋白铰链区(的一部分)。特别是,在其中fab分子与fc结构域亚基的n末端融合的情况下,可通过包含附加的肽接头或不含附加的肽接头的免疫球蛋白铰链区或其一部分融合。
117、在特定的方面,fc结构域包含促进fc结构域的第一亚基与第二亚基的缔合的修饰。人igg fc结构域的两个亚基之间最广泛的蛋白质-蛋白质相互作用位点在ch3结构域中。因此,在一些方面,该修饰在fc结构域的ch3结构域中进行。
118、在具体的方面,该促进fc结构域的第一亚基和第二亚基的缔合的修饰为所谓的“突出物入孔(knob-into-hole)”修饰,其包括在fc结构域的两个亚基中的一个的“突出物”修饰和fc结构域的两个亚基中的另一个的“孔”修饰。“突出物入孔”技术描述于例如:us 5,731,168;us 7,695,936;ridgway等人,prot eng 9,617-621(1996);以及carter,jimmunolmeth 248,7-15(2001)。通常,该方法包括在第一多肽的界面处引入一个突起(“突出物”),并且在第二多肽的界面中引入一个对应的空腔(“孔”),以使该突起可定位于空腔中,从而促进异源二聚体形成并阻碍同源二聚体形成。通过用较大侧链(例如酪氨酸或色氨酸)替换第一多肽界面上的较小的氨基酸侧链来构建突起。通过将较大氨基酸侧链替换为较小的氨基酸侧链(例如丙氨酸或苏氨酸),在第二多肽的界面中形成与突起具有相同或相近大小的互补空腔。
119、因此,在一些方面,该fc结构域的该第一亚基的该ch3结构域中的氨基酸残基被具有较大侧链体积的氨基酸残基取代,从而在该第一亚基的该ch3结构域内产生突起,该突起为可位在该第二亚基的ch3结构域内的空腔中,并且该fc结构域的该第二亚基的该ch3结构域中的氨基酸残基被具有较小侧链体积的氨基酸残基取代,从而在该第二亚基的该ch3结构域内产生空腔,该第一亚基的该ch3结构域内的该突起为可位在该空腔内。优选地,该具有较大侧链体积的氨基酸残基选自由以下项所组成的组:精氨酸(r)、苯丙氨酸(f)、酪氨酸(y)和色氨酸(w)。优选地,该具有较小侧链体积的氨基酸残基选自由以下项所组成的组:丙氨酸(a)、丝氨酸(s)、苏氨酸(t)和缬氨酸(v)。可通过改变编码多肽的核酸(例如通过针对特定位点的突变或通过胜肽合成)来制备突起和空腔。
120、在具体的这些方面,在fc结构域的第一亚基中,在366位的苏氨酸残基被色氨酸残基(t366w)取代,并且在该fc结构域的第二亚基中,在407位的酪氨酸残基被缬氨酸残基(y407v)取代,并且任选地,在366位的苏氨酸残基被丝氨酸残基(t366s)取代,并且在368位的亮氨酸残基被丙氨酸残基(l368a)取代(根据kabat eu索引编号)。在另外的方面,在fc结构域的第一亚基中,354位的丝氨酸残基又被半胱氨酸残基替换(s354c)或356位的谷氨酸残基被半胱氨酸残基替换(e356c)(特别是354位的丝氨酸残基被半胱氨酸残基替换),并且在fc结构域的第二亚基中,349位的酪氨酸残基又被半胱氨酸残基替换(y349c)(根据kabateu索引编号)。在优选的方面,fc结构域的第一亚基包含氨基酸取代s354c和t366w,并且fc结构域的第二亚基包含氨基酸取代y349c、t366s、l368a和y407v(根据kabat eu索引编号)。
121、在一些方面,fc结构域包含降低与fc受体的结合和/或效应子功能的一种或多种氨基酸取代。
122、在特定的方面,fc受体为fcγ受体。在一些方面中,fc受体为人fc受体。在一些方面中,fc受体为活化fc受体。在具体的方面,fc受体为活化人fcγ受体,更具体地人fcγriiia、fcγri或fcγriia,最具体地人fcγriiia。在一些方面,效应子功能是选自补体依赖性细胞毒性(cdc)、抗体依赖性细胞介导的细胞毒性(adcc)、抗体依赖性细胞吞噬作用(adcp)和细胞因子分泌的组中的一种或多种。在特定的方面,效应子功能为adcc。
123、通常,在fc结构域的两个亚基中的每个中都存在相同的一个或多个氨基酸取代。在一些方面,一个或多个氨基酸取代降低了fc结构域与fc受体的结合亲和力。在一些方面,一个或多个氨基酸取代将fc结构域与fc受体的结合亲和力降低至少2倍、至少5倍或至少10倍。
124、在一些方面,fc结构域包含在选自e233、l234、l235、n297、p331和p329(根据kabateu索引编号)的组的位置处的氨基酸取代。在更具体的方面,fc结构域包含在选自l234、l235和p329(根据kabat eu索引编号)的组的位置处的氨基酸取代。在一些方面中,fc结构域包含l234a和l235a(根据kabat eu索引编号)的氨基酸取代。在一些此类方面,fc结构域为igg1fc结构域,特别是人igg1fc结构域。在一些方面,fc结构域包含在位置p329的氨基酸取代。在更具体的方面,氨基酸取代为p329a或p329g,特别是p329g(根据kabat eu索引编号)。在一些方面,fc结构域包含在位置p329的氨基酸取代,以及在选自e233、l234、l235、n297和p331(根据kabat eu索引编号)的位置的另一个氨基酸取代。在更具体的方面,另一个氨基酸取代为e233p、l234a、l235a、l235e、n297a、n297d或p331s。在特定方面,fc结构域包含在位置p329、l234和l235(根据kabat eu索引编号)的氨基酸取代。在更特定的方面,fc结构域包含氨基酸突变l234a、l235a和p329g(“p329g lala”、“pglala”或“lalapg”)。具体地,在优选方面中,fc结构域的每个亚基包含氨基酸取代l234a、l235a和p329g(根据kabateu索引编号),即在fc结构域的第一亚基和第二亚基中的每个中,234位的亮氨酸残基被丙氨酸残基替换(l234a),235位的亮氨酸残基被丙氨酸残基替换(l235a),并且329位的脯氨酸残基被甘氨酸残基替换(p329g)(根据kabat eu索引编号)。在一些此类方面,fc结构域为igg1fc结构域,特别是人igg1fc结构域。
125、在一些方面,t细胞双特异性抗体的靶细胞抗原是癌胚抗原(cea)。
126、除非另有说明,否则“癌胚抗原”或“cea”(也称为癌胚抗原相关细胞粘附分子5(ceacam5)),是指源自任何脊椎动物的任何天然cea,该脊椎动物包括哺乳动物,诸如灵长类动物(例如人)、非人灵长类动物(例如食蟹猴)和啮齿动物(例如小鼠和大鼠)。该术语涵盖“全长”、未处理的cea以及在细胞处理中得到的任何形式的cea。该术语亦涵盖天然生成的cea变体,例如,剪接变体或等位基因变体。在一些方面,cea为人cea。人cea的氨基酸序列显示于uniprot(www.uniprot.org)登录号p06731或ncbi(www.ncbi.nlm.nih.gov/)refseqnp_004354.2。在一些方面,cea是细胞膜结合的cea。在一些方面,cea是在细胞表面表达的cea,例如癌细胞。
127、结合cea的用于本发明的有用的t细胞双特异性抗体描述于例如pct公开号wo2014/131712(通过引用整体并入本文)中。
128、在一些方面,t细胞双特异性抗体包含结合cd3的第一抗原结合部分和结合cea的第二抗原结合部分。
129、在一些方面,第一抗原结合部分包含:含有seq id no:28的重链cdr(hcdr)1、seqid no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区。
130、在一些方面,第二抗原结合部分包含:含有seq id no:36的重链cdr(hcdr)1、seqid no:37的hcdr2和seq id no:38的hcdr3的重链可变区;以及含有seq id no:39的轻链cdr(lcdr)1、seq id no:40的lcdr2和seq id no:41的lcdr3的轻链可变区。
131、在一些方面,cea cd3双特异性抗体包含
132、(i)第一抗原结合部分,该第一抗原结合部分结合至cd3并且包含:含有seq idno:28的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区;以及
133、(ii)第二抗原结合部分,该第二抗原结合部分结合至cea,并且包含:含有seq idno:36的重链cdr(hcdr)1、seq id no:37的hcdr2和seq id no:38的hcdr3的重链可变区;以及含有seq id no:39的轻链cdr(lcdr)1、seq id no:40的lcdr2和seq id no:41的lcdr3的轻链可变区。
134、在一些方面,第一抗原结合部分包含:重链可变区序列,其与seq id no:34的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:34的重链可变区序列和seq id no:35的轻链可变区序列。
135、在一些方面,第二抗原结合部分包含:重链可变区序列,其与seq id no:42的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:43的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分包含seq id no:42的重链可变区序列和seq id no:43的轻链可变区序列。
136、在一些方面,t细胞双特异性抗体包含结合cea和/或由第一和第二亚基组成的fc结构域的第三抗原结合部分,如本文所述。
137、在优选的方面,t细胞双特异性抗体包含
138、(i)结合至cd3的第一抗原结合部分,其包含:含有seq id no:28的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区,其中第一抗原结合部分是交叉fab分子,其中fab轻链与fab重链的可变区或恒定区,特别是恒定区是经交换的;
139、(ii)结合至cea的第二抗原结合部分和第三抗原结合部分,其包含:含有seq idno:36的重链cdr(hcdr)1、seq id no:37的hcdr2和seq id no:38的hcdr3的重链可变区;以及含有seq id no:39的轻链cdr(lcdr)1、seq id no:40的lcdr2和seq id no:41的lcdr3的轻链可变区,其中第二抗原结合部分和第三抗原结合部分各为fab分子,特别是常规fab分子;
140、(iii)由第一亚基和第二亚基所构成的fc结构域,
141、其中该第二抗原结合部分在该fab重链的c末端融合至该第一抗原结合部分的该fab重链的n末端,并且该第一抗原结合部分在该fab重链的c末端融合至该fc结构域的该第一亚基的n末端,并且其中该第三抗原结合部分在该fab重链的c末端融合至该fc结构域的该第二亚基的n末端。
142、在一些方面,t细胞双特异性抗体(结合cea和cd3)的第一抗原结合部分包含:重链可变区序列,其与seq id no:34的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:34的重链可变区序列和seq id no:35的轻链可变区序列。
143、在一些方面,t细胞双特异性抗体(结合cea和cd3)的第二抗原结合部分和(在存在时的)第三抗原结合部分包含:重链可变区序列,其与seq id no:42的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:43的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分和(在存在时的)第三抗原结合部分包含seq id no:42的重链可变区和seq id no:43的轻链可变区。
144、根据上述方面的fc结构域可以单独或组合地并入上文关于fc结构域描述的所有特征。
145、在一些方面,t细胞双特异性抗体(结合cea和cd3)的fc结构域包含促进fc结构域的第一和第二亚基缔合的修饰,和/或fc结构域包含减少与fc受体和/或效应子功能结合的一个或多个氨基酸取代。
146、在一些方面,抗原结合部分和fc区通过肽接头彼此融合,特别是通过seq id no:45和seq id no:47中的肽接头。
147、在一些方面,t细胞双特异性抗体(结合cea和cd3)包含:含有与seq id no:44的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq idno:45的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:46的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;以及含有与seq id no:47的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽。在一些方面,t细胞双特异性抗体(结合cea和cd3)包含:含有seq idno:44的序列的多肽(特别是两种多肽);含有seq id no:45的序列的多肽;含有seq id no:46的序列的多肽;以及含有seq id no:47的序列的多肽。
148、在优选的方面,t细胞双特异性抗体是cibisatamab(who药物信息(药物的国际非专利名称),推荐的inn:list 80,2018,vol.32,no.3,p.438)。
149、在一些方面,t细胞双特异性抗体的靶细胞抗原是hla-2/wt1。
150、除非另有说明,否则“wt1”,也称为“wilms肿瘤1”或“wilms肿瘤蛋白”是指来自任何脊椎动物来源的任何天然wt1,该脊椎动物来源包括哺乳动物,诸如灵长类动物(例如人)、非人灵长类动物(例如食蟹猴)和啮齿动物(例如小鼠和大鼠)。该术语涵盖“全长”、未处理的wt1以及在细胞处理中得到的任何形式的wt1。该术语还涵盖天然生成的wt1变体,例如,剪接变体或等位基因变体。在一些方面,wt1是人wt1,特别是是seq id no:21的蛋白质。人wt1描述于uniprot(www.uniprot.org)登录号p19544(输入版本215)中,并且人wt1的氨基酸序列也示于seq id no:21中。
151、“vld”、“vld肽”或“wt1vld”是指具有氨基酸序列vldfappga(seq id no:22;seq idno:21的wt1蛋白质的37-45位)的wt1衍生肽。
152、“rmf”、“rmf肽”或“wt1rmf”意指具有氨基酸序列rmfrnapyl(seq id no:23;seq idno:21的wt1蛋白质的126-134位)的wt1衍生肽。
153、“hla-a2”、“hla-a*02”、“hla-a02”或“hla-a*2”(可互换使用)是指hla-a血清型组中的人白细胞抗原血清型。hla-a2蛋白质(由相应的hla基因编码)构成相应的i类mhc(主要组织相容性复合物)蛋白质的α链,其进一步包含β2微球蛋白亚基。特异性hla-a2蛋白质是hla-a201(也称为hla-a0201、hla-a02.01或hla-a*02:01)。在特定方面,本文所述的hla-a2蛋白质是hla-a201。人hla-a2的例示性序列于seq id no:24中给出。
154、“hla-a2/wt1”是指hla-a2分子与wt1衍生肽(在本文中也称为“wt1肽”),具体地rmf或vld肽(分别为“hla-a2/wt1rmf”和“hla-a2/wt1vld”)的复合物。本发明中使用的双特异性抗体可以与hla-a2/wt1rmf或hla-a2/wt1vld复合物特异性结合。
155、用于本发明的与hla-a2/wt1结合的有用的t细胞双特异性抗体被描述于例如pct公开号wo 2019/122052(通过引用整体并入本文)中。
156、在一些方面,t细胞双特异性抗体包含结合cd3的第一抗原结合部分,和结合hla-a2/wt1,特别是hla-a2/wt1rmf的第二抗原结合部分。
157、在一些方面,第一抗原结合部分包含:含有seq id no:1的重链cdr(hcdr)1、seqid no:2的hcdr2和seq id no:3的hcdr3的重链可变区;以及含有seq id no:4的轻链cdr(lcdr)1、seq id no:5的lcdr2和seq id no:6的lcdr3的轻链可变区。
158、在一些方面,第二抗原结合部分包含:含有seq id no:9的重链cdr(hcdr)1、seqid no:10的hcdr2和seq id no:11的hcdr3的重链可变区;以及含有seq id no:12的轻链cdr(lcdr)1、seq id no:13的lcdr2和seq id no:14的lcdr3的轻链可变区。
159、在一些方面,t细胞双特异性抗体包含
160、(i)第一抗原结合部分,该第一抗原结合部分结合至cd3并且包含:含有seq idno:1的重链cdr(hcdr)1、seq id no:2的hcdr2和seq id no:3的hcdr3的重链可变区;以及含有seq id no:4的轻链cdr(lcdr)1、seq id no:5的lcdr2和seq id no:6的lcdr3的轻链可变区;以及
161、(ii)第二抗原结合部分,该第二抗原结合部分结合至hla-a2/wt1并且包含:含有seq id no:9的重链cdr(hcdr)1、seq id no:10的hcdr2和seq id no:11的hcdr3的重链可变区;以及含有seq id no:12的轻链cdr(lcdr)1、seq id no:13的lcdr2和seq id no:14的lcdr3的轻链可变区。
162、在一些方面,第一抗原结合部分包含:重链可变区序列,其与seq id no:7的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:8的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:7的重链可变区序列和seq id no:8的轻链可变区序列。
163、在一些方面,第二抗原结合部分包含:重链可变区序列,其与seq id no:15的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:16的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分包含seq id no:15的重链可变区序列和seq id no:16的轻链可变区序列。
164、在一些方面,t细胞双特异性抗体包含结合hla-a2/wt1和/或由第一和第二亚基组成的fc结构域的第三抗原结合部分,如本文所述。
165、在优选的方面,t细胞双特异性抗体包含
166、(i)结合至cd3的第一抗原结合部分,其包含:含有seq id no:1的重链cdr(hcdr)1、seq id no:2的hcdr2和seq id no:3的hcdr3的重链可变区;以及含有seq id no:4的轻链cdr(lcdr)1、seq id no:5的lcdr2和seq id no:6的lcdr3的轻链可变区,其中第一抗原结合部分是交叉fab分子,其中fab轻链与fab重链的可变区或恒定区,特别地可变区是经交换的;
167、(ii)结合至hla-a2/wt1的第二抗原结合部分和第三抗原结合部分,其包含:含有seq id no:9的重链cdr(hcdr)1、seq id no:10的hcdr2和seq id no:11的hcdr3的重链可变区;以及含有seq id no:12的轻链cdr(lcdr)1、seq id no:13的lcdr2和seq id no:14的lcdr3的轻链可变区,其中该第二抗原结合部分和该第三抗原结合部分各为fab分子,特别是为常规fab分子;
168、(iii)由第一亚基和第二亚基所构成的fc结构域,
169、其中该第二抗原结合部分在该fab重链的c末端融合至该第一抗原结合部分的该fab重链的n末端,并且该第一抗原结合部分在该fab重链的c末端融合至该fc结构域的该第一亚基的n末端,并且其中该第三抗原结合部分在该fab重链的c末端融合至该fc结构域的该第二亚基的n末端。
170、在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)的第一抗原结合部分是交叉fab分子,其中该fab轻链和该fab重链的这些可变区是经交换的,并且其中该t细胞双特异性抗体的该第二抗原结合部分和(在存在时的)第三抗原结合部分是常规fab分子,其中在该恒定结构域cl中,124位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且123位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且在该恒定结构域ch1中,147位的氨基酸是独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代,并且213位的氨基酸独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代。
171、特别是,在上述方面,在(ii)下的第二fab分子和第三fab分子的恒定结构域cl中,124位的氨基酸可被赖氨酸(k)取代(根据kabat编号),并且123位的氨基酸可被赖氨酸(k)或精氨酸(r)(特别是被精氨酸(r))取代(根据kabat编号),并且在(ii)下的第二fab分子和第三fab分子的恒定结构域ch1中,147位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号),并且213位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号)。
172、在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)的第一抗原结合部分包含:重链可变区序列,其与seq id no:7的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:8的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:7的重链可变区序列和seq id no:8的轻链可变区序列。
173、在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)的第二抗原结合部分和(在存在时的)第三抗原结合部分包含:重链可变区序列,其与seq id no:15的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:16的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分和(在存在时的)第三抗原结合部分包含seq id no:15的重链可变区和seq id no:16的轻链可变区。
174、根据上述方面的fc结构域可以单独或组合地并入上文关于fc结构域描述的所有特征。
175、在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)的fc结构域包含促进fc结构域的第一和第二亚基缔合的修饰,和/或fc结构域包含减少与fc受体和/或效应子功能结合的一个或多个氨基酸取代。
176、在一些方面,抗原结合部分和fc区通过肽接头彼此融合,特别是通过seq id no:18和seq id no:20中的肽接头。
177、在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)包含:含有与seq idno:17的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:18的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:19的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;以及含有与seq id no:20的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽。在一些方面,t细胞双特异性抗体(结合hla-a2/wt1和cd3)包含:含有seq id no:17的序列的多肽(特别是两种多肽);含有seq id no:18的序列的多肽;含有seq id no:19的序列的多肽;以及含有seq id no:20的序列的多肽。
178、在一些方面,t细胞双特异性抗体的靶细胞抗原是cd20。
179、除非另有说明,否则“cd20”,也称为“b淋巴细胞抗原b1”是指来自任何脊椎动物来源的任何天然cd20,该脊椎动物来源包括哺乳动物,诸如灵长类动物(例如人)、非人灵长类动物(例如食蟹猴)和啮齿动物(例如小鼠和大鼠)。该术语涵盖“全长”、未处理的cd20以及在细胞处理中得到的任何形式的cd20。该术语还涵盖天然生成的cd20变体,例如,剪接变体或等位基因变体。在一些方面,cd20为人cd20。人cd20描述于uniprot(www.uniprot.org)登录号p11836(输入版本200)中,并且人cd20的氨基酸序列也示于seq id no:60中。
180、用于本发明与cd20结合的有用的t细胞双特异性抗体被描述于例如pct公开号wo2016/020309(通过引用整体并入本文)中。
181、在一些方面,t细胞双特异性抗体包含结合cd3的第一抗原结合部分和结合cd20的第二抗原结合部分。
182、在一些方面,第一抗原结合部分包含:含有seq id no:28的重链cdr(hcdr)1、seqid no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区。
183、在一些方面,第二抗原结合部分包含:含有seq id no:48的重链cdr(hcdr)1、seqid no:49的hcdr2和seq id no:50的hcdr3的重链可变区;以及含有seq id no:51的轻链cdr(lcdr)1、seq id no:52的lcdr2和seq id no:53的lcdr3的轻链可变区。
184、在一些方面,t细胞双特异性抗体包含
185、(i)第一抗原结合部分,该第一抗原结合部分结合至cd3并且包含:含有seq idno:28的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区;以及
186、(ii)第二抗原结合部分,该第二抗原结合部分结合至cd20并且包含:含有seq idno:48的重链cdr(hcdr)1、seq id no:49的hcdr2和seq id no:50的hcdr3的重链可变区;以及含有seq id no:51的轻链cdr(lcdr)1、seq id no:52的lcdr2和seq id no:53的lcdr3的轻链可变区。
187、在一些方面,第一抗原结合部分包含:重链可变区序列,其与seq id no:34的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:34的重链可变区序列和seq id no:35的轻链可变区序列。
188、在一些方面,第二抗原结合部分包含:重链可变区序列,其与seq id no:54的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:55的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分包含seq id no:54的重链可变区序列和seq id no:55的轻链可变区序列。
189、在一些方面,t细胞双特异性抗体包含结合cd20和/或由第一和第二亚基组成的fc结构域的第三抗原结合部分,如本文所述。
190、在优选的方面,t细胞双特异性抗体包含
191、(i)结合至cd3的第一抗原结合部分,其包含:含有seq id no:28的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:30的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区,其中第一抗原结合部分是交叉fab分子,其中fab轻链与fab重链的可变区或恒定区,特别地可变区是经交换的;
192、(ii)结合至cd20的第二抗原结合部分和第三抗原结合部分,其包含:含有seq idno:48的重链cdr(hcdr)1、seq id no:49的hcdr2和seq id no:50的hcdr3的重链可变区;以及含有seq id no:51的轻链cdr(lcdr)1、seq id no:52的lcdr2和seq id no:53的lcdr3的轻链可变区;其中该第二抗原结合部分和该第三抗原结合部分各为fab分子,特别是常规fab分子;
193、(iii)由第一亚基和第二亚基所构成的fc结构域,
194、其中该第二抗原结合部分在该fab重链的c末端融合至该第一抗原结合部分的该fab重链的n末端,并且该第一抗原结合部分在该fab重链的c末端融合至该fc结构域的该第一亚基的n末端,并且其中该第三抗原结合部分在该fab重链的c末端融合至该fc结构域的该第二亚基的n末端。
195、在一些方面,t细胞双特异性抗体(结合cd20和cd3)的第一抗原结合部分是交叉fab分子,其中该fab轻链和该fab重链的这些可变区是经交换的,并且其中该t细胞双特异性抗体的该第二抗原结合部分和(在存在时的)第三抗原结合部分是常规fab分子,其中在该恒定结构域cl中,124位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且123位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且在该恒定结构域ch1中,147的氨基酸是独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代,并且213位的氨基酸独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代。
196、特别是,在上述方面,在(ii)下的第二fab分子和第三fab分子的恒定结构域cl中,124位的氨基酸可被赖氨酸(k)取代(根据kabat编号),并且123位的氨基酸可被赖氨酸(k)或精氨酸(r)(特别是被精氨酸(r))取代(根据kabat编号),并且在(ii)下的第二fab分子和第三fab分子的恒定结构域ch1中,147位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号),并且213位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号)。
197、在一些方面,t细胞双特异性抗体(结合cd20和cd3)的第一抗原结合部分包含:重链可变区序列,其与seq id no:34的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:34的重链可变区序列和seq id no:35的轻链可变区序列。
198、在一些方面,t细胞双特异性抗体(结合cd20和cd3)的第二抗原结合部分和(在存在时的)第三抗原结合部分包含:重链可变区序列,其与seq id no:54的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:55的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分和(在存在时的)第三抗原结合部分包含seq id no:54的重链可变区和seq id no:55的轻链可变区。
199、根据上述方面的fc结构域可以单独或组合地并入上文关于fc结构域描述的所有特征。
200、在一些方面,t细胞双特异性抗体(结合cd20和cd3)的fc结构域包含促进fc结构域的第一和第二亚基缔合的修饰,和/或fc结构域包含减少与fc受体和/或效应子功能结合的一个或多个氨基酸取代。
201、在一些方面,抗原结合部分和fc区通过肽接头彼此融合,特别是通过seq id no:57和seq id no:59中的肽接头。
202、在一些方面,t细胞双特异性抗体(结合cd20和cd3)包含:含有与seq id no:56的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq idno:57的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:58的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;以及含有与seq id no:59的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽。在一些方面,t细胞双特异性抗体(结合cd20和cd3)包含:含有seq idno:56的序列的多肽(特别是两种多肽);含有seq id no:57的序列的多肽;含有seq id no:58的序列的多肽;以及含有seq id no:59的序列的多肽。
203、在优选的方面,t细胞双特异性抗体是glofitamab(who药物信息(药物的国际非专利名称),推荐的inn:list 83,2020,vol.34,no.1,p.39)。
204、在一些方面,t细胞双特异性抗体的靶细胞抗原是cd19。
205、除非另有说明,否则术语“cd19”代表分化簇19(也称为b淋巴细胞抗原cd19或b淋巴细胞表面抗原b4),并且是指源自任何脊椎动物的任何天然cd19,该脊椎动物包括哺乳动物,诸如灵长类动物(例如人)、非人灵长类动物(例如食蟹猴)和啮齿动物(例如小鼠和大鼠)。该术语涵盖“全长”、未处理的cd19以及在细胞处理中得到的任何形式的cd19。该术语还涵盖天然生成的cd19变体,例如,剪接变体或等位基因变体。在一些方面,cd19为人cd19。另见人蛋白质uniprot(www.uniprot.org)登录号p15391(版本211),或ncbi(www.ncbi.nlm.nih.gov/)refseq np_001761.3。人cd19的例示性序列于seq id no:81中给出。
206、结合cd19的用于本发明的有用的t细胞双特异性抗体描述于例如ep申请号20181056.1和20180968.8(通过引用整体并入本文)中。
207、在一些方面,t细胞双特异性抗体包含结合cd3的第一抗原结合部分和结合cd19的第二抗原结合部分。
208、在一些方面,第一抗原结合部分包含:含有seq id no:61的重链cdr(hcdr)1、seqid no:29的hcdr2和seq id no:62的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区。
209、在其他方面,第一抗原结合部分包含:含有seq id no:64的重链cdr(hcdr)1、seqid no:29的hcdr2和seq id no:65的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区。
210、在一些方面,第二抗原结合部分包含:含有seq id no:67的重链cdr(hcdr)1、seqid no:68的hcdr2和seq id no:69的hcdr3的重链可变区;以及含有seq id no:70的轻链cdr(lcdr)1、seq id no:71的lcdr2和seq id no:72的lcdr3的轻链可变区。
211、在一些方面,t细胞双特异性抗体包含
212、(i)第一抗原结合部分,该第一抗原结合部分结合至cd3并且包含:含有seq idno:61的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:62的hcdr3的重链可变区,或含有seq id no:64的hcdr1、seq id no:29的hcdr2和seq id no:65的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区;以及
213、(ii)第二抗原结合部分,该第二抗原结合部分结合至cd19并且包含:含有seq idno:67的重链cdr(hcdr)1、seq id no:68的hcdr2和seq id no:69的hcdr3的重链可变区;以及含有seq id no:70的轻链cdr(lcdr)1、seq id no:71的lcdr2和seq id no:72的lcdr3的轻链可变区。
214、在一些方面,第一抗原结合部分包含:重链可变区序列,其与seq id no:63的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;或重链可变区序列,其与seq idno:66的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:63的重链可变区序列或seq id no:66的重链可变区序列和seq id no:35的轻链可变区序列。
215、在一些方面,第二抗原结合部分包含:重链可变区序列,其与seq id no:73的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq idno:74的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分包含seq id no:73的重链可变区序列和seq id no:74的轻链可变区序列。
216、在一些方面,t细胞双特异性抗体包含结合cd19和/或由第一和第二亚基组成的fc结构域的第三抗原结合部分,如本文所述。
217、在优选的方面,t细胞双特异性抗体包含
218、(i)结合至cd3的第一抗原结合部分,其包含:含有seq id no:61的重链cdr(hcdr)1、seq id no:29的hcdr2和seq id no:62的hcdr3的重链可变区,或含有seq id no:64的hcdr1、seq id no:29的hcdr2和seq id no:65的hcdr3的重链可变区;以及含有seq id no:31的轻链cdr(lcdr)1、seq id no:32的lcdr2和seq id no:33的lcdr3的轻链可变区,其中第一抗原结合部分是交叉fab分子,其中fab轻链和fab重链的可变区或恒定区,特别是可变区是经交换的;
219、(ii)结合至cd19的第二抗原结合部分和第三抗原结合部分,其包含:含有seq idno:67的重链cdr(hcdr)1、seq id no:68的hcdr2和seq id no:69的hcdr3的重链可变区;以及含有seq id no:70的轻链cdr(lcdr)1、seq id no:71的lcdr2和seq id no:72的lcdr3的轻链可变区;其中该第二抗原结合部分和该第三抗原结合部分各为fab分子,特别是常规fab分子;
220、(iii)由第一亚基和第二亚基所构成的fc结构域,
221、其中该第二抗原结合部分在该fab重链的c末端融合至该第一抗原结合部分的该fab重链的n末端,并且该第一抗原结合部分在该fab重链的c末端融合至该fc结构域的该第一亚基的n末端,并且其中该第三抗原结合部分在该fab重链的c末端融合至该fc结构域的该第二亚基的n末端。
222、在一些方面,t细胞双特异性抗体(结合cd19和cd3)的第一抗原结合部分是交叉fab分子,其中该fab轻链和该fab重链的这些可变区是经交换的,并且其中该t细胞双特异性抗体的该第二抗原结合部分和(在存在时的)第三抗原结合部分是常规fab分子,其中在该恒定结构域cl中,124位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且123位的氨基酸独立地经赖氨酸(k)、精氨酸(r)或组氨酸(h)(根据kabat编号)取代,并且在该恒定结构域ch1中,147的氨基酸是独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代,并且213位的氨基酸独立地经谷氨酸(e)或天冬氨酸(d)(根据kabat eu索引编号)取代。
223、特别是,在上述方面,在(ii)下的第二fab分子和第三fab分子的恒定结构域cl中,124位的氨基酸可被赖氨酸(k)取代(根据kabat编号),并且123位的氨基酸可被赖氨酸(k)或精氨酸(r)(特别是被精氨酸(r))取代(根据kabat编号),并且在(ii)下的第二fab分子和第三fab分子的恒定结构域ch1中,147位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号),并且213位的氨基酸可被谷氨酸(e)取代(根据kabat eu索引编号)。
224、在一些方面,t细胞双特异性抗体(结合cd19和cd3)的第一抗原结合部分包含:重链可变区序列,其与seq id no:63的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;或重链可变区序列,其与seq id no:66的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:35的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第一抗原结合部分包含seq id no:63的重链可变区序列或seq id no:66的重链可变区序列和seq id no:35的轻链可变区序列。
225、在一些方面,t细胞双特异性抗体(结合cd19和cd3)的第二抗原结合部分和(在存在时的)第三抗原结合部分包含:重链可变区序列,其与seq id no:73的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同;以及轻链可变区序列,其与seq id no:74的氨基酸序列至少约95%、96%、97%、98%、99%或100%相同。在一些方面,第二抗原结合部分和(在存在时的)第三抗原结合部分包含seq id no:73的重链可变区和seq id no:74的轻链可变区。
226、根据上述方面的fc结构域可以单独或组合地并入上文关于fc结构域描述的所有特征。
227、在一些方面,t细胞双特异性抗体(结合cd19和cd3)的fc结构域包含促进fc结构域的第一和第二亚基缔合的修饰,和/或fc结构域包含减少与fc受体和/或效应子功能结合的一个或多个氨基酸取代。
228、在一些方面,抗原结合部分和fc区通过肽接头彼此融合,特别是通过seq id no:75、seq id no:76和seq id no:77中的肽接头。
229、在一些方面,t细胞双特异性抗体(结合cd19和cd3)包含:含有与seq id no:78的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq idno:75的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:77的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;以及含有与seq id no:79的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽。在一些方面,t细胞双特异性抗体(结合cd19和cd3)包含:含有seq idno:78的序列的多肽(特别是两种多肽);含有seq id no:75的序列的多肽;含有seq id no:77的序列的多肽;以及含有seq id no:79的序列的多肽。
230、在其他方面,t细胞双特异性抗体(结合cd19和cd3)包含:含有与seq id no:78的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq idno:76的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;含有与seq id no:77的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽;以及含有与seq id no:80的序列至少80%、85%、90%、95%、96%、97%、98%或99%相同的序列的多肽。在一些方面,t细胞双特异性抗体(结合cd19和cd3)包含:含有seq idno:78的序列的多肽(特别是两种多肽);含有seq id no:76的序列的多肽;含有seq id no:77的序列的多肽;以及含有seq id no:80的序列的多肽。
231、在一些方面,所述疾病(待由t细胞双特异性抗体治疗)是癌症。
232、如本文所用,“治疗”(及其语法变体,诸如“治疗(treat)”或“治疗(treating)),是指试图改变待治疗个体的疾病自然进程的临床干预,并且可以是为了预防或在临床病理学的进程中进行。期望的治疗效果包括但不限于预防疾病的发生或复发、减轻症状、减轻疾病的任何直接或间接病理后果、预防转移、降低疾病进展的速度、改善或减轻疾病状态、缓解或改善预后。
233、术语“癌症”是指通常以不受调节的细胞增殖为特征的哺乳动物生理状况。癌症的实例包括但不限于癌、淋巴瘤、母细胞瘤、肉瘤和白血病。癌症的更多非限制性实例包括血液学癌症(诸如白血病)、膀胱癌、脑癌、头颈癌、胰腺癌、胆管癌、甲状腺癌、肺癌、乳腺癌、卵巢癌、子宫癌、宫颈癌、子宫内膜癌、食道癌、结肠癌、结肠直肠癌、直肠癌、胃癌、前列腺癌、皮肤癌、鳞状细胞癌、肉瘤、骨癌和肾癌。其他细胞增殖性疾患包括但不限于位在以下部位中的肿瘤:腹部、骨骼、乳房、消化系统、肝、胰腺、腹膜、内分泌腺(肾上腺、甲状旁腺、垂体、睾丸、卵巢、胸腺、甲状腺)、眼、头和颈、神经系统(中枢和外周)、淋巴系统、骨盆、皮肤、软组织、脾脏、胸部和泌尿生殖系统。还包括癌前病症或病变和癌症转移。
234、在一些方面,癌症是表达t细胞双特异性抗体的靶细胞抗原的癌症。
235、在一些方面,癌症是表达癌胚抗原(cea)的癌症(特别是在一些方面,其中t细胞双特异性抗体的靶细胞抗原是cea)。“cea阳性癌症”或“表达cea的癌症”是指特征在于癌细胞上cea表达或过表达的癌症。cea的表达可以通过例如免疫组织化学(ihc)或流式细胞术测定来确定。在一些方面,癌症表达cea。在一些方面,癌症在至少20%、优选至少50%或至少80%的肿瘤细胞中表达cea,如使用cea特异性抗体通过免疫组织化学(ihc)所确定。
236、在一些方面,癌症是结肠癌、肺癌、卵巢癌、胃癌、膀胱癌、胰腺癌、子宫内膜癌、乳腺癌、肾癌、食道癌、前列腺癌或本文所述的其他癌症。
237、在特定方面,癌症是选自由结肠直肠癌、肺癌、胰腺癌、乳腺癌和胃癌所组成的组的癌症。在优选的方面,癌症为结肠直肠癌(crc)。在一些方面,结肠直肠癌为转移性结肠直肠癌(mcrc)。在一些方面,结肠直肠癌是微卫星稳定(mss)的结肠直肠癌。在一些方面,结肠直肠癌是微卫星稳定的转移性结肠直肠癌(mss mcrc)。
238、在一些方面,癌症是表达wilms肿瘤蛋白(wt1)的癌症(特别是在一些方面,其中t细胞双特异性抗体的靶细胞抗原是hla-a2/wt1)。“wt1阳性癌症”或“表达wt1的癌症”是指特征在于癌细胞中wt1表达或过表达的癌症。wt1的表达可以通过例如定量实时pcr(测量wt1mrna水平)、流式细胞术、免疫组织化学(ihc)或蛋白印迹法来确定。在一些方面,癌症表达wt1。在一些方面,癌症在至少20%、优选至少50%或至少80%的肿瘤细胞中表达wt1,如使用wt1特异性抗体通过免疫组织化学(ihc)确定。
239、在一些方面,癌症为血液学癌症。血液学癌症的非限制性实例包括:白血病(例如急性淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、慢性淋巴细胞白血病(cll)、慢性骨髓性白血病(cml)、毛细胞白血病(hcl))、淋巴瘤(例如非霍奇金淋巴瘤(nhl)、霍奇金淋巴瘤)、骨髓瘤(例如多发性骨髓瘤(mm))、骨髓增生异常综合征(mds)和骨髓增生性疾病。
240、在某些方面,癌症选自由以下项所组成的组:血液学癌症(诸如白血病)、肾癌、膀胱癌、皮肤癌、肺癌、结肠直肠癌、乳腺癌、脑癌、头颈癌和前列腺癌。
241、在特定方面,癌症是血液学癌症,特别是是白血病,最特别是是急性淋巴细胞性白血病(all)或急性骨髓性白血病(aml)。在优选的方面,癌症是急性骨髓性白血病(aml)。在另外的特定方面,癌症是骨髓增生异常综合征(mds)。
242、在一些方面,癌症是表达cd20的癌症(特别是在一些方面,其中t细胞双特异性抗体的靶细胞抗原是cd20)。“cd20阳性癌症”或“表达cd20的癌症”是指特征在于癌细胞中cd20表达或过表达的癌症。cd20的表达可以通过例如定量实时pcr(测量cd20 mrna水平)、流式细胞术、免疫组织化学(ihc)或蛋白印迹法来确定。在一些方面,癌症表达cd20。在一些方面,癌症在至少20%、优选至少50%或至少80%的肿瘤细胞中表达cd20,如使用cd20特异性抗体通过免疫组织化学(ihc)确定。
243、在一些方面,癌症是b细胞癌,特别是cd20阳性b细胞癌。在一些方面,癌症选自由以下项所组成的组:非霍奇金淋巴瘤(nhl)、急性淋巴细胞性白血病(all)、慢性淋巴细胞白血病(cll)、弥漫性大b细胞淋巴瘤(dlbcl)、滤泡性淋巴瘤(fl)、套细胞淋巴瘤(mcl)、边缘区淋巴瘤(mzl)、多发性骨髓瘤(mm)或霍奇金淋巴瘤(hl)。在特定方面,癌症选自由以下项所组成的组:非霍奇金淋巴瘤(nhl)、急性淋巴细胞性白血病(all)、慢性淋巴细胞白血病(cll)、弥漫性大b细胞淋巴瘤(dlbcl)、滤泡性淋巴瘤(fl)、套细胞淋巴瘤(mcl)和边缘区淋巴瘤(mzl)。在更特定的方面,癌症是nhl,特别是复发性/难治性(r/r)nhl。在一些方面,癌症为dlbcl。在一些方面,癌症为fl。在一些方面,癌症为mcl。在一些方面,癌症为mzl。
244、在一些方面,癌症是表达cd19的癌症(特别是在一些方面,其中t细胞双特异性抗体的靶细胞抗原是cd19)。“cd19阳性癌症”或“表达cd19的癌症”是指特征在于癌细胞中cd19表达或过表达的癌症。cd19的表达可以通过例如定量实时pcr(测量cd19 mrna水平)、流式细胞术、免疫组织化学(ihc)或蛋白印迹法来确定。在一些方面,癌症表达cd19。在一些方面,癌症在至少20%、优选至少50%或至少80%的肿瘤细胞中表达cd19,如使用cd19特异性抗体通过免疫组织化学(ihc)确定。
245、在一些方面,癌症是b细胞癌,特别是cd19阳性b细胞癌。在一些方面,癌症是b细胞淋巴瘤或b细胞白血病。在一些方面,癌症为非霍奇金淋巴瘤(nhl)、急性淋巴细胞性白血病(all)或慢性淋巴细胞白血病(cll)。
246、在一些方面,癌症可由t细胞双特异性抗体治疗。在一些方面,t细胞双特异性抗体适用于治疗癌症。
247、在一些方面,癌症是实体瘤癌症。“实体瘤癌症”是指形成位于患者体内特定位置的离散肿瘤块(也包括肿瘤转移)的恶性肿瘤,诸如肉瘤或癌(与例如血癌诸如白血病相反,其通常不形成实体瘤)。实体瘤癌症的非限制性实例包括膀胱癌、脑癌、头颈癌、胰腺癌、肺癌、乳腺癌、卵巢癌、子宫癌、宫颈癌、子宫内膜癌、食道癌、结肠癌、结肠直肠癌、直肠癌、胃癌、前列腺癌、皮肤癌、鳞状细胞癌、骨癌、肝癌和肾癌。在本发明的背景下考虑的其他实体瘤癌症包括但不限于位在以下部位中的肿瘤:腹部、骨骼、乳房、消化系统、肝、胰腺、腹膜、内分泌腺(肾上腺、甲状旁腺、垂体、睾丸、卵巢、胸腺、甲状腺)、眼、头和颈、神经系统(中枢和外周)、淋巴系统、骨盆、皮肤、软组织、肌肉、脾脏、胸部和泌尿生殖系统。还包括癌前病症或病变和癌症转移。
248、在一些方面,其中t细胞双特异性抗体的靶细胞抗原是cd19,所述疾病(待由t细胞双特异性抗体治疗)是自身免疫性疾病。在具体的方面,自身免疫性疾病为狼疮,特别是系统性红斑狼疮(sle)或狼疮肾炎(ln)。
249、本文“个体”或“受试者”为哺乳动物。哺乳动物包括但不限于驯养的动物(例如牛、绵羊、猫、狗和马)、灵长类动物(例如人和非人类灵长类动物诸如猴)、兔以和啮齿类动物(例如小鼠和大鼠)。在某些方面,受试者或个体为人。在一些方面,个体患有疾病,特别是可由t细胞双特异性抗体治疗或待治疗的疾病。在一些方面,个体患有癌症,特别是可由t细胞双特异性抗体治疗或待治疗的癌症。特别地,本文中的个体是正在经历或已经经历癌症的一种或多种体征、症状或其他指标的有资格接受治疗的任何单一人类受试者。在一些方面,个体患有癌症或已被诊断患有癌症,特别是上文所述的任何癌症。在一些方面,个体患有局部晚期或转移性癌症或已被诊断患有局部晚期或转移性癌症。个体之前可能已经接受过t细胞双特异性抗体或另一种药物治疗,或者没有接受过这种治疗。在特定方面,患者之前没有接受过t细胞双特异性抗体治疗。在开始t细胞双特异性抗体疗法之前,患者可能已经接受过包含一种或多种药物而不是t细胞双特异性抗体的疗法的治疗。
250、在一些方面,个体的一种或多种细胞因子的血清水平升高。在一些方面,该升高的血清水平与向个体施用t细胞双特异性抗体有关。该升高的血清水平特别是与健康个体的血清水平和/或未施用t细胞双特异性抗体的个体(包括同一个体)中的血清水平相比(即在这种情况下血清水平与未施用t细胞双特异性抗体的血清水平相比升高)。在一些方面,该一种或多种细胞因子选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组。
251、根据本发明任一方面的细胞因子优选为促炎细胞因子,特别是选自由il-2、tnf-α、ifn-γ、il-6和il-1β所组成的组的一种或多种细胞因子。在一些方面,细胞因子为il-2。在一些方面,细胞因子为tnf-α。在一些方面,细胞因子为ifn-γ。在一些方面,细胞因子为il-6。在一些方面,细胞因子为il-1β。
252、优选地,根据本发明的任何方面的t细胞为细胞毒性t细胞。在一些方面,t细胞为cd4+或cd8+t细胞。在一些方面,t细胞为cd4+t细胞。
253、在一些方面,用t细胞双特异性抗体治疗或施用t细胞双特异性抗体可导致个体中的反应。在一些方面,反应可以是完全反应。在一些方面,反应可以是治疗停止后的持续反应。在一些方面,反应可以是治疗停止后持续的完全反应。在其他方面,反应可以是部分反应。在一些方面,反应可以是治疗停止后持续的部分反应。在一些方面,与单独使用t细胞双特异性抗体的治疗或施用t细胞双特异性抗体(即不使用tki)相比,使用t细胞双特异性抗体的治疗或施用t细胞双特异性抗体和tki可以改善反应。在一些方面,与单独用t细胞双特异性抗体(即,没有tki)治疗的相应患者群体相比,t细胞双特异性抗体和tki的治疗或施用可以增加患者群体中的反应率。
254、t细胞双特异性抗体可单独或连同其他药剂用于治疗。例如,t细胞双特异性抗体可以与至少一种附加治疗剂联合施用。在某些方面,附加治疗剂是抗癌剂,例如化疗剂、肿瘤细胞增殖抑制剂或肿瘤细胞凋亡活化剂。
255、氨基酸序列
256、
257、
258、
259、
260、
261、
262、
263、
264、
265、
266、
267、
- 还没有人留言评论。精彩留言会获得点赞!