新的二环化合物的制作方法
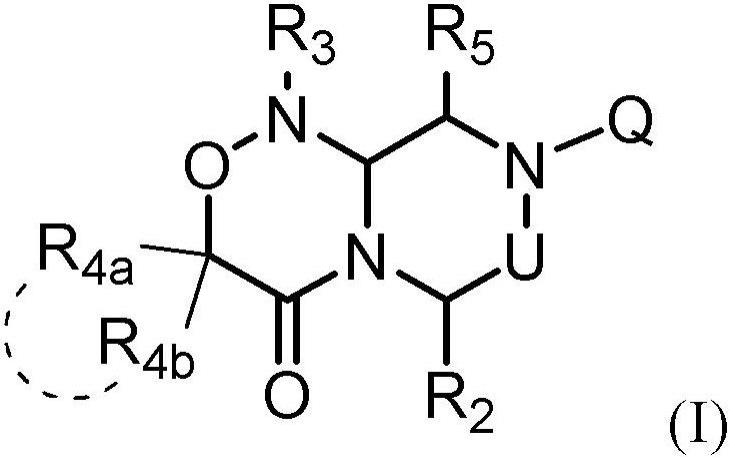
[]本发明涉及一种新的二环化合物。更具体地,本发明涉及一种新的具有notch抑制作用的二环化合物。
背景技术:
0、[背景技术]
1、notch信号传递是一种在哺乳动物的发育和组织稳态中起着不可或缺的作用的进化保守途径。notch受体和配体含有单次(single-pass)跨膜结构域,在细胞表面上表达,并且因此,notch信号传递在介导表达受体和配体的相邻细胞之间的通讯中尤为重要。在啮齿类动物和人类中发现了四种已知的notch受体,被称为notch 1至notch 4。notch受体是由最初作为单个多肽合成的细胞外和细胞内结构域组成的异源二聚体蛋白。受体-配体相互作用触发涉及γ-分泌酶活性的notch受体多肽的一系列蛋白水解性裂解。γ-分泌酶活性从质膜内侧裂解notch细胞内结构域,其转移至细胞核以形成转录因子复合物。notch细胞内结构域(nicd)是蛋白的活性形式。各种notch信号传递功能包括增殖、分化、细胞凋亡、血管生成、迁移和自我更新(非专利文献1-3)。
2、另外,nicd通过易位到细胞核并与rbp-j和maml(它们是dna结合蛋白)形成稳定的复合物来活化靶基因hes1和hes5的转录。
3、因此,可以抑制各种notch信号功能的化合物可以是对涉及该功能的各种疾病有用的药物。
4、[文献列表]
5、[非专利文献]
6、非专利文献1:bray,nature reviews molecular cell biology,7:678-689(2006)。
7、非专利文献2:fortini,developmental cell 16:633-647(2009)。
8、非专利文献3:ables,j.l.等人,neurosci.,12:269-283(2011)。
9、[发明概述]
10、[本发明要解决的问题]
11、本发明的目的是提供一种具有notch抑制作用的化合物和含有该化合物并对多种疾病有用的药物。
12、[解决问题的方式]
13、本发明的发明人在解决上述问题的尝试中已经进行了深入研究,并发现具有特定结构的化合物显示出优异的notch信号转导抑制作用(在下文中也被称作notch抑制剂),并完成了本发明。
14、即,本发明涉及以下内容。
15、[1]由下式(i)表示的化合物或其药学上可接受的盐:
16、
17、其中
18、q表示下式(i-1)至(i-2)中的任一个:
19、
20、*是与n(氮原子)的结合位点;
21、r1a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
22、r1b是氢、任选地被取代的烷基或-w11-w12-r13
23、其中
24、w11是-(co)-或-(so2)-,
25、w12是键、-o-或-n(r14)-,
26、r13是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基,
27、r14是氢或任选地被取代的烷基,
28、r13和r14可以结合形成饱和的或不饱和的4-7元环,其可含有碳原子、氮原子或氧原子,且芳基环或杂芳基环可以稠合至所述环,
29、取代基-x15-r15可以取代在形成的饱和的或不饱和的4-7元环上或稠合的芳基环或杂芳基环上,
30、x15是-o-、-nh-或单键,
31、r15是氢、任选地被取代的烷基、任选地被取代的芳基或任选地被取代的杂芳基;
32、r1c是任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基或任选地被取代的杂芳基;
33、u是-(co)-或-ch2-,
34、r2是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
35、r3是-w31-w32-r33
36、其中
37、w31是-(co)-、-(so2)-或-ch2-
38、w32是-o-、-nh-或单键,和
39、r33是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
40、r4a是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
41、r4b是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
42、r4a和r4b任选地与所键合的碳一起形成螺环,所述螺环任选地在环中具有氧原子或氮原子;且
43、r5是氢或任选地被取代的烷基;
44、前提条件是,不包括(3r,6s)-3-乙基-8-异戊基-6-(2-(甲硫基)乙基)-4,7-二氧代六氢吡嗪并[2,1-c][1,2,4]噁二嗪-1(6h)-甲酸异丙酯。
45、[2][1]的化合物或其药学上可接受的盐,其中
46、r1a是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基或任选地被取代的芳基烷基;
47、r1b是氢、任选地被取代的烷基或-w11’-w12’-r13’
48、其中
49、w11’是-(co)-,
50、w12’是-nh-且
51、r13’是任选地被取代的烷基或任选地被取代的芳基烷基;
52、r2是任选地被取代的烷基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基或任选地被取代的环烃基烷基;
53、r3是-w31’-w32’-r33’
54、其中
55、w31’是-(co)-、-(so2)-或-ch2-,
56、w32’是-o-、-nh-或单键,且
57、r33’是任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
58、r4a是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基;
59、r4b是氢或任选地被取代的烷基;
60、r4a和r4b任选地与所键合的碳一起形成螺环,所述螺环任选地在环中具有氧原子或氮原子;
61、r5是氢或任选地被取代的烷基。
62、[3][1]的化合物或其药学上可接受的盐,所述化合物由下式(ia)表示:
63、
64、其中
65、r1aa是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
66、r1ba是氢、任选地被取代的烷基或-w11a-w12a-r13a
67、其中
68、w11a是-(co)-或-(so2)-,
69、w12a是键、-o-或-nh-,且
70、r13a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
71、r2a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
72、r3a是-w31a-w32a-r33a
73、其中
74、w31a是-(co)-或-(so2)-,
75、w32a是-o-或-nh-,且
76、r33a是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
77、r4aa是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
78、r4ba是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
79、r4aa和r4ba任选地与所键合的碳一起形成螺环;且
80、r5a是氢或任选地被取代的烷基;
81、前提条件是,不包括(3r,6s)-3-乙基-8-异戊基-6-(2-(甲硫基)乙基)-4,7-二氧代六氢吡嗪并[2,1-c][1,2,4]噁二嗪-1(6h)-甲酸异丙酯。
82、[4][3]的化合物或其药学上可接受的盐,其中
83、r1aa是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基或任选地被取代的芳基烷基;
84、r1ba是氢、任选地被取代的烷基或-w11a’-w12a’-r13a’
85、其中
86、w11a’是-(co)-,
87、w12a’是-nh-,且
88、r13a’是任选地被取代的烷基或任选地被取代的芳基烷基;
89、r2a是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基;
90、r3a是-w31a’-w32a’-r33a’
91、其中
92、w31a’是-(co)-,
93、w32a’是-o-或-nh-,且
94、r33a’是任选地被取代的烷基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基或任选地被取代的环烃基烷基;
95、r4aa是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基;
96、r4ba是氢;
97、r5a是氢。
98、[5][1]或[2]的化合物或其药学上可接受的盐,其中
99、r1a是任选地被取代的烷基、任选地被取代的芳基、任选地被取代的环烃基或任选地被取代的芳基烷基;
100、r1b是氢、任选地被取代的烷基或-w11’-w12’-r13’
101、其中
102、w11’是-(co)-,
103、w12’是-nh-且
104、r13’是任选地被取代的烷基或任选地被取代的芳基烷基。
105、[6][3]或[4]的化合物或其药学上可接受的盐,其中
106、r1aa是任选地被取代的烷基、任选地被取代的芳基、任选地被取代的环烃基或任选地被取代的芳基烷基;
107、r1ba是氢、任选地被取代的烷基或-w11a’-w12a’-r13a’
108、其中
109、w11a’是-(co)-,
110、w12a’是-nh-,且
111、r13a’是任选地被取代的烷基或任选地被取代的芳基烷基。
112、[7][1]或[2]的化合物或其药学上可接受的盐,其中
113、r1c是任选地被取代的杂环烃基。
114、[8][1]或[2]的化合物或其药学上可接受的盐,其中
115、u是-(co)-。
116、[9][1]或[2]的化合物或其药学上可接受的盐,其中
117、r2是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基。
118、[10][3]或[4]的化合物或其药学上可接受的盐,其中
119、r2a是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基。
120、[11][1]或[2]的化合物或其药学上可接受的盐,其中
121、r3是-w31’-w32’-r33’
122、其中
123、w31’是-(co)-或-ch2-,
124、w32’是-o-、-nh-或单键,且
125、r33’是任选地被取代的烷基、任选地被取代的芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
126、[12][1]或[2]的化合物或其药学上可接受的盐,其中
127、r4a是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基,
128、r4b是氢,且
129、r5是氢。
130、[13][3]或[4]的化合物或其药学上可接受的盐,其中
131、r4aa是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基,
132、r4ba是氢,且
133、r5a是氢。
134、[14]药物组合物,其包含[1]至[13]中的任一项的化合物或其药学上可接受的盐和任选的药学上可接受的载体或稀释剂。
135、[15][14]的药物组合物,其中所述组合物包含有效量的所述化合物。
136、[16]治疗或预防涉及notch信号转导的疾病的方法,所述方法包括以有效治疗或预防所述疾病的量给有此需要的对象施用[1]至[13]中的任一项的化合物或其药学上可接受的盐或[14]或[15]的组合物。
137、[17]用于治疗或预防涉及notch信号转导的疾病的药剂,其包含[1]至[13]中的任一项的化合物或其药学上可接受的盐。
138、[18]根据[1]至[13]中的任一项的化合物或其药学上可接受的盐或[14]或[15]的组合物,其用作治疗或预防涉及notch信号转导的疾病的药物。
139、[发明效果]
140、本发明的式(i)的化合物抑制notch信号转导并因此可以用于治疗多种涉及notch信号转导的疾病。
141、[附图简述]
142、[图1]图1显示了d-10的1h nmr(400mhz,cdcl3)数据。
143、[图2]图2显示了d-13-int1的1h nmr(400mhz,cdcl3)数据。
144、[图3]图3显示了d-13的1h nmr(400mhz,cdcl3)数据。
145、[图4]图4显示了d-8的1h nmr(400mhz,cdcl3)数据。
146、[图5]图5显示了d-12的1h nmr(400mhz,cdcl3)数据。
147、[图6]图6显示了d-82的1h nmr(400mhz,cdcl3)数据。
148、[图7]图7显示了b-128-int1的1h nmr(400mhz,cdcl3)数据。
149、[图8]图8显示了b-128的1h nmr(400mhz,cdcl3)数据。
150、[图9]图9显示了b-72的1h nmr(400mhz,cdcl3)数据。
151、[图10]图10显示了a-22-int2的1h nmr(400mhz,cdcl3)数据。
152、[图11]图11显示了a-22-int3的1h nmr(400mhz,cdcl3)数据。
153、[图12]图12显示了a-22-int4的1h nmr(400mhz,cdcl3)数据。
154、[图13]图13显示了a-22-int5的1h nmr(400mhz,cdcl3)数据。
155、[图14]图14显示了a-22-int6的1h nmr(400mhz,cdcl3)数据。
156、[图15]图15显示了a-22的1h nmr(400mhz,cdcl3)数据。
157、[图16]图16显示了a-43-int3的1h nmr(400mhz,cdcl3)数据。
158、[图17]图17显示了a-43的1h nmr(400mhz,dmso)数据。
159、[图18]图18显示了a-60-int2的1h nmr(400mhz,cdcl3)数据。
160、[图19]图19显示了a-60-int3的1h nmr(400mhz,dmso)数据。
161、[图20]图20显示了a-60的1h nmr(400mhz,cdcl3)数据。
162、[图21]图21显示了a-52-int2的1h nmr(400mhz,dmso)数据。
163、[图22]图22显示了a-52-int3的1h nmr(400mhz,cdcl3)数据。
164、[图23]图23显示了a-52-int4的1h nmr(400mhz,dmso)数据。
165、[图24]图24显示了a-52-int5的1h nmr(400mhz,dmso)数据。
166、[图25]图25显示了a-52-int6的1h nmr(400mhz,dmso)数据。
167、[图26]图26显示了a-52的1h nmr(400mhz,cdcl3)数据。
168、[图27]图27显示了i-128的1h nmr(400mhz,cdcl3)数据。
169、[图28]图28显示了i-182的1h nmr(300mhz,cdcl3)数据。
170、[实施方案的描述]
171、定义
172、除非另有说明,否则在本说明书和权利要求书中使用的以下术语对于本技术的目的应具有下述含义。
173、除非另外指出,否则“低级”是指构成给定基团的碳原子的数目是1至6。
174、除非另有说明,否则“任选地被取代”是指给定基团可以通过可用化合价仅由氢取代基组成,或者可以通过可用化合价进一步包含一个或多个非氢取代基。一般而言,非氢取代基可以是可与指定要被取代的给定基团的原子结合的任何取代基。取代基的例子包括、但不限于-r6、-or6、-cor6、-coor6、-ocor6、-conr6r7、-nr6r7、-nr7cor6、-nr7coor6、-sr6、-so2r6、-so2nr6r7、-so2or6、-oso2r6、-nhc(nhr6)nr7、-nhc(nh2)nh、-cn、-no2、卤素和亚甲基二氧基,其中r6和r7独立地选自氢,直链的或支链的、环状的或非环状的、被取代的或未被取代的烷基链、芳基、杂芳基、芳基烷基和杂芳基烷基部分。
175、“卤素”是指氟、氯、溴或碘。“卤代”是指氟代、氯代、溴代或碘代。
176、“烷基”是指具有碳原子链的直链的或支链的、饱和的脂族基团。通常使用cx-y烷基,其中x和y指示链中碳原子的数目。链中碳原子的数目优选为1-10,更优选1-6,进一步优选1-4。烷基的非排它性例子包括甲基、乙基、丙基、异丙基、丁基、仲丁基、异丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、己基、异己基等。
177、“烯基”是指含有至少一个碳-碳双键的直链或支链碳链。通常使用cx-y烯基,其中x和y指示链中碳原子的数目。链中碳原子的数目优选为2-10,更优选2-6。烯基的非排它性例子包括乙烯基(ethenyl或vinyl)、烯丙基、异丙烯基、2-甲基烯丙基、1-戊烯基、己烯基、庚烯基、1-丙烯基、2-丁烯基、2-甲基-2-丁烯基等。
178、“炔基”是指含有至少一个碳-碳三键的直链或支链碳链。通常使用cx-y炔基,其中x和y指示链中碳原子的数目。链中碳原子的数目优选为2-10,更优选2-6。炔基的非排它性例子包括乙炔基、炔丙基、3-甲基-1-戊炔基、2-庚炔基等。
179、除非另外指出,否则“亚烷基”是指直链的或支链的、饱和的脂族多价碳链。通常使用cx-y亚烷基,其中x和y指示链中碳原子的数目。链中碳原子的数目优选为1-10,更优选1-6。亚烷基的非排它性例子包括亚甲基(-ch2-)、亚乙基(-ch2ch2-)、甲基亚甲基(-ch(ch3)-)、1,2-亚丙基(-ch2ch(ch3)-)、1,3-亚丙基(-ch2ch2ch2-)、1,2-亚丁基(-ch2ch(ch2ch3)-)、1,3-亚丁基(-ch2ch2ch(ch3)-)、1,4-亚丁基(-ch2ch2ch2ch2-)、2-甲基四亚甲基(-ch2ch(ch3)ch2ch2-)、五亚甲基(-ch2ch2ch2ch2ch2-)、1,2,3-丙烷三基、1,3,3-丙烷三基等。
180、“杂原子”是指不是碳原子和氢原子的原子。杂原子的特定例子包括、但不限于氮、氧和硫。
181、“芳基”是指单环或多环基团,其中每个环是芳族的或者当与一个或多个环稠合时形成芳族环。通常使用cx-y芳基,其中x和y指示环集合中碳原子的数目。所述环中碳原子的数目优选为6-14,更优选6-10。芳基的非排它性例子包括苯基、萘基、茚基、薁基、联苯基、芴基、蒽基、非那烯基等。“芳基”可以部分地氢化。部分地氢化的芳基的非排它性例子包括四氢萘基、茚满基等。
182、“杂芳基”是指单环或多环芳族基团,其中至少一个环原子是杂原子且其余环原子是碳。通常使用“x-y元杂芳基”,其中x和y指示环集合中碳原子和杂原子的数目。所述环中碳原子和杂原子的数目优选为5-14,更优选5-10。单环杂芳基包括、但不限于具有5或6个环原子的环状芳族基团,其中至少一个环原子是杂原子且其余环原子是碳。氮原子可以任选地季铵化且硫原子可以任选地氧化。本发明的单环杂芳基的非排它性例子包括、但不限于衍生自呋喃、咪唑、异噻唑、异噁唑、噁二唑、噁唑、1,2,3-噁二唑、吡嗪、吡唑、哒嗪、吡啶、嘧啶、吡咯、噻唑、1,3,4-噻二唑、三唑和四唑的那些。“杂芳基”也包括、但不限于二环或三环,其中所述杂芳基环稠合至1或2个环,所述环独立地选自芳基环、环烃基环和另一个单环杂芳基或杂环烃基环。二环或三环杂芳基的非排它性例子包括、但不限于衍生自苯并呋喃(例如苯并[b]呋喃)、苯并噻吩(例如苯并[b]噻吩)、苯并咪唑、苯并三嗪(例如苯并[e][1,2,4]三嗪、苯并[d][1,2,3]三嗪)、吡啶并嘧啶(例如吡啶并[4,3-d]嘧啶、吡啶并[3,4-d]嘧啶、吡啶并[3,2-d]嘧啶、吡啶并[2,3-d]嘧啶)、吡啶并吡嗪(例如吡啶并[3,4-b]吡嗪、吡啶并[2,3-b]吡嗪)、吡啶并哒嗪(例如吡啶并[2,3-c]哒嗪、吡啶并[3,4-c]哒嗪、吡啶并[4,3-c]哒嗪、吡啶并[3,2-c]哒嗪)、吡啶并三嗪(例如吡啶并[2,3-d][1,2,3]三嗪、吡啶并[3,4-d][1,2,3]三嗪、吡啶并[4,3-d][1,2,3]三嗪、吡啶并[3,2-d][1,2,3]三嗪、吡啶并[3,4-e][1,2,4]三嗪、吡啶并[3,2-e][1,2,4]三嗪)、苯并噻二唑(例如苯并[c][1,2,5]噻二唑)、呋喃并吡啶(例如呋喃并[3,2-b]吡啶、呋喃并[3,2-c]吡啶、呋喃并[2,3-c]吡啶、呋喃并[2,3-b]吡啶)、噁唑并吡啶(例如噁唑并[4,5-b]吡啶、噁唑并[4,5-c]吡啶、噁唑并[5,4-c]吡啶、噁唑并[5,4-b]吡啶)、噻唑并吡啶(例如噻唑并[4,5-b]吡啶、噻唑并[4,5-c]吡啶、噻唑并[5,4-c]吡啶、噻唑并[5,4-b]吡啶)、咪唑并吡啶(例如咪唑并[1,2-a]吡啶、咪唑并[4,5-c]吡啶、咪唑并[1,5-a]吡啶)、喹唑啉、噻吩并吡啶(例如噻吩并[2,3-c]吡啶、噻吩并[3,2-b]吡啶、噻吩并[2,3-b]吡啶)、吲嗪、喹啉、异喹啉、酞嗪、喹喔啉、噌啉、萘啶、喹嗪、吲哚、异吲哚、吲唑、吲哚啉、苯并噁唑、苯并吡唑、苯并噻唑、吡唑并吡啶(例如吡唑并[1,5-a]吡啶)、咪唑并嘧啶(例如咪唑并[1,2-a]嘧啶、咪唑并[1,2-c]嘧啶、咪唑并[1,5-a]嘧啶、咪唑并[1,5-c]嘧啶)、吡咯并吡啶(例如吡咯并[2,3-b]吡啶、吡咯并[2,3-c]吡啶、吡咯并[3,2-c]吡啶、吡咯并[3,2-b]吡啶)、吡咯并嘧啶(例如吡咯并[2,3-d]嘧啶、吡咯并[3,2-d]嘧啶、吡咯并[1,2-c]嘧啶、吡咯并[1,2-a]嘧啶)、吡咯并吡嗪(例如吡咯并[2,3-b]吡嗪、吡咯并[1,2-a]吡嗪)、吡咯并哒嗪(例如吡咯并[1,2-b]哒嗪)、三唑并吡啶(例如三唑并[1,5-a]吡啶)、蝶啶、嘌呤、咔唑、吖啶、萘嵌间二氮杂苯、1,10-菲咯啉、二苯并氧硫杂环己二烯(phenoxathiin)、吩噁嗪、吩噻嗪、吩嗪等的那些。所述二环或三环杂芳基环可以通过杂芳基本身或它所稠合的芳基、环烃基或杂环烃基连接至母体分子。
183、“环烃基”是指非芳族的、饱和的或部分不饱和的、单环的、稠合的二环或桥连多环基团。通常使用cx-y环烃基,其中x和y指示环集合中碳原子的数目。所述环中碳原子的数目优选为3-10,更优选3-8。环烃基的非排它性例子包括环丙基、环丁基、环戊基、环己基、环己烯基、2,5-环己二烯基、二环[2.2.2]辛基、金刚烷-1-基、十氢萘基、二环[2.2.1]庚-1-基等。
184、“杂环烃基”是指在本技术中定义的环烃基,前提条件是,一个或多个形成环的原子是独立地选自n、o或s的杂原子。通常使用cx-y杂环烃基,其中x和y指示环集合中碳原子和杂原子的数目。所述环中碳原子和杂原子的数目优选为3-10,更优选3-8。杂环烃基的非排它性例子包括哌啶基、4-吗啉基、4-哌嗪基、吡咯烷基、全氢吡咯烷基、1,4-二氮杂全氢环庚三烯基(1,4-diazaperhydroepinyl)、1,3-二氧杂环己烷基、1,4-二氧杂环己烷基等。
185、此外,上述定义可以应用于其中连接了上述取代基的基团。例如,“芳基烷基”是指被一个或多个芳基取代的直链或支链烷基,诸如苯甲基、1-苯基乙基、2-苯基乙基、3-苯基丙基、1-萘基甲基、2-萘基甲基等。“杂芳基烷基”是指被一个或多个杂芳基取代的直链或支链烷基。
186、“环烃基烷基”是指被一个或多个环烃基(例如,环丙基、环丁基、环戊基、环己基、环己烯基、2,5-环己二烯基、二环[2.2.2]辛基、金刚烷-1-基、十氢萘基、二环[2.2.1]庚-1-基)取代的直链或支链烷基。“杂环烃基烷基”是指被一个或多个杂环烃基取代的直链或支链烷基。
187、本文中使用的“单环”是指单环的、饱和的或不饱和的碳环,或单环的、饱和的或不饱和的杂环。通常使用“x元单环”,其中x指示环集合中碳原子和杂原子的数目。所述环中碳原子和杂原子的数目优选为4-7,更优选5或6。“单环杂环”是指单环的、芳族或非芳族环,其中至少一个环原子是杂原子(优选s、n或o)且其余环原子是碳。所述氮原子可以任选地季铵化且所述硫原子可以任选地氧化。
188、单环饱和碳环的非排它性例子包括环丙烷、环丁烷、环戊烷、环己烷、环庚烷等。
189、单环不饱和碳环的非排它性例子包括环丙烯、环丁烯、环戊烯、环己烯、环庚烯、环戊二烯、苯等。
190、单环饱和杂环的非排它性例子包括吡咯烷、哌啶、吗啉、哌嗪、1,3-二氧杂环己烷、1,4-二氧杂环己烷等。
191、单环不饱和杂环的非排它性例子包括吡唑、二氢吡咯、吡咯、二氢吡唑、咪唑、噻吩、噻唑、异噻唑、噻二唑、呋喃、噁唑、异噁唑、噁二唑、吡啶、哒嗪、嘧啶、吡嗪、三嗪等。
192、本文中使用的“螺环”是指饱和的或不饱和的环烃(cycloalkane)或饱和的或不饱和的杂环烃(heterocycloalkane)。
193、“环烃”是指非芳族的、饱和的或部分不饱和的、单环的、稠合的二环或桥连多环。通常使用cx-y环烃,其中x和y指示环集合中碳原子的数目。所述环中碳原子的数目优选为3-10,更优选3-8。环烃的非排它性例子包括环丙烷、环丁烷、环戊烷、环己烷、环庚烷、环辛烷等。
194、“杂环烃”是指如在本技术中定义的环烃,前提条件是,形成环的原子中的一个或多个是独立地选自n、o和s的杂原子。通常使用cx-y杂环烃,其中x和y指示环集合中碳原子和杂原子的数目。所述环中碳原子和杂原子的数目优选为3-10,更优选3-8。杂环烃的非排它性例子包括哌啶、吗啉、哌嗪、吡咯烷、全氢吡咯嗪、四氢呋喃、四氢吡喃、1,3-二氧杂环己烷、1,4-二氧杂环己烷等。
195、“饱和的或不饱和的4-7元环”是指属于上述单环的4-7元环。
196、“受保护的衍生物”是指其中一个或多个反应位点被保护基团封闭的化合物的衍生物。合适的保护基团的综合列表可以参见t.w.greene,protecting groups in organicsynthesis,第5版,john wiley&sons,inc.2014。
197、“异构体”是指具有相同的分子式但它们的原子的键合性质或顺序或它们的原子在空间中的排列不同的任何化合物。其原子在空间中排列不同的异构体被称为“立体异构体”。不是彼此镜像的立体异构体被称为“非对映异构体”,且为不可重叠镜像的立体异构体被称为“对映异构体”或有时被称为“光学异构体”。与四个不同取代基键合的碳原子被称为“手性中心”。具有一个手性中心的化合物具有两种相反手性的对映异构形式。两种对映异构形式的混合物被称为“外消旋混合物”。具有超过一个手性中心的化合物具有2n-1个对映异构体对,其中n是手性中心的数目。具有超过一个手性中心的化合物可以作为单个非对映异构体或作为非对映异构体的混合物存在,后者被称为“非对映异构体混合物”。当存在一个手性中心时,可以通过该手性中心的绝对构型来表征立体异构体。绝对构型是指与手性中心相连的取代基的空间排列。对映异构体通过其手性中心的绝对构型来表征,并通过cahn、ingold和prelog的r-和s-顺序规则进行描述。立体化学命名法的惯例、立体化学的确定方法和立体异构体的分离是本领域众所周知的(例如,参见“advanced organicchemistry”,第4版,march,jerry,john wiley&sons,new york,1992)。本发明的化合物可以包括这些异构体。
198、“动物”包括人类、非人哺乳动物(例如,小鼠、大鼠、狗、猫、兔、牛、马、绵羊、山羊、猪、鹿等)和非哺乳动物(例如,禽类等)。
199、“疾病”具体包括动物或其部分的任何不健康状况,并且包括可能由应用于该动物的医学或兽医疗法引起或偶然发生的不健康状况,即这样的疗法的“副作用”。
200、“药学上可接受的”是指可用于制备通常安全的、无毒的且在生物学上或其它方面均无不良影响的药物组合物的物质,并且包括对于兽医学应用以及人类药物应用而言可接受的物质。
201、“药学上可接受的盐”或“盐”是指本发明的化合物的盐,其如上定义是药学上可接受的,并且其具有期望的药理学活性。这样的盐包括与以下酸形成的酸加成盐:无机酸诸如盐酸、氢溴酸、硫酸、硝酸、磷酸等;或有机酸诸如乙酸、丙酸、己酸、庚酸、环戊烷丙酸、羟乙酸、丙酮酸、乳酸、丙二酸、琥珀酸、苹果酸、马来酸、富马酸、酒石酸、柠檬酸、苯甲酸、邻-(4-羟基苯甲酰基)苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、1,2-乙烷二磺酸、2-羟基乙磺酸、苯磺酸、对氯苯磺酸、2-萘磺酸、对甲苯磺酸、樟脑磺酸、4-甲基二环[2.2.2]辛-2-烯-1-甲酸、葡庚糖酸、4,4′-亚甲基双(3-羟基-2-烯-1-甲酸)、3-苯基丙酸、三甲基乙酸、叔丁基乙酸、三氟乙酸、月桂基硫酸、葡糖酸、谷氨酸、羟基萘甲酸、水杨酸、硬脂酸、粘康酸等。
202、药学上可接受的盐还包括存在的酸性质子能够与无机碱或有机碱反应时可形成的碱加成盐。可接受的无机碱包括氢氧化钠、碳酸钠、氢氧化钾、氢氧化铝和氢氧化钙。可接受的有机碱包括乙醇胺、二乙醇胺、三乙醇胺、氨丁三醇、n-甲基葡糖胺等。
203、“有效治疗的量”是指当施用给动物以治疗疾病时足以实现对疾病的这种治疗的量。
204、“有效预防的量”是指当施用给动物以预防疾病时足以实现对疾病的这种预防的量。
205、“有效量”等于“有效治疗的量”和“有效预防的量”。
206、“治疗”是指本发明的化合物的任何施用,并包括:
207、(1)防止疾病在可能易患该疾病但尚未经历或表现出该疾病的病状或症状的动物中发生,
208、(2)抑制正在经历或表现出患病者的病状或症状的动物的疾病(即,阻止病状和/或症状的进一步发展),或
209、(3)改善正在经历或表现出患病者的病状或症状的动物的疾病(即,逆转病状和/或症状)。
210、关于本文提供的所有定义,应该注意的是,所述定义应当解释为开放式的,在这一意义上,可以包括除指定的取代基之外的其它取代基。
211、在本发明中,公开了由下式(i)表示的化合物或其药学上可接受的盐:
212、
213、其中
214、q表示下式(i-1)至(i-2)中的任一个:
215、
216、*是与n(氮原子)的结合位点;
217、r1a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
218、r1b是氢、任选地被取代的烷基或-w11-w12-r13
219、其中
220、w11是-(co)-或-(so2)-,
221、w12是键、-o-或-n(r14)-,
222、r13是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基,
223、r14是氢或任选地被取代的烷基,
224、r13和r14可以结合形成饱和的或不饱和的4-7元环,其可以含有碳原子、氮原子或氧原子,且芳基环或杂芳基环可以稠合至所述环,
225、取代基-x15-r15可以取代在形成的饱和的或不饱和的4-7元环上或稠合的芳基环或杂芳基环上,
226、x15是-o-、-nh-或单键,
227、r15是氢、任选地被取代的烷基、任选地被取代的芳基或任选地被取代的杂芳基;
228、r1c是任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基或任选地被取代的杂芳基;
229、u是-(co)-或-ch2-,
230、r2是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
231、r3是-w31-w32-r33
232、其中
233、w31是-(co)-、-(so2)-或-ch2-
234、w32是-o-、-nh-或单键,且
235、r33是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
236、r4a是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
237、r4b是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
238、r4a和r4b任选地与所键合的碳一起形成螺环,所述螺环任选地在环中具有氧原子或氮原子;且
239、r5是氢或任选地被取代的烷基。
240、在式(i)的另一个实施方案中,公开了具有下式(ia)的化合物或其药学上可接受的盐:
241、
242、其中
243、r1aa是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
244、r1ba是氢、任选地被取代的烷基或-w11a-w12a-r13a
245、其中
246、w11a是-(co)-或-(so2)-,
247、w12a是键、-o-或-nh-,且
248、r13a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
249、r2a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
250、r3a是-w31a-w32a-r33a
251、其中
252、w31a是-(co)-或-(so2)-,
253、w32a是-o-或-nh-,且
254、r33a是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
255、r4aa是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
256、r4ba是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
257、r4aa和r4ba任选地与所键合的碳一起形成螺环;且
258、r5a是氢或任选地被取代的烷基。
259、在式(i)或(ia)的一个实施方案中,r1a(在式(ia)的情况下,r1aa)是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
260、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
261、任选地被取代的烯基的例子包括乙烯基、烯丙基、1-丙烯基、2-甲基烯丙基等。
262、任选地被取代的炔基的例子包括乙炔基、1-丙炔基等。
263、任选地被取代的芳基和任选地被取代的杂芳基的例子包括联苯基、苯基、吡啶基、嘧啶基、哒嗪基、吡嗪基、三嗪基、吡咯基、噻吩基、呋喃基、噻唑基、噁唑基、咪唑基、四氢萘基、萘基、喹啉基、异喹啉基、喹唑啉基、喹喔啉基、噌啉基、萘啶基、苯并三嗪基、茚基、吡啶并嘧啶基、吡啶并吡嗪基、吡啶并哒嗪基、吡啶并三嗪基、苯并呋喃基、苯并噻吩基、吲哚基、吲唑基、苯并噁唑基、苯并咪唑基、苯并噻唑基、苯并噻二唑基、呋喃并吡啶基、噻吩并吡啶基、吡咯并吡啶基(pyrropyridinyl)、噁唑并吡啶基、噻唑并吡啶基、咪唑并吡啶基等。
264、任选地被取代的环烃基的例子包括环丙基、环丁基、环戊基、环己基、环庚基、金刚烷基等。
265、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4-二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4--二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
266、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
267、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2-二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
268、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
269、在式(i)或(ia)的另一个实施方案中,r1a(在式(ia)的情况下,r1aa)是氢、任选地被取代的烷基(例如,丁基、丙基、甲基、ch2conh2、ch2oh、2,2-二苯基乙基、萘基甲基、ch2cooh、苯基乙基)、任选地被取代的芳基(例如,萘基、苯基)、任选地被取代的杂芳基(例如,吡啶基)、任选地被取代的环烃基(例如,环己基)、任选地被取代的芳基烷基(例如,苄基、羟基苄基)、任选地被取代的杂芳基烷基或任选地被取代的环烃基烷基。
270、在式(i)的一个实施方案中,r1b是氢、任选地被取代的烷基或-w11-w12-r13
271、其中
272、w11是-(co)-或-(so2)-,
273、w12是键、-o-或-n(r14)-,
274、r13是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基,
275、r14是氢或任选地被取代的烷基,
276、r13和r14可以结合形成饱和的或不饱和的4-7元环,其可以含有碳原子、氮原子或氧原子,且芳基环或杂芳基环可以稠合至所述环,
277、取代基-x15-r15可以取代在形成的饱和的或不饱和的4-7元环上或稠合的芳基环或杂芳基环上,
278、x15是-o-、-nh-或单键,
279、r15是氢、任选地被取代的烷基、任选地被取代的芳基或任选地被取代的杂芳基。
280、在式(ia)的一个实施方案中,r1ba是氢、任选地被取代的烷基或-w11a-w12a-r13a
281、其中
282、w11a是-(co)-或-(so2)-,
283、w12a是键、-o-或-nh-,且
284、r13a是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
285、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
286、任选地被取代的烯基的例子包括乙烯基、烯丙基、1-丙烯基、2-甲基烯丙基等。
287、任选地被取代的炔基的例子包括乙炔基、1-丙炔基等。
288、任选地被取代的芳基和任选地被取代的杂芳基的例子包括联苯基、苯基、吡啶基、嘧啶基、哒嗪基、吡嗪基、三嗪基、吡咯基、噻吩基、呋喃基、噻唑基、噁唑基、咪唑基、四氢萘基、萘基、喹啉基、异喹啉基、喹唑啉基、喹喔啉基、噌啉基、萘啶基、苯并三嗪基、茚基、吡啶并嘧啶基、吡啶并吡嗪基、吡啶并哒嗪基、吡啶并三嗪基、苯并呋喃基、苯并噻吩基、吲哚基、吲唑基、苯并噁唑基、苯并咪唑基、苯并噻唑基、苯并噻二唑基、呋喃并吡啶基、噻吩并吡啶基、吡咯并吡啶基(pyrropyridinyl)、噁唑并吡啶基、噻唑并吡啶基、咪唑并吡啶基等。
289、任选地被取代的环烃基的例子包括环丙基、环丁基、环戊基、环己基、环庚基、金刚烷基等。
290、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4--二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4-二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
291、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
292、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2-二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
293、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
294、饱和的或不饱和的4-7元环(其可以含有碳原子、氮原子或氧原子)的例子包括烃环诸如苯、环庚间三烯、环戊烷、环己烷、环庚烷、1-环戊烯、2-环戊烯、3-环戊烯、1-环己烯、2-环己烯、3-环己烯、1-环庚烯、2-环庚烯、3-环庚烯、2.4-环庚二烯等,和杂环诸如吡啶、吡嗪、嘧啶、咪唑、呋喃、噻吩、二氢吡啶、二氮杂环庚三烯、氧杂氮杂环庚三烯、吡咯烷、哌啶、六亚甲基亚胺、七亚甲基亚胺、四氢呋喃、哌嗪、高哌嗪、四氢氧氮杂环庚三烯(tetrahydroxazepine)、吗啉、硫代吗啉、吡咯、吡唑、1,2,3-三唑、噁唑、噁唑烷、噻唑、噻唑烷、异噁唑、咪唑啉、三唑、噻二唑、噁二唑、噁噻二唑、三嗪等等。
295、在式(i)的另一个实施方案中,r1b是氢、任选地被取代的烷基或-w11’-w12’-r13’
296、其中
297、w11’是-(co)-,
298、w12’是-nh-,且
299、r13’是任选地被取代的烷基(例如,-(ch2)2oh、-(ch2)3oh、戊基、己基、-(ch2)2conh2、-(ch2)3conh2)、任选地被取代的环烃基、任选地被取代的芳基烷基(例如,-(ch2)2ph、-(ch2)3ph、-(ch2)3ph(oh))、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。在式(ia)的另一个实施方案中,r1ba是氢、任选地被取代的烷基或-w11a’-w12a’-r13a’
300、其中
301、w11a’是-(co)-,
302、w12a’是-nh-,且
303、r13a’是任选地被取代的烷基(例如,-(ch2)2oh、-(ch2)3oh、戊基、己基、-(ch2)2conh2、-(ch2)3conh2)、任选地被取代的环烃基、任选地被取代的芳基烷基(例如,-(ch2)2ph、-(ch2)3ph、-(ch2)3ph(oh))、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。在式(i)或(ia)的另一个实施方案中,r2(在式(ia)的情况下,r2a)是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
304、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
305、任选地被取代的烯基的例子包括乙烯基、烯丙基、1-丙烯基、2-甲基烯丙基等。
306、任选地被取代的炔基的例子包括乙炔基、1-丙炔基等。
307、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4-二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4--二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
308、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
309、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2--二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
310、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
311、在式(i)或(ia)的另一个实施方案中,r2(在式(ia)的情况下,r2a)是氢、任选地被取代的烷基(例如,甲基、丙基、丁基、-(ch2)4nh2、-ch2oh、-ch2conh2、-ch2ch2conh2、-ch2cooh、胍基丙基)、任选地被取代的芳基烷基(例如,苄基、羟基苄基)、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基(例如,环己基甲基)。
312、在式(i)的另一个实施方案中,r3是-w31-w32-r33
313、其中
314、w31是-(co)-、-(so2)-或-ch2-
315、w32是-o-、-nh-或单键,且
316、r33是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基;
317、r4a是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
318、在式(ia)的另一个实施方案中,r3a是-w31a-w32a-r33a
319、其中
320、w31a是-(co)-或-(so2)-,
321、w32a是-o-或-nh-,且
322、r33a是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
323、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
324、任选地被取代的芳基和任选地被取代的杂芳基的例子包括联苯基、苯基、吡啶基、嘧啶基、哒嗪基、吡嗪基、三嗪基、吡咯基、噻吩基、呋喃基、噻唑基、噁唑基、咪唑基、四氢萘基、萘基、喹啉基、异喹啉基、喹唑啉基、喹喔啉基、噌啉基、萘啶基、苯并三嗪基、茚基、吡啶并嘧啶基、吡啶并吡嗪基、吡啶并哒嗪基、吡啶并三嗪基、苯并呋喃基、苯并噻吩基、吲哚基、吲唑基、苯并噁唑基、苯并咪唑基、苯并噻唑基、苯并噻二唑基、呋喃并吡啶基、噻吩并吡啶基、吡咯并吡啶基(pyrropyridinyl)、噁唑并吡啶基、噻唑并吡啶基、咪唑并吡啶基等。
325、任选地被取代的环烃基的例子包括环丙基、环丁基、环戊基、环己基、环庚基、金刚烷基等。
326、任选地被取代的杂环烃基的例子包括哌啶基、4-吗啉基、4-哌嗪基、吡咯烷基、全氢吡咯烷基、1,3-二氧杂环己烷基、1,4-二氧杂环己烷基、四唑基等。
327、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4-二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4--二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
328、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
329、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2--二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
330、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
331、在式(i)的另一个实施方案中,r3是-w31’-w32’-r33’
332、其中
333、w31’是-(co)-、-(so2)-或-ch2-,
334、w32’是-o-、-nh-或单键,且
335、r33’是任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基、任选地被取代的杂环烃基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
336、在式(ia)的另一个实施方案中,r3a是-w31’-w32’-r33’
337、其中
338、w31’是-(co)-,
339、w32’是-o-或-nh-,且
340、r33’是任选地被取代的烷基(例如,甲基、丙基、丁基、戊基、己基、二苯基丙基)、任选地被取代的芳基烷基(例如,苄基、萘基甲基、羟基苯基乙基、苯基乙基)、任选地被取代的杂芳基烷基(例如,吡啶基甲基)、任选地被取代的环烃基烷基(例如,环己基甲基)或任选地被取代的杂环烃基烷基。
341、在式(i)或(ia)的一个实施方案中,r4a(在式(ia)的情况下,r4aa)是任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
342、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
343、任选地被取代的烯基的例子包括乙烯基、烯丙基、1-丙烯基、2-甲基烯丙基等。
344、任选地被取代的炔基的例子包括乙炔基、1-丙炔基等。
345、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4--二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4-二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
346、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
347、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2-二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
348、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
349、在式(i)或(ia)的另一个实施方案中,r4a(在式(ia)的情况下,r4a)是任选地被取代的烷基(例如,甲基、乙基、丙基、丁基、胍基丙基、-ch2oh、-ch2conh2、-ch2ch2conh2)、任选地被取代的芳基烷基(例如,苄基、羟基苄基)、任选地被取代的环烃基烷基(例如,环己基甲基)。
350、在式(i)或(ia)的一个实施方案中,r4b(在式(ia)的情况下,r4ba)是氢、任选地被取代的烷基、任选地被取代的烯基、任选地被取代的炔基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基、任选地被取代的环烃基烷基或任选地被取代的杂环烃基烷基。
351、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
352、任选地被取代的烯基的例子包括乙烯基、烯丙基、1-丙烯基、2-甲基烯丙基等。
353、任选地被取代的炔基的例子包括乙炔基、1-丙炔基等。
354、任选地被取代的芳基烷基的例子包括未被取代的芳基烷基或具有烷基的芳基烷基,诸如苄基、α-甲基苄基、苯乙基、α-甲基苯乙基、α,α-二甲基苄基、α,α-二甲基苯乙基、4-甲基苯乙基、4-甲基苄基、4-异丙基苄基等;具有芳基或芳基烷基的芳基烷基,诸如4-苄基苄基、4-苯乙基苄基、4-苯基苄基等;具有被取代的氧基的芳基烷基,诸如4-甲氧基苄基、4-正十四烷基氧基苄基、4-正十七烷基氧基苄基、3,4-二甲氧基苄基、4-甲氧基甲基苄基、4-乙烯基氧基甲基苄基、4-苄氧基苄基、4-苯乙基氧基苄基等;具有羟基的芳基烷基,诸如4-羟基苄基、4-羟基-3-甲氧基苄基等;具有卤素原子的芳基烷基,诸如4-氟苄基、3-氯苄基、3,4-二氯苄基等;2-糠基、二苯基甲基、1-萘基甲基、2-萘基甲基等。
355、任选地被取代的杂芳基烷基的例子包括2-吡啶基甲基、3-吡啶基甲基、2-嘧啶基甲基、5-嘧啶基甲基、3-哒嗪基甲基、2-吲哚基甲基、5-吲哚基甲基、2-苯并呋喃基甲基、5-吲哚基甲基、2-苯并噻吩基甲基、5-苯并噻吩基甲基、6-氟-2-苯并呋喃基甲基、6-氯-2-苯并呋喃基甲基、6-甲氧基-2-苯并呋喃基甲基、6-氟-2-苯并噻吩基甲基、6-氯-2-苯并噻吩基甲基、6-甲氧基-2-苯并噻吩基甲基和6-苯基-3-哒嗪基甲基等。
356、任选地被取代的环烃基烷基的例子包括环丙基甲基、氟环丙基甲基、氯环丙基甲基、溴环丙基甲基、碘环丙基甲基、甲基环丙基甲基、1,1-二甲基环丙基甲基、1,2-二甲基环丙基甲基、羟基环丙基甲基、甲氧基环丙基甲基、乙氧基环丙基甲基、甲氧基羰基环丙基甲基、甲基氨基甲酰基环丙基甲基、环丙基乙基、环己基甲基、环丙基己基等。
357、任选地被取代的杂环烃基烷基的例子包括(2-四氢呋喃基)甲基、(2-四氢噻吩基)甲基等。
358、在式(i)的另一个实施方案中,r4b是氢或任选地被取代的烷基(例如,甲基)。
359、在式(ia)的另一个实施方案中,r4ba是氢。
360、在式(i)的另一个实施方案中,r4a和r4b可以与所键合的碳一起形成螺环。可以由r4a和r4b与所键合的碳一起形成的螺环是例如环丙烷等。
361、所述螺环可以在环中含有氧原子或氮原子。
362、在式(i)或(ia)的一个实施方案中,r5(在式(ia)的情况下,r5a)是氢或任选地被取代的烷基。
363、任选地被取代的烷基的例子包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、叔戊基、氨基甲基、氨基乙基、氨基丙基、氨基丁基、羧基甲基、羧基乙基、羧基丙基、羧基丁基、氨基甲酰基甲基、氨基甲酰基乙基、氨基甲酰基丙基、氨基甲酰基丁基、甲氧基甲基、甲氧基乙基、甲氧基丙基、甲氧基丁基、甲硫基甲基、甲硫基乙基、甲硫基丙基、甲硫基丁基、羟甲基、羟乙基、羟丙基、羟丁基、乙氧基羰基甲基、乙氧基羰基乙基、苄氧基甲基、苄氧基乙基、苄氧基丙基、苄氧基丁基、胍基甲基、胍基乙基、胍基丙基等。
364、在式(i)或(ia)的另一个实施方案中,r5(在式(ia)的情况下,r5a)是氢。
365、式(i)的一个优选实施方案是具有下式(ii)的化合物或其药学上可接受的盐:
366、
367、其中r1a’是氢、任选地被取代的烷基、任选地被取代的芳基、任选地被取代的杂芳基、任选地被取代的环烃基或任选地被取代的芳基烷基;
368、r1b’是氢、任选地被取代的烷基或-w11a’-w12a’-r13a’
369、其中
370、w11a’是-(co)-,
371、w12a’是-nh-,且
372、r13a’是任选地被取代的烷基或任选地被取代的芳基烷基;
373、r2’是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基;
374、r3’是-w31a’-w32a’-r33a’
375、其中
376、w31a’是-(co)-,
377、w32a’是-o-或-nh-,且
378、r33a’是任选地被取代的烷基、任选地被取代的芳基烷基、任选地被取代的杂芳基烷基或任选地被取代的环烃基烷基;
379、r4a’是任选地被取代的烷基、任选地被取代的芳基烷基或任选地被取代的环烃基烷基;
380、r4b’是氢;且
381、r5’是氢。
382、在下文中,具有式(i)、(ia)或式(ii)的化合物也被称作“本发明的化合物”。
383、本发明的化合物的一般合成描述于以下“制备方法”中。在制备方法和实施例中使用的缩写如下。
384、acoh:乙酸
385、boc:叔丁氧基羰基
386、t-buoh:叔丁醇
387、cbz:苄氧基羰基
388、cdcl3:氘代氯仿
389、cip:2-氯-1,3-二甲基咪唑鎓六氟磷酸盐
390、dbu:1,8-二氮杂双环[5.4.0]十一碳-7-烯
391、dce:1,2-二氯乙烷
392、dcm:二氯甲烷
393、diad:偶氮二甲酸二异丙酯
394、dibal:二异丁基铝
395、dic:n,n’-二异丙基碳二亚胺
396、diea:n,n-二异丙基乙胺
397、dipea:n-乙基-n-异丙基-丙-2-胺
398、dmf:n,n-二甲基甲酰胺
399、dmso:二甲亚砜
400、dmt-mm:4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉鎓氯化物
401、eto(oet):乙氧基
402、etoac:乙酸乙酯
403、etoh:乙醇
404、fmoc:9-芴基甲氧羰基
405、hatu:1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化物六氟磷酸盐
406、mecn:乙腈
407、meo(ome):甲氧基
408、meoh:甲醇
409、nhpi:n-羟基邻苯二甲酰亚胺
410、nmm:n-甲基吗啉
411、oac(aco):乙酰氧基
412、pbf:2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基
413、pe:ea:石油醚:乙酸乙酯
414、pg:氨基保护基团
415、ph:苯基
416、phthn:n-邻苯二甲酰亚胺基
417、pph3:三苯基膦
418、rt:室温
419、tbs:叔丁基二甲基甲硅烷基
420、tbscl:叔丁基(氯)二甲基甲硅烷
421、tbu:叔丁基
422、thf:四氢呋喃
423、tlc:薄层色谱法
424、trt:三苯甲基
425、制备方法
426、1)制备方法1
427、在其中u是-(co)-的情况下;
428、
429、[步骤1]中间体d的合成
430、根据已知的方法,诸如使用由式i-a表示的化合物(其中r5如上文所定义)和由式i-b表示的醛化合物(其中q如上文所定义)的还原烷基化,或使用由式i-c表示的化合物(其具有q和离去基团x,其中q如上文所定义)的取代反应,可以合成中间体d,其中q和r5如上文所定义。“离去基团”是指从经历消除反应或取代反应中的反应的有机化合物释放的原子或原子团。离去基团的例子包括、但不限于卤素基团、甲磺酰氧基、三氟甲磺酰氧基和甲苯磺酰氧基。
431、另外,通过已知的方法诸如下面所示的还原烷基化或使用离去基团x的取代反应,也可以合成中间体d。
432、
433、在由式i-d、i-e和i-f表示的化合物的每个式中,q和r5如上文所定义,且x是离去基团。
434、[步骤2]中间体b的合成
435、可以如下合成中间体b:使中间体d与中间体e的羧酸衍生物(其中r2如上文所定义,且pg是氨基保护基团)进行酰胺化缩合反应,随后进行去保护反应。在酰胺化缩合反应中,可以应用通常已知的酰胺化试剂和条件。hatu和dmt-mm优选作为缩合剂,dmf、meoh、thf等优选作为溶剂,且反应温度优选为0℃至溶剂的沸点。氨基保护基团的例子包括苄氧基羰基(cbz)、叔丁氧基羰基(boc)、叔戊氧基羰基、异冰片基氧基羰基、4-甲氧基苄氧基羰基、氯甲酸苄酯(cl-z)、溴甲酸苄酯(br-z)、金刚烷氧基羰基、三氟乙酰基、邻苯二甲酰基、甲酰基、2-硝基苯基亚磺酰基、二苯基硫膦基、9-芴基甲氧羰基(fmoc)、三苯甲基(trt)等。在去保护反应中,可以应用通常已知的反应。当式中的pg是fmoc基团时,在作为溶剂的乙酸乙酯、thf、meoh或二氯甲烷中使用哌啶或dbu作为去保护试剂的去保护反应是优选的。当pg是cbz基团时,在h2气氛下在作为溶剂的甲醇、乙醇或thf中使用钯催化剂诸如pd(oh)2、pd/c等的去保护反应是优选的。反应温度优选为0℃至溶剂的沸点。
436、[步骤3]化合物(i)的合成
437、可以如下合成化合物(i),其中式中的符号如上文所定义:使中间体b与中间体a(r3、r4a和r4b如上文所定义)进行酰胺化缩合反应,随后在酸存在下进行闭环反应。在酰胺化缩合反应中,可以应用通常已知的酰胺化试剂和条件。hatu或dmt-mm优选作为缩合剂,dmf、meoh、thf等优选作为溶剂,且反应温度优选为0℃至溶剂的沸点。作为用于闭环反应的酸,甲酸是优选的,并且甲酸也可以用作溶剂。反应温度优选为0℃至使用的溶剂的沸点。
438、通过下述方法可以制备中间体a。
439、
440、在nano3/h2so4条件下,可以将氨基酸衍生物i-g(r4a和r4b如上文所定义)的氨基转化成羟基。通过通常已知的方法,诸如在john wiley&sons,inc的“greene’s protectivegroups in organic synthesis,第5版”中描述的那些,可以将得到的中间体i-h(r4a和r4b如上文所定义)的羧酸基团转化成中间体i-i(pg2是羧酸的保护基团且式中的其它符号如上文所定义)。羧酸的保护基团的例子包括甲基、乙基、叔丁基、苄基、甲氧基甲基、三苯基甲基等。在mitsunobu反应条件下可以将i-i的羟基转化成n-羟基邻苯二甲酰亚胺基团。使用肼将中间体i-j(式中的符号如上文所定义)的邻苯二甲酰亚胺基团去保护,产生中间体i-k(式中的符号如上文所定义)。通过使用三光气用i-k和r33-x(r33如上文所定义,且x是氨基或醇基)进行缩合反应,可以合成中间体i-m(式中的符号如上文所定义)。通过保护基团pg2的去保护可以得到中间体a。
441、2)制备方法2
442、
443、通过下述方案,使用中间体b(其中q是-ch(-r1a)(-cootbu)且式中的其它符号如所定义的),可以合成化合物(i),其中q是-ch(-r1a)(-r1b),r1b是-(co)-nh-r13,且式中的其它符号如上文所定义。在闭环反应中,将叔丁酯基团去保护并在hcooh存在下转化成羧酸基团。在i-o(式中的符号如上文所定义)和中间体c(r13如上文所定义)的酰胺化缩合反应中,可以应用通常已知的酰胺化试剂和条件。hatu、cip或dmt-mm优选作为缩合剂,dmf、meoh、thf等优选作为溶剂,且反应温度优选为0℃至溶剂的沸点。
444、3)制备方法3
445、
446、可以如下合成化合物(i),其中r3是-(co)-nh-r33:进行中间体ab-1(pg是氨基保护基团,式中的其它符号如上文所定义)的去保护反应,随后使用三光气进行与胺衍生物r33-nh2的缩合反应。通过通常已知的方法或上述的步骤-1、步骤-2和步骤3,可以制备ab-1。
447、氨基保护基团pg的代表性例子包括苄氧基羰基(cbz)、9-芴基甲氧羰基(fmoc)等。在去保护反应中,可以应用通常已知的反应。当式中的pg是fmoc基团时,在作为溶剂的乙酸乙酯或二氯甲烷中使用哌啶或dbu作为去保护试剂的去保护反应是优选的。当pg是cbz基团时,在h2气氛下在作为溶剂的甲醇、乙醇或thf中使用钯催化剂诸如pd(oh)2、pd/c等的去保护反应是优选的。反应温度优选为0℃至使用的溶剂的沸点。在缩合反应中,dcm、dce、thf等是优选的溶剂,且反应温度优选为0℃至使用的溶剂的沸点。
448、4)制备方法4
449、
450、通过使用中间体i-p、醇衍生物r33-oh和三光气的反应,可以合成化合物(i),其中r3是-(co)-o-r33。dcm、dce、thf等是优选的溶剂,且反应温度优选为0℃至使用的溶剂的沸点。
451、5)制备方法5
452、
453、通过使用中间体i-p和r33-cooh(或r33-cocl)的酰胺化缩合反应,可以合成化合物(i),其中r3是-(co)-r33。dmf、dcm、dce、thf、meoh等优选作为溶剂,且反应温度优选为0℃至溶剂的沸点。当使用r33-cooh时,通常已知的酰胺化试剂诸如hatu、cip或dmt-mm用作缩合剂。
454、6)制备方法6
455、
456、通过使用中间体i-p和r33-so2cl的反应,可以合成化合物(i),其中r3是-(so2)-r33。dcm、dce、thf等是优选的溶剂。反应温度优选为0℃至使用的溶剂的沸点。
457、7)制备方法7
458、
459、通过在还原剂存在下使用中间体i-p和醛试剂r33-cho的反应,可以合成化合物(i),其中r3是-(ch2)-r33。通常已知的还原试剂诸如三乙酰氧基硼氢化钠、氰基硼氢化钠、四氢硼酸钠、四氢硼酸锂、thf-硼烷复合物、吡啶-硼烷复合物、甲基吡啶-硼烷复合物、二异丁基氢化铝(dibal)、氢化铝锂等优选作为还原试剂。meoh、thf、氯仿、dcm、dce、乙醚、二异丙基醚等优选作为溶剂。反应温度优选为-78℃至溶剂的沸点。
460、8)制备方法8
461、
462、通过下述方案,使用中间体ab-2和还原试剂,可以合成化合物(i),其中u是-(ch2)-。通过通常已知的方法或上述的步骤-1、步骤-2和步骤3,可以制备ab-2。通常已知的还原试剂诸如三乙酰氧基硼氢化钠、氰基硼氢化钠、四氢硼酸钠、四氢硼酸锂、thf-硼烷复合物、吡啶-硼烷复合物、甲基吡啶-硼烷复合物、二异丁基氢化铝(dibal)、氢化铝锂等优选作为还原试剂。meoh、thf、氯仿、dcm、dce、乙醚、二异丙基醚等优选作为溶剂,且反应温度优选为-78℃至溶剂的沸点。
463、每个步骤中的保护基团不限于在方案中具体指明的保护基团(例如,二乙缩醛基团),并且可以使用通常已知的保护基团诸如二甲缩醛基团。通过与保护基团相对应的一般方法,可以进行步骤2或步骤3中的去保护。当r1a、r1b、r13、r2、r3、r4a、r4b或r5具有受保护的官能团时,可以在任何步骤中进行去保护。在反应的每个步骤中合成的化合物可以不经分离直接用于下一步反应。在步骤3的条件下,可以同时进行闭环反应和去保护反应。
464、要在环化反应中得到的化合物可以通过常规方法诸如萃取、水洗、酸洗、碱洗、结晶、重结晶、硅胶柱色谱法分离和纯化。
465、进一步解释,本发明的化合物、其盐及其衍生物在选择性药理作用选择性、安全性(各种毒性和安全性药理学)、药代动力学性能、理化性质等方面都是优异的,并因此可以证实作为药物的活性成分的有效性。
466、关于药理作用选择性的试验的例子包括、但不限于对各种药理学靶受体的抑制或活化测定,对各种药理学靶酶、离子通道或转运蛋白的抑制测定,用于评价各种药理作用的细胞试验,等。
467、关于安全性的试验的例子包括、但不限于以下清单,包括细胞毒性试验(例如,使用hl60细胞、肝细胞等的试验等)、遗传毒性试验(例如,埃姆斯试验、小鼠淋巴瘤tk试验、染色体畸变试验、微核试验等)、皮肤致敏试验(例如,buehler方法、gpmt方法、apt方法、llna试验等)、皮肤光敏化试验(例如,adjuvant和strip方法等)、眼刺激试验(例如,单次滴注、短期持续滴注、重复滴注等)、心血管系统的安全性药理学试验(例如,遥测方法、apd方法、herg抑制测定等)、中枢神经系统的安全性药理学试验(例如,fob方法、irwin方法的修改版本等)、呼吸系统的安全性药理学试验(例如,使用呼吸功能测量装置的测量方法、使用血液气体分析仪的测量方法等)、一般毒性试验等。
468、关于药代动力学性能的试验的例子包括、但不限于以下清单,包括细胞色素p450酶抑制或诱导试验、细胞渗透性试验(例如,使用caco-2细胞、mdck细胞等的试验等)、药物转运蛋白atp酶测定、口服吸收试验、血液浓度转变测量试验、代谢试验(例如,稳定性试验、代谢物分子种类试验、反应性试验等)、溶解度试验(例如,基于浊度法的溶解度试验等)等。
469、关于理化性质的试验的例子包括、但不限于以下清单,包括化学稳定性试验(例如,使用hplc等的稳定性试验等)、分配系数(例如,使用辛醇相/水相的分配试验等)、电离常数试验、结晶试验等。
470、在另一个实施方案中,提供了一种通过施用本发明的化合物治疗多种疾病的方法。本发明的化合物可以用于预防或治疗受notch信号转导途径控制的疾病。
471、在一个实施方案中,使用诱导多西环素的慢病毒载体进行与notch信号转导途径的抑制作用有关的筛选(关于具体程序,参见实施例)。
472、这里的受试化合物是在本说明书中描述的化合物,即本发明的化合物。通常,将受试化合物以几种不同的浓度进行测试,并且所述浓度根据测定条件部分地进行选择。
473、通过与notch细胞内结构域相互作用,本发明的化合物可以抑制notch信号转导。
474、本发明也涉及使用含有本发明的一种或多种化合物的文库的前药。前药通常被设计为在通过酶促和/或化学水解吸收的过程中或之后在体内释放活性药物。前药方案是通过化学衍生化为水溶性更高的化合物来改善水溶性差的药物的口服生物利用度或静脉内施用的有效手段。增加含有羟基的药物的水溶性的最常用的前药方案是制备含有可电离基团的酯;例如,磷酸酯基团、羧酸酯基团、烷基氨基基团(fleisher等人,advanced drugdelivery reviews,115-130,1996;davis等人,cancer res.,7247-7253)。
475、在其它方面,本发明提供了含有本发明的化合物的药物组合物。这些组合物可以用于在下面详细描述的本发明的各种方法。
476、本发明的药物组合物被配制成与其预期的施用途径相容。施用途径的例子包括胃肠外施用,例如静脉内、真皮内、皮下、口服(例如、吸入)、透皮(局部)、透粘膜和直肠施用。用于胃肠外(特别是静脉内)、真皮内或皮下应用的溶液或混悬剂(例如,注射剂)可以包括以下组分:无菌稀释剂诸如注射用水、盐水溶液、不挥发性油、聚乙二醇、丙三醇、丙二醇或其它合成溶剂;抗菌剂诸如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂诸如抗坏血酸或亚硫酸氢钠;螯合剂诸如乙二胺四乙酸;缓冲剂诸如乙酸盐、柠檬酸盐或磷酸盐;以及用于调节张力的试剂,诸如氯化钠或右旋糖。另外,可以用酸或碱诸如盐酸或氢氧化钠调节ph。可以将胃肠外制剂包封在由玻璃或塑料制成的安瓿瓶、一次性注射器或多次剂量管形瓶中。
477、适合于注射使用的药物组合物包括无菌水溶液(在水溶性的情况下)或分散体以及用于即时制备无菌可注射溶液或分散体的无菌粉剂。对于静脉内施用,合适的载体包括生理盐水、抑制细菌的水、cremophor eltm(basf,parsippany,nj)或磷酸盐缓冲盐水(pbs)。在所有情况下,该组合物必须是无菌的,并且应该以易于注射的程度流动。其在生产和贮存条件下必须是稳定的,并且必须被保存免于微生物(诸如细菌和真菌)的污染作用。所述载体可以是含有例如水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)和它们的合适混合物的溶剂或分散介质。可以维持适当的流动性,例如,通过使用包衣诸如卵磷脂,通过维持所需的粒度(在分散体的情况下)和通过使用表面活性剂。微生物的作用的阻止可以通过各种抗细菌剂和抗真菌剂实现,例如,对羟基苯甲酸酯类、氯丁醇、苯酚、抗坏血酸、硫柳汞等。在许多情况下,优选在组合物中包括等渗剂,例如,糖、多元醇诸如甘露醇、山梨醇、氯化钠。通过在组合物中包括延迟吸收的试剂,例如,单硬脂酸铝和明胶,可以延长可注射组合物的吸收。
478、可以如下制备无菌可注射溶液:将活性化合物(例如,具有通式(i)的化合物)以需要的量与所需的上文列举的一种成分或多种成分的组合一起掺入适当的溶剂中,随后过滤灭菌。通常,如下制备分散体:将活性化合物掺入无菌媒介物中,所述媒介物含有分散介质和所需的来自上面列举的那些的其它成分。就用于制备无菌可注射溶液的无菌粉末而言,优选的制备方法是真空干燥和冷冻干燥,其由其先前无菌过滤的溶液得到活性成分和任何另外所需成分的粉末。
479、口服组合物通常包括惰性稀释剂或可食用的载体。它们可以被包封在明胶胶囊中或压成片剂。为了口服治疗施用的目的,所述活性化合物可以与赋形剂掺合并以片剂、糖锭剂或胶囊剂的形式使用。
480、口服组合物也可以使用液体载体制备以用作漱口剂,其中在液体载体中的化合物口服施用,并经漱口和吐出或咽下。药学上相容的粘合剂和/或辅料可以被包括为所述组合物的一部分。片剂、丸剂、胶囊剂、糖锭剂等可以含有任意下述成分或相似性质的化合物:粘合剂诸如微晶纤维素、黄蓍胶或明胶;赋形剂诸如淀粉或乳糖,崩解剂诸如藻酸、primogel或玉米淀粉;润滑剂诸如硬脂酸镁或sterotes;助流剂诸如胶体二氧化硅;甜味剂诸如蔗糖或糖精;或调味剂i诸如薄荷、水杨酸甲酯或橙味剂。
481、对于通过吸入施用,所述化合物以气溶胶喷雾的形式从加压容器或分配器(其含有合适的抛射剂,例如,气体诸如二氧化碳)或喷雾器递送。
482、全身施用还可以通过透粘膜或透皮方式。对于透粘膜或透皮施用,在制剂中使用适合要渗透的屏障的渗透剂。这样的渗透剂是本领域中普遍已知的,并且包括例如,对于透粘膜施用而言,清洁剂、胆汁盐和夫西地酸衍生物。通过使用鼻喷雾剂或栓剂可以实现透粘膜施用。对于透皮施用,将活性化合物配制成本领域普遍已知的软膏剂、油膏剂、凝胶或乳膏剂。
483、所述化合物还可以制备成用于直肠递送的栓剂(例如,与常规栓剂基质诸如可可脂和其它甘油酯一起)或保留灌肠剂的形式。
484、在一个实施方案中,将活性化合物与保护所述化合物免于从身体中快速消除的载体一起制备,诸如控释制剂,包括植入物和微囊化递送系统。可以使用可生物降解的、生物相容的聚合物,诸如乙烯-醋酸乙烯酯、聚酸酐、聚乙醇酸、胶原、聚原酸酯和聚乳酸。用于制备这样的制剂的方法对本领域技术人员来说是显而易见的。所述材料还可以商购自alzacorporation和nova pharmaceuticals,inc.。脂质体混悬液(包括用针对病毒抗原的单克隆抗体靶向受感染的细胞的脂质体)也可以用作药学上可接受的载体。这些可以根据本领域技术人员已知的方法来制备,例如,如在美国专利号4,522,811中所述。
485、有利的是,为了施用容易和剂量的均匀度,可以以剂量单位形式配制口服或胃肠外组合物。本文中使用的剂量单位形式是指适合作为要治疗的对象的单位剂量的物理上离散的单位;每个单位含有经计算会产生期望的治疗效果的预定量的活性化合物以及所需的药物载体。本发明的剂量单位形式的规格决定于且直接取决于:活性化合物的独有特征和要实现的特定治疗效果,和本领域中固有的为了治疗个体配混这样的活性化合物的限制。
486、例如,在某些实施方案中,本发明的药物组合物是适合以单位剂型口服施用的药物组合物,诸如含有约1mg至约1g本发明的化合物的片剂或胶囊剂。在某些其它的实施方案中,本发明的药物组合物是适合静脉内、皮下或肌肉内注射的药物组合物。患者可以接受例如约1μg/kg至约1g/kg的本发明化合物的静脉内、皮下或肌肉内剂量。借助于快速推注或通过在一段时间内连续输注,可以给予静脉内、皮下和肌肉内剂量。可替换地,患者接受与每日胃肠外剂量大致相等的每日口服剂量,每天施用所述组合物1至4次。
487、优选地,可以将本发明的式(i)的化合物静脉内(特别优选地,通过连续滴注或快速静脉内施用)施用给包括人在内的哺乳动物。
488、在这种情况下,根据各种因素诸如患者的体重和/或年龄、和/或症状的程度和施用途径,适当地选择剂量。例如,通过连续滴注施用,用于静脉内施用的式(i)的化合物的剂量通常在1-10000mg/天/m2人体表面积的范围内,优选在1-5000mg/天/m2人体表面积的范围内,且更优选10-5000mg/天/m2人体表面积。
489、含有本发明的化合物的药物组合物可以用于受notch信号转导途径调节的疾病。更具体地,抑制notch信号的化合物提供了一种用于抑制hes1和hes5的表达以及促进神经干细胞的分化的方法,并且有望成为新型神经再生药物的候选物。
490、本发明还提供了用于促进神经干细胞的分化的方法,其包括使神经干细胞与有效促进神经干细胞分化的量的根据式(i)的化合物接触。这样的方法还可用于治疗神经变性疾病(例如,青光眼、黄斑变性、帕金森病和阿尔茨海默氏病)和对神经系统的损伤。“神经干细胞”是指能够在适当条件下分化成神经元、星形胶质细胞或少突神经胶质细胞的克隆原性的、未分化的、多潜能细胞。如果神经干细胞在化合物存在下表现出比在化合物不存在下统计学上显著更高的分化程度,则所述化合物促进神经干细胞的分化。使用涉及体外培养的干细胞或动物模型的测定,可以鉴定这样的化合物(albranches等人,biotechnol.lett.25:725-30,2003;deng等人,exp.neurol.182:373-82,2003;munoz-elias等人,stem cells 21:437-48,2003;kudo等人,biochem.pharmacol.66:289-95,2003;wan等人,chin.med.j.116:428-31,2003;kawamorita等人,hum.cell 15:178-82,2002;stavridis和smith,biochem.soc.trans.31:45-9,2003;pachemik等人,reprod.nutr.dev.42:317-26,2002;fukunaga等人,出处同上)。所述神经干细胞可以是培养的干细胞、从其来源组织新鲜分离的干细胞、或在其来源生物体内的干细胞。因此,神经干细胞与根据本发明的化合物的接触可以在体外(对于培养的或新鲜分离的干细胞)或在体内(对于在其来源生物体内的干细胞)进行。所得到的分化的神经细胞如果在体外产生,则可以移植到需要它的组织中(lacza等人,出处同上;chu等人,出处同上;fukunaga等人,出处同上)。这样的组织包括遭受创伤或神经变性疾病的脑组织或其它神经组织。
491、以下非限制性实施例示例本发明的化合物、组合物和使用方法。
492、[实施例]
493、在下面通过参考制备实施例、实施例、参考实施例和实验实施例更详细地解释本发明。但是,本发明的范围不限于此。
494、在实施例中,使用bruker avance iii 400、bruker avance iii 400hd和brukeravance neo 40或bruker avance iii 300测量1h nmr。
495、使用gilson-gx-28或waters fractionlynx系统进行制备型hplc(prep-hplc)。使用的制备条件如下。
496、一般制备型hplc条件(acoh):
497、柱:c30-ug 25mmid*150mml,5μm
498、流动相a:含有0.10%v/v乙酸的水
499、流动相b:乙腈
500、紫外检测波长:220nm
501、流速:25ml/min
502、温度:室温
503、梯度时间表:
504、0min b=x%,a=100-x%
505、0.01-10.99min线性梯度
506、11.00min b=y%,a=100-y%
507、11.01-11.20min b=y%,a=100-y%
508、11.21-13.00min b=100%
509、13.01-15.00min b=z%,a=100-z%
510、x、y和z值取决于化合物的种类。
511、一般制备型hplc条件(tfa):
512、柱:l-column2 ods 20mmid*150mml,5μm
513、流动相a:含有0.10%v/v tfa的水
514、流动相b:含有0.10%v/v tfa的乙腈
515、紫外检测波长:220nm
516、流速:20ml/min
517、温度:室温
518、梯度时间表:
519、0min b=x%,a=100-x%
520、0.01-6.99min线性梯度
521、7.00min b=y%,a=100-y%
522、7.01-10.99min b=100%
523、11.00-12.00min b=z%,a=100-z%
524、x、y和z值取决于化合物的种类。
525、使用下述方法a至d进行lcms分析。
526、(方法a)
527、使用agilent 1100 lc&agilent g1956a,(elsd:1260 infinity)测量lcms。在表1或表2中描述的条件下进行分析。
528、[表1]
529、
530、[表2]
531、
532、(方法b)
533、系统:shimadzu uflc/ms系统(shimadzu-2020质谱仪)
534、柱:用于色谱柱的ods柱
535、洗脱剂:a(含有0.04%tfa的水)和b(含有0.04%tfa的乙腈)
536、(方法c)
537、系统:shimadzu uflc/ms系统(shimadzu-2020质谱仪)
538、柱:用于色谱柱的ods柱
539、洗脱剂:a(5mm aconh4/水)和b(5mm aconh4/乙腈)
540、(方法d)
541、系统:water 2795系统
542、柱:develosil c30-ug-5,50x4.6mm,nomura chemical co.,ltd.
543、洗脱剂:a(含有0.1%hcooh的水)和b(含有0.1%hcooh的乙腈)。
544、流速:1.0ml/min
545、制备实施例1:中间体d-10的合成
546、
547、向2,2-二乙氧基乙-1-胺75g(0.67mol)在meoh(1.0l)中的溶液中加入环己烷甲醛89g(0.67mol)。搅拌过夜以后,在0℃向混合物中加入硼氢化钠38.2g(1.0mol),在室温搅拌1.5小时。将混合物浓缩并将残余物溶解在乙酸乙酯(1.0l)中,用水(1.0l)和盐水(1.0l)洗涤,经硫酸钠干燥,过滤并蒸发。通过减压蒸馏(140℃,5-10mmhg)得到目标物质d-10(130g,无色油,收率85%)。
548、d-10的1h nmr(400mhz,cdcl3)数据显示在图1中。
549、根据与上述相同的方法或已知的方法合成中间体d-1、d-2、d-3、d-55、d-67、d-135、d-137、d-157、d-158、d-178、d-179和d-182。
550、制备实施例2:中间体d-13的合成
551、
552、2-1)d-13-int1的合成
553、在室温向n-苄基-2,2-二乙氧基乙-1-胺(200g,0.90mol)和丙烯酰胺(77g,1.08mol)在thf(4.0l)中的溶液中加入sio2(40g)。回流7天后,将混合物过滤并蒸发。通过快速色谱法得到目标物质d-13-int1(194g,黄色液体,收率82%)。
554、得到的化合物的1h nmr(400mhz,cdcl3)数据显示在图2中。
555、2-2)d-13的合成
556、将d-13-int1(90g,0.3mol)和pd(oh)2/c(9g)在meoh中的混合物在h2(50psi)下在室温搅拌3小时。tlc表明反应结束。将反应混合物过滤并将滤液浓缩以提供为黄色油的粗产物d-13,将其直接使用。
557、d-13的1h nmr(400mhz,cdcl3)数据显示在图3中。
558、根据与上述相同的方法或已知的方法合成中间体d-58。
559、制备实施例3:中间体d-8的合成
560、
561、向2-溴-1,1-二乙氧基乙烷(50g,0.69mol)在mecn(0.7l)中的溶液中加入碳酸钾(94.5g,0.69mol)和正丁基胺(50g,0.69mol)。回流过夜后,将混合物过滤并蒸发。将残余物溶解在乙酸乙酯(1.0l)中,用水(0.5l)和盐水(0.5l)洗涤,经硫酸钠干燥,过滤并蒸发。通过减压蒸馏(70℃,5-10mmhg)得到目标物质d-8(71g,无色油,55%收率)。
562、d-8的1h nmr(400mhz,cdcl3)数据显示在图4中。
563、根据与上述相同的方法或已知的方法合成中间体d-32、d-50、d-53、d-73、d-128和d-161。
564、制备实施例4:中间体d-12的合成
565、
566、将2-溴丙烷(300g,2.44mol)、2,2-二乙氧基乙胺(341g,2.56mol)和碳酸钾(674g,4.88mol)在mecn(3.0l)中的溶液在80℃搅拌16小时。将溶液过滤并将滤液浓缩。将粗产物溶解在乙酸乙酯(2.0l)中,用水(1.0l)和盐水(1.0l)洗涤;经无水硫酸钠干燥,然后过滤和蒸发以产生为黄色油的d-12的期望产物(300g,1.71mol,70%收率),将其不经纯化用于下一步。
567、d-12的1h nmr(400mhz,cdcl3)数据显示在图5中。
568、根据与上述相同的方法或已知的方法合成中间体d-28、d-30、d-31、d-33和d-70。
569、制备实施例5:中间体d-82的合成
570、
571、向(2s)-2-氨基己酸叔丁酯(310g,1.66mol)在甲醇(2.50l)中的溶液中加入2,2-二甲氧基乙醛(315.92g,1.82mol,274.72ml,60%纯度),然后加入ch3cooh(2.10g,34.97mmol,2ml),将混合物搅拌16小时。然后在0℃加入nabh3cn(124.82g,1.99mol),将混合物温热至20℃并搅拌2小时。tlc(石油醚∶乙酸乙酯=2∶1)显示大部分的起始材料((2s)-2-氨基己酸叔丁酯)被消耗。将反应混合物在真空下浓缩以产生黄色油。将黄色油通过柱色谱法(sio2,石油醚∶乙酸乙酯=20∶1至5∶1)纯化以提供为浅黄色油的d-82(530g,1.92mol,58%收率)。
572、d-82的1h nmr(400mhz,cdcl3)数据显示在图6中。
573、根据与上述相同的方法或已知的方法合成中间体d-80、d-91、d-94、d-180和d-183。
574、中间体d的列表显示在表3(表3-1和表3-2)中。
575、[表3-1]
576、
577、[表3-2]
578、
579、在表4(表4-1和表4-2)中显示的所有中间体e是商购可得的或根据已知的方法合成。
580、[表4-1]
581、
582、[表4-2]
583、
584、制备实施例6:中间体b-128的合成
585、
586、6-1)b-128-int1的合成
587、在冰浴中向2,2-二乙氧基-n-乙基-乙胺(d-128,11.0g,68.2mmol)、(2s)-2-(9h-芴-9-基甲氧基羰基氨基)丙酸(e-15,21.2g,68.2mmol)和n,n-二异丙基乙胺(17.6g,136mmol,24.0ml)在dcm(200ml)中的搅拌混合物中逐份加入hatu(25.9g,68.2mmol)。在0℃搅拌30分钟以后,将反应混合物在10℃搅拌16小时。tlc(石油醚/乙酸乙酯=3∶1)显示反应结束。将反应混合物用水、盐水洗涤,经无水硫酸钠干燥,过滤并浓缩以产生粗产物,将其通过柱色谱法(sio2,石油醚/乙酸乙酯=10∶1至2∶1)纯化以提供产物b-128-int1(23.0g,50.6mmol,74%收率)。
588、b-128-int1的1h nmr(400mhz,cdcl3)数据显示在图7中。
589、6-2)中间体b-128的合成
590、将b-128-int1(23.0g,50.6mmol)、pd/c(5.00g,10%w/w)在etoac(200ml,含有1%v/v哌啶)中的混合物在50psi在h2下搅拌48小时。将反应混合物过滤并将滤液在减压下浓缩以产生粗产物,将其通过柱色谱法(sio2,ch2cl2∶meoh=1∶0至20∶1)纯化以产生b-128(10.5g,45.3mmol,89%收率)。
591、b-128的1h nmr(400mhz,cdcl3)数据显示在图8中。
592、制备实施例7:中间体b-72的合成
593、
594、以与制备实施例6:6-1)中相同的方式,通过使用d-128和e-69合成b-72-int1。
595、在氮气下向b-72-int1(56.0g,79.6mmol)在etoh(300ml)中的溶液中加入pd/c(6g,10%纯度)。将悬浮液在真空下脱气并用氢气吹扫几次。将混合物在氢气(15psi)下在25℃搅拌72小时。将反应混合物过滤并将滤液在减压下浓缩以产生b-72(35.0g,45.3mmol,57%收率)。
596、b-72的1h nmr(400mhz,cdcl3)数据显示在图9中。
597、中间体b的列表显示在表5(表5-1至表5-15)中。根据制备实施例6、制备实施例7或已知的方法,使用对应的中间体d和中间体e合成中间体b。
598、[表5-1]
599、
600、[表5-2]
601、
602、[表5-3]
603、
604、[表5-4]
605、
606、[表5-5]
607、
608、[表5-6]
609、
610、[表5-7]
611、
612、[表5-8]
613、
614、[表5-9]
615、
616、[表5-10]
617、
618、[表5-11]
619、
620、[表5-12]
621、
622、[表5-13]
623、
624、[表5-14]
625、
626、[表5-15]
627、
628、制备实施例8:中间体a-22的合成
629、
630、8-1)a-22-int2的合成
631、将a-22-int1(400g,3.42mol)放入10-l三颈烧瓶中,并加入0.5mh2so4(5.2l)。将反应冷却至0℃,然后逐滴加入2mol/l nano2(2.6l),加入结束以后,将反应在室温搅拌过夜。该时间以后,将反应混合物用乙酸乙酯(ea)(3x3l)萃取。将合并的ea萃取物经na2so4干燥,过滤并浓缩。将得到的粗制固体从石油醚中重结晶以提供化合物a-22-int2(230g)。
632、a-22-int2的1h nmr(400mhz,cdcl3)数据显示在图10中。
633、8-2)a-22-int3的合成
634、将dic(533g,4.23mol)和cucl(8g,0.08mol)在t-buoh(325.6g,4.4mol)中的溶液在氮气下在室温搅拌5天。将反应用dcm(1l)稀释。在0℃将a-22-int2(200g,1.69mol)逐份加入溶液中。将反应在室温搅拌5小时,然后在硅藻土垫上过滤。将滤液用饱和na2co3水溶液和盐水洗涤,然后经na2so4干燥,浓缩并将残余物通过蒸馏纯化以提供a-22-int3(200g)。
635、a-22-int3的1h nmr(400mhz,cdcl3)数据显示在图11中。
636、8-3)a-22-int4的合成
637、在-20℃至-40℃向a-22-int3(100g,0.57mol)、pph3(194.1g,0.74mol)和化合物n-羟基邻苯二甲酰亚胺(110.8g,0.68mol)在dcm(1l)中的搅拌溶液中加入diad(157.6g,0.74mol)。在相同温度保持40min以后,将反应混合物浓缩并通过快速色谱法(pe∶ea=100∶1-10∶1)直接纯化以提供a-22-int4(73.8g)。
638、a-22-int4的1h nmr(400mhz,cdcl3)数据显示在图12中。
639、8-4)a-22-int5的合成
640、在0℃向a-22-int4(100g,0.31mol)在dcm(500ml)和mecn(100ml)中的搅拌溶液中加入nh2nh2 h2o(39.2g,0.78mol)。加入以后,将混合物温热至室温并在相同温度搅拌3小时,然后过滤。将滤液用饱和na2co3水溶液和盐水洗涤,然后经na2so4干燥,过滤并浓缩以提供a-22-int5(54g)。将粗产物直接使用。
641、a-22-int5的1h nmr(400mhz,cdcl3)数据显示在图13中。
642、8-5)a-22-int6的合成
643、在-10℃给1000ml的3颈烧瓶装入溶解在dcm(200ml)中的1-萘甲醇(31.6g,200mmol)。然后缓慢地逐滴加入diea(35ml),溶液变成淡红色。搅拌5min以后,缓慢地逐份加入三光气(固体,29.6g,0.1mol)以保持温度低于0℃。加入以后,将混合物在该温度搅拌20min,使用tlc监测反应。可以发现起始材料被耗尽。缓慢地逐滴加入在dcm(100ml)中的a-22-int5(32g,0.17mol)以保持温度低于0℃,并将混合物在该温度搅拌20分钟。加入diea直到不再形成烟。然后将混合物在室温搅拌30min。tlc鉴定反应结束。然后将混合物用300ml的dcm稀释,并将有机层用水和盐水洗涤,经na2so4干燥,过滤并浓缩以产生残余物,将其通过快速色谱法(pe∶ea 100∶1-10∶1)纯化以产生a-22-int6(36g)。
644、a-22-int6的1h nmr(400mhz,cdcl3)数据显示在图14中。
645、8-6)中间体a-22的合成
646、将a-22-int6(25g,67mmol)溶解在甲酸(250ml)中。在室温搅拌6小时以后,将混合物浓缩。将残余物通过制备型hplc纯化以提供a-22(13g)。
647、a-22的1h nmr(400mhz,cdcl3)数据显示在图15中。
648、制备实施例9:中间体a-43的合成
649、
650、以与在制备实施例8:8-1)-8-3)中相同的方式合成a-43-int2。
651、在25℃在氮气保护下向a-43-int2(10.0g,21.1mmol)在chcl3(100ml)和乙醇(100ml)中的溶液中加入pd/c(1.20g,10%纯度)。将悬浮液在真空下脱气并用h2吹扫3次,并在15psi在氢气下搅拌8小时。将混合物过滤并将滤液浓缩以得到为黄色油的a-43-int3(43.0g,96.5mmol,91%收率)。
652、a-43-int3的1h nmr(400mhz,cdcl3)数据显示在图16中。
653、以与在制备实施例8:8-4)-8-6)中相同的方式使用a-43-int3合成a-43。
654、a-43的1h nmr(400mhz,dmso)数据显示在图17中。
655、制备实施例10:中间体a-60的合成
656、
657、通过与在制备实施例9中由a-43-int1合成a-43-int2的方法类似的方法,合成a-60-int2。
658、a-60-int2的1h nmr(400mhz,cdcl3)数据显示在图18中。
659、在0℃向a-60-int2(500mg,1.63mmol)和咪唑(222mg,3.26mmol)在二氯甲烷(5ml)中的溶液中加入tbscl(369mg,2.49mmol),并将混合物在20℃搅拌2小时。将反应混合物用二氯甲烷(10ml)稀释,并用水(10ml x 2)洗涤,将有机相浓缩并通过柱色谱法(石油醚/乙酸乙酯=100/1-20/1)纯化以得到为无色油的产物a-60-int3(500mg,1.19mmol,73%)。
660、a-60-int3的1h nmr(400mhz,dmso)数据显示在图19中。
661、以与在制备实施例8:8-4)-8-6)中相同的方式通过使用a-60-int3合成a-60。
662、a-60的1h nmr(400mhz,cdcl3)数据显示在图20中。
663、制备实施例11:中间体a-52的合成
664、
665、11-1)a-52-int2的合成
666、(对于两批)
667、在氮气下在-20℃向a-52-int1(665g,2.18mol)、2-羟基异吲哚啉-1,3-二酮(391g,2.4mol)和三苯基膦(745g,2.84mol)在thf(7.0l)中的溶液中加入偶氮二甲酸二异丙酯(574g,2.84mol,552ml)。然后将混合物温热至20℃并搅拌16小时。tlc(石油醚∶乙酸乙酯=5∶1)显示起始材料(a-52-int1)被完全耗尽。将反应混合物在减压下浓缩以产生残余物,然后将其倒入乙酸乙酯(1.0l)和石油醚(10.0l)的混合物中,将许多白色固体分离出,过滤并将有机层在减压下浓缩以产生残余物,并通过柱色谱法(sio2,石油醚∶乙酸乙酯=50∶1至15∶1)纯化,以产生为白色固体的a-52-int2(1.80kg,83%收率)。
668、a-52-int2的1h nmr(400mhz,dmso)数据显示在图21中。
669、11-2)a-52-int3的合成
670、(对于14批)
671、在0℃向a-52-int2(120g,267mmol)在mecn(720ml)中的溶液中加入氢氟酸(33.4g,801mmol,30.3ml,48%纯度)在h2o中的溶液。然后将混合物在20℃搅拌15分钟。tlc(石油醚∶乙酸乙酯=5∶1)显示起始材料(a-52-int2)被完全耗尽。将反应混合物通过加入饱和nahco3水溶液(1.0l)淬灭,然后用乙酸乙酯(1.0l)萃取。将合并的有机层用盐水(750ml)洗涤,经无水硫酸钠干燥,过滤并在减压下浓缩以产生作为黄色油得到的a-52-int3(1.20kg,3.58mol,96%收率)。
672、a-52-int3的1h nmr(400mhz,cdcl3)数据显示在图22中。
673、11-3)a-52-int4的合成
674、(对于两批)
675、在-20℃历时2小时缓慢地向a-52-int3(600g,1.79mol)和4-4-3b(586g,1.79mol)、pph3(563g,2.15mol)在dcm(8.0l)中的溶液中加入偶氮二甲酸二异丙酯(434g,2.15mol,417ml)。将混合物在20℃搅拌16小时。tlc(石油醚∶乙酸乙酯=3∶1)显示主要斑点是期望的化合物。将反应混合物在减压下浓缩以产生残余物。将残余物与石油醚(4.0l)和乙酸乙酯(4.0l)一起研磨并将许多白色固体分离出,过滤并将有机层在减压下浓缩以产生残余物。将残余物通过柱色谱法(sio2,石油醚∶乙酸乙酯=50∶1至5∶1)纯化以产生粗产物,然后将粗产物溶解在etoh(8.0l)中并搅拌约2小时,沉淀出许多白色固体,过滤以提供为白色固体的a-52-int4(2.0kg,3.10mol,87%收率)。
676、a-52-int4的1h nmr(400mhz,dmso)数据显示在图23中。
677、11-4)a-52-int5的合成
678、(对于3批)
679、在氮气下在20℃向a-52-int4(100g,155mmol)在etoh(400ml)和chcl3(400ml)中的溶液中加入pd/c(5.0g,155mmol,10%纯度)。将悬浮液在真空下脱气并用氢气吹扫几次。将混合物在氢气(45psi)下在40℃搅拌48小时。tlc(石油醚∶乙酸乙酯=2∶1)显示起始材料(a-52-int4)被完全耗尽。将反应混合物过滤并在减压下浓缩以产生残余物。将残余物溶解在thf(1.0l)中并在减压下浓缩以产生为白色固体的a-52-int5(110g,292mmol,63%收率)。
680、a-52-int5的1h nmr(400mhz,dmso)数据显示在图24中。
681、11-5)a-52-int6和a-52的合成
682、(对于5批)
683、向a-52-int5(136g,292mmol)在thf(1.8l)中的溶液中加入碳酸铯(353g,1.08mol)和2,2,4,6,7-五甲基-3h-苯并呋喃-5-磺酰氯(209g,723mmol)。将混合物在45℃搅拌16小时。tlc(石油醚∶乙酸乙酯=1∶1)显示检测到一个新的主要斑点。将反应混合物通过在23℃加入水(2.0l)淬灭,然后用乙酸乙酯(2.0l x 2)萃取。将合并的有机层经无水硫酸钠干燥,过滤并在减压下浓缩以产生残余物。将残余物通过柱色谱法(石油醚∶乙酸乙酯=20∶1至1∶1)纯化以提供为白色固体的a-52-int6(400g,636mmol,44%收率)。
684、a-52-int6的1h nmr(400mhz,dmso)数据显示在图25中。
685、以与在制备实施例8中相同的方式通过使用a-52-int6合成a-52。
686、a-52的1h nmr(400mhz,cdcl3)数据显示在图26中。
687、根据与上述相同的方法或已知的方法通过使用对应的起始材料合成在表6(表6-1至表6-7)中所示的中间体a。
688、[表6-1]
689、
690、[表6-2]
691、
692、[表6-3]
693、
694、[表6-4]
695、
696、[表6-5]
697、
698、[表6-6]
699、
700、[表6-7]
701、
702、在表7中所示的所有中间体c是商购可得的或根据已知的方法合成。
703、[表7]
704、
705、实施例1:i-128的合成
706、
707、向a-36(123mg,0.50mmol,0.50mmol/ml在meoh中)、b-128(0.40mmol,0.40mmol/ml在meoh中,1.0当量)在甲醇(2ml)中的溶液中加入4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉鎓氯化物n-水合物(dmt-mm)(0.45mmol,0.45mmol/ml在meoh中,1.1当量)。将混合物在10℃静置2小时,然后在减压下浓缩。将残余物用二氯甲烷(10ml)稀释,并用饱和碳酸氢钠溶液(5ml)、盐水(5ml)洗涤,经无水硫酸钠干燥,过滤并浓缩。将粗产物溶解在甲酸(3ml)中并在10℃静置2天。将混合物在减压下浓缩并将残余物通过制备型hplc(fa)纯化以产生产物i-128。
708、i-128的1h nmr(400mhz,cdcl3)数据显示在图27中。
709、参考实施例1
710、
711、将化合物ref1-1(4.05g,6.5mmol)溶解在甲酸(30ml)中并将混合物在25℃搅拌1天。将混合物在减压下浓缩并将残余物通过制备型hplc纯化以产生化合物ref1-2。
712、实施例2:i-129的合成
713、
714、以与在实施例1和参考实施例1中相同的方式使用a-129和b-129合成i-129-int1。
715、在25℃向i-129-int1(0.09mmol,0.045mmol/ml在n,n-dmf中,1.0当量)、c-82(0.18mmol,0.09mmol/ml在dmf中,2.0当量)在dmf(2.0ml)中的溶液中加入在dmf(0.5ml)中的1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化物六氟磷酸盐(hatu)(0.14mmol,0.28mmol/ml在dmf中,1.5当量)和在dmf(0.5ml)中的n-乙基-n-异丙基-丙-2-胺(dipea)(0.28mmol,0.56mmol/ml在dmf中,3.0当量)。将混合物在25℃搅拌2小时。将反应混合物过滤以产生滤液,并将滤液通过制备型hplc(fa条件)纯化以产生目标化合物i-129。
716、根据以上方法或已知的方法使用在表8(表8-1至表8-3)中所示的中间体合成化合物i-1至i-140、i-153至i-157、i-161至i-165和i-176至i-180。
717、[表8-1]
718、
719、[表8-2]
720、
721、[表8-3]
722、
723、实施例3:i-141的合成
724、
725、ex3-1)i-141-int1的合成
726、在环境温度将ab-141(86mg)和pd/c(5重量%,33mg)在thf(3ml)中的搅拌混合物暴露于h2(气球压力)。将反应混合物搅拌2小时,然后移去h2。在硅藻土垫上过滤并蒸发滤液,提供为深棕色固体的i-141-int1(70mg)。将粗制的固体不经进一步纯化用在下一反应中。
727、lcms(方法b):m/z=421.4[m+h]+。
728、ex3-2)i-141的合成
729、在环境温度向i-141-int1(70mg)、acoh(60μl)、3-苯基丙醛(i-141-int2,88μl)在dce(4ml)中的溶液中加入nabh(oac)3(140mg)。搅拌1天以后,加入1mol/l氢氧化钠水溶液(30ml)。将有机层分离,用水(10ml)洗涤,经na2so4干燥,在真空中浓缩,并通过制备型hplc(柱:c30-ug-5,mecn/0.1%acoh溶液=20/80-70/30)纯化以产生为白色固体的i-141(21mg)。
730、lcms(方法b):m/z=539.6[m+h]+。
731、实施例4:i-145的合成
732、
733、在环境温度向ab-145(25mg)、acoh(10μl)、喹啉-2-甲醛(7.8mg)在dce(1ml)中的溶液中加入nabh(oac)3(71mg)。搅拌1天以后,加入1mol/l氢氧化钠水溶液(1.0ml)。将有机层分离,经na2so4干燥,在真空中浓缩,并通过制备型hplc(柱:c30-ug-5,mecn/0.1%acoh溶液=10/90-60/40)纯化以产生为浅黄色固体的i-145(5.6mg)。
734、lcms(方法b):m/z=671.4[m+h]+。
735、实施例5:i-147的合成
736、
737、ex5-1)i-147-int1的合成
738、在环境温度向ab-5(0.26g)在thf(5ml)中和na2co3(0.11g)在水(5ml)中的搅拌两相混合物中加入boc2o(0.13g)。搅拌1小时以后,将混合物用etoac(50ml)和饱和nahco3水溶液(20ml)稀释。将有机层分离,经na2so4干燥,在真空中浓缩,并通过色谱法(sio2,正己烷∶acoet=90∶10-20∶80,梯度)纯化以产生为白色无定形物的i-147-int1(0.32g)。
739、lcms(方法b):m/z=545.3[m-tbu+h]+,623.3[m+na]+。
740、ex5-2)i-147-int2的合成
741、在环境温度将i-147-int1(0.32g)和pd/c(5重量%,57mg)在thf(5ml)中的搅拌混合物暴露于h2(气球压力)。将反应混合物搅拌1小时,然后移去h2。在硅藻土垫上过滤并蒸发滤液,提供为白色固体的i-147-int2(0.22g)。将粗制的固体不经进一步纯化用在下一反应中。
742、lcms(方法b):m/z=367.2[m-boc+h]+,411.2[m-tbu+h]+。
743、ex5-3)i-147-int3的合成
744、在环境温度向i-147-int2(80mg)、acoh(10μl)、3-苯基丙醛(i-141-int2,53μl)在dce(2ml)中的溶液中加入nabh(oac)3(0.17g)。搅拌1天以后,加入2mol/l氢氧化钠水溶液(10ml)。将有机层分离,用水(10ml)洗涤,经na2so4干燥,在真空中浓缩,并通过制备型hplc(柱:c30-ug-5,mecn/0.1%acoh溶液=50/50-100/0)纯化以产生i-147-int3(42mg)。
745、lcms(方法d):m/z=529.1[m-tbu+h]+,607.2[m+na]+。
746、ex5-4)i-147的合成
747、向装有i-147-int3(20mg)的烧瓶中加入甲酸(1ml),并将混合物在环境温度静置。4天以后,将混合物在真空中浓缩。将残余物通过制备型hplc(柱:c30-ug-5,mecn/0.1%acoh溶液=30/70-80/20)纯化以产生为白色固体的i-147(13mg)。
748、lcms(方法d):m/z=485.1[m+h]+。
749、实施例6:i-148的合成
750、
751、ex6-1)i-148-int1的合成
752、将ab-148(0.99g)和钯碳(10%重量)(0.31g)在thf(20ml)中的混合物在氢气气氛下在室温搅拌1小时。将混合物通过硅藻土过滤。将滤液在真空中浓缩以产生为深棕色固体的i-148-int1(0.74g)。
753、lcms(方法b):m/z=381.4[m+h]+
754、ex6-2)i-148-int3的合成
755、向i-148-inti(0.15g)、i-148-int2(0.22g)和乙酸(99μl)在1,2--二氯乙烷(7ml)中的溶液中加入三乙酰氧基硼氢化钠(0.25g)。将混合物在室温搅拌16小时。向混合物中加入1mol/l naoh水溶液(20ml)和氯仿(40ml)。将有机层分离,然后用水(20ml)洗涤。将有机层经na2so4干燥并在真空中浓缩。将残余物通过柱色谱法(sio2,acoet∶meoh=80∶20-20∶80,梯度)纯化以产生为无色油的i-148-int3(0.16g)。
756、lcms(方法b):m/z=604.6[m+h]+
757、ex6-3)i-148-int4的合成
758、将i-148-int4(0.16g)和钯碳(10%重量)(56mg)在thf(3ml)中的混合物在氢气气氛下在室温搅拌1小时。将混合物通过硅藻土过滤。将滤液在真空中浓缩以产生为深棕色油的i-148-int4(0.16g)。
759、lcms(方法b):m/z=606.6[m+h]+
760、ex6-4)i-148-int5的合成
761、将i-148-int4(0.14g)和甲酸(2.0ml)的混合物在室温静置1小时。将混合物在真空中浓缩。向残余物中加入氯仿(30ml)和na2co3(3.0g)。将混合物在室温搅拌30分钟。将混合物过滤,并将滤液在真空中浓缩以产生为淡黄色油的i-148-int5(0.17g)。
762、lcms(方法b):m/z=506.5[m+h]+
763、ex6-5)i-148的合成
764、向i-148-int5(22mg)、i-148-int6(11mg)和n-乙基-n-异丙基丙-2-胺(11μl)在1,2-二氯乙烷(2ml)中的混合物中加入hatu(25mg)。在室温搅拌2.5小时以后,向混合物中加入i-148-int6(11mg)、n-乙基-n-异丙基丙-2-胺(11μl)和hatu(25mg)。在室温搅拌1小时以后,向混合物中加入1mol/l hcl水溶液(10ml),然后用氯仿(20ml)萃取。将有机层用nahco3水溶液(10ml)、然后用水(10ml)洗涤。将有机层经na2so4干燥并在真空中浓缩。将残余物通过制备型hplc(柱:c30-ug-5,mecn/0.1%acoh溶液=20/80-70/30)纯化以产生为白色固体的i-148(0.6mg)。
765、lcms(方法b):m/z=714.6[m+h]+
766、实施例7:i-149的合成
767、
768、在室温向i-148-int5(31mg)在1,2-二氯乙烷(2ml)中的溶液中加入对甲苯磺酰氯(12mg)和吡啶(49mg)。在相同温度搅拌17小时以后,加入氯仿(10ml)和水(20ml)。将有机层分离,用盐水(10ml)洗涤,经na2so4干燥,并在真空中浓缩。将残余物通过制备型hplc(条件(acoh):b=20-70%)纯化。将收集的级分合并并在真空中浓缩。将水溶液冷冻干燥以产生为白色固体的i-149(0.5mg)。
769、lcms(方法b):m/z=660.5[m+h]+。
770、实施例8:i-159和i-160的合成
771、
772、向通过冰/水浴冷却的ab-159(0.96g)在thf(20ml)中的溶液中加入bh3·thf(0.9mol/l在thf中,7.5ml)。在0℃搅拌1小时和在室温搅拌2小时以后,逐滴加入meoh(4ml)。将混合物在真空中浓缩并通过柱色谱法(nh sio2,正己烷∶acoet=80∶20-0∶100,梯度)纯化以产生为无色油的i-159(0.17g)和i-160(0.27g)。
773、lcms(i-159,方法d):m/z=489.1[m+h]+
774、lcms(i-160,方法d):m/z=475.2[m+h]+
775、实施例9:i-173的合成
776、
777、在室温向i-148-int1(20mg)在1,2-二氯乙烷(4ml)中的溶液中加入3-苯甲酰基苯甲酸(21mg)、吡啶(67mg)和2-氯-1,3-二甲基-4,5-二氢1h-咪唑-3-鎓六氟磷酸盐(cip,100mg)。在相同温度搅拌4小时以后,加入饱和碳酸氢钠水溶液(50ml)和氯仿(20ml)。将有机层分离,然后用1mol/l hcl(15ml)、饱和碳酸氢钠水溶液(20ml)和盐水(10ml)洗涤,经na2so4干燥,并在真空中浓缩。将残余物通过制备型hplc(条件(acoh):b=10-60%)纯化。将收集的级分合并并在真空中浓缩。将水溶液冷冻干燥以产生为白色固体的i-173(10mg)。
778、lcms(方法b):m/z=589.4[m+h]+。
779、实施例10:i-182的合成
780、
781、ex10-1)i-182-int1的合成
782、将ab-182(2.0g)和钯碳(10%重量)(0.51g)在thf(20ml)中的混合物在氢气气氛下在室温搅拌100分钟。将混合物通过硅藻土过滤。将滤液在真空中浓缩以产生为淡黄绿色固体的i-182-int1(1.5g)。
783、lcms(方法b):m/z=368.2[m+h]+
784、ex10-2)i-182的合成
785、向i-182-int1(0.10g)和吡啶(88μl)在1,2-二氯乙烷(3ml)中的混合物中加入i-148-int2(0.16g)。在室温搅拌2小时和在60℃搅拌3天以后,将混合物倒入饱和碳酸氢钠水溶液中,然后用氯仿萃取。将有机层用nahco3水溶液(10ml)、然后用水(10ml)洗涤。将有机相经mgso4干燥并在真空中浓缩以产生粗产物(0.12g),将其通过制备型hplc纯化以产生为白色固体的i-182(20mg)。
786、lcms(方法b):m/z=522.2[m+h]+
787、i-182的1h nmr(300mhz,cdcl3)数据显示在图28中。
788、根据与实施例3(制备方法7)类似的方法或已知的方法使用在表9中所示的中间体ab和试剂合成化合物i-141至i-143。
789、根据与实施例4类似的方法或已知的方法使用在表9中所示的中间体ab和试剂合成化合物i-144至i-146。
790、根据与实施例7类似的方法或已知的方法使用在表9中所示的中间体ab和试剂合成化合物i-149至i-152。
791、根据与实施例8(制备方法8)类似的方法或已知的方法使用在表9中所示的中间体ab合成化合物i-158至i-160。
792、根据与实施例9(制备方法5)类似的方法或已知的方法使用在表9中所示的中间体ab和试剂合成化合物i-166至i-175。
793、根据与实施例10(制备方法6)类似的方法或已知的方法使用在表9中所示的中间体ab和试剂合成化合物i-181至i-182。
794、[表9]
795、 化合物编号 中间体ab 试剂 程序 i-141 ab-141 i-141-int2 实施例3 i-142 ab-142 i-141-int2 实施例3 i-143 ab-143 i-141-int2 实施例3 i-144 ab-145 i-144-int1 实施例4 i-145 ab-145 i-145-int1 实施例4 i-146 ab-145 i-146-int1 实施例4 i-147 ab-147 i-141-int2 实施例5 i-148 ab-148 i-148-int6 实施例6 i-149 ab-148 i-149-int1 实施例7 i-150 ab-148 i-150-int1 实施例7 i-151 ab-148 i-151-int1 实施例7 i-152 ab-148 i-152-int1 实施例7 i-158 ab-158 实施例8 i-159 ab-159 实施例8 i-160 ab-159 实施例8 i-166 ab-159 i-166-int1 实施例9 i-167 ab-159 i-167-int1 实施例9 i-168 ab-159 i-168-int1 实施例9 i-169 ab-159 i-169-int1 实施例9 i-170 ab-159 i-170-int1 实施例9 i-171 ab-148 i-171-int1 实施例9 i-172 ab-148 i-172-int1 实施例9 i-173 ab-148 i-173-int2 实施例9 i-174 ab-148 i-174-int1 实施例9 i-175 ab-148 i-175-int1 实施例9 i-181 ab-182 i-151-int1 实施例10 i-182 ab-182 i-182-int2 实施例10
796、中间体ab的化学结构显示在表10(表10-1至表10-2)中。根据在实施例1中的方法或已知的方法,通过使用在表10中列出的对应的中间体a和b合成中间体ab。
797、[表10-1]
798、
799、[表10-2]
800、
801、中间体a和b的化学结构分别显示在表6和5中。在表9中列出的试剂的化学结构显示在表11中。
802、[表11]
803、
804、化合物i-1至i-183的化合物名称和分子量的测量结果显示在表12(表12-1至表12-28)中。
805、[表12-1]
806、
807、[表12-2]
808、
809、[表12-3]
810、
811、[表12-4]
812、
813、[表12-5]
814、
815、[表12-6]
816、
817、[表12-7]
818、
819、[表12-8]
820、
821、[表12-9]
822、
823、[表12-10]
824、
825、[表12-11]
826、
827、[表12-12]
828、
829、[表12-13]
830、
831、[表12-14]
832、
833、[表12-15]
834、
835、[表12-16]
836、
837、[表12-17]
838、
839、[表12-18]
840、
841、[表12-19]
842、
843、[表12-20]
844、
845、[表12-21]
846、
847、[表12-22]
848、
849、[表12-23]
850、
851、[表12-24]
852、
853、[表12-25]
854、
855、[表12-26]
856、
857、[表12-27]
858、
859、[表12-28]
860、
861、实验实施例:notch测定
862、我们使用了cellsensor t-rextm nicd csl-bla hela细胞系,该细胞系通过hela细胞的慢病毒转导用驱动β-内酰胺酶报道基因表达的notch应答元件(csl-bla)以及dox(多西环素)可诱导的nicd(notch细胞内结构域)构建体工程改造。dox向这些细胞的添加使得受调节的nicd转录因子表达和随后的β-内酰胺酶表达。
863、具体来说,使用了以下方案。
864、notch测定方案(方法2)
865、1.用echo将40nl/孔的工作浓度的1000x化合物添加至384-孔测定板。
866、2.将细胞铺板:将35μl/孔的hela/t-rextm nicd csl-bla细胞以103个细胞/孔完全培养基加入384-孔平板中。
867、3.将5μl在测定培养基中的8x多西环素加入处理过的孔中,并将5μl测定培养基加入未处理的且无细胞的对照孔中。
868、4.将测定板在增湿37℃/5%co2培养箱中温育16-20小时。
869、5.根据手册制备6x liveblazertm-fret b/g底物(ccf4-am)混合物,并且应当在没有直接强光的情况下进行细胞加载。
870、6.从增湿37℃/5%co2培养箱取出测定板。将8μl来自步骤5的6x底物混合物加入每个孔中。覆盖平板以防止光照和蒸发。在室温温育4小时。
871、7.使用以下滤光片选择读出测定板:
872、
873、8.数据分析:利用测定板布局来识别无细胞孔的位置。这些对照孔用于背景扣除。确定无细胞孔在460nm(平均蓝色背景)和530nm(平均绿色背景)的平均发射。从所有蓝色发射数据中减去平均蓝色背景(在460nm收集的数据)。从所有绿色发射数据中减去平均绿色背景(在530nm收集的数据)。通过将减去背景的蓝色发射值除以减去背景的绿色发射值,计算每个孔的蓝色/绿色发射比率。
874、代替步骤1至步骤3,还可以进行以下步骤a至步骤d。后续步骤同方法2,在步骤4之后(方法1)。
875、a.将细胞铺板:将32μl/孔的hela/t-rextm nicd csl-bla细胞以103个细胞/孔完全培养基加入384-孔平板中。
876、b.在测定培养基中制备10x化合物。
877、c.将4μl化合物或在测定培养基中的1%dmso加入细胞中。
878、d.将4μl在测定培养基中的10x多西环素加入处理过的孔中,并将4μl测定培养基加入未处理的且无细胞的对照孔中。
879、结果显示在表13(表13-1至表13-2)中。
880、[表13-1]
881、
882、
883、[表13-2]
884、
885、
886、[工业适用性]
887、本发明的化合物抑制notch信号转导,并因此可以用于治疗涉及notch信号转导的疾病。
888、尽管以上仅详细描述了本发明的一些示例性实施方案,但是本领域技术人员将容易认识到,在不实质上背离本发明的新颖教导和优点的情况下,在示例性实施方案中的许多修改是可能的。因此,所有这样的修改都意图被包括在本发明的范围内。
889、本技术是基于在美国提交的美国临时专利申请号63/090,185(提交日期:2020年10月10日),其内容完整并入本文。
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!