一种基于还原敏感聚合物递送阳离子铂药的纳米粒的制备方法
13061,doi:10.1021/ja405475y(2013).
9.3 park,g.y.,wilson,j.j.,song,y.&lippard,s.j.phenanthriplatin,a monofunctional dna-binding platinum anticancer drug candidate with unusual potency and cellular activity profile.proc natl acad sci u s a 109,11987-11992,doi:10.1073/pnas.1207670109(2012).
10.4 chen,h.et al.delivery of cationic platinum prodrugs via reduction sensitive polymer for improved chemotherapy.small 17,e2101804,doi:10.1002/smll.202101804(2021).
技术实现要素:
11.本发明设计并合成了phenanthriplatin即phenii,同时还开发出具有gsh响应能力的负电荷聚合物poly poly-2-hd-co-hpmda,并通过共价结合将phenii键合在poly poly-2-hd-co-hpmda高分子的支链上,形成表面带负电的纳米粒子(np-phenii),可以很好的改善菲啶铂的毒性并提高其疗效。
12.为实现上述目的,本发明采用了以下技术方案。
13.(1)聚合物poly-2-hd-co-hpmda的合成
14.将2-羟乙基二硫化物(2-hydroxyethyl disulfide,2-hd)和1,2,4,5-环己烷四甲酸二酐(1,2,4,5-cyclohexanetetracarboxylic dianhydride,hpmda)置于圆底烧瓶中,然后将dmf加入到烧瓶中连续搅拌48小时;随后,为了将聚合物封端24小时,加入mpeg,通过透析并真空干燥得到负电荷聚合物(poly-2-hd-co-hpmda);
15.2-羟乙基二硫化物与1,2,4,5-环己烷四甲酸二酐的摩尔比优选为1:1,mpeg优选为mpeg
2k
,2-羟乙基二硫化物与mpeg的摩尔比为5:1。
16.(2)phenanthriplatin即phenii的合成
17.将顺铂(cisplatin)、agno3分散在超干n,n-二甲基甲酰胺(dmf)中,55℃避光搅拌16h后,溶液由深黄色变为浅灰色混浊液体;过滤后,将菲啶(phenanthridine)溶解在滤液中,55℃避光搅拌16h后,旋蒸除去dmf,加入甲醇溶解,过滤除去沉淀,加无水乙醚使固体沉降收集;固体用甲醇和乙醚洗涤,最后干燥收集得到固体粉末;
18.顺铂(cisplatin)、agno3、菲啶(phenanthridine)的摩尔比为1:0.9:0.9。
19.(3)poly-2-hd-co-hpmda-phenii的合成
20.将步骤(2)phenii、agno3溶解在超干dmf中,55℃避光搅拌16h后,溶液由深黄色变为浅灰色混浊液体,过滤后,将步骤(1)poly-2-hd-co-hpmda溶解在滤液中,在55℃下在黑暗中搅拌16小时后,通过透析去除dmf,冷冻干燥;
21.phenii、agno3、poly-2-hd-co-hpmda的摩尔比为1:1:3.4。
22.(4)表面带负电的纳米粒子np-phenii的制备
23.将poly-2-hd-co-hpmda-phenii溶于dmf中并逐滴加入蒸馏水中,在室温下搅拌10分钟,通过透析去除dmf,通过离心分离收集上清液即得到np-phenii。
24.本发明的优点:
25.1本方案采用双(2-羟乙基)二硫化物与1,2,4,5-环己烷四甲酸二酐共聚合成对gsh(谷胱甘肽)敏感的聚合物,该聚合物生物安全性良好,可降解。
26.2本方案采用上述聚合物与带正电菲啶铂药共价结合形成poly-2-hd-co-hpmda-phenii,可降低菲啶铂的毒性,增强其靶向性以及有效性。
附图说明
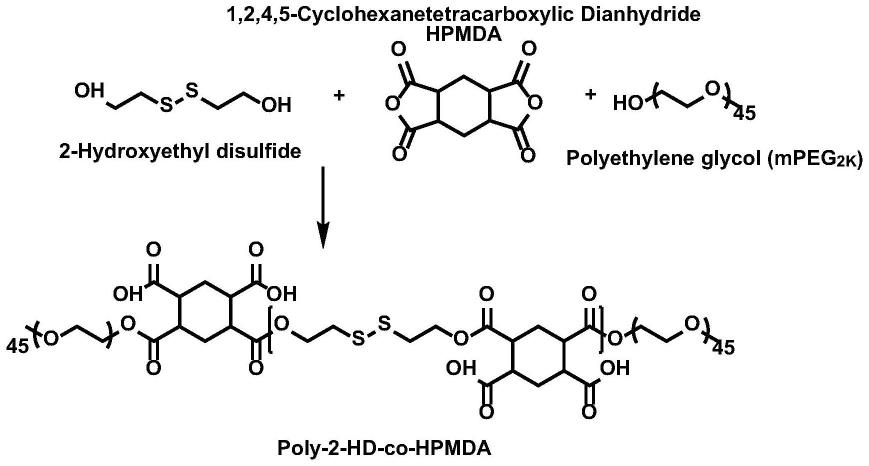
27.图1、为高分子(poly-2-hd-co-hpmda)的合成
28.图2.phenanthriplatin(phenii)的合成
29.图3.poly-2-hd-co-hpmda-phenii的合成
30.图4.poly(2-hd-co-hpmda)-peg在d
6-dmso中的核磁氢谱
31.图5.phenii在d
6-dmso中的核磁氢谱
32.图6.poly-2-hd-co-hpmda-phenii在d
6-dmso中的核磁氢谱
33.图7.np-phenii的制备和表征
34.图8.激光共聚焦用于可视化a549ddp细胞对荧光纳米粒的內吞过程。红色荧光来自纳米粒包裹的cyanine5.5 nhs ester,蓝色荧光来自dapi染色的细胞核,绿色荧光来自f-action染色的细胞膜
35.图9.cisplatin,phenii以及np-phenii与不同细胞系作用48h时细胞存活率曲线
36.图10.cisplatin,phenii以及np-phenii与a549ddp细胞系作用24h时细胞凋亡图(a)和凋亡统计(b)
37.图11.np-phenii的体内分布
38.图12.np-phenii的抑瘤效果。
具体实施方式
39.下面结合实施例对本发明做进一步说明,但本发明并不限于以下实施例。
40.实施例1
41.1.1高分子(poly-2-hd-co-hpmda)的合成
42.将2-羟乙基二硫化物(2-hydroxyethyl disulfide,2-hd,0.1mm,)和1,2,4,5-环己烷四甲酸二酐(1,2,4,5-cyclohexanetetracarboxylic dianhydride,hpmda)(0.11mm,246.6mg)置于50ml圆底烧瓶中,然后将10ml dmf加入到烧瓶连续搅拌48小时。随后,为了将聚合物封端24小时,加入mpeg
2k
(0.02mmol,400mg)。通过透析并真空干燥得到负电荷聚合物(poly-2-hd-co-hpmda),干燥产物用1h nmr分析(图4)。
43.1.2 phenanthriplatin(phenii)的合成
44.将顺铂(cisplatin,300mg,1mm)、agno3(153mg,0.9mm)分散在30毫升超干n,n-二甲基甲酰胺(dmf)中。55℃避光搅拌16h后,溶液由深黄色变为浅灰色混浊液体。过滤后,将菲啶(phenanthridine,153mg,0.9mmol)溶解在滤液中。55℃避光搅拌16h后,旋蒸除去dmf,加入30ml甲醇溶解,过滤除去沉淀,加无水乙醚使固体沉降收集。固体用甲醇和乙醚洗涤3次,最后干燥收集得到固体粉末,干燥产物用1h nmr分析(图5)。
45.1.3 poly-2-hd-co-hpmda-phenii的合成
46.将phenii(505.0mg,1.0mmol)、agno3(170mg,1.0mmol)溶解在10ml的超干dmf中。55℃避光搅拌16h后,溶液由深黄色变为浅灰色混浊液体。过滤后,将poly(2-hd-co-hpmda)-peg(2500mg)溶解在滤液中。在55℃下在黑暗中搅拌16小时后,通过透析去除dmf
(分子截止量为3500)。冷冻干燥后,干燥的产品通过1h nmr进行分析(图6)。
47.1.4 np-phenii的制备和表征
48.将poly-2-hd-co-hpmda-phenii(30mg)溶于1ml dmf中并逐滴加入10ml蒸馏水中,在室温下搅拌10分钟。通过透析去除dmf(分子截流量为3500),通过离心分离(3000rpm.,5min)收集上清液(np-phenii)。np-phenii的形态通过tem(ht-7700,hitachi,japan)表征。np-phenii的尺寸由malvern zetasizer nano zs90激光粒度分析仪(nano zs,uk)表征。通过电感耦合等离子体质谱法(inductively coupled plasma mass spectrometry,icp-ms)定量测定纳米粒子中pt的浓度。
49.1.5 np-phenii的体外细胞摄取
50.将poly-2-hd-co-hpmda-phenii(30mg/ml)和cyanine5.5 nhs ester(1mg)溶解在1ml dmf中,并在室温下搅拌10分钟。通过透析去除dmf(分子截止mw=3500)。通过离心分离(5000rpm.,5min)收集上清液(np@cyanine5.5 nhs ester)。
51.通过clsm和流式细胞术分析细胞内np@cyanine5.5 nhs ester检测。对于clsm观察,将a549ddp细胞以每孔3
×
104个细胞的密度接种到24孔分室载玻片(thermo scientific,usa)中,并与补充有10%fbs(1ml)的rpmi1640在37℃下孵育12小时.去除培养基后,将细胞用等价的cyanine5.5 nhs ester浓度(10μg/ml)的np@cyanine5.5 nhs ester处理0.5小时、3小时和6小时,然后去除培养基,将细胞与fitc鬼笔环肽一起孵育根据制造商的协议。随后,将细胞用dapi染色,然后用激光共聚焦显微镜(olympus fv1000-ix81,olympus,japan)观察。
52.1.6 np-phenii对各种癌细胞的细胞活力
53.利用mtt测定来检查np-phenii对癌细胞(bel-7404、a549、bel-7404ddp、a549ddp)的活力。将细胞以每孔5,000个细胞的密度接种在96孔板(thermo scientific,美国)中并培养12小时。细胞分别与终浓度为0.005、0.05、0.5、5、10、20、40μm pt的cisplatin、phenii、np-phenii孵育48小时。然后,在孔中加入用rpmi1640(100μl)稀释的10%mtt。37℃培养4h后,每孔加入10%sds(100μl),37℃培养12h。通过酶标仪(spectramax)在570nm(峰值吸光度)和650nm(背景吸光度)下测试孔的吸光度。细胞活力表示为测试孔和对照孔的吸光度的比率。
54.1.7 np-phenii对a549ddp细胞的细胞凋亡
55.将a549ddp细胞以每孔2
×
105个细胞的密度接种在12孔板(thermo scientific,美国)中并培养12小时。细胞与cisplatin、phenii、np-phenii一起孵育24小时,最终浓度为10μm的pt。按照制造商的说明收集细胞并通过膜联蛋白v-fitc/pi细胞凋亡试剂盒染色。样品最终通过流式细胞术(becton dickinson and company,usa)进行分析。
56.1.8体内fl成像和生物分布分析:
57.将poly-2-hd-co-hpmda-phenii(30mg/ml)和cyanine7.5 nhs ester(1mg)溶解在1ml dmf中,并在室温下搅拌10分钟。通过透析去除dmf(分子截止mw=3500)。通过离心分离(5000rpm.,5min)收集上清液(np@cyanine7.5 nhs ester)。
58.llc细胞(1
×
106)皮下注射到雌性c57小鼠的右臀部。当肿瘤体积达到约200mm3时,对小鼠进行静脉注射。注入np@cyanine7.5 nhs ester。注射后,在ivis光谱成像系统(spectrum ct,perkinelmer,ex/em=740nm/800nm)上记录1、4、8、10、12、24小时的fl信号。
对于生物分布研究,注射后24小时后处死小鼠,收获肿瘤和正常器官并成像。
59.1.9 llc实体瘤的建立和治疗效果
60.将llc细胞(1
×
106)皮下注射到雌性c57小鼠的右侧。小鼠静脉注射。当肿瘤大小达到100mm3时,分别以3.5mg pt kg-1
的剂量注射pbs、顺铂、phenii和np-phenii。每隔一天记录一次肿瘤体积。
61.2.实验结果与讨论
62.2.1 np-phenii的制备和表征
63.我们首先合成了phenanthriplatin(phenii),如图2所示,随后通过1h nmr对其进行表征(图4)。其次,合成了具有二硫键的还原敏感聚合物poly(2-hd-co-hpmda)-peg,并通过1h nmr对其进行了表征(图5)。当全身给药时,带正电荷的phenii将被免疫系统细胞识别或可能发生非特异性结合,并会迅速清除,导致显着的脱靶毒性。此后,poly-2-hd-co-hpmda链段上的羧酸与phenii共价形成聚合物poly-2-hd-co-hpmda-phenii,poly-2-hd-co-hpmda-phenii通过1h nmr表征(图6)。poly-2-hd-co-hpmda和poly-2-hd-co-hpmda-phenii本质上是两亲性的,因此可以分别自组装成纳米颗粒(np、np-phenii)(图7中a)。通过动态光散射(dls)(图7c),np-phenii的平均直径为63.24nm,这与tem结果非常一致(平均直径=~40nm,图7中b)。np和np-phenii的zeta电位为-22.6
±
1.769mv和-5.67
±
0.44mv(图7中d),这表明np-phenii屏蔽了phenii的正电荷。具有二硫键的poly-2-hd-co-hpmda-phenii在gsh存在下很容易降解,以验证np-phenii在gsh存在下是否可以裂解并释放phenii。通过电子显微镜可以观察到np-phenii在gsh的孵育下降解成小碎片(图7中e),dls的结果也表明np-phenii的粒径在gsh的孵育下发生了显着变化(图7中f)。这表明np-phenii在gsh存在下被裂解。纳米粒子的解离必然伴随着药物的释放。研究表明,当np-phenii的条件为ph7.4时,24小时后pt的释放量仅为33%左右。但在10mmgsh的存在下,24小时后pt的释放量达到约86%(图7中g)。综上所述,上述结果表明,poly-2-hd-co-hpmda-phenii不仅可以自组装成稳定的纳米颗粒,而且可以在gsh存在下快速降解和释放药物。
64.2.2细胞内吞实验
65.clsm可以将纳米粒的內吞过程可视化,采用染料cyanine5.5 nhs ester标记纳米粒,显示红光,用dapi染细胞核,显示蓝光,用f-action染细胞质,显示绿光,如图8所示。红色荧光显示在细胞质中,表明纳米粒确实能被细胞內吞,先绿色荧光分布在红色周围,红色荧光分布蓝色荧光四周,且没有重叠,表明纳米粒不会进入细胞核,并且二价铂是在细胞质从被释放,然后进入细胞核发挥作用。从1-7h,我们观察到红色荧光强度逐渐加强,说明纳米粒的內吞具有时间依赖性,內吞作用随着作用时间的延长而加强。
66.2.3细胞毒性实验
67.采用mtt法测定cisplatin,phenii以及np-phenii对bel7404和bel7404/ddp,a549和a549/ddp两对亲本株和顺铂耐药株的细胞毒性,药物作用时间为48h,实验结果如图9所示。药物浓度增大,其毒性会增强,并且对于以上两对细胞系,细胞毒性:phenii》np-phenii》cisplatin。结果可以说明纳米粒降低了phenii的毒性,但是显著克服了cisplatin耐药。
68.2.4细胞凋亡实验
69.探究cisplatin,phenii以及np-phenii对细胞凋亡产生的影响,我们采用annexin v/fitc与pi双染的方法,利用流式细胞术检测药物处理相同时间后细胞凋亡的情况。如图
10显示,q2-ul:pi阳性,annexin v阴性,为细胞坏死;q2-ur:pi和annexin v双阳性,为细胞晚期凋亡;q2-lr:pi阴性,annexin v阳性,为细胞早期凋亡;q2-ll:pi和annexin v双阴性,为正常细胞。可以看出,对照组细胞大多处在左下区域,即大多为正常细胞,经过不同药物处理后,坏死、早期凋亡、晚期凋亡的细胞明显增加。在所有的处理手段中,np-phenii效果仅次于phenii。图10中b更加直观反映出,np-phenii处理过后的细胞,凋亡比例是是高于顺铂的。这说明np-phenii的效果比游离cisplatin的效果要好,显著克服了cisplatin耐药。
70.2.5 np-phenii的体内分布
71.见图11.
72.2.6 np-phenii的抗肿瘤效果
73.最后,在患有llc肺肿瘤的小鼠身上评估了np-phenii的抗癌活性。结果显示,与顺铂和np-phenii相比,np-phenii显着抑制肿瘤生长(图12中b)。顺铂(3.5mg pt kg-1
)治疗小鼠肿瘤生长抑制率仅为49.18%。然而,np-phenii处理的小鼠的肿瘤抑制率为80.51%。结果显示,np-phenii组肿瘤重量为0.49
±
0.3g,明显小于顺铂组(1.31
±
0.16g),这说明np-phenii具有优良的抗癌作用。
74.与传统的phenanthriplatin相比较可以发现,设计出来的poly-2-hd-co-hpmda-phenii可通过gsh触发释放铂药,而且可以增长phenanthriplatin的血液循环,增强phenanthriplatin的肿瘤靶向性,其中水分子很容易脱离,从而可以与dna碱基一个位点发生配位。开发出具有降低响应能力的负电荷聚合物poly(2-hd-co-hpmda)-peg,以封装带正电荷的phenpt(ii),通过静电相互作用形成中性电荷纳米粒子(phenpt(ii)nps),可以很好的改善毒性和提高疗效,更好的抑制dna复制过程,使之发生凋亡。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1