2-氰基非那烯酮类化合物在制备治疗耐药肿瘤的药物中的应用
1.本发明属于医药化学技术领域,具体涉及2-氰基非那烯酮类化合物在制备治疗抗顺 铂、阿霉素等化疗药和帕纳提尼、他莫昔芬、维纳托克等靶向抗癌药耐药肿瘤的药物中的 应用。
背景技术:
2.利用细胞毒剂类药物进行的化疗和针对特定致癌靶点的靶向药物治疗是目前肿瘤治 疗的主要药物治疗手段。但是,无论化疗和靶向药物治疗都面临继发耐药的难题,肿瘤最 终在应激调控下对多种不同分子机制的抗癌药产生交叉耐药,进入几乎“无药可用”的终 末期。除了转运蛋白p-gp的药物泵出机制,肿瘤细胞往往通过应激诱导的肿瘤基因突变 发展出耐药的细胞株。例如,kras突变与接受帕尼单抗治疗的结肠癌患者的复发和耐药 密切相关;p53突变与多种肿瘤对化疗产生的交叉耐药性正相关;egfr-c797s突变是导 致第三代egfr-tkis耐药的最常见的继发突变。但是,以基因突变为靶点的逆转耐药的 策略同样面临挑战,肿瘤基因突变具有高频性,在靶向药物攻击下极易发生新的突变。另 外,在基因非突变依赖的耐药肿瘤中,细胞通过旁路激活机制逃避靶向初始标志物的抗癌 药,例如bcr-abl非突变依赖的tkis耐药,无法通过升级换代tkis解决。因此,目前 亟需寻找对多种不同机制的抗癌药耐药的肿瘤细胞中具有一定共性的靶标和治疗药物,实 现“广谱逆转耐药”。
3.hsp70蛋白作为分子伴侣蛋白,在不同细胞环境和压力因素下通过招募不同的分子伴 侣和辅助伴侣蛋白发生构象改变,结合并调控多种客户蛋白,以分子机器的形式和机制维 持蛋白质组的稳定。hsp70被发现在多种肿瘤中高表达,尤其是在肿瘤基因突变和抗癌药 等“环境压力”的胁迫下,hsp70在化疗和靶向抗癌药治疗的过程中应激性上调,因此被 认为与多种癌症以及多种抗癌药的耐药性相关。
4.近年来,凋亡的关键调控因子bcl-2家族蛋白与hsp70的相互作用开始被发现。其中, bcl-2家族中的bim被发现是hsp70的辅助伴侣蛋白,结合于hsp70蛋白nbd区的别构 位点,抑制hsp70的atp酶活性,影响其sbd区(底物结合区)的构象和客户蛋白的折 叠。尤其是,在肿瘤基因突变和抗癌药的胁迫下,hsp70和bim都能够通过细胞应激加强 它们之间的ppi,重塑hsp70的分子伴侣机器的运行机制,通过结合和稳定某些特定的抗 凋亡客户蛋白,形成多蛋白复合物,发挥促进肿瘤细胞生存的作用。
技术实现要素:
5.鉴于此,本发明旨在提供2-氰基非那烯酮类化合物在制备治疗耐药肿瘤的药物中的应 用,所述的2-氰基非那烯酮类化合物的结构如通式i所示:
[0006][0007]
其中:
[0008]
r1选自取代或未取代的c
1-8
烷基、c
2-8
烯基、c
2-8
炔基、c
3-8
环烷基、c
3-8
环烯基,所 述的取代选自下述基团:c
1-3
烷基、c
2-3
烯基、c
2-3
炔基、苯基、呋喃基、噻吩基、吡啶基、 萘基、oh、i、br、cl、f、no2、nhch3、n(ch3)2、cn、cf3;
[0009]
r2选自c
1-8
烷基、取代的c
1-8
烷基或xr3;
[0010]
所述取代的c
1-8
烷基是由下述基团任意取代的c
1-8
烷基:oh、och3、i、br、cl、 no2、nh2、nhch3、n(ch3)2、ch(och3)2、cho、cn、cooh、cooch3、cooc2h5、 吗啉基、硫吗啉基或哌嗪基;
[0011]
所述的x选自(ch2)m、(ch2)mconh(ch2)n或m、n为1-6的整数;
[0012]
所述r3选自取代或未取代的苯基、萘基、苯并呋喃基、噻吩基或吲哚基,所述取代 选自下述基团:c
1-4
烷基、c
2-4
烯基、c
2-4
炔基、苯基、oh、i、br、cl、no2、cooh、 so3h、coor4、conhr4、so3r4、so2nhr4、or4或nr4r5,其中,r4和r5分别选自h、 c
1-4
烷基、c
2-4
烯基、c
2-4
炔基。
[0013]
进一步的,所述的r1是环己烷基。
[0014]
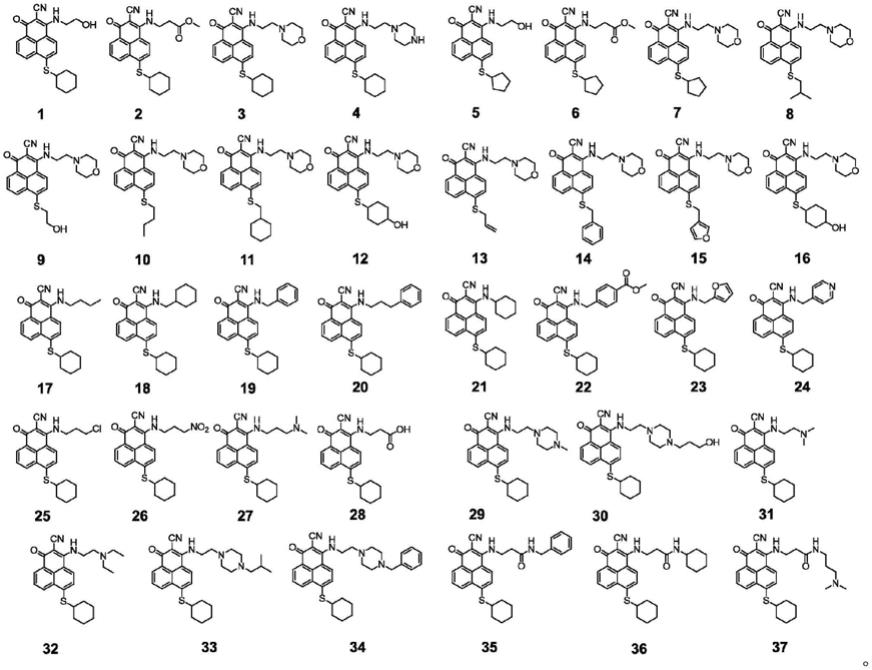
进一步的,所述的2-氰基非那烯酮类化合物选自:
[0015][0016]
进一步的,所述的药物包括所述的2-氰基非那烯酮类化合物中的一种或二种以上化合 物。
[0017]
进一步的,所述的药物包含9-700mg的所述的2-氰基非那烯酮类化合物。
[0018]
进一步的,所述的药物的剂型包括片剂、锭剂、滴剂、注射制剂、颗粒剂、霜剂、软 膏剂、栓剂、凝胶剂或胶囊制剂。
[0019]
进一步的,所述的耐药肿瘤为化疗药和/或靶向抗癌药耐药的肿瘤。
[0020]
进一步的,化疗药包括顺铂(ddp)、阿霉素(adriamycin)、紫杉醇(paclitaxel)、 阿糖胞苷(cytarabine)、依托泊苷(etoposide),靶向抗癌药包括帕纳替尼(ponatinib)、索拉菲 尼(sorafenib)、奥希替尼(osimertinib)、他莫昔芬(tamoxifen)、维纳托克(venetoclax)。
[0021]
进一步的,所述的耐药肿瘤包括第3代bcr-abl激酶抑制剂帕纳替尼(ponatinib)耐 药的慢性粒细胞白血病、顺铂(ddp)耐药的慢性粒细胞白血病、bcl-2靶向药维纳托克 (venetoclax)耐药的b细胞淋巴瘤和急性淋巴瘤白血病、依托泊苷(etoposide)耐药的非霍 奇金淋巴瘤和急性淋巴白血病、他莫昔芬(tamoxifen)耐药的乳腺癌、阿霉素(adriamycin) 耐药的乳腺癌、第3代egfr激酶抑制剂奥希替尼(osimertinib)耐药的肺癌、紫杉醇 (paclitaxel)耐药的肺癌、多靶点激酶抑制剂索拉菲尼(sorafenib)耐药的肝癌、顺铂(ddp) 耐药的肝癌、阿糖胞苷(cytarabine)耐药的急性髓性白血病。
[0022]
进一步的,所述的耐药肿瘤的细胞系包括第3代bcr-abl激酶抑制剂帕纳替尼 (ponatinib)耐药的慢性粒细胞白血病细胞系k562/pr、bv173/pr,顺铂(ddp)耐药的慢 性粒细胞白血病细胞系k562/ddp、bv173/ddp,bcl-2靶向药维纳托克(venetoclax)耐 药的b细胞淋巴瘤细胞系、急性淋巴瘤白血病细胞系ri-1/vr、rs4;11/vr,依托泊苷 (etoposide)
耐药的nhl和all细胞系ri-1/er、rs4;11/er;他莫昔芬(tamoxifen)耐药的 乳腺癌细胞系mcf-7/tmr;阿霉素(adriamycin)耐药的乳腺癌细胞系mcf-7/adr、 sk-br3/adr;第3代egfr激酶抑制剂奥希替尼(osimertinib)耐药的肺癌细胞系 hcc827/or、h1975/or;紫杉醇(paclitaxel)耐药的肺癌细胞系hcc827/pr、h1975/cr, 多靶点激酶抑制剂索拉菲尼(sorafenib)耐药的肝癌细胞系hnhuh7/sr,顺铂(ddp)耐药 的肝癌细胞系sk-hep1/ddp;阿糖胞苷(cytarabine)耐药的急性髓性白血病细胞系 u937/cr、thp-1/cr、molm13/cr、shi-1/cr。
附图说明
[0023]
图1.利用免疫共沉淀实验检测细胞中hsp70/bim二聚体的水平,其中,(a)免疫沉 淀复合物经hsp70抗体显色后的曝光条带照片;(b)耐药肿瘤细胞、原代肿瘤细胞系和 正常细胞中hsp70/bim免疫沉淀复合物里hsp70的含量占hsp70总含量的百分比的对比。
[0024]
图2.k562/pr细胞转染hsp70和bim干扰rna后hsp70和bim蛋白表达水平相比 野生型k562/pr细胞的变化情况。
[0025]
图3.小鼠急性毒性实验中三组小鼠平均体重变化趋势。
[0026]
图4.化合物在荷瘤小鼠模型体内抑制化疗药和靶向抗癌药耐药肿瘤细胞生长活性实 验中腹腔注射给药结束后实验组和对照组的小鼠体重和瘤组织重量的对比。
具体实施方式
[0027]
本发明以上所述及的所有技术方案中,使用的术语“烷基/烯基/炔基”包括直链烷基 和支链烷基。如提及单个烷基如“丙基”,则只特指直链烷基,如提及单个支链烷基如“异 丙基”,则只特指支链烷基。又如“c
1-4
烷基”包括、甲基、乙基、正丙基、异丙基和叔 丁基。类似的规则也适用于本说明书中使用的其它基团。
[0028]
下述非限制性实施例可以使本领域的普通技术人员更全面地理解本发明,但不以任何 方式限制本发明。下述实施例中,如无特殊说明,所使用的实验方法均为常规方法,所用 原料和试剂等均可从化学或生物试剂公司购买或从已公开的方法制备。
[0029]
本发明实施例中使用的化合物结构如下所示:
[0030][0031]
上述化合物的具体合成过程参考中国发明专利2-氰基非那烯酮类化合物及其在白血 病治疗中的应用(申请号:202110164854.3)。
[0032]
实施例1:通过荧光偏振分析法检测本发明的化合物在体外解离hsp70/bim二聚体的能力
[0033]
合成一个带有21个氨基酸的bimbh3肽段(氨基酸:79-99: qediirniarhlaqvgdsmdr),并在n端标记上6-羧基荧光素琥珀酰亚胺酯(fam) 作为荧光标签(fam-bim)。竞争结合实验中所用的反应体系为gst-hsp70蛋白(300nm), 和fam-bim多肽(20nm)溶于反应缓冲液中(100mm k3po4,ph 7.5;100μg/ml牛γ 白蛋白;0.02%叠氮化钠)。在96孔板中,每孔加入100μl反应体系,然后加入1μl不 同浓度的溶于dmso的待检测化合物的母液(0-10mm),终浓度为0-100μm。同时设 立两个对照组,一个对照组为反应体系中只含有hsp70和fam-bim(相当于0%抑制率), 另一对照组中的反应体系只含有fam-bim肽段。96孔板经过1个小时的避光孵育后,于 酶标仪上检测。荧光极化值(mp)在由485nm波长激发产生的发射波长530nm下测量。 ki值通过wang等人报道的计算方程得到。计算ki的程序可以通过以下网址免费获得: http://sw16.im.med.umich.edu/software/calc ki/。
[0034]
按照上述相同的试验方法检测化合物1-37解离hsp70/bim二聚体的能力,以已知 hsp70抑制剂mkt-077、4-无取代和4-硫吗啉取代的非那烯化合物为对照。结果发现本发 明的化合物1-37都能有效解离hsp70/bim二聚体,它们与hsp70蛋白的竞争结合常数(ki) 均是μm级,其中优选技术方案的化合物(1-4、29-34)与hsp70蛋白的竞争解离常数小 于1.0μm,属于比较强的竞争性解离化合物,说明本发明的化合物确实有较强的与hsp70 蛋白竞争结合bim的能力。4-无取代和4-硫吗啉取代的非那烯化合物的竞争解离常数(ki) 大于30μm,即没有明显的竞争性解离效果,说明本发明中的化合物对于hsp70/bim二聚 体的竞争性
解离依赖于化合物4-烷基巯基取代基。具体结果如表1所示。
[0035]
表1.本发明的化合物解离hsp70/bim二聚体的能力实验结果
[0036][0037]
实施例2:构建不同的耐药细胞系
[0038]
根据ccle数据库收集的22种肿瘤类型约1000个肿瘤细胞系的mrna表达数据, 我们主要选择乳腺癌、肺癌、白血病、肝癌等肿瘤细胞系,建立多种不同抗癌药耐药的肿 瘤细胞系。
[0039]
采用药物浓度梯度递增法,建立不同机制的靶向药、化疗药耐药的肿瘤细胞系,包括 第3代bcr-abl激酶抑制剂帕纳替尼(ponatinib)耐药的慢性粒细胞白血病(cml)细胞 系k562/pr、bv173/pr;顺铂(ddp)耐药的cml细胞系k562/ddp、bv173/ddp;bcl-2 靶向药venetoclax耐药的b细胞淋巴瘤(nhl)细胞系和急性淋巴瘤白血病(all)细胞 系ri-1/vr、rs4;11/vr;依托泊苷(etoposide)耐药的nhl和all细胞系ri-1/er、 rs4;11/er;他莫昔芬(tamoxifen)耐药的乳腺癌细胞系mcf-7/tmr;阿霉素(adriamycin) 耐药的乳腺癌细胞系mcf-7/adr、sk-br3/adr;第3代egfr激酶抑制剂奥希替尼 (osimertinib)耐药的肺癌细胞系hcc827/or、h1975/or;紫杉醇(paclitaxel)耐药的肺癌 细胞系hcc827/pr、h1975/cr;多靶点激酶抑制剂索拉菲尼(sorafenib)耐药的肝癌细胞系 hnhuh7/sr;顺铂耐药的肝癌细胞系sk-hep1/ddp;阿糖胞苷(cytarabine)耐药的急性髓 性白血病(aml)细胞系u937/cr、thp-1/cr、molm13/cr、shi-1/cr。细胞库中还 包括相应的未经诱导耐药的原代肿瘤细胞系k562、bv173、ri-1、rs4;11、mcf-7、sk-br3、 hcc827、h1975、hnhuh7、sk-hep1、u937、thp-1、molm13、shi-1,以及正常细胞 系mef,baf3,mcf10a,hek-293t等。
[0040]
建立耐药的肿瘤细胞系的实验过程如下:在低耐药阶段,每次增加浓度为上一个浓度 的1.5倍,在中等及高耐药阶段,每次增加浓度为上一个浓度的1.25倍,每到一个新的浓 度点,均冻存已经稳定诱导的抗性细胞,分别命名r1,r2,r3等,直至诱导的耐药的细胞 ic
50
值为敏感细胞的ic
50
值的30倍或者更高。耐药肿瘤细胞系在进行后续的细胞生物学 实验前,pbs洗去药物,在不含有药物的培养基中培养、传代三次。
[0041]
实施例3:通过流式细胞技术检测本发明的化合物诱导肿瘤治疗药物耐药细胞系的凋亡情 况
[0042]
细胞凋亡是细胞的基本特征之一,它在机体的胚胎发育、组织修复、内环境的稳定
等 方面起着十分重要的作用。在正常细胞中,磷脂酰丝氨酸(ps)只分布在细胞膜脂质双层 的内侧,而在细胞凋亡早期,细胞膜中的磷脂酰丝氨酸(ps)由脂膜内侧翻向外侧。膜联 蛋白
ⅴ
是一种分子量为35-36kd的ca依赖性磷脂结合蛋白,能与细胞凋亡过程中翻转到 膜外的ps高亲和力特异性结合。用标记了fitc的膜联蛋白
ⅴ
作为荧光探针,利用流式 细胞仪或荧光显微镜可检测细胞凋亡的发生。而pi(碘化丙啶)是一种dna染料,可在 535nm左右的紫外光激发,在615nm处发出红色荧光。因此带有膜联蛋白v-fitc的细胞 是发生了凋亡的细胞,而染上pi的细胞即为总的细胞量,通过统计不同的细胞数目,从 而可以计算出发生凋亡的细胞比例。
[0043]
本实验通过annexin-v/propidium iodide staining by flow cytometry试剂盒(碧云天, 苏州,中国c1063)检测本发明化合物1-4、29-34(一系列不同浓度)用于实施例2中构 建的不同机制的抗癌药耐药的肿瘤细胞系、未经诱导耐药的原代肿瘤细胞系和正常细胞 系,24h后细胞凋亡情况。
[0044]
主要的实验步骤如下:
[0045]
1.细胞收集:上述化合物处理24小时后的悬浮细胞直接收集到10ml的离心管中, 每样本细胞数为5
×
106/ml,1000r/min离心5min,弃去培养液;
[0046]
2.用孵育缓冲液洗涤1次,500~1000r/min离心5min;
[0047]
3.用100μl的标记溶液(annexin-v/pi)重悬细胞,室温下避光孵育10~15min;
[0048]
4.500~1000r/min离心5min沉淀细胞,孵育缓冲液洗1次;
[0049]
5.加入荧光(sa-flous)溶液4℃下孵育20min,避光并不时振动,通过流式细 胞仪,检测化合物诱导细胞的凋亡情况。以未加入检测化合物的作为对照组。
[0050]
流式细胞仪分析:流式细胞仪激发光波长用488nm,用一波长为515nm的通带滤器 检测fitc荧光,另一波长大于560nm的滤器检测pi。
[0051]
结果判断:在双变量流式细胞仪的散点图上,左下象限显示活细胞,为(fitc-/pi-); 右上象限是非活细胞,即坏死细胞,为(fitc+/pi+);而右下象限为凋亡细胞,显现 (fitc+/pi-)。据此结果统计凋亡细胞占总细胞数的百分比,然后以log
10
(化合物浓度) 为横轴,凋亡细胞所占百分比为纵轴拟合凋亡曲线,利用曲线计算当50%细胞凋亡时化合 物浓度,即凋亡诱导半数起效浓度(ec
50
)。具体结果如表2所示。
[0052]
表2.本发明化合物凋亡诱导半数起效浓度(ec
50
,μm)
[0053]
[0054][0055]
结果显示,本发明的化合物对于多种不同机理靶向药、化疗药耐药的肿瘤细胞系,都 能够高效的诱导肿瘤细胞凋亡(ec
50
<5μm),其诱导靶向药、化疗药耐药的肿瘤细胞系 凋亡的活性显著高于化合物诱导相对应的未经导耐药的原代肿瘤细胞系凋亡的活性(除慢 性粒细胞白血病细胞系k562和bv173以外ec
50
》15μm,且k562和bv173中ec
50
值 大于相应经抗癌药诱导耐药的细胞系k562/pr、bv173/pr、k562/ddp和bv173/ddp的 5倍以上),而对正常血液、组织细胞系等未表现出明显的凋亡诱导活性(ec
50
>20μm), 说明本发明的化合物对多种不同类型抗癌药耐药的肿瘤细胞均能有效抑制和杀伤,即具有
ꢀ“
广谱逆转抗癌药耐药”的功能。同时,此类化合物对耐药肿瘤细胞的抑制和杀伤具有较 好的选择性和安全性(相对于正常细胞)。4-无取代和4-硫吗啉取代的非那烯化合物对于 上述抗癌药耐药的肿瘤细胞系,未表现出高效诱导肿瘤细胞凋亡活性(ec
50
>25μm), 说明本发明的化合物对慢性粒细胞白血病细胞的抑制和杀伤依赖于化合物4-烷基巯基取 代基。
[0056]
实施例4:细胞中hsp70/bim二聚体的水平与本发明的化合物的关系
[0057]
首先检测实施例2中构建的不同机制的抗癌药耐药的肿瘤细胞系、未经诱导耐药的原 代肿瘤细胞系和正常细胞系中hsp70/bim二聚体的水平。以k562/pr为例,正常培养细 胞,达到106/ml后,离心收集细胞。在2%chaps裂解缓冲液中4℃裂解10分钟,考马 斯亮蓝
粒24小时后,分别加入0-20μm代表性化合物3、31、32、34作用24小时,流式细胞仪 检测细胞凋亡,计算凋亡诱导半数起效浓度(ec
50
)。流式细胞仪的操作方法如实施例3 所述,实验结果如表3所示。
[0064]
表3.本发明化合物对转染hsp70和bim干扰质粒后的化疗药和靶向抗癌药耐药细胞 的凋亡诱导半数起效浓度(ec
50
,μm)
[0065][0066][0067]
实验结果显示,hsp70和bim分别缺失的第3代bcr-abl激酶抑制剂帕纳替尼 (ponatinib)耐药的慢性粒细胞白血病(cml)细胞系k562/pr、bcl-2靶向药venetoclax 耐药的b细胞淋巴瘤(nhl)细胞系ri-1/vr、他莫昔芬(tamoxifen)耐药的乳腺癌细胞系 mcf-7/tmr、阿霉素(adriamycin)耐药的乳腺癌细胞系sk-br3/adr、第3代egfr激酶 抑制剂奥希替尼(osimertinib)耐药的肺癌细胞系hcc827/or、紫杉醇(paclitaxel)耐药的 肺癌细胞
系hcc827/pr、顺铂耐药的肝癌细胞系sk-hep1/ddp、阿糖胞苷(cytarabine)耐 药的急性髓性白血病(aml)细胞系u937/cr中,化合物3、31、32、34诱导凋亡的能 力相比野生型实验组均被阻碍。上述结果表明:本发明的化合物诱导化疗药和靶向抗癌药 耐药的肿瘤细胞凋亡依赖hsp70和bim两种蛋白,即化合物诱导细胞凋亡依赖hsp70/bim 二聚体的存在。
[0068]
实施例6:本发明化合物的安全性能
[0069]
通过小鼠急性毒性试验考察本发明化合物的安全性能,本实验以最具代表性的化合物 31为例,说明实验过程。
[0070]
早晨9:00选取6只雄性balb/c小鼠(体重在28-29g范围内)随机分为3组,分别称 取体重,并计算平均值,当晚9点禁食,不禁水。
[0071]
配制化合物31药物,分为3个剂量组,a组(给药终浓度3mg/kg)、b组(给药终浓 度5mg/kg)和对照组c组(50%dmso(溶剂))按体重腹腔注射药物,至实验终浓度。c 组给予同等量dmso溶液,各组加药条件如表4所示。
[0072]
表4.小鼠急性毒性试验中各组小鼠体重和加药剂量
[0073][0074]
第二天早晨9:30注射药物完毕,并称取各组小鼠的体重,然后每天早晨9:30分别称 量各组小鼠的体重并观察小鼠的状态,实验进行7天。
[0075]
实验结果显示,给药后a,b,c组小鼠均出现状态萎靡,约1小时后均正常进食, 实验过程中a、b、c组6只小鼠生活状态良好,皮毛齐整,眼睛红亮,无不良反应,无 死亡,进食进水正常,体重有明显增加。小鼠每日体重变化数据如图3。
[0076]
将上述称量完体重后的小鼠脱臼处死,解剖观察并取肝组织进行下一步实验。
[0077]
解剖观察:对6只小鼠进行解剖,观察内脏的特点,发现加药组(a、b组)和对照 组(c组)的小鼠,没有明显区别;肾脏、心脏的颜色正常,鲜红,无毒理表现;肝脏为 正常颜色,形状正常,无畸变,没有发现毒理症状。如表5所示,三组小鼠肝脏平均重量 无明显差别,肝脏重量与小鼠体重成正相关。a、b组小鼠肝脏组织石蜡包埋切片,he 染色未见炎症反应。
[0078]
表5.腹腔注射后第7天解剖6只小鼠的肝脏重量和体重
[0079][0080]
小鼠急性毒性试验结论:一次性注射高达5mg/kg的化合物31对小鼠无明显毒副作用。 解剖实验进一步证明,化合物31对小鼠的内脏没有毒理效应;体重监测,可以看出化合 物31对小鼠的体重有没有明显的影响。
[0081]
化合物1-4,29-30,32-34均使用相同方法测定小鼠急性毒性,结果显示化合物1-4, 29-30,32-34对小鼠的内脏均没有毒理效应,且对小鼠的体重没有明显影响。
[0082]
实施例7.化合物在荷瘤小鼠模型体内抑制化疗药和靶向抗癌药耐药细胞细胞生长活性
[0083]
根据急性毒性测试结果,随机选取3组6周龄裸鼠(每组4只),皮下移植第3代 bcr-abl激酶抑制剂帕纳替尼(ponatinib)耐药的慢性粒细胞白血病(cml)细胞系 k562/pr细胞,一组作为对照,另两组每天分别注射0.3mg/kg化合物31或32。具体实 验内容如表6所示。
[0084]
表6.化合物对小鼠的体内抑制慢性粒细胞白血病活性的实验内容
[0085][0086]
小鼠试验结论:如图4所示,从本试验的数据看出,本发明的化合物31和32在5mg/kg 的剂量以下对小鼠没有明显毒副作用,以0.3mg/kg的剂量给移植人第3代bcr-abl激酶 抑制剂帕纳替尼(ponatinib)耐药的慢性粒细胞白血病(cml)细胞系k562/pr的裸鼠连续 给药14天,发现用药组的小鼠的肿瘤块大小明显小于对照组,肿瘤抑制率达到50%(按瘤 重计算),而且相对于对照组体重没有明显变化。
[0087]
化合物31和32均使用相同方法测定在小鼠模型体内抑制bcl-2靶向药venetoclax耐 药的b细胞淋巴瘤(nhl)细胞系ri-1/vr、他莫昔芬(tamoxifen)耐药的乳腺癌细胞系 mcf-7/tmr、阿霉素(adriamycin)耐药的乳腺癌细胞系sk-br3/adr、第3代egfr激酶 抑制剂奥希替尼(osimertinib)耐药的肺癌细胞系hcc827/or、紫杉醇(paclitaxel)耐药的 肺癌细胞系hcc827/pr、顺铂耐药的肝癌细胞系sk-hep1/ddp、阿糖胞苷(cytarabine)耐 药的急性髓性白血病(aml)细胞系u937/cr的肿瘤生长活性,结果显示化合物31和32在上述所有模型中的肿瘤抑制率均在50%以上(按瘤重计算,如图4)。
[0088]
上述结果表明:本发明中的顺铂、阿霉素等化疗药和帕纳提尼、他莫昔芬、维纳托克 等靶向抗癌药耐药的肿瘤细胞的生长,且无明显毒副作用,可以有效用于化疗药和靶向抗 癌药耐药肿瘤的预防和治疗。
[0089]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管 参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依
然 可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行 等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方 案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1