一种GSDMD抑制剂在动脉粥样硬化中的应用
一种gsdmd抑制剂在动脉粥样硬化中的应用
技术领域
1.本发明涉及一种gsdmd抑制剂在动脉粥样硬化中的应用,属于生物医药技术 领域。
背景技术:
2.动脉粥样硬化是一种慢性免疫、炎症性疾病,动脉粥样硬化斑块中数量最多 的三种细胞是巨噬细胞、内皮细胞与平滑肌细胞,斑块进展过程中伴随着这三类 细胞的不断更替。研究发现程序性细胞死亡影响了斑块局部细胞的更新,在动脉 粥样硬化进展中发挥了重要作用。最近研究发现细胞焦亡作为一种程序性细胞死 亡方式,与细胞凋亡不同,细胞焦亡是一种促炎性细胞死亡,其在动脉粥样硬化 与脓毒症疾病发生发展过程中发挥了重要作用,而gsdmd(gasdermin d)是介导 细胞焦亡的关键分子。细胞焦亡发生过程中,活化的半胱天冬酶-1(caspase-1) 或半胱天冬酶-4/5/11(caspase-4/5/11),将gsdmd剪切成gsdmd的n末端 产物(gsdmd-n),而gsdmd-n多聚体在细胞膜上形成孔道,不仅介导高迁移率 族蛋白b1(hmgb1)、白介素1-β(il-1β)、白介素18(il-18)等炎症因子的 释放,也最终导致了伴随细胞膜胀裂和焦亡标志物乳酸脱氢酶(ldh)释放的细 胞焦亡。既往研究发现全身敲除apoe-/-小鼠caspase-1可以改善血管炎症,抑 制动脉粥样硬化的进展。
[0003][0004]
细胞焦亡是以细胞肿胀、细胞膜裂解,伴随着hmgb1、il-1β与il-18等 炎症因子和ldh释放为主要特征的促炎性细胞死亡,也是一种重要的宿主抗胞 内病原体感染的天然免疫防御机制。当细胞受到细菌与病毒等外源性病原相关分 子模式刺激时,细胞浆中感受分子(nlrp1、nlrp2、nlrp3、nlrc4、aim2等模 式识别受体)、接头蛋白(凋亡相关斑点样蛋白(apoptosis associatedspeck-like proteincontaining a card,asc))和效应分子(caspase-1)组 成炎症小体,活化caspase-1/gsdmd,介导细胞焦亡,并释放hmgb1、il-1β与 il-18炎症因子和ldh。全身敲除小鼠gsdmd可以显著提高lps诱导的脓毒血 症小鼠的存活率,并降低小鼠体内炎症水平。所以,细胞焦亡在动脉粥样硬化与 脓毒症疾病发生发展过程中发挥了重要作用,而gsdmd是介导细胞焦亡的关键分 子;本技术领域亟需解决是否可以利用针对gsdmd的多肽抑制剂作为动脉粥样硬 化与脓毒血症防治的潜在药物。
技术实现要素:
[0005]
本发明的目的是为解决利用针对gsdmd的多肽抑制剂作为防治动脉粥样 硬化与脓毒血症的潜在药物的技术问题。
[0006]
为达到解决上述问题的目的,本发明所采取的技术方案是提供一种gsdmd抑 制剂;z-llsd-fmk,其化学结构如式(i)所示;和z-fltd-fmk,分子式c
35h47
fn4o9, 分子量686.76;
[0007][0008]
式(i),分子式c
31h47
fn4o9,分子量638.72。
[0009]
优选地,所述gsdmd抑制剂竞争性抑制含半胱氨酸的天冬氨酸蛋白水解酶 caspase1、caspase4/5/11对于gsdmd的剪切作用。
[0010]
本发明提供一种gsdmd抑制剂在制备防治动脉粥样硬化制剂中的应用。
[0011]
优选地,所述gsdmd抑制剂设为多肽抑制剂。
[0012]
优选地,所述gsdmd多肽抑制剂设为四肽抑制剂。
[0013]
本发明一种gsdmd抑制剂在制备防治脓毒血症制剂中的应用。
[0014]
优选地,所述gsdmd抑制剂设为多肽抑制剂。
[0015]
优选地,所述gsdmd多肽抑制剂设为四肽抑制剂。
[0016]
相比现有技术,本发明具有如下有益效果:
[0017]
本发明提出的gsdmd抑制剂是根据gsdmd被剪切位点的n端四个氨基酸合成 的多肽抑制剂,该抑制剂将与caspase1和caspase4/5/11结合,竞争性抑制这 些酶对gsdmd的剪切作用,降低gsdmd介导的细胞焦亡,从而可在体内抑制细胞 焦亡并用于防治动脉粥样硬化与脓毒血症。
附图说明
[0018]
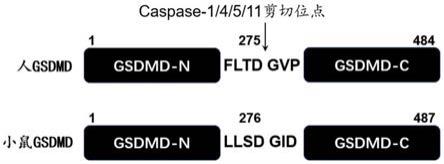
图1为gsdmd作为caspase酶底物的剪切位点原理图;
[0019]
图2为小鼠源性多肽抑制剂z-llsd-fmk化学结构;
[0020]
图3为各周龄apoe-/-小鼠血管中血管组织caspase-1、gsdmd与β-actin的 western blot图。图中随着周龄增大,caspase-1与gsdmd活化水平上升。
[0021]
图4为caspase-1抑制剂与gsdmd抑制剂对apoe-/-小鼠动脉粥样硬化的影响 图。其中a图为主动脉根部横切面he染色图;与对照组相比,caspase-1抑制 剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂组均显著降低了斑块 面积,且各抑制剂组之间斑块面积无明显差异;
[0022]
b图为主动脉根部动脉粥样硬化斑块面积统计图;横坐标代表各个实验组, 纵坐标代表平均病变面积mm2(mean lesion area);与对照组相比,caspase-1 抑制剂组、gsdmd
抑制剂组与caspase-1抑制剂加gsdmd抑制剂组均显著降低了 斑块面积,且各抑制剂组之间斑块面积无明显差异;图中**表示与对照组相比, p《0.01。
[0023]
c图为血清甘油三酯水平统计图;横坐标代表各个实验组,纵坐标代表甘油 三酯水平mmol/l(triglycerides);与对照组相比,caspase-1抑制剂组、gsdmd 抑制剂组与caspase-1抑制剂加gsdmd抑制剂组,各组之间血脂水平无显著差异。
[0024]
d图为血清总胆固醇水平统计图;横坐标代表各个实验组,纵坐标代表血清 总胆固醇水平mmol/l(total cholesterol);与对照组相比,caspase-1抑制 剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂组,各组之间血清总 胆固醇水平无显著差异。
[0025]
e图为血清非高密度脂蛋白胆固醇水平统计图;横坐标代表各个实验组,纵 坐标代表血清非高密度脂蛋白胆固醇水平mmol/l(non-hdl cholesterol);与 对照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd 抑制剂组,各组之间血清非高密度脂蛋白胆固醇水平无显著差异。
[0026]
f图为血清高密度脂蛋白胆固醇水平统计图;横坐标代表各个实验组,纵坐 标代表血清高密度脂蛋白胆固醇水平mmol/l(hdl cholesterol);与对照组相 比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂 组,各组之间血清高密度脂蛋白胆固醇水平无显著差异。
[0027]
图5为caspase-1抑制剂与gsdmd抑制剂对apoe-/-小鼠血管炎症的影响图。 其中a图为主动脉根部动脉粥样硬化斑块内巨噬细胞免疫荧光染色图,红色为 f4/80(巨噬细胞标志物)阳性染色;与对照组相比,caspase-1抑制剂组、gsdmd 抑制剂组与caspase-1抑制剂加gsdmd抑制剂组均显著降低了斑块内巨噬细胞浸 润面积。
[0028]
b图为主动脉根部动脉粥样硬化斑块内巨噬细胞浸润面积统计图;横坐标代 表各个实验组,纵坐标代表巨噬细胞浸润面积mm2(f4/80area);与对照组相 比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂 组均显著降低了斑块内巨噬细胞浸润面积,且各抑制剂组之间浸润面积无明显差 异;图中**表示与对照组相比,p《0.01。
[0029]
c图为血管组织vcam-1、mcp-1与β-actin的western blot图;从图中 得出:与对照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制 剂加gsdmd抑制剂组vcam-1、mcp-1蛋白表达水平降低。
[0030]
d图为血管组织vcam-1表达统计图;横坐标代表各个实验组,纵坐标代表 vcam-1/β-actin蛋白表达水平比值(vcam-1/β-actin fold change);与对 照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd 抑制剂组均显著降低,且各抑制剂组之间无明显差异;图中**表示与对照组相比, p《0.01。
[0031]
e图为血管组织mcp-1表达统计图。横坐标代表各个实验组,纵坐标代表 mcp-1/β-actin蛋白表达水平比值(mcp-1/β-actin fold change);与对照 组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑 制剂组均显著降低,且各抑制剂组之间无明显差异;图中**表示与对照组相比, p《0.01;*表示与对照组相比,p《0.05。
[0032]
图6为caspase-1抑制剂与gsdmd抑制剂对apoe-/-小鼠血管中 caspase-1/gsdmd通路活化水平的影响图。
[0033]
其中a图为血管组织nlrp3、caspase-1、gsdmd、il-1β、hmgb1与β-actin 的western blot图;从图中得出:与对照组相比,caspase-1抑制剂组、gsdmd 抑制剂组与caspase-1抑
制剂加gsdmd抑制剂组均显著降低了血管nlrp3、il-1 β、hmgb1蛋白表达水平以及caspase-1与gsdmd活动水平。
[0034]
b图为血管组织nlrp3表达统计图;横坐标代表各个实验组,纵坐标代表 nlrp3/β-actin蛋白表达水平比值(nlrp3/β-actin fold change);与对照 组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑 制剂组,均显著降低,且各抑制剂组之间无明显差异;图中**表示与对照组相比, p《0.01。
[0035]
c图为血管组织hmgb1表达统计图。横坐标代表各个实验组,纵坐标代表 hmgb1/β-actin蛋白表达水平比值(hmgb1/β-actin fold change);与对照 组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑 制剂组,均显著降低,且各抑制剂组之间无明显差异;图中**表示与对照组相比, p《0.01。
[0036]
图7为caspase-1抑制剂与gsdmd抑制剂对脓毒血症小鼠存活和炎症水平的 影响。
[0037]
其中a图为小鼠存活率统计图;横坐标代表生存时间(小时),纵坐标代表 存活率(survial,%);图中四根曲线分别代表对照组、caspase-1抑制剂组、gsdmd 抑制剂组与caspase-1抑制剂加gsdmd抑制剂组。图中**表示与对照组相比, p《0.01;*表示与对照组相比,p《0.05。
[0038]
b图为血浆ldh水平统计图;横坐标代表各个实验组,纵坐标代表血浆ldh 水平u/l(plasma levels of ldh,u/l);与对照组相比,caspase-1抑制剂组、 gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂组均显著降低,且各抑制剂 组之间无明显差异;图中**表示与对照组相比,p《0.01;*表示与对照组相比, p《0.05。
[0039]
c图为血浆hmgb1水平统计图;横坐标代表各个实验组,纵坐标代表血浆 hmgb1水平ng/ml(plasma levels of hmgb1,ng/ml);与对照组相比,caspase-1 抑制剂组、gsdmd抑制剂组与caspase-1抑制剂加gsdmd抑制剂组均显著降低, 且各抑制剂组之间无明显差异;图中**表示与对照组相比,p《0.01;*表示与对 照组相比,p《0.05。
[0040]
图8为caspase-1抑制剂与gsdmd抑制剂对脓毒血症小鼠脾脏中 caspase-1/gsdmd通路活化水平的影响。图中显示血管组织caspase-1、gsdmd 与β-actin的western blot图。与对照组相比,caspase-1抑制剂组、gsdmd 抑制剂组与caspase-1抑制剂加gsdmd抑制剂组caspase-1、gsdmd活化水平均 显著降低。
具体实施方式
[0041]
为使本发明更明显易懂,兹以优选实施例,并配合附图作详细说明如下:
[0042]
本发明提供一种gsdmd抑制剂;z-llsd-fmk,其化学结构如式(i)所示; 和z-fltd-fmk,分子式c
35h47
fn4o9,分子量686.76;
[0043][0044]
式(i),分子式c
31h47
fn4o9,分子量638.72。
[0045]
gsdmd抑制剂竞争性抑制含半胱氨酸的天冬氨酸蛋白水解酶caspase1、 caspase4/5/11对于gsdmd的剪切作用。
[0046]
本发明提供的一种gsdmd抑制剂在制备防治动脉粥样硬化制剂中的应用。 gsdmd抑制剂设为多肽抑制剂,设为四肽抑制剂。
[0047]
本发明提供的一种gsdmd抑制剂在制备防治脓毒血症制剂中的应用。 gsdmd抑制剂设为多肽抑制剂,设为四肽抑制剂。
[0048]
gsdmd多肽抑制剂:根据gsdmd肽链中caspase1和caspase4/5/11的剪 切位点-dg氨基酸位点(人d275g276,小鼠d276g277),如附图1:设计的 gsdmd多肽抑制剂为4肽(小鼠源性llsd),并通过多肽修饰增强该抑制剂 的细胞通透性。小鼠源性多肽抑制剂为z-llsd-fmk(分子式c
31h47
fn4o9,分子 量638.72,)。此外,与之对应的人源性多肽抑制剂为z-fltd-fmk(分子式 c
35h47
fn4o9,分子量686.76)。
[0049]
实施例1
[0050]
gsdmd多肽抑制剂对动脉粥样硬化的防治作用:
[0051]
1.采用5周龄apoe-/-小鼠予以高脂饲料(21%脂肪,0.15%胆固醇)喂养, 分别在6、8、11、14、18周龄取材,进行western blot方法检测了血管中caspase-1 与gsdmd活化水平;结果发现随着动脉粥样硬化的进展,血管组织中caspase-1 与gsdmd活化水平明显增加(如附图3),这提示caspase-1/gsdmd通路活 化水平可能在动脉粥样硬化进程中发挥了重要作用。
[0052]
2.采用5周龄apoe-/-小鼠予以高脂饲料喂养9周后,分别予以对照组以对照 溶剂;caspase-1抑制剂组以z-yvad-fmk(caspase-1抑制剂,腹腔注射,200 微克/天);gsdmd抑制剂组以z-llsd-fmk(gsdmd抑制剂,腹腔注射, 200微克/天)或caspase-1抑制剂加gsdmd抑制剂组以 z-yvad-fmk+z-llsd-fmk(腹腔注射,各200微克/天);干预4周后,采用 he染色检测了apoe-/-小鼠主动脉根部动脉粥样硬化斑块面积;结果发现,与对 照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂+gsdmd 抑制剂组均显著降低了斑块面积,且各抑制剂组之间斑块面积无明显差异,而各 组之间血脂水平无显著差异(如图4)。这表明caspase-1/gsdmd在动脉粥样 硬化中发挥了重要作用,且gsdmd抑制剂可在体通过非降脂
作用抑制动脉粥样 硬化进展。
[0053]
3.检测apoe-/-小鼠血管炎症水平;结果发现,与对照组相比,caspase-1抑 制剂组、gsdmd抑制剂组与caspase-1抑制剂+gsdmd抑制剂组均显著降低了 斑块内巨噬细胞浸润面积,且降低了血管中vcam-1与mcp-1蛋白表达水平(如 图5)。同时检测了apoe-/-小鼠血管caspase-1/gsdmd通路活化水平;结果发 现,与对照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂 +gsdmd抑制剂组均显著降低了血管nlrp3、il-1β、hmgb1蛋白表达水平以 及caspase-1与gsdmd活动水平(如图6)。这表明gsdmd多肽抑制剂可在 体抑制caspase-1/gsdmd通路活化水平,降低血管炎症。
[0054]
实施例2
[0055]
gsdmd多肽抑制剂对脓毒血症的防治作用:
[0056]
采用10周龄c57小鼠,分别予以对照组以对照溶剂;caspase-1抑制剂组以 z-yvad-fmk(caspase-1抑制剂,腹腔注射,200微克/天);gsdmd抑制剂 组以z-llsd-fmk(gsdmd抑制剂,腹腔注射,200微克/天)或caspase-1抑 制剂加gsdmd抑制剂组以z-yvad-fmk+z-llsd-fmk(腹腔注射,各200 微克/天);干预5天,在第5天同时腹腔注射一次lps(20mg/kg);结果发现, 与对照组相比,caspase-1抑制剂组、gsdmd抑制剂组与caspase-1抑制剂 +gsdmd抑制剂组均显著提高了小鼠存活率,降低了血浆ldh与hmgb1水平, 且各抑制剂组之间无明显差异(如图7)。同时检测了小鼠脾脏caspase-1/gsdmd 通路活化水平;结果发现,与对照组相比,caspase-1抑制剂组、gsdmd抑制 剂组与caspase-1抑制剂+gsdmd抑制剂组均显著降低了脾脏caspase-1与 gsdmd活动水平(如图8)。这表明gsdmd多肽抑制剂可在体抑制 caspase-1/gsdmd通路活化水平,有效防治脓毒血症的进展。
[0057]
综上所述,本发明建立了apoe-/-小鼠动脉粥样硬化模型,采用本发明设计 的gsdmd多肽抑制剂进行腹腔注射在体干预,利用he染色、免疫荧光及分子 生物学技术,评估斑块面积、血管炎症及caspase-1/gsdmd通路活化水平,发 现gsdmd多肽抑制剂降低了血管炎症与动脉粥样硬化斑块面积,并抑制了 caspase-1/gsdmd通路活化水平。同时,本发明还建立了脓毒血症小鼠模型, 采用本发明设计的gsdmd多肽抑制剂进行腹腔注射在体干预,利用分子生物学 技术,评估了小鼠存活率、炎症因子及caspase-1/gsdmd通路活化水平,发现 gsdmd多肽抑制剂降低了全身炎症,提高了小鼠存活率,并抑制了 caspase-1/gsdmd通路活化水平。这些提示gsdmd多肽抑制剂可用于防治动 脉粥样硬化与脓毒血症。
[0058]
以上所述,仅为本发明的较佳实施例,并非对本发明任何形式上和实质上的 限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明的前提下, 还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。凡 熟悉本专业的技术人员,在不脱离本发明的精神和范围的情况下,当可利用以上 所揭示的技术内容而做出的些许更动、修饰与演变的等同变化,均为本发明的等 效实施例;同时,凡依据本发明的实质技术对上述实施例所作的任何等同变化的 更动、修饰与演变,均仍属于本发明的技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1