ICAM1或其编码基因在制备胃癌治疗或诊断产品中的用途的制作方法
本发明涉及医药领域,特别是涉及icam1或其编码基因在制备胃癌治疗或诊断产品中的用途。
背景技术:
1、胃癌是最常见的恶性肿瘤之一,发病率和死亡率均较高,分别位于恶性肿瘤的第5位和第4位,严重威胁人类的生命健康。胃癌是一种高度异质性肿瘤,不同亚型之间呈现出较大的差异化。目前已有多种对胃癌的分型方法,传统分型方法基于肿瘤的外观形态,对临床指导意义有限,不能有效指导个体化治疗的靶向用药。2014年,肿瘤基因组计划(thecancer genome atlas,tcga)在nature上提出了一种全新的分型方法——tcga分型,将胃癌分为染色体不稳定型(cin型)、微卫星不稳定型(msi型)、染色体稳定型(gs型)和人类四型孢疹病毒阳性型(ebv型),使肿瘤分类从传统的形态学转向以分子特征为基础的分子分型,使个体化精准治疗成为可能。tcga分型中,染色体不稳定型(cin)胃癌发病比例最高,约占49.8%,发病部位多位于胃食管结合部,预后较差。
2、cin是指染色体区域中dna发生拷贝数改变或结构异常,从而导致染色体发生不可逆的易位、扩增或缺失的现象,最常扩增的区域包括染色体1q、5p、6p、7p、7q、8q、13q、19p、20p、20q,最常丢失的区域包括染色体3p、4p、4q、5q、6q、9p、14q、18q、21q。cin亚型胃癌多属于lauren分型中的肠型,具有tp53基因频繁突变和rtks基因扩增的特点。研究显示,cin能够驱动肿瘤中异质性的克隆进化,进而获得耐药性。引起cin的分子机制复杂多样,目前已知的可能性有:(1)有丝分裂过程中检查点缺陷、动粒障碍、姐妹染色单体凝聚和分离缺陷、中心体扩增和端粒功能障碍等导致的染色体分离异常。(2)细胞周期检查点缺陷:cdk激酶过度活跃会使dna损伤的细胞细胞周期延续,含受损dna的细胞增殖;tp53突变消除g1-s检查点会导致基因扩增、缺失和基因组重排。(3)致癌基因诱导的有丝分裂应激:致癌基因ras过表达导致中心体过度复制、后期桥的产生和多极纺锤体的形成;met过表达可通过pi3k-akt途径诱导多中心体形成;raf癌基因中braf突变可诱导异常纺锤体、多中心体、染色体错误分离和非整倍体。(4)复制压力:有丝分裂前错误和受损的复制叉进程导致复制压力。18q号染色体上3个cin抑制基因pign(mcd4)、rkhd2(mex3c)、znf516(kiaa0222),18q丢失与非整倍体在腺瘤-癌转变时相关。cin抑制基因沉默导致dna复制压力、结构染色体异常和染色体错误分离。在病理检查中,恶性肿瘤的增殖活性常用有丝分裂细胞比例或有丝分裂指数来表示,因此靶向有丝分裂被认为是癌症治疗的有力手段。但靶向有丝分裂具有挑战性,因为它会损伤正常增殖的细胞,导致严重不良反应,因此鉴定分子缺陷、降低药物不良反应是开发抑制有丝分裂的抗肿瘤药物的关键所在。
3、gs亚型胃癌(gsgc)患者约占胃癌总体患者的20%,初诊年龄偏低(中位年龄59岁),约73%属于lauren分型中的弥漫型,该型cdh1、rhoa基因突变率高,且常见cldn18-arhgap26(graf)融合现象。随后,bo hwa sohn等研究者通过分析tcga项目的基因表达数据并基于4种亚型的基因表达特征建立预测模型,利用该模型分别检测了两个独立队列中各亚型与预后的相关性,结果均表明ebv亚型的预后最佳,msi和cin亚型患者预后次之,而gs亚型的预后最差。可见,gsgc多数是弥漫型胃癌,转移较快且预后最差,这类致死性较高的胃癌亚型具有重要未满足的医学需求。
4、抗体偶联药物(antibody drug conjugate,adc)将小分子细胞毒药物与靶向特异性抗原的单克隆抗体通过连接子进行偶联,使药物能够选择性地靶向肿瘤,抗体药物以其高特异性、安全性和有效性的特点成为全球抗肿瘤药物研发的热点。adc药物利用单克隆抗体的靶向性,特异性识别肿瘤细胞表面抗原,内化后进入细胞,转运至溶酶体中,释放细胞毒药物,发挥dna酶抑制或微管抑制作用,诱导细胞死亡。adc药物既具有小分子细胞毒药物的抗肿瘤效应,又具有高选择性、较好的稳定性和良好的药代动力学优点。adc药物自提出至今一直在创新优化,目前已经过三次变革,第三代adc药物通过对抗体进行改造,在特定位点插入非天然氨基酸实现定点偶联,实现了更多新靶点的发现、载药值的提高和连接子的优化的目标。全球目前已有14个adc药物已获批,在血液瘤和少数实体瘤中取得了良好的治疗效果。目前,除了her2和cd靶点外,c-met、egfr、bcma、trop2和cd20也是adc药物研发的热门靶点。尽管adc类药物在实体瘤中展现出了可观的治疗潜力,但是目前适应于胃癌的adc类药物屈指可数。目前已批准上市的抗体偶联药物t-dm1、t-dxd和rc48可用于胃癌治疗,这3种adc药物采用的靶蛋白均为her2,在乳腺癌中取得良好的治疗效果,在胃癌中生存获益较小,治疗效果有限,可能是因为her2过表达在不同癌种中功能不同。trastuzumabderuxtecan(t-dxd)(ds-8201;)是首个获fda批准用于治疗胃癌的adc药物。早在2019年时,由第一三共和阿斯利康合作开发的新型靶向her2的adc类药物ds-8201获批用于治疗转移性her2阳性乳腺癌。ds-8201由人源化抗her2抗体trastuzumab可裂解的四肽连接体和dna拓扑异构酶i抑制剂dxd组成,药物/抗体比值(dar)高达8。随后,2021年1月15日,fda批准了ds-8201用于治疗局部晚期或转移性her2阳性胃癌或胃食管交界处腺癌的成年患者,这些患者先前已接受过以曲妥珠单抗为基础的治疗方案。另一款用于胃癌治疗的ds-8201获批用于治疗转移性her2阳性乳腺癌adc类药物是2021年6月获批上市的disitamab vedotin(rc48,)。rc48由荣昌生物制药(烟台)有限公司自主研发,是国内第一款上市的国产adc药物,适应症为her2阳性晚期或转移性胃癌。rc48-adc的抗体是我国自主研发的全新人源化抗her2抗体——迪西妥单抗,相比曲妥珠单抗抗原识别位点略有不同,与her2受体的亲和力更强,在肿瘤细胞的内吞效果好;毒性分子mmae分子较小并且对多种肿瘤细胞具有毒性作用;rc48-adc连接子可裂解,可以更好地发挥旁杀效应。然而,her2阳性患者仅占总体胃癌患者的17-20%,且常见于肠型胃癌和位于胃近端或胃食管交界处癌症患者,因此gsgc和cin患者未能从靶向her2的adc药物中明显获益,开发针对不同分子分型的新靶点和及其靶向的adc药物对gsgc或cin患者这一群体具有重大意义。随着抗体技术的成熟,adc药物应用范围也逐渐扩大,越来越多新的靶点用于药物研发当中,开发her2外的新靶点对胃癌的免疫治疗十分必要。
5、icam1(细胞间黏附分子-1,cd54)是一种跨膜糖蛋白,是免疫球蛋白超家族成员之一,是一种广泛分布的细胞黏附分子,介导了细胞-细胞和细胞-细胞外基质的相互作用、细胞信号转导、免疫炎性反应和血管生成等生理过程。目前已发现其在多种癌症中过表达,如胰腺癌、三阴性乳腺癌、黑色素瘤和甲状腺癌等,过表达的icam1一方面可脱落进入血液,成为可溶型的sicam1,sicam1与淋巴细胞相关抗原-1(lfa-1)或mac-1相互作用,竞争性抑制icam1-lfa-1依赖的非主要组织相容性复合体(mhc)限制性的免疫识别,另一方面与肿瘤细胞附近高表达lfa-1的浸润淋巴细胞结合增强,降低肿瘤细胞之间的黏附,介导了肿瘤的发生、侵袭和转移。
技术实现思路
1、鉴于以上所述现有技术的缺点,本发明的目的在于提供icam1或其编码基因在制备胃癌治疗或诊断产品中的用途,用于解决现有技术中的问题。
2、为实现上述目的及其他相关目的,本发明提供icam1或其编码基因作为分子识别靶标在制备染色体不稳定型胃癌诊断或治疗产品中的用途。
3、本发明还提供特异性结合icam1的物质在制备染色体不稳定型胃癌治疗或诊断产品中的用途。
4、本发明提供icam1或其编码基因作为分子识别靶标在制备基因组稳定型胃癌诊断或治疗产品中的用途。
5、本发明还提供特异性结合icam1的物质在制备基因组稳定型胃癌治疗或诊断产品中的用途。
6、优选的,所述特异性结合icam1的物质选自抗体偶联药物或其药学上可接受的盐或溶剂化合物。
7、本发明还提供一种抗体偶联药物或其药学上可接受的盐,所述抗体偶联药物的结构如下所示:ab-(l-d)n,其中ab为抗icam1抗体,l为连接子,d为细胞毒剂,n为1-40的整数。
8、优选的,所述抗icam1抗体的重链和轻链氨基酸序列分别如seq id no.7和8所示。
9、优选的,所述抗体偶联药物选自anti-icam1 mab-mc-vc-pab-mmae(简称为icam1-mmae)或anti-icam1 mab-mc-ggfg-dxd(简称为icam1-dxd)。
10、本发明还提供所述抗体偶联药物的制备方法,包括如下步骤:
11、1)将二硫键还原剂与抗icam1抗体混合,使抗icam1抗体半胱氨酸中的二硫键至少部分被还原成巯基;
12、2)将连接子、细胞毒剂与步骤1)的产物混合,使抗icam1抗体与连接子偶联得到所述抗体偶联药物。
13、如上所述,本发明的icam1或其编码基因在制备胃癌治疗或诊断产品中的用途,具有以下有益效果:
14、第一,adc药物在胃癌中已上市的药物较少,主要以her2为靶点进行设计,相较于乳腺癌等适应症,在胃癌中治疗效果不够理想。本发明所使用的icam1靶点是一个新颖且有效的胃癌adc药物设计的靶点。
15、第二,icam1靶点广泛分布于cin亚型的胃癌细胞中,在正常细胞中不表达,这种蛋白表达的差异可以有效介导adc药物准确靶向肿瘤组织而不杀伤正常组织,安全性高,克服了目前临床常见化疗药物严重不良反应的缺点。
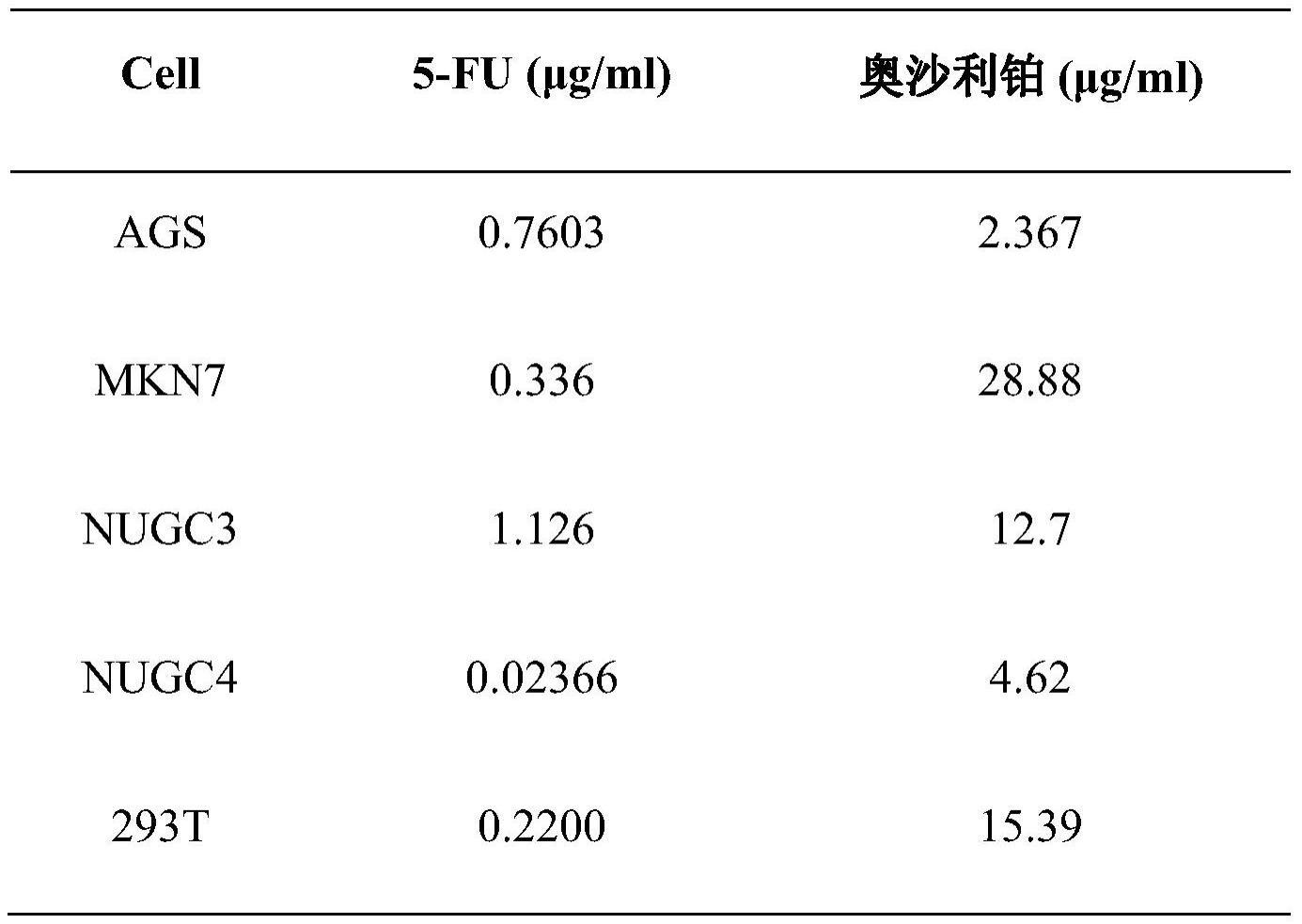
16、第三,anti-icam1 mab-mc-vc-pab-mmae治疗效果更好,连接子和细胞毒剂更佳,且优于目前临床常见的胃癌化疗药物5-氟尿嘧啶和奥沙利铂,有望成为具有临床价值的药物。
- 还没有人留言评论。精彩留言会获得点赞!