伊曲康唑微丸、制备方法及伊曲康唑微丸胶囊与流程
1.本发明涉及药物制剂技术领域,具体涉及一种伊曲康唑微丸、制备方法及伊曲康唑微丸胶囊。
背景技术:
2.伊曲康唑即(
±
)-顺式-4-[4-[4[4-[[2-(2,4-二氯苯基)-2-(1h-1,2,4-三唑-1-基-甲基)-1,3-二氧杂环戊烷-4-基]甲氧基]-1-哌嗪基]苯基]-2,4-二氢-2-(1-甲基丙基)-3h-1,2,4-三唑-3-酮,是一种广谱抗真菌化合物,可用于治疗系统性真菌感染所知病症,例如曲霉病、念珠菌病、隐球菌性脑膜炎、组织胞浆菌病、孢子丝菌病、副球孢子菌病、着色真菌病、芽生菌病、妇科外阴阴道念珠菌病、皮肤科/眼科花斑癣、皮肤真菌病、真菌性角膜炎、口腔念珠菌病及由皮肤癣菌和/或酵母菌引起的甲真菌病等。
[0003]
伊曲康唑微丸是伊曲康唑的常见剂型,但是在实现本发明的过程中,本发明的发明人发现,现有的伊曲康唑微丸因存在析晶现象而稳定性较差。
技术实现要素:
[0004]
因此,本发明要解决的技术问题在于克服现有伊曲康唑微丸稳定性较差的缺陷,从而提供一种伊曲康唑微丸、制备方法及伊曲康唑微丸胶囊。
[0005]
为此,本发明提供一种伊曲康唑微丸,所述伊曲康唑微丸包括丸芯以及包覆在所述丸芯表面的包衣层,其中,所述包衣层中含有伊曲康唑和黄原胶,所述黄原胶呈溶胀状态。
[0006]
可选的,所述黄原胶的分子量为2
×
106。
[0007]
可选的,在所述伊曲康唑微丸中,相对于100重量份的所述伊曲康唑,所述丸芯的含量为180重量份,所述黄原胶的含量为5~15重量份。
[0008]
可选的,所述包衣层中还含有分散载体,相对于100重量份的所述伊曲康唑,所述分散载体的含量为140重量份。
[0009]
可选的,所述丸芯选蔗糖丸芯和/或微晶纤维素丸芯。
[0010]
可选的,所述分散载体选自羟丙甲纤维素、羧甲基纤维素或羟丙基纤维素中的至少一种。
[0011]
可选的,所述丸芯的粒径为600~710μm,所述伊曲康唑微丸的粒径为900~1100μm。
[0012]
本发明还提供了一种伊曲康唑微丸的制备方法,包括如下操作:
[0013]
取含药混悬液,对丸芯进行喷液包衣,干燥,得到微丸中间品,其中,所述含药混悬液中含有伊曲康唑、黄原胶和溶剂;
[0014]
对所述微丸中间品进行熟化以使所述黄原胶发生溶胀。
[0015]
可选的,所述黄原胶的分子量为2
×
106。
[0016]
可选的,在所述含药混悬液中,相对于100重量份的所述伊曲康唑,所述黄原胶的
用量为5~15重量份,所述溶剂的用量为2300体积份,其中当重量份的单位为kg时体积份的单位为l。
[0017]
可选的,在进行喷液包衣时,相对于100重量份的所述伊曲康唑,所述丸芯的用量为180重量份。
[0018]
可选的,所述含药混悬液中还含有分散载体,相对于100重量份的所述伊曲康唑,所述分散载体的用量为140重量份。
[0019]
可选的,所述丸芯选自蔗糖丸芯和/或微晶纤维素丸芯。
[0020]
可选的,所述分散载体选自羟丙甲纤维素、羧甲基纤维素或羟丙基纤维素中的至少一种。
[0021]
可选的,所述溶剂选自乙醇、二氯甲烷和水中的至少一种,优选为乙醇与二氯甲烷的混合液,乙醇与二氯甲烷的体积比为8:15。
[0022]
可选的,所述含药混悬液的制备方法包括:取伊曲康唑与所述分散载体,溶于溶剂后,加入黄原胶。
[0023]
可选的,所述喷液包衣的条件包括:进风温度为35~40℃,出风温度为30~35℃。
[0024]
可选的,所述干燥的条件包括:进风温度为40~45℃、出风温度为30~35℃,干燥时间为0.5h。
[0025]
可选的,所述熟化的条件包括:熟化温度为98~102℃,相对湿度为30~40%rh,熟化时间为6~10h。
[0026]
本发明还提供了一种伊曲康唑微丸胶囊,含有上述任一项所述的伊曲康唑微丸,或者通过上述任一项所述的制备方法制备的伊曲康唑微丸。
[0027]
本发明技术方案,具有如下优点:
[0028]
1.本发明提供的伊曲康唑微丸,包括丸芯以及包覆在所述丸芯表面的包衣层,所述包衣层中含有伊曲康唑和呈溶胀状态的黄原胶。溶胀状态的黄原胶能够显著提升包衣层的致密性,有效阻断高温、高湿等环境因素对微丸内部的影响,从而避免伊曲康唑发生重结晶,抑制析晶现象,因此,本发明的伊曲康唑微丸具有较好的稳定性。
[0029]
2.本发明提供的伊曲康唑微丸,包衣层中含有溶胀状态的黄原胶以及特定含量的分散载体,使得包衣层中的伊曲康唑药物具有良好的溶出环境,因此,该伊曲康唑微丸具有较高的溶出度。
[0030]
3.本发明提供的伊曲康唑微丸的制备方法,通过结合使用黄原胶和熟化工艺,能够显著改善伊曲康唑微丸的析晶问题,有效提升伊曲康唑微丸的稳定性。具体的,一方面熟化工艺能够提升微丸包衣层的致密性,另一方面黄原胶能够在熟化过程中快速溶胀,进一步提升包衣层的致密性,从而使得包衣层能够有效阻断高温、高湿等环境因素对微丸内部的影响,避免伊曲康唑在高温、高湿等条件下发生重结晶,从而抑制伊曲康唑的抑制析晶现象,因此,本发明的伊曲康唑微丸制备方法能够显著提升伊曲康唑微丸的稳定性。
附图说明
[0031]
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前
提下,还可以根据这些附图获得其他的附图。
[0032]
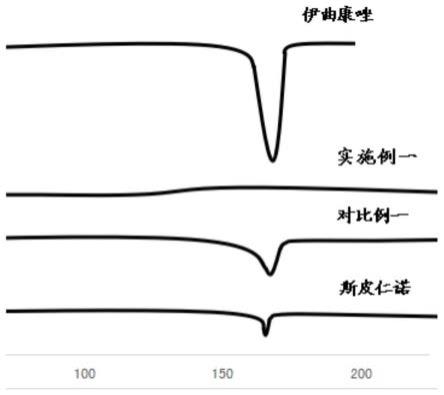
图1是本发明实验例2中各伊曲康唑微丸胶囊的dsc扫描曲线图。
具体实施方式
[0033]
提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
[0034]
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
[0035]
实施例1
[0036]
本实施例提供一种伊曲康唑微丸的制备方法,包括如下操作:
[0037]
(1)取伊曲康唑0.12kg、分散载体(羟丙甲纤维素)0.168kg,溶于2.76l溶剂(乙醇和二氯甲烷按照体积比8:15的混合液)中,溶解完全后加入黄原胶0.012kg,待黄原胶分散完全后,得到含药混悬液;
[0038]
(2)取操作(1)所得含药混悬液,在流化床中对0.216kg丸芯(蔗糖丸芯,粒径为600~710μm)进行喷液包衣,干燥后得到微丸中间品;其中,喷液包衣阶段的进风温度为35~40℃,出风温度为30~35℃,干燥阶段的进风温度为40~45℃、出风温度为30~35℃,时间为0.5h;
[0039]
(3)取操作(2)所得微丸中间品,置于100℃、35%rh相对湿度的恒温恒湿箱中熟化8h,得到伊曲康唑微丸。
[0040]
本实施例制备得到的伊曲康唑微丸包括丸芯以及包覆在丸芯表面的包衣层,其中,包衣层中含有伊曲康唑、分散载体(羟丙甲纤维素)和呈溶胀状态的黄原胶。在该伊曲康唑微丸中,相对于100重量份的伊曲康唑,丸芯(蔗糖丸芯)的含量为180重量份,黄原胶的含量为10重量份,分散载体(羟丙甲纤维素)的含量为140重量份。经检测,该伊曲康唑微丸的粒径为900~1100μm。
[0041]
实施例2
[0042]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本实施例中,黄原胶的使用量为0.006kg。
[0043]
本实施例制备得到的伊曲康唑微丸中,相对于100重量份的伊曲康唑,黄原胶的含量为5重量份。
[0044]
实施例3
[0045]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本实施例中,黄原胶的使用量为0.018kg。
[0046]
本实施例制备得到的伊曲康唑微丸中,相对于100重量份的伊曲康唑,黄原胶的含量为15重量份。
[0047]
实施例4
[0048]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本实施例中,分散载体(羟丙甲
纤维素)的使用量为0.18kg。
[0049]
本实施例制备得到的伊曲康唑微丸中,相对于100重量份的伊曲康唑,分散载体(羟丙甲纤维素)的含量为150重量份。
[0050]
实施例5
[0051]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本实施例操作(3)中熟化的温度为98℃,相对湿度为40%rh,熟化时间为6h。
[0052]
实施例6
[0053]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本实施例操作(3)中熟化的温度为102℃,相对湿度为30%rh,熟化时间为10h。
[0054]
实施例7
[0055]
按照实施例1的方法制备伊曲康唑微丸,不同的是:使用等量的羧甲基纤维素替换羟丙甲纤维素。
[0056]
实施例8
[0057]
按照实施例1的方法制备伊曲康唑微丸,不同的是:使用等量的羟丙基纤维素替换羟丙甲纤维素。
[0058]
对比例1
[0059]
按照实施例1的方法制备伊曲康唑微丸,不同的是:本对比例不进行操作(3)中的熟化处理。
[0060]
实验例1
[0061]
将实施例1-6、对比例1制得的伊曲康唑微丸灌装成胶囊,装量430mg
±
4%,并将各伊曲康唑微丸胶囊与斯皮仁诺(批号kjj1hcq)放入加速条件(60℃,75%rh)下进行加速试验2个月。
[0062]
加速试验结束后,取出各伊曲康唑微丸胶囊,照溶出度测定法(中国药典2020年版四部通则第一法)进行溶出试验,以900ml介质溶液(ph1.0的盐酸溶液)为溶出介质,转速每分钟50转,依法操作。分别于第60分钟和第120分钟取样,按照紫外-可见分光光度法(通则0401)测试溶出度,结果见表1。
[0063]
表1加速试验2个月后各伊曲康唑微丸胶囊溶出度
[0064]
胶囊60min溶出度,%120min溶出度,%实施例189.099.8实施例287.592.0实施例378.496.5实施例476.679.5实施例588.891.3实施例679.694.7对比例173.975.3斯皮仁诺87.890.2
[0065]
由表1可以看出,本发明方法制备得到的伊曲康唑微丸制备成胶囊后,具有较高的溶出度。
[0066]
实验例2
[0067]
取实验例1中加速试验2个月后的由实施例1、对比例1的伊曲康唑微丸制备的胶囊、斯皮仁诺(批号kjj1hcq),以及伊曲康唑原料,利用dsc差示扫描量热法进行热分析,具体操作如下:
[0068]
以空铝坩埚为参比物,另一坩埚中称取5mg样品至差热扫描量热仪中,升温速度10℃/min-1
,升温范围30~250℃,氮气50ml/min-1
环境下测定其热曲线。
[0069]
扫描得到的dsc曲线如图1所示,由图1可以看出,由对比例1的伊曲康唑微丸制备的胶囊和斯皮仁诺(批号kjj1hcq)在加速条件(60℃,75%rh)2个月加速试验后,dsc扫描曲线中出现了伊曲康唑的熔融峰,这说明由对比例1的伊曲康唑微丸制备的胶囊以及斯皮仁诺(批号kjj1hcq)中的无定形伊曲康唑已经出现了重结晶;而由实施例1的伊曲康唑微丸制备的胶囊,在加速条件(60℃,75%rh)2个月加速试验后,dsc扫描曲线中未出现伊曲康唑的熔融峰,这说明由实施例1的伊曲康唑微丸制备的胶囊中的伊曲康唑仍然保持非晶态。
[0070]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1