一种覆盖TF-PEG-PLGA涂层的载药ZIF-8纳米粒及其制备方法与应用
一种覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法与应用
技术领域
1.本发明涉及生物医学检测技术领域,特别涉及覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法与应用。
背景技术:
2.胶质瘤是人中枢神经系统中最常见的原发性肿瘤,约占所有原发恶性脑肿瘤的80%,其中胶质母细胞瘤(glioblastoma,gbm)为第iv级胶质瘤,约占胶质瘤总数的54%,具有高发病率、高复发率、高病死率和低治愈率的特点。手术辅以放射治疗及化疗是gbm目前主要的治疗手段。然而,由于gbm的浸润性生长方式,手术难以完全切除,而且放疗存在放疗抗性的问题。化疗药物的应用可以改善手术及放疗患者的预后,而化疗药物的血脑屏障穿透能力以及化疗毒副作用制约了其在gbm治疗中的应用。
3.传统化疗药物治疗脑肿瘤存在着血脑屏障通透性问题以及药物毒副反应的问题,解决以上问题的突破口在于提高药物的血脑屏障的通透性以及肿瘤的靶向性,肿瘤组织靶向给药有利于降低药物的毒副作用,
4.因此,有必要开发一种具有血脑屏障通透性及肿瘤靶向性的载药纳米粒。
技术实现要素:
5.本发明目的是提供一种覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法与应用,本发明的纳米粒具有血脑屏障通透性的、肿瘤靶向性的、针对颅脑肿瘤靶向递药,为颅内肿瘤高效、靶向给药提供了理想的载体,在颅内肿瘤应用方面具有广阔的前景。
6.为了实现上述目的,本发明采用如下技术方案:
7.在本发明的第一方面,提供了一种覆盖tf-peg-plga涂层的载药zif-8纳米粒的制备方法,所述方法包括:
8.将目标药物、2-甲基咪唑、硝酸锌加入甲醇溶液中混合进行第一反应,后纯化溶于甲醇,获得载药zif-8纳米粒溶液;
9.后进行以下操作a或者操作b:
10.操作a:
11.将cooh-peg-plga活化后与转铁蛋白在pbs中混匀进行第二反应,后纯化溶于pbs,获得转铁蛋白修饰的peg-plga溶液,简称tf-peg-plga;
12.将所述载药zif-8纳米粒溶液和所述转铁蛋白修饰的peg-plga溶液混匀,获得覆盖tf-peg-plga涂层的载药zif-8纳米粒,简称zif-8/tf-peg-plga;
13.或者操作b:
14.将所述载药zif-8纳米粒溶液与cooh-peg-plga在pbs中混匀,后纯化溶于pbs,获得载药@zif-8/peg-plga悬液;
15.将所述载药@zif-8/peg-plga悬液活化后与转铁蛋白混合,后纯化溶于甲醇获得
覆盖tf-peg-plga涂层的载药zif-8纳米粒,简称zif-8/tf-peg-plga。
16.进一步地,所述目标药物包括芦荟大黄素、顺铂、紫杉醇和吲哚菁绿中的一种。
17.进一步地,所述目标药物、2-甲基咪唑、硝酸锌的质量比为1:(15~17):(7~8)。
18.进一步地,所述第一反应和所述第二反应的条件均包括:以200~300rpm的转速进行磁力搅拌,室温反应0.5~2h,后静置。
19.进一步地,cooh-peg-plga活化的方法包括:先将所述cooh-peg-plga采用1-乙基-(3-二甲基氨基丙基)碳酰二亚胺(edc)、n-羟基丁二酰亚胺(nhs)活化所述cooh-peg-plga上的羧基。
20.进一步地,所述操作a中和所述操作b中,所述转铁蛋白与所述cooh-peg-plga的质量比均为1:(700~800)。
21.进一步地,所述操作a中,所述载药zif-8纳米粒溶液和所述转铁蛋白修饰的peg-plga溶液的体积比为(6~8):(2~4);所述操作b中,所述载药zif-8纳米粒溶液与cooh-peg-plga的体积比为(6~8):(2~4)。
22.进一步地,所述方法还包括:
23.将所述覆盖tf-peg-plga涂层的载药zif-8纳米粒经过离心纯化、除菌、在表面活性剂存在的条件下溶解。
24.在本发明的第二方面,提供了所述方法制备得到的覆盖tf-peg-plga涂层的载药zif-8纳米粒,所述纳米粒为核壳结构:
25.核层,为载药的zif-8纳米粒;
26.壳层,包裹于所述核层的外周,所述壳层为转铁蛋白修饰的peg-plga。
27.在本发明的第三方面,提供了所述的覆盖tf-peg-plga涂层的载药zif-8纳米粒在制备用于颅脑肿瘤靶向递药的载药纳米粒药物中的应用。
28.本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
29.本发明利用肿瘤靶向性的zif-8纳米粒包被抗肿瘤药物芦荟大黄素、外层包被能增强药物血脑屏障通透性的tf-peg-pl涂层,由于zif-8有肿瘤微环境释放特性,可以实现肿瘤的靶向性;转铁蛋白(transferrin,tf)可以与血脑屏障特异高表达的转铁蛋白受体结合,以载体转运的方式穿透血脑屏障,从而增强纳米粒血脑屏障的穿透能力;利用plga的生物相容性一方面增强药物的水溶性,另一方面增强药物的血脑屏障穿透能力;聚乙二醇(peg-plga)的应用可以延长药物的体内循环时间。该载药纳米粒可以增强药物的血脑屏障穿透能力,增强药物的肿瘤靶向能力而增强药物的抗肿瘤效率且降低药物毒副反应。因而本发明将有望在脑肿瘤靶向给药方面具有良好的应用前景,与现有技术相比,本发明具有如下的有益效果:
30.(1)增强药物血脑屏障通透能力,提高颅内组织药物浓度。
31.(2)如图8所示,本发明的覆盖tf-peg-plga涂层的载药zif-8纳米粒可以改善药物肿瘤富集及靶向能力,增强肿瘤组织药物分布而减少正常组织药物分布,增强抗肿瘤效应而减少毒副不良反应。
32.(3)本发明使用纳米材料,生物相容性好,能提高药物水溶性、稳定性和体内循环时间。
附图说明
33.为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。
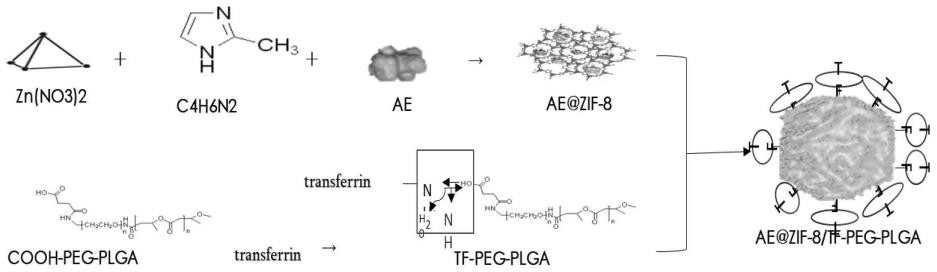
34.图1为ae@zif-8/tf-peg-plga纳米粒构建示意图;
35.图2为纳米粒体内递送示意图;
36.图3为纳米粒透射电镜外观图;
37.图4为纳米粒粒度图;
38.图5为纳米粒表面ζ电位图;
39.图6为纳米粒紫外吸收图谱;
40.图7为纳米粒体外释放图;
41.图8为纳米粒颅内分布及肿瘤富集图。
具体实施方式
42.下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
43.在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
44.除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买获得或者可通过现有方法获得。
45.本发明的总体思路如下:
46.根据本发明一种典型的实施方式,提供一种覆盖tf-peg-plga涂层的载药zif-8纳米粒的制备方法,所述方法包括:
47.步骤s101、将目标药物、2-甲基咪唑、硝酸锌加入甲醇溶液中混合进行第一反应,后纯化溶于甲醇,获得载药zif-8纳米粒溶液;
48.上述技术方案中,
49.所述甲醇溶液为纯的甲醇溶液;
50.所述目标药物包括芦荟大黄素。在其他实施方式中,所述目标药物还可以为顺铂、紫杉醇、吲哚菁绿;
51.所述目标药物、2-甲基咪唑、硝酸锌的质量比为1:(15~17):(7~8)。该质量比范围有利于获得最好的药物包封率。
52.所述第一反应的条件均包括:以200~300rpm的转速进行磁力搅拌,室温反应0.5~2h,后静置。
53.作为一种具体的实施方式,所述纯化方式为离心沉淀清洗,甲醇环境下,12000rpm,10分钟,洗涤三次,取沉淀,行后续反应。
54.步骤s102、将cooh-peg-plga活化后与转铁蛋白在pbs中混匀进行第二反应,后纯
化溶于pbs,获得转铁蛋白修饰的peg-plga溶液,简称tf-peg-plga;
55.上述技术方案中,
56.所述cooh-peg-plga在进行所述修饰反应之前,先将所述cooh-peg-plga采用1-乙基-(3-二甲基氨基丙基)碳酰二亚胺(edc)、n-羟基丁二酰亚胺(nhs)活化所述cooh-peg-plga上的羧基。
57.所述转铁蛋白与所述cooh-peg-plga的质量比为1:(700~800)。该质量比范围有利于获得最好的转铁蛋白连接率;
58.作为一种具体的实施方式,所述纯化方法为,离心沉淀清洗,甲醇环境下,12000rpm,10分钟,洗涤两次。
59.步骤s103、将所述载药zif-8纳米粒溶液和所述转铁蛋白修饰的peg-plga溶液混匀,获得覆盖tf-peg-plga涂层的载药zif-8纳米粒,简称zif-8/tf-peg-plga。
60.上述技术方案中,
61.所述载药zif-8纳米粒溶液和所述转铁蛋白修饰的peg-plga溶液的体积比为(6~8):(2~4)。该体积比范围有利于获得更好的载药率、转铁蛋白连接率以及可实用的纳米粒径;所述质量比若过大有降低转铁蛋白连接率的不利影响,若过小所制备的纳米粒粒径过大,不适用于颅内给药。
62.所述方法还包括:
63.将所述覆盖tf-peg-plga涂层的载药zif-8纳米粒经过离心纯化、除菌、在表面活性剂存在的条件下溶解。所述除菌方法为75%乙醇浸泡。所述表面活性剂包括1%泊洛沙姆。
64.根据本发明另一种典型的实施方式,提供一种覆盖tf-peg-plga涂层的载药zif-8纳米粒的制备方法,所述方法包括:
65.步骤s201、将目标药物、2-甲基咪唑、硝酸锌加入甲醇溶液中混合进行第一反应,后纯化溶于甲醇,获得载药zif-8纳米粒溶液;
66.步骤s202、将所述载药zif-8纳米粒溶液与cooh-peg-plga在pbs中混匀,后纯化溶于pbs,获得载药@zif-8/peg-plga悬液;
67.上述技术方案中,
68.所述载药zif-8纳米粒溶液与cooh-peg-plga的体积比为(6~8):(2~4)。
69.步骤s203、将所述载药@zif-8/peg-plga悬液活化后与转铁蛋白混合,后纯化溶于甲醇获得覆盖tf-peg-plga涂层的载药zif-8纳米粒,简称zif-8/tf-peg-plga。
70.上述技术方案中,所述转铁蛋白与所述cooh-peg-plga的质量比均为1:(700~800)。
71.下面将结合实施例及实验数据对本技术的一种覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法与应用进行详细说明。
72.实施例1、覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法
73.取75mg硝酸锌溶于2.5ml样品瓶中(a瓶),120w超声浴2分钟溶解;取165mg二甲基咪唑和10mg芦荟大黄素共溶于5ml甲醇中(b瓶),120w超声浴5分钟溶解,室温条件下磁力搅拌5分钟,250转/分钟。将a瓶逐滴加入b瓶中,室温条件下,避光250分/转磁力搅拌1小时,4℃静置1小时。12000转/分离心10分钟,取沉淀得产物ae@zif-8纳米粒,甲醇重悬,再次离
心,重复三次,终产物以5ml甲醇重悬。
74.取10mgcooh-peg-plga溶于4.5ml磷酸盐缓冲液(pbs)中,120w超声浴5分钟溶解,再逐滴加入1mg/ml1-乙基-(3-二甲基氨基丙基)碳酰二亚胺(edc)、1mg/mln-羟基丁二酰亚胺(nhs)各250μl,室温条件下磁力搅拌4小时,250转/分钟。逐滴加入1mg/ml的转铁蛋白水溶液,避光继续搅拌2小时,4℃静置过夜。12000转/分离心10分钟,取沉淀得tf-peg-plga,pbs重悬,再次离心,重复三次,合成产物以5mlpbs重悬。
75.将上述ae@zif-8甲醇溶液与tf-peg-plga水溶液按体积比7:3比例混合,室温避光条件下磁力搅拌4小时,250转/分钟。12000转/分离心10分钟,取沉淀得终产物ae@zif-8/tf-peg-plga,再次用甲醇重悬,12000转/分离心10分钟,重复两次。用75%乙醇重悬,浸泡30分钟,离心,沉淀用包含1%泊洛沙姆的生理盐水洗涤两次。
76.实施例2、覆盖tf-peg-plga涂层的载药zif-8纳米粒及其制备方法
77.取75mg硝酸锌溶于2.5ml样品瓶中(a瓶),120w超声浴2分钟溶解;取165mg二甲基咪唑和10mg芦荟大黄素共溶于5ml甲醇中(b瓶),120w超声浴5分钟溶解,室温条件下磁力搅拌5分钟,250转/分钟。将a瓶逐滴加入b瓶中,室温条件下,避光250分/转磁力搅拌1小时,4℃静置1小时。12000转/分离心10分钟,取沉淀得产物ae@zif-8纳米粒,甲醇重悬,再次离心,重复三次,终产物以5ml甲醇重悬。
78.取10mgcooh-peg-plga溶于4.5ml磷酸盐缓冲液(pbs)中,120w超声浴5分钟溶解,将ae@zif-8溶液与peg-plga溶液按7:3比例混合,室温条件下避光磁力搅拌4分钟,250转/分钟。得ae@zif-8/peg-plga溶液,离心,12000转/分离心10分钟,甲醇重悬洗涤两次,得7mlae@zif-8/peg-plga悬液。
79.将ae@zif-8/peg-plga悬液逐滴加入1mg/ml的1-乙基-(3-二甲基氨基丙基)碳酰二亚胺(edc)、1mg/ml的n-羟基丁二酰亚胺(nhs)各250μl,室温条件下磁力搅拌4小时,250转/分钟。逐滴加入1mg/ml的转铁蛋白水溶液,避光继续搅拌2小时,4℃静置过夜。12000转/分离心10分钟,取沉淀得终产物ae@zif-8/tf-peg-plga,再次用甲醇重悬,12000转/分离心10分钟,重复两次。用75%乙醇重悬,浸泡30分钟,离心,沉淀用包含1%泊洛沙姆的生理盐水洗涤两次。
80.实验例1、性能测定
81.对实施例1和实施例2制备得到的覆盖tf-peg-plga涂层的载药zif-8纳米粒进行性能测定,纳米粒透射电镜的结构、纳米粒粒度、纳米粒表面ζ电位的测定;
82.纳米粒透射电镜外观图如图3所示,表明zif-8、ae@zif-8等到成功的制备,tf-peg-plga涂层成功附着于纳米粒表面。
83.纳米粒粒度图如图4所示,表明所制备的纳米粒粒径均一,可用于颅内药物递送。
84.纳米粒表面ζ电位图如图5所示,表明所制备的纳米粒均呈弱负电荷,有利于跨血脑屏障转运。
85.纳米粒紫外吸收图谱如图6所示,根据所形成的ae紫外吸收峰(255nm),表明ae成功包封于zif-8及tf-peg-plga/zif-8纳米粒。
86.纳米粒肿瘤微环境释放性能示意图如图7所示,纳米粒在肿瘤ph微环境(ph=5.5)中得到释放,而在中性环境中保持稳定。
87.纳米粒血脑屏障穿透性及肿瘤靶向性示意图如图8所示,相较于空白药物组,纳米
组在颅内有更高的分布,且可在肿瘤组织中富集,表明纳米粒具有血脑屏障穿透能力及肿瘤靶向能力。
88.最后,还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
89.尽管已描述了本发明的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。
90.显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1