一种铁死亡抑制剂在制备治疗胃炎的药物中的应用
1.本发明属于医药技术领域,具体涉及一种铁死亡抑制剂在制备治疗胃炎的药物中的应用。
背景技术:
2.慢性萎缩性胃炎(chronic atrophic gastritis,cag)是一种“炎症
→
萎缩
→
化生(metaplasia)
→
异型增生”为突出病理特征的胃癌癌前病变,与肠型胃癌(intestinal gc)发生密切相关。其中,化生作为cag病理进程的重要节点,是肠型胃癌早期防控关键,但形成机制并不完全清楚。因此,有关化生形成病因与机制研究,对肠型胃癌早期防控具有重要意义。
3.中国专利文献cn113940309a公开了课题组一种模拟度高、稳定持久、具有特定表型的、高效的慢性萎缩性胃炎病变的模拟方法:将基因编辑小鼠grim-19flox/flox与atp4b-cre基因编辑小鼠杂交,获得胃黏膜特异性壁细胞grim-19敲除小鼠品系(grim-19-/-/atp4b-cre,spf级),该基因敲除小鼠在8月龄具有慢性萎缩性胃炎肠上皮化生早期病变即自发性解痉多肽表达化生(spasmolytic polypeptide expressing metaplasia,spem),且能够稳定表达,不会反复,可作为小鼠慢性萎缩性胃炎病理模型研究。
4.铁死亡(ferroptosis),又称铁依赖性死亡,作为一种不同于细胞凋亡、坏死和自噬的新型调节性细胞死亡形式,与多种疾病密切相关如神经退行性变、肿瘤、缺血再灌注损伤、肾脏损伤以及肝纤维化等。铁死亡以胞内脂质过氧化物集聚为典型特征,其中胞内过量fe
2+
经fenton反应导致抗氧化谷胱甘肽(gsh)耗竭与谷胱甘肽过氧化物酶4(gpx4)失活,进而诱导脂质过氧化物积聚从而引起铁死亡。
5.ferrostain-1是目前公认的铁死亡抑制剂,是一种人工合成的通过还原机制来防止膜脂的损伤从而抑制细胞死亡的抗氧化剂。中国专利文献cn111529518a公开了铁死亡抑制剂ferrostatin-1明显改善了淹溺引起的小鼠肺损伤和细胞损伤,对淹溺导致的肺损伤具有显著的保护作用;中国专利文献cn113440509a公开了铁死亡抑制剂ferrostatin-1明显提高了细胞内gpx4的含量,显著抑制了磨损颗粒刺激成骨细胞内ros的生成,减少了成骨细胞铁死亡,且体内实验ferrostatin-1腹腔注射对磨损颗粒所诱导的骨溶解存在显著的抑制效应。但目前尚无铁死亡抑制剂及其衍生物在慢性萎缩性胃炎方面作用中的报道。
技术实现要素:
6.针对现有技术中的上述不足,本发明提供了一种铁死亡抑制剂在制备治疗胃炎的药物中的新用途,本发明首次发现了grim-19缺失诱导人胃黏膜上皮细胞增殖减慢、活力降低的机制为铁死亡,而非凋亡、坏死、自噬等其他死亡形式。
7.本发明的目的在于提供铁死亡抑制剂ferrostatin-1可作为grim-19缺失为特征的慢性萎缩胃炎疾病的治疗靶点,ferrostatin-1可通过提高胃黏膜组织gpx4水平,特异性催化谷胱甘肽将脂质过氧化物转化为类脂醇的硒蛋白,将铁死亡发生进程中的毒性产物清
除,从而进一步抑制铁死亡的发生。此外,ferrostatin-1能明显减少小鼠胃黏膜壁细胞grim-19缺失引起的胃黏膜组织炎症细胞和炎症因子浸润,spem指标降低,有效抑制慢性萎缩性胃炎的病理进程,为慢性萎缩性胃炎药物研发和创新提供新思路。
8.为实现上述目的,本发明解决其技术问题所采用的技术方案是:
9.铁死亡抑制剂在制备治疗胃炎的药物中的应用。
10.进一步地,铁死亡抑制剂以ferrostatin-1为活性成分,辅以其药学上可以接受的载体、赋形剂、稀释剂、辅剂、媒介物或其组合。
11.进一步地,铁死亡抑制剂中的活性成分为ferrostatin-1衍生物、异构体或药学上可接受的盐。
12.进一步地,胃炎为慢性萎缩性胃炎。
13.进一步地,慢性萎缩性胃炎为由grim-19基因缺陷诱导引发的慢性萎缩性胃炎。
14.进一步地,铁死亡抑制剂可抑制spem基因的表达。
15.进一步地,铁死亡抑制剂可提高慢性萎缩性胃炎模型中铁死亡标志蛋白谷胱甘肽过氧化物酶4(gpx4)水平。
16.进一步地,铁死亡抑制剂可减少慢性萎缩性胃炎模型中小鼠胃黏膜组织l-6、tnf-α、vegf、gm-csf、il-1β、il-33等炎症因子的表达。
17.进一步地,铁死亡抑制剂可保护胃黏膜组织。
18.进一步地,药物为片剂、栓剂、注射剂或胶囊剂。
19.进一步地,药物为注射剂,采用腹腔注射给药,给药剂量为1~1.5mg/kg。
20.本发明的有益效果:
21.本发明发现铁死亡抑制剂ferrostatin-1体内注射可明显提高小鼠胃黏膜组织gpx4水平,抑制胃黏膜壁细胞铁死亡病理进程,从而有效减少了小鼠胃黏膜组织l-6、tnf-α、vegf、gm-csf、il-1β、il-33等炎症因子的表达,spem指标显著降低,有效抑制了慢性萎缩性胃炎病理进程,可用于慢性萎缩性胃炎的治疗。ferrostatin-1体外处理ges-1-134细胞,可提高细胞gpx4水平,抑制铁死亡病理进程,从而增强细胞活力。体内外实验证实铁死亡抑制剂ferrostatin-1可用于慢性萎缩性胃炎的治疗,可为慢性萎缩性胃炎药物研发和创新提供新思路。
附图说明
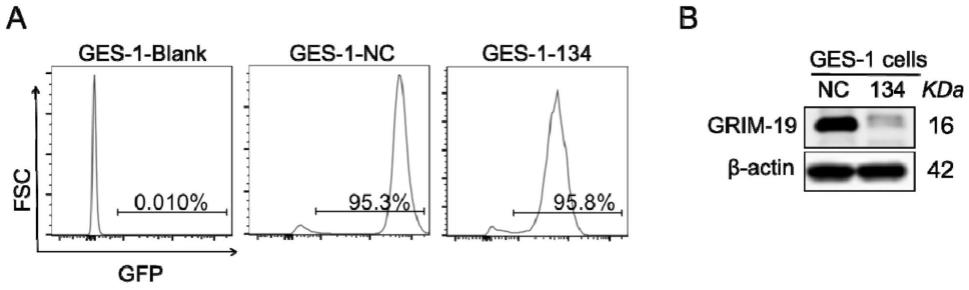
22.图1为grim-19敲除人胃黏膜上皮ges-1细胞(ges-1-134)单克隆构建图;其中,a为单克隆流式细胞仪gfp阳性检测图;b为蛋白免疫印迹检测ges-1-134细胞grim-19蛋白表达分析;
23.图2为ges-1-134细胞活力检测结果;
24.图3为ges-1-134细胞凋亡、坏死与自噬检测;其中,a为流式检测ges-1-134细胞凋亡与坏死情况;b为蛋白免疫印迹检测ges-1-134细胞自噬标志物lc3i/lc3ii蛋白表达分析;
25.图4为ges-1-134细胞和grim-19-/-小鼠胃黏膜组织铁死亡标志蛋白检测;其中,a为蛋白免疫印迹检测ges-1-134细胞铁死亡标志蛋白(cox2、gpx4、fth1、tfr)表达水平;b为蛋白免疫印迹检测grim-19-/-小鼠胃黏膜组织铁死亡标志蛋白(cox2、gpx4、fth1、tfr)表达
水平;
26.图5为ges-1-134细胞和grim-19-/-小鼠胃黏膜组织透射电镜图;其中,a为ges-1-134细胞线粒体表型透射电镜分析;b为grim-19-/-小鼠胃黏膜组织线粒体表型透射电镜分析;
27.图6为ges-1-134细胞和grim-19-/-小鼠胃黏膜组织铁离子检测;其中,a为ges-1-134细胞fe
2+
含量检测;b为grim-19-/-小鼠胃黏膜组织普鲁士蓝染色(*<0.05);
28.图7为ges-1-134细胞脂质氧化(mda)检测(***<0.001);
29.图8为铁死亡抑制剂ferrostatin-1干预后ges-1-134细胞活力检测(***<0.001);
30.图9为铁死亡抑制剂ferrostatin-1干预后ges-1-134细胞和grim-19-/-小鼠胃黏膜组织铁死亡标志物蛋白检测;其中,a为蛋白免疫印迹检测铁死亡抑制剂ferrostatin-1(0、5μm、10μm)处理ges-1-134细胞铁死亡标志蛋白(cox2、gpx4、fth1、tfr)表达水平;b为蛋白免疫印迹检测铁死亡抑制剂ferrostatin-1干预grim-19-/-小鼠胃黏膜组织铁死亡标志蛋白(cox2、gpx4、fth1、tfr)表达水平;
31.图10为铁死亡抑制剂ferrostatin-1干预后ges-1-134细胞和grim-19-/-小鼠胃黏膜组织炎症因子表达检测;其中,a为蛋白免疫印迹检测ferrostatin-1干预后ges-1-134细胞il-6、tnf-α、vegf、gm-csf、il-1β、il-33蛋白表达水平;b为蛋白免疫印迹检测剂ferrostatin-1干预后grim-19-/-小鼠胃黏膜组织il-6、tnf-α、vegf、gm-csf、il-1β、il-33蛋白表达水平;
32.图11为铁死亡抑制剂ferrostatin-1干预后grim-19-/-小鼠胃黏膜组织spem病理进程检测分析;其中,a为蛋白免疫印迹检测胃黏膜组织spem标志物tff2、mist1、clusterin-1、he4、muc6蛋白水平;b为免疫荧光检测gif、gsii及mist免疫荧光三标分析(bar:50μm)(***<0.001)。
33.具体实施例方式
34.下面对本发明的具体实施例方式进行描述,以便于本技术领域的技术人员理解本发明,但应该清楚,本发明不限于具体实施例方式的范围,对本技术领域的普通技术人员来讲,只要各种变化在所附的权利要求限定和确定的本发明的精神和范围内,这些变化是显而易见的,一切利用本发明构思的发明创造均在保护之列。
35.实施例1体外构建ges-1-134细胞模型
36.1、慢病毒载体系统构建
37.本发明采用的是上海吉凯基因技术有限公司crispr/cas9单载体慢病毒系统
38.(1)gv393慢病毒的框架结构为u6-sgrna-eifla-cas9-flag-p2a-egfp;
39.(2)目的基因信息:
40.目的基因名称基因物种基因idgenbank idndufa13(grim-19)human51079nm_015965
41.(3)目的sgrna引物序列:
42.ndufa-13-sgrna-134-fcaccgtgctccagtgcccgtagatc/ndufa-13-sgrna-134-raaacgatctacgggcactggagcacnc-sgrna-fcaccgcgcttccgcggcccgttcaa/
nc-sgrna-raaacttgaacgggccgcggaagcgc
43.2、ges-1(人正常胃黏膜上皮细胞)感染
44.(1)将ges-1细胞按照1000个细胞/孔接种96孔板;
45.(2)细胞生长密度达30-40%左右时感染;
46.①
感染前,使用完全培养基1:25稀释hitransg p感染增强液,备用;
47.②
按照moi=50计算病毒使用量;
48.③
37
③
、5%co2培养箱培养,感染8-16小时左右观察细胞形态换液;
49.④
感染72小时,显微镜下观察感染效果。
50.3、流式细胞术分选细胞
51.应用流式细胞仪分选gfp阳性细胞,将阳性细胞稀释成单个细胞,进行单克隆增殖,即可获得获得高纯度gfp阳性细胞,如图1a所示。
52.4、免疫蛋白印迹检测grim-19表达分析,具体过程如下:
53.(1)用ripa裂解液(碧云天)冰上裂解细胞30min以上;
54.(2)12000rpm/10min,收集上清;
55.(3)加入对应体积sds-page蛋白上样缓冲液,金属浴100
③
/10min;
56.(4)sds-page电泳;
57.(5)室温封闭30min;
58.(6)敷一抗,4
③
孵育摇床过夜;
59.(7)洗膜,tbst清洗三次,每次10min;
60.(8)敷二抗,室温摇床孵育1小时;
61.(9)洗膜,tbst清洗三次,每次10min;
62.(10)显影。
63.如图1b所示ges-1-134grim-19蛋白水平相比于对照明显减少,提示人正常胃黏膜细胞ges-1grim-19敲除模型构建成功。
64.实施例2ges-1-134细胞增值检测活力分析
65.利用cck-8试剂盒(索莱宝)分析ges-1-nc和ges-1-134细胞增殖活力变化,具体过程如下:
66.(1)5000个细胞/孔接种于96孔板;
67.(2)37
③
、5%co2分别培养24、48、72小时;
68.(3)检测时向每孔加入10ulcck-8溶液;
69.(4)将培养板在培养箱内孵育1小时;
70.(5)酶标仪测定450nm处吸光度。
71.结果如图2所示,ges-1-134与对照相比细胞增殖速度减慢,活力降低。
72.实施例3ges-1-134细胞凋亡分析
73.利用凋亡试剂盒分析ges-1-134凋亡,具体过程如下:
74.(1)收集5
×
105细胞;
75.(2)pbs漂洗两次(2000rpm/5min);
76.(3)binding buffer:7-aad=10:1,加入50μl染液、混匀、避光反应15min;
77.(4)binding buffer:annexin v-pe=450:1,加入450μl染液、混匀、避光反应
15min;
78.(5)1小时内流式细胞仪检测。
79.结果如图3a所示,相比于对照ges-1-nc,ges-1-134凋亡分析无明显差别,证明grim-19缺失诱导胃黏膜上皮细胞速度减慢,活力降低方式并非凋亡。
80.实施例4ges-1-134细胞自噬分析
81.利用蛋白免疫印迹方法检测ges-1-134自噬标志蛋白lc3i和lc3ii的表达水平。如图3b所示ges-1-134相比于对照组自噬标志物lc3i和lc3ii无增加趋势,证实grim-19缺失诱导胃黏膜上皮细胞增殖减慢、活性降低方式并非自噬。
82.实施例5ges-1-134细胞和grim-19-/-小鼠胃黏膜组织铁死亡标志物表达分析
83.利用蛋白免疫印迹检测ges-1-134细胞和grim-19-/-小鼠胃黏膜组织中铁死亡相关标志蛋白的表达。结果如图4a所示。
84.与ges-1-nc细胞相比,ges-1-134细胞谷胱甘肽过氧化物酶4(gpx4)、铁蛋白(fth1)下降,环氧合酶(cox-2)、转铁蛋白受体(tfr)升高,这提示grim-19在人正常胃黏膜上皮细胞被敲除后,fe
2+
过载、脂质过氧化物清除能力减弱,铁死亡发生。同样在小鼠胃黏膜组织中,图4b所示grim-19
fl/-、grim-19-/-小鼠胃黏膜组织相比于对照组铁死亡标志蛋白与体外有同样的趋势,这提示小鼠胃黏膜壁细胞grim-19缺失诱导壁细胞受损的机制为铁死亡。
85.实施例6ges-1-134细胞和grim-19-/-小鼠胃黏膜组织电镜分析
86.利用透射电镜分析技术检测grim-19-/-小鼠胃黏膜组织和ges-1-134细胞线粒体结构变化,具体过程如下:
87.(1)将新鲜组织切成1mm3大小,立马加入电镜固定液,4
③
冰箱保存(可存放3-6个月)择期送电镜室检测;
88.(2)细胞消化1
×
106,1200rpm/10min,形成ep管底部紧密的细胞团快,吸净上清液,沿管壁轻轻加入固定液(请勿破坏样品团块),4
③
冰箱保存(可存放3-6个月)择期送电镜室检测。
89.透射电镜分析技术分析如图5a所示,与ges-1-nc相比,ges-1-134细胞内线粒体结构和数量有明显改变:数目减少、膜密度增加、嵴减少,而这些符合细胞铁死亡形态学特征;图5b与对照鼠相比,grim-19-/-小鼠胃黏膜组织细胞线粒体结构有相似改变:线粒体膜密度增加、嵴减少且出现结构紊乱的板状嵴。以上体内外透射电镜分析证实了了grim-19缺失诱导人胃黏膜上皮细胞和小鼠胃黏膜壁细胞线粒体发生铁死亡形态学改变。
90.实施例7ges-1-134细胞亚铁离子检测分析
91.胞内过量fe2+经fenton反应导致抗氧化谷胱甘肽(gsh)耗竭与谷胱甘肽过氧化物酶4(gpx4)失活,进而诱导脂质过氧化物积聚从而引起铁死亡。利用亚铁离子比色法试剂盒(elabscience)检测ges-1-34细胞fe
2+
含量,具体过程如下:
92.(1)收集4-6
×
106个细胞;
93.(2)加入试剂一进行匀浆;
94.(3)1000g/10min,取上清备用;
95.(4)加入试剂二,37
③
孵育10min;
96.(5)12000g/10min,取上清备用;
97.(6)酶标仪532nm测定od值。
98.结果如图6a所示,ges-1-134细胞fe
2+
增多,提示grim-19敲除诱导胃黏膜上皮细胞fe
2+
增多,后续fe
2+
可经fenton反应促进铁死亡的发生。
99.实施例8grim-19-/-小鼠胃黏膜组织普鲁士蓝铁离子检测分析
100.利用普鲁士蓝试剂盒(索莱宝)检测小鼠胃黏膜组织铁离子表达情况,具体过程如下:
101.(1)组织固定;
102.(2)常规脱水包埋;
103.(3)切片烤片;
104.(4)滴染perls染色工作液15min;
105.(5)蒸馏水洗5min;
106.(6)滴染核固红液10min;
107.(7)自来水洗;
108.(8)常规脱水透明;
109.(9)中性树脂封片。
110.结果如图6b所示,与对照组相比grim-19-/-小鼠胃黏膜组织铁离子明显增多,提示胃黏膜组织铁离子过载进一步加剧铁死亡的发生。
111.实施例9ges-1-134细胞脂质氧化(mda)检测分析
112.动物或植物细胞发生氧化应激(oxidative stress)时,会发生脂质氧化。利用脂质氧化(mda)检测试剂盒(碧云天),分析ges-1-134和小鼠胃黏膜组织脂质氧化水平,具体过程如下:
113.(1)取1
×
106细胞裂解;
114.(2)10000g/10min收集上清;
115.(3)加入0.1ml mda工作液,100
③
金属浴15min;
116.(4)1000g/10min,收集上清;
117.(5)酶标仪532nm测定吸光度。
118.结果如图7所示,与对照图相比ges-1-134细胞mda显著上升,提示grim-19敲除引起人胃黏膜上皮细胞mda增加,进一步促进铁死亡的发生。实施例10ferrostatin-1干预ges-1-134细胞增殖活力检测分析
119.利用cck-8试剂盒分析铁死亡抑制剂ferrostatin-1干预ges-1-134细胞增殖活力变化。结果如图8所示,铁死亡抑制剂ferrostatin-1干预ges-1-134细胞后增殖能力提高、活力恢复。
120.实施例11ferrostatin-1干预ges-1-134细胞和grim-19-/-小鼠铁死亡标志物表达分析
121.利用蛋白免疫印迹检测ferrostatin-1干预ges-1-134细胞和grim-19-/-小鼠胃黏膜组织铁死亡标志物表达分析。
122.铁死亡抑制剂ferrostatin-1处理ges-1-134细胞后,如图9a所示铁死亡标志蛋白gpx4、fth1上升、cox-2、tfr下降,提示ferrostatin-1有效抑制了grim-19敲除人胃黏膜上皮ges-1细胞铁死亡病理进程。体内实验ferrostatin-1注射grim-19-/-小鼠,如图9b所示
gpx4、fth1、cox-2、tfr有相同的变化趋势,以上体内外实验证实铁铁死亡抑制剂ferrostatin-1有效抑制了grim-19缺陷诱导胃黏膜细胞铁死亡病理进程。
123.实施例12ferrostatin-1干预ges-1-134细胞和grim-19-/-小鼠炎症因子表达分析
124.利用白免疫印迹技术检测铁死亡抑制剂ferrostatin-1干预ges-1-134细胞和grim-19-/-小鼠后其炎症因子的表达情况。
125.结果如图10所示,铁死亡抑制剂ferrostatin-1体外干预ges-1-134细胞后,炎症因子il-6、tnf-α、vegf、gm-csf、il-1β、il-33显著降低;体内实验证明与pbs注射对照相比,fer-1组炎症因子il-6、tnf-α等也明显降低,以上提示体内外实验证实了铁死亡抑制剂ferrostatin-1能够减少grim-19敲除人胃黏膜上皮细胞和壁细胞特异性grim-19敲除小鼠胃黏膜组炎症因子的表达,有效减缓胃黏膜组织炎症反应,抑制慢性萎缩性胃炎病理进程。
126.实施例13ferrostatin-1干预grim-19-/-小鼠胃黏膜组织spem标志物分析
127.利用蛋白免疫印迹技术检测铁死亡抑制剂ferrostatin-1腹腔注射grim-19-/-小鼠后,胃黏膜组织spem标志物的表达情况。
128.结果如图11a所示,与pbs注射对照相比,铁死亡抑制剂ferrostatin-1组,tff2、mist1、clusterin-1、he4、muc6的表达明显减弱,这提示铁死亡抑制剂ferrostatin-1能够有效抑制grim-19-/-小鼠慢性萎缩性胃炎spem病理进程。实施例14ferrostatin-1干预grim-19-/-小鼠胃黏膜组织spem标志物gif/gsii/mist1共定位分析
129.运用免疫荧光技术检测铁死亡抑制剂ferrostatin-1腹腔注射小鼠后,胃黏膜组织spem标志物gif、gsii、mist1阳性共定位表达分析,具体过程如下:
130.(1)oct包埋组织;
131.(2)切片;
132.(3)4%pfa固定;
133.(4)血清封闭;
134.(5)4
③
过夜孵育一抗;
135.(6)pbs漂洗三次;
136.(7)室温孵育二抗2小时;
137.(8)pbs漂洗三次;
138.(9)dapi复染10min;
139.(10)pbs漂洗三次;
140.(11)抗荧光衰弱剂封片。
141.结果如图11b所示,与pbs组相比,fer-1,gif
+
、gsii
+
、mist1
+
组阳性细胞数明显减少,gif
+
/gsⅱ+
和gif
+
/mist1+双阳性、gif
+
/gsii
+
/mist1
+
三阳性细胞数量均增少,提示铁死亡抑制剂ferrostatin-1能够有效抑制慢性萎缩性胃炎spem病理进程。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1