一种甘草酸胶束水凝胶递送系统及其制备方法和应用
1.本发明涉及医药食品材料技术,具体涉及一种甘草酸胶束水凝胶递送系统及其制备方法和应用。
背景技术:
2.目前,临床上部分药物和天然产物溶解性低,稳定性差,生物利用率低,从而导致治疗效果不佳,甚至引发严重的毒副作用。因此,寻找高效,低毒的递送系统具有显著的临床意义。为了解决上述一系列问题,研究人员开发了很多递送系统例如纳米粒子,胶束,囊泡,脂质体,水凝胶等。其中,囊泡,胶束,脂质体由于具有特殊的核壳结构能够有效地包埋疏水性化合物,但是这些体系通常不稳定,容易聚集,而且进入血液后容易泄露药物,因此阻碍了其临床应用。水凝胶由三维网络封存大量的水组成,具有好的生物相容性,高的载药率,可控的持续释放行为和可调节的机械性能,受到了研究者的广泛关注。然而,由于水凝胶是亲水性的,疏水性药物和水凝胶不相溶,它容易聚集或沉淀在水凝胶里,这样会导致水凝胶的可注射性,力学性能和稳定性下降,同时现有的凝胶大部分是基于聚合物制备的,对于合成的聚合物,大部分是难降解或降解慢的,这可能会导致一些系统毒性,且天然的聚合物大部分是亲水性的,通常需要化学修饰,这会导致制备成本增加。因此,开发一种简单,通用,有效和生物相容性好的混合体系的递送系统具有重要的意义。
技术实现要素:
3.本发明提供了一种甘草酸胶束水凝胶递送系统及其制备方法和应用,用以解决目前现有水凝胶材料对疏水性化合物相容性差所导致的性能和稳定性下降的技术问题以及现有水凝胶材料的毒性和成本问题。
4.为解决上述技术问题,本发明采用以下技术方案:
5.一种甘草酸胶束水凝胶递送系统的制备方法,包括以下步骤:
6.(1)将疏水性化合物和/或亲水性化合物与甘草酸溶解于溶剂中,得到混合溶液;
7.(2)将所述混合溶液蒸发去除溶剂,得到薄膜;向所述薄膜中添加水或pbs溶液,于超声条件下水化,得到胶束溶液;
8.(3)对所述胶束溶液进行加热,冷却后即得所述甘草酸胶束水凝胶递送系统。
9.上述技术方案的设计思路在于,本技术通过自组装的胶束水凝胶构成了疏水性化合物的递送系统,结合了胶束和水凝胶的优点,它不仅能够自发地去封装疏水性药物在疏水核和结合亲水性药物在亲水壳,还具备了水凝胶的优势,在可控地持续释放药物和可调节的机械性能以匹配周围的组织的同时,还表现出了很好的可注射性、自愈合能力和良好的生物相容性。同时本技术采用甘草酸自发地组装成胶束去封装疏水性化合物,一方面避免了现有技术采用聚合物制备凝胶所带来的毒性问题,通过甘草酸疏水的五环三萜结构和亲水的双葡萄糖醛酸结构即可实现胶束的自发组装,无需进行改性,节约了递送体系的制备成本,另一方面甘草酸本身也具有药物属性和药理活性,可辅助发挥药物效果,甚至与包
载的药物和化合物形成协同作用,提高药效(比如利用甘草酸递送系统递送黄岑素);本发明的制备方法简单,条件温和,原料易得,适于大规模产业化的生产。
10.作为上述技术方案的进一步优选,步骤(1)中所述甘草酸与疏水性化合物的质量比为(1~20):1。甘草酸与疏水性化合物的添加量比例是能否形成胶束溶液的重要参数之一,二者质量比过低或过高都将导致难以胶束溶液。
11.作为上述技术方案的进一步优选,步骤(1)中所述溶剂包括甲醇、乙醇、丙酮、氯仿和四氢呋喃中的至少一种,进一步优选为甲醇。上述几种溶剂对体系内化合物溶解性好,且价格较低、易于获得,利于制备成本的控制。作为上述技术方案的进一步优选,步骤(2)中采用旋蒸工艺除去所述混合溶液中的溶剂,旋蒸工艺的温度为37~60℃,转速为60~150rpm。
12.作为上述技术方案的进一步优选,步骤(2)中所述pbs溶液的浓度为0.001~0.1m,ph值为7.0~9.0。ph的高低也是能否形成胶束溶液的重要参数之一,过低或过高都将导致难以胶束溶液。
13.作为上述技术方案的进一步优选,步骤(2)中所述水化操作在25~40℃下进行超声处理,超声处理的功率为100~600w,超声处理的时间为20~40min。
14.作为上述技术方案的进一步优选,步骤(3)中所述胶束溶液的加热温度为45~70℃;加热后的冷却时间为20~60min。温度是能否形成凝胶的重要参数之一,低于45℃不能生成凝胶,温度高于70℃会破坏胶束,导致内载的化合物泄露。
15.作为上述技术方案的进一步优选,步骤(2)中得到所述胶束溶液后,对所述胶束溶液采用滤膜进行过滤,所述滤膜的孔径为0.22μm。过滤可除去胶束溶液中未被胶束包裹的疏水性化合物。
16.作为上述技术方案的进一步优选,所述疏水性化合物包括姜黄素、白藜芦醇、槲皮素、黄岑素,大黄酸、大黄素、紫杉醇、地塞米松、喜树碱、维生素和β-胡萝卜素中的至少一种;所述亲水性化合物包括多糖类、氨基酸类、蛋白类、多肽类、水溶性多酚类、糖苷类和核苷酸类化合物中的至少一种。
17.基于同一技术构思,本发明还提供一种甘草酸胶束水凝胶递送系统,由上述制备方法制得。
18.基于同一技术构思,本发明还提供一种上述甘草酸胶束水凝胶递送系统的应用,所述甘草酸胶束水凝胶递送系统用于体内疏水性活性物质和/或亲水性活性物质的递送。
19.与现有技术相比,本发明的优点在于:
20.本发明的递送系统,可应用于体内疏水性活性物质、亲/疏水性复合活性物质的递送,结合了胶束和水凝胶的优点,在可控地持续释放药物和可调节的机械性能以匹配周围的组织的同时,还表现出了很好的可注射性、自愈合能力和良好的生物相容性,避免了现有技术采用聚合物制备凝胶所带来的毒性问题,无需进行改性,节约了递送体系的制备成本,还可辅助发挥药物效果,且水凝胶体系稳定,可长时间保存;本发明的递送系统制备方法简单,条件温和,原料易得,适于大规模产业化的生产。
附图说明
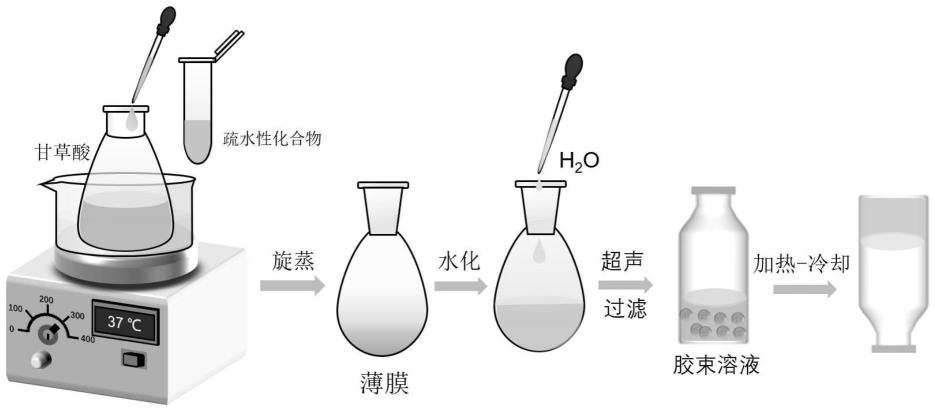
21.图1为实施例1的甘草酸胶束水凝胶递送系统的制备流程图;
22.图2为实施例1采用甘草酸与不同疏水药物形成的胶束溶液的外观形貌图;
23.图3为实施例1的甘草酸@姜黄素胶束水凝胶及中间转化态的微观形貌图;
24.图4为实施例1的甘草酸@姜黄素胶束水凝胶的粘度与剪切变稀曲线(图中左侧a)以及水凝胶的储能模量和耗损模量变化图(图中右侧b);
25.图5为实施例1的甘草酸@姜黄素胶束水凝胶的药物累计释放曲线;
26.图6为实施例1的甘草酸@姜黄素胶束水凝胶储存稳定性测试图。
具体实施方式
27.以下结合具体实施例对本发明作进一步详细说明。
28.实施例1:
29.本实施例的甘草酸胶束水凝胶递送系统可用于体内疏水性活性物质的递送,由以下制备方法制得,制备流程如图1所示,包括以下步骤:
30.(1)分别称取10mg姜黄素、白藜芦醇、槲皮素、维生素d和β-胡萝卜素放置于不同的圆底烧瓶中,分别加入50mg的甘草酸和100ml甲醇溶液于37℃下搅拌使其完全溶解的到混合溶液;
31.(2)将混合溶液放置于旋转蒸发仪上旋蒸除去甲醇溶剂,温度设置为37℃,转速为70rpm,溶剂去除后得到一层均匀的薄膜。随后加入5ml水,并置于超声仪中超声水化30min,并用0.22μm的滤膜过滤除去未包载的疏水化合物,得到甘草酸@疏水药物的胶束溶液,不同负载药物所形成的胶束溶液形貌如图2所示;
32.(3)将所得到的甘草酸@疏水药物的胶束溶液于60℃下加热冷却后得到甘草酸@疏水药物胶束水凝胶。
33.对本实施例所得到的甘草酸@疏水药物胶束水凝胶中的甘草酸@姜黄素胶束水凝胶进行流变性能和自修复性能测试,通过测试水凝胶的储能模量(g
′
)和耗损模量(g
″
)变化来检测样品的状态,当g
′
>g
″
时,为凝胶状态;当g
′
<g
″
时,为溶液状态,具体步骤为:将制备得到的甘草酸@姜黄素胶束水凝胶放到流变仪上,设置实验参数,实验中温度设置为25℃,使用的平行板直径为50mm,间隙设为0.1mm。黏度-剪切速率扫描:频率为10rad
·
s-1
,剪切速率为0.1~101/s。循环应变扫描:实验分为三个阶段:第一阶段在低应力下,设置应力为1%,时间为120s;第二阶段在高应力下,设置应力为50%,时间保持120s;第三阶段从高应力变到低应力下,应力为1%,时间保持120s,观察每个阶段g
′
和g
″
的变化情况。结果如图4所示,由图可知,粘度与剪切变稀曲线表现出该凝胶随着剪切速率的增大,粘度降低,这表明甘草酸@姜黄素胶束水凝胶具有很好的剪切变稀性能;时间应变扫描显示,第一阶段,在低应力1%下,储能模量(g
′
)一直高于耗损模量(g
″
),表面样品是凝胶状态;第二阶段,当应力加大到50%时,储能模量(g
′
)一直小于耗损模量(g
″
),表面样品处于溶液状态:第三阶段,当从高应力变到低应力时,储能模量(g
′
)大于耗损模量(g
″
),这表明当应力减小时,样品从溶液状态变回凝胶状态。以上试验表明甘草酸@姜黄素胶束水凝胶具有很好的剪切变稀以及自修复能力。
34.对本实施例所得到的甘草酸@疏水药物胶束水凝胶中的甘草酸@姜黄素胶束水凝胶进行了体外药物缓释能力测试,除本实施例的甘草酸@姜黄素胶束水凝胶(甘草酸浓度为1.0wt%),还增加了两组甘草酸浓度为2.0wt%、3.0wt%的甘草酸@姜黄素胶束水凝胶(也即在制备过程中添加的甘草酸分别为100mg和150mg),具体测试方法为:在离心管中分别加
入0.6ml浓度为1.0wt%、2.0wt%和3.0wt%的甘草酸@疏水药物胶束水凝胶,然后在凝胶上面加入0.6ml的pbs缓冲溶液(0.01m,ph=7.4),置于37℃恒温水浴摇床中;在不同时间点,取出0.3ml的上层溶液,同时补加0.3ml等温的新鲜pbs溶液;然后用紫外吸收光谱检测药物的吸光度,计算的药物累计释放量,并绘制药物累计释放曲线。结果如图5所示,由图可知,所有的甘草酸@疏水药物胶束水凝胶都具有长效缓释的能力,能够缓慢释放7天以上,甘草酸浓度为1.0wt%,在前60h内释放速率相对比较快,后面释放速度相对缓慢均匀。另外两个浓度的凝胶都表现出相对较慢的释放速率。另外,随着甘草酸的浓度增大,释放速率减慢,缓释时间越长。这是因为随着甘草酸的浓度增大,自组装形成的纳米纤维网络越紧密,缓释速率就越慢。
35.对本实施例所得到的甘草酸@疏水药物胶束水凝胶中的甘草酸@姜黄素胶束水凝胶的稳定性进行了测试,结果如图6所示,结果显示,本发明的递送系统具有良好的稳定性,可长时保存至少六个月。
36.本实施例还进一步研究了甘草酸@姜黄素胶束水凝胶及中间转化态的微观形貌,设置了三组实验,三组实验的区别在于制备过程中步骤(2)中水化反应添加的水分别为5ml、50ml和100ml,实验结果如图3所示,由图可知,当甘草酸的浓度大于临界胶束浓度时,甘草酸能够在水中自组装去封装疏水性药物形成球形胶束。然后随着浓度的增大,胶束进一步自组装形成微凝胶,当甘草酸浓度高于0.5wt%时,胶束自组装成水凝胶。
37.以上所述仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例。对于本技术领域的技术人员来说,在不脱离本发明技术构思前提下所得到的改进和变换也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1