一种利用声信号进行组织分类的激光消融系统
1.本发明属于医疗器械相关技术领域,更具体地,涉及一种利用声信号进行组织分类的激光消融系统。
背景技术:
2.紫外光在消融病理组织的过程中,可以被生物物质和有机化合物充分吸收,其原理之一为光化学机制,即355nm光子的能量大于病理组织的分子键的结合能,最终导致分子键解离;其二是光热机制,光子被血液中的细胞大分子吸收,这种振动导致的产热比水的蒸发温度更大,最终爆炸成气相,产生的热能导致动脉粥样硬化中的胶原蛋白和蛋白质纤维软化;其三是光机械机制,蒸汽泡的快速膨胀和内爆导致导管尖端前方斑块的机械破裂,穿透较浅。
3.常见的高能量低重频的消融系统虽然可对病理组织有效消融,但其产生的高能量容易导致血管穿孔并发症的发生,且不具备实时消融时对组织分类辨别的能力以及针对不同生物组织通过自身的反馈—控制调节激光能量和脉冲频率的能力,因此需要一种能够识别病理组织并且能针对病理组织进行消融的系统,以此减少血管穿孔的风险。
技术实现要素:
4.针对现有技术的以上缺陷或改进需求,本发明提供了一种利用声信号进行组织分类的激光消融系统,解决激光消融过程中血管穿孔以及风险高的问题。
5.为实现上述目的,按照本发明的一个方面,提供了一种利用声信号进行组织分类的激光消融系统,该激光消融系统包括、消融导管、消融导丝、声波信号分析单元、激光控制单元、激光器和耦合单元,其中:
6.所述消融导管呈中空状,所述消融导丝设置在所述消融导管中且突出于所述消融导管,其先于所述消融导管与待检测组织进行接触,在与待检测组织接触后收集该待检测组织的声波信号,并将该声波信号传递给所述声波信号分析单元;
7.所述声波信号分析单元在收到所述消融导丝传递的声波信号后进行分析,以此判断所述待检测组织是否为病理组织,然后将判断结果反馈给所述激光控制单元;所述激光控制单元根据反馈的判断结果调控所述激光器发射激光的能量;
8.所述耦合单元用于将所述激光器发射的激光进行聚集并将激光的能量传递给所述消融导管,该消融导管传输激光并将激光能量作用在病理组织上,以此对病理组织进行消融。
9.进一步优选地,所述消融导丝包括消融近端和消融远端,远端的前方设置有驻极体话筒,通过该驻极体话筒收集待检测组织的声波信号。
10.进一步优选地,所述消融近端的材料为340不锈钢、340l不锈钢和316不锈钢中的一种,具备强抗腐蚀性;所述消融远端为铂镍合金和铂银合金。
11.进一步优选地,所述消融近端的长度为140mm~300mm,消融远端的长度为10mm~
40mm。
12.进一步优选地,所述激光消融系统还包括控制中心,该控制中心同时与声波信号分析单元和激光控制单元连接,用于根据待检测组织的类型设定所述激光控制单元中参数的参数值。
13.进一步优选地,所述声波信号分析单元包括预处理、特征提取、模式识别;所述预处理用于对收集到的声波信号进行过滤和降噪,所述特征提取用于对预处理后的声波信号进行特征提取,所述模式识别用于根据提取的特征判断待检测组织是否为病理组织。
14.进一步优选地,所述预处理包括预加重和加窗分帧,所述预加重通过在消融导丝始端增强高频成分,以补偿高频成分在传输过程中的最大衰减;所述加窗分帧是对所述声波信号以帧为单位进行处理。
15.进一步优选地,所述特征提取是将预处理后的声波信号进行离散傅里叶变换,然后过滤,对过滤后的声波信号进行计算以此获得其对数能量,对该对数能量进行离散余弦变换,舍弃直流成分,以此获得mfccs特征,即实现特征提取。
16.进一步优选地,所述模式识别采用多核svm作为分类器进行识别判断。
17.总体而言,通过本发明所构思的以上技术方案与现有技术相比,具备下列有益效果:
18.1.本发明提供的激光消融系统中通过消融导管和消融导丝的相互配合,消融导丝用于实时判断当前组织是否为病理组织,消融导管用于传导激光能量进行病理组织的消融,二者相互配合,实现检测和消融的一体化;
19.2.本发明提供的利用声波信号进行组织分类的激光消融系统,一方面在消融前判断待检测组织是否为病理组织,另一方面通过实时检测消融过程中的声波信号,实现对消融过程的实时检测,当声波信号分析单元判断当前组织为非病理组织时,停止消融过程,实现病理组织的识别和消融过程的在线监测,有效提高消融对病理组织的针对性和减少血管穿孔的风险,从而提高激光疗效和安全性;
20.3.本发明提供的消融导丝,耐腐蚀且弯曲性能好,适应血管的形态,其一方面能引导消融导管进入待处理部位,另一方面能实现对待处理组织的声波信号的实时采集;
21.4.本发的激光系统中的声波信号分析单元,其在消融前对待检测组织的声波信号分析,判断其是否为病理组织,决定了消融过程是否开始,其在消融开始后,判断当前处理部位是否仍为病理组织,决定了消融过程是否结束,实现功能的高度集成,提高激光消融的精度和智能化程度。
附图说明
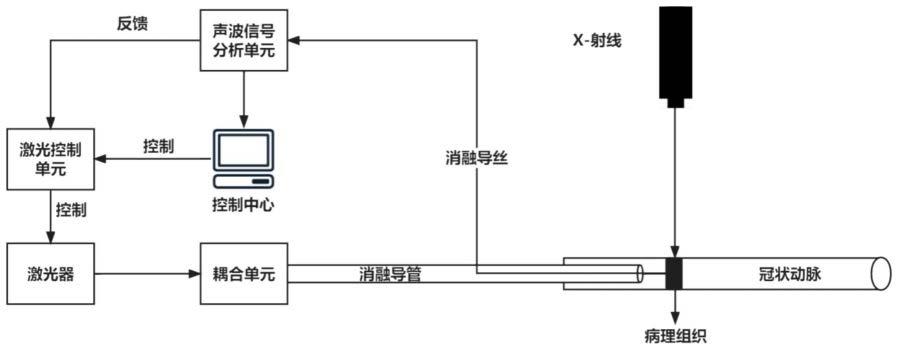
22.图1是按照本发明的优选实施例所构建的一种利用声信号进行组织分类的激光消融系统的结构示意图;
23.图2是按照本发明的优选实施例所构建的消融导丝的结构示意图;
24.图3是按照本发明的优选实施例所构建的激光消融系统进行激光消融的流程示意图;
25.图4是按照本发明的优选实施例所构建的声波分析单元进行声波信号分析的流程图;
26.图5是按照本发明的优选实施例所构建的声波信号分析进行声波信号分析的流程展开图。
具体实施方式
27.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
28.如图1所示,一种利用声信号进行组织分类的激光消融系统包括控制中心,激光控制单元,声波信号分析单元,声波信号记录单元,声波信号收集单元,激光器,耦合单元,消融导管,消融导丝。
29.激光控制单元控制激光器输出低重频高脉冲能量的激光,在本实施例中,激光器发射355nm紫外激光,耦合进消融导管作用于病理组织上对其进行消融。
30.如图2所示,消融导丝包括消融近端和消融远端两部分,其中消融近端与声波信号分析单元相连,材料可选择为340不锈钢、340l不锈钢或316不锈钢,具备强抗腐蚀性,且良好的弯曲性能可确保消融导丝推进至目标动脉分支。消融远端与消融近端之间通过焊接相连,消融远端的材料可选择铂镍合金和铂银合金,该类合金强度高,弹性好且弹性后效低,可有效适应复杂的血管内环境。消融远端的前端设置有驻极体话筒,其与消融远端通过焊接相连,驻极体话筒与病理组织直接接触,其体积小,结构简单,电声性能好,可在血液环境下收集激光消融生物组织的声波信号。
31.消融近端的长度范围为140~300mm,消融远端的长度范围为10~40mm,以适应不同弯曲程度的血管环境。介入手术的常规入路为股动脉入路,考虑到操控消融导丝的准确性和便利性,如在四肢动脉粥样硬化中,可采用消融近端为140mm,消融远端为10mm的消融导丝;在主动脉粥样硬化中,可采用消融近端为300mm,消融远端的长度为40mm的消融导丝。
32.激光器在预热之后,先将消融导管内腔经肝素化冲洗,然后将其末端连接至激光器进行耦合校准;消融导丝经血管到达待处理部位后,将消融导管沿消融导丝缓慢向待检测组织推进。其中,消融导丝的作用主要包括:其一是引导消融导管作用于待检测组织;其二是通过声波信号分析单元收集消融导丝回传的声波信号,再通过声波分析单元对声波信号进行记录,对当前记录的信号通过对应的算法进行实时分析,得到实时被消融的组织的种类,确保消融效率准确性和安全性。
33.激光控制单元通过控制激光器输出低重频高脉冲能量的激光。在具体实施例中,一般使用但不局限于低重频高脉冲能量的激光器,如准分子激光器,其穿透组织所需的阈值通常称为注量,一般范围在30~80mj/mm,注量越高,对病理组织的消融效应就越大,其注量越低,消融效应就越小,其激光脉冲频率在25~80hz之间调整,同样脉冲频率越高,其对病理组织的消融效应就越大,在手术实施过程中,激光控制单元100通常从较低的注量和脉冲频率开始,以逐渐适应病理组织以及确保安全性。
34.在病理组织处,消融导丝引导消融导管,且消融导丝与病理组织总是时刻接触的,所以在消融导管消融病理组织时,消融导丝总是能回传消融时产生的声波信号,消融导丝上的驻极体话筒对当前消融时回传的声波信号进行收集,以便进行后续的声波处理;也就
是说,在使用激光器进行组织消融的过程中,消融导丝也会持续收集消融过程中产生的声波信号并回传给信号分析单元,通过在信号分析单元中设定实时分析的时间间隔,比如消融时没100ms分析判断一次,判断当前正在消融的是病理组织还是非病理组织,当当前消融的组织为非病理组织后,停止激光消融过程,以此实现激光消融过程的在线控制。
35.在消融的过程中,注射透视造影剂,用x射线观察消融导管以及消融导丝所处的位置,防止在消融病理组织的过程中对周围的血管壁造成损伤。使用生理盐水对病理组织进行冲洗以稀释周边的血液被稀释之后的血液由于不易吸收能量被消融,从而被稀释的血液因消融产生的声波信号较小,将减小其对最终采集处理的声波信号的影响(噪声),将一定程度上提高采集以及最终判断是否病理组织的准确度,提高消融过程中的安全性。
36.本发明提供的消融系统适应情况包括但不局限于消融慢性完全闭塞病变(cto)以及动脉支架内再狭窄(isr)。在打开慢性全闭塞(cto)血管的情况下,消融导丝不能穿过病理组织,因此用于消融的消融导管不能滑动,不能按照习惯的使用模式由消融导丝引导。因此,使用没有消融导丝支撑的导管增加了血管壁损伤的风险,包括撕裂和穿孔。现有技术中并不存在一种实用和简单的实时解决方案可以实时检测消融导管是否正在消融病理组织。因此,对病理组织进行分类的在线声波监测将是一个重大突破,并将血管穿孔的风险降至最低。另一个应用是针对动脉支架内再狭窄(isr)。当支架断裂时,或当导丝穿过多个支架的支柱时,同样可以通过在线声波监测来判断被消融的对象类型。
37.声波信号分析单元好包括声波的收集模块和记录模块,通过收集模块对消融导丝回传的声波信号进行收集,然后经过声波记录模块对所收集的声波信号进行记录,然后进行预处理,经消除环境噪声后,对当前的记录信号进行相关算法的处理。其中收集模块主要功能是通过夹持消融导丝且利用声波收集器对声波进行收集。对于不同组织类型的不同声学特性的来源,应当是组织的机械特性(体积模量和弹性模量)、吸收系数和几何形状的组合,这些都与激光同组织相互作用时产生的独特声学特征有关。
38.在激光消融病灶期间进行实时组织分类所采用的算法:通过mfccs提取消融组织的声波信号特征,并通过多核svm对消融组织的声波信号特征进行分类,基于单实验下的数万个声音信号,可分辨验证不同的液体以及正在被消融的组织且具备较高的准确率(》98%)。通过上述利用声波信号进行组织分类的激光消融系统,可以在激光消融过程中对消融组织进行实时监测,从而能够有效的提高消融对病理组织的针对性和减少血管穿孔的风险,从而提高激光疗效和安全性。
39.如图3所示,上述消融系统进行消融按照下列步骤进行:
40.s1所述消融导丝与待检测组织接触,收集其声波信号并将该声波信号传递给所述声波信号分析单元;
41.s2所述声波信号分析单元对声波信号进行分析判断待检测组织是否为病理组织,同时将判断结果反馈给所述激光控制系统,所述激光控制单元按照下列方式之一对所述激光器进行控制:
42.s21当待检测组织为病理组织时,在激光控制系统中设定激光参数并按照该参数控制所述激光器发出激光,耦合系统将所述激光器发出的激光进行耦合,并将耦合后的激光传递给所述消融导管,消融导管对病理组织进行消融;
43.所述消融导丝实时收集病理组织消融过程中的声波信号,并传递给所述声波信号
分析单元,返回步骤s2,直至待检测组织为非病理组织,以此实现病理组织的实时监测与消融;
44.s22当待检测组织为非病理组织时,激光控制系统控制所述激光器不发出激光,调整所述消融导丝的位置,返回步骤s1。
45.如图4所示,声波光信号分析单元的分析过程分为三个阶段:预处理、特征提取、模式识别。由于收集到的消融组织的声波信号在传输过程中高频成分衰减大,低频成分衰减小,因此对消融组织的声波信号进行预处理,预处理包括预加重和加窗分帧,其中预加重通过在消融导丝始端增强高频成分,以补偿高频成分在传输过程中的最大衰减,且预加重对噪声没有影响,因此有效的提高了消融组织的声波信号的信噪比。加窗分帧使消融组织的声波信号以帧为单位进行处理,且加窗有利于减小分帧后的组织声波信号与原始消融组织声波信号之间的误差,在实施例中采用的窗函数为hamming窗。将预处理后的声波信号进行特征提取,在模式库中进行训练后,最终通过模式匹配对声波信号进行判断,从而判断当前的生物组织是病理组织还是非病理组织。
46.mfccs特征提取的主要作用是消融过程中生物组织声波信号的数据挖掘和模式识别,使生物组织声波信号的样本集从高维特征空间映射到低维特征空间,映射后的样本集具有良好的可分性。
47.如图5所示,将预处理后的消融组织声波信号进行离散傅里叶变换,然后经mel频率滤波器组进行过滤,进一步计算得到声波信号的对数能量,计算其离散余弦变换,舍弃直流成分,提取得到消融组织声波信号的mfccs特征。以svm作为分类器识别判断不同种类的消融生物组织,采用多核svm比单核svm的灵活性更高,多核svm映射时,高维空间成为由多个特征空间组合而成的组合空间。由于组合空间充分发挥了各个基本核的不同特征映射能力,能够将异构数据的不同特征分量分别通过相应的核函数得到解决,使消融组织种类的识别准确率更高。
48.基于mfccs和svm的生物组织识别包括下列步骤:首先,将信号重新缩放到最小值-1和最大值1,然后提取mfcc特征;输入mfcc的数据为每个单脉冲(脉冲持续时间为3ms,对应577个离散点);在计算出信号的特征后,使用“fitcecoc”函数对数据(由每个信号特征组成)进行训练,并拟合svm多类模型。当运行超参数优化时,结果之间的差异很小,因此从算法中排除超参数。
49.在声波信号分析单元对声波信号分析后,所得结果将反馈给控制中心及激光控制单元。如果声波信号反馈当前的消融组织是病理组织,则反馈给控制中心,方便控制中心的进一步操作,如增加单脉冲能量或增加脉冲频率以增加消融的速度;如当前声波信号反馈当前的消融组织是非病理组织,则在反馈给控制中心的同时,激光控制单元通过自身的反馈—控制原则自动减小单脉冲激光能量和脉冲频率,极度情况下激光器控制单元会自动关闭激光器,防止血管穿孔,有效的提高安全性。
50.区别于现有常见的高能量低重频的消融系统,其虽然可对病理组织有效消融,但其产生的高能量容易导致血管穿孔并发症的发生,且不具备实时消融时对病理组织以及非病理组织进行分类辨别的能力。本发明公开利用在355nm紫外激光消融冠状动脉粥样硬化过程中记录的声波,来分类被消融的组织类型,在激光消融血管期间进行组织分类通过mfccs提取消融组织的声波信号特征,并通过多核svm对消融组织的声波信号特征进行分
类,基于单实验下的数万个声音信号,可分辨验证消融组织的不同种类,以此实现消融过程的实时监测,从而能够有效的提高消融对病理组织的针对性和减少血管穿孔的风险,从而提高激光疗效和安全性。
51.本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1