一种蜂王浆提取物及其提取方法和应用与流程
1.本发明涉及材料领域,具体涉及一种蜂王浆提取物及其提取方法和应用。
背景技术:
2.蜂王浆又名蜂王乳、蜂皇浆等,由5~15日龄工蜂舌腺和上颚腺分泌,呈乳白色或淡黄色,是一种专门用来喂养蜂王及3日龄幼蜂的特殊浆状物质。新鲜蜂王浆中水分含量占62.5%~70.0%,干物质含量占30.0%~37.5%,蛋白质在其干重中所占比例最高,另外还含有脂类、糖类、游离氨基酸、维生素、矿物质、活性蛋白酶等物质,具有延缓衰老、增强机体免疫力、抗氧化、抗肿瘤、抗菌、抗高血压等多项生理保健功效。
3.皮肤含有许多发色团,包括黑色素和类胡萝卜素,他们以波长相关的方式散射和吸收入射光,导致光能密度随着皮肤深度的增加而降低。尽管uvb辐射大部分被角质层阻挡,但uva辐射可以穿透皮肤表皮,引起氧化应激。同时uva辐射后细胞基质金属蛋白酶-1(mmp-1)上调,导致细胞外基质(ecm)降解。真皮主要由细胞外基质(ecm)和成纤维细胞组成。在衰老过程中,真皮层会发生显著变化。胶原蛋白量的减少阻碍了成纤维细胞和ecm之间的相互作用,从而导致成纤维细胞功能的恶化和真皮胶原蛋白的量进一步减少。弹性纤维是由弹性蛋白沉积在由原弹性蛋白和其他糖蛋白组成的微原纤维支架上形成,起到调节皮肤顺应性和弹性的重要作用。临床表现为皮肤紧致。基质金属蛋白-1(mmp-1)是一个普遍存在的内肽酶家族,可以降解ecm蛋白,是引发胶原纤维断裂的主要蛋白。其他ecm成分,包括糖胺聚糖(gags)和蛋白聚糖(pgs),也会在老化过程中发生变化,最终导致皮肤起皱和失去弹性。
4.氧化应激的实质是因自由基产生过多和(或)清除不足,过多的自由基在人体内产生一系列负面作用。氧化应激的产生既有内部因素,也有外在原因,内部因素包括急、慢性感染,血脂、血糖异常,外在的因素如吸烟、喝酒、运动过度、服用某些药物和经常饱餐,此外日光浴(紫外线辐射)过多也会引起氧化应激。大部分学者比较认可的仍是1956年harman提出的衰老自由基学说,自由基的清除剂单独使用一般都不是很理想,例如sod如果单独使用将是不合理的,有可能起不到抗氧化作用。实验证明,sod(超氧化物歧化酶)只有与gp(谷胱甘肽酶)或cat(过氧化氢酶)一起联合使用才会起到很好的抗氧化作用。蜂王浆中起到自由基清除剂作用的主要包括有机酸类、酚类、酶蛋白和小分子肽。但是作为化妆品添加剂,对于用量是有限制的,蜂王浆或蜂王浆酶解产物成分复杂,起到清除自由基作用的成分含量有限。cn112494412a公开的一种皮肤紧致涂抹式面膜使用到蜂王浆提取物3-4%,但并未提供提取物提取方法以及在该面膜中的主要作用。
技术实现要素:
5.为了克服上述现有技术存在的问题,本发明的目的之一在于提供一种蜂王浆提取物的提取方法。
6.本发明的目的之二在于提供一种蜂王浆提取物。
7.本发明的目的之三在于提供一种化妆品添加剂。
8.本发明的目的之四在于提供一种化妆品。
9.本发明的目的之五在于提供一种蜂王浆提取物在洗护用品或保健品中的应用。
10.为了实现上述目的,本发明所采取的技术方案是:
11.本发明的第一个方面在于提供一种蜂王浆提取物的提取方法,包括以下步骤:
12.s1:将蜂王浆酶解,使用2kd~3kd(道尔顿)的滤膜超滤,然后使用9kd~10kd(道尔顿)的超滤膜超滤,得到滤液;
13.s2:调节所述滤液的ph,然后使用阴离子交换树脂进行纯化,制得所述蜂王浆提取物。
14.优选地,所述蜂王浆提取物的分子量为5kd~9kd(道尔顿)。
15.优选地,所述蜂王浆在使用前先除杂;进一步优选地,所述蜂王浆在使用前配制成水溶液,过滤除去不溶物。
16.优选地,所述将蜂王浆酶解的步骤具体为:调节蜂王浆的ph为1.5~3,然后加入0.2wt%~0.4wt%的胃蛋白酶在37℃~42℃的温度下酶解2~3h;调节蜂王浆的ph为7~8,然后加入0.2wt%~0.4wt%的胰蛋白酶在37℃~42℃的温度下酶解2~3h。
17.优选地,在蜂王浆的ph为1.8~2.5时,加入0.25wt%~0.3wt%的胃蛋白酶;进一步优选地,在蜂王浆的ph为2时,加入0.3wt%的胃蛋白酶。
18.优选地,在蜂王浆的ph为7~7.5时,加入0.25wt%~0.3wt%的胰蛋白酶;进一步优选地,在蜂王浆的ph为7.5时,加入0.3wt%的胰蛋白酶。
19.优选地,所述步骤s1还包括离心步骤;所述离心步骤位于酶解步骤之后。
20.优选地,所述离心速率为15000~25000r/min;进一步优选地,所述离心速率为18000~22000r/min;再进一步优选地,所述离心速率为19000~21000r/min。
21.优选地,所述离心温度为0~5℃;进一步优选地,所述离心温度为1~4℃。
22.优选地,所述离心时间为10~40min;进一步优选地,所述离心时间为20~30min。
23.优选地,所述步骤s1中,先使用2kd~3kd的滤膜超滤,然后使用10kd的超滤膜超滤,得到滤液;进一步优选地,所述步骤s1中,先使用3kd的滤膜超滤,然后使用10kd的超滤膜超滤,得到滤液。
24.优选地,所述调节所述滤液的ph的步骤具体为:使用碱液调节滤液的ph至中性。
25.优选地,所述碱液包括碳酸氢钠溶液、氨水、氢氧化钠溶液中的至少一种。
26.优选地,所述使用阴离子交换树脂进行纯化的步骤具体为:使用阴离子交换树脂吸附,水洗、盐洗,将盐洗得到的洗脱液脱盐脱水。
27.优选地,所述阴离子交换树脂为弱碱性阴离子交换树脂。
28.优选地,所述弱碱性阴离子交换树脂包括弱碱性丙烯酸类阴离子交换树脂、含有n(ch2ch3)2官能团的弱碱性阴离子交换树脂中的至少一种。
29.优选地,所述弱碱性丙烯酸类阴离子交换树脂包括fpa53。
30.优选地,所述含有n(ch2ch3)2官能团的弱碱性阴离子交换树脂包括fpda-13。
31.优选地,所述盐洗步骤为采用氯化钠溶液进行洗脱。
32.优选地,所述氯化钠溶液的浓度为0-0.5mol/l,但不为0;进一步优选地,所述氯化钠溶液的浓度为0.1-0.5mol/l;再进一步优选地,所述氯化钠溶液的浓度为0.4-0.5mol/l。
33.优选地,所述洗脱温度为0~30℃;进一步优选地,所述洗脱温度为0~10℃。
34.优选地,所述将盐洗得到的洗脱液脱盐脱水的步骤具体为:将盐洗得到的洗脱液使用150d~300d(道尔顿)的纳滤膜脱盐脱水。
35.优选地,所述脱盐终点为透过液的电导率小于0.1ms。
36.优选地,所述步骤s2中还包括冻干步骤;所述冻干步骤位于纯化步骤之后。
37.优选地,所述冻干步骤具体为:预冻温度为-45℃~-50℃,主干燥温度为-20℃~-25℃,末端干燥温度为0℃~10℃。
38.本发明的第二个方面在于提供一种蜂王浆提取物,采用本发明第一个方面提供的提取方法制得,所述蜂王浆提取物的分子量为5kd~9kd。
39.本发明的第三个方面在于提供一种化妆品添加剂,包括本发明第二个方面提供的蜂王浆提取物。
40.优选地,所述化妆品添加剂中,所述蜂王浆提取物的含量为0.000002wt%~0.00003wt%。
41.优选地,所述化妆品添加剂中还包括葡糖氨基葡聚糖。
42.优选地,所述葡糖氨基葡聚糖与蜂王浆提取物的质量比为1:(0.5~2)。
43.本发明的第四个方面在于提供一种化妆品,包括化妆品添加剂。
44.优选地,所述化妆品中,化妆品添加剂的含量为0.000002wt%~0.00003wt%。
45.本发明的第五个方面在于提供本发明第二个方面提供的蜂王浆提取物在洗护用品或保健食品中的应用。
46.本发明的有益效果是:本发明中的提取方法可以提取出分子量为5kd~9kd的蜂王浆提取物,提取方法简单,易操作,适用于工业化推广应用。
47.本发明中的蜂王浆提取物具有优异的紧致皮肤、抗皱、消炎的作用,具有优异的ros、tnf-α和mmp-1抑制效果,此外,可以提高皮肤中的i型胶原蛋白和弹性蛋白的含量,使皮肤保持紧致。
48.本发明中的蜂王浆提取物作为化妆品添加剂时,较小的添加量均可以提高化妆品的紧致、抗皱、消炎效果,同时,蜂王浆提取物因来源于天然蜂王浆,不会产生皮肤过敏效应,与其他成分的相容性好,适用于各种类型的化妆品。
具体实施方式
49.以下结合实例对本发明的具体实施作进一步详细说明,但本发明的实施和保护不限于此。需要指出的是,以下若为有未特别详细说明之过程,均是本领域技术人员可参照现有技术实现或理解的。所用试剂或仪器未注明生产厂商者,视为可以通过市售购买得到的常规产品。
50.实施例1
51.本例中的蜂王浆提取物按照以下提取方法提取,具体包括以下步骤:
52.1)选用冷冻的蜂王浆1.0kg,按照体积比1:4配置成蜂王浆水溶液,滤布过滤除去不溶物,滤液用1mol/l的盐酸溶液调节ph至2.0,加入0.3%胃蛋白酶混合均匀,在37℃~42℃温度下恒温酶解2.5h,酶解液用25%氨水调节ph至7.5,加入0.3%胰蛋白酶,在37℃~42℃温度下恒温酶解2h,得到酶解液;
53.2)上述酶解液在20000r/min,1-4℃条件下离心20min,收集上清液过滤,滤液通过3kd的一级超滤膜过滤,收集未透过一级超滤膜的物质,然后再使用10kd的二级超滤膜超滤,收集透过液。
54.3)使用25%氨水调节ph至6.8-7.2,然后加入到20l的fpda-13阴离子交换树脂进行吸附,纯化水冲洗后,使用0.4mol/l的氯化钠水溶液10-20℃洗脱收集洗脱液,洗脱液再经过纳滤脱盐(透过液电导率<0.1ms为脱盐终点)脱水得到蜂王浆提取物浓缩液,测定水含量约为85%,加入纯化水稀释至固含量10%,设定冻干参数(-45℃/5h,-30℃/1h,-23℃/15h,0℃/2h,10℃/4h)进行冻干得到蜂王浆提取物,蜂王浆提取物的分子量为5kd~9kd。
55.性能测试:
56.细胞准备:
57.按照《t/shrh031—2020化妆品紧致、抗皱功效测试-体外成纤维细胞i型胶原蛋白含量测定》、《t/shrh 032-2020化妆品紧致、抗皱功效测试-体外角质形成细胞活性氧(ros)抑制测试方法》7细胞准备的方法,将来自冷冻保存的细胞培养物以6000个/孔的密度接种于96孔板,以100000个/孔的密度接种于6孔板并在检测前传代两次。前期试验结果证明:角质细胞以6000个/孔的密度接种于96孔板,在接种24h后,触合度达到45%~60%;角质细胞以100000个/孔的密度接种于6孔板,在接种24h后,融合度达到45%-60%;成纤维细胞以5000个/孔的密度接种于96孔板,在接种24h后,融合度达到45%~60%。其中,角质细胞的配制方法为:使用500ml人角质细胞无血清基础培养基(kbm)加入0.0001ng/ml人重组人表皮生长因子,5μg/ml胰岛素,0.5μg/ml氢化可的松,30μg/ml庆大霉素,15μg/ml两性霉素,30μg/ml垂体提取物以及添加165μl氯化钙溶液。成纤维细胞的配制方法为:用89%高糖dmem加入10%fbs和1%青霉素-链霉素(penicillin-streptomycin)混匀备用。
58.受试物的制备
59.2.83%蜂王浆提取物:28.3mg的原料溶解于971.7mg的dmem完全培养基中,37℃水浴加热20min。
60.0.0000283%蜂王浆提取物:按1:9稀释比例依次从2.83%的蜂王浆提取物的母液中采用dmem完全培养基进行梯度稀释配置。
61.0.0000142%蜂王浆提取物:按1:1稀释比例从0.0000283%的蜂王浆提取物中采用dmem完全培养基进行配置。
62.0.00000283%蜂王浆提取物:按l:9稀释比例从0.0000283%的蜂王浆提取物中采用dmem完全培养基进行配置。
63.0.0000142%复配物组:按1:1稀释比例将0.0000283%的蜂王浆提取物与0.0000283%的葡糖氨基葡聚糖进行1:1混合配置。
64.阳性对照组:使用0.05%ve为本实验的阳性对照物,用无水乙醇将ve稀释至5%(m/v),后按照体积比1:99用细胞培养基稀释至0.05%。使用100ng/ml tgf-β1为本实验的阳性对照物,取2μl tgf-β1溶液加入998μl完全培养箱稀释至100ng/ml使用。
65.活性氧检测方法:
66.按照《t/shrh 032-2020化妆品紧致、抗皱功效测试-体外角质形成细胞活性氧(ros)抑制测试方法》9试验步骤的程序,对细胞进行消化接种、诱导给药、光照刺激、装载探针并用荧光显微镜进行检测,检测对象:空白对照组、阴性对照组、阳性对照组和实施例组,
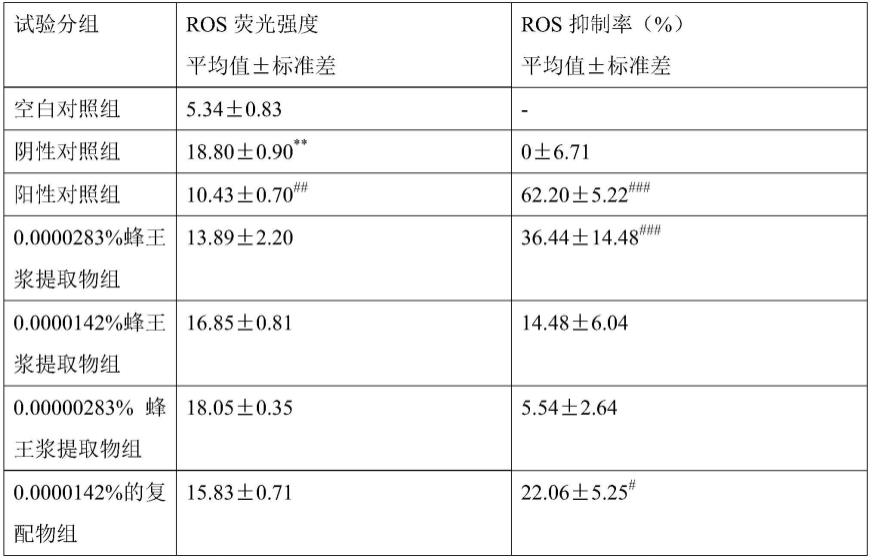
其中,实施例组是将实施例1中制得的蜂王浆提取物稀释分别配制质量百分数为0.0000283%(1μmol)蜂王浆提取物组、0.00000283%(0.1μmol)蜂王浆提取物组、0.0000142%(0.5μmol)蜂王浆提取物组和0.0000142%(0.5μmol)的复配物组;所有实施例组均进行5j光照刺激。空白对照组是指未接种细胞的空白培养基;阴性对照组是指接种细胞后进行5j光照刺激;阳性对照组是指接种细胞后进行5j光照刺激,并给0.05%的ve。判定标准为:试验应符合质量标准为光照刺激下,ve能检出抑制ros产生的效果,且与光照刺激相比,阳性对照ve组的ros抑制率≥30%,则认为试验系统有效。在试验满足有效性验证的基础上,受试物与阴性对照相比,ros抑制率为正值,且荧光强度值具有显著性差异(p《0.05),说明受试物在该浓度下具有抑制ros的作用。活性氧的测试数据如下表1所示:
67.表1 ros检测数据
[0068][0069]
注:“#”表示与阴性对照组对比结果,“#”:p<0.5;“**”和“##”:p<0.01;“###”:p<0.0001。
[0070]
由此可知,光照刺激下,0.0000283%蜂王浆提取物组和0.0000142%复配物组的ros的抑制率与阴性对照组相比,有显著性差异,抑制率分别约为36%和22%,进一步表明本发明中的蜂王浆提取物具有优异的抑制ros的作用。
[0071]
光照刺激下mmp-1检测方法:
[0072]
使用《t/shrh032—2020化妆品紧致、抗皱功效测试-体外角质形成细胞活性氧(ros)抑制测试方法》9试验步骤的程序,对细胞进行消化接种、诱导给药、光照刺激;按照《syringaresinol inhibits uva-induced mmp-1expression by suppression of mapk/ap-1 signaling in hacat keratinocytes and human dermal fibroblastes》文献中记载的方法使用elisa检测提取诱导后的细胞上清液。检测对象:空白对照组、阳性对照组和实施例组,其中,实施例组是将实施例1中制得的蜂王浆提取物稀释分别配制质量百分数为0.0000283%(1μmol)蜂王浆提取物组、0.00000283%(0.1μmol)蜂王浆提取物组、0.0000142%(0.5μmol)蜂王浆提取物组和0.0000142%(0.5μmol)的复配物组。空白对照组
是指未接种细胞的空白培养基;阳性对照组是指使用100ng/ml tgf-β1。判定标准为:试验应符合的质量标准为光照刺激下,阳性对照组能检出抑制mmp-1产生的效果,且与光照刺激相比,阳性对照组的mmp-1抑制率≥30%,则认为试验系统有效。在试验满足有效性验证的基础上,实施例组与阳性对照组相比,mmp-1抑制率为正值,且具有显著性差异(p《0.05),说明实施例组中的受试物在该受试浓度下,具有抑制mmp-1生成的能力。mmp-1测试结果如下表2所示:
[0073]
表2 mmp-1的检测结果
[0074][0075]
注:“*”表示与空白对照组对比结果,“***”:p<0.0001。
[0076]
由表2可知,在光照刺激下0.0000283%蜂王浆提取物组、0.0000142%蜂王浆提取物组、0.00000283%蜂王浆提取物组、0.0000142%复配物组的mmp-1抑制率与空白对照组相比,均有显著性差异,抑制率分别为24%、20%、14%和23%。
[0077]
胶原蛋白和弹性蛋白含量测试
[0078]
按照《t/shrh 031—2020化妆品紧致、抗皱功效测试-体外成纤维细胞i型胶原蛋白含量测定》9试验步骤的程序,对细胞进行消化接种、诱导给药、elisa检测上清液的炎症因子。检测对象:空白对照组、阳性对照组和实施例组,其中,实施例组是将实施例1中制得的蜂王浆提取物稀释分别配制质量百分数为0.0000283%(1μmol)蜂王浆提取物组、0.00000283%(0.1μmol)蜂王浆提取物组、0.0000142%(0.5μmol)蜂王浆提取物组和0.0000142%(0.5μmol)的复配物组。空白对照组是指未接种细胞的空白培养基;阳性对照组是指使用100ng/ml tgf-β1。胶原蛋白含量测试的判定标准为:阳性对照组能检出i型胶原蛋白含量上调的效果,且与空白对照组相比,阳性对照组中的i型胶原蛋白含量上调率需≥20%,则认为试验系统有效。在试验满足有效性验证的基础上,受试物与空白对照组相比,i型胶原蛋白的含量上调,且具有显著性差异(p《0.05),说明受试物在该受试浓度下,具有促进i型胶原蛋白合成的能力,具体测试结果如表3所示。弹性蛋白含量测试的判定标准为:阳性对照组均能检出弹性蛋白含量上调的效果,且与空白对照组相比,阳性对照组的弹性蛋白含量上调率需≥20%,则认为试验系统有效。在试验满足有效性验证的基础上,实施
例组的受试物与空白对照组相比,弹性蛋白的含量上调,且具有显著性差异(p《0.05),说明受试物在该受试浓度下,具有促进弹性蛋白合成的能力,具体测试结果如表4所示。
[0079]
表3胶原蛋白测试结果
[0080][0081]
注:“*”表示与空白对照组对比结果,“**”表示p<0.01,“***”表示p<0.0001。
[0082]
由表3可知,与空白对照组相比,0.0000283%蜂王浆提取物组、0.0000142%蜂王浆提取物组、0.00000283%蜂王浆提取物组、0.0000142%复配物组的i型胶原蛋白含量具有显著性增长,上调率分别为37%、28%、22%、33%。
[0083]
表4弹性蛋白测试结果
[0084][0085]
注:“**”表示p<0.01,“***”表示p<0.0001。
[0086]
由表4可知,与空白对照组相比,0.0000283%蜂王浆提取物组、0.0000142%蜂王浆提取物组、0.00000283%蜂王浆提取物组、0.0000142%复配物组的弹性蛋白含量具有显著性增长,上调率分别为29%、20%、9%、19%。
[0087]
舒缓实验结果:
[0088]
使用《t/shrh 032—2020化妆品紧致、抗皱功效测试-体外角质形成细胞活性氧
(ros)抑制测试方法》9试验步骤的程序,对细胞进行消化接种、诱导给药、光照剌激;按照《t/shrh034—2021化妆品舒缓功效测试-体外tnf-α炎症因子含量测定脂多糖诱导巨噬细胞系炎症细胞模型测试方法》的方法使用elisa检测上清液的炎症因子。检测对象:空白对照组、阴性对照组、阳性对照组和实施例组,其中,实施例组是将实施例1中制得的蜂王浆提取物稀释分别配制质量百分数为0.0000283%(1μmol)蜂王浆提取物组、0.00000283%(0.1μmol)蜂王浆提取物组、0.0000142%(0.5μmol)蜂王浆提取物组和0.0000142%(0.5μmol)的复配物组;所有实施例组均进行5j光照刺激。空白对照组是指未接种细胞的空白培养基;阴性对照组是指接种细胞后进行5j光照刺激;阳性对照组是指接种细胞后进行5j光照刺激,并给100μg/ml的地塞米松。判定标准为:在光照刺激下,阳性对照组能检出抑制tnf-α产生的效果,且与阴性对照组相比,阳性对照组的tnf-α抑制率≥30%,则认为试验系统有效。在试验满足有效性验证的基础上,受试物与阴性对照组相比,tnf-α的抑制率为正值,且具有显著性差异(p《0.05),说明受试物在该受试浓度下,具有抑制光照下炎症因子释放的能力。tnf-α的测试数据如下表5所示:
[0089]
表5 tnf-α测试结果
[0090][0091]
注:“##”表示p<0.01,“***”和“###”表示p<0.0001。
[0092]
由表5可知,与阴性对照组相比,0.0000283%蜂王浆提取物组、0.0000142%蜂王浆提取物组、0.00000283%蜂王浆提取物组、0.0000142%复配物组的tnf-α抑制率均有显著性差异,抑制率分别为33%、26%、18%、28%。
[0093]
上面对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下做出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1