医用仿生等离子体钛合金骨科植入物的制备及实验方法
1.本发明涉及医用材料技术领域,具体为医用仿生等离子体钛合金骨科植入物的制备及实验方法。
背景技术:
2.钛合金具有高比强度,高热强度,小密度,良好的抗蚀性、低温性能和吸气性能等优点,可用于制造植入体;但现有的钛合金植入体由于自身所表现出的生物惰性使其与植入部位的整合性差,因此无法促进成骨,虽然表面改性技术可以提高钛合金的表面生物活性,但其仍存在以下缺陷:一是存在工艺复杂和制造成本高的问题;二是容易因感染、炎症刺激等因素导致植入体松动,进而会影响治疗效果,最终可能会导致植入失败;三是钛合金植入体表面涂层多为金属元素,生物活性因子释放较快,具有一定的副作用,不能稳定持久的促进成骨。
技术实现要素:
3.本发明的目的在于提供医用仿生等离子体钛合金骨科植入物的制备及实验方法,以解决上述背景技术中提出的问题。
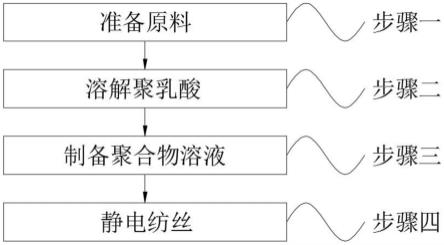
4.为实现上述目的,本发明提供如下技术方案:医用仿生等离子体钛合金骨科植入物的制备方法,包括步骤一,准备原料;步骤二,溶解聚乳酸;步骤三,制备聚合物溶液;步骤四,静电纺丝;
5.其中上述步骤一中,以质量百分比含量之和为1计,取10%的聚乳酸(pla)、88%的溶剂和2%的盐酸盐米诺环素(mino)备用;其中,溶剂采用三氯甲烷和二甲基甲酰胺制备溶剂配置而成;
6.其中上述步骤二中,取步骤一中所称取的溶剂和pla,将pla溶于溶剂中,得到混合溶液;
7.其中上述步骤三中,取步骤二中所制备的混合溶液和步骤一中所称取的mino,将mino加入混合溶液中形成聚合物溶液;
8.其中上述步骤四中,取步骤三中所制备的聚合物溶液,对其施加外接电压,使聚合物在外加电场的作用下形成射流,利用金属钛片接收射流,使射流最终在钛片上固化为纳米纤维的材料结构,得到负载10%pla+2%mino的钛片。
9.优选的,所述步骤四中,外接电压为15kv。
10.优选的,所述步骤四中,推进器推进速率为5ul/min。
11.优选的,所述步骤四中,金属钛片接收射流的接收距离为15cm,时间为5min。
12.医用仿生等离子体钛合金骨科植入物的实验方法,包括步骤一,材料准备;步骤二,麻醉固定大鼠;步骤三,植入植入体;步骤四,术后管理;步骤五,获取种植体标本;步骤六,结果分析;
13.其中上述步骤一中,选用健康成年sd大鼠共三组,每组各6只,准备6个纯钛棒、6个
喷涂pla的钛棒以及6个喷涂10%pla+2%mino的钛棒;
14.其中上述步骤二中,腹腔注射麻醉成年健康sd大鼠,将其以俯卧位固定于手术台上;
15.其中上述步骤三中,首先去除sd大鼠双侧后肢手术切口附近毛发,常规碘伏酒精消毒,切开皮肤、筋膜;然后逐层钝性分离肌肉,翻起筋膜和骨膜,显露股骨上段;再以低速钻破除一侧皮质并定位,逐级备洞,形成直径为1.6mm的孔,并与髓腔贯通,每侧股骨制备1个孔,三组sd大鼠分别植入纯钛棒、喷涂pla的钛棒、喷涂10%pla+2%mino的钛棒,最后分层缝合关闭伤口;
16.其中上述步骤四中,术后三天内予以青霉素肌注,每日两次;
17.其中上述步骤五中,术后选择在种植体植入2周、4周和6周三个时间点处死动物,连同股骨一起整体取出种植体标本;
18.其中上述步骤六中,用4%甲醛进行固定后通过mico-ct,he染色及免疫组化等技术检验各组骨髓间充质干细胞(mscs)的增殖和粘附效果。
19.优选的,所述步骤三中,备洞时用生理盐水冷却,防止温度过高造成的骨组织灼伤。
20.优选的,所述步骤六中,检验结果为:喷涂10%pla+2%mino的钛棒可以在sd大鼠体内促进骨髓间充质干细胞(mscs)的增殖和粘附。
21.与现有技术相比,本发明的有益效果是:本发明所制备的钛合金骨科植入物以聚乳酸和盐酸盐米诺环素作为涂层原料,对骨髓间充质干细胞的增殖和粘附具有良好的促进效果,同时也具备对大肠杆菌和金黄色葡萄球菌的抑制效果,可以有效提升骨组织的修复能力和速度,降低感染和炎症的风险;本发明采用静电纺丝工艺制备纳米涂层,具有工艺简单、成本低廉的优点。
附图说明
22.图1为本发明的制备方法流程图;
23.图2为本发明的静电纺丝作业图;
24.图3为本发明的实验方法流程图;
25.图4为本发明的sd大鼠手术过程示意图;
26.图5为本发明的sd大鼠股骨连同植入体外观图;
27.图6为第1天检测出的骨髓间充质干细胞的细胞活力条形图;
28.图7为第3天检测出的骨髓间充质干细胞的细胞活力条形图;
29.图8为第7天检测出的骨髓间充质干细胞的细胞活力条形图;
30.图9为大肠杆菌培养皿实物图;
31.图10为金黄色葡萄球菌培养皿实物图。
具体实施方式
32.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他
实施例,都属于本发明保护的范围。
33.请参阅图1-2,本发明提供的一种实施例:医用仿生等离子体钛合金骨科植入物的制备方法,包括步骤一,准备原料;步骤二,溶解聚乳酸;步骤三,制备聚合物溶液;步骤四,静电纺丝;
34.其中上述步骤一中,以质量百分比含量之和为1计,取10%的聚乳酸(pla)、88%的溶剂和2%的盐酸盐米诺环素(mino)备用;其中,溶剂采用三氯甲烷和二甲基甲酰胺制备溶剂配置而成;
35.其中上述步骤二中,取步骤一中所称取的溶剂和pla,将pla溶于溶剂中,得到混合溶液;
36.其中上述步骤三中,取步骤二中所制备的混合溶液和步骤一中所称取的mino,将mino加入混合溶液中形成聚合物溶液;
37.其中上述步骤四中,取步骤三中所制备的聚合物溶液,对其施加15kv外接电压,使聚合物在外加电场的作用下形成射流,利用金属钛片接收射流,使射流最终在钛片上固化为纳米纤维的材料结构,得到负载10%pla+2%mino的钛片;其中,推进器推进速率为5ul/min,金属钛片接收射流的接收距离为15cm,时间为5min。
38.请参阅图3-5,本发明提供的一种实施例:医用仿生等离子体钛合金骨科植入物的实验方法,包括步骤一,材料准备;步骤二,麻醉固定大鼠;步骤三,植入植入体;步骤四,术后管理;步骤五,获取种植体标本;步骤六,结果分析;
39.其中上述步骤一中,选用健康成年sd大鼠共三组,每组各6只,准备6个纯钛棒、6个喷涂pla的钛棒以及6个喷涂10%pla+2%mino的钛棒;
40.其中上述步骤二中,腹腔注射麻醉成年健康sd大鼠,将其以俯卧位固定于手术台上;
41.其中上述步骤三中,首先去除sd大鼠双侧后肢手术切口附近毛发,常规碘伏酒精消毒,切开皮肤、筋膜;然后逐层钝性分离肌肉,翻起筋膜和骨膜,显露股骨上段;再以低速钻破除一侧皮质并定位,逐级备洞,形成直径为1.6mm的孔,并与髓腔贯通,备洞时用生理盐水冷却,防止温度过高造成的骨组织灼伤,每侧股骨制备1个孔,三组sd大鼠分别植入纯钛棒、喷涂pla的钛棒、喷涂10%pla+2%mino的钛棒,最后分层缝合关闭伤口;
42.其中上述步骤四中,术后三天内予以青霉素肌注,每日两次;
43.其中上述步骤五中,术后选择在种植体植入2周、4周和6周三个时间点处死动物,连同股骨一起整体取出种植体标本;
44.其中上述步骤六中,用4%甲醛进行固定后通过mico-ct,he染色及免疫组化等技术检验各组骨髓间充质干细胞(mscs)的增殖和粘附效果,检验结果为:喷涂10%pla+2%mino的钛棒可以在sd大鼠体内促进骨髓间充质干细胞(mscs)的增殖和粘附。
45.试验例:
46.按照上述实施例中所提供的制备方法,制备出负载10%pla+0.5%mino的钛片、负载10%pla+1%mino的钛片、负载10%pla+2%mino的钛片,通过cck-8及扫描电镜等技术分别检测其对骨髓间充质干细胞(mscs)增殖和细胞粘附的能力,结果如图6-8,检测负载10%pla+2%mino的钛片对大肠杆菌和金黄色葡萄球菌的抑制作用,结果如图9-10。
47.基于上述,本发明通过静电纺丝制备负载纳米材料的钛合金,具有工艺简单,成本
低廉的优点,通过采用pla和mino作为原料,可以改变钛合金的表面生物活性,使其具备促进骨髓间充质干细胞(mscs)的增殖和粘附的功能,能稳定持久的促进成骨,同时对大肠杆菌和金黄色葡萄球菌也具备良好的抑制效果。
48.对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。不应将权利要求中的任何附图标记视为限制所涉及的权利要求。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1