治疗黑色素瘤的靶向纳米制剂及其载体和应用
本发明属于医药,涉及药物载体、药物组合物以及制备和应用,具体涉及治疗黑色素瘤的靶向纳米制剂及其载体和应用。
背景技术:
1、黑色素瘤是一种皮肤癌,近几年,其发病率在世界范围内显著上升。并且,恶性黑色素瘤是皮肤癌的主要致死形式,占所有皮肤癌相关死亡的90%以上。恶性黑色素瘤是来源于皮肤和其他组织黑色素细胞高度恶化、发病隐匿的肿瘤,其在浅色皮肤人群中高发。黑色素瘤的发病因素包括遗传易感性、皮肤黑色素沉着、紫外线辐射等环境因素。
2、黑色素瘤的早期诊断发现是治疗黑色素瘤的关键,耐药性的产生是黑色素瘤的一个重要特征。目前,手术、化疗和免疫疗法是最常见的治疗方法。然而,这些方法在很大程度上受到晚期癌症诊断、药物脱靶、全身毒性和药物引起的不良反应的限制。一般黑色素瘤早期发生时可通过手术切除,然而在恶性黑色素瘤中,手术并未达到预期,化疗是目前最常使用的癌症治疗方法,目前,临床上治疗黑色素瘤的药物包括维莫非尼、达卡巴嗪、紫杉醇等等,化疗药物通常在初期表现出良好的效果,但在后期,患者会出现严重的副作用和耐药性,除此之外,化疗会对机体神经系统、肾脏、肝脏等造成明显毒副作用,并严重影响患者的生活质量。为了克服目前黑色素瘤治疗的不足,我们需要提出新的治疗方法,而纳米药物递送系统的出现可以精准靶向肿瘤,在减少副作用的同时,提高药物在肿瘤部位的浓度。纳米药物递送系统通过epr效应(enhanced permeability and retention effect,epr)等被动靶向肿瘤组织,通过药物的持续释放提高药物的生物利用度,同时防止药物被网状内皮系统清除,减少全身毒性。此外,肿瘤的细胞内环境目前被认为是影响肿瘤治疗的决定性因素。特别令人感兴趣的是分子靶向配体,如抗体、多肽、fa等的纳米级给药系统被应用于肿瘤治疗中。这种有针对性的、个性化的纳米药物递送系统根据肿瘤细胞的分子特征及其微环境增加了药物在肿瘤区域有针对性的积累,并且可以控制药物的释放,从而减少药物的副作用,进一步的降低患者治疗的风险。其中,il4rpep-1是一种il4r结合肽,在肿瘤微环境中il4rpep-1优先与黑色素瘤细胞表面高度表达il4r受体相结合。因此,在本发明中我们通过在纳米载体表面修饰上il4rpep-1以增强药物递送系统的主动靶向能力。
3、目前,传统的药物疗法由于缺乏治疗效果、对健康组织的高毒性和对癌细胞的非特异性而受到严重限制。除此之外,传统化疗药物在血液循环中的稳定性和溶解度普遍较差,缺乏选择性输送能力。近些年,研究发现单一药物在治疗早期癌症可能显示疗效好,但随着治疗时间的延长药物的临床药效却随之降低,这可能与治疗过程中肿瘤细胞获得性多药耐药性相关。获得性多药耐药性的出现导致大量的抗癌药物(dox、ptx、达拉菲尼等)迅速的从肿瘤细胞中被清除,使得低水平的药物无法有效杀死肿瘤细胞,最终导致化疗失败。这意味着病人必须改变到选择其它新的药物治疗,然而一个新的药物可能会给患者带来更多潜在的副作用和昂贵的治疗成本。
4、近年来,研究发现两种或两种以上具有相似或不同药理机制的多种药物同时给予的联合化疗往往是一种优于单一治疗的治疗策略。asb是一种生物口服利用的丝氨酸/苏氨酸蛋白激酶akt抑制剂。cxb作为环氧化酶-2(cyclooxygenase-2,cox-2)的选择性抑制剂,在临床主要作为一种抗炎止痛药物存在。
5、目前尚未有使用asb和cxb组合的纳米药物递送系统治疗黑色素瘤的报道。
技术实现思路
1、为解决现有技术中存在的上述技术问题,本发明提供治疗黑色素瘤的靶向纳米制剂及其载体和应用。
2、本发明的第一个目的是提供一种具有可生物降解和靶向递送的简单实用的纳米药物递送载体,并进一步验证该纳米递送系统在体外细胞实验中良好的抗癌作用和较低的毒副作用。
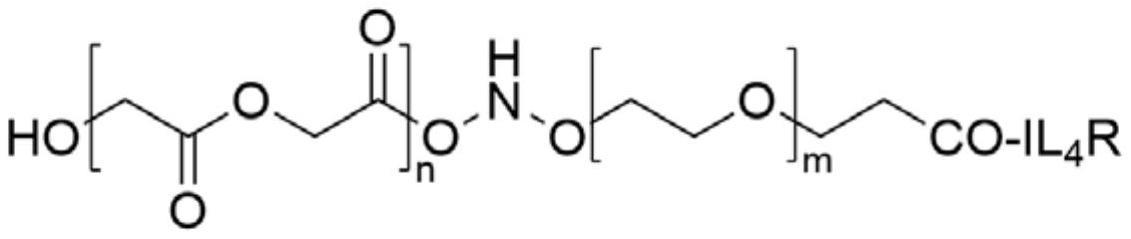
3、一种纳米药物递送载体,所述递送载体为il4rpep-1-聚乳酸羟基乙酸共聚物-聚乙二醇纳米颗粒,所述il4rpep-1-聚乳酸羟基乙酸共聚物-聚乙二醇纳米颗粒化学结构如式ⅰ所示:
4、
5、其中,所述il4rp为il4rpep-1,所述n=50,m=40-70。
6、进一步的,聚乳酸羟基乙酸共聚物的分子质量为38000-54000da;聚乙二醇的分子质量为2000-3500da;il4rpep-1的氨基酸序列为crkrldrnc。
7、进一步的,所述纳米药物递送载体的粒径为为154.6-175.5nm。
8、本发明的第二个目的是提供前述纳米药物递送载体的制备方法,所述方法包括以下步骤:
9、(1)plga-nhs的制备:称取1-100mg当量的plga溶解于丙酮中,加入edc和nhs,室温条件下反应4~12h,形成活化的plga-nhs;
10、(2)plga-peg聚合物的制备:向步骤(1)形成的活化的plga-nhs中加入100mg当量的peg,室温条件下继续搅拌12-48h,产物进行透析、真空冷冻干燥,得到plga-peg聚合物;优选的,所述透析的分子截留量为4000da;
11、(3)il4rpep-1-plga-peg三嵌段聚合物的制备:将步骤(2)得到的plga-peg聚合物配置成10mg/ml的溶液,il4rpep-1配置成5mg/ml的溶液,将plga-peg聚合物溶液和il4rpep-1溶液按1:1体积比反应,室温下添加edc、nhs进行催化,遮光搅拌反应12-48h,产物进行透析、真空冷冻干燥,获得il4rpep-1-plga-peg三嵌段聚合物;优选的,遮光搅拌反应温度为4℃;
12、(4)ipp nps的制备:将1-100mg当量的il4rpep-1-plga-peg三嵌段聚合物加入到丙酮溶液中,充分溶解,将其加入到质量百分比1-20%聚乙烯醇溶液中,在4℃条件下超声;超声结束后,将其加入到等体积的ddh2o中,最后通过离心法得到il4rpep-1-聚乳酸羟基乙酸共聚物-聚乙二醇纳米颗粒;优选的,所述超声在4℃条件下。
13、本发明的第三个目的是提供一种药物组合物,所述药物组合物包括前述的纳米药物递送载体,所述药物组合物还包括阿氟色替和塞来昔布,所述纳米药物递送载体包载阿氟色替和塞来昔布。
14、进一步的,所述纳米药物递送载体、阿氟色替、塞来昔布的质量比分别为5:1:1。
15、本发明的第四个目的是提供前述的纳米药物递送载体或前述的药物组合物在制备治疗肿瘤的药物中的应用。
16、进一步的,所述肿瘤为黑色素瘤。将asb和cxb联合使用,并通过纳米药物递送载体进行靶向递送,对体外黑色素瘤的发展具有明显抑制作用。
17、本发明技术方案相对于现有技术具有以下有益效果:
18、在本发明中,通过制备一种新型纳米药物递送系统ipp nps,用于共递送asb和cxb至黑色素瘤细胞中。分别利用asb和cxb药理学特征,在杀伤黑色素瘤细胞的同时通过激活细胞毒性cd8+t淋巴细胞的浸润、促使肿瘤相关m2型巨噬细胞重编程为m1型巨噬细胞等,通过协同作用在抑制黑色素瘤生长的同时重塑肿瘤免疫微环境,提高抗肿瘤活性,进而改善黑色素瘤的病理进程。
19、本发明首次利用ipp nps药物递送系统递送asb和cxb联合治疗黑色素瘤。具体来说,首先合成ipp nps药物递送系统,并对其进行表征和体外释放、摄取机制研究。在此基础上合成载药asb&cxb ipp nps,在一方面利用人黑色素瘤细胞a375、sk-mel-28作为模式细胞,进行体外asb抗肿瘤药效评估,通过cck-8、tunel和流式结果发现asb在两种人黑色素瘤细胞中都表现出很强的促进肿瘤细胞凋亡的能力,且具有剂量依赖性,而载药的nps提高其抗肿瘤能力。另一方面,在本发明中我们通过诱导人单核细胞白血病细胞thp-1成巨噬细胞,加入il4和il13刺激使其极化为m2型。在分子水平上,我们发现cxb能促使巨噬细胞m2向m1型转变,而载药的nps促进了这一种重编程效应。综上所述。本发明发现cxb可以通过促使巨噬细胞重编程改善肿瘤免疫抑制微环境。同时,我们还分别在细胞水平和动物水平全面评估其安全性。本发明所公开的ipp nps药物递送系统靶向共递送asb和cxb可以有效的改善黑色素瘤治疗效果。
20、本发明构建用于协同给药的ipp nps药物递送系统,并对其生物安全性和肿瘤靶向性进行了全面评估。我们利用该纳米药物递送系统兼具主动和被动靶向的优势,成功将asb和cxb联合递送到黑色素瘤组织部位。与此同时,体外对asb和cxb联合作用效果进行评估,结果显示其药效大于单独使用药效,该组合能明显抑制黑色素瘤的生长,改善肿瘤免疫抑制微环境,具有较强的抗黑色素瘤功效。
- 还没有人留言评论。精彩留言会获得点赞!