一种具有靶向功能的治疗脑卒中的氢化可的松多功能超声微泡的制作方法
1.本发明涉及生物医用技术领域,具体涉及一种具有靶向功能的治疗脑卒中的氢化可的松多功能超声微泡。
背景技术:
2.脑梗死又称缺血性卒中,中医称之为卒中或中风。本病系由各种原因所致的局部脑组织区域血液供应障碍,导致脑组织缺血缺氧性病变坏死,进而产生临床上对应的神经功能缺失表现。缺血性脑卒中一方面是血管堵塞导致大脑局部区域血流减少,另外一个重要的病理过程是缺血后坏死和凋亡引起神经细胞死亡,脑缺血坏死会激活脑内m2型小胶质细胞在局部发挥吞噬作用,充当脑内巨噬细胞功能;然后向m1型转化,在脑损伤区域分泌大量炎症前介质,加剧神经元的死亡。针对继发炎症抑制m1型活性,促进m2型转化以利于神经突触的再连接以重塑神经功能网络是脑卒中治疗的中的热点问题。
3.血脑屏障(blood-brain barrier,bbb)是脑微血管周围的复杂的、发挥主动和被动功能的屏障系统,由于bbb的存在,不仅严格限制了血液中的神经毒性物质、炎症因子、免疫细胞等进入中枢神经系统(cns),同时也使得具有潜在应用价值的治疗脑损伤和脑肿瘤的药物应用受到限制。开放血脑屏障及靶向调控小胶质细胞是实现脑卒中炎症有效治疗的关键,超声联合造影剂可介导血脑屏障的短暂性安全开放,通过技术偶联实现药物靶向输送至小胶质细胞的重要靶点,相关药物可以抑制m1型小胶质细胞活性,促进m2型增殖及神经功能网络的重建。现有技术中常常通过薄膜水化法制作超声微泡,通过化学联合将靶向剂及靶向药物与微泡进行链接,制作出含有靶向作用的药物超声微泡,普通薄膜水化法制备的粒子粒径在0.2-5um之间,粒径大小较大,不易通过肺循环及血脑屏障,因而制备一种粒径小,容易通过肺循环与血脑屏障的微泡是本领域技术人员亟需解决的技术问题。
技术实现要素:
4.本发明针对上述问题,提供了一种具有靶向功能的治疗脑卒中的氢化可的松多功能超声微泡。解决了现有技术中微泡粒径过大,不易通过血脑屏障的问题。
5.为了实现上述目的,本发明所采用的技术方案如下:本发明的一种具有靶向功能的治疗脑卒中的氢化可的松多功能超声微泡,主要以dspc(2-二硬脂酰-sn-甘油-3-磷酸-线)和dspe-peg2000(1,2-二硬脂酰-sn-甘油-3-将磷酸乙醇胺
‑ꢀ
n-[甲氧基(聚乙二醇)-2000])为载体,加载靶向剂dpps(1,2
ꢀ‑
二棕榈酰-sn-甘油酸
‑ꢀ
o-3-膦
‑ꢀ
l-丝氨酸),包括0.9质量份的dspc,0.05质量份的dspe-peg2000,0.05质量份的靶向剂dpps,每1ml微泡中添加0.4mg氢化可的松。
[0006]
进一步地,所述多功能超声微泡的制备方法如下:一种加载氢化可的松且具有靶向功能的磷脂微泡(hp-mbs)的制备:s1:将dspc(2-二硬脂酰-sn-甘油-3-磷酸-线)、胆固醇、dspe-peg2000(1,2-二硬
脂酰-sn-甘油-3-将磷酸乙醇胺
‑ꢀ
n-[甲氧基(聚乙二醇)-2000])以及dpps(1,2
ꢀ‑
二棕榈酰-sn-甘油酸
‑ꢀ
o-3-膦
‑ꢀ
l-丝氨酸)按照摩尔比为80-90:0-10:5:5溶于乙醇中形成2mg/l的脂类混合物,记为溶液1,将氢化可的松溶于三氯甲烷形成溶液2,将溶液2加入溶液1中,其中溶液1占溶液2的质量比为0.05-0.2;s2:将步骤s1中制备的溶液放入旋转蒸发器中进行旋转蒸发,并将装溶液的烧瓶置于恒温水浴中,所述恒温水浴的温度为40-45℃,可以加快有机溶剂的蒸发;s3:蒸发结束后,将烧瓶内的溶液置于真空干燥箱中干燥以除去有机溶剂残留物,所述烧瓶开口处覆盖一层设有若干小孔的伞膜,在干燥的过程中可以有效避免灰尘或污染物的进入;s4:给干燥的脂质膜中加入1ml pbs,以最大速度将溶液涡旋三次,每次10s,使脂质膜能够均匀的悬浮在溶液中,再将其置入水浴超声仪中超声处理15s,使脂质膜能够更均匀的悬浮在溶液中,超声结束后静置8h以上,从而使脂质物质能够有效的进行水合;s5:将1,2-丙二醇、丙三醇以及步骤s4中所得溶液在3ml的玻璃小瓶中进行混合,混合均匀后用全氟丙烷对瓶内进行填充,填充完成后在摇床上搅拌45s即得。
[0007]
更进一步地,所述步骤s1中将dspc、胆固醇、dspe-peg2000以及dpps按照摩尔比为80:10:5:5溶于乙醇中形成溶液1,将氢化可的松溶于三氯甲烷形成溶液2,将溶液2加入溶液1中,其中溶液1占溶液2的质量比为0.05。
[0008]
更进一步地,所述步骤s1中将dspc、胆固醇、dspe-peg2000以及dpps按照摩尔比为85:5:5:5溶于乙醇中形成溶液1,将氢化可的松溶于三氯甲烷形成溶液2,将溶液2加入溶液1中,其中溶液1占溶液2的质量比为0.1。
[0009]
更进一步地,所述步骤s1中将dspc、胆固醇、dspe-peg2000以及dpps按照摩尔比为90:0:5:5溶于乙醇中形成溶液1,将氢化可的松溶于三氯甲烷形成溶液2,将溶液2加入溶液1中,其中溶液1占溶液2的质量比为0.2。
[0010]
更进一步地,所述多功能超声微泡的平均粒径为1.54
±
0.51μm,浓度为2mg/ml。
[0011]
更进一步的,所述步骤s5中1,2-丙二醇、丙三醇与所述步骤s4中pbs的体积比为1:1:10。
[0012]
进一步地,所述步骤s5中摇床为vialmix摇床。
[0013]
与现有技术相比,本发明的有益效果:本发明方法在旋转蒸发后增加了真空干燥的环节,将有机溶剂彻底蒸发滤掉,加入缓冲液后,采用超声波仪进行再次粉碎处理使处理过的微泡粒径稳定在1.45um左右,具有穿过肺循环与血脑屏障的安全性。此外将脂质体与氢化可的松用不同溶剂溶解,最大限度增加了其溶解度,为获得氢化可的松较高的包封率奠定了基础。
[0014]
采用本发明方法制备的多功能超声微泡联合utmd(超声靶向微泡破坏技术)不仅可以打开血脑屏障,微泡上面还可以链接靶向剂及靶向药物,能够在血脑屏障开放后高效、快速、精准的对靶向区域进行治疗。血脑屏障打开后,在药物可以进入大脑的同时,全身血液的毒素也有可能会进入大脑,靶向药物的另一个功能是加快血脑屏障的关闭,在靶向给药的同时加速血脑屏障的关闭,最大限度的治疗疾病同时保护大脑。
附图说明
[0015]
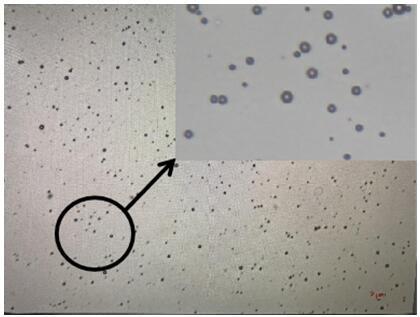
图1是本发明的多功能超声微泡在显微镜明场下的结构图2是本发明的多功能超声微泡的粒径分布图图3是本发明的多功能超声微泡在静置不同时间后的粒径图图4是本发明的多功能超声微泡稀释不同比例后的造影效果图图5为不同浓度的多功能超声微泡与huvec细胞相结合的细胞活力图图6为不同浓度的多功能超声微泡与raw细胞相结合的细胞活力图图7为连接荧光剂的多功能超声微泡与huvec细胞及raw细胞结合的荧光图图8为连接荧光剂的多功能超声微泡与huvec细胞及raw细胞结合的荧光折线图图9为m2型小胶质细胞数量随着hp-mbs诱导时间的变化图图10为m1型小胶质细胞数量与m2型小胶质细胞数量随着hp-mbs诱导时间的变化图图11为大鼠试验中经过不同处理后的大鼠在相同时间内大脑伊思文蓝的渗出量示意图图12 为试验大鼠脑实质中伊文思蓝的组织含量。
具体实施方式
[0016]
为了使本发明的目的及优点更加清楚明白,以下结合实施例对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
[0017]
以下实施例中所涉及的仪器、试剂、材料等,若无特别说明,均为现有技术中已有的常规仪器、试剂、材料等,可通过正规商业途径获得。下列实施例中所涉及的实验方法、检测方法等,若无特别说明,均为现有技术中已有的常规实验方法、检测方法等。
实施例
[0018]
本实施例中一种具有靶向功能的治疗脑卒中的氢化可的松多功能超声微泡,主要以dspc和dspe-peg2000为载体,加载靶向剂dpps,包括0.9质量份的dspc,0.05质量份的dspe-peg2000,0.05质量份的靶向剂dpps,每1ml微泡中添加0.4mg氢化可的松。具体制备方法如下:s1:将dspc(2-二硬脂酰-sn-甘油-3-磷酸-线)、胆固醇、dspe-peg2000(1,2-二硬脂酰-sn-甘油-3-将磷酸乙醇胺
‑ꢀ
n-[甲氧基(聚乙二醇)-2000])以及dpps(1,2
ꢀ‑
二棕榈酰-sn-甘油酸
‑ꢀ
o-3-膦
‑ꢀ
l-丝氨酸)分别按照摩尔比为80:10:5:5、85:5:5:5及90:0:5:5溶于乙醇中形成2mg/l的脂类混合物,记为溶液1,将氢化可的松溶于三氯甲烷形成溶液2,将溶液2加入溶液1中,其中溶液1占溶液2的质量比分别为为0.05、0.1和0.2;s2:将步骤s1中制备的溶液放入旋转蒸发器中进行旋转蒸发,并将装溶液的烧瓶置于恒温水浴中,所述恒温水浴的温度为40-45℃,可以加快有机溶剂的蒸发;s3:蒸发结束后,将烧瓶内的溶液置于真空干燥箱中干燥以除去有机溶剂残留物,所述烧瓶开口处覆盖一层设有若干小孔的伞膜,在干燥的过程中可以有效避免灰尘或污染物的进入;s4:给干燥的脂质膜中加入1ml pbs,以最大速度将溶液涡旋三次,每次10s,使脂
utmd-0.5heb、hp-mbs-utmd-1heb、hp-mbs-utmd-2heb、hp-mbs-utmd-4heb、hp-mbs-utmd-6heb、hp-mbs-utmd-8heb、hp-mbs-utmd-10heb),每组3只,对照组通过尾静脉向大鼠注射1ml生理盐水,实验组分别注入1ml含氢化可的松和不含氢化可的松的mbs,按照分组进行utmd500s,在不同时间点(0h、0.5h、1h、2h、4h、6h、8h、10h)通过尾静脉向大鼠注射5 ml/kg的2%伊文思蓝(eb),在相同时间点测量伊文思蓝渗出量,参照附图11。循环2小时后,通过腹腔注射戊巴比妥钠(100 mg/kg)麻醉动物,然后用肝素生理盐水灌流,再用4%多聚甲醛灌注,大鼠四肢僵硬停止,断头取脑称重拍照,将称重后的脑组织粉碎加入10ml体积分数4%甲酰胺中萃取脑实质中渗出的伊文思蓝,通过测量610 nm的吸光度确定伊文思蓝的浓度,并根据线性标准曲线量化伊文思蓝的组织含量,并以伊文思蓝(ng)/组织(g)表示,参照附图12。
[0029]
由附图12可知,在相同时间点用含有氢化可的松微泡进行爆破,伊文思蓝的渗出量远低于用不含有氢化可的松微泡爆破的伊文思蓝渗出量,说明含有氢化可的松的微泡在提前关闭血脑屏障方面起到了很大作用。
[0030]
综上,采用本发明方法制备的多功能超声微泡粒径小,在utmd技术的辅助下不仅可以打开血脑屏障,还可以在微泡上面链接靶向剂及靶向药物,能够在血脑屏障开放后高效、快速、精准的对靶向区域进行治疗。血脑屏障打开后,在药物可以进入大脑的同时,全身血液的毒素也有可能会进入大脑,靶向药物能够加快血脑屏障的关闭,在靶向给药的同时加速血脑屏障的关闭,在最大限度治疗疾病的同时保护大脑。
[0031]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1