X射线显影化合物及其制备方法、X射线显影微球及其制备方法与流程
x射线显影化合物及其制备方法、x射线显影微球及其制备方法
技术领域
1.本技术涉及x射线下可视化的栓塞技术领域,且特别涉及一种x射线显影化合物及其制备方法、x射线显影微球及其制备方法。
背景技术:
2.自经导管动脉栓塞术(transcatheter arterial embolization,简称tae)的概念提出40多年来,选择合适的栓塞材料是该技术发展关键的一环。由于碘原子对x射线的强吸收,含碘化合物,尤其是含碘有机化合物,可在x射线检测下人体内显影。因此,可以在栓塞材料上连接含碘的有机化合物,从而使栓塞材料具有x射线显影的功能。
3.专利cn102781974b描述了采用碘代苄溴或甲磺酸苄酯在碱性条件下修饰聚乙烯醇(pva)微球,得到具有碘代苄基醚结构的聚乙烯醇栓塞物,此栓塞物具有x射线下显影功能。但是此方法在显影修饰的同时消耗羟基,致使修饰后的pva亲水性变差。
4.专利114805644a描述了在碱性催化剂条件下将环氧氯丙烷接枝到聚乙烯醇上,在聚乙烯醇上引入了氯原子,得到活化的聚乙烯醇;再由活化的聚乙烯醇与碘代苄醇通过醚化反应,使得碘代苄基接枝到聚乙烯醇上,进而得到了含碘的聚乙烯醇聚合物。该聚合物在非生理溶液可溶且在生理条件下不溶,可用作医学治疗中液体栓塞材料,具有稳定性和显影效果。此方法所述显影测基的化学结构为-och2ch(oh)ch2or,r为碘代苄基。此方法在显影修饰的同时生成一个羟基,可较好保持pva的亲水性能,但是显影修饰需要两步反应,工艺复杂。此外,在工艺中引入活性的氯离子,氯代烃的生物安全性有待考证,此工艺的安全性风险较大。
技术实现要素:
5.针对现有技术的不足,本技术实施例的目的包括提供一种x射线显影化合物及其制备方法、x射线显影微球及其制备方法,基于一类新的显影化合物,能够与聚乙烯醇微球一步反应,工艺安全性好,得到具有x射线显影功能的聚乙烯醇微球,且其亲水性较好。
6.第一方面,本技术实施例提供了一种x射线显影化合物,x射线显影化合物的结构式如下:
[0007][0008]
其中,n是1-5的整数。
[0009]
在上述技术方案中,通过醚键连接碘代芳基与环氧基,形成x射线显影化合物,该显影化合物中的环氧基容易与聚乙烯醇微球中的羟基发生一步反应,以使聚乙烯醇微球具有显影功能,并且制备的显影微球亲水性较好。
[0010]
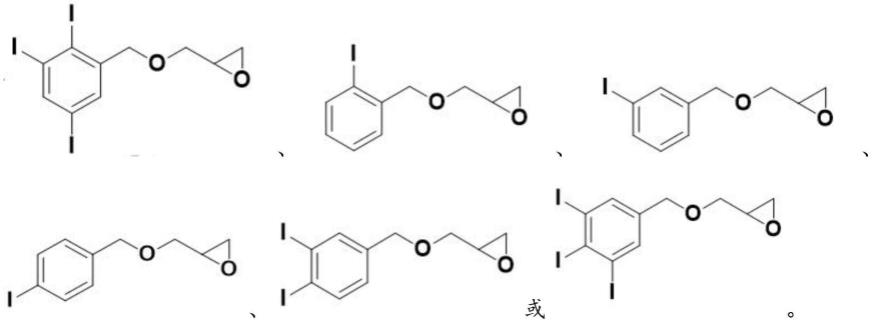
在本技术的部分实施例中,x射线显影化合物的结构式为:
[0011][0012]
第二方面,本技术提供一种上述x射线显影化合物的制备方法,反应式一:
[0013][0014]
上述技术方案中,由碘代苄醇类化合物与3-环氧丙烷通过一步反应可以得到显影化合物,其反应条件较为温和,制备较为简单。
[0015]
第三方面,本技术提供一种x射线显影微球,显影微球的结构式如下:
[0016][0017]
其中,n是1-5的整数,通过控制交联反应条件和时间可以得到m值不同的x射线显影微球,其中m是大于1的正整数。
[0018]
在上述技术方案中,该x射线显影微球的亲水性较好。
[0019]
在本技术的部分实施例中,显影微球的结构式如下:
[0020][0021]
第四方面,本技术提供一种x射线显影微球的制备方法,包括:在有机酸或有机碱的催化作用下,使上述x射线显影化合物的环氧基与聚乙烯醇微球上的至少部分羟基反应,以形成醚键结合。
[0022]
在上述技术方案中,可以使x射线显影微球的制备较为简单,直接一步反应就可以使聚乙烯醇微球具有显影功能,同时,得到的显影微球的亲水性较好。
[0023]
在本技术的部分实施例中,催化剂为有机酸,制备方法包括:
[0024]
反应式二:
[0025][0026]
在上述条件下,以有机酸作为催化剂,在温度较低的情况下一步反应,对聚乙烯醇微球进行修饰,以得到显影微球。
[0027]
在本技术的部分实施例中,x射线显影化合物与聚乙烯醇微球的质量比为(1.5-3):1;x射线显影化合物与有机酸的质量比为1:(0.1-2)。
[0028]
在本技术的部分实施例中,有机酸为甲磺酸、三氟甲磺酸、对甲苯磺酸、三氟乙酸中的至少一种;溶剂为二甲基亚砜、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮中的至少一种。
[0029]
在本技术的部分实施例中,催化剂为有机碱,所述制备方法包括:
[0030]
反应式三:
[0031][0032]
在本技术的部分实施例中,x射线显影化合物与聚乙烯醇微球的质量比为(1.5-3):1;x射线显影化合物与有机碱的质量比为1:(0.5-3)。
[0033]
在本技术的部分实施例中,有机碱为三乙胺、二异丙基乙胺、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,4-二氮杂二环[2.2.2]辛烷中的至少一种;溶剂为二甲基亚砜、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮中的至少一种。
附图说明
[0034]
为了更清楚地说明本技术实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本技术的某些实施例,因此不应被看作是对范围的限定。
[0035]
图1为本技术实施组提供的聚乙烯醇原料湿球的光学图片;
[0036]
图2为实施例一提供的显影微球的光学图片;
[0037]
图3为实施例二提供的显影微球的光学图片;
[0038]
图4为实施例三提供的显影微球的光学图片;
[0039]
图5为实施例四提供的显影微球的光学图片;
[0040]
图6为实施例五提供的显影微球的光学图片;
[0041]
图7为实施例六提供的显影微球的光学图片;
[0042]
图8为实施例七提供的显影微球的光学图片;
[0043]
图9为实施例八提供的显影微球的光学图片;
[0044]
图10为实施例九提供的显影微球的光学图片;
[0045]
图11为实施例十提供的显影微球的光学图片;
[0046]
图12为实施例十一提供的显影微球的光学图片;
[0047]
图13为实施例十二提供的显影微球的光学图片;
[0048]
图14为对比例一提供的显影微球的光学图片;
[0049]
图15为对比例二提供的显影微球的光学图片。
具体实施方式
[0050]
为使本技术实施例的目的、技术方案和优点更加清楚,下面对本技术的技术方案进行清楚、完整地描述。
[0051]
x射线显影化合物
[0052]
本技术中,x射线显影化合物的结构式如下:
[0053][0054]
其中,n是1-5的整数。
[0055]
在上述技术方案中,i原子的作用是在x射线照射下显影,i原子的个数可以是1个、2个、3个、4个或5个。i原子的取代个数并不会导致显影剂与微球结合后的显影微球亲水性、悬浮性等差异。
[0056]
在上述技术方案中,通过醚键连接碘代芳基与环氧基,形成x射线显影化合物,该显影化合物中的环氧基容易与聚乙烯醇微球中的羟基发生一步反应,以使聚乙烯醇微球具有显影功能,并且制备的显影微球亲水性较好。
[0057]
在一些实施例中,x射线显影化合物的结构式可以为:
[0058][0059]
在另一些实施例中,x射线显影化合物的结构式还可以为:
[0060][0061]
x射线显影化合物的制备方法
[0062]
上面介绍了x射线显影化合物的结构式以后,下面对x射线显影化合物的制备方法进行具体介绍,其通过反应式一提供的方法进行制备,反应式一如下:
[0063][0064]
可选地,在绝氧环境中,将化合物ii、化合物iii、四丁基硫酸氢铵(2-20mol%)和四氢呋喃(thf)混合均匀形成溶液;在0-5℃的条件下加入40-60%(w/w)氢氧化钠或/和氢氧化钾溶液,反应20-40min后升至室温反应4-24h。
[0065]
例如:氮气保护下,在单口反应瓶中依次加入化合物ii(1.0eq.)、化合物iii(1.1eq.)、四丁基硫酸氢铵(2-20mol%)和thf,充分搅拌溶解。0-5℃下加入40-60%(w/w)氢氧化钠溶液,反应20-40min后升至室温反应4-24h。tlc监控原料反应完全后,低温下减压
旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得化合物i。
[0066]
x射线显影微球
[0067]
该x射线显影微球的结构式如下:
[0068][0069]
其中,n是1-5的整数。
[0070]
在上述技术方案中,该x射线显影微球的亲水性较好。
[0071]
在一些实施例中,显影微球的结构式可以为:
[0072][0073]
在另一些实施例中,显影微球的结构式还可以为:
[0074][0075]
x射线显影微球的制备方法
[0076]
本技术中,在有机酸或有机碱的催化作用下,使上述x射线显影化合物的环氧基与
聚乙烯醇微球上的至少部分羟基反应,以形成醚键结合。可以使x射线显影微球的制备较为简单,直接一步反应就可以使聚乙烯醇微球具有显影功能,同时,得到的显影微球的亲水性较好。
[0077]
其中,聚乙烯醇微球的制备方法为:聚乙烯醇与n-(2,2-二甲氧基乙基)-2-丙烯酰胺进行酸催化反应,得到n-(2,2-二甲氧基乙基)-2-丙烯酰胺接枝的大分子聚乙烯醇单体;将大分子聚乙烯醇单体与带磺酸基的水溶性单体、引发剂和水配制成水相,机械搅拌下将水相加入油相中,形成油包水的反相悬浮聚合体系;将此反相悬浮聚合体系升温至反应温度,加入催化剂进行悬浮聚合反应;反应得到聚乙烯醇微球,经净化、干燥过程后得到聚乙烯醇微球干球。
[0078]
可选地,将聚乙烯醇溶解在水中,然后加入n-(2,2-二甲氧基乙基)-2-丙烯酰胺,加入盐酸在室温下反应10h及以上,再使用氢氧化钠中和,得到大分子聚乙烯醇单体溶液。将醋酸丁酸纤维素溶解在乙酸丁酯中形成油相;将丙烯酰胺基-2-甲基丙磺酸钠盐溶于水中,加入大分子聚乙烯醇单体溶液和过硫酸钾形成水相。在搅拌条件下,将水相滴加至油相,滴加完毕后升温至50-60℃,加入四甲基乙二胺,反应7-9h。经过一系列纯化后干燥得到聚乙烯醇微球干球。
[0079]
在一些实施例中,催化剂为有机酸,制备方法包括:
[0080]
反应式二:
[0081][0082]
可选地,将聚乙烯醇微球干球、x射线显影化合物i和溶剂混合后加热溶胀,溶胀后加入有机酸,于40-90℃下反应24-48h。反应后清洗、除杂。
[0083]
其中,x射线显影化合物与聚乙烯醇微球的质量比为(1.5-3):1;x射线显影化合物与有机酸的质量比为1:(0.1-2)。有机酸为甲磺酸、三氟甲磺酸、对甲苯磺酸、三氟乙酸中的至少一种;溶剂为二甲基亚砜(dmso)、n,n-二甲基甲酰胺(dmf)、n,n-二甲基乙酰胺、n-甲基吡咯烷酮(nmp)中的至少一种。
[0084]
作为示例性地,反应的温度为40℃、50℃、60℃、70℃、80℃或90℃;反应的时间为24h、28h、32h、36h、40h、44h或48h;x射线显影化合物与聚乙烯醇微球的质量比为1.5:1、2:1、2.5:1或3:1;x射线显影化合物与有机酸的质量比为1:0.1、1:0.5、1:1、1:1.5或1:2。
[0085]
例如:将聚乙烯醇微球干球、x射线显影化合物i和dmso混合后加热溶胀,溶胀后加入甲磺酸,于40-90℃反应24-48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸。
[0086]
在另一些实施例中,催化剂为有机碱,所述制备方法包括:
[0087]
反应式三:
[0088][0089]
可选地,将聚乙烯醇微球干球、x射线显影化合物i和溶剂混合后加热溶胀,溶胀后加入有机碱,于60-120℃下反应24-48h。反应后清洗、除杂。
[0090]
其中,x射线显影化合物与聚乙烯醇微球的质量比为(1.5-3):1;x射线显影化合物与有机碱的质量比为1:(0.5-3)。有机碱为三乙胺、二异丙基乙胺、1,8-二氮杂双环[5.4.0]十一碳-7-烯、1,4-二氮杂二环[2.2.2]辛烷中的至少一种;溶剂为二甲基亚砜、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮中的至少一种。
[0091]
作为示例性地,反应的温度为60℃、70℃、80℃、90℃、100℃、110℃或120℃;反应的时间为24h、28h、32h、36h、40h、44h或48h;x射线显影化合物与聚乙烯醇微球的质量比为1.5:1、2:1、2.5:1或3:1;x射线显影化合物与有机碱的质量比为1:0.5、1:1、1:1.5、1:2、1:2.5或1:3。
[0092]
例如:将聚乙烯醇微球干球、x射线显影化合物i和dmso混合后加热溶胀,溶胀后加入二异丙基乙胺,于60-120℃反应24-48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱。
[0093]
基于上述的x射线显影化合物i,通过一步反应制备得到的x射线显影微球,且显影微球的亲水性较好。
[0094]
为使本技术实施例的目的、技术方案和优点更加清楚,下面将对本技术实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0095]
实施例1:化合物i-1的合成
[0096][0097]
氮气保护下,在单口反应瓶中依次加入化合物ii-1(20.6mmol,10g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30min后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-1(9.5g,85%),为浅黄色黏稠油状液体(纯度98%)。
[0098]
将得到的目标产物i-1经hplc(高效液相色谱),lcms(液相质谱)和1h-nmr(核磁氢谱)表征。方法如下:
[0099]
hplc:测试仪器为安捷伦1260型高效液相色谱仪;色谱柱为十八烷基键合硅胶柱;流动相为0.1%磷酸水溶液和甲醇;检测器为vwd检测器;取0.1mg左右样品于样品瓶中,加dmso溶解后直接进样检测;根据积分面积确定产品纯度。
[0100]
lcms:测试仪器为安捷伦1260-6125型高效液相色谱质谱联用仪;色谱柱为十八烷基键合硅胶柱;流动相为0.1%甲酸水溶液和甲醇;检测器为质谱检测器;取0.1mg左右样品于样品瓶中,加dmso溶解后直接进样检测,识别主要离子峰。
[0101]1h-nmr:测试仪器为bruker 400m核磁测试仪;采用探头为常温氢谱探头;取20-30mg样品加入核磁管中,加入0.3-0.5ml氘代氯仿溶解后测试。得到的目标产物i-1的核磁氢谱为:1h nmr(400mhz,cdcl3)δ8.07(d,j=2.1hz,1h),7.84(d,j=2.1hz,1h),4.65-4.56(m,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.17(m,1h),2.82(t,j=4.7hz,1h),2.65-2.63(m,1h);ms(esi):m/z 543(m+h
+
)。
[0102]
实施例2:化合物i-2的合成
[0103][0104]
氮气保护下,在单口反应瓶中依次加入化合物ii-2(20.6mmol,4.8g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30分钟后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-2(5.38g,90%),为浅黄色油状液体(纯度98%)。检测方法同实施例1,得到结果为:1h nmr(400mhz,cdcl3)δ7.39-7.26(m,4h),4.65-4.60(m,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.17(m,1h),2.82(t,j=4.7hz,1h),2.66-2.64(m,1h);ms(esi):m/z 291(m+h
+
)。
[0105]
实施例3:化合物i-3的合成
[0106][0107]
氮气保护下,在单口反应瓶中依次加入化合物ii-3(20.6mmol,4.8g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30分钟后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-3(5.44g,91%),为浅黄色油状液体(纯度98%)。检测方法同实施例1,得到结果为:1h nmr(400mhz,cdcl3)δ7.41-7.25(m,4h),4.64-4.53(m,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.17(m,1h),2.82(t,j=4.7hz,1h),2.66-2.63(m,1h);ms(esi):m/z 291(m+h
+
)。
[0108]
实施例4:化合物i-4的合成
[0109][0110]
氮气保护下,在单口反应瓶中依次加入化合物ii-4(20.6mmol,4.8g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30分钟后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-4(5.68g,95%),为浅黄色油状液体(纯度98%)。检测方法同实施例1,得到结果为:1h nmr(400mhz,cdcl3)δ7.45(d,j=13.2hz,2h),7.05(d,j=13.2hz,2h),4.68(s,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.17(m,1h),2.82(t,j=4.7hz,1h),2.66-2.63(m,1h);ms(esi):m/z 291(m+h
+
)。
[0111]
实施例5:化合物i-5的合成
[0112][0113]
氮气保护下,在单口反应瓶中依次加入化合物ii-5(20.6mmol,7.4g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30分钟后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-5(5.44g,91%),为浅黄色油状液体(纯度98%)。检测方法同实施例1,得到结果为:1h nmr(400mhz,cdcl3)δ7.63(dd,j=11.2,3.2hz,1h),7.45(dd,j=11.2,5.4hz,1h),7.18(dd,j=5.4,3.2hz,1h),4.64-7.55(m,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.18(m,1h),2.82(t,j=4.7hz,1h),2.65-2.63(m,1h);ms(esi):m/z 417(m+h
+
)。
[0114]
实施例6:化合物i-6的合成
[0115][0116]
氮气保护下,在单口反应瓶中依次加入化合物ii-6(20.6mmol,10g)、化合物iii(20.6mmol,1.6ml)、四丁基硫酸氢铵(1.0mmol,339.5mg)和thf(50ml),充分搅拌溶解。0℃下加入5ml 50%(w/w)氢氧化钠溶液,反应30分钟后升至室温反应4-24小时。tlc监控原料反应完全后,低温下减压旋干thf,加入无水乙醚和饱和氯化钠溶液。分液,有机相用饱和食盐水洗涤3次,无水硫酸钠干燥后过滤,减压旋干得目标化合物i-6(9.7g,87%),为浅黄色黏稠油状液体(纯度98%)。检测方法同实施例1,得到结果为:1h nmr(400mhz,cdcl3)δ8.03(s,2h),4.68(s,2h),3.82(dd,j=11.4,3.0hz,1h),3.46(dd,j=11.4,5.9hz,1h),3.21-3.18(m,1h),2.82(t,j=4.7hz,1h),2.63-2.60(m,1h);ms(esi):m/z 543(m+h
+
)。
[0117]
实施组:pva干球的制备:
[0118]
在装有顶置式机械搅拌250ml三口瓶中加入100ml纯化水,加入约15g的pva(型号1888),升温至95℃溶解,降至室温;加入0.7654g的n-(2,2-二甲氧基乙基)-2-丙烯酰胺(naaada),随后加入10ml浓盐酸,反应在室温进行14小时,然后使用2.5m的氢氧化钠溶液中和至ph=7,得到大分子聚乙烯醇单体溶液。
[0119]
在装有顶置式机械搅拌1l三口瓶中加入600ml乙酸丁酯,加入18g醋酸丁酸纤维素溶解,得到油相;8.61g的丙烯酰胺基-2-甲基丙磺酸钠盐(amps钠)溶于60ml水中,加入160g大分子聚乙烯醇单体溶液,加入1.5g过硫酸钾,得到水相。
[0120]
转速设为400rpm,将水相滴加至油相中;滴加完毕后升温至55℃,加入2.2ml四甲基乙二胺,反应8h。经过一系列纯化后干燥得到原料干球。
[0121]
实施例一:化合物i-1有机酸催化下制备显影微球
[0122][0123]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-1和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为632mg。取部分干球测量其干球碘含量为40.1%。计算其湿球碘含量为127mg/ml。
[0124]
实施例二:化合物i-1有机碱催化下制备显影微球
[0125][0126]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-1和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为567mg。取部分干球测量其干球碘含量为30.1%。计算其湿球碘含量为85.3mg/ml。
[0127]
实施例三:化合物i-2有机酸催化下制备显影微球
[0128][0129]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-2和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为551mg。取部分干球测量其干球碘含量为15.1%。计算其湿球碘含量为41.6mg/ml。
[0130]
实施例四:化合物i-2有机碱催化下制备显影微球
[0131][0132]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-2和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为502mg。取部分干球测量其干球碘含量为13.3%。计算其湿球碘含量为33.4mg/ml。
[0133]
实施例五:化合物i-3有机酸催化下制备显影微球
[0134][0135]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-3和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为535mg。取部分干球测量其干球碘含量为15.0%。计算其湿球碘含量为40.1mg/ml。
[0136]
实施例六:化合物i-3有机碱催化下制备显影微球
[0137]
[0138]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-3和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为515mg。取部分干球测量其干球碘含量为14.1%。计算其湿球碘含量为36.3mg/ml。
[0139]
实施例七:化合物i-4有机酸催化下制备显影微球
[0140][0141]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-4和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为530mg。取部分干球测量其干球碘含量为16.7%。计算其湿球碘含量为44.3mg/ml。
[0142]
实施例八:化合物i-4有机碱催化下制备显影微球
[0143][0144]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-4和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为533mg。取部分干球测量其干球碘含量为13.7%。计算其湿球碘含量为36.5mg/ml。
[0145]
实施例九:化合物i-5有机酸催化下制备显影微球
[0146][0147]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-5和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为618mg。取部分干球测量其干球碘含量为32.7%。计算其湿球碘含量为101mg/ml。
[0148]
实施例十:化合物i-5有机碱催化下制备显影微球
[0149][0150]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-5和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为603mg。取部分干球测量其干球碘含量为30.2%。计算其湿球碘含量为91.1mg/ml。
[0151]
实施例十一:化合物i-6有机酸催化下制备显影微球
[0152][0153]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-6和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml甲磺酸,保持60℃反应24h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和酸,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为698mg。取部分干球测量其干球碘含量为42.3%。计算其湿球碘含量为147.6mg/ml。
[0154]
实施例十二:化合物i-6有机碱催化下制备显影微球
[0155][0156]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球、10g化合物i-6和125ml dmso(二甲基亚砜),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入5ml二异丙基乙胺,升温至80℃反应48h。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为652mg。取部分干球测量其干球碘含量为40.7%。计算其湿球碘含量为132.7mg/ml。
[0157]
对比例一:显影微球的制备
[0158][0159]
氮气保护下,在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球和300ml nmp(n-甲基吡咯烷酮),调节搅拌转速为100rpm/min,于60℃加热溶胀。溶胀后加入
10g研碎的naoh,混合搅拌10分钟。加入100g 2,3,5-三碘苄溴,反应48h后降至室温。反应后将微球依次用nmp、dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为425mg。取部分干球测量其干球碘含量为10.7%。计算其湿球碘含量为22.7mg/ml。实验显示采用专利cn102781974b描述工艺,得到的显影微球碘含量低,且微球体积膨胀,反应过程中微球结构被部分破坏。由于2,3,5-三碘苄溴优先在微球表面反应,使表面亲水性变差,反应试剂难于到达微球内部,干球碘含量偏低。由于微球结构部分破坏,微球体积膨胀,一定体积微球的干重降低,致使湿球碘含量偏低。
[0160]
对比例二:显影微球的制备
[0161][0162]
在顶端装有机械搅拌桨的三口瓶中加入5g聚乙烯醇微球干球和50ml纯化水,调节搅拌转速为100rpm/min,于90℃加热溶胀。溶胀后加入11g环氧丙烷和0.25g naoh催化剂,于70℃反应,将反应液缓慢滴加到盛有甲醇沉淀剂的烧杯中,边滴加边用玻璃棒搅拌,pva微球再用甲醇反复抽滤洗涤三次后放于50~60℃下干燥至恒重,得到活化聚乙烯醇微球。
[0163]
在氮气流下,将得到的活化聚乙烯醇溶解于50ml无水nmp。在130℃下将反应混合物搅拌5分钟;然后使温度降至50℃。添加55g 2,3,5-三碘苄基醇(0.113mol),并搅拌反应混合物10分钟。然后,在10分钟内添加0.05g磨碎并干燥的naoh。在4小时之后,降至室温。反应后将微球依次用dmso、10%碳酸氢钠和水洗涤,除去残留的杂质和碱,得到显影微球。实验发现,制得的微球表面形貌较差,大量微球粘连在一起,无法分开。取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量为512mg。取部分干球测量其干球碘含量为17.3%。计算其湿球碘含量为44.3mg/ml。由于微球的表面变差和粘连,致使2,3,5-三碘苄醇难以到达微球内部,碘含量偏低。
[0164]
图1为本技术实施组提供的聚乙烯醇湿球的光学图片;图2为实施例一提供的显影微球的光学图片;图3为实施例二提供的显影微球的光学图片;图4为实施例三提供的显影微球的光学图片;图5为实施例四提供的显影微球的光学图片;图6为实施例五提供的显影微球的光学图片;图7为实施例六提供的显影微球的光学图片;图8为实施例七提供的显影微球的光学图片;图9为实施例八提供的显影微球的光学图片;图10为实施例九提供的显影微球的光学图片;图11为实施例十提供的显影微球的光学图片;图12为实施例十一提供的显影微球的光学图片;图13为实施例十二提供的显影微球的光学图片。从图1以及图2-图13可以看出,聚乙烯醇微球湿球的形貌良好,经过显影修饰以后,得到的产品为形貌良好,亲水性良好的球形。
[0165]
图14为对比例一提供的显影微球的光学图片。从图14可以看出,对比例一提供的微球体积膨胀、破坏。图15为对比例二提供的显影微球的光学图片。从图15可以看出,对比例二提供的微球形貌差,大量粘连。
[0166]
检测实施例一-实施例十二以及对比例一和对比例二提供的显影微球的性能进行检测,测试结果如表1,其测试方法如下:
[0167]
取2.0ml湿球,用丙酮干燥后,105℃下烘干5h至恒重后称量其重量。取部分干球测量其干球碘含量。
[0168]
称取约5mg样品于无尘灰纸上,按照《中国药典》第二部操作,吸收液为:10ml5g/l氢氧化钠与10ml 1%维生素c,急速通氧1min,用表面皿覆盖瓶口,静置10min,点燃包有样品的滤纸尾部,迅速将瓶塞插入燃烧瓶中,按紧瓶塞,并用少量水封闭瓶口,燃烧完毕后(应无灰色、黑色碎片或颗粒,若燃烧后留有应无灰色、黑色碎片或颗粒,表示供试品燃烧不完全,遇此情况应重新取样燃烧),立即充分振摇,使生成的烟雾完全吸入吸收液中,放置15min,开启瓶塞,用少量水冲洗瓶塞及铂丝,合并洗液及吸收液,同时同法做空白实验。加入3滴署红指示剂,用0.01mol/l硝酸银标准滴定液滴定,记录消耗体积,平行操作两次。
[0169]
计算:
[0170]
x=(c
×v×
127
×m湿球
)/(m
×v湿球
)
×
100%
[0171]
x:为样品中碘含量;
[0172]
c:为硝酸银浓度,mol/l;
[0173]
v:为硝酸银消耗体积,ml;
[0174]
m:为样品质量,mg;
[0175]
m(湿球):为湿球质量,mg;
[0176]
v(湿球):为湿球体积,ml;
[0177]
127:为碘的相对分子质量。
[0178]
湿球碘含量计算公式如下:
[0179]
湿球碘含量=(微球干重
×
干球碘含量)/湿球体积
[0180]
hu值测试方法:将各实施例显影微球进行micro ct测试,对根据上面方法制备的显影微球样品的不透射线性进行评估。在nunc冻存管小瓶中将珠粒悬浮于0.5%琼脂糖凝胶,使用装备有钨阳极的微型ct成像系统扫描器,利用微计算机断层扫描技术(微型ct成像系统),对显影微球的不透射线性进行测试。然后将图像分割从孔隙结构中分离出聚合物以便报告聚合物辐射密度。然后,使用在同一天得到的水标准品计算以hu为单位的辐射密度。
[0181]
表1显影微球的性能
[0182]
[0183]
从表1可以看出,在有机酸或有机碱的催化作用下,本技术提供的x射线显影化合物,均可以通过一步反应使聚乙烯醇微球具有显影功能。且使用有机酸作为催化剂,得到的显影微球的碘含量更高,hu值也更高,显影能力更强。
[0184]
以上所描述的实施例是本技术一部分实施例,而不是全部的实施例。本技术的实施例的详细描述并非旨在限制要求保护的本技术的范围,而是仅仅表示本技术的选定实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1