富勒烯制剂在制备治疗肠道癌症的药物中的应用的制作方法
1.本发明涉及生物医药领域,特别涉及一种用于治疗肠道癌症的口服富勒烯混悬液。
背景技术:
2.富勒烯是由不同数目的碳原子组成的具有封闭的球型笼状结构,含有大量的共轭双键和最低空分子轨道(lumo),表现出独特的电子特性,与良好的生物安全性,被誉为“自由基海绵”,因此常被应用于纳米医药领域。
3.结肠癌已成为全球发病率与死亡率排名第三的癌症,结肠部位免疫细胞的大量聚集,导致免疫系统紊乱,大大增强其致癌率,最终造成肿瘤的发生与发展,其中最具有代表性的就是结直肠癌(crc)。
4.目前较为常见的治疗crc的方法主要集中在手术治疗与药物治疗上。其中药物治疗包括以下几种:
①
非甾体抗炎药治疗;
②
抗生素治疗;
③
pd-l1或ctla-4等免疫检查点疗法;
④
针对炎症因子的细胞因子拮抗剂治疗,如il-6的抑制剂等。这些药物均可在一定程度上减轻肿瘤的发展。但是传统的手术方法会造成组织损伤进而引发炎症,进一步刺激crc的发生与发展。非甾体抗炎药物与抗炎药物的长期使用会引发机体严重的副作用,包括肝功能与肾功能障碍,诱导消化道损伤等。pd-l1或ctla-4等免疫检查点疗法治愈率低,且伴随着过敏,肝肺功能障碍等副作用。因此开发一种具有显著治疗效果且长期服用对机体无明显毒副作用的药物应用于crc的药物迫在眉睫。
技术实现要素:
5.本发明的目的在于提供一种用于治疗肠道癌症的富勒烯制剂,其对肠道癌症有较为明显的抑制效果。
6.本发明的一方面,提供一种富勒烯制剂在制备治疗肠道癌症的药物中的应用,所述富勒烯制剂包括富勒烯或富勒烯衍生物和药用辅料,所述药用辅料包括微晶纤维素。
7.在一些具体实施方式中,所述富勒烯制剂由下述重量百分比的富勒烯或富勒烯衍生物及药用辅料制备而成:富勒烯或富勒烯衍生物10-20%、药用辅料80-90%。
8.在一些具体实施方式中,所述药用辅料还包括选自选自二氧化硅、共聚维酮、羧甲基纤维素、羟丙基纤维素、硬脂富马酸钠、没食子酸丙酯、丁羟茴醚或枸橼酸中的一种或多种。
9.在一些具体实施方式中,所述富勒烯制剂由下述重量百分比的富勒烯或富勒烯衍生物及辅料制备而成:富勒烯或富勒烯衍生物占比10-20%、微晶纤维素占比60-85%以及选自硬脂富马酸钠、没食子酸丙酯、丁羟茴醚和枸橼酸的辅料总占比0.1-25%。
10.在一些体实施方式中,所述富勒烯制剂中,富勒烯或富勒烯衍生物占比为10-20%,例如可以为10-15%、15%-20%、10%、12%、13%、16%、18%。
11.在一些体实施方式中,所述富勒烯制剂中,微晶纤维素占比60-85%,例如可以为
65-80%、65-70%、60%、62%、64%、66%、70%、75%、76%、78%、80%。
12.在一些体实施方式中,所述富勒烯制剂中,选自硬脂富马酸钠、没食子酸丙酯、丁羟茴醚和枸橼酸的辅料总占比0.1-25%,例如可以为0.1-5%、0.1-10%、0.1-15%、0.1-20%、5-10%、5-15%、5-20%。
13.其中,硬脂富马酸钠、没食子酸丙酯、丁羟茴醚和枸橼酸的质量比可以为1∶(1-5)∶(1-10),例如可以为1∶2∶3、1∶1∶2、1∶1∶2、1∶3∶5、1∶5∶10。
14.在一些具体实施方式中,所述制剂为混悬剂、片剂、溶液剂、丸剂、散剂或胶囊剂。
15.在一些具体实施方式中,所述富勒烯或富勒烯衍生物选自c
2n
、m@c
2n
、m2@c
2n
、ma@c
2n
、m3n@c
2n
、m2c2@c
2n
、m2s@c
2n
、m2o@c
2n
和m
xa3-x
n@c
2n
中的任一种或其混合物,其中,m和a均为金属元素,所述m和a均选自sc、y和镧系金属元素中的任意一种。
16.优选地,所述富勒烯选自含c
2n
的一种或多种富勒烯分子,其中2n为碳原子数,30≤n≤60。
17.优选地,所述富勒烯选自c
60
、c
70
、c
76
、c
78
、c
ε0
、c
82
、c
84
的一种或多种;优选的,所述富勒烯为c
60
、c
70
或c
82
。
18.在一些具体实施方式中,所述富勒烯制剂为片剂或混悬剂。
19.优选地,所述片剂通过将富勒烯或富勒烯衍生物与药用辅料混匀压片制备得到。
20.在一些具体实施方式中,所述混悬剂通过将所述片剂溶于水制备得到。
21.在一些具体实施方式中,所述肠道癌症为结直肠癌。
22.在一些具体实施方式中,所述结直肠癌为原发性结肠癌。
23.本发明的有益效果:
24.①
本发明提供的富勒烯制剂便于制备,且给药方式便捷;
25.②
具有优异的生物安全性,长期服用,对身体无明显毒副作用;
26.③
具有优异的治疗效果,可以显著抑制crc的发生与发展。
27.④
促进肠道部位p53基因的表达。
28.综上所述,本发明富勒烯混悬剂为crc的治疗提供了一种安全便捷有效的治疗药物。
29.显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
附图说明
30.图1示出了实施例1中富勒烯混悬剂ofts的ms谱图;
31.图2示出了实施例1中富勒烯混悬剂ofts的hplc谱图;
32.图3示出了实施例2中lps可以显著促进ct26细胞的生长(*p《0.05);
33.图4示出了实施例2中ofts可以显著抑制肿瘤细胞的增殖(*p《0.05,**p《0.01);
34.图5示出了实施例3中小鼠肠道照片;
35.图6示出了实施例3中小鼠结肠长度统计结果(**p《0.01),***p《0.001;
36.图7示出了实施例3中小鼠肠道纵向剖开照片;
37.图8示出了实施例3中小鼠肿瘤评分结果(*p《0.05);
38.图9示出了实施例4ofts可以显著增加抑癌基因p53表达。
39.图10示出了实施例5ofts长期服用对小鼠主要脏器的安全性评估结果。
具体实施方式
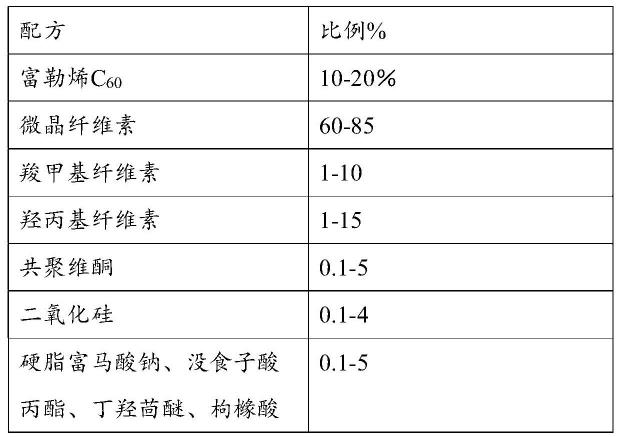
40.实施例1:制备富勒烯混悬剂ofts
[0041][0042]
合成方法:按上述配方混合富勒烯及辅料,高速搅拌均匀,随后用压片机将其压成片状,制成易于口服的富勒烯片剂。在小鼠身上验证其抑瘤原发性结肠癌效果时,将富勒烯片剂溶于水中,制备成粒径为2.5μm左右的富勒烯混悬剂ofts,用于小鼠灌胃给药。
[0043]
结构表征:使用基质辅助激光解析电离飞行时间质谱(maldi-tof-ms)。
[0044]
高效液相色谱(hplc,lc-2030,岛津):c18色谱柱(4.6*250mm,安捷伦),水-甲苯作为流动相,紫外检测器(检测波长:310nm),流量为1ml/min,对ofts的纯度进行检测。
[0045]
结论:maldi-tof-ms(图1)和hplc(图2)检测结果显示ofts中c
60
纯度较高;
[0046]
实施例2:ofts对结肠癌细胞生长的抑制作用
[0047]
细胞:ct26结肠癌细胞;
[0048]
分组:ct26细胞加正常培养基,对照组为脂多糖(lps)刺激后的ct26细胞加正常培养基,实验组是lps刺激后的ct26细胞加不同浓度ofts的培养基;
[0049]
wst-8检测肿瘤细胞的增殖情况:ct26细胞使用含10%胎牛血清的1640培养基培养。将ct26细胞以5
×
104的密度种于96孔板中,在37℃培养箱中孵育24小时细胞贴壁后,分别用不同浓度lps刺激ct26细胞24小时之后,加入wst-8试剂与细胞在37℃培养箱孵育1小时后,用酶标仪检测细胞在450nm处的吸光度,通过吸光度值来反映细胞的增殖情况。
[0050]
确定lps刺激ct26细胞的最适浓度后,重新将ct26细胞以5
×
104/孔的密度种于96孔板中,在37℃培养箱中孵育24小时,待细胞贴壁后,用4μg/ml lps刺激ct26细胞24小时,换掉培养基,使用不同剂量的待测样品处理细胞4小时。然后加入wst-8试剂与细胞在37℃培养箱孵育1小时后,用酶标仪检测细胞在450nm处的吸光度,通过吸光度值来反映细胞的增殖情况。
[0051]
结论:相比于ct26细胞,加入4μg/ml与10μg/ml lps处理的ct26细胞吸光度显著增加,表明lps可以显著促进ct26细胞的生长(图3)。50μg/ml和100μg/ml的ofts与lps处理过的ct26共孵育后,吸光度相对于lps处理的ct26细胞显著降低,表明ofts可以显著抑制肿瘤
细胞的增殖(图4)。
[0052]
实施例3:ofts对原发性结肠癌的抑制作用
[0053]
1、动物模型与分组
[0054]
小鼠:c57bl/6j小鼠;
[0055]
分组:正常组小鼠,对照组小鼠,治疗组小鼠;
[0056]
造模方法:c57bl/6j小鼠购买自华阜康公司,适应1周后,对照组和实验组小鼠均腹腔注射致突变性剂氧化偶氮甲烷(aom,10mg/kg),用无菌水喂养7天。对照组第8-13天开始喂养炎症剂葡聚糖硫酸钠(dss)水(1.8%,w/v),第14-28天饲喂无菌水,这是一个dss循环。此模型需经过3次dss循环。三次dss循环后开始有肿瘤生成,然后开始喂养无菌水直至第80天。治疗组从第7天开始灌胃ofts,每天1次(50mg/kg)。在第80天时对小鼠进行取材。空白组为不做任何处理的健康小鼠。
[0057]
2、抑瘤效果
[0058]
在第80天时,将小鼠处死,取出小鼠的结肠进行拍照,并测量结肠长度。之后用生理盐水将结肠内粪便冲洗干净,纵向剖开拍照,并进行肿瘤大小与个数的测量。
[0059]
结论:对照组小鼠相较于正常组小鼠在第80天取材时,结肠长度明显短于正常小鼠,且结肠部位肿瘤生长较为明显,说明原发性结肠癌模型造模成功(图5-图6)。经ofts治疗的小鼠,结肠长度相较于对照组小鼠有了显著性增长,并且肿瘤的评分也显著性降低,说明ofts对于原发性结肠癌有较为明显的抑制效果(图7-图8)。
[0060]
实施例4:ofts促进肠道部位p53基因的表达
[0061]
蛋白免疫印迹检测肠道组织p53的表达:在第80天时,将对照组与ofts组小鼠的结直肠取出,清除干净内容物后,取适量组织,在液氮中研磨碾碎后,用含有蛋白酶磷酸酶抑制剂混合物的裂解缓冲液裂解。随后,将裂解液在5x上样缓冲液中煮沸5分钟,然后用sds-聚丙烯酰胺凝胶溶解,转移至pvdf膜上。分别用抗p53和抗gapdh的抗体进行孵育,然后将膜与结合的二抗一起孵育,所有抗体均已在封闭缓冲液中稀释,并通过增强的化学发光试剂盒可视化抗原-抗体反应。
[0062]
结论:相比于对照组对照组,ofts可以显著增加小鼠肠道处p53的表达(图9)。
[0063]
实施例5:ofts长期服用对小鼠主要脏器的安全性评估
[0064]
在第80天时,将小鼠处死,取出治疗组小鼠的主要脏器进行he染色,评估长期服用ofts的安全性。
[0065]
结论:ofts组小鼠主要脏器染色无明显变化,说明长期服用ofts对机体无明显毒副作用(图10)。
[0066]
本技术针对活性成分富勒烯制备了本文所述的富勒烯制剂,对辅料与活性成分的相容性进行了研究,考察了不同组成富勒烯制剂的药效以及不同辅料对富勒烯产品性能(例如稳定性、生物利用度等)的影响。同时,令人惊讶地发现,实施例1的富勒烯混悬液具有最佳的药效和产品稳定性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1