AT56联合索拉非尼在外周T细胞淋巴瘤中的应用
at56联合索拉非尼在外周t细胞淋巴瘤中的应用
技术领域
1.本发明属于医药技术领域,具体涉及at56联合索拉非尼在外周t细胞淋巴瘤中的应用。
背景技术:
2.公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.外周t细胞淋巴瘤(peripheralt-celllymphoma,ptcl)是来源于胸腺后不同阶段的t细胞异常增生形成的恶性肿瘤,属于非霍奇金淋巴瘤中的一种特殊亚型。ptcl的发病率低且具有地域差异。该病具有高度的侵袭性,且在生物学行为、临床表现、预后及转归等方面存在高度异质性,疾病进展迅速,诊断时多为晚期。目前ptcl的治疗主要以放化疗为主,临床上一线治疗进展长期停滞,缺乏特异高效的靶向治疗手段,患者的5年生存率不足30%,临床上亟待发现新型药物和联合用药方案以改善ptcl患者的临床获益。
4.索拉非尼(sorafenib),是一种多靶点激酶抑制剂,2005年获fda批准上市,用于治疗无法手术或远处转移的肝细胞癌、晚期肾癌及局部复发或转移的进展性的难治性分化型甲状腺癌。此外,索拉非尼可通过抑制胱氨酸/谷氨酸反向转运蛋白xct诱发肿瘤细胞内的铁死亡,从而参与肿瘤的发生发展。铁死亡是一种新型的依赖于细胞内铁累积及毒性脂质过氧化物ros的细胞程序性死亡方式。越来越多的临床前研究表明,诱导铁死亡是一种有效的肿瘤治疗及抵抗耐药的治疗策略。目前的研究发现索拉非尼在多种非霍奇金淋巴瘤中发挥显著的抗肿瘤作用,一项ii期临床试验结果表明索拉非尼在复发难治淋巴瘤中具有一定的治疗效果且耐受性好,但是单药治疗的抗肿瘤活性较低。因此,需要深入探索基于索拉非尼的新型联合用药方案以提高淋巴瘤患者的临床疗效。
5.ptgds是一种具有催化前列腺素代谢和脂质转运双重功能的蛋白,at56是高度特异性靶向ptgds蛋白的小分子抑制剂。目前,关于ptgds及at56的研究主要聚焦于神经系统疾病、炎症、免疫失调、寄生虫感染等。最近的研究发现ptgds可通过调节细胞增殖、细胞周期、远处转移和干细胞特性等生物学功能,在多种肿瘤的发生发展中扮演重要角色。然而,目前关于ptgds和at56在ptcl中的研究国内外尚未见报道。
技术实现要素:
6.针对现有技术存在的不足,本发明提供at56联合索拉非尼在外周t细胞淋巴瘤中的应用。本发明首次发现ptgds特异性抑制剂at56可显著抑制ptcl的生长,at56联合索拉非尼在ptcl细胞及小鼠模型中均展示出较好的抗肿瘤效果。本发明阐明ptgds特异性抑制剂at56和索拉非尼的联合抗肿瘤效果,探讨at56对ptcl中铁死亡进程的调节作用及分子机制,为深入探索ptcl新型药物及联合用药方案奠定坚实的理论基础。基于上述研究成果,从而完成本发明。
7.具体的,本发明涉及以下技术方案:
8.本发明的第一个方面,提供at56联合索拉非尼在制备外周t细胞淋巴瘤治疗药物中的应用。
9.根据本发明,“治疗”的概念表示任一适用于治疗肿瘤及相关疾病的措施,或者对于这种表现的疾病或所表现出来的症状进行预防性治疗,或者避免这种疾病的复发,例如在结束了治疗时间段之后的复发或对已经发作的疾病的症状进行治疗,或预先介入性的防止或抑制或减少该类疾病或症状的发生。
10.如上所述,本发明通过研究发现,at56可增强索拉非尼对ptcl细胞的增殖抑制能力,并增强其对脂质过氧化的促进作用,表明其对ptcl中铁死亡过程具有促进作用。进一步动物学实验结果表明,at56联合索拉非尼在小鼠模型中展示出良好的抗肿瘤效果,显著优于单独用药。
11.因此,本发明的第二个方面,提供上述at56联合索拉非尼在如下任意一种或多种中的应用:
12.a)抑制外周t细胞淋巴瘤细胞增殖或制备抑制外周t细胞淋巴瘤细胞增殖的产品;
13.b)促进外周t细胞淋巴瘤细胞铁死亡或制备促进外周t细胞淋巴瘤细胞铁死亡的产品;
14.c)抑制外周t细胞淋巴瘤生长或制备抑制外周t细胞淋巴瘤生长的产品。
15.其中,所述b)中,促进外周t细胞淋巴瘤细胞铁死亡至少表现为促进肿瘤组织(细胞)中的铁离子聚集和/或促进肿瘤组织(细胞)脂质过氧化。
16.本发明的第三个方面,提供一种药物组合物,其活性成分包含at56和索拉非尼。
17.所述药物组合物具有治疗外周t细胞淋巴瘤的作用,具体表现为:
18.a)抑制外周t细胞淋巴瘤细胞增殖;
19.b)促进外周t细胞淋巴瘤细胞铁死亡;
20.c)抑制外周t细胞淋巴瘤生长。
21.本发明的第四个方面,提供一种治疗外周t细胞淋巴瘤的方法,所述方法包括:向受试者施用上述药物组合物。
22.以上一个或多个技术方案的有益技术效果:
23.上述技术方案首次报道了ptgds特异性抑制剂at56可显著抑制ptcl的生长,且具有时间依赖性和浓度依赖性。体内和体外实验结果证实at56通过诱导ptcl细胞中的铁离子聚集促进铁死亡过程。而且,at56联合索拉非尼在ptcl细胞及小鼠模型中均展示出较好的抗肿瘤效果。本发明可推动at56和索拉非尼联合用药方案的深入研究及临床应用,为构建新型高效的联合用药策略、优化ptcl临床诊疗方案提供坚实的理论依据和实验基础,具有良好的实际推广应用之价值。
附图说明
24.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
25.图1为at56与索拉非尼的分子结构及分子式示意图;其中,a为at56,b为索拉非尼。
26.图2为本发明实施例中at56可显著抑制ptcl细胞的增殖水平,且抑制作用呈浓度
依赖性和时间依赖性。
27.图3为本发明实施例中tmt蛋白定量检测中,at56处理及对照处理的ptcl细胞中铁死亡相关的差异基因表达热图。
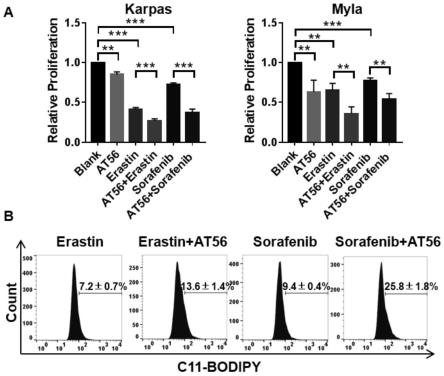
28.图4为本发明实施例中at56(100μm)增强铁死亡激动剂(5μm索拉非尼和5μm erastin)的抗淋巴瘤效果;其中,a为不同处理方式对ptcl的增殖抑制结果图;b为不同处理方式对ptcl的脂质过氧化促进结果图。
29.图5为本发明实施例中ptcl小鼠异种移植模型中,at56和索拉非尼的联合抗淋巴瘤作用;其中,a为不同处理组小鼠的肿瘤生长曲线;b为不同处理组小鼠中解剖分离后的肿瘤图片。
30.图6为本发明实施例中铁死亡抑制剂ferrostatin-1可部分回复at56的抗淋巴瘤作用;其中,a为加入ferrostatin-1后可部分回复at56的增殖抑制作用;b为加入ferrostatin-1可部分回复at56对脂质过氧化的促进作用。
31.图7为本发明实施例中at56处理后ptcl细胞中铁死亡相关蛋白的表达水平。
32.图8为本发明实施例中铁离子螯合剂dfo可部分回复at56的抗淋巴瘤作用;其中,a为加入dfo后可部分回复at56的增殖抑制作用;b为加入dfo可部分回复at56对脂质过氧化的促进作用。
33.图9为本发明实施例中不同处理组小鼠的肿瘤组织中铁离子浓度水平图。
具体实施方式
34.应该指出,以下详细说明都是例示性的,旨在对本技术提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本技术所属技术领域的普通技术人员通常理解的相同含义。
35.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本技术的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
36.本发明的一个典型具体实施方式中,提供at56联合索拉非尼在制备外周t细胞淋巴瘤治疗药物中的应用。
37.根据本发明,“治疗”的概念表示任一适用于治疗肿瘤及相关疾病的措施,或者对于这种表现的疾病或所表现出来的症状进行预防性治疗,或者避免这种疾病的复发,例如在结束了治疗时间段之后的复发或对已经发作的疾病的症状进行治疗,或预先介入性的防止或抑制或减少该类疾病或症状的发生。
38.其中,所述at56(c
25h27
n5)是一种有效、选择性和具有口服活性的脂钙蛋白型前列腺素d合酶的抑制剂,其cas号为162640-98-4,其结构式如图1的a中所示。
39.所述索拉非尼(c
21h16
clf3n4o3)是一种多靶点激酶抑制剂,其cas号为284461-73-0,其结构式如图1的b中所示。
40.如上所述,本发明通过研究发现,at56可增强索拉非尼对ptcl细胞的增殖抑制能力,并增强其对脂质过氧化的促进作用,表明其对ptcl中铁死亡过程具有促进作用。进一步动物学实验结果表明,at56联合索拉非尼在小鼠模型中展示出良好的抗肿瘤效果,显著优
于单独用药。
41.所述at56与索拉非尼的摩尔比为1-20:1。
42.因此,本发明的又一具体实施方式中,提供上述at56联合索拉非尼在如下任意一种或多种中的应用:
43.a)抑制外周t细胞淋巴瘤细胞增殖或制备抑制外周t细胞淋巴瘤细胞增殖的产品;
44.b)促进外周t细胞淋巴瘤细胞铁死亡或制备促进外周t细胞淋巴瘤细胞铁死亡的产品;
45.c)抑制外周t细胞淋巴瘤生长或制备抑制外周t细胞淋巴瘤生长的产品。
46.所述at56与索拉非尼的摩尔比为1-20:1。
47.其中,所述b)中,促进外周t细胞淋巴瘤细胞铁死亡至少表现为促进肿瘤组织(细胞)中的铁离子聚集和/或促进肿瘤组织(细胞)脂质过氧化。
48.a)-c)中,所述产品可以为药物或者试验用品,所述试验用品具体可以为试验试剂,从而供基础研究使用,用于构建相关肿瘤细胞或动物模型,进而研究诸如肿瘤细胞中的铁死亡相关机制问题。
49.当所述产品为药物时,所述药物至少还包括一种非药物活性成分。所述非药物活性成分包括药学上可接受的载体、赋形剂和/或稀释剂。
50.本发明的又一具体实施方式中,提供一种药物组合物,其活性成分包含at56和索拉非尼。
51.所述at56与索拉非尼的摩尔比为1-20:1。
52.所述药物组合物具有治疗外周t细胞淋巴瘤的作用,具体表现为:
53.a)抑制外周t细胞淋巴瘤细胞增殖;
54.b)促进外周t细胞淋巴瘤细胞铁死亡;
55.c)抑制外周t细胞淋巴瘤生长。
56.本发明的又一具体实施方式中,所述药物组合物至少还包括一种非药物活性成分。所述非药物活性成分包括药学上可接受的载体、赋形剂和/或稀释剂。
57.本发明的又一具体实施方式中,所述非药物活性成分包括:
58.药学上相容的无机或有机酸或碱、聚合物、共聚物、嵌段共聚物、单糖、多糖、离子和非离子型表面活性剂或脂质;药理上无害的盐(优选氯化钠)、调味剂、维生素(优选维生素a或维生素e、生育酚或维生素原)、抗氧化剂(优选抗坏血酸),以及稳定剂和/或防腐剂。
59.所述药物制剂的给药剂型包括:液体剂型、固体剂型、外用制剂和喷剂;
60.本发明又一具体实施方式中,包括以下剂型:真溶液类、胶体类、微粒剂型、乳剂剂型、混旋剂型、片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、栓剂、冻干粉针剂、包合物、填埋剂、贴剂、擦剂。
61.本发明的又一具体实施方式中,提供一种治疗外周t细胞淋巴瘤的方法,所述方法包括:向受试者施用上述药物组合物。
62.所述受试者是指已经是治疗、观察或实验的对象的动物,优选指哺乳动物,最优选指人。
63.以下通过实施例对本发明做进一步解释说明,但不构成对本发明的限制。应理解这些实施例仅用于说明本发明而不用于限制本发明的范围。
64.实施例
65.实验方法
66.1.细胞培养
67.本研究使用的人源ptcl细胞株karpas-299、myla3676细胞购买于atcc,使用含10%胎牛血清的imdm完全培养基、在含有5%co2的37℃细胞培养箱中培养,每2-3天更换培养基并传代,取生长状态较好的细胞进行后续实验。
68.2.cell counting kit-8(cck-8)检测ptcl细胞的增殖水平
69.使用dmso溶解at56、索拉非尼、erastin、ferrostatin-1(fer-1)、deferoxamine(dfo)粉末,分别配制浓度为125mm、50mm、10mm、10mm、500mm的母液。收集处于对数生长期且状态良好的ptcl细胞,离心后去除上清,用imdm完全培养基重悬细胞并在显微镜下计数,按照每孔104个细胞/90μl将ptcl细胞接种于96孔细胞培养板上,根据浓度换算公式加入10μl不同浓度的药物,设置空白孔和三个重复孔,轻轻摇晃混匀,将96孔板置于含有5%co2的37℃细胞培养箱中继续培养;48-72小时后每孔加入10μlcck8试剂,注意不要产生气泡,37℃避光孵育1-4小时后,使用酶标仪检测450nm处各孔的吸光度值(od值),根据检测结果绘制ptcl细胞的生长曲线。
70.3.tmt(tandem mass tag)定量蛋白检测及生物信息学分析
71.收集处于对数生长期且状态良好的ptcl细胞,按照每孔3
×
105个细胞/2ml将ptcl细胞接种于6孔细胞培养板上,根据浓度换算公式,加入终浓度为100μm的at56,设置空白对照孔和三个重复孔。将6孔板置于含有5%co2的37℃细胞培养箱中继续培养,48小时后收集细胞。蛋白提取、定量、酶切、同位素标记、肽段富集及质谱检测由北京诺禾致源科技公司完成。根据tmt检测结果进行生物学信息分析,按照p《0.05、fc(fold change)》1筛选at56加药组与对照组之间的铁死亡相关的差异表达蛋白并绘制热图。
72.4.c11-bodipy法检测ptcl细胞中的脂质过氧化
73.使用imdm完全培养基重悬生长状态良好的ptcl细胞,在6孔板中接种3
×
105个/2ml的细胞,加入指定浓度的药物,轻轻摇晃后将6孔板置于37℃含5%co2培养箱中,孵育48小时后收集细胞。使用无血清imdm培养基稀释c11-bodipy探针至终浓度为2.5μm,加入ptcl细胞中后轻轻吹打混匀重悬细胞,置于37℃含5%co2培养箱中避光孵育30分钟,每隔5分钟轻轻颠倒混匀,使细胞与探针充分接触。探针装载完成后使用无血清imdm培养基洗涤细胞,重复3次,以去除未进入细胞内的c11-bodipy探针。使用预冷的pbs重悬细胞,400目滤网过滤细胞悬液后,将细胞转移至标记好的流式管中,上机检测阳性细胞比例。
74.5.构建ptcl异种移植小鼠模型
75.本研究使用的3-4周龄scid beige雌性小鼠购买于北京维通利华实验动物公司,饲养中使用无菌饮用水、饲料及垫料,保持无菌、恒温(25℃)和恒湿(70%)的饲养环境。动物研究过程中严格遵循arrie准则及山东省立医院动物保护和研究使用伦理委员会的原则。将实验小鼠按照简单随机法分为4个小组,对照组、at56组、索拉非尼组、at56联合索拉非尼组,每组6只小鼠。收集处于对数生长期且状态良好的ptcl细胞,调整细胞密度为1
×
108个/ml,加入等体积的matrigel基质胶并混合均匀,取200μl混合液接种至小鼠的右下肢外侧皮下,肉眼可见形成卵圆形皮丘,继续于无菌环境中进行饲养。待瘤体高于皮肤表面后,开始给予药物处理,索拉非尼(80mg/kg)采用腹腔注射给药,通过灌胃实现at56(80mg/
kg)给药。每日用游标卡尺测量瘤体大小并记录,a=肿瘤长径,b=肿瘤短径,肿瘤体积(v)=(a
×
b2)
×
0.5,绘制肿瘤生长曲线。15天后脱颈处死小鼠,解剖分离完整的皮下肿瘤,拍照保存。收集小鼠组织后,分别置于4%多聚甲醛及-80℃超低温冰箱保存,以备后续实验使用。
76.6.蛋白提取和蛋白质免疫印迹分析(western blotting)
77.收集处理后的ptcl细胞,使用预冷的pbs重悬并洗涤细胞,重复3遍,离心去除上清,根据细胞团块大小加入适量(40-150μl)的蛋白裂解液(ripa:pmsf:磷酸酶抑制剂体积比为100:1:1),涡旋振荡混匀,冰上孵育30分钟,置于4℃离心机12000rpm离心30分钟后,吸取含有蛋白的上清,使用bca法检测蛋白浓度后,将上清与loading buffer按照体积3:1的比例混匀,100℃金属浴10min,使蛋白发生变性,置于-80℃冰箱保存备用。根据目的蛋白的分子量大小,配制7.5-12%的电泳凝胶,置于电泳槽中并加入适量的电泳缓冲液,在各个加样孔中依次加入40μg蛋白或4μl蛋白marker,200v恒压电泳,根据蛋白marker及溴酚蓝的位置确定电泳时间。提前剪好与凝胶大小相对应的pvdf膜,置于甲醇中浸泡1-2分钟。将切割好的凝胶、pvdf膜及转印滤纸浸入转膜缓冲液中,自下而上分别放置:转印滤纸-pvdf膜-凝胶-转印滤纸,小心赶出气泡后放入半干转印槽中,10v恒压条件下转膜30分钟。将pvdf膜置于用tbst配制的10%脱脂牛奶中,室温封闭1-2小时。后将pvdf膜置于用一抗稀释液配制的适当浓度的一抗溶液中,置于摇床上4℃孵育过夜。tbst清洗pvdf膜3遍后,置于10%脱脂牛奶配制的二抗溶液中,室温孵育1小时,再次清洗pvdf膜,滴加提前配制的显影液(a液:b液=1:1)后,使用amersham imager 600凝胶成像仪器进行成像,使用image j软件分析条带灰度值,评估目的分子的表达水平。
78.7.比色法检测小鼠组织中的铁离子水平
79.铁离子检测试剂盒购买于abcam公司(货号:ab83366)。收集新鲜的小鼠肿瘤组织,使用预冷的pbs洗涤3遍,擦干后置于精密电子天平称量组织重量。根据组织重量加入100-200μl缓冲液,超声震荡破碎组织(5分钟),4℃离心机16000g离心10分钟,收集上清后置于冰上保存。按照试剂盒说明书,在96孔板中加入100μl标准品/组织上清液,37℃恒温敷箱中平衡30分钟,加入100μl铁离子探针,轻轻震荡混合均匀,继续置于37℃恒温敷箱中避光孵育60分钟。使用酶标仪检测593nm处各孔的吸光度值(od值),根据吸光度值绘制铁离子浓度标准曲线,计算小鼠肿瘤组织中铁离子浓度水平。
80.实验结果:
81.1.图1显示了at56和索拉非尼的分子结构示意图及分子式。
82.2.图2显示了at56可显著抑制ptcl细胞的增殖水平,且抑制作用呈浓度依赖性和时间依赖性。结果表明了at56的体外抗淋巴瘤作用。
83.3.图3显示了tmt蛋白定量检测中,at56处理及对照处理的ptcl细胞中铁死亡相关的差异基因表达热图。结果表明了at56对ptcl细胞中铁死亡相关基因表达水平的调节作用。
84.4.图4显示了at56可增强铁死亡激动剂(索拉非尼和erastin)的抗淋巴瘤效果。图4a中,at56(100μm)、索拉非尼(5μm)和erastin(5μm)单药均可抑制ptcl细胞的增殖水平,加入at56(100μm)后可增强索拉非尼(5μm)和erastin(5μm)的增殖抑制能力。图4b中,加入at56(100μm)可增强索拉非尼(5μm)和erastin(5μm)对脂质过氧化的促进作用。结果表明了
at56对ptcl中铁死亡过程的促进作用。
85.5.图5显示了在ptcl小鼠异种移植模型中,at56和索拉非尼的联合抗淋巴瘤作用。图5a展示了不同组小鼠的肿瘤生长曲线,at56和索拉非尼单药均可抑制淋巴瘤的生长,加入at56可增强索拉非尼的体内抗肿瘤作用。图5b展示了不同组小鼠中解剖分离后的肿瘤图片,联合用药组的肿瘤大小及体积明显小于对照组及单药治疗组。结果表明了at56和索拉非尼的体内联合抗肿瘤作用。
86.6.图6显示了铁死亡抑制剂ferrostatin-1可部分回复at56的抗淋巴瘤作用。图6a中,at56抑制ptcl细胞的增殖,加入ferrostatin-1后可部分回复at56的增殖抑制作用。图6b中,加入ferrostatin-1可部分回复at56对脂质过氧化的促进作用。结果表明了at56在ptcl中抗肿瘤作用对铁死亡的依赖性。
87.7.图7显示了at56处理后ptcl细胞中铁死亡相关蛋白的表达水平。随着at56浓度的升高,铁死亡相关转录因子nrf2的表达水平下降,nrf2的负调控因子keap1的表达水平显著升高,表明了ptcl细胞中铁死亡过程的激活。铁死亡过程主要是由铁离子聚集及脂质过氧化驱动的,我们通过开展实验进一步探究接受at56处理的ptcl细胞中铁死亡的驱动因素。western blotting结果表明,接受at56处理的ptcl细胞中,ncoa4、fth和ftl表达水平显著升高,表明ptcl细胞中存在铁离子的异常聚集。但是,脂质代谢关键酶acsl4表达水平下降,氧化调节分子xct和gpx4表达水平升高,表明ptcl细胞内出现脂质代谢及过氧化的代偿性抑制。结果表明了at56对铁死亡及铁离子聚集的潜在调节作用。
88.8.图8显示了铁离子螯合剂dfo可部分回复at56的抗淋巴瘤作用。图8a中,at56抑制ptcl细胞的增殖能力,加入dfo后可部分回复at56的增殖抑制作用。图8b中,加入dfo可部分回复at56对脂质过氧化的促进作用。结果表明了at56的铁死亡诱导作用对铁离子聚集的依赖性。
89.9.图9显示了不同组小鼠的肿瘤组织中铁离子浓度水平,at56单药组小鼠的肿瘤组织中的铁离子水平高于空白对照组,at56和索拉非尼联合用药可显著促进肿瘤组织中的铁离子聚集。
90.综上,上述研究首次发现ptgds特异性抑制剂at56可显著抑制ptcl的生长,且具有时间依赖性和浓度依赖性。体内和体外实验结果证实at56通过诱导ptcl细胞中的铁离子聚集促进铁死亡过程。而且,at56联合索拉非尼在ptcl细胞及小鼠模型中均展示出较好的抗肿瘤效果。
91.本发明可推动at56和索拉非尼联合用药方案的深入研究及临床应用,为构建新型高效的联合用药策略、优化ptcl临床诊疗方案提供坚实的理论依据和实验基础。
92.最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1