Wee1激酶抑制剂在治疗癌症疾病中的应用的制作方法
本发明属于药物化学领域,涉及癌症治疗领域,具体涉及wee1激酶抑制剂在治疗具有h3k27m突变癌症疾病上的应用。
背景技术:
1、真核细胞的生长和分裂过程称之为细胞周期。细胞通过细胞周期从新生细胞逐渐成长并分裂为两个细胞来进行繁殖。细胞周期大致包括g1、s、g2和m几个周期:g1期也称为生长期,这个阶段的特点是细胞代谢活跃,大量合成细胞生长所需的蛋白质、糖类、脂类和rna等使细胞从一个新分裂的年轻细胞迅速成长到成熟细胞。也有一些细胞完成g1期后不再进行细胞周期的循环停留在这一阶段称之为g0期;s期的主要特点是dna合成复制,细胞染色体由二倍体转变为四倍体,之后细胞进入g2期。这个阶段的特点是一方面细胞继续生长,另外对合成的dna进行检查修复为细胞进入有丝分裂做好准备。细胞周期的最后一个阶段为m期,在这个阶段细胞通过有丝分裂由一个母细胞分裂为两个相同的子细胞,完成细胞繁殖。细胞周期的整个过程中存在多个细胞周期检验点(cell cycle checkpoint),这包括g1/s或g1检查点和g2/m或g2检查点。它们的主要功能之一是检查确保细胞周期过程中遗传信息(dna)复制的准确性及是否使细胞向前进入细胞周期的下一个阶段。
2、每个细胞周期检验点都是由多个因子组成的系统通过复杂的机制工作的。比如,g2-m检验点使用复杂的过程检查dna损伤。这个细胞周期检验点中的一个重要激酶为cdk1,其和cyclin-b1组成复合体(nurse,p.,1990,nature 344,503-508)。cdk1的活化及失活对细胞从g2期进入有丝分裂(m)及随后有丝分裂的完成起着至关重要的作用。cdk1的活性控制是通过多重机制来调节的,包括与周期蛋白a(cyclin-a)或细胞周期蛋白b(cyclin-b)的结合以及磷酸化和去磷酸化。wee1激酶磷酸化cdk1并抑制其活性,从而延迟细胞进入有丝分裂。
3、wee1是个酪氨酸激酶,通过磷酸化cdk1上的酪氨酸15(y15)从而抑制cdk1的活性(mcgowan,c.h.,等人,1993,the embo journal 12,75-85;parker,l.l.,等人,1992,science 257,1955-1957)。因此,wee1是cdk1活性的关键抑制性调节酶,在g2/m期检测点起重要作用(o’connell,等人,1997,the embo journal 16,545-554)。wee1的丧失或失活会导致细胞过早进入有丝分裂,引起有丝分裂的失败和细胞死亡(stumpff,j.,等人,2004,curr biol 14,2143-2148)。一些肿瘤细胞的g1/s期细胞周期检验点有功能缺陷或丧失,严重依赖g2/m期检测点来保障细胞生长、分裂的进行(sancar,a.,等人,2004,annual reviewof biochemistry 73,39-85)。在癌细胞中,g1/s检查点的功能常常由于p53突变等原因而丧失。当dna损伤发生时,这些细胞严重依赖g2/m检查点功能,并且对wee1功能丧失敏感。(wang,y.,等人,2004,cancer biology&therapy 3,305-313)。
4、抑制wee1的活性可以选择性促使细胞周期检查点有缺陷的癌细胞死亡,对细胞周期检查点正常的正常细胞则作用甚小。因此,wee1激酶抑制剂有可能用于癌症及其他具有细胞周期检查点缺陷疾病的靶向药物。
5、近年来,已报道和公开了多种wee1激酶抑制剂,包括wo2007126122(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2019028008、wo2019173082和wo202021032(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2015092431和wo2018162932(取代的2,3-二氢嘧啶并[4,5-d]嘧啶-4(1h)-酮类化合物),wo2019037678(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2020210377和wo2020210383(取代的杂环化合物)、wo2020210375、wo2020210380、wo2020210381(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2018133829(l,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)和wo2019085933(l,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮大环类化合物)。其中,adavosertib(azd1775)是第一个进入临床的wee1激酶抑制剂,目前处于临床ii期研究中。现处于临床阶段的wee1激酶抑制剂还有zn-c3和debio-0123,处于临床i期。还有多种wee1激酶抑制剂目正处于临床前研究阶段,如dn-1609和nuv-569等。
6、wo2018090939公开了如下式i化合物或其可药用盐或前药作为wee1激酶抑制剂。
7、
8、其中,a是n或cr15;
9、r1为氢,可被取代的c1-c8烷基,可被取代的c2-c8烯基,可被取代的c3-c8环烷基,可被取代的芳基,可被取代的杂环基或可被取代的杂芳基;
10、r2为可被取代的碳环基,可被取代的杂环基,可被取代的芳基,或可被取代的杂芳基;
11、r3-r7和r15独立为氢、卤素、可被取代的氨基、可被取代的烷氧基、可被取代的c1-c10烷基、卤烷基、烯基、炔基、羟基烷基、氨基烷基、羧基烷基、硝基、氰基、酰氨基、羟基、巯基、酰氧基、叠氮基、羧基、亚乙基二氧基,羟基酰氨基或可被取代的烷硫基。
12、wo2019011228公开了如下式ii化合物或其可药用盐或前药作为wee1激酶抑制剂。
13、
14、其中,a'是n或cr6';
15、r1'为氢,可被取代的c1-c8烷基,可被取代的c2-c8烯基,可被取代的c3-c8环烷基,可被取代的芳基,可被取代的杂环基或可被取代的杂芳基;
16、r2'为可被取代的碳环基,可被取代的杂环基,可被取代的芳基,或可被取代的杂芳基;
17、r3'-r6'独立为氢、卤素、可被取代的氨基、可被取代的烷氧基、可被取代的c1-c10烷基(如卤烷基、羟基烷基、氨基烷基和羧基烷基)、烯基、炔基、硝基、氰基、酰氨基、羟基、巯基、酰氧基、叠氮基、羧基、亚乙基二氧基、羟基酰氨基或可被取代的烷硫基。
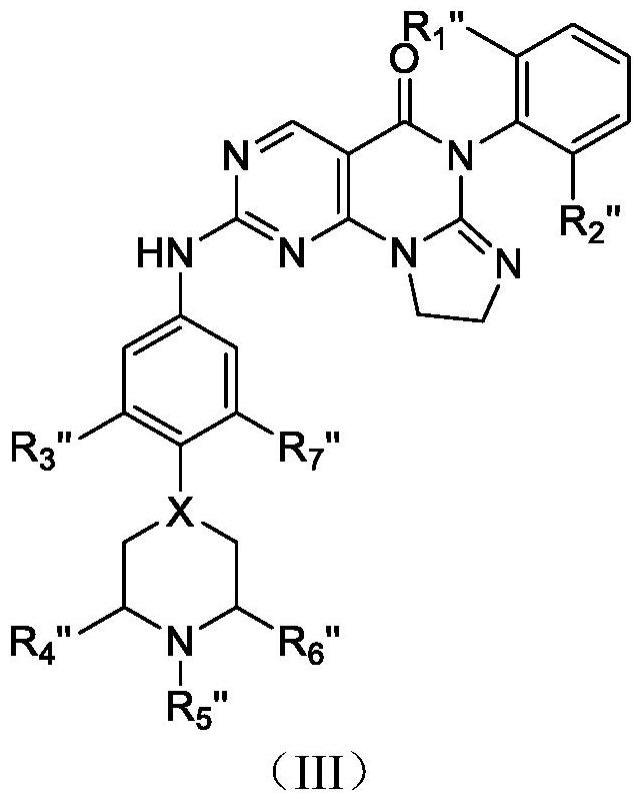
18、另外,wo2021073491公开了如下式iii化合物或其可药用盐或前药作为wee1激酶抑制剂。
19、
20、其中,r1”和r2”独立为卤素;r3”为卤素、c1-c4烷基或c1-c4烷氧基;r4”和r6”独立为h或c1-c4烷基;r5”为h或c1-c4烷基;r7”为h、卤素、c1-c4烷基或c1-c4烷氧基;x为ch或n。
21、组蛋白修饰是表观遗传信息的一种形式,与基因调控密切相关。组蛋白3(h3)27位的赖氨酸是甲基化位点,其甲基化如h3k27me2和h3k27me3可能在表观遗传机制中发挥重要作用。组蛋白h3.3蛋白由h3f3a和h3f3b基因编码。h3(h3k27m)第27位赖氨酸突变为蛋氨酸,常见于儿科胶质母细胞瘤(gbm),尤其是儿童弥漫性内生型桥脑胶质瘤(dipg)(khuong-quang da等,acta neuropathol,2012,124:439-47)。h3k27m突变改变了h3的甲基化状态,并导致表观遗传发生变化,从而全局影响基因表达(harutyunyan,a.s等,cell rep,2020,33:108390-430)。这种h3k27m突变似乎是肿瘤发生的驱动事件。h3k27m在多达30%的小儿成胶质细胞瘤患者中被发现,而在dipg中则为60%(wan,y.c.e.等,curr pharmacol rep,2018,4:292–300)。
22、弥漫性中线胶质瘤(dmg)是指发生于胼胝体、三脑室、丘脑、脑干等中线结构的高级别脑胶质瘤。该病因发病部位及浸润性生长的特点,治疗困难,预后极差。由于h3k27m的独特突变,2016年who中枢神经系统肿瘤分类中将其单独分为一个新的类型。确诊需满足肿瘤位于中枢神经系统中线部位,呈弥漫性生长以及伴有h3k27m突变,无论其组织学形态是否符合高级别特征均诊断为ⅳ级(david n louis等,acta neuropathol.2016jun;131(6):803-20)。h3k27m突变在老年胶质瘤和其他类型肿瘤极少,但在儿童中线胶质瘤中较常见。研究表明h3k27m突变与患者的预后具有显著的相关性:例如,对于8岁时诊断为野生型h3的丘脑胶质瘤患者,总生存期(os)约为11年,而对于10岁时诊断为h3k27m突变的丘脑胶质瘤患者,总生存期仅为1.8年,h3k27m突变的儿童丘脑胶质瘤5年生存率为6.3%,而野生型h3为68.8%(scott ryall等,acta neuropathol commun.2016,4:93-102)。无论是高级别(hgg)还是低级别胶质瘤(lgg),具有h3k27m突变的胶质瘤患者具有更短的生存期。
23、目前弥漫性中线胶质瘤在治疗方面主要采用以手术和辅助放化疗为主要的综合治疗,但儿童dmg患者的生存预后仍很差。对于dmg患者,尤其是具有致命性h3k27m突变的患者,迫切需要找到一种有效的治疗方式。
24、本发明发现wee1激酶抑制剂在负荷人h3k27m突变的弥漫性中线胶质瘤的小鼠模型中有很好的药效,可以观察到明显的抑制效果,为临床上h3k27m突变的弥漫性中线胶质瘤患者提供了一种潜在的治疗方式。
技术实现思路
1、本发明发现,通过抑制wee1活性可以有效地抑制具有h3k27m突变的弥漫性中线胶质瘤癌细胞的生长,这对此疾病的治疗具有重要意义。
2、本发明提供了wee1激酶抑制剂用于治疗具有h3k27m突变的癌症疾病,特别是用于治疗具有h3k27m突变的弥漫性中线胶质瘤的方法。在一个实施例中,wee1激酶抑制剂是式i化合物。在一个实施例中,式i化合物用于治疗具有h3k27m突变的癌症疾病,例如h3k27m突变的胶质瘤,尤其h3k27m突变的弥漫性中线胶质瘤。
3、本发明也提供wee1激酶抑制剂在制备用于治疗具有h3k27m突变的癌症疾病药物中的用途。在一个实施例中,所述wee1激酶抑制剂是式i化合物。在一个实施例中,所述具有h3k27m突变的癌症疾病是具有h3k27m突变的胶质瘤,尤其是h3k27m突变的弥漫性中线胶质瘤。
4、本发明也提供一种治疗具有h3k27m突变的癌症疾病的方法,所述方法为向有需求的受试者施用有效量的wee1激酶抑制剂。在一个实施例中,该方法包括施用有效量的式i化合物。在一个实施例中,所述具有h3k27m突变的癌症疾病是具有h3k27m突变的胶质瘤,尤其是h3k27m突变的弥漫性中线胶质瘤。
5、具体而言,本发明包括有用的wee1激酶抑制剂,尤其为小分子wee1激酶抑制剂。这些抑制剂包括但不限于本文所述,特别是,包括但不限于azd1775、zc-03、debio-0123、dn-1609、nuv-569、wo2007126122(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2019028008、wo2019173082和wo202021032(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2015092431和wo2018162932(取代的2,3-二氢嘧啶并[4,5-d]嘧啶-4(1h)-酮类化合物),wo2019037678(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2020210377和wo2020210383(取代的杂环化合物)、wo2020210375、wo2020210380、wo2020210381(取代的1,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2018133829(l,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮类化合物)、wo2019085933(l,2-二氢-3h-吡唑并[3,4-d]嘧啶-3-酮大环类化合物)、wo2018090939、wo2019011228和wo2021073491所公开的化合物。
6、在一个或多个实施方案中,该方法包括施用有效量的式i、ii或iii的化合物或其立体异构体、药学上可接受的盐或前药。
7、在一个或多个实施方案中,具有h3k27m突变的癌症是具有h3k27m突变的胶质瘤,包括但不限于胶质母细胞瘤、儿童弥漫性脑桥胶质瘤和弥漫性中线胶质瘤。
- 还没有人留言评论。精彩留言会获得点赞!