用于修饰的的制作方法
用于修饰的mhc表达的溶瘤病毒
1.交叉引用
2.本技术要求
2021
年4月
30
日提交的美国临时申请第
63/182,243
号的权益,该美国临时申请通过引用以其整体并入
。
3.背景
4.在美国,癌症是第二大死亡原因
。
商业可用疗法的挑战存在于癌细胞的选择性靶向
、
局部基因表达以及到达和改变肿瘤微环境
(tme)。
因此,仍然需要改进的组合物和使用方法来应对这些挑战
。
5.概述
6.本文提供了组合物,其中组合物包含:溶瘤病毒,其中溶瘤病毒包含基因组修饰,其中基因组修饰包括编码
mhc i
抑制剂的外源核酸
。
本文还提供了组合物,其中基因组修饰还包括:编码
mhc ii
抑制剂的内源核酸的缺失或功能性缺失;或导致
mhc ii
呈递的激活或增强的激活的外源核酸
。
本文还提供了组合物,其中基因组修饰还包括:编码
mhc ii
抑制剂的内源核酸的缺失或功能性缺失;和导致
mhc ii
呈递的激活或增强的激活的外源核酸
。
本文还提供了组合物,其中编码
mhc ii
抑制剂的内源核酸的缺失或功能性缺失包括编码蛋白
a35
的痘苗病毒基因的缺失或功能性缺失
。
本文还提供了组合物,其中编码蛋白
a35
的痘苗病毒基因的缺失或功能性缺失是基因
wr158
的缺失或功能性缺失
。
本文还提供了组合物,其中导致
mhc ii
呈递的激活或增强的激活的外源核酸编码选自以下的蛋白:凋亡抑制剂蛋白;坏死性细胞死亡激活剂蛋白;自噬增强剂蛋白;天冬酰胺内肽酶;
ii
类反式激活因子;干扰素-γ
;
toll
样受体激活剂;或树突状细胞成熟激活剂
。
本文还提供了组合物,其中外源核酸编码自噬增强剂蛋白,并且其中自噬增强剂蛋白是
hmgb1
或其功能性结构域或变体
。
本文还提供了组合物,其中外源核酸编码树突状细胞成熟激活剂,其中树突状细胞成熟激活剂包括骨桥蛋白
(osteopontin)、tnf-α
或其功能性片段或变体
。
本文还提供了组合物,其中由外源核酸编码的蛋白与分泌序列
、
细胞透化结构域
(cell permeabilizing domain)
或其组合融合
。
本文还提供了组合物,其中溶瘤病毒是痘病毒
、
腺相关病毒
、
腺病毒
、
新城疫病毒
(ndv)、
呼肠孤病毒
(rv)、
门戈病毒
、
黏液瘤病毒
(myxv)、
麻疹病毒
(mv)、
单纯疱疹病毒
(hsv)、
痘苗病毒
(vv)、
水泡性口炎病毒
(vsv)
和脊髓灰质炎病毒
(pv)。
本文还提供了组合物,其中痘病毒包括乙型昆虫痘病毒
(betaentomopoxvirus)、
亚塔痘病毒
(yatapoxvirus)、
鹿痘病毒
(cervidpoxvirus)、
丙型昆虫痘病毒
(gammaentomopoxvirus)、
兔痘病毒
(leporipoxvirus)、
猪痘病毒
(suipoxvirus)、
软疣痘病毒
(molluscipoxvirus)、
鳄鱼痘病毒
(crocodylidpoxvirus)、
甲型昆虫痘病毒
(alphaentomopoxvirus)、
山羊痘病毒
(capripoxvirus)、
禽痘病毒
(avipoxvirus)
或副痘病毒
(parapoxvirus)。
本文还提供了组合物,其中痘病毒是痘苗病毒
。
本文还提供了组合物,其中
mhc i
抑制剂引起
mhc i
呈递的抑制或部分抑制
。
本文还提供了组合物,其中编码
mhc i
抑制剂的外源核酸包含编码一种或更多种牛痘病毒蛋白的基因
。
本文还提供了组合物,其中编码
mhc i
抑制剂的外源核酸包含编码牛痘蛋白
cpxv012
或其功能性片段或变体的基因
。
本文还提供了组合物,其中编码
mhc i
抑制剂的外源核酸包含编码牛痘蛋白
cpxv203
或其功能性片段或变体的基因
。
本文还提供
了组合物,其中编码
mhc i
抑制剂的外源核酸包含编码以下至少一种的基因:
eb
病毒
(epstein-barr virus)
编码的核抗原1蛋白;单纯疱疹病毒编码的
icp47
蛋白;单纯疱疹病毒编码的
ul49.5
蛋白;巨细胞病毒编码的
us6、us2、us3、us11
或
gp48
蛋白;
eb
病毒编码的
bnlf2a
蛋白;腺病毒编码的
e3-19k
蛋白;人类免疫缺陷病毒或猿免疫缺陷病毒编码的
nef
蛋白;卡波西肉瘤相关疱疹病毒编码的
kk3、virf3
或
kk5
蛋白;或者
irf7
或
irf3
的显性负性形式
。
本文还提供了组合物,其中
mhc i
抑制剂包括
tap
抑制剂
。
本文还提供了组合物,其中
tap
抑制剂完全或主要在被感染的细胞内起作用
。
本文还提供了组合物,其中基因组修饰减少靶向病毒感染的肿瘤细胞的免疫应答,并增加靶向病毒感染的肿瘤细胞周围细胞的免疫应答
。
本文还提供了组合物,还包含胸苷激酶基因的缺失
。
本文还提供了组合物,还包含编码透明质酸酶的外源核酸
。
本文还提供了组合物,其中透明质酸酶为
ph-20
或
hysa。
本文还提供了组合物,其中溶瘤病毒是痘苗病毒,并且痘苗病毒是
western reserve
毒株痘苗病毒
(atcc vr-1354)、copenhagen
毒株
、ihd
毒株
、wyeth
毒株
(atcc vr-325)、nycboh
毒株
、tian tan
毒株
、lister
毒株
、ankara
毒株
(atcc vr-1508
或
attc vr1566)、ussr
毒株或
acam2000
毒株
。
7.本文提供了组合物,其中组合物包含溶瘤病毒,其中溶瘤病毒包含基因组修饰;其中基因组修饰包括编码
a35
蛋白的痘苗病毒基因的缺失或功能性缺失
、
以及编码牛痘蛋白
cpxv012
或牛痘蛋白
cpxv203
的外源基因的插入
。
本文还提供了组合物,其中溶瘤病毒是痘病毒
、
腺相关病毒
、
腺病毒
、
新城疫病毒
(ndv)、
呼肠孤病毒
(rv)、
门戈病毒
、
黏液瘤病毒
(myxv)、
麻疹病毒
(mv)、
单纯疱疹病毒
(hsv)、
痘苗病毒
(vv)、
水泡性口炎病毒
(vsv)
和脊髓灰质炎病毒
(pv)。
本文还提供了组合物,其中痘病毒包括乙型昆虫痘病毒
、
亚塔痘病毒
、
鹿痘病毒
、
丙型昆虫痘病毒
、
兔痘病毒
、
猪痘病毒
、
软疣痘病毒
、
鳄鱼痘病毒
、
甲型昆虫痘病毒
、
山羊痘病毒
、
禽痘病毒或副痘病毒
。
本文还提供了组合物,其中溶瘤病毒是痘苗病毒
。
本文还提供了组合物,其中编码牛痘蛋白
cpxv012
的外源基因位于编码痘苗病毒
a35
蛋白的基因的基因座
。
本文还提供了组合物,其中编码牛痘蛋白
cpxv203
的外源基因位于编码痘苗病毒
a35
蛋白的基因的基因座
。
本文还提供了组合物,其中基因组修饰还包括以下至少一种:编码趋化因子受体或其功能性结构域或变体的外源核酸;或编码细胞因子或其功能性结构域或变体的外源核酸
。
本文还提供了组合物,包含编码细胞因子或其功能性结构域或变体的外源核酸,其中细胞因子包括以下至少一种:白细胞介素-2(il-2)、
白细胞介素-15/
白细胞介素-15ra(il15/il15ra)、
白细胞介素-7(il-7)
或其功能性结构域或变体
。
本文还提供了组合物,其中基因组修饰包括编码包含细胞因子和代谢调节剂蛋白的融合蛋白的外源核酸的插入
。
本文还提供了组合物,包含编码趋化因子受体或其功能性结构域或变体的外源核酸,其中趋化因子受体包括以下至少一种:
cxcr4、ccr2
或其功能性结构域或变体
。
本文还提供了组合物,其中趋化因子受体包括
cxcr4
或其功能性结构域或变体
。
本文还提供了组合物,其中趋化因子受体包括
ccr2
或其功能性结构域或变体,其中
ccr2
包括野生型
ccr2
或突变的
ccr2。
本文还提供了组合物,其中编码趋化因子受体或其功能性结构域或变体的外源核酸包含密码子优化的序列
。
本文还提供了组合物,其中编码趋化因子受体或其功能性结构域或变体的外源核酸包含非密码子优化的序列
。
本文还提供了组合物,其中基因组修饰包括病毒基因的突变或完全缺失或部分缺失,所述病毒基因包括以下至少一种:痘苗病毒的
a52r、b15r、k7r、a46r、n1l、e3l、k1l、m2l、c16、n2r、b8r、b18r
或
vh1
或其功能性结构域或
片段或变体,或其任何组合
。
本文还提供了组合物,还包含胸苷激酶基因的缺失
。
本文还提供了组合物,还包含编码透明质酸酶的外源核酸
。
本文还提供了组合物,其中透明质酸酶为
ph-20
或
hysa。
本文还提供了组合物,其中溶瘤病毒是痘苗病毒,并且痘苗病毒是
western reserve
毒株痘苗病毒
(atcc vr-1354)、copenhagen
毒株
、ihd
毒株
、wyeth
毒株
(atcc vr-325)、nycboh
毒株
、tian tan
毒株
、lister
毒株
、ankara
毒株
(atcc vr-1508
或
attc vr1566)、ussr
毒株或
acam2000
毒株
。
8.本文提供了药物组合物,包含根据本文描述的组合物和药学上可接受的赋形剂
。
本文还提供了药物组合物,其中赋形剂包括以下一种或更多种:缓冲剂
、
稳定剂
、
抗氧化剂
、
黏合剂
、
稀释剂
、
分散剂
、
速率控制剂
、
润滑剂
、
助流剂
、
崩解剂
、
增塑剂
、
防腐剂或其任何组合
。
本文还提供了药物组合物,其中赋形剂包括磷酸氢二钠二水合物
、
磷酸二氢钠二水合物
、
氯化钠
、
肌醇
、
山梨醇或其任何组合
。
本文还提供了药物组合物,其中药物组合物不包含防腐剂
。
本文还提供了药物组合物,其还包含防腐剂
、
稀释剂和运载体中的一种或更多种
。
本文还提供了药物组合物,该药物组合物还包含另外的活性成分或其盐
。
本文还提供了药物组合物,其中赋形剂是无菌水
。
本文还提供了还包含另外的活性成分的药物组合物,其中另外的活性成分是抗癌剂或另外的溶瘤病毒
。
9.本文提供了减少癌细胞生长的方法,该方法包括向癌细胞施用:本文描述的组合物或药物组合物
。
10.本文提供了用于治疗癌症的方法,该方法包括:向患有癌症的受试者施用本文描述的组合物或药物组合物
。
本文还提供了方法,其中施用包括瘤内施用
、
腹膜内施用
、
口服施用
、
静脉内施用
、
鼻内施用
、
舌下施用
、
直肠施用
、
透皮施用或其任何组合
。
本文还提供了方法,包括施用另外的疗法,其中另外的疗法包括化学疗法
、
放疗
、
用另外的病毒进行的溶瘤病毒疗法
、
用免疫调节蛋白治疗
、car t
细胞疗法
、
抗癌剂或其任何组合
。
本文还提供了方法,其中另外的疗法包括施用免疫调节剂,免疫调节剂包括抗
cd33
抗体及其可变区
、
抗
cd11b
抗体及其可变区
、cox2
抑制剂
、
细胞因子
、
趋化因子
、
抗
ctla4
抗体或其抗原结合片段
、
抗
pd-1
抗体或其抗原结合片段
、
抗
pd-l1
抗体或其抗原结合片段或
tlr
激动剂
。
11.本文提供了治疗方法,包括向有相应需要的受试者施用本文描述的组合物或药物组合物
。
本文还提供了方法,其中施用包括瘤内施用
。
本文还提供了方法,其中施用包括全身施用
。
本文还提供了方法,其中全身施用包括以下至少一种:腹膜内施用
、
口服施用
、
静脉内施用
、
鼻内施用
、
舌下施用
、
直肠施用
、
透皮施用或其任何组合
。
本文还提供了方法,其中受试者患有癌症,并且其中癌症是以下至少一种:黑素瘤
、
肝细胞癌
、
乳腺癌
、
肺癌
、
非小细胞肺癌
、
腹膜癌
、
前列腺癌
、
膀胱癌
、
卵巢癌
、
白血病
、
淋巴瘤
、
肾细胞癌
、
胰腺癌
、
上皮癌
、
胃
/ge
结合部腺癌
、
宫颈癌
、
结肠癌
、
结肠直肠癌
、
十二指肠癌
、
胰腺腺癌
、
腺样囊性癌
、
肉瘤
、
间皮瘤
、
多形性胶质母细胞瘤
、
星形细胞瘤
、
多发性骨髓瘤
、
前列腺上皮癌
、
肝细胞癌
、
胆管癌
、
胰腺腺癌
、
头颈部鳞状细胞癌
、
宫颈鳞状细胞癌
、
骨肉瘤
、
上皮性卵巢癌
、
急性淋巴母细胞淋巴瘤
、
骨髓增生性肿瘤或其任何组合
。
本文还提供了方法,其中组合物或药物组合物以约
106pfu/ml
至约
10
10
pfu/ml
溶瘤病毒的剂量施用
。
本文还提供了方法,其中组合物或药物组合物以约
3x 109pfu/ml
溶瘤病毒的剂量施用
。
本文还提供了方法,其中组合物或药物组合物以三个剂量施用,并且其中三个剂量中的每一个以独立于任何其他剂量的施用量和施用时间段施用
。
本文还提供了方法,其中三个剂量以第一剂量
、
第二剂量和第三剂量施用,并
且其中第一剂量低于第二剂量,并且第二剂量低于第三剂量
。
本文还提供了方法,其中三个剂量以第一剂量
、
第二剂量和第三剂量施用,并且其中第一剂量高于第二剂量,并且第二剂量高于第三剂量
。
本文还提供了方法,其中三个剂量的施用时间段各自独立地为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周
、
约
12
周
、
约4个月
、
约5个月
、
约6个月
、
约7个月
、
约8个月
、
约9个月
、
约
10
个月
、
约
11
个月或约1年
。
本文还提供了方法,其中组合物或药物组合物独立地包括液体剂型,该液体剂型以约
1ml
至约
5ml、
约
5ml
至
10ml、
约
15ml
至约
20ml、
约
25ml
至约
30ml、
约
30ml
至约
50ml、
约
50ml
至约
100ml、
约
100ml
至
150ml、
约
150ml
至约
200ml、
约
200ml
至约
250ml、
约
250ml
至约
300ml、
约
300ml
至约
350ml、
约
350ml
至约
400ml、
约
400ml
至约
450ml、
约
450ml
至
500ml、
约
500ml
至
750ml、
或约
750ml
至
1000ml
的体积施用
。
本文还提供了方法,其中组合物或药物组合物以液体剂型
、
固体剂型
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
本文还提供了方法,其中组合物或药物组合物的施用持续时间为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周
、
约
12
周
、
约4个月
、
约5个月
、
约6个月
、
约7个月
、
约8个月
、
约9个月
、
约
10
个月
、
约
11
个月或约1年
。
本文还提供了方法,其中组合物或药物组合物每天一次
、
每天两次
、
每周一次
、
每两周一次或每三周一次施用
。
本文还提供了方法,其中组合物或药物组合物作为团注或缓慢输注施用
。
本文还提供了方法,其中施用组合物或药物组合物在施用第一剂量后约1小时至约3天后产生第一峰值病毒载量,并且在施用第一剂量后约3天至约
10
天后产生第二峰值病毒载量
。
本文还提供了方法,包括施用另外的疗法,其中另外的疗法的施用持续时间为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周或约
12
周
。
本文还提供了方法,其中另外的疗法每天一次
、
每天两次
、
每1天一次
、
每2天一次
、
每3天一次
、
每4天一次
、
每5天一次
、
每6天一次
、
每1周一次
、
每2周一次
、
每3周一次
、
每4周一次
、
每6周一次
、
每7周一次
、
每8周一次
、
每9周一次
、
每
10
周一次
、
每
12
周一次
、
每4个月一次
、
每5个月一次
、
每6个月一次
、
每7个月一次
、
每8个月一次
、
每9个月一次
、
每
10
个月一次
、
每
11
个月一次或每1年一次施用
。
本文还提供了方法,其中另外的疗法以液体剂型
、
固体剂型
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
本文还提供了方法,其中另外的疗法口服
、
静脉内
、
通过瘤内注射
、
通过腹膜内注射或通过辐射施用
。
本文还提供了方法,其中另外的疗法包括化学疗法
、
放疗
、
用另外的病毒进行的溶瘤病毒疗法
、
用免疫调节蛋白治疗
、car t
细胞疗法
、
抗癌剂或其任何组合
。
本文还提供了方法,其中另外的疗法包括施用免疫调节剂,免疫调节剂包括抗
cd33
抗体及其可变区
、
抗
cd11b
抗体及其可变区
、cox2
抑制剂
、
细胞因子
、
趋化因子
、
抗
ctla4
抗体或其抗原结合片段
、
抗
pd-1
抗体或其抗原结合片段
、
抗
pd-l1
抗体或其抗原结合片段或
tlr
激动剂
。
本文还提供了方法,其中另外的疗法包括施用抗癌剂,其中抗癌剂是化疗剂
。
本文还提供了方法,其中受试者是人类
。
12.本发明的其他目标
、
特征和优点将从以下详细描述变得明显
。
然而,应当理解,详细描述和具体实例,虽然指示本发明的优选的实施方案,但仅通过说明性方式给出,因为对本领域技术人员而言,本发明的精神和范围内的各种变化和修改从该详细描述将是明显的
。
13.附图简述
14.本公开内容的新颖的特征特别地在所附权利要求书中阐述
。
通过参考以下对利用本公开内容的原理的说明性实施方案加以阐述的详细描述以及附图,将会对本公开内容的特征和优点获得更好的理解
。
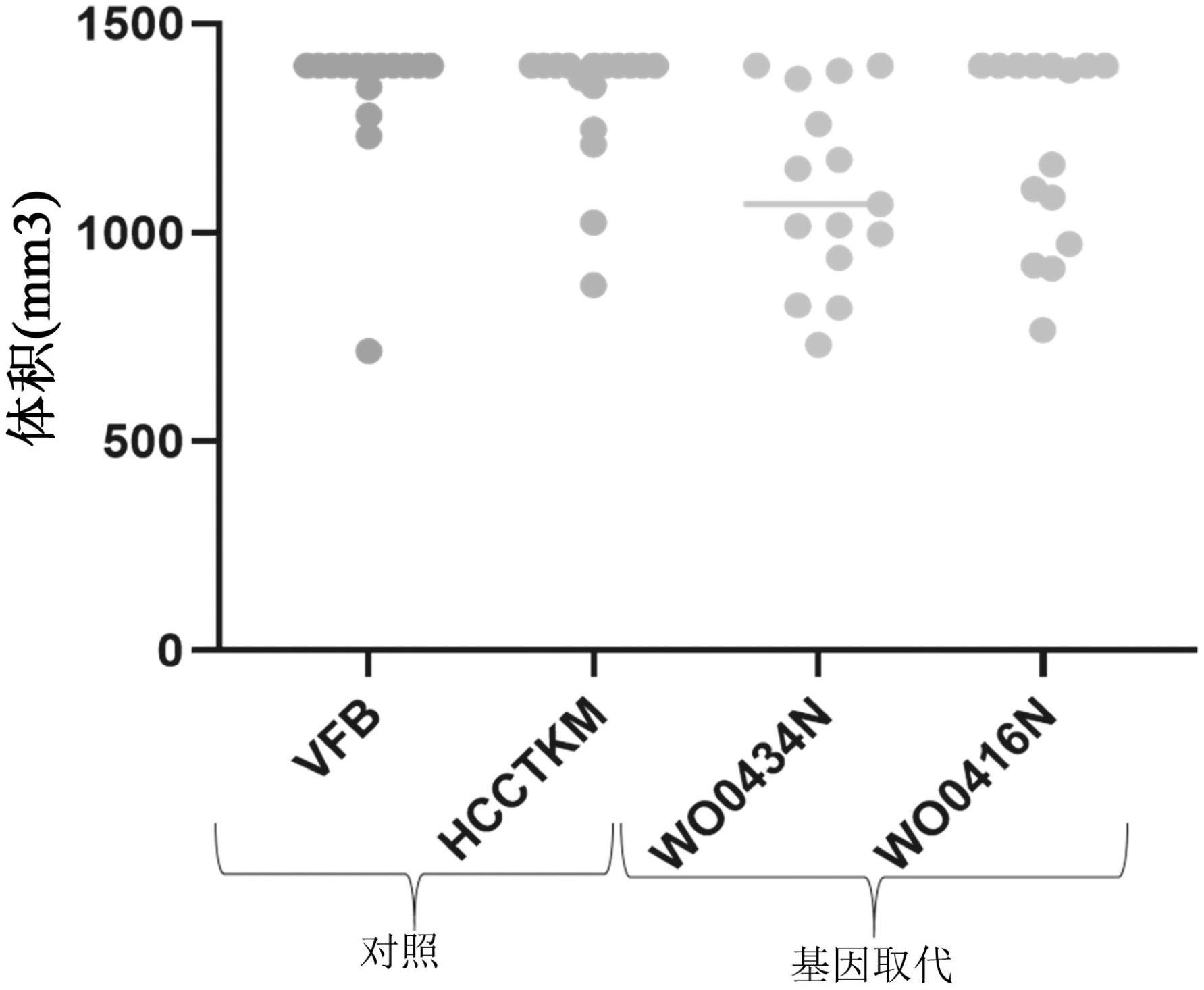
15.图1描绘了用媒介物配制的缓冲液
(vfb)
或重组痘苗病毒
(
包含:
tk
缺失
(hcctkm)
;
tk
和
a52r
缺失以及用牛痘
cpxv012
基因取代编码
a35
蛋白的基因
(wo0434n)
;或
tk
和
a52r
缺失而不插入外源核酸
(wo416n))
处理后,
b16
肿瘤体积的变化,在y轴上以立方毫米示出
。
16.图
2a
和图
2b
描绘了在用媒介物配制的缓冲液
(vfb)
或重组痘苗病毒
(
包含:
(1)tk
基因缺失和编码牛痘病毒
v012
蛋白的核酸的插入;
(2)wr158
基因缺失和编码牛痘病毒
v012
蛋白的核酸的插入;
(3)tk
基因缺失和编码显性负性干扰素调节因子
7(dnirf7)
的核酸的插入;或
(4)tk
基因缺失和编码病毒干扰素调节因子
3(virf3)
的核酸的插入
)
处理后,
renca(
图
2a)
或
emt6(
图
2b)
肿瘤体积的变化,在y轴上以立方毫米示出
。
17.本公开内容详述
18.虽然本文已经示出和描述了本公开内容的优选实施方案,但对于本领域技术人员将明显的是,此类实施方案仅通过示例的方式提供
。
本领域技术人员现将想到不偏离本公开内容的许多变化
、
改变和替换
。
应当理解,可以在实践本公开内容时采用本文描述的本公开内容的实施方案的各种替代方案
。
19.在一些实施方案中,本公开内容提供了重组溶瘤病毒和使用所述溶瘤病毒治疗癌症的方法
。
在一些实施方案中,本公开内容的溶瘤病毒在病毒基因组中包含编码外源核酸的修饰,以通过重塑肿瘤微环境和增强的全身递送来增强溶瘤免疫疗法
。
本公开内容还涉及用于癌症治疗的包含这样的溶瘤病毒的物质的组合物和使用方法以及药盒
。
20.某些定义
21.如本文所用,单数形式单数形式“一个
/
种
(a)”、“一个
/
种
(an)”和“该
/
所述
(the)”可以指单数以及复数两者,除非上下文另外明确指示
。
如本文所用,术语“包括
/
包含
(comprise)”可以意指“包括
/
包含
(include)”。
因此,“在病毒基因组中包含一个或更多个修饰”可以意指“在病毒中包含至少一个修饰”,而不排除其他元件
。
在有冲突的情况下,应以本说明书包括术语的解释为准
。
另外,材料
、
方法和实例仅为说明性的而并非意图限制
。
术语“约
(about)”或“大约
(approximately)”可以意指在如由本领域普通技术人员确定的特定值的可接受误差范围之内,这将部分地取决于值如何被测量或确定,例如,测量系统的局限性
。
例如,根据给定值的实践,“约”可以表示在1个或大于1个标准差内
。
在本技术和权利要求书中描述特定值的情况下,除非另有说明,术语“约”应被假定为意指特定值的可接受误差范围,诸如由术语“约”修饰的值的
±
10
%
。
22.如本文定义的术语“重组溶瘤病毒”包括被设计为缺失或功能性缺失一个或更多个内源核酸序列和
/
或插入或部分插入一个或更多个外源核酸序列的溶瘤病毒毒株
。
该术语还包括在相同或不同基因座处用一个或更多个外源核酸取代病毒基因组中的一个或更多个内源核酸序列
。
23.如本文所用的术语“有效量”可以指足以实现有益或期望结果的剂
(
诸如本文公开的重组溶瘤病毒,以及其他抗癌剂
)
的量
。
有效量
(
也称为治疗有效量
)
可以取决于以下一种或更多种而变化:被治疗的受试者和疾病状况
、
受试者的体重和年龄
、
疾病状况的严重程度
、
施用方式等,这可以由本领域普通技术人员容易地确定
。
有益的治疗作用可以包括但不
限于诊断确定的实现;疾病
、
症状
、
紊乱或病理状况的改善;减少或预防疾病
、
症状
、
紊乱或状况的发作;并且通常对抗疾病
、
症状
、
紊乱或病理状况
。
24.综述
25.本文提供了涉及抑制病毒感染的细胞内主要组织相容性复合体
(mhc)i
类呈递的组合物和方法,作为(i)减少靶向病毒和病毒感染的细胞的免疫应答同时增加靶向周围肿瘤的免疫应答的手段
。
本文还提供了用于重组溶瘤病毒的组合物和方法,该重组溶瘤病毒被工程化为激活主要组织相容性复合体
(mhc)ii
类在整个肿瘤微环境中的呈递,同时还帮助克服由肿瘤介导的
mhc ii
呈递的下调介导的对免疫肿瘤学疗法
(
例如,免疫检查点抑制剂疗法
)
的免疫抗性
。
26.在一些实施方案中,重组溶瘤病毒是痘苗病毒,其中痘苗病毒可以被修饰,使得病毒(i)被缺失了痘苗病毒的天然
mhc ii
抑制剂;及
(ii)
已被工程化为表达来自牛痘病毒的
mhc i
抑制剂
。
在一些方面,本文示出了用编码驱动牛痘蛋白
cpxv012(ncbi
登录号
np_619801)(seq id no:2)
表达的病毒启动子
p7.5(seq id no:1)
的
dna
序列或用编码牛痘蛋白
cpxv203
的
dna
序列取代编码蛋白
a35(ncbi
登录号
yp_233040)
的痘苗病毒基因
wr158
可以导致比没有这种取代的相同病毒更高的治疗活性
。
27.在一些实施方案中,
mhc i
抑制剂可以选自一种或更多种
tap
抑制剂,诸如
ul49.5
;
icp47
;
us6
,
bnlf2a。
28.在一些实施方案中,
mhc ii
呈递的更好的激活可以通过其他方法实现,包括或不包括痘苗病毒的天然
mhc ii
抑制剂的缺失
。
这些其它方法包括但不限于在重组痘苗病毒中进行修饰,使得通过编码以下至少一种的基因的插入来修饰病毒基因组:凋亡抑制剂蛋白或坏死性细胞死亡激活剂蛋白;自噬增强剂蛋白
(
例如
hmgb1)
;天冬酰胺内肽酶;
ii
类反式激活因子
(ciita)
;干扰素-γ
;
toll
样受体
(tlr)
激活剂;树突状细胞
(dc)
成熟激活剂
(
例如骨桥蛋白或
tnf-α
)
或
fas
配体
。
29.在一些实施方案中,主要组织相容性复合体
(mhc)i
类呈递的抑制可以通过其他方法实现,包括或不包括来自表达
mhc i
抑制剂的牛痘病毒的基因的插入
。
这些其它方法包括但不限于在病毒基因组中插入外源基因,该外源基因来自来源于疱疹病毒的一种或更多种
mhc i
抑制剂,诸如
eb
病毒编码的核抗原
1(ebna1)
或
bnlf2a
蛋白
、
单纯疱疹病毒编码的
icp47
或
ul49.5
蛋白
、
单纯疱疹病毒编码的蛋白
、
人类巨细胞病毒
(hcmv)
编码的
us6、us2、us3、us11
或
gp48
蛋白
、eb
病毒编码的
bnlf2a
蛋白
、
卡波西肉瘤相关疱疹病毒
(kshv)
编码的
kk3、virf3
或
kk5
蛋白或
irf7
的显性负性形式
。
30.下调
mhc i
的其他病毒蛋白包括例如腺病毒编码的
e3-19k
蛋白
、
人类免疫缺陷病毒1编码的
nef
蛋白
、
人类免疫缺陷病毒2编码的
nef
蛋白和猿免疫缺陷病毒1编码的
nef
蛋白
。
31.溶瘤病毒
32.本文提供了包含经修饰的溶瘤病毒的组合物
。
修饰包括添加本文描述的外源核酸
。
进一步的修饰包括添加本文描述的基因组修饰
。
本文描述的组合物中包含的示例性溶瘤病毒包括但不限于痘病毒
、
腺相关病毒
、
腺病毒
、
新城疫病毒
(ndv)、
呼肠孤病毒
(rv)、
门戈病毒
、
黏液瘤病毒
(myxv)、
麻疹病毒
(mv)、
单纯疱疹病毒
(hsv)、
痘苗病毒
(vv)、
水泡性口炎病毒
(vsv)
和脊髓灰质炎病毒
(pv)。
这些溶瘤病毒具有特异性靶向癌细胞的倾向,并且在
病毒复制时引起显著的细胞死亡和肿瘤消退
。
在一些实施方案中,本文描述的溶瘤病毒通过诸如直接裂解所述细胞
、
刺激对所述细胞的免疫应答
、
凋亡
、
毒性蛋白的表达
、
自噬和蛋白合成的关闭
、
抗肿瘤免疫的诱导或其任何组合的机制杀伤癌症或肿瘤细胞
。
在一些实施方案中,痘病毒包括乙型昆虫痘病毒
、
亚塔痘病毒
、
鹿痘病毒
、
丙型昆虫痘病毒
、
野兔痘病毒
、
猪痘病毒
、
软疣痘病毒
、
鳄鱼痘病毒
、
甲型昆虫痘病毒
、
山羊痘病毒
、
禽痘病毒或副痘病毒
。
在一些实施方案中,痘病毒包括痘苗病毒
。
在一些实施方案中,痘病毒是痘苗病毒
。
33.基于这些方法,还提供了用于肿瘤疗法的组合物和方法,使得靶向肿瘤中被感染的细胞的免疫应答减少,而相反,未被感染的肿瘤细胞被更好地靶向
(
例如,这种方法可以减少抗病毒免疫,有利于抗肿瘤免疫应答
)。
34.本文提供了掺入了基因组修饰的重组病毒,该基因组修饰包括插入
、
突变或缺失,以及本文描述的外源基因的插入
。
在一些实施方案中,这样的修饰是通过与转移载体的自发重组产生的
。
例如,载体可以是环状质粒或线性
dna
片段,可以包含将被添加到病毒基因组中的期望的
dna
序列,随后是在强病毒启动子下的编码
floxxed
荧光报告物蛋白的基因
。
这样的组分的侧翼可以是
200
个至
1000
个碱基长度的
dna
序列,该序列与紧接在期望的整合位点之前和之后的病毒基因组
dna
同源,其指导载体有效载荷加报告物的位点特异性整合
。
将纯化的载体
dna
转染到病毒敏感的黏附细胞系中,例如:在6孔细胞培养板的单个孔中以大约一百万个细胞接种的
143b。
转染的细胞然后被病毒感染,载体
dna
意图整合到该病毒中
。
载体和病毒基因组之间的重组在病毒复制期间自发发生
。
感染后一至三天,通过移除培养基并裂解细胞单层,从转染的细胞中收获重组病毒
(
与亲本病毒一起
)。
通过噬斑选择从亲本病毒中纯化重组病毒
。
多孔板
(
例如,
96
孔,被处理用于黏附细胞培养
)
在噬斑选择的当天,每孔接种
1.2
×
104-3.0
×
104
个之间的细胞
。
将包含重组病毒和亲本病毒混合物的裂解物声处理,然后在细胞培养基中稀释,并分布在接种的
96
孔板第一行的孔之间
。
将来自感染行的培养基混合并转移到板中下一个相邻的细胞行中
。
对选择板中的所有行进行系列稀释过程
。
被感染的板在细胞培养箱中储存两到三天,以允许噬斑形成
。
由重组病毒形成的噬斑由于报告物表达而发出荧光,并使用荧光显微镜鉴定
。
使用单通道微量移液器手动挑选重组噬斑,通常从每个噬斑中挑选
0.5
微升至
3.0
微升的物质
。
优选的噬斑是圆的,报告物强度均匀,并且在它们的孔中是单独的
。
将挑选的噬斑冷冻
、
解冻,然后稀释并用于感染另外的
96
孔选择板
。
在几轮选择后,获得了重组噬斑的纯群体
(
完全
gfp
阳性
)。
然后通过用在病毒启动子下编码
cre
重组酶的载体转染细胞,从病毒基因组中缺失报告物
。
转染的细胞被报告物阳性病毒感染,允许表达的
cre
去除
floxxed
报告物
。
以与先前描述的相同的方式通过噬斑选择
(
靶向单独在它们的孔中的缺乏
gfp
的噬斑
)
纯化无报告物病毒
。
35.重组痘苗病毒
36.在一些实施方案中,溶瘤病毒是痘苗病毒
。
如本文可互换使用的,术语“重组痘苗病毒”或“重组痘苗病毒”可以涉及已被修饰的痘苗病毒
。
示例性修饰包括但不限于引入病毒主链突变,以表达痘苗病毒的基因
/
肽,或缺失基因,其中修饰尤其促进增强的免疫应答
。
在一些实施方案中,引入病毒主链突变包括一种或更多种毒力基因的完全缺失或部分缺失,或一种或更多种病毒毒力基因
(
非限制性实例包括已知抑制参与
th1
免疫应答或参与先天免疫信号传导的细胞因子的基因,或免疫应答的其他组分的抑制剂,或用与来自其他痘病毒的功能相当的效力更强或更弱的基因交换的痘苗毒力基因
)
的取代
。
37.病毒基因组中的修饰可以在基因组内的一个或更多个位置处
。
在一些实施方案中,病毒基因组中的修饰连续地位于基因组中
。
在一些实施方案中,病毒基因组中的修饰分布在整个基因组中
。
38.示例性痘苗病毒包括但不限于通过包含本文描述的融合构建体进行修饰的以下毒株:
western reserve
痘苗病毒
(atcc vr-1354)、
痘苗病毒
ankara(atcc vr-1508)、
痘苗病毒
ankara(atcc vr-1566)、
痘苗病毒毒株
wyeth(atcc vr-1536)
或痘苗病毒
wyeth(atcc vr-325)。
此外,在一些实施方案中,重组痘苗病毒是野生型或减毒痘苗病毒株的修饰形式
。
痘苗病毒毒株的非限制性实例包括痘苗病毒的
western reserve
毒株
、copenhagen
毒株
、wyeth(nycboh)
毒株
、tian tan
毒株
、lister、ussr、ankara、nyvac
毒株和重组痘苗病毒
ankara(mva)。
包含在本文描述组合物中的另外的示例性毒株是以下但不限于以下:
western reserve
毒株痘苗病毒
、copenhagen
毒株
、ihd
毒株
、wyeth
毒株
、nycboh
毒株
、tian tan
毒株
、lister
毒株
、ankara
毒株
、ussr
毒株或
acam2000
毒株
。
如本文阐述修饰的基础痘苗病毒株本身可以包含相对于其亲本毒株的一个或更多个突变,例如但不限于以下一个或更多个:
tk
中的缺失
(
本文也称为“tk
‑”
)
;
a52
中的缺失
(
本文也称为“a52
‑”
)。
示例性痘苗病毒是
western reserve
痘苗病毒
。
任何已知的痘苗病毒,或其对应于本文提供的或本领域技术人员已知的修饰,也涵盖在本技术的范围内
。
39.抑制
mhc i
呈递的修饰
40.肽在主要组织相容性复合体i或
mhc i
上的呈递是肽呈递在细胞上以向免疫系统发出病毒感染细胞警报的途径
。
例如,被感染的细胞可以在
mhc i
上呈递病毒肽,从而提醒细胞毒性
t
淋巴细胞破坏这些细胞
。
当宿主被重组溶瘤病毒感染时,
mhc i
上肽的呈递可以被抑制
。
41.在本公开内容的一些实施方案中,本文提供了重组溶瘤病毒的修饰,其提供了对
mhc i
呈递的抑制或部分抑制
。
修饰可以包括外源性
mhc i
抑制剂的插入或部分插入
。mhc i
抑制剂的插入可以由编码所述
mhc i
抑制剂的外源核酸提供
。
编码所述
mhc i
抑制剂的外源核酸可以插入到溶瘤病毒基因组的核酸序列中,诸如牛痘病毒
。
在某些情况下,
mhc i
抑制剂被插入到非编码区中
。
在其他情况下,抑制剂被插入到溶瘤病毒的编码病毒蛋白的核酸序列中
。
在某些情况下,
mhc i
抑制剂被插入到溶瘤病毒基因组的允许病毒在肿瘤细胞中复制的区域中
。
在某些情况下,关于牛痘病毒,
mhc i
抑制剂可以插入到至少1个
、
至少2个
、
至少3个
、
至少4个
、
至少5个
、
至少6个
、
至少7个
、
至少8个
、
至少9个或至少
10
个基因中
。
编码牛痘病毒蛋白的基因可以是
cpxv012、cpxv203
或其任何组合
。
在一些实施方案中,牛痘病毒蛋白,包括取代
、
插入和缺失的任何组合,可以产生与病毒基因或由该基因编码的病毒蛋白的野生型序列具有小于
100
%
、99
%
、98
%
、97
%
、96
%
、95
%
、94
%
、93
%
、92
%
、91
%
、90
%或更小序列同源性的序列
。mhc i
呈递可以降低至少1%
、
至少2%
、
至少5%
、
至少
10
%
、
至少
15
%
、
至少
20
%
、
至少
25
%
、
至少
30
%
、
至少
35
%
、
至少
40
%
、
至少
45
%
、
至少
50
%
、
至少
55
%
、
至少
65
%
、
至少
70
%
、
至少
75
%
、
至少
80
%
、
至少
85
%
、
至少
95
%或至少
100
%
。
42.在一些实施方案中,外源核酸可以编码至少一种
tap
抑制剂
。
在一些实施方案中,外源核酸可以编码选自由以下组成的组的至少一种基因:
eb
病毒编码的核抗原
1(ebna1)
蛋白
、
单纯疱疹病毒编码的
icp47
蛋白
、
单纯疱疹病毒编码的
ul49.5
蛋白
、
人类巨细胞病毒
(hcmv)
编码的
us6、us2、us3
或
us11
蛋白
、eb
病毒编码的
bnlf2a
蛋白
、
腺病毒编码的
e3-19k
蛋
白
、
巨细胞病毒编码的
gp48
蛋白
、
人类免疫缺陷病毒编码的
nef
蛋白
、
卡波西肉瘤相关疱疹病毒
(kshv)
编码的
kk3、virf3
或
kk5
蛋白或
irf7
的显性负性形式
。
43.激活
mhc ii
类呈递的修饰
44.在本公开内容的一些实施方案中,本文提供了导致
mhc ii
呈递的激活的重组溶瘤病毒的修饰,其中该修饰可以包括以下至少一种:
i)
一种或更多种
mhc ii
抑制剂
(
例如,天然
mhc ii
抑制剂
)
的缺失或部分缺失;
ii)
凋亡抑制剂蛋白或坏死性细胞死亡激活剂蛋白的插入;或其任何组合
。
修饰可以是溶瘤病毒基因的缺失
。
修饰可以是
a35
编码基因的缺失
(
完全或部分缺失
)。a35
编码缺失的修饰可以是病毒基因
wr158
的缺失或功能性缺失
。
在一些实施方案中,
mhc ii
抑制剂,包括取代
、
插入和缺失的任何组合,可以产生与病毒基因或由该基因编码的病毒蛋白的野生型序列
(
即病毒的天然
mhc ii
抑制剂
)
具有小于
100
%
、99
%
、98
%
、97
%
、96
%
、95
%
、94
%
、93
%
、92
%
、91
%
、90
%或更小序列同源性的序列
。
与不包含激活或增强
mhc ii
呈递的修饰但在其他方面相同的病毒相比,
mhc ii
呈递可以被激活或增强至少1%
、
至少2%
、
至少5%
、
至少
10
%
、
至少
15
%
、
至少
20
%
、
至少
25
%
、
至少
30
%
、
至少
35
%
、
至少
40
%
、
至少
45
%
、
至少
50
%
、
至少
55
%
、
至少
65
%
、
至少
70
%
、
至少
75
%
、
至少
80
%
、
至少
85
%
、
至少
95
%或至少
100
%
。
45.引起
mhc ii
呈递的激活或增强的修饰可以包括选自由以下组成的组的一种或更多种基因的插入:凋亡抑制剂蛋白或坏死性细胞死亡激活剂蛋白;自噬增强剂蛋白;天冬酰胺内肽酶;
ii
类反式激活因子
(ciita)
;干扰素-γ
;
toll
样受体
(tlr)
激活剂;树突状细胞
(dc)
成熟激活剂
(
例如骨桥蛋白或
tnf-α
)。
在某些情况下,
mhc ii
增强剂可以被修饰以包含分泌序列和细胞透化结构域,以提供免疫旁观者效应
(immunological bystander effect)。
在一些情况下,自噬增强剂蛋白包括
hmgb1、pias3、light、itac、
分形趋化因子,其功能性结构域或片段或变体,或其任何组合
。
在一些情况下,自噬增强剂蛋白包括
hmgb1。
在一些情况下,
hmgb1
包括如在
seq id no:4
中列出的核酸序列或在
seq id no:5
中列出的氨基酸序列
。
在一些情况下,分泌序列包括
ige
来源的信号序列
。
在一些情况下,
ige
来源的信号序列包括如在
seq id no:6
中列出的核酸序列或在
seq id no:7
中列出的氨基酸序列
。
在一些情况下,用
ige
来源的信号序列修饰
hmgb1
,其中修饰的
hmgb1
包括如在
seq id no:8
中列出的核酸序列或在
seq id no:9
中列出的氨基酸序列
。
46.同时的
mhc ii
上调
(
理想情况下发生在未被感染的细胞中,但这不是必需的
)
导致更有效的对肿瘤抗原的靶向
(
例如,
mhc ii
下调是对抗
pd1/pdl1
抗体的常见肿瘤耐药机制之一
)。
47.本文提供了重组溶瘤病毒的修饰,其提供了如本文描述的
mhc i
呈递的抑制或部分抑制,并且还提供了如本文描述的
mhc ii
呈递的激活
。
在一些情况下,修饰是在基因组的单独的位置
。
在一些情况下,修饰是在基因组的相同位置
。
在一些情况下,修饰是在基因组的相邻位置
。
48.其他多重修饰
49.在一些实施方案中,本文提供了包含重组溶瘤病毒的疫苗,所述重组溶瘤病毒在病毒基因组
(
本文也称为病毒主链
)
中含有插入
、
突变或缺失
。
在溶瘤痘苗病毒的情况下,它们优选是重组的或被选择为具有低毒性并在靶组织中积累
。
在一些实施方案中,病毒主链
/
病毒基因组中的修饰是使痘苗病毒为非复制性或包含不良复制能力的修饰
。
这样的修饰的
非限制性实例可包括下列病毒基因中的突变:
tk、a1、a2、vh1、a33、i7、f13l、a36r、a34r、a46r、a49r、b8r、b14r、b15r、b18r、c12l、c4、c16、spi-1、spi-2、b15r、vgf、e3l、k1l、k3l、k7r、a41l、m2l、n1l、a52r
,其功能性结构域或片段或变体,或其任何组合
。
50.在一些实施方案中,关于痘苗病毒,病毒主链突变选自由以下组成的组:
a52r
基因的完全或部分缺失;
tk
基因的完全或部分缺失;
f13l
基因的完全或部分缺失;
a36r
基因的完全或部分缺失;
a34r
基因的完全或部分缺失;
b8r
基因的完全或部分缺失;基因;
b18r
基因的完全或部分缺失;
c12l
基因的完全或部分缺失;
c4
基因的完全或部分缺失;
c16
基因的完全或部分缺失;
spi-1
基因的完全或部分缺失;
spi-2
基因的完全或部分缺失;
vgf
基因的完全或部分缺失;
e3l
基因的完全或部分缺失;
k3l
基因的完全或部分缺失;
a41l
基因的完全或部分缺失;基因;
a52r
基因的完全或部分缺失;
b15r
基因的完全或部分缺失;
k7r
基因的完全或部分缺失;
b14r
基因的完全或部分缺失;
n1l
基因的完全或部分缺失;
k1l
基因的完全或部分缺失;
m2l
基因的完全或部分缺失;
a49r
基因的完全或部分缺失;
vh1
基因的完全或部分缺失;
a33
基因的完全或部分缺失;
a1
的全部或部分缺失;
a2
基因的完全或部分缺失;
i7
基因的完全或部分缺失,以及
a46r
基因的完全或部分缺失
。
如本文所用的,提及病毒基因可以通过提及由该基因编码的蛋白来进行
(
例如,
a33
基因可以意指编码
a33
蛋白的基因
)。
51.在一些实施方案中,溶瘤病毒的病毒主链突变,包括取代
、
插入和缺失的任何组合,可以产生与病毒基因或由该基因编码的病毒蛋白的野生型序列具有小于
100
%
、99
%
、98
%
、97
%
、96
%
、95
%
、94
%
、93
%
、92
%
、91
%
、90
%或更小序列同源性的序列
。
在一些实施方案中,病毒基因和由其编码的蛋白选自由以下组成的组:
tk、a1、a2、vh1、a33、i7、f13l、a36r、a34r、a46r、a49r、b8r、b14r、b15r、b18r、c12l、c4、c16、spi-1、spi-2、b15r、vgf、e3l、k1l、k3l、k7r、a41l、m2l、n1l
和
a52r。
52.在一些实施方案中,病毒主链可以包含病毒蛋白
(
例如,病毒抗原
)
的氨基酸序列中的1种
、2
种
、3
种
、4
种
、5
种或更多种突变
。
在一些实例中,病毒抗原选自由以下组成的组:
tk、a1、a2、vh1、a33、i7、f13l、a36r、a34r、a46r、a49r、b8r、b14r、b15r、b18r、c12l、c4、c16、spi-1、spi-2、b15r、vgf、e3l、k1l、k3l、k7r、a41l、m2l、n1l
和
a52r。
53.在一些实施方案中,本公开内容提供了在病毒基因组
(
病毒主链
)
中包含一种或更多种突变的重组溶瘤病毒,使得该突变增加了免疫应答的
t
细胞臂
(t-cell arm)。
突变可以是病毒基因组
(
溶瘤病毒的野生型或减毒天然毒株
)
中一个或更多个核酸的添加
、
缺失或取代
。
54.在非限制性实例中,突变可以是已知抑制参与
th1
免疫应答的细胞因子的基因的完全或部分缺失
。
作为非限制性实例,突变可以是编码
b8r(
干扰素
γ
(ifn-g)
结合蛋白
)
;
c12l(
白细胞介素-18(il-18)
结合蛋白
)
的核酸的缺失
。
55.在另外的非限制性实例中,突变可以是先天免疫信号传导中基因的完全或部分缺失
。
作为非限制性实例,突变可以是编码
b18r(i
型干扰素
(ifn)
结合蛋白
)
;
a52r(
核因子
κ
b(nf-κ
b)
抑制剂蛋白
)
;
e3l(
蛋白激酶
(pkr)
抑制剂
)
;
c4
,
c16(sting
途径抑制剂
)
的核酸的缺失
。
56.在另外的非限制性实例中,突变可以是编码用于抑制免疫应答的其他组分的蛋白的基因的完全或部分缺失
。
作为非限制性实例,突变可以是编码
b15、k7、b14、n1、k1、m2、a49、vh1、a46
或其组合的核酸的完全或部分缺失
。
病毒主链突变也可以包括用主要是来自
其他痘病毒的功能相当的有效基因取代溶瘤毒力基因
。
57.本公开内容的多肽的氨基酸序列变体可以是取代的
、
插入的或缺失的变体
。
与野生型相比,编码病毒多肽的基因中的突变可影响多肽的1个
、2
个
、3
个
、4
个
、5
个
、6
个
、7
个
、8
个
、9
个
、10
个
、11
个
、12
个
、13
个
、14
个
、15
个
、16
个
、17
个
、18
个
、19
个
、20
个
、21
个
、22
个
、23
个
、24
个
、25
个
、26
个
、27
个
、28
个
、29
个
、30
个
、31
个
、32
个
、33
个
、34
个
、35
个
、36
个
、37
个
、38
个
、39
个
、40
个
、41
个
、42
个
、43
个
、44
个
、45
个
、46
个
、47
个
、48
个
、49
个
、50
个
、51
个
、52
个
、53
个
、54
个
、55
个
、56
个
、57
个
、58
个
、59
个
、60
个
、61
个
、62
个
、63
个
、64
个
、65
个
、66
个
、67
个
、68
个
、69
个
、70
个
、71
个
、72
个
、73
个
、74
个
、75
个
、76
个
、77
个
、78
个
、79
个
、80
个
、81
个
、82
个
、83
个
、84
个
、85
个
、86
个
、87
个
、88
个
、89
个
、90
个
、91
个
、92
个
、93
个
、94
个
、95
个
、96
个
、97
个
、98
个
、99
个
、100
个
、110
个
、120
个
、130
个
、140
个
、150
个
、160
个
、170
个
、180
个
、190
个
、200
个
、210
个
、220
个
、230
个
、240
个
、250
个
、275
个
、300
个
、325
个
、350
个
、375
个
、400
个
、425
个
、450
个
、475
个
、500
个或更多个非连续或连续氨基酸
。
58.缺失变体可缺少天然或野生型蛋白的一个或更多个残基
。
单个残基可以被缺失,或结构域
(
诸如催化或结合结构域
)
的全部或部分可以被缺失
。
终止密码子可以被引入
(
通过取代或插入
)
编码核酸序列中以产生截短的蛋白
。
插入突变体通常涉及在多肽的非末端点添加物质
。
这可以包括插入免疫反应性表位或简单的一个或更多个残基
。
也可以产生末端添加物,称为融合蛋白
。
59.取代变体通常在蛋白内的一个或更多个位点含有一个氨基酸与另一个氨基酸的交换,并且可以被设计成调节多肽的一个或更多个特性,具有或不具有其他功能或特性的损失
。
取代可以是保守的,即一个氨基酸被用形状和电荷相似的氨基酸替代
。
保守取代可以包括,例如,以下的变化:丙氨酸到丝氨酸;精氨酸到赖氨酸;天冬酰胺到谷氨酰胺或组氨酸;天冬氨酸到谷氨酸;半胱氨酸到丝氨酸;谷氨酰胺到天冬酰胺;谷氨酸到天冬氨酸;甘氨酸到脯氨酸;组氨酸到天冬酰胺或谷氨酰胺;异亮氨酸到亮氨酸或缬氨酸;亮氨酸到缬氨酸或异亮氨酸;赖氨酸到精氨酸;甲硫氨酸到亮氨酸或异亮氨酸;苯丙氨酸到酪氨酸
、
亮氨酸或甲硫氨酸;丝氨酸到苏氨酸;苏氨酸到丝氨酸;色氨酸到酪氨酸;酪氨酸到色氨酸或苯丙氨酸;缬氨酸到异亮氨酸或亮氨酸
。
可选地,取代可以是非保守的,从而影响多肽的功能或活性
。
非保守性变化通常包括用化学上不同的残基取代残基,诸如用极性或带电氨基酸取代非极性或不带电氨基酸,并且反之亦然
。
60.本文提供的溶瘤病毒包含在病毒基因组中另外的插入
、
突变
、
缺失或取代
。
溶瘤病毒可以包含外源核酸的一个或更多个另外插入或部分插入,该外源核酸编码趋化因子受体
、trif
蛋白或其功能性结构域中的一种或更多种,或瘦素
、
白细胞介素-2(il2)、
白细胞介素-15/
白细胞介素-15ra(il15/il15 ra)、
白细胞介素-7(il-7)、
瘦素-白细胞介素融合蛋白
(
例如,实施例1中示为
l2
的瘦素-il2
融合蛋白
)
中的一种或更多种
。
在一些情况下,核酸编码如
seq id no:10
中列出的
il15
氨基酸序列
。
在一些情况下,核酸编码如
seq id no:13
或
14
的任一项中列出的
il-7
氨基酸序列
。
修饰
(
诸如趋化因子受体的插入
)
是野生型和
/
或突变型
ccl5、cxcr4、ccr2、ccl2
的插入
。
在一些情况下,核酸编码如
seq id no:18-20
的任何一个中列出的
cxcr4
氨基酸序列
。
在一些情况下,核酸编码如
seq id no:18
中列出的
cxcr4
氨基酸序列
。
在一些情况下,核酸编码如
seq id no:23-24
的任何一个中列出的
ccr2
氨基酸序列
。
溶瘤病毒还可以包含来自以下的一个或更多个基因的一个或更多个另外的缺失或部
分缺失:
tk、a1、a2、vh1、a33、i7、f13l、a36r、a34r、a46r、a49r、b8r、b14r、b15r、b18r、c12l、c4、c16、spi-1、spi-2、b15r、vgf、e3l、k1l、k3l、k7r、a41l、m2l、n1l、a52r
,其功能性结构域或片段或变体,或其任何组合
。
在一些情况下,本文提供的溶瘤病毒可以包含
a52r
基因的完全或部分缺失和趋化因子受体诸如
ccr2
的插入
。
在一些情况下,本文提供的溶瘤病毒可以包含
a52r
基因的完全或部分缺失和趋化因子受体诸如
ccr2
的插入
。
在一些情况下,本文提供的溶瘤病毒可以包含以下至少一种的完全或部分缺失:
a52r
或
tk
病毒基因,以及编码融合蛋白
(
例如,与细胞因子融合的代谢调节蛋白,诸如瘦素-il2
融合蛋白
)
的外源核酸的插入
。
61.透明质酸
(ha)
是
ecm
的结构元件,并且是由重复的二糖单元组成的高分子量直链糖胺聚糖
。
它可以广泛分布在结缔组织
、
上皮组织和神经组织中,并且其表达水平可以在许多类型的肿瘤中显著升高
。
透明质酸酶是催化
ha
降解的酶家族
。
迄今为止,在人类中鉴定出至少五种功能性透明质酸酶:
hyal1、hyal2、hyal3、hyal4
和
hyal5(
也称为
ph-20
或
spam1)
,其中
ph-20
是迄今为止已知的在相对中性的
ph
起作用的唯一一种
。
在本公开内容的一些情况下,将透明质酸酶与其他肿瘤靶向治疗剂
(
诸如转基因,在本文中也称为外源核酸
)
组合可以至少通过减少
ecm
并增强治疗剂在肿瘤内和肿瘤之间的转运来促进经修饰的溶瘤病毒的治疗效果
。
62.本文的一些实施方案公开了经修饰的溶瘤病毒,其可包含编码能够降解透明质酸的膜结合蛋白
(
诸如透明质酸酶
)
的外源核酸
。
应当注意,如本文所用的术语“透明质酸酶”可指催化肿瘤中
ha
的降解的任何酶或其片段,包括但不限于
ph-20
及其来自其他物种的同源物,以及其他具有类似酶功能的工程化
/
设计蛋白
。
如本文所用,透明质酸酶可指一类透明质酸降解酶
。
在一些情况下,
ph-20
包括如由
seq id no:26
描述的氨基酸序列
。
在一些情况下,透明质酸酶括如在
seq id no:28
中列出的氨基酸序列
。
在一些情况下,透明质酸酶另外包含分泌序列
。
在一些情况下,分泌序列包括
ige
来源的信号序列
。
在一些情况下,
ige
来源的信号序列包括如在
seq id no:7
中列出的氨基酸序列
。
在一些情况下,具有
ige
来源的信号序列的透明质酸酶包括在
seq id no:29
中列出的核酸序列或在
seq id no:30
中列出的氨基酸序列
。
63.重组痘苗病毒的疫苗
、
药物组合物和递送
64.本公开内容还提供了用于治疗癌症的药物或免疫原性组合物
。
另外,在一些实施方案中,本公开内容还提供了药物或免疫原性组合物,其可以包含含有如上描述的重组痘苗病毒和合适运载体的疫苗
。
疫苗可以作为药盒提供,其包含如上描述的基于重组痘苗病毒的疫苗或如上描述的基于重组痘苗病毒的疫苗的药物组合物
。
用于疫苗递送的药物组合物可以用于肠胃外或口服递送或鼻递送
。
药物组合物可以向人类施用至少一次
。
药物组合物可以向人类施用多于一次
。
65.本文还提供了用作药物或疫苗的重组痘苗病毒
、
包含重组痘苗病毒的组合物和
/
或疫苗
。
66.在一些实施方案中,包含如本文提供的包含重组痘苗病毒的疫苗的药物组合物可以以
106pfu
至
109pfu
的剂量
、
以
106pfu
至
5x 108pfu
或
107pfu
至
108pfu
的剂量向受试者施用
。
本文提供的重组痘苗病毒也可以以
106pfu、107pfu、108pfu
或
5x 108pfu
的剂量向受试者施用
。
本文提供的重组痘苗病毒可以以
107pfu、108pfu
,或
5x 108pfu
的剂量向受试者施用
。
67.本文描述的重组痘苗病毒
、
疫苗组合物或药物组合物可以以
104pfu/ml
至
109pfu/ml、105pfu/ml
至
5x10
8 pfu/ml、106pfu/ml
至
108pfu/ml、
或
107pfu/ml
至
108pfu/ml
的浓度范围在溶液中配制
。
在一些实施方案中,用于人类的疫苗接种剂量可以包括约
106pfu
至
109pfu
,包括约
106pfu、
约
107pfu
或约
108pfu
的剂量
。
在一些实施方案中,用于人类的剂量可以包括至少约
2x 107pfu、
至少约
3x 107pfu、
至少约
5x 107pfu、
至少约
1x 108pfu、
至少约
2x 108pfu
,体积为
0.1ml
至
0.5ml。
68.本文提供的药物
/
免疫原性组合物通常可以包含一种或更多种药学上可接受和
/
或批准的运载体
、
添加剂
、
抗生素
、
防腐剂
、
佐剂
、
稀释剂和
/
或稳定剂
。
这样的辅助物质可以是水
、
盐水
、
甘油
、
乙醇
、
润湿剂或乳化剂
、ph
缓冲物质等
。
合适的运载体通常是大的
、
代谢缓慢的分子,诸如蛋白
、
多糖
、
聚乳酸
、
聚乙醇酸
、
聚氨基酸
、
氨基酸共聚物
、
脂质聚集体等
。
69.可以采用同源的初免-加强方案,其中本文定义的重组痘苗病毒可以以第一剂量施用
。
可以给予本文定义的重组痘苗病毒的一次或更多次随后施用,以加强第一次施用中提供的免疫应答
。
在一些实施方案中,由重组痘苗病毒递送的一种或更多种抗原可以与第一次施用的抗原相同或相似
。
70.包含如本文提供的重组痘苗病毒的药物组合物可以以单剂量或多
(
诸如
2、3、4
个等
)
剂量向受试者施用
。
重组痘苗病毒可以在第一次
(
初免
)
施用和第二次
(
加强
)
施用中施用
。
第一剂量可以包含约
106pfu/ml
至约
109pfu/ml
重组痘苗病毒,并且第二剂量可以包含约
106pfu/ml
至约
109pfu/ml
重组痘苗病毒
。
第一和第二剂量可以包含至少
1000pfu/ml
修饰的疫苗病毒
。
71.疫苗或药物
/
免疫原性组合物的第二剂量可以在施用第一剂量后
24
小时至约3个月
(
诸如约7天至约2个月
)
施用
。
第二剂量可以是加强剂量
。
72.重组痘苗病毒或包含重组痘苗病毒的药物
/
免疫原性组合物可以腹膜内
、
全身
、
局部
、
肠胃外
、
皮下
、
静脉内
、
肌肉内或鼻内施用
。
疫苗可以与佐剂一起施用,诸如本文描述的佐剂
。
73.本公开内容的另一方面涉及一种用于影响受试者的免疫应答的方法,包括向受试者施用本文描述的重组痘苗病毒
、
包含该重组痘苗病毒的疫苗
、
或包含重组痘苗病毒的药物
/
免疫原性组合物或本文描述的疫苗组合物
。
74.免疫接种方案可以包括在单剂量疫苗
、
多剂量中用多于一种抗原一起免疫接种,以及用每个剂量中具有不同抗原的多剂量免疫接种
。
在一些实施方案中,免疫接种方案可以包括用抗原和佐剂免疫接种
。
在本发明的上下文中,佐剂可以包括细胞因子和其他免疫调节分子,诸如刺激免疫应答的
tlr(toll
样受体
)
激动剂及其衍生物
。
75.本文还提供了通过施用本文描述的重组痘苗病毒来治疗疾病
、
紊乱或状况的方法
。
在一些实施方案中,向受试者施用的本公开内容的重组痘苗病毒的量可以在约
103和
10
12
个感染性病毒颗粒或噬斑形成单位
(pfu)
之间,或在约
105pfu
和
10
10
pfu
之间,或在约
105pfu
和
108pfu
之间,或在约
108pfu
和
10
10
pfu
之间
。
在一些实施方案中,向受试者施用的本公开内容的重组痘苗病毒的量可以在约
103和
10
12
个病毒颗粒或噬斑形成单位
(pfu)
之间,或在约
105pfu
和
10
10
pfu
之间,或在约
105pfu
和
108pfu
之间,或在约
108pfu
和
10
10
pfu
之间
。
在一些实施方案中,本公开内容的重组痘苗病毒可以以可包含约
103pfu/
剂至约
104pfu/
剂
、
约
104pfu/
剂至约
105pfu/
剂
、
约
105pfu/
剂至约
106pfu/
剂
、
约
107pfu/
剂至约
108pfu/
剂
、
约
108pfu/ml、
约
7x 108pfu/ml、
约
8x 108pfu/ml、
约
9x 108pfu/ml、
约
109pfu/ml、
约
2x 109pfu/ml、
约
3x 109pfu/ml、
约
4x 109pfu/ml、
约
5x109pfu/ml、
约
6x 109pfu/ml、
约
7x 109pfu/ml、
约
8x 109pfu/ml、
约
9x 109pfu/ml、
约
10
10
pfu/ml、
约
2x 10
10
pfu/ml、
约
3x 10
10
pfu/ml、
约
4x 10
10
pfu/ml、
约
5x 10
10
pfu/ml、
约
6x 10
10
pfu/ml、
约
7x 10
10
pfu/ml、
约
8x 10
10
pfu/ml、
约
9x 10
10
pfu/ml、
约
10
10
pfu/ml、
约
2x 10
10
pfu/ml、
约
3x 10
10
pfu/ml、
约
4x 10
10
pfu/ml、
约
5x 10
10
pfu/ml、
约
6x 10
10
pfu/ml、
约
7x 10
10
pfu/ml、
约
8x 10
10
pfu/ml、
约
9x 10
10
pfu/ml、
约
10
11
pfu/ml、
约
2x 10
11
pfu/ml、
约
3x 10
11
pfu/ml、
约
4x 10
11
pfu/ml、
约
5x 10
11
pfu/ml、
约
6x 10
11
pfu/ml、
约
7x 10
11
pfu/ml、
约
8x 10
11
pfu/ml、
约
9x 10
11
pfu/ml、
或约
10
12
pfu/ml、
约
10
12
pfu/ml
至约
10
13
pfu/ml、
约
10
13
pfu/ml
至约
10
14
pfu/ml、
或约
10
14
pfu/ml
至约
10
15
pfu/ml
的剂量施用
。
在一些实施方案中,本公开内容的重组痘苗病毒可以以可包含
5x 109pfu/ml
的剂量施用
。
在一些实施方案中,本公开内容的重组痘苗病毒可以以可包含高达
5x 109pfu/ml
的剂量施用
。
80.在一些情况下,在可以通过注射施用重组痘苗病毒时,剂量可以包括约每次注射
103个病毒颗粒
、
每次注射
104个病毒颗粒
、
每次注射
105个病毒颗粒
、
每次注射
106个病毒颗粒
、
每次注射
107个病毒颗粒
、
每次注射
108个病毒颗粒
、
每次注射
109个病毒颗粒
、
每次注射
10
10
个病毒颗粒
、
每次注射
10
11
个病毒颗粒
、
每次注射
10
12
个病毒颗粒
、
每次注射
2x 10
12
个病毒颗粒
、
每次注射
10
13
个病毒颗粒
、
每次注射
10
14
个病毒颗粒
、
或每次注射
10
15
个病毒颗粒
。
在另外的情况下,在通过注射施用重组痘苗病毒时,剂量可以包括每次注射约
103个感染性病毒颗粒
、
每次注射
104个感染性病毒颗粒
、
每次注射
105个感染性病毒颗粒
、
每次注射
106个感染性病毒颗粒
、
每次注射
107个感染性病毒颗粒
、
每次注射
108个感染性病毒颗粒
、
每次注射
109个感染性病毒颗粒
、
每次注射
10
10
个感染性病毒颗粒
、
每次注射
10
11
个感染性病毒颗粒
、
每次注射
10
12
个感染性病毒颗粒
、
每次注射
2x 10
12
个感染性病毒颗粒
、
每次注射
10
13
个感染性病毒颗粒
、
每次注射
10
14
个感染性病毒颗粒
、
或每次注射
10
15
个感染性病毒颗粒
。
在另外的实施方案中,本公开内容的重组痘苗病毒可以以可以为约
103组织培养抑制剂剂量
50
%
(pfu)/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、104pfu/kg、3x 108pfu/kg、4x10
8 pfu/kg、5x10
8 pfu/kg、3x 109pfu/kg、4x 109pfu/kg、5x 109pfu/kg、3x10
10 pfu/kg、4x10
10 pfu/kg
或
4x10
10 pfu/kg
的剂量施用
。
注意,本文
10
x
可选地表示为
1ex。
在某些实施方案中,重组痘苗病毒可以以一剂或更多剂施用
。
在某些实施方案中,该病毒可以以足以诱导肿瘤中至少约
20
%的细胞
、
肿瘤中至少约
30
%的细胞
、
肿瘤中至少约
40
%的细胞
、
肿瘤中至少约
50
%的细胞
、
肿瘤中至少约
60
%的细胞
、
肿瘤中至少约
70
%的细胞
、
肿瘤中至少约
80
%的细胞或肿瘤中至少约
90
%的细胞发生溶瘤的量施用
。
81.在某些实施方案中,单剂量的重组病毒可指在1小时
、2
小时
、5
小时
、10
小时
、15
小时
、20
小时或
24
小时的时间段内向受试者或肿瘤施用的量
。
在某些实施方案中,剂量可以随时间或通过单独的注射来扩展
。
在某些实施方案中,可以向受试者施用多于一个剂量
(
例如,2个
、3
个
、4
个
、5
个
、6
个或更多个剂量
)
的痘苗病毒,例如,其中第二治疗可以在第一治疗后的
1、2、3、4、5、6、7
天或周内进行
。
在某些实施方案中,可以在
1、2、3、4、5、6、7
或更多天或周的时间段内向受试者施用多于一个剂量的修饰的溶瘤病毒
。
在某些实施方案中,如本文描述的重组痘苗病毒或药物组合物可以在约1周至约2周
、
约2周至约3周
、
约3周至约4周
、
约4周至约5周
、
约6周至约7周
、
约7周至约8周
、
约8周至约9周
、
约9周至约
10
周
、
约
10
周至约
11
周
、
约
11
周至约
12
周
、
约
12
周至约
24
周
、
约
24
周至约
48
周
、
约
48
周或约
52
周或更长的时间段内施用
。
在某些情况下,如本文描述的重组病毒或药物组合物的施用频率可以是每日一次
、
每日两次
、
每周一次
、
每三周一次
、
每四周一次
(
或每月一次
)、
每8周一次
(
或每2个月一次
)、
每
12
周一次
(
或每3个月一次
)
或每
24
周一次
(
每6个月一次
)。
在本文公开的方法的一些实施方案中,重组痘苗病毒或药物组合物可以独立地以用于第一时间段的初始剂量
、
以用于第二时间段的中间剂量和以用于第三时间段的高剂量施用
。
在一些实施方案中,初始剂量可以低于中间剂量,并且中间剂量可以低于高剂量
。
在本文公开的方法的一些实施方案中,重组痘苗病毒或药物组合物可以独立地以用于第一时间段的高剂量
、
以用于第二时间段的中间剂量和以用于第三时间段的低剂量施用
。
在一些实施方案中,初始剂量可以高于中间剂量,并且中间剂量可以高于低剂量
。
在一些实施方案中,第一
、
第二和第三时间段可以独立地为约1周至约2周
、
约2周至约3周
、
约3周至约4周
、
约4周至约5周
、
约6周至约7周
、
约7周至约8周
、
约8周至约9周
、
约9周至约
10
周
、
约
10
周至约
11
周
、
约
11
周至约
12
周
、
约
12
周至约
24
周
、
约
24
周至约
48
周
、
约
48
周或约
52
周或更长
。
在一些实施方案中,本文描述的重组溶瘤痘苗病毒可以使用初免-加强方案施用
。
82.在一些实例中,根据本文描述的任何治疗方法,可以在施用如本文描述的修饰的溶瘤痘苗病毒或包含该修饰的溶瘤痘苗病毒的药物组合物之前
、
同时和之后使受试者进食碳水化合物减少的饮食,例如,生酮饮食
。
在某些实施方案中,受试者可以进食饮食,该饮食可以包括摄入每天少于
500
克的碳水化合物
、
每天少于
450
克的碳水化合物
、
每天少于
450
克的碳水化合物
、
每天少于
400
克的碳水化合物
、
每天少于
350
克的碳水化合物
、
每天少于
300
克的碳水化合物
、
每天少于
250
克的碳水化合物
、
每天少于
200
克的碳水化合物
、
每天少于
150
克的碳水化合物
、
每天少于
100
克的碳水化合物
、
每天少于
90
克的碳水化合物
、
每天少于
80
克的碳水化合物
、
每天少于
70
克的碳水化合物
、
每天少于
60
克的碳水化合物
、
每天少于
50
克的碳水化合物
、
每天少于
40
克的碳水化合物
、
每天少于
30
克的碳水化合物
、
每天少于
20
克的碳水化合物
、
或每天少于
10
克的碳水化合物
。
83.用于将本公开内容的重组痘苗病毒或包含该重组痘苗病毒的药物组合物递送至癌细胞或肿瘤细胞的示例性方法可以是经由瘤内注射
。
然而,也可以使用替代的施用方法,例如,静脉内
、
经由输注
、
肠胃外
、
静脉内
、
皮内
、
肌肉内
、
透皮
、
直肠
、
尿道内
、
阴道内
、
鼻内
、
鞘内或腹膜内
。
施用途径可随肿瘤的位置和性质而不同
。
在某些实施方案中,施用途径可以是牙内
、
透皮
、
肠胃外
、
静脉内
、
肌肉内
、
鼻内
、
皮下
、
局部
(regional)(
例如,在肿瘤附近,特别是肿瘤的血管或邻近血管
)、
经皮
(percutaneous)、
鞘内
、
气管内
、
腹膜内
、
动脉内
、
膀胱内
、
瘤内
、
吸入
、
灌注
、
通过灌洗或口服
。
可注射剂量的重组痘苗病毒可以作为团注或缓慢输注施用
。
在某些实施方案中,修饰的溶瘤痘苗病毒可以从植入患者内的源向患者施用
。
在某些实施方案中,修饰的溶瘤痘苗病毒的施用可以通过在选定时间段内连续输注来进行
。
在一些情况下,如本文描述的重组痘苗病毒或包含该重组痘苗病毒的药物组合物可以通过在约
15
分钟
、
约
30
分钟
、
约
45
分钟
、
约
50
分钟
、
约
55
分钟
、
约
60
分钟
、
约
75
分钟
、
约
90
分钟
、
约
100
分钟或约
120
分钟或更长的时间段内输注而以治疗有效剂量施用
。
本公开内容的重组痘苗病毒或药物组合物可以作为液体剂量施用,其中施用的总体积为约
1ml
至约
5ml、
约
5ml
至
10ml、
约
15ml
至约
20ml、
约
25ml
至约
30ml、
约
30ml
至约
50ml、
约
50ml
至约
100ml、
约
100ml
至
150ml、
约
150ml
至约
200ml、
约
200ml
至约
250ml、
约
250ml
至约
300ml、
约
300ml
至约
350ml、
约
350ml
至约
400ml、
约
400ml
至约
450ml、
约
450ml
至
500ml、
约
500ml
至
750ml、
或约
750ml
至
1000ml。
84.使用重组溶瘤病毒的方法
85.如上描述,本文描述的重组溶瘤病毒或包含其的药物组合物或疫苗可用于癌症
、
癌症免疫疗法和肿瘤治疗
。
肿瘤可以是实体瘤和液体瘤,包括但不限于黑素瘤
、
肝细胞癌
、
乳腺癌
、
肺癌
、
非小细胞肺癌
、
腹膜癌
、
前列腺癌
、
膀胱癌
、
卵巢癌
、
白血病
、
淋巴瘤
、
肾细胞癌
、
胰腺癌
、
上皮癌
、
胃
/ge
结合部腺癌
、
宫颈癌
、
结肠癌
、
结肠直肠癌
、
十二指肠癌
、
胰腺腺癌
、
腺样囊性癌
、
肉瘤
、
间皮瘤
、
多形性胶质母细胞瘤
、
星形细胞瘤
、
多发性骨髓瘤
、
前列腺上皮癌
、
肝细胞癌
、
胆管癌
、
胰腺腺癌
、
头颈部鳞状细胞癌
、
宫颈鳞状细胞癌
、
骨肉瘤
、
上皮性卵巢癌
、
急性淋巴母细胞淋巴瘤或骨髓增生性肿瘤
。
因此,本公开内容的一些实施方案提供了通过施用如本文描述的重组溶瘤病毒或包含其的药物或免疫原性组合物进行的癌症
、
肿瘤治疗方法,癌症免疫疗法
。
86.如上描述,本文描述的重组痘苗病毒或包含其的药物组合物或疫苗可用于癌症治疗
、
癌症免疫疗法和肿瘤治疗
。
肿瘤可以是实体瘤和液体瘤,包括但不限于黑素瘤
、
肝细胞癌
、
乳腺癌
、
肺癌
、
非小细胞肺癌
、
腹膜癌
、
前列腺癌
、
膀胱癌
、
卵巢癌
、
白血病
、
淋巴瘤
、
肾细胞癌
、
胰腺癌
、
上皮癌
、
胃
/ge
结合部腺癌
、
宫颈癌
、
结肠癌
、
结肠直肠癌
、
十二指肠癌
、
胰腺腺癌
、
腺样囊性癌
、
肉瘤
、
间皮瘤
、
多形性胶质母细胞瘤
、
星形细胞瘤
、
多发性骨髓瘤
、
前列腺上皮癌
、
肝细胞癌
、
胆管癌
、
胰腺腺癌
、
头颈部鳞状细胞癌
、
宫颈鳞状细胞癌
、
骨肉瘤
、
上皮性卵巢癌
、
急性淋巴母细胞淋巴瘤或骨髓增生性肿瘤
。
因此,本公开内容的一些实施方案提供了通过施用如本文描述的重组痘苗病毒或包含其的药物或免疫原性组合物进行的癌症
、
肿瘤治疗方法,癌症免疫疗法
。
87.可以通过本公开内容的方法治疗的癌细胞包括来自以下的细胞:膀胱
、
血液
、
骨
、
骨髓
、
脑
、
乳腺
、
结肠
、
食管
、
胃肠
、
牙龈
、
头
、
肾
、
肝
、
肺
、
鼻咽
、
颈
、
卵巢
、
前列腺
、
皮肤
、
胃
、
睾丸
、
舌或子宫
。
另外,癌症可以具体地属于以下组织学类型,但不限于这些组织学类型:恶性赘生物;癌;未分化癌;巨细胞癌和梭形细胞癌;小细胞癌;乳头状癌;鳞状细胞癌;淋巴上皮癌;基底细胞癌;毛基质癌;移行细胞癌;乳头状移行细胞癌;腺癌;恶性胃泌素瘤;胆管癌;肝细胞癌;混合型肝细胞癌和胆管癌;小梁腺癌;腺样囊性癌;腺瘤性息肉中的腺癌;家族性结肠息肉腺癌;实体癌;恶性类癌瘤;细支气管肺泡腺癌;乳头状腺癌;嫌色细胞癌;嗜酸性细胞癌;嗜酸性腺癌;嗜碱性细胞癌;透明细胞腺癌;颗粒细胞癌;滤泡性腺癌;乳头状和滤泡性腺癌;非包膜性硬化癌
(nonencapsulating sclerosing carcinoma)
;肾上腺皮质癌;子宫内膜样癌;皮肤附件癌;大汗腺腺癌;皮脂腺癌;盯聍腺癌;黏液表皮样癌;囊腺癌;乳头状囊腺癌;乳头状浆液性囊腺癌;黏液性囊腺癌;黏液腺癌;印戒细胞癌;浸润性导管癌;髓样癌;小叶癌;炎性癌;乳腺佩吉特病
(paget’s disease)
;腺泡细胞癌;腺鳞癌;腺癌伴鳞状化生;恶性胸腺瘤;恶性卵巢间质瘤;恶性泡膜细胞瘤;恶性粒层细胞瘤;恶性男性母细胞瘤
(androblastoma)
;支持细胞癌
(sertoli cell carcinoma)
;恶性莱迪希细胞瘤;恶性脂质细胞瘤;恶性副神经节瘤;恶性乳腺外副神经节瘤;嗜铬细胞瘤;血管球肉瘤;恶性黑素瘤;无黑色素性黑素瘤;浅表扩散性黑素瘤;巨大色素痣内恶性黑素瘤;上皮样细胞黑素瘤;恶性蓝痣;肉瘤;纤维肉瘤;恶性纤维组织细胞瘤;黏液肉瘤;脂肪肉瘤;平滑肌肉瘤;横纹肌肉
瘤;胚胎性横纹肌肉瘤;肺泡横纹肌肉瘤;间质肉瘤;恶性混合瘤;苗勒混合瘤
(mullerian mixed tumor)
;肾母细胞瘤;肝母细胞瘤;癌肉瘤;恶性间叶瘤;恶性布伦纳瘤
(brenner tumor)
;恶性叶状瘤;滑膜肉瘤;恶性间皮瘤;无性细胞瘤;胚胎性癌;恶性畸胎瘤;恶性卵巢甲状腺肿;绒毛膜癌;恶性中肾瘤;血管肉瘤;恶性血管内皮瘤;卡波西肉瘤;恶性血管外皮细胞瘤;淋巴管肉瘤;骨肉瘤;近皮质骨肉瘤;软骨肉瘤;恶性软骨母细胞瘤;间叶性软骨肉瘤;骨巨细胞瘤;尤因肉瘤;恶性牙源性肿瘤;成釉细胞牙肉瘤;恶性成釉细胞瘤;成釉细胞纤维肉瘤;恶性松果体瘤;脊索瘤;恶性神经胶质瘤;室管膜瘤;星形细胞瘤;原浆性星形细胞瘤;纤维性星形细胞瘤;星形母细胞瘤;胶质母细胞瘤;少突神经胶质瘤;少突神经胶质母细胞瘤;原始神经外胚层瘤;小脑肉瘤;成神经节细胞瘤;神经母细胞瘤;视网膜母细胞瘤;嗅神经源性肿瘤;恶性脑膜瘤;神经纤维肉瘤;恶性神经鞘瘤;恶性颗粒细胞瘤;恶性淋巴瘤;霍奇金病;霍奇金症
(hodgkin's)
;副肉芽肿;恶性小淋巴细胞性淋巴瘤;恶性弥漫性大细胞淋巴瘤;恶性滤泡性淋巴瘤;蕈样肉芽肿病;其他特定的非霍奇金淋巴瘤;恶性组织细胞增生症;多发性骨髓瘤;肥大细胞肉瘤;免疫增生性小肠病;白血病;淋巴样白血病;浆细胞白血病;红白血病;淋巴肉瘤细胞性白血病;髓样白血病;嗜碱性粒细胞白血病;嗜酸性粒细胞白血病;单核细胞白血病;肥大细胞白血病;巨核母细胞性白血病;髓样肉瘤;以及多毛细胞白血病
。
在一些情况下,可以使用本公开内容的重组溶瘤病毒,诸如有利于全身递送的重组溶瘤痘苗病毒,来治疗转移性实体癌
。
在一些情况下,可以使用本公开内容的重组溶瘤病毒,诸如有利于全身递送的重组溶瘤病毒,来治疗诸如对于瘤内递送治疗剂的目的无法接近或难以接近的实体癌
。
在一些实例中,可以使用本公开内容的重组溶瘤病毒,诸如有利于全身递送并形成增加量的
eev
的重组溶瘤痘苗病毒,来治疗与游离脂肪酸表达增加相关的癌症
。
88.组合疗法
89.在一些方面,本公开内容的方法包括将本文公开的重组溶瘤病毒或包含该重组溶瘤病毒的药物或免疫原性组合物在一种或更多种另外的疗法之前
、
之后或与其组合地施用
。
所述另外的疗法的实例可包括但不限于化学疗法
、
放射疗法
、
采用另外的病毒的溶瘤病毒疗法
、
采用免疫调节蛋白的治疗
、
抗癌剂或其任何组合
。
相对于修饰的病毒诸如溶瘤痘苗病毒的施用,另外的疗法可以同时或相继地施用
。
在某些实施方案中,本公开内容的方法可包括在一种或更多种抗癌剂或癌症疗法之前
、
之后或与其组合地施用如本文公开的修饰的溶瘤病毒
。
抗癌剂可包括但不限于化疗剂
、
放疗剂
、
细胞因子
、
免疫检查点抑制剂
、
抗血管生成剂
、
凋亡诱导剂
、
抗癌抗体和
/
或抗细胞周期蛋白依赖性激酶剂
。
在某些实施方案中,癌症疗法可包括化学疗法
、
生物疗法
、
放射疗法
、
免疫疗法
、
激素疗法
、
抗血管疗法
、
冷冻疗法
、
毒素疗法和
/
或手术或其组合
。
在某些实施方案中,本公开内容的方法可包括在本公开内容的修饰的溶瘤病毒之前
、
之后或与其组合地施用本文公开的重组病毒
。
90.在某些实施方案中,使用重组溶瘤病毒的治疗可以单独使用或与一种或更多种免疫调节剂组合使用
。
免疫调节剂可包括能够抑制与肿瘤或癌症相关的抗病毒免疫的任何化合物
、
分子或物质
。
在某些实施方案中,免疫调节剂可以能够抑制对修饰的病毒的先天免疫或适应性免疫
。
免疫调节剂的非限制性实例包括抗
cd33
抗体或其可变区
、
抗
cd11b
抗体或其可变区
、cox2
抑制剂例如塞来昔布
、
细胞因子诸如
il-12、gm-csf、il-2(
具有
seq id no:33
或
34
中列出的氨基酸序列
)、ifn3
和
ifn-g
以及趋化因子诸如
mip-1、mcp-1
和
il-8。
在某些实
施方案中,免疫调节剂可包括免疫检查点调节剂,例如但不限于抗
ctla4、
抗
pd-1
和抗
pd-l1
和
tlr
激动剂
(
例如,聚
i:c)。
在一些实例中,免疫调节剂可包括免疫检查点抑制剂,如
pd-1
的拮抗剂
(
例如,与
pd-1
结合的拮抗剂抗体
)、pd-l1
的拮抗剂
(
例如,与
pd-l1
结合的拮抗剂抗体
)、ctla-4
的拮抗剂
(
例如,与
ctla-4
结合的拮抗剂抗体
)、a2ar
的拮抗剂
(
例如,与
a2ar
结合的拮抗剂抗体
)、b7-h3
的拮抗剂
(
例如,与
b7-h3
结合的拮抗剂抗体
)、b7-h4
的拮抗剂
(
例如,与
b7-h4
结合的拮抗剂抗体
)、btla
的拮抗剂
(
例如,与
btla
结合的拮抗剂抗体
)、ido
的拮抗剂
(
例如,与
ido
结合的拮抗剂抗体
)、kir
的拮抗剂
(
例如,与
kir
结合的拮抗剂抗体
)、lag3
的拮抗剂
(
例如,与
lag3
结合的拮抗剂抗体
)、tim-3
的拮抗剂
(
例如,与
tim3
结合的拮抗剂抗体
)。
在一些实施方案中,所述另外的疗法可包括施用免疫检查点调节剂
。
在一个实例中,免疫检查点调节剂可以是
tgn1412。
在一个实例中,免疫检查点调节剂可以是
nktr-214。
在一个实例中,免疫检查点调节剂可以是
medi0562。
在一个实例中,免疫检查点调节剂可以是
medi6469。
在一个实例中,免疫检查点调节剂可以是
medi6383。
在一个实例中,免疫检查点调节剂可以是
jtx-2011。
在一个实例中,免疫检查点调节剂可以是
keytruda(
帕博利珠单抗
)。
在一个实例中,免疫检查点调节剂可以是
opdivo(
纳武利尤单抗
)。
在一个实例中,免疫检查点调节剂可以是易普利姆玛
(ipilimumab)。
在一个实例中,免疫检查点调节剂可以是曲美木单抗
(tremelimumab)。
在一个实例中,免疫检查点调节剂可以是
tecentriq(
阿特珠单抗
)。
在一个实例中,免疫检查点调节剂可以是
mga271。
在一个实例中,免疫检查点调节剂可以是
indoximod。
在一个实例中,免疫检查点调节剂可以是
epacadostat。
在一个实例中,免疫检查点调节剂可以是利瑞鲁单抗
(lirilumab)。
在一个实例中,免疫检查点调节剂可以是
bms-986016。
在一个实例中,免疫检查点调节剂可以是
mpdl3280a。
在一个实例中,免疫检查点调节剂可以是阿维鲁单抗
(avelumab)。
在一个实例中,免疫检查点调节剂可以是德瓦鲁单抗
(durvalumab)。
在一个实例中,免疫检查点调节剂可以是
medi4736。
在一个实例中,免疫检查点调节剂可以是
medi4737。
在一个实例中,免疫检查点调节剂可以是
trx518。
在一个实例中,免疫检查点调节剂可以是
mk-4166。
在一个实例中,免疫检查点调节剂可以是乌瑞卢单抗
(urelumab)(bms-663513)。
在一个实例中,免疫检查点调节剂可以是
pf-05082566(pf-2566)。
91.在某些实例中,在所述另外的疗法是放射的情况下,示例性的剂量可以是
5,000rad(50gy)
至
100,000rad(1000gy)
,或
50,000rad(500gy)
,或所述范围内的其他合适的剂量
。
可选地,放射剂量可以是约
30
至
60gy、
约
40
至约
50gy、
约
40
至
48gy
或约
44gy
,或所述范围内的其他合适的剂量,其中该剂量例如通过如上描述的剂量学研究来确定
。
如本文所用的“gy”可指等于
100rad
的放射的特定吸收剂量的单位
。gy
是“戈瑞
(gray)”的缩写
。
92.在某些实例中,在所述另外的疗法是化学疗法的情况下,示例性化疗剂可以包括但不限于烷化剂
(
例如,氮芥衍生物
、
乙烯亚胺
、
烷基磺酸盐
、
肼和三嗪
、
亚硝基脲
(nitrosureas)
和金属盐
)、
植物生物碱
(
例如,长春花生物碱
、
紫杉烷类
、
鬼臼毒素和喜树碱类似物
)、
抗肿瘤抗生素
(
例如,蒽环类
、
色霉素类等
)、
抗代谢物
(
例如,叶酸拮抗剂
、
嘧啶拮抗剂
、
嘌呤拮抗剂和腺苷脱氨酶抑制剂
)、
拓扑异构酶i抑制剂
、
拓扑异构酶
ii
抑制剂和其他抗赘生物剂
(miscellaneous antineoplastics)(
例如,核糖核苷酸还原酶抑制剂
、
肾上腺皮质类固醇抑制剂
、
酶
、
抗微管剂和类视黄醇
)。
示例性化疗剂可以包括但不限于阿那曲唑
、
比卡鲁胺
、
硫酸博莱霉素
、
白消安
、
白消安注射液
、
卡培他滨
、n4-戊氧基羰基-5-脱氧-5-氟
胞苷
、
卡铂
、
卡莫司汀
、
苯丁酸氮芥
、
顺铂
、
克拉屈滨
、
环磷酰胺
、
阿糖胞苷
(cytarabine)、
阿糖胞苷
(cytosine arabinoside)、
阿糖胞苷脂质体注射液
、
达卡巴嗪
、
更生霉素
、
盐酸柔红霉素
、
柠檬酸柔红霉素脂质体注射液
、
地塞米松
、
多西他赛
、
盐酸多柔比星
、
依托泊苷
、
磷酸氟达拉滨
、5-氟尿嘧啶
、
氟他胺
、tezacitibine、
吉西他滨
(
二氟脱氧胞苷
)、
羟基脲
、
伊达比星
、
异环磷酰胺
、
伊立替康
、l-天冬酰胺酶
、
亚叶酸钙
、
美法仑
、6-巯基嘌呤
、
甲氨蝶呤
、
米托蒽醌
、
麦罗塔
(mylotarg)、
紫杉醇
、phoenix、
喷司他丁
、
具有卡莫司汀植入物的聚苯丙生
20、
柠檬酸他莫昔芬
、
替尼泊苷
、6-硫代鸟嘌呤
、
塞替派
、
替拉扎明
、
注射用盐酸拓扑替康
、
长春碱
、
长春新碱
、
长春瑞滨
、
依布替尼
、idelalisib
和维布妥昔单抗
。
93.示例性烷化剂可以包括但不限于氮芥
、
乙烯亚胺衍生物
、
烷基磺酸盐
、
亚硝基脲和三氮烯,诸如:尿嘧啶氮芥
、
甲川氯
、
环磷酰胺
、
异环磷酰胺
、
美法仑
、
苯丁酸氮芥
、
哌泊溴烷
、
三亚乙基蜜胺
、
三亚乙基硫代磷酰胺
、
替莫唑胺
、
塞替派
、
白消安和达卡巴嗪
。
另外的示例性烷化剂包括但不限于奥沙利铂
、
替莫唑胺
、
更生霉素
、l-pam、l-沙可来新
(l-sarcolysin)、
六甲基三聚氰胺
、
卡莫司汀
、
苯达莫司汀
、
白消安;卡铂
、
洛莫司汀
、
顺铂
、
苯丁酸氮芥
、
环磷酰胺
、
达卡巴嗪
、
六甲蜜胺
、
异环磷酰胺
、
泼尼莫司汀
(prednimustine)、
丙卡巴肼
、
二氯甲基二乙胺
、
链脲佐菌素
、
塞替派
、
环磷酰胺和苯达莫司汀
hcl。
94.示例性蒽环类可以包括但不限于例如多柔比星
、
博莱霉素
、
柔红霉素
、
道诺霉素
、
盐酸红比霉素
、
米托蒽醌
、
表柔比星
、
伊达比星
、
丝裂霉素
c、
格尔德霉素
、
除莠霉素
、
近灰霉素
(ravidomycin)
和去乙酰基近灰霉素
。
95.示例性长春花生物碱可以包括但不限于酒石酸长春瑞滨
、
长春新碱
、
长春地辛
、
长春碱和长春瑞滨
。
96.示例性蛋白酶体抑制剂可以包括但不限于硼替佐米;卡非佐米
(carfilzomib)(px-171-007、(s)-4-甲基-n-((s)-1-(((s)-4-甲基-1-((r)-2-甲基环氧乙烷-2-基
)-1-氧代戊烷-2-基
)
氨基
)-1-氧代-3-苯基丙烷-2-基
)-2-((s)-2-(2-吗啉代乙酰氨基
)-4-苯基丁酰氨基
)-戊酰胺
)
,
marizomib(npi-0052)
,柠檬酸伊沙佐米
(ixazomib citrate)
,
delanzomib
,和
o-甲基-n-[(2-甲基-5-噻唑基
)
羰基
]-l-丝氨酸-o-甲基-n-[(1s)-2-[(2r)-2-甲基-2-环氧乙烷基
]-2-氧代-1-(
苯基甲基
)
乙基
]-l-丝氨酰胺
。
[0097]
如本文所用的,“与
......
组合”可以意指将重组病毒,诸如如本文描述的溶瘤痘苗病毒或包含该溶瘤痘苗病毒的药物组合物,与另外的疗法如包含一种或更多种剂的另外的疗法作为治疗方案或计划的一部分施用于受试者
。
在某些实施方案中,组合使用可以不要求在施用前将重组病毒与一种或更多种剂物理合并,也不要求其在同一时间范围内施用
。
例如,非限制性地,重组病毒和一种或更多种剂可以同时施用于所治疗的受试者,或者可以同一时间施用或以任何顺序或在不同的时间点相继地施用
。
[0098]
在各种实施方案中,另外的疗法可以以液体剂型
、
固体剂型
、
栓剂
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
在某些实施方案中,另外的疗法经约1周至约2周
、
约2周至约3周
、
约3周至约4周
、
约4周至约5周
、
约6周至约7周
、
约7周至约8周
、
约8周至约9周
、
约9周至约
10
周
、
约
10
周至约
11
周,约
11
周至约
12
周
、
约
12
周至约
24
周
、
约
24
周至约
48
周
、
约
48
周或约
52
周或更长的时间段施用
。
在某些情况下,所述另外的疗法的施用频率可以是每日一次
、
每日两次
、
每周一次
、
每三周一次
、
每四周一次
(
或每月一次
)、
每8周一次
(
或每2个月一次
)、
每
12
周一次
(
或每3个月一
次
)
或每
24
周一次
(
每6个月一次
)。
在某些实施方案中,治疗患有癌症的受试者的方法可包括向该受试者施用有效量的本公开内容的重组痘苗病毒,例如修饰的重组病毒
。
在某些实施方案中,本公开内容的方法还可包括向受试者施用有效量的一种或更多种剂
。
例如,非限制性地,该剂可以是如上所述的抗癌剂
、
免疫调节剂或其任何组合
。
如本文所用的,“抗癌剂”可以是具有抗癌作用的任何分子
、
化合物
、
化学物质或组合物
。
抗癌剂包括但不限于化疗剂
、
放疗剂
、
细胞因子
、
免疫检查点抑制剂
、
抗血管生成剂
、
凋亡诱导剂
、
抗癌抗体和
/
或抗细胞周期蛋白依赖性激酶剂
。
[0099]
另外的实施方案
[0100]
本文提供了重组溶瘤病毒,其包含病毒基因组中的修饰,其中所述修饰包括以下至少一种:编码
mhc ii
类抑制剂的内源核酸的缺失或功能性缺失;导致
mhc ii
类呈递的激活或增强的激活的外源核酸的插入;以及编码完全或主要在被感染的细胞内起作用的
mhc i
类抑制剂的外源核酸的插入
。
本文还提供了重组溶瘤病毒,其包含编码
mhc ii
类抑制剂的内源核酸的缺失或功能性缺失,其中所述缺失或功能性缺失导致
mhc ii
类呈递的增加,并且其中溶瘤病毒是痘苗病毒
。
本文还提供了重组溶瘤病毒,其包含编码
mhc ii
类抑制剂的内源核酸的缺失或功能性缺失,其中编码
mhc ii
类抑制剂的内源核酸的缺失或功能性缺失包括编码痘苗病毒的蛋白
a35
的基因的缺失
。
本文还提供了重组溶瘤病毒,其中编码痘苗病毒蛋白
a35
的基因的缺失或功能性缺失是基因
wr158
的缺失或功能性缺失
。
本文还提供了重组溶瘤病毒,其中修饰包括导致
mhc ii
类呈递的激活或增强的激活的外源核酸的插入,并且其中外源核酸编码:凋亡抑制剂蛋白或坏死性细胞死亡激活剂蛋白;自噬增强剂蛋白;天冬酰胺内肽酶;
ii
类反式激活因子;干扰素-γ
;
toll
样受体激活剂;或树突状细胞成熟激活剂
。
本文还提供了包含自噬增强剂蛋白的重组溶瘤病毒,其中自噬增强剂蛋白是
hmgb1
或其功能性结构域或变体
。
本文还提供了包含树突状细胞成熟激活剂的重组溶瘤病毒,其中树突状细胞成熟激活剂包括骨桥蛋白或
tnf-α
或其功能性片段或变体
。
本文还提供了重组溶瘤病毒,其中编码的
mhc ii
上调蛋白与分泌序列
、
细胞透化结构域或其组合融合,以实现整个肿瘤的
mhc ii
上调
。
本文还提供了重组溶瘤病毒,其中修饰包括编码
mhc i
类抑制剂的外源核酸的插入,并且其中该插入导致
mhc i
类呈递的抑制或部分抑制
。
本文还提供了重组溶瘤病毒,其中编码
mhc i
类抑制剂的外源核酸的插入包括编码一种或更多种牛痘病毒蛋白的基因的插入
。
本文还提供了重组溶瘤病毒,其中编码
mhc i
类抑制剂的外源核酸的插入包括编码牛痘蛋白
cpxv012
或其功能性片段或变体的基因的插入
。
本文还提供了重组溶瘤病毒,其中编码
mhc i
类抑制剂的外源核酸的插入包括编码牛痘蛋白
cpxv203
或其功能性片段或变体的基因的插入
。
本文还提供了重组溶瘤病毒,其中编码
mhc i
类抑制剂的外源核酸的插入包括编码以下至少一种的基因的插入:
eb
病毒编码的核抗原1蛋白;单纯疱疹病毒编码的
icp47
蛋白;单纯疱疹病毒编码的
ul49.5
蛋白;巨细胞病毒编码的
us6、us2、us3、us11
或
gp48
蛋白;
eb
病毒编码的
bnlf2a
蛋白;腺病毒编码的
e3-19k
蛋白;人类免疫缺陷病毒或猿免疫缺陷病毒编码的
nef
蛋白;卡波西肉瘤相关疱疹病毒编码的
kk3、virf3
或
kk5
蛋白;或者
irf7
或
irf3
的显性负性形式
。
本文还提供了重组溶瘤病毒,其中
mhc i
类抑制剂包括
tap
抑制剂
。
本文还提供了重组溶瘤病毒,其中
tap
抑制剂完全或主要在被感染的细胞内起作用
。
本文还提供了重组溶瘤病毒,其中病毒基因组中的修饰降低靶向病毒感染的肿瘤细胞的免疫应答,并增加靶向病毒感染的肿瘤细胞周围细胞的免疫应答
。
本文还提供了重组溶瘤病
毒,其中胸苷激酶基因被从病毒基因组中缺失
。
本文还提供了重组溶瘤病毒,其还包含编码透明质酸酶的外源核酸
。
本文还提供了重组溶瘤病毒,其中透明质酸酶为
ph-20
或
hysa。
本文还提供了重组溶瘤病毒,其中溶瘤病毒是痘苗病毒,并且痘苗病毒是
western reserve
毒株痘苗病毒
(atcc vr-1354)、copenhagen
毒株
、ihd
毒株
、wyeth
毒株
(atcc vr-325)、nycboh
毒株
、tian tan
毒株
、lister
毒株
、ankara
毒株
(atcc vr-1508
或
attc vr1566)、ussr
毒株或
acam2000
毒株
。
[0101]
本文提供了重组溶瘤病毒,其包含病毒基因组中的修饰,其中该修饰包括编码
a35
蛋白的痘苗病毒基因的缺失或功能性缺失,以及编码牛痘蛋白
cpxv012
或牛痘蛋白
cpxv203
的外源基因的插入
。
本文还提供了重组溶瘤病毒,其中该修饰使得编码牛痘蛋白
cpxv012
的外源基因的插入位于编码痘苗病毒
a35
蛋白的基因座
。
本文还提供了重组溶瘤病毒,其中修饰使得编码牛痘蛋白
cpxv203
的外源基因的插入位于编码痘苗病毒
a35
蛋白的基因座
。
本文还提供了重组溶瘤病毒,其还包含病毒基因组中的另外的修饰
。
本文还提供了重组溶瘤病毒,其中另外的修饰包括以下至少一种:编码趋化因子受体或其功能性结构域或变体的外源核酸的插入;或编码细胞因子或其功能性结构域或变体的外源核酸的插入
。
本文还提供了重组溶瘤病毒,其包含编码细胞因子或其功能性结构域或变体的外源核酸,其中细胞因子包括以下至少一种:白细胞介素-2(il-2)、
白细胞介素-15/
白细胞介素-15ra(il15/il15ra)、
白细胞介素-7(il-7)
或其功能性结构域或变体
。
本文还提供了重组溶瘤病毒,其中另外的修饰包括编码包含细胞因子和代谢调节剂蛋白的融合蛋白的外源核酸的插入
。
本文还提供了重组溶瘤病毒,包含编码趋化因子受体或其功能性结构域或变体的外源核酸,其中趋化因子受体包括以下至少一种:
cxcr4、ccr2
或其功能性结构域或变体
。
本文还提供了重组溶瘤病毒,其中趋化因子受体包括
cxcr4
或其功能性结构域或变体
。
本文还提供了重组溶瘤病毒,其中趋化因子受体包括
ccr2
或其功能性结构域或变体,其中
ccr2
包括野生型
ccr2
或突变的
ccr2。
本文还提供了重组溶瘤病毒,其中编码趋化因子受体或其功能性结构域或变体的外源核酸包含密码子优化的序列
。
本文还提供了重组溶瘤病毒,其中编码趋化因子受体或其功能性结构域或变体的外源核酸包含非密码子优化的序列
。
本文还提供了重组溶瘤病毒,其中另外的修饰包括病毒基因的突变或完全缺失或部分缺失,所述病毒基因包括以下至少一种:痘苗病毒的
a52r、b15r、k7r、a46r、n1l、e3l、k1l、m2l、c16、n2r、b8r、b18r、vh1
或其功能性结构域或片段或变体,或其任何组合
。
本文还提供了重组溶瘤病毒,其中胸苷激酶基因被从病毒基因组中缺失
。
本文还提供了重组溶瘤病毒,其还包含编码透明质酸酶的外源核酸
。
本文还提供了重组溶瘤病毒,其中透明质酸酶为
ph-20
或
hysa。
本文还提供了重组溶瘤病毒,其中溶瘤病毒是痘苗病毒,并且痘苗病毒是
western reserve
毒株痘苗病毒
(atcc vr-1354)、copenhagen
毒株
、ihd
毒株
、wyeth
毒株
(atcc vr-325)、nycboh
毒株
、tian tan
毒株
、lister
毒株
、ankara
毒株
(atcc vr-1508
或
attc vr1566)、ussr
毒株或
acam2000
毒株
。
[0102]
本文提供了包含根据本文描述的任何实施方案的重组溶瘤病毒的免疫原性组合物
。
[0103]
本文提供了包含根据本文描述的任何实施方案的重组溶瘤病毒或免疫原性组合物以及增溶剂
、
赋形剂或药学上可接受的运载体中的至少一种的药物组合物
。
本文还提供了药物组合物,其中赋形剂包括以下一种或更多种:缓冲剂
、
稳定剂
、
抗氧化剂
、
黏合剂
、
稀
释剂
、
分散剂
、
速率控制剂
、
润滑剂
、
助流剂
、
崩解剂
、
增塑剂
、
防腐剂或其任何组合
。
本文还提供了药物组合物,其中赋形剂包括磷酸氢二钠二水合物
、
磷酸二氢钠二水合物
、
氯化钠
、
肌醇
、
山梨醇或其任何组合
。
本文还提供了药物组合物,其中药物组合物不包含防腐剂
。
本文还提供了药物组合物,其还包含防腐剂
、
稀释剂和运载体中的一种或更多种
。
本文还提供了药物组合物,其还包含另外的活性成分或其盐
。
本文还提供了药物组合物,其中增溶剂是无菌水
。
本文还提供了药物组合物,其还包含另外的活性成分,其中另外的活性成分是抗癌剂或另外的溶瘤病毒
。
[0104]
本文提供了减少癌细胞生长的方法,示例性方法包括向癌细胞施用有效量的根据本文描述的任何实施方案的重组溶瘤病毒
、
免疫原性组合物或药物组合物
。
[0105]
本文提供了使肿瘤生长消退的方法,示例性方法包括向肿瘤施用有效量的根据本文描述的任何实施方案的重组溶瘤病毒
、
免疫原性组合物或药物组合物
。
本文还提供了方法,其中肿瘤位于受试者体内,并且施用包括向受试者施用
。
本文还提供了方法,包括施用另外的疗法,其中另外的疗法包括化学疗法
、
放疗
、
用另外的病毒进行的溶瘤病毒疗法
、
用免疫调节蛋白治疗
、car t
细胞疗法
、
抗癌剂或其任何组合
。
本文还提供了方法,其中另外的疗法包括施用免疫调节剂,免疫调节剂包括抗
cd33
抗体及其可变区
、
抗
cd11b
抗体及其可变区
、cox2
抑制剂
、
细胞因子
、
趋化因子
、
抗
ctla4
抗体或其抗原结合片段
、
抗
pd-1
抗体或其抗原结合片段
、
抗
pd-l1
抗体或其抗原结合片段或
tlr
激动剂
。
[0106]
一种治疗方法,包括向有相应需要的受试者施用有效量的根据本文描述的任何实施方案的重组溶瘤病毒
、
免疫原性组合物或药物组合物
。
本文还提供了方法,其中施用包括瘤内施用
。
本文还提供了方法,其中施用包括全身施用
。
本文还提供了方法,其中全身施用包括以下至少一种:腹膜内施用
、
口服施用
、
静脉内施用
、
鼻内施用
、
舌下施用
、
直肠施用
、
透皮施用或其任何组合
。
本文还提供了方法,其中受试者患有癌症,并且其中癌症是以下至少一种:黑素瘤
、
肝细胞癌
、
乳腺癌
、
肺癌
、
非小细胞肺癌
、
腹膜癌
、
前列腺癌
、
膀胱癌
、
卵巢癌
、
白血病
、
淋巴瘤
、
肾细胞癌
、
胰腺癌
、
上皮癌
、
胃
/ge
结合部腺癌
、
宫颈癌
、
结肠癌
、
结肠直肠癌
、
十二指肠癌
、
胰腺腺癌
、
腺样囊性癌
、
肉瘤
、
间皮瘤
、
多形性胶质母细胞瘤
、
星形细胞瘤
、
多发性骨髓瘤
、
前列腺上皮癌
、
肝细胞癌
、
胆管癌
、
头颈部鳞状细胞癌
、
宫颈鳞状细胞癌
、
骨肉瘤
、
上皮性卵巢癌
、
急性淋巴母细胞淋巴瘤
、
骨髓增生性肿瘤或其任何组合
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物以包含约
106pfu/ml
至约
10
10
pfu/ml
重组痘苗病毒的剂量施用
。
本文还提供了方法,其中重组溶瘤病毒或药物组合物以包含约
3x 109pfu/ml
重组痘苗病毒的剂量施用
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物独立地以用于第一时间段的初始剂量
、
以用于第二时间段的中间剂量和以用于第三时间段的高剂量施用
。
本文还提供了方法,包括独立地施用初始剂量
、
中间剂量和高剂量,其中初始剂量低于中间剂量,并且中间剂量低于高剂量
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物独立地以用于第一时间段的高剂量
、
以用于第二时间段的中间剂量和以用于第三时间段的低剂量施用
。
本文还提供了方法,包括独立地施用初始剂量
、
中间剂量和低剂量,其中初始剂量高于中间剂量,并且中间剂量高于低剂量
。
本文还提供了方法,其中第一
、
第二和第三时间段分别为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周
、
约
12
周
、
约4个月
、
约5个月
、
约6个月
、
约7个月
、
约8个月
、
约9个月
、
约
10
个月
、
约
11
个月或
约1年
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物独立地包括液体剂型,该液体剂型以约
1ml
至约
5ml、
约
5ml
至
10ml、
约
15ml
至约
20ml、
约
25ml
至约
30ml、
约
30ml
至约
50ml、
约
50ml
至约
100ml、
约
100ml
至
150ml、
约
150ml
至约
200ml、
约
200ml
至约
250ml、
约
250ml
至约
300ml、
约
300ml
至约
350ml、
约
350ml
至约
400ml、
约
400ml
至约
450ml、
约
450ml
至
500ml、
约
500ml
至
750ml、
或约
750ml
至
1000ml
的体积施用
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物以液体剂型
、
固体剂型
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物的施用持续时间为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周
、
约
12
周
、
约4个月
、
约5个月
、
约6个月
、
约7个月
、
约8个月
、
约9个月
、
约
10
个月
、
约
11
个月或约1年
。
本文还提供了方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物每天一次
、
每天两次
、
每周一次
、
每两周一次或每三周一次施用
。
本文还提供了一些方法,其中重组溶瘤病毒
、
免疫原性组合物或药物组合物作为团注或缓慢输注施用
。
本文还提供了方法,其中施用重组溶瘤病毒
、
免疫原性组合物或药物组合物在施用第一剂量后约1小时至约3天后产生第一峰值病毒载量,并且在施用第一剂量后约3天至约
10
天后产生第二峰值病毒载量
。
本文还提供了方法,包括施用另外的疗法,其中另外的疗法的施用持续时间为约1天
、
约2天
、
约3天
、
约4天
、
约5天
、
约6天
、
约1周
、
约2周
、
约3周
、
约4周
、
约6周
、
约7周
、
约8周
、
约9周
、
约
10
周或约
12
周
。
本文还提供了方法,其中另外的疗法每天一次
、
每天两次
、
每1天一次
、
每2天一次
、
每3天一次
、
每4天一次
、
每5天一次
、
每6天一次
、
每1周一次
、
每2周一次
、
每3周一次
、
每4周一次
、
每6周一次
、
每7周一次
、
每8周一次
、
每9周一次
、
每
10
周一次
、
每
12
周一次
、
每4个月一次
、
每5个月一次
、
每6个月一次
、
每7个月一次
、
每8个月一次
、
每9个月一次
、
每
10
个月一次
、
每
11
个月一次或每1年一次施用
。
本文还提供了方法,其中另外的疗法以液体剂型
、
固体剂型
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
本文还提供了方法,其中另外的疗法以液体剂型
、
固体剂型
、
可吸入剂型
、
鼻内剂型
、
脂质体制剂
、
包含纳米颗粒的剂型
、
包含微粒的剂型
、
聚合物剂型或其任何组合施用
。
本文还提供了方法,其中另外的疗法口服
、
静脉内
、
通过瘤内注射
、
通过腹膜内注射或通过辐射施用
。
本文还提供了方法,其中另外的疗法包括化学疗法
、
放疗
、
用另外的病毒进行的溶瘤病毒疗法
、
用免疫调节蛋白治疗
、car t
细胞疗法
、
抗癌剂或其任何组合
。
本文还提供了方法,其中另外的疗法包括施用免疫调节剂,免疫调节剂包括抗
cd33
抗体及其可变区
、
抗
cd11b
抗体及其可变区
、cox2
抑制剂
、
细胞因子
、
趋化因子
、
抗
ctla4
抗体或其抗原结合片段
、
抗
pd-1
抗体或其抗原结合片段
、
抗
pd-l1
抗体或其抗原结合片段或
tlr
激动剂
。
本文还提供了方法,其中另外的疗法包括施用抗癌剂,其中抗癌剂是化疗剂
。
本文还提供了方法,其中受试者是人类
。
实施例
[0107]
以下实施例进一步说明了所描述的实施方案,而非限制本公开内容的范围
。
[0108]
实施例1:肿瘤模型
[0109]
在肿瘤模型系统中,将重组痘苗病毒与不含本文描述的修饰的相同病毒毒株进行比较进行测定
。
下表列出了用于测试的病毒及其病毒基因组中的修饰:
[0110]
表1[0111][0112]
上表1示出了研究中使用的病毒是重组痘苗病毒
wo0434n(
示出为
a52r-mutcxcr4tk-158-cpx012+)
和参考痘苗病毒
wo0416n(a52r-mutcxcr4 tk-)。wo0434n
的修饰是通过缺失
tk
基因,并用
p7.5
驱动的突变体
cxcr4
取代
a52
基因,以及用牛痘病毒基因
cpxv012
取代
a35
基因
(wr158)。
参考痘苗病毒
wo0416n
缺失了
tk
基因,并用
p7.5
驱动的突变体
cxcr4
取代了
a52
基因
。
对照为痘苗病毒
western reserve
胸苷激酶阴性
(wr.tk-)
毒株
(hcctkm)
和媒介物配制的缓冲液
(vfb)。p7.5
启动子的核酸序列由
seq id no:1
定义
。
突变体
cxcr4
基因的核酸序列由
seq id no:15
定义
。cpxv012
的核酸序列由
seq id no:2
定义
。
本研究在
b16
肿瘤模型中进行
。
病毒施用后
17
天测量每组和对照的肿瘤体积
。
在图1中示出的结果指示与参考病毒
wo0416n
或对照
hcctkm
和
vfb
相比,
wo0434n
病毒的治疗活性增强
。
[0113]
实施例2:毒株表征
[0114]
为了评估给定病毒在细胞类型中是有复制能力的还是复制缺陷的,通过使用来自感染了重组病毒的哺乳动物或啮齿动物的血清的
pcr
测定
、
病毒噬斑测定或其任何组合来评估重组痘苗病毒的复制能力
。
对于病毒噬斑测定,用痘苗病毒感染组织培养瓶中易感细胞的汇合单层
。
孵育后,细胞病变效应
(cpe)
通过清除细胞单层的晕圈或圆形的形成来观察和可视化
。
用增加黏度的溶液替换细胞培养基
。
替换溶液包括明胶或羧甲基纤维素
。
病毒噬斑测定通过用增加细胞对比度的剂染色通过肉眼或通过显微镜来可视化
。
感染后可以孵育4小时至
48
小时,然后可以观察噬斑
。
染色剂是结晶紫
。
对于基于
pcr
的测定,使用基于
qpcr
的方法对痘苗病毒含量进行定量
。
[0115]
实施例3:肿瘤生长抑制
[0116]
在癌症小鼠模型中进行动物测定,以评估本文描述组合物对肿瘤生长的影响
。
简而言之,将修饰的痘苗病毒瘤内注射
(it)
到携带
renca
和
emt6
肿瘤的小鼠中
。
[0117]
将修饰的痘苗病毒与媒介物配制的缓冲液
(vfb)
进行比较进行评估
。
第1组用包含
tk
基因缺失
、
编码牛痘病毒
v012
蛋白
(cpxv012)
的核酸
(seq id no:2)
的插入
、p7.5
启动子
(seq id no:1)
和
loxp
序列
(seq id no:35)
的修饰的痘苗病毒处理
。
第2组用包含
wr158
基因缺失
、
编码
cpxv012
蛋白的核酸
(seq id no:2)
的插入
、p7.5
启动子
(seq id no:1)
和
loxp
序列
(seq id no:35)
的修饰的痘苗病毒处理
。
第3组用包含
tk
基因缺失和编码显性负性干扰素调节因子7的核酸
(dnirf7
,
seq id no:36)
的插入的痘苗病毒处理
。
第4组用包含
tk
基因缺失和编码病毒干扰素调节因子3的核酸
(virf3
,
seq id no:38)
的插入的修饰的痘苗病毒处理
。
[0118]
将
renca
细胞或
emt6
细胞肿瘤皮下植入
balb/c
小鼠
。
小鼠被分成
10
只一组
。
用单剂量
1x10
7 pfu
修饰的痘苗病毒或媒介物对照对肿瘤进行注射
。
[0119]
在
23
天后测量带有
renca
肿瘤的小鼠的肿瘤体积,如图
2a
中示出
。
用表达牛痘病毒
v012
和
virf3
的病毒处理的组显示出最有效的
renca
肿瘤体积减少
。
[0120]
在
27
天后测量带有
emt6
肿瘤的小鼠的肿瘤体积,如图
2b
中示出
。
用表达牛痘病毒
v012
和
dnirf7
的病毒处理的组显示出最有效的
emt6
肿瘤体积减少
。
[0121]
虽然本文已经示出和描述了本发明的优选实施方案,但对于本领域技术人员将明显的是,此类实施方案仅通过示例的方式提供
。
本领域技术人员现将想到不偏离本发明的许多变化
、
改变和替换
。
应当理解,可以在实践本发明时采用本文描述的本发明的实施方案的各种替代方案
。
所附权利要求意图限定本发明的范围,并且从而涵盖在这些权利要求范围内的方法和结构及其等同物
。
[0122]
表2:序列
[0123]
[0124]
[0125]
[0126]
[0127]
[0128]
[0129]
[0130]
[0131]
[0132]
[0133]
[0134]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1