重酒石酸间羟胺注射液及其制备方法与流程
本申请涉及但不限于药物制剂领域,尤指一种重酒石酸间羟胺注射液及其制备方法。
背景技术:
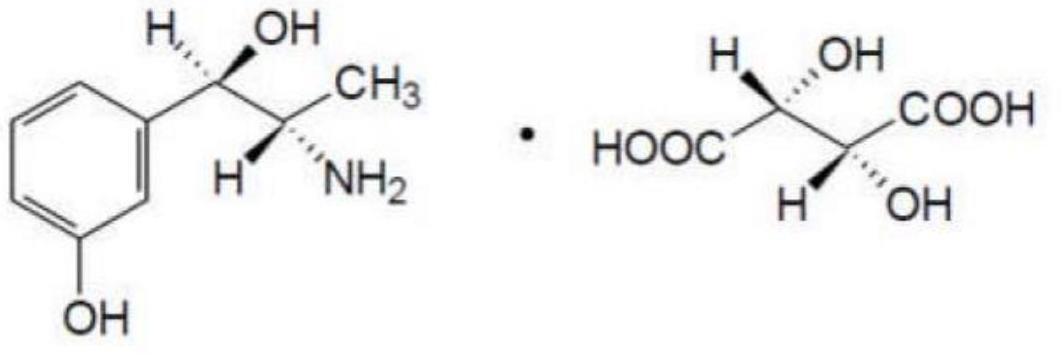
1、重酒石酸间羟胺,cas号为33402-03-8,结构式如下:
2、
3、根据重酒石酸间羟胺的强制降解实验结果猜测,重酒石酸间羟胺对氧敏感,易被氧化(3%双氧水,7天处理后,有关物质方法检出0.26%的降解杂质,含量方法检出1.6%的降解杂质)。
4、重酒石酸间羟胺注射液,规格1ml:10mg,为α肾上腺素受体激动药,适应症为:防治椎管内阻滞麻醉时发生的急性低血压;用于出血、药物过敏、手术并发症及脑外伤或脑肿瘤合并休克而发生的低血压,本品可用于辅助性对症治疗;也可用于心源性休克或败血症所致的低血压。
5、重酒石酸间羟胺的原研公司为phebra pty ltd,于2018年1月16日在澳大利亚批准上市,其商品名为处方组成[1]如下:
6、
7、
8、亚硫酸盐是添加到某些药物产品中以抑制活性药物成分氧化的化学物质。活性药物成分的氧化可能导致药品不稳定和效力的丧失。用于抑制这种氧化过程的亚硫酸盐包括亚硫酸氢钠、焦亚硫酸钠、亚硫酸钠、亚硫酸氢钾和焦亚硫酸钾等。最近的研究表明,亚硫酸盐可能引起某些易感人群,特别是哮喘患者的过敏反应[2]-[3]。因此亚硫酸盐的添加应慎重。
9、重酒石酸间羟胺注射液原研处方中添加了抗氧剂焦亚硫酸钠,因此可能引起过敏反应。
10、中国专利申请cn107157925a公开了一种重酒石酸间羟胺注射液及其制备方法,每10000ml重酒石酸间羟胺注射液中包含:重酒石酸间羟胺190g,氯化钠90~110g,亚硫酸氢钠10~20g,依地酸钙钠0.05~0.2g,硫辛酸0.01~0.1g,余量为水。重酒石酸间羟胺注射液的制备方法包括:步骤一、浓配:取注射用水,通氮,之后将亚硫酸氢钠和氯化钠溶解,再依次加入硫辛酸、依地酸钙钠和重酒石酸间羟胺,通氮至饱和,过滤;步骤二、稀配:在不间断地通入氮气情况下,加注射用水至配制量,循环过滤至澄明,得到半成品;步骤三、将半成品过滤后充氮灌封,流通蒸汽100℃灭菌15分钟,检漏,冷却,得到重酒石酸间羟胺注射液。其制备工艺利用方法和物质简单有效、成本较低,各项指标均符合国家食品药品监督管理局的相关规定。但此专利申请的重酒石酸间羟胺注射液配方中含抗氧剂亚硫酸氢钠,可能引起过敏反应。
11、中国专利申请cn106389312a公开了一种重酒石酸间羟胺注射液的药物组合物,该药物组合物由重酒石酸间羟胺、氯化钠、焦亚硫酸钠、依地酸盐和水组成,每10000ml组合物中由重酒石酸间羟胺185-195g,氯化钠80-90g,焦亚硫酸钠10-21g,依地酸盐为依地酸二钠或依地酸钙钠,含量为0.1-0.5g,余量为水。但此专利申请的重酒石酸间羟胺注射液配方中含抗氧剂焦亚硫酸钠,可能引起过敏反应。
12、中国专利申请cn103371969a公开了一种重酒石酸间羟胺注射液及其制剂工艺,所述重酒石酸间羟胺注射液的成分为:每10000ml注射液内含,重酒石酸间羟胺189g,氯化钠68g~102g,焦亚硫酸钠16g~24g,注射用水加至10000ml。其重酒石酸间羟胺注射液的质量符合国家食品药品监督管理局的相关规定。但此专利申请的重酒石酸间羟胺注射液配方中含抗氧剂焦亚硫酸钠,可能引起过敏反应。
13、中国专利申请cn112245387a公开了一种重酒石酸间羟胺注射液的组成及制备方法,重酒石酸间羟胺注射液的处方由重酒石酸间羟胺、氯化钠、l-肌肽和注射用水组成,其中l-肌肽用量为2-8mg/ml。该重酒石酸间羟胺注射液组成简单,质量稳定,制备工艺简便高效,无需特殊设备和惰性气体的填充,经终端灭菌(f0≥12)后制得成品杂质水平低,安全性良好。但此专利申请的重酒石酸间羟胺注射液配方中含抗氧剂l-肌肽,而l-肌肽通常用于口服食品添加剂或化妆品中,缺乏注射给药的安全性数据(fda inactive ingredient(iig)数据库无收载),不能随意添加在注射剂配方中,否则可能带来不可预知的副作用。
14、因此,亟需一种既能避免重酒石酸间羟胺氧化,又不会带来其它副作用的重酒石酸间羟胺注射液及其制备方法。
技术实现思路
1、以下是对本文详细描述的主题的概述。本概述并非是为了限制本申请的保护范围。
2、本申请提供了一种重酒石酸间羟胺注射液及其制备方法,该重酒石酸间羟胺注射液中不含有抗氧化剂,可以避免亚硫酸盐、l-肌肽等抗氧化剂的副作用,而且重酒石酸间羟胺的稳定性较好。
3、本申请提供了一种重酒石酸间羟胺注射液,每1ml注射液包括:
4、重酒石酸间羟胺 18.05mg至19.95mg
5、渗透压调节剂 8.075mg至8.925mg
6、注射用水余量;
7、并且,所述重酒石酸间羟胺注射液中不含有抗氧化剂。
8、在本申请的实施例中,每1ml注射液可以包括:
9、重酒石酸间羟胺 19mg
10、渗透压调节剂 8.5mg
11、注射用水 余量;
12、并且,所述重酒石酸间羟胺注射液中不含有抗氧化剂。
13、在本申请的实施例中,所述渗透压调节剂可以选自氯化钠、葡萄糖、磷酸盐和枸橼酸盐中的任意一种或多种。
14、在本申请的实施例中,所述渗透压调节剂可以为氯化钠。
15、本申请实施例还提供了如上所述的重酒石酸间羟胺注射液的制备方法,包括:
16、称量:按照配比称量重酒石酸间羟胺、渗透压调节剂和注射用水;
17、配制:将一部分注射用水加入到配制罐内,在搅拌状态下依次加入渗透压调节剂和重酒石酸间羟胺,搅拌至所述渗透压调节剂和所述重酒石酸间羟胺溶解,补加注射用水至全量,搅拌均匀,得到药液;
18、过滤:对所述药液进行过滤;
19、灌封:将过滤后的药液灌装在药剂容器中,封口;
20、灭菌。
21、在本申请的实施例中,所述过滤可以包括采用直径为0.2微米的聚偏氟乙烯滤芯过滤。
22、在本申请的实施例中,所述灭菌的温度可以为121℃,所述灭菌的时间可以≥12分钟。
23、在本申请的实施例中,所述灭菌的时间可以为12分钟至25分钟。
24、本申请实施例的重酒石酸间羟胺注射液及其制备方法,通过去除抗氧剂可以避免抗氧剂引起的副作用,而且改善了制剂对氧气的敏感性(无需严格控氧),降低了生产控制成本;同时,可以在不添加抗氧剂的情况下,有效控制成品的有关物质水平并且获得良好的产品稳定性。
25、本申请的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本申请而了解。本申请的其他优点可通过在说明书中所描述的方案来实现和获得。
技术特征:
1.一种重酒石酸间羟胺注射液,其特征在于,每1ml注射液包括:
2.根据权利要求1所述的重酒石酸间羟胺注射液,其中,每1ml注射液包括:
3.根据权利要求1或2所述的重酒石酸间羟胺注射液,其中,所述渗透压调节剂选自氯化钠、葡萄糖、磷酸盐和枸橼酸盐中的任意一种或多种。
4.根据权利要求3所述的重酒石酸间羟胺注射液,其中,所述渗透压调节剂为氯化钠。
5.一种根据权利要求1至4中任一项所述的重酒石酸间羟胺注射液的制备方法,其特征在于,包括:
6.根据权利要求5或所述的制备方法,其中,所述过滤包括采用直径为0.2微米的聚偏氟乙烯滤芯过滤。
7.根据权利要求5或6所述的制备方法,其中,所述灭菌的温度为121℃,所述灭菌的时间≥12分钟。
8.根据权利要求7所述的制备方法,其中,所述灭菌的时间为12分钟至25分钟。
技术总结
一种重酒石酸间羟胺注射液及其制备方法,每1ml注射液所述重酒石酸间羟胺注射液包括:18.05mg至19.95mg重酒石酸间羟胺、8.075mg至8.925mg渗透压调节剂和余量的注射用水,并且所述重酒石酸间羟胺注射液中不含有抗氧化剂。本申请实施例的重酒石酸间羟胺注射液中不含有抗氧化剂,可以避免抗氧化剂的副作用,而且重酒石酸间羟胺的稳定性较好。
技术研发人员:林韶辉,孙超
受保护的技术使用者:北京世桥生物制药有限公司
技术研发日:
技术公布日:2024/1/11
- 还没有人留言评论。精彩留言会获得点赞!