蛋白配体结合亲和力预测方法、装置、系统及存储介质与流程
本发明涉及药物设计,更具体地说,涉及一种蛋白配体结合亲和力预测方法、装置、系统及存储介质。
背景技术:
1、计算机辅助药物设计(computer aided drug design)是以计算机化学为基础,通过计算机的模拟、计算和预算药物与受体生物大分子之间的关系,设计和优化先导化合物的方法。计算机辅助药物设计实际上就是通过模拟和计算受体与配体的这种相互作用,进行先导化合物的优化与设计。计算机辅助药物设计大致包括活性位点分析法、数据库搜寻、全新药物设计。
2、在药物设计过程中,基于众多理化性质,与靶点蛋白有较高的结合亲和力是配体分子能够成药的必要条件。过去二十年来,分子对接(docking)在药物设计中得到了广泛的应用,其有能力进行千万级别分子数据库的筛选,但打分函数不准确以及采样不足限制了这种方法的精度,因此其多应用于粗筛阶段得到苗头化合物。
3、相较之下,自由能微扰方法(free energy perturbation,fep)严格基于统计物理和分子动力学,可以对结合位点构象变化进行有效采样,从而精准评估蛋白与配体的结合自由能。虽然fep的算法理论早在20世纪末便已被提出,但至今仍然存在准备模拟流程繁杂、消耗计算资源庞大、计算模拟准确度差、精度低等问题。
技术实现思路
1、有鉴于此,针对于上述技术问题,本发明提供一种蛋白配体结合亲和力预测方法,包括:
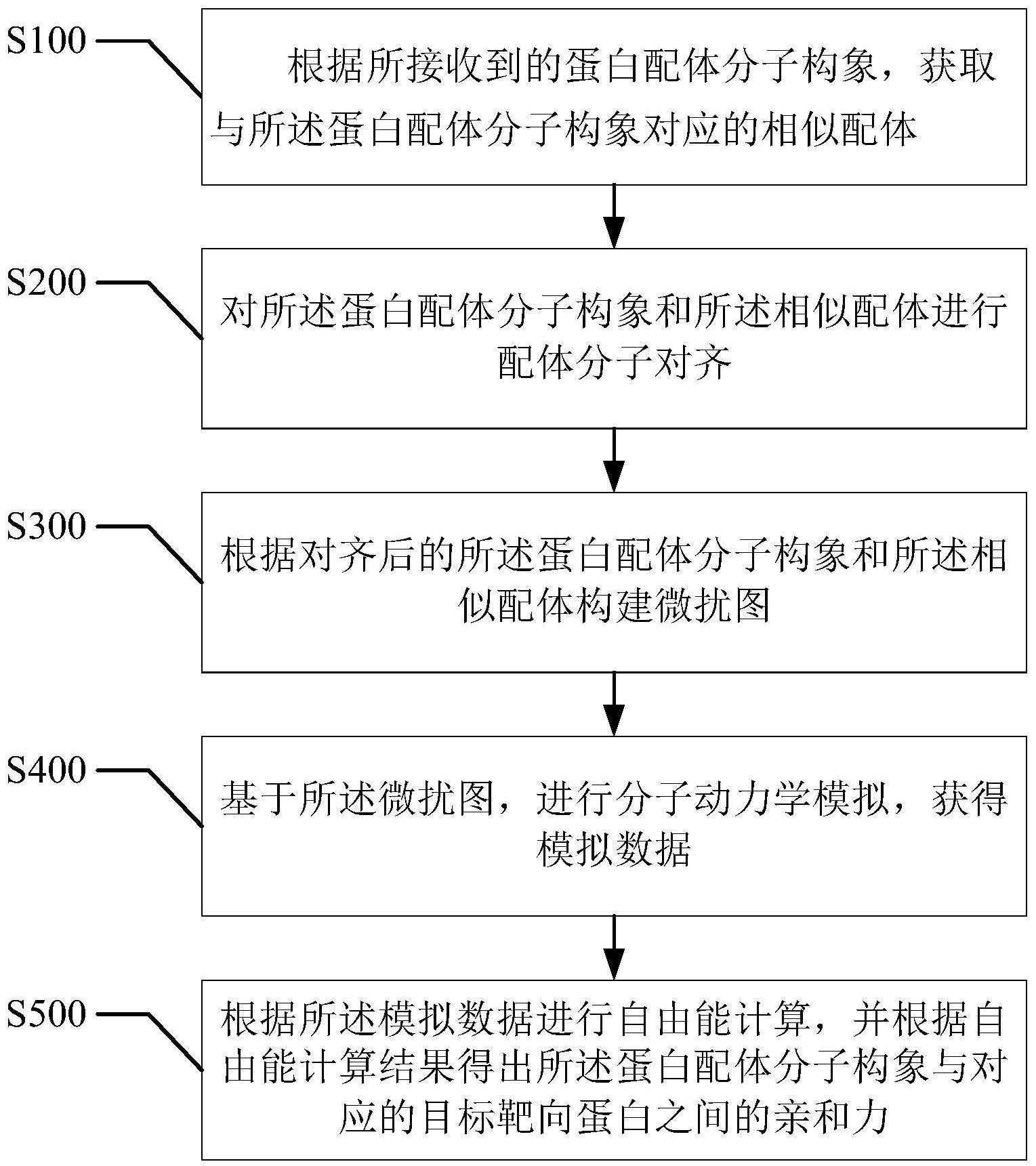
2、根据所接收到的蛋白配体分子构象,获取与所述蛋白配体分子构象对应的相似配体;
3、对所述蛋白配体分子构象和所述相似配体进行配体分子对齐;
4、根据对齐后的所述蛋白配体分子构象和所述相似配体构建微扰图;
5、基于所述微扰图,进行分子动力学模拟,获得模拟数据;
6、根据所述模拟数据进行自由能计算,并根据自由能计算结果得出所述蛋白配体分子构象与对应的目标靶向蛋白之间的亲和力。
7、优选地,所述根据所接收到的蛋白配体分子构象,获取与所述蛋白配体分子构象对应的相似配体,包括:
8、对所述蛋白配体分子构象进行结构整理;
9、针对结构整理后的所述蛋白配体分子构象,获取待筛选的相似配体。
10、优选地,所述对所述蛋白配体分子构象进行结构整理,包括:
11、获取所述蛋白配体分子构象的蛋白特征参数;
12、根据所述蛋白特征参数判断当前的所述蛋白配体分子构象是否能够进行自由能计算;
13、若当前的所述蛋白配体分子构象不能进行自由能计算,则根据所述蛋白特征参数,对所述蛋白配体分子构象进行如下一项或多项的结构整理:
14、a保留或删除所述蛋白配体分子构象中的特定链;
15、b确定所述蛋白配体分子构象中的最优构象;
16、c补全所述蛋白配体分子构象中缺失的侧链原子;
17、d根据残基类型补充所述蛋白配体分子构象中的氢原子;
18、e根据预设ph值计算所述蛋白配体分子构象各极性氨基酸的质子化状态;
19、f对所述蛋白配体分子构象的结构中能量最小化;
20、g对所述蛋白配体分子构象进行单点突变。
21、优选地,所述对所述蛋白配体分子构象和所述相似配体进行配体分子对齐,包括:
22、基于所述蛋白配体分子构象的二维结构和三维结构,判断所述蛋白配体分子构象是否为预设复杂体系;
23、若所述蛋白配体分子构象不为预设复杂体系,则对所述蛋白配体分子构象与所述相似配体的进行基于刚性对齐方法和/或柔性对齐方法的配体分子对齐;
24、若所述蛋白配体分子构象为预设复杂体系,则对所述蛋白配体分子构象与所述相似配体的进行基于限制性对接方法的配体分子对齐。
25、优选地,所述对所述蛋白配体分子构象与所述相似配体的进行基于限制性对接方法的配体分子对齐,包括:
26、若所述相似配体与所述蛋白配体分子构象的骨架之间为接近结构骨架,则基于所述相似配体的配体骨架,对所述蛋白配体分子构象与所述相似配体施加限制性对接;
27、若所述蛋白配体分子构象的基团能与所述相似配体的基团产生相互作用,则基于所述相似配体的药效基团,对所述蛋白配体分子构象与所述相似配体施加限制性对接;
28、若所述蛋白配体分子构象与蛋白结合时,通过共价键与靶蛋白残基能发生不可逆结合,则针对所述蛋白配体分子构象与所述相似配体中形成共价键的位置施加限制性对接。
29、优选地,所述根据对齐后的所述蛋白配体分子构象和所述相似配体构建微扰图,包括:
30、将对齐后的所述蛋白配体分子构象和所述相似配体分别进行两两配对连边,得到pair对;
31、针对每个所述pair对进行配体分子间相似度计算,得到分子指纹相似度;
32、根据所述分子指纹相似度得到所述微扰图。
33、优选地,所述根据所述分子指纹相似度得到所述微扰图,包括:
34、以分子指纹相似度为权重指标,进行modified federov迭代计算,得到合理连边数量;
35、根据所述合理连边数量得到所述微扰图。
36、优选地,所述根据对齐后的所述蛋白配体分子构象和所述相似配体构建微扰图之后,还包括:
37、若预设反应体系中包含有成键断键结构变化,则获取构建所述微扰图后的所述蛋白配体分子构象和所述相似配体映射的3d结构;
38、基于所述3d结构,将所述蛋白配体分子构象的成键原子和/或断键原子加入至所述微扰图中。
39、优选地,所述基于所述微扰图,进行分子动力学模拟,获得模拟数据,包括:
40、获取与反应体系对应的预设md参数,并通过所述预设md参数采样,进行分子动力学模拟,获得所述模拟数据;
41、优选地,所述通过所述预设md参数采样,包括:
42、采用rest2增强采样方法,对所述微扰图中结构进行升高温度,针对跨过能垒障碍的结构的势能面采样,并在针对微扰图结构的初始和末尾窗口的采样中恢复至正常温度。
43、优选地,所述根据所述模拟数据进行自由能计算,并根据自由能计算结果得出所述蛋白配体分子构象与对应的目标靶向蛋白之间的亲和力,包括:
44、根据所述模拟数据,分别计算所述蛋白配体分子构象和/或所述相似配体筛选后的分子对与所述目标靶向蛋白的自由能变化,根据所述自由能变化获得相对自由能差值;将所述相对自由能差值作为所述自由能计算结果;
45、根据自由能计算结果评价所述分子对中分子对应所述目标靶向蛋白的亲和力;
46、优选地,所述分子对中包括筛选后的第一分子和第二分子;所述自由能变化包括第一自由能变化和第二自由能变化;所述分别计算所述蛋白配体分子构象和/或所述相似配体筛选后的分子对与所述目标靶向蛋白的自由能变化,根据所述自由能变化获得相对自由能差值;将所述相对自由能差值作为所述自由能计算结果,包括:
47、计算所述第一分子与所述目标靶向蛋白结合的第一自由能变化;并且,计算所述第二分子与所述目标靶向蛋白结合的第二自由能变化;
48、计算所述第二自由能变化和所述第一自由能变化的差值,作为所述相对自由能差值;
49、优选地,所述根据自由能计算结果评价所述分子对中分子对应所述目标靶向蛋白的亲和力,包括:
50、判断所述自由能计算结果中的所述相对自由能差值是否小于0;
51、若所述相对自由能差值是否小于0,则所述第一分子针对于所述目标靶向蛋白的亲和力大于所述第二分子。
52、此外,为解决上述问题,本发明还提供一种蛋白配体结合亲和力预测装置,包括:
53、获取模块,用于根据所接收到的蛋白配体分子构象,获取与所述蛋白配体分子构象对应的相似配体;
54、对齐模块,用于对所述蛋白配体分子构象和所述相似配体进行配体分子对齐;
55、构建模块,用于根据对齐后的所述蛋白配体分子构象和所述相似配体构建微扰图;
56、模拟模块,用于基于所述微扰图,进行分子动力学模拟,获得模拟数据;
57、计算模块,用于根据所述模拟数据进行自由能计算,并根据自由能计算结果得出所述蛋白配体分子构象与对应的目标靶向蛋白之间的亲和力。
58、此外,为解决上述问题,本发明还提供一种蛋白配体结合亲和力预测系统,包括存储器以及处理器,所述存储器中存储有蛋白配体结合亲和力预测程序,所述处理器运行所述蛋白配体结合亲和力预测程序以使所述蛋白配体结合亲和力预测系统执行如上述所述的蛋白配体结合亲和力预测方法。
59、此外,为解决上述问题,本发明还提供一种计算机可读存储介质,所述计算机可读存储介质上存储有蛋白配体结合亲和力预测程序,所述蛋白配体结合亲和力预测程序被处理器执行时实现如上述所述的蛋白配体结合亲和力预测方法。
60、本发明提供了一种蛋白配体结合亲和力预测方法、装置、系统及存储介质,其中,所述方法包括:根据所接收到的蛋白配体分子构象,获取与所述蛋白配体分子构象对应的相似配体;对所述蛋白配体分子构象和所述相似配体进行配体分子对齐;根据对齐后的所述蛋白配体分子构象和所述相似配体构建微扰图;基于所述微扰图,进行分子动力学模拟,获得模拟数据;根据所述模拟数据进行自由能计算,并根据自由能计算结果得出所述蛋白配体分子构象与对应的目标靶向蛋白之间的亲和力。
61、本发明通过对蛋白配体分子构象和相似配体进行限制性对接,从而实现配体分子对齐,构建结构的微扰图,进行分子动力学模拟后再实施自由能计算,并根据计算结果能够评估所输入的蛋白配体分子构象与对应目标靶向蛋白之间的亲和力。本发明提供了一种fep完整解决方案,将自由能微扰理论、分子动力学和高性能计算相结合,能够以化学精度高效评估蛋白质与配体的结合亲和力,设计和计算过程简便,大大提高了药物设计的精度和准确度。
- 还没有人留言评论。精彩留言会获得点赞!