卡谷氨酸原料药和卡谷氨酸固体制剂及其制备方法与流程
本发明涉及医药领域。具体地,本发明涉及卡谷氨酸原料药和卡谷氨酸固体制剂及其制备方法。
背景技术:
1、nags(乙酰谷氨酸合成酶)缺乏症,是尿素循环代谢异常的其中一种,这种疾病是由于尿素缺乏所造成。nags缺乏使得nag合成不足,影响氨进入尿素循环代谢,导致丙氨酸、谷氨酰氨酸、谷氨酸、氨的堆积。
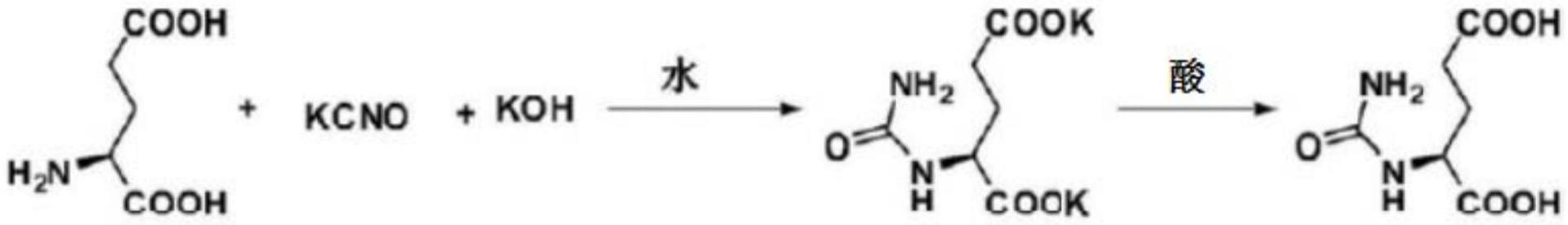
2、卡谷氨酸,化学名:n-氨基甲酰-l-谷氨酸或(2s)-2-(氨甲酰氨基)戊二酸,化学式:c6h10n2o5(结构式如下式(ⅰ)所示)。主要是治疗儿童和成人肝脏n-乙酰谷氨酸合成酶(nags)缺乏所致急性或慢性高氨血症。
3、
4、刻痕片是一种比较特别的片剂,它既可以整片服用,也可以掰片(一片或多片)后服用。刻痕片外观形状与普通片一样,多为圆形、椭圆形或胶囊形,一般是在普通片上多了一道刻痕(一字型)或两道刻痕(十字行),也有更多道刻痕的。刻痕的作用一方面是用于识别它与非刻痕片,另一方便是为了便于掰片。老年患者、儿童和一些特殊病人在吞服固体片剂时有时比较困难,可通过将整片掰成多片而解决这方面的问题;有些药物比较特殊,生产线无法满足最小剂量的片剂要求,为此可通过刻痕片放大剂量解决。
5、然而,刻痕片也存在很多问题,例如,有些刻痕片不易被掰开,那么大部分患者会选择放弃掰片,刻痕片也就失去了它的刻痕价值,部分剂量也随之放弃使用;刻痕片掰开过程中会出现粉末或碎片从而重量损失,造成掰开片重量不均一,影响药效及安全性。
6、对于卡谷氨酸片剂而言,其正反面沿纵向具3个刻痕,刻痕具有等分剂量的作用,沿刻痕掰片,可将卡谷氨酸片剂掰为1/2片,进一步掰为1/4片。其按患者体重不同,很多情况需要掰成1/4片,如果掰开片重量不均一或重量损失较大,会严重影响药效,另外,按照国家药品监督管理局药品审评中心发布的《仿制口服片剂功能性刻痕设计和研究的一般要求》:分割后的部分的质量应能符合整片的质量标准。结合中国药典2020年版四部通则【重量差异】项的要求,1/4片的重量差异限度应为±5%,超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。另外,国外市售卡谷氨酸片1/4片片重重量差异不符合中国药典2020年版四部通则【重量差异】项的要求。
7、因此,研发一种掰开片重量均一、重量损失小符合要求的卡谷氨酸固体制剂及其制备方法显得很有必要。
技术实现思路
1、本发明旨在至少在一定程度上解决现有技术中存在的技术问题至少之一。为此,本发明提出了卡谷氨酸固体制剂及其制备方法和卡谷氨酸原料药的制备方法,利用本发明的制备d90粒径为200~600μm的卡谷氨酸原料药的方法可以获得d90粒径为200~600μm的卡谷氨酸原料药,利用该卡谷氨酸原料药制备的卡谷氨酸固体制剂经掰成1/4片后重量损失少,1/4片重量均一,崩解时间短,溶解均一性好,方便服用;卡谷氨酸原料药的制备方法操作简便,所得到的卡谷氨酸原料药粒径可控,适于规模化推广应用。
2、在本发明的一个方面,本发明提出了一种制d90粒径为200~600μm的备卡谷氨酸原料药的方法。根据本发明的实施例,所述方法包括:将卡谷氨酸铵盐、卡谷氨酸粗品与酸液混合,结晶,收集并洗涤晶体,得到所述卡谷氨酸原料药,基于所述卡谷氨酸铵盐和卡谷氨酸粗品的总摩尔量,所述卡谷氨酸铵盐与卡谷氨酸粗品的摩尔比为1~9:1。
3、发明人发现,卡谷氨酸原料药的粒径会影响卡谷氨酸固体制剂经分割后的重量损失,当卡谷氨酸原料药d90的粒径为200~600μm时,以其作为原料药制备的卡谷氨酸固体制剂经分割后的重量损失较少。与此同时,该卡谷氨酸固体制剂崩解时间较短,溶解性好,方便服用。
4、进一步地,发明人发现,采用卡谷氨酸铵盐和卡谷氨酸粗品复配进行加酸反应,可以控制所得到的晶体(卡谷氨酸原料药)的d90粒径为200~600μm。并且收率高、纯度高,操作简便、成本低,适于工业化生产。
5、根据本发明的实施例,所述混合包括:将所述卡谷氨酸铵盐和卡谷氨酸粗品溶于水中进行搅拌,边搅拌边向混合液中滴加酸液,当反应液达到预定ph值时,停止搅拌,进行结晶;滴加过程中,控制反应液的温度为0~8℃。
6、根据本发明的实施例,所述酸液的滴加速度为10~80g/min,优选为10~66g/min。
7、根据本发明的实施例,所述搅拌的转速控制为50~180转/分,优选为50~150转/分。
8、在本发明的另一方面,本发明提出了卡谷氨酸原料药。根据本发明的实施例,所述卡谷氨酸原料药由前面所述制备d90粒径为200~600μm的卡谷氨酸原料药的方法制备获得的。
9、在本发明的又一方面,本发明提出了一种卡谷氨酸固体制剂。根据本发明的实施例,所述卡谷氨酸固体制剂包括:所述卡谷氨酸原料药的d90粒径为200~600μm;所述辅料包括微晶纤维素,所述微晶纤维素包括第一微晶纤维素和第二微晶纤维素;所述第一微晶纤维素的休止角为55度以上,且所述第二微晶纤维素的休止角为46度以下;或者所述第一微晶纤维素的型号选自ph-f20jp和kg1000的至少之一;且所述第二微晶纤维素的型号选自ph101、ph102、ph112、ph200、ph301、ph302、uf701和uf702的至少之一。
10、发明人为了解决卡谷氨酸固体制剂经掰成1/4片后重量损失达不到中国药典的要求的技术问题,对卡谷氨酸原料药及辅料进行了研究。发明人发现,采用同时采用d90粒径为200~600μm的卡谷氨酸原料药的粒径会影响,
11、目前,固体制剂领域中采用的辅料类型众多,复配关系更是多不胜数,在对辅料进行筛选优化过程中惊奇地发现,采用两种不同类型的微晶纤维素进行复配使用,重量损失较小,其中,采用上述第一微晶纤维素和第二微晶纤维素复配使用,所得固体制剂不仅经分割后重量损失较小,效果较佳,而且崩解时间较短,溶解后均一性好,方便服用。
12、根据本发明的实施例,所述卡谷氨酸原料药是采用前面所述制备d90粒径为200~600μm的卡谷氨酸原料药的方法制备获得的。
13、根据本发明的实施例,所述辅料进一步包括崩解剂、粘合剂、润湿剂和助流剂的至少之一。
14、根据本发明的实施例,所述崩解剂选自交联羧甲基纤维素钠、羧甲基纤维素钙、交联聚维酮和羧甲基淀粉钠中的至少之一;所述粘合剂选自羟丙甲纤维素、聚维酮、羟丙基纤维素和羧甲基纤维素钠的至少之一;所述润湿剂选自十二烷基硫酸钠、硬脂富马酸钠中的至少之一;所述助流剂选自二氧化硅、滑石粉中的至少之一。
15、根据本发明的实施例,所述第一微晶纤维素占药片总重的1~50%、5~45%、10~45%、10~40%、10~35%。
16、根据本发明的实施例,基于所述卡谷氨酸固体制剂的总质量,所述卡谷氨酸固体制剂包括:30~50质量%的卡谷氨酸原料药;以及余量的辅料。
17、根据本发明的实施例,所述卡谷氨酸固体制剂包括:30~50重量份的卡谷氨酸原料药;50~55重量份的微晶纤维素;2~4重量份的交联羧甲基纤维素钠;1~4重量份的羟丙甲纤维素;0.4~0.8重量份的十二烷基硫酸钠;0.2~0.6重量份的二氧化硅;以及0.1~2重量份的硬脂富马酸钠。
18、根据本发明的实施例,所述卡谷氨酸固体制剂的剂型为片剂,所述片剂表面设置有刻痕,优选正反面各有三条平行刻痕。
19、根据本发明的实施例,当沿刻痕将所述片剂掰成1/4片时,1/4片的重量差异限度为±5%,超出重量差异限度的不多于2片,并且,不多于1片超出限度1倍。
20、在本发明的又一方面,本发明提出了一种制备前面所述卡谷氨酸固体制剂的方法。根据本发明的实施例,所述方法包括:将所述卡谷氨酸原料药以及包含第一微晶纤维素和第二微晶纤维素的辅料进行混合和制片。由此,根据本发明实施例的方法所得固体制剂不仅经分割后重量损失较小,效果较佳,而且崩解时间较短,溶解后均一性好,方便服用。另外,该制备方法操作简便、快捷、成本低,适于规模化生产。
21、根据本发明的实施例,上述卡谷氨酸固体制剂的制备方法包括:
22、步骤1:将上述第二微晶纤维素、第一微晶纤维素、交联羧甲基纤维素钠、羟丙甲纤维素进行干燥处理;
23、步骤2:将卡谷氨酸原料药和上述已干燥的第二微晶纤维素、第一微晶纤维素、交联羧甲基纤维素钠、羟丙甲纤维素置于混合机中混合均匀;
24、步骤3:将十二烷基硫酸钠过60目筛,加入步骤2的混合物料中,继续混合均匀;
25、步骤4:将二氧化硅、硬脂富马酸钠过80目筛,加入步骤3中混合物料中,在混合均匀后,压片。
26、本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
27、本发明的有益效果在于:
28、1、本发明卡谷氨酸固体制剂经分割后的重量损失少,例如当沿刻痕将片剂掰成1/4片时,1/4片的重量差异限度为±5%,超出重量差异限度的不多于2片,并且,不多于1片超出限度1倍;
29、2、本发明卡谷氨酸固体制剂崩解时限短;
30、3、本发明卡谷氨酸原料药的制备方法操作简便,所得到的卡谷氨酸原料药粒径可控,可将卡谷氨酸原料药的d90的粒径控制为200~600μm。
- 还没有人留言评论。精彩留言会获得点赞!