一种多功能声激活型半导体聚合物纳米免疫药物及制备方法及应用
本发明涉及一种用于癌症治疗的纳米免疫药物,特别是调控肿瘤微环境的纳米免疫药物,属于有机半导体纳米材料。
背景技术:
1、根据世界卫生组织发布的数据报告,癌症病例相较于数年前已呈现减少趋势,但有些癌症的发病率却逐年攀升。目前,常见的癌症治疗手段有手术切除、放射治疗和化学治疗,但是上述治疗方法创伤性大、易复发,还会出现恶心呕吐等不同程度的副作用。此外,单一的治疗方式往往达不到良好的治疗效果。因此,设计出一种能够联合多种治疗方式的癌症策略是非常有必要的。
2、近年来,纳米材料在医学和生物科学领域交叉应用研究得到了广泛的发展、尤其是恶性肿瘤的早期诊断和治疗方面,与传统药物及治疗方式相比,纳米粒子小尺寸、易于修饰等优势,具有应用于各种临床治疗的潜力,例如药物传递、癌症的靶向诊断和治疗、分子手术、医学成像和纳米机器人等。
3、免疫治疗近年来在生物医学领域有着越来越广泛的应用。免疫治疗是指通过激活自身免疫系统来杀伤癌细胞。免疫治疗与传统治疗不同,它不仅可以抑制肿瘤的生长和转移,还可以形成长期的免疫记忆,防止肿瘤复发。在过去的几年里,涉及调节人类免疫系统来攻击癌细胞的癌症免疫疗法为肿瘤学领域带来了一场变革,增强宿主免疫系统对抗肿瘤的免疫疗法一定程度上推动了癌症治疗。然而,单模型免疫治疗往往应答率有限,偶尔会出现免疫相关不良反应(iraes),如细胞因子风暴、器官衰竭和造血系统功能障碍等情况。因此,纳米药物已被引入癌症免疫治疗,因其可调节的物理化学特性,能够增强药物与免疫细胞之间的相互作用,有望解决这些关键问题,更重要的是,纳米医学可以作为一个组装平台,允许其他的治疗方式(如化疗、光疗、放疗等)与免疫治疗相辅相成,有望改善免疫反应,而不牺牲破坏系统免疫耐受性,从而提高治疗效果,但纳米技术支持的癌症免疫治疗领域仍处于发展的早期阶段,仍有待被探索。
4、由于游离的免疫药物在体内的半衰期短、肿瘤选择性和富集量不足以及易引起严重的全身不良反应等原因,免疫药物经全身系统给药后难以实现安全、有效的免疫治疗。目前,开发肿瘤微环境和光响应型药物递送体系是解决该问题的主要策略。然而,肿瘤微环境响应型药物的特异性和可控性有限,仍然具有导致毒副作用的风险。由于光的组织穿透能力较弱,光响应型药物递送体系往往只能用于浅层肿瘤的治疗,并不适用于临床上大多数的深层组织中的肿瘤,这很大程度上制约了其临床转化和应用。因此,如何实现深层组织中肿瘤的安全高效免疫治疗是一个亟待解决的关键科学问题。声动力治疗(sdt)作为一种无创且精准的新型肿瘤治疗方法,利用超声波的强穿透性能够有效杀伤组织深部的癌细胞,在癌症治疗方面的应用越来越广泛。作为一种无创治疗方法,声动力治疗通过使用声敏剂耗氧产生剧毒活性氧(ros),所以,氧在促进足够的ros产生中起着决定性的作用。然而,由于实体肿瘤内的缺氧肿瘤微环境(tme),sdt的疗效可能受到限制,因此我们设计了一种通过阻断肿瘤细胞线粒体呼吸链阻止线粒体呼吸的方法来增加肿瘤微环境中氧气的含量,以此达到增强sdt的治疗效果。
5、相关研究表明,人体内存在的一类特殊气体信号分子,包括一氧化氮、一氧化碳和硫化氢(h2s)等,对癌症、炎症和心血管疾病都具有独特的治疗作用。气体药物相较于传统化疗药物有更多的优势,首先,气体不容易产生耐药性,这是许多化疗药物都会面临的问题。其次,气体采用供体形式给药,不是直接给药的方式,这使得气体具有更高的安全性和有效运输率,因此气体药物被誉为绿色药物,成为一种新兴的、具有广阔应用前景的治疗策略。h2s是重要的内源性气体传递分子,具有内在的生化特性,在正常和病理条件下均发挥其多种生理作用,在癌症治疗中具有强大的治疗效果。h2s可以通过抑制细胞色素c氧化酶活性来重塑氧代谢,导致线粒体功能障碍,从而抑制细胞呼吸和耗氧量,达到调节tme氧气含量的目的。
6、检索国内外文献,尚没有发现关于以单线态氧响应型外壳作为载体包覆药物外接透明质酸酶构建的纳米递送系统的相关报道。
技术实现思路
1、针对现有技术的问题,本发明提供了一种多功能声激活型半导体聚合物纳米免疫药物,其特征在于,以单线态氧响应型外壳作为载体包覆药物,外接透明质酸酶构建的纳米递送系统。
2、优选的是,本发明的单线态氧响应型外壳为dspe-tk-peg。
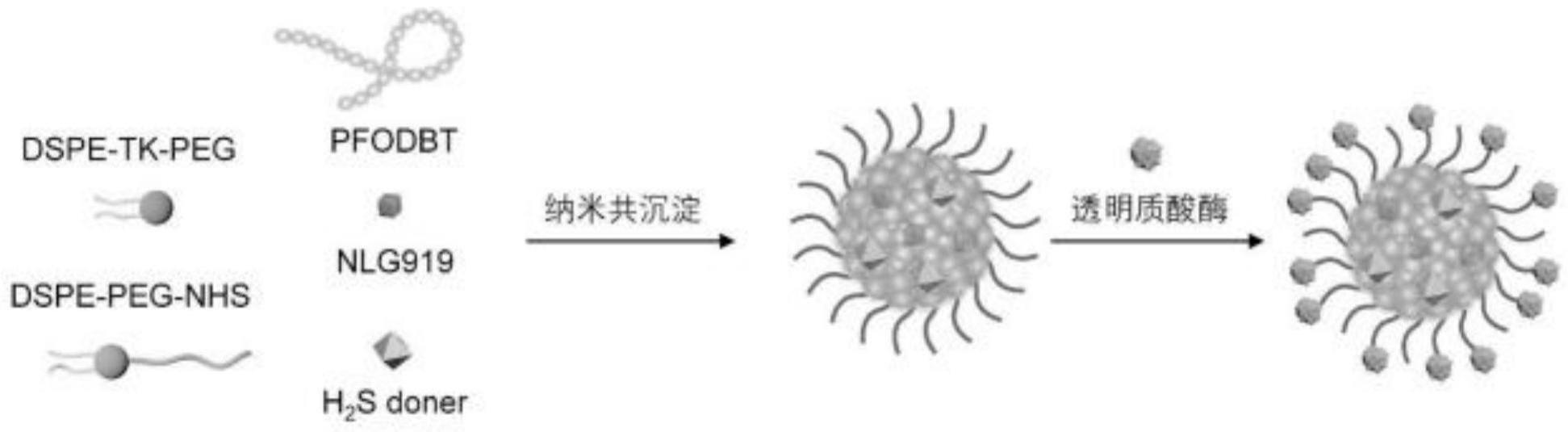
3、优选的是,本发明还包括:光敏剂pfodbt、nlg919以及小分子h2sdoner。
4、一种多功能声激活型半导体聚合物纳米免疫药物的制备方法,包括以下步骤:
5、步骤(1):将dspe-tk-peg、dspe-peg-nhs、光敏剂pfodbt、nlg919以及小分子h2sdoner溶解在四氢呋喃中;
6、步骤(2):将上述步骤(1)的混合溶液在超声条件下加入到四氢呋喃水溶液中,超声;
7、步骤(3):使用旋转蒸发仪将四氢呋喃充分挥发;
8、步骤(4):使用pes膜过滤装置过膜;
9、步骤(5):使用透析袋透析;
10、步骤(6):加入透明质酸酶搅拌;
11、步骤(7):使用超滤管超滤,得到纳米免疫药物。
12、优选的是,本发明步骤(1)将dspe-tk-peg、dspe-peg-nhs、光敏剂pfodbt、h2sdoner以及nlg919溶解在四氢呋喃中,dspe-tk-peg:dspe-peg-nhs:光敏剂pfodbt:h2sdoner:nlg919的质量比为10:10:0.25:1:0.5。
13、优选的是,本发明步骤(2)中四氢呋喃的水溶液,四氢呋喃与超纯水的比例为1:9,总体积为10ml;超声的时间为30min。
14、优选的是,本发明步骤(4)中使用的pes膜过滤装置的分子截留量的0.22μm;
15、优选的是,本发明步骤(5)中透析的条件为:透析袋的截留分子量为10000;透析时间为24h。
16、优选的是,本发明步骤(6)中搅拌的条件为:室温环境下,搅拌12-24h。
17、优选的是,本发明步骤(7)中超滤管的截留量为50000;离心机参数为:3500rpm,4℃,30min。
18、一种多功能声激活型半导体聚合物纳米免疫药物在声动力治疗与气体治疗以及免疫疗法的肿瘤联合治疗中的应用。所述的抗肿瘤方面包括重塑种瘤微环境促进免疫细胞浸润、原位胰腺癌的治疗以及抑制肿瘤转移和侵袭。
19、结果如下:
20、(1)uv-vis测试结果
21、参考说明书附图2,本发明制备的spnh、spnhi和spnhih在540nm和处390nm处分别存在光敏剂pfodbt和h2sdoner的表面等离子体共振峰,spnhih在280nm处包含了nlg919和haase两者的峰,所以spnhih在280nm处的峰值明显高于spnh和spnhi。由此可见,pfodbt、h2sdoner和nlg919已成功包被在纳米颗粒中,haase也被顺利接上。
22、(2)水合动力学直径及zeta电势测试结果
23、参考说明书附图3a-3b,分别为spnh、spnhi和spnhih的水动力学粒径和表面电势情况。动态光散射测量表明,制备的spnh、spnhi和spnhih水动力学粒径分别为39.5nm、40.9nm和46.4nm,呈现增加趋势。它们表现出相似的负表面,zeta电位在-33.6至-22.0mv之间。
24、(3)透射电子显微镜测试结果
25、参考说明书附图4,spnh、spnhi和spnhih全部呈现尺寸均匀且分散性良好的球形形态,spnhih因外接了透明质酸酶,相较于spnh、spnhi的粒径更大。
26、(4)纳米免疫药物的nlg919释放测试结果
27、参考说明书附图5a-5b,在超声0min、5min、10min、15min以及20min时间下的药物释放百分比分别为1%、47%、67%、86%和91%,结果表明超声时间越长,nlg919的释放越充分,说明该纳米材料具有优良的可控释放效果。
28、(5)细胞毒性测试结果
29、参考说明书附图6,在spnh、spnhi和spnhih浓度分别为0μg/ml、3.125μg/ml、6.25μg/ml、12.5μg/ml、25μg/ml以及50μg/ml的条件下与4t1细胞共孵育24h,细胞存活率均在90%以上,说明spnh、spnhi和spnhih三种材料对细胞几乎没有毒性。(6)3d细胞球渗透测试结果
30、参考说明书附图7所示,通过构建三维多细胞肿瘤球体,研究纳米颗粒的渗透能力。spnh和spnhi组在150μm处可以观察到纳米颗粒的红色荧光信号,而spnhih处理组在120μm深度处仍能检测到红色荧光信号。且在相同深度下,spnhih处理组的荧光强度远高于spnh和spnhi组,spnhih荧光强度定量是spnh和spnhi组的1.7倍左右,表现出优异的渗透效果。
31、(7)单线态氧生成量检测结果
32、参考说明书附图8所示,使用超声波治疗仪对spnh、spnhi和spnhih进行超声(1.0w/cm2),然后加入单线态氧绿色荧光探针检测单线态氧的生成情况。如图所示,使用超声治疗仪超声5min后,spnh和spnhi组出现了明显的荧光,说明有单线态氧生成,spnhih组的单线态氧生成能力更强,荧光强度是spnh和spnhi的3.2倍,具有出色的光动力治疗效果。
33、(8)[ru(dpp)3]cl2氧指示探针检测结果
34、参考说明书附图9所示,由于肿瘤微环境呈现乏氧状态,pbs–超声组和pbs+超声组中[ru(dpp)3]cl2氧指示探针没有发生猝灭;spnh–超声和spnhi–超声组由于产生了h2s,h2s气体通过抑制线粒体呼吸链中的细胞色素氧化酶阻断线粒体呼吸,从而使肿瘤微环境中的氧气含量增多,使部分[ru(dpp)3]cl2氧指示探针发生了猝灭;spnhih–超声组由于透明质酸酶的存在,重塑了肿瘤微环境更有利于药物渗透,能够使肿瘤细胞吞噬更多的药物,氧气含量增加最为明显,故探针颜色最弱。spnh+超声和spnhi+超声组进行超声治疗,消耗部分氧气转化为成单线态氧,从而使探针颜色高于spnh–超声和spnhi–超声组;spnhih+超声组的渗透更强,消耗的氧气也最多,所以探针颜色更为明显。
35、(9)药物富集荧光成像
36、参考说明书附图10所示,建立c57bl/6小鼠胰腺癌原位瘤模型,随机分为5组(n=3),分别注射spnh、spnhi和spnhih(0.2ml、0.3mg/ml)的pbs溶液。在注射后0、4、8、12、24和36小时,分别使用激发和发射波长分别为520和700nm的ivis光谱成像系统对小鼠进行实时荧光成像。spnh、spnhi和spnhih分别注射到小鼠体内后,肿瘤区域的荧光强度随时间累计逐渐增加,并在注射后24h达到最大值,采用livingimage4.3软件测量肿瘤区域的荧光强度,结果表明,在24h时,spnhih组的荧光强度是spnh和spnhi的1.46倍,表明纳米粒子有效地聚集到肿瘤中。
37、(10)小鼠存活率及体重监测结果
38、将spnh、spnhi和spnhih分别经尾静脉注射到小鼠体内,待注射24h后,进行超声治疗。参考说明书附图11-a所示,治疗42天后,spnhih+超声组小鼠存活率仍为100%,远高于其他分组。参考说明书附图11-b所示,体重均呈现稳定增加趋势,无异常情况。
39、本发明采用上述技术方案,与现有技术相比具有如下优点:
40、(1)本发明制备方法简易,主体材料获得途径便捷,生物安全性好;
41、(2)本发明有效降解肿瘤细胞的细胞外基质,重塑肿瘤微环境,增强免疫细胞浸润;
42、(3)本发明使用材料新颖,并通过级联反应增强联合治疗效果,实现药物疗效最大化;
43、(4)本发明包裹的药物具有控释效果,可以提高药物的安全性、有效性和利用率。
- 还没有人留言评论。精彩留言会获得点赞!