一种提高球囊表面药物利用率的方法及制备的球囊与流程
本发明涉及医药,尤其涉及一种提高球囊表面药物利用率的方法及制备的球囊。
背景技术:
1、随着经济社会的发展,医药行业也在快速发展,人们对于医疗器械的需求和要求也越来越高,尤其是药械组合产品。以医疗器械作用为主的药械组合产品(本指导原则简称为药械组合医疗器械),预期可能使产品在疾病的预防、治疗等过程中更加安全和有效。微创介入手术为治疗动脉粥样硬化提供了替代方法,且由于其通常引起的并发症较少,可更快痊愈,相对于开放式手术相对便宜,逐渐成为患者及医生的首选。
2、传统经皮腔内血管成形术(pta)治疗中,医生以pta球囊治疗血管狭窄或阻塞。pta球囊的主要缺点是短期再狭窄的几率很高。尽管支架植入术的长期通畅率较pta球囊高,但患者亦受到常见并发症的困扰,如血栓形成、支架断裂,以及因新生内膜增生引起的支架内再狭窄(isr)。药物涂覆球囊治疗为一种创新的治疗方法,使用涂覆抗增殖药物的血管成形术球囊。与pta球囊相比,涂在球囊上的药物可有效抑制新生内膜增生,从而减少晚期管腔丢失及再狭窄。与支架植入术相比,药物涂覆球囊治疗可显著降低血栓形成的风险,避免支架断裂及支架内再狭窄,更重要的是,在人体中实现了介入无植入的价值主张。
3、药物涂覆球囊表面一般涂覆内皮细胞抗增殖药物和涂层,涂层可以减少输送过程中的药物损失,协助药物快速有效地释放到血管壁内,持续抑制内膜增生,避免血管再狭窄。
4、目前市场上的药物涂覆球囊25%~35%的药物会损失在球囊输送过程中,球囊扩张时药物损失约20%,球囊回撤时药物损失约10%~20%,与血管接触的药物损失约10%~20%,球囊扩张进入血管组织的药物仅有5%~15%左右。大量脱落的药物颗粒在下游可能导致栓塞,导致下游血管萎缩,更有甚者可能导致介入治疗后血流缓慢流动或围手术期心肌梗死。
5、此外,目前的药物球囊普遍存在药物利用率低的问题,体外硅胶中的模拟吸收仅3.15%±0.78%(药物涂层球囊药物释放和微粒脱落的体外评估方法[j]. 中国医疗器械杂志, 2017, 41(2):4)。
6、提高药物利用率,降低扩张及回撤过程中脱落至血管中的药物是目前亟需解决的问题。
7、目前已有的提高药物利用率的方法主要有两种:一种是处理药物涂层,因球囊表面已涂覆药物,处理时需避免直接接触药物涂层;因球囊比较细长,球囊部分容易晃动,湿的涂层容易碰壁,造成涂层损坏,这种涂层处理方法对操作要求高,不易实现;第二种是配制过饱和药物溶液并多次喷涂,过饱和溶液是一种非稳定态溶液,药物很容易结晶析出,很难维持溶液过饱和状态,而且过饱和紫杉醇溶液在喷涂过程中极易堵塞管路,实际操作难度极高。
技术实现思路
1、有鉴于此,本发明要解决的技术问题在于提供一种提高球囊表面药物利用率的方法及制备的球囊,本发明提供的方法操作简便,且有效提高了球囊表面药物的利用率。
2、为达到上述目的,本发明提供了一种提高球囊表面药物利用率的方法,包括以下步骤:
3、s1)采用溶剂对球囊表面进行处理并干燥;
4、s2)使干燥后的球囊与含药溶液接触,在球囊表面形成药物涂层;
5、s3)对形成药物涂层后的球囊进行溶剂蒸汽处理。
6、本发明在形成药物涂层之前对裸球囊进行溶剂处理,可大幅提高药物吸收率,体外模拟吸收率由目前的约3%提升至30%,吸收率提高约10倍。该现象是因为溶剂表面处理裸球囊后,使原本干燥的裸球囊表面残留了微量溶剂,在药物喷涂后,这部分溶剂覆盖在药物涂层以下,延长了溶剂挥发的时间,使药物结晶的时间更长,结晶结构更加完善,降低了原有的球囊与涂层之间的结合力,大幅提高药物吸收率;再经过溶剂蒸汽处理后,形成的晶体尺寸更小,扩张产生的小粒径药物微粒占比更多,尺寸小更利于吸收,也提高了药物吸收率。
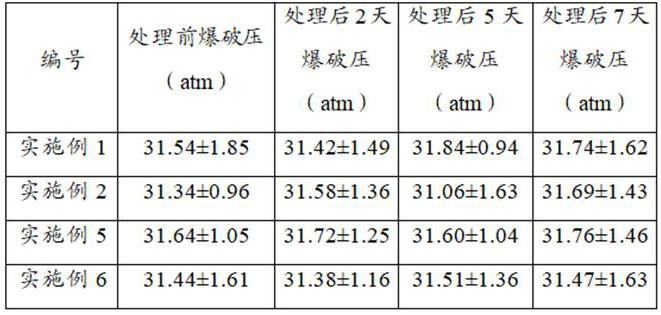
7、优选的,所述步骤s1)中的溶剂选自甲醇、乙醇、丙醇、丁醇、丙酮、乙酸乙酯、四氢呋喃中的任意一种或多种,更优选为甲醇、乙醇、丙醇、丁醇中的任意一种或多种,上述溶剂,尤其是醇类溶剂不会对球囊表面造成损伤,不影响球囊的理化性能,爆破压及疲劳性能不会产生变化。
8、优选的,所述溶剂还可含有一定的水分,水分含量优选为0~20%。水分的添加可进一步降低涂层牢固度。
9、优选的,所述采用溶剂对球囊表面进行处理的温度为-10~40℃,更优选为20~25℃;时间优选为1s~24h,更优选为5s~1h。
10、本发明对采用溶剂对球囊表面进行处理的方法并无特殊限定,使溶剂与球囊表面接触即可,优选的方式为喷涂、液滴、浸泡、湿布擦拭中的任意一种或多种。
11、溶剂处理球囊表面后进行干燥处理。
12、本发明对干燥的方法并无特殊限定,去除球囊表面的溶剂即可,优选的干燥方式为真空干燥、烘干、自然晾干、吹干、擦干中的任意一种或多种。
13、所述真空干燥的温度优选为-10~40℃,更优选为20~25℃。
14、所述烘干的温度优选为-10~40℃,更优选为20~25℃。
15、自然晾干、吹干、擦干的温度为室温即可。
16、所述干燥的时间优选为1s~1h,更优选为10s~1h。
17、然后使干燥后的球囊与含药溶液接触,在球囊表面形成药物涂层。本发明对上述干燥后的球囊与含药溶液接触的方法并无特殊限定,可以为本领域技术人员熟知的喷涂药物涂层的方法,优选为超声喷涂、微液滴、浸涂中的任意一种或多种,更优选为超声喷涂,超声喷涂形成的涂层更为均匀,涂层牢固度更高。
18、本发明对上述药物的种类并无特殊限定,现有适用于球囊表面喷涂的药物均可,在本发明的一些具体实施例中,所述药物为紫杉醇药物,药物浓度优选为1wt%~3wt%。溶剂可以选自乙醇、甲醇、异丙醇、丙酮等中的一种或几种混合。
19、然后对形成药物涂层后的球囊进行溶剂蒸汽处理,使药物溶解再析出形成新的药物晶体。
20、本发明溶剂蒸汽处理采用的装置为不完全密封的装置,优选的所述装置设置有开孔。
21、在本发明的一些具体实施例中,采用的装置如图1所示。其包括一个设置有开孔的容器,所述容器的形状不限,包括但不限于立方体、长方体、圆柱体等。容器中设置有敞口的溶剂盛放装置,例如烧杯、烧瓶等,用于溶剂的挥发。在具体操作过程中,优选将球囊置于溶剂盛放装置上方且不接触。
22、本发明将喷涂后的药物球囊置于含有溶剂的不密封容器中进行溶剂蒸气处理,溶剂挥发产生的蒸气会重新溶解药物涂层,溶剂从不密封容器中逐步挥发,容器内的溶剂含量逐步减少,溶解的药物涂层逐步析出,形成新的药物晶体。新形成的药物晶体结晶更充分,形成了双晶体结构,晶体结构更完善,可以延长药物代谢时间,使药效更持久。同时,本处理装置简便,加工方便,易于操作。
23、开孔容器的孔大小会影响溶剂含量的变化速度,进而影响药物涂层结构,优选的,所述开孔的总面积与装置的体积的比例为1cm2:(5~1000)cm3,更优选为1cm2:(50~1000)cm3。所述开孔的数量无需限定,可以为1个、2个、3个、4个或更多,总面积满足上述比例即可。所述开孔的形状无需限定,包括但不限于圆形、椭圆形、三角形、四边形、其他多边形等。所述开孔的位置无需限定,可位于容器的顶部、任一侧壁或分布于多个侧壁等。
24、作为本发明的另一种实施方式,上述开孔设置为可打开可闭合的开孔,在进行溶剂蒸汽处理时,先闭合开孔使容器密闭一段时间,再打开开孔使溶剂挥发进行溶剂蒸气处理,密闭时间可选的为0-4h。
25、所述溶剂蒸汽处理的溶剂优选为甲醇、乙醇、丙醇、异丙醇、丁醇等中的一种或几种混合。
26、上述溶剂中还可含有一定的水分,水分含量优选为0.01%~60%(质量百分比),更优选为1%~20%。水的加入有助于形成新的药物晶体,例如紫杉醇·2h2o 晶体。
27、所述溶剂蒸汽处理的时间优选为1~48h,1~24h。
28、所述溶剂蒸汽处理的温度优选为-10~40℃,更优选为20℃~40℃。
29、本发明还提供了上述方法制备的药物涂覆球囊。
30、所述球囊表面涂覆的药物具有较高的结晶程度,其166℃的焓值大于7j/g,更优选大于9j/g。
31、与现有技术相比,本发明提供了一种提高球囊表面药物利用率的方法,包括以下步骤:s1)采用溶剂对球囊表面进行处理并干燥;s2)使干燥后的球囊与含药溶液接触,在球囊表面形成药物涂层;s3)对形成药物涂层后的球囊进行溶剂蒸汽处理。本发明通过巧妙的溶剂预处理,改变了球囊的理化性能,改善了药物涂层的结晶性能,使球囊与药物涂层之间具有适宜的结合力,大幅提高药物吸收率,涂层牢固度与吸收率达到了较好的平衡点。在血管内输送过程、球囊扩张过程和球囊回撤过程中,保证药物涂层在球囊上有足够的牢固度,药物损失少;同时,在扩张过程中,改善结晶后的药物有利于组织吸收。该方法简便易行,操作简便,易于实际规模化生产,可大幅提升药物涂覆医疗器械的药物吸收率。
- 还没有人留言评论。精彩留言会获得点赞!