喷雾干燥的分散体和制剂的制作方法
本公开涉及式i化合物,或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体(sdd)或其药物组合物。更具体地,其涉及式i化合物的组合物,其可用于治疗和预防可用btk抑制剂治疗的疾病,包括btk相关疾病和病症。
背景技术:
1、btk是一种属于tec家族激酶的细胞质的、非受体酪氨酸激酶(herman,s.e.m.等人,blood.2011,117(23):6287–6296)。btk的结构具有几个结构域:n-末端普列克底物蛋白同源(ph)结构域、富含脯氨酸的tec同源结构域、两个src同源结构域(sh3,随后是sh2)和c-末端激酶结构域(btk-kd)(marcotte,d.j.等人,protein sci.2010,19(3):429–439)。
2、btk在造血细胞中表达,不包括t细胞和浆细胞,并且参与b细胞发育的所有方面,包括增殖、成熟、分化、凋亡和细胞迁移(wu j.,等人,j hematol oncol.2016;9:80)。btk还在特定的骨髓细胞中表达,包括单核细胞/巨噬细胞、嗜中性粒细胞和肥大细胞。在这些骨髓细胞中,btk已经被指示在免疫复合物介导的fcγr和fcεr的激活中,其可能有助于类风湿性关节炎的发病机理(whang 2014)。破骨细胞的成熟也需要btk,因此抑制btk可以预防与类风湿性关节炎相关的骨侵蚀。
3、pip3(磷脂酰肌醇-3,4,5-三磷酸)的产生和与btk的ph结构域的结合以及src家族激酶对btk的tyr-551的磷酸化刺激btk的膜定位和激活。btk的激活导致ca2+动员和nf-κb和map(促分裂原活化蛋白)激酶通路的激活(honigberg等人proc.natl.acad.sci.u.s.a.2010jul 20;107(29):13075–13080)。
4、在不同的癌症和自身免疫性病症中已经证实了异常的btk表达和/或活性。
5、btk抑制剂的实例公开于wo17/103661中。
6、需要提供用于btk抑制剂的改进制剂,特别是用于表现出低溶解度的btk抑制剂的改进制剂。此外,需要提供制剂以增加btk抑制剂的血浆浓度和/或提供一致的血浆浓度。本发明提供了满足这些需要中的一种或多种的各种制剂。
技术实现思路
1、在一种形式中,本发明提供了药物组合物,其包含以约5%w/w至约30%w/w的量存在的式i化合物;
2、
3、以约5%w/w至约30%w/w的量存在的hpmcas聚合物;以约30%w/w至约60%w/w的量存在的微晶纤维素;以约10%w/w至约60%w/w的总量存在的甘露醇或乳糖一水合物或其组合;以约0.5%w/w至约5%w/w的总量存在的羟基乙酸淀粉钠或交联羧甲基纤维素钠或其组合;和以约0.05%w/w至约2%w/w的量存在的硬脂酸镁;和任选地,存在时含量为约0.3%w/w至约0.6%w/w的二氧化硅,并且其中总量不大于100%。
4、在一种形式中,本发明提供了药物组合物,其包含以约5%w/w至约30%w/w的量存在的式i化合物;以约5%w/w至约30%w/w的量存在的hpmcas聚合物;以约30%w/w至约60%w/w的量存在的微晶纤维素;以约10%w/w至约60%w/w的总量存在的甘露醇或乳糖一水合物或其组合;以约0.5%w/w至约5%w/w的总量存在的羟基乙酸淀粉钠或交联羧甲基纤维素钠或其组合;和以约0.05%w/w至约2%w/w的量存在的硬脂酸镁;和任选地,存在时含量为约0.3%w/w至约0.6%w/w的二氧化硅,并且其中总量不大于100%。
5、在一种形式中,本发明提供了药物组合物,其包含以约5%w/w至约30%w/w的量存在的式i化合物;以约5%w/w至约30%w/w的量存在的hpmcas聚合物;以约30%w/w至约60%w/w的量存在的微晶纤维素;以约10%w/w至约60%w/w的量存在的乳糖一水合物;以约0.5%w/w至约5%w/w的总量存在的交联羧甲基纤维素钠;和以约0.05%w/w至约2%w/w的量存在的硬脂酸镁;和存在时含量为约0.3%w/w至约0.6%w/w的二氧化硅,并且其中总量不大于100%。
6、在一个实施方案中,式i化合物与hpmcas聚合物的比率为约1:4至约4:1。在另一个实施方案中,式i化合物与hpmcas聚合物的比率为约1:1。
7、在另一种形式中,本发明提供了药物组合物,其包含以约21%w/w至约23%w/w的量存在的式i化合物;以约21%w/w至约23%w/w的量存在的hpmcas聚合物;以约38%w/w至约39%w/w的量存在的微晶纤维素;以约12%w/w至约13%w/w的量存在的甘露醇;以约4%w/w至约6%w/w的量存在的羟基乙酸淀粉钠;和以约0.4%w/w至约0.6%w/w的量存在的硬脂酸镁,并且其中总量不大于100%w/w。
8、在另一种形式中,本发明提供了药物组合物,其包含以约21%w/w至约23%w/w的量存在的式i化合物;以约21%w/w至约23%w/w的量存在的hpmcas聚合物;以约33%w/w至约34%w/w的量存在的微晶纤维素;以约16%w/w至约17%w/w的量存在的乳糖一水合物;以约2%w/w至约6%w/w的量存在的交联羧甲基纤维素钠;以约0.4%w/w至约0.6%w/w的量存在的硬脂酸镁;和以约0.4%w/w至约0.6%w/w的量存在的二氧化硅,并且其中总量不大于100%。
9、在另一种形式中,本发明提供了药物组合物,其包含以约21%w/w至约23%w/w的量存在的式i化合物;以约21%w/w至约23%w/w的量存在的hpmcas聚合物;以约25%w/w至约26%w/w的量存在的微晶纤维素;以约25%w/w至约26%w/w的量存在的甘露醇;以约4%w/w至约6%w/w的量存在的羟基乙酸淀粉钠;和以约0.4%w/w至约0.6%w/w的量存在的硬脂酸镁,并且其中总量不大于100%w/w。
10、在又一种形式中,本发明提供了药物组合物,其包含以约8%w/w的量存在的式i化合物;以约8%w/w的量存在的hpmcas聚合物;以约40%w/w的量存在的微晶纤维素;以约40%w/w的量存在的甘露醇;以约3.5%w/w的量存在的羟基乙酸淀粉钠;和以约0.3%w/w的量存在的硬脂酸镁。
11、在一个实施方案中,将如上所述的药物组合物配制成片剂。在另一个实施方案中,药物组合物包含约25mg至约220mg的式i化合物。在又一个实施方案中,药物组合物包含选自以下之一的量的式i化合物:约25mg、约50mg和约100mg。
12、在另一种形式中,本发明提供了用于治疗需要其的对象的btk相关癌症的方法,所述方法包括向所述对象施用如上所述的药物组合物。在一个实施方案中,btk相关癌症选自:套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞性淋巴瘤、瓦尔登斯特伦巨球蛋白血症和边缘区淋巴瘤。
13、在另一种形式中,本发明提供了治疗需要治疗的对象的癌症的方法。该方法包括向所述对象施用剂量为约20mg至约120mg的式i化合物。所述癌症选自以下癌症:套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞性淋巴瘤、瓦尔登斯特伦巨球蛋白血症和边缘区淋巴瘤。在某些实施方案中,所述剂量选自以下之一:约25mg、约50mg和约100mg。
14、在另一种形式中,本发明提供了如上所述的药物组合物用于治疗选自以下的btk相关癌症的用途:套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞性淋巴瘤、瓦尔登斯特伦巨球蛋白血症和边缘区淋巴瘤,其中式i化合物以约20mg至120mg的剂量施用。在某些实施方案中,施用式i化合物的剂量选自以下:约25mg、约50mg和约100mg。
15、在又一种形式中,本发明提供了用于治疗选自以下的btk相关癌症的如上所述的药物组合物:套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞性淋巴瘤、瓦尔登斯特伦巨球蛋白血症和边缘区淋巴瘤。在某些实施方案中,以选自以下之一的剂量施用式i化合物:约25mg、约50mg和约100mg。
16、在其它形式中,本发明提供了式i化合物:
17、
18、所述式i化合物在其喷雾干燥的分散体或其药物组合物中,可用于治疗和预防可用btk抑制剂治疗的疾病,包括btk相关的疾病和病症。
19、因此,本文提供了包含式i化合物和醋酸羟丙甲纤维素琥珀酸酯(hpmcas)聚合物的喷雾干燥的分散体。
20、在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式与hpmcas聚合物的比率为约1:4至约4:1。在一些实施方案中,式i化合物与hpmcas聚合物的比率为约1:1。在一些实施方案中,hpmcas聚合物是hpmcas-mg。
21、本文还提供了制备喷雾干燥的分散体的方法,其中在喷雾干燥之前将式i化合物溶解在一种或多种有机溶剂中。在一些实施方案中,在喷雾干燥之前将式i化合物或其药学上可接受的盐、无定形或多晶型物形式溶解在优选比率为约80:20wt/wt二氯甲烷:甲醇的二氯甲烷:甲醇中。在其它实施方案中,将式i化合物溶解在甲醇中。在仍其它实施方案中,将式i化合物的形式a溶解在一种或多种有机溶剂中。
22、本文还提供了一种药物组合物,其包含:包含喷雾干燥的分散体和一种或多种药物赋形剂的第一组合物,其中所述喷雾干燥的分散体包含hpmcas聚合物和式i化合物或其药学上可接受的盐、无定形或多晶型物形式。
23、在一些实施方案中,在喷雾干燥的分散体中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式与hpmcas聚合物的比率为约1:4至约4:1。在一些实施方案中,在喷雾干燥的分散体中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式与hpmcas聚合物的比率为约1:1。在一些实施方案中,hpmcas聚合物是hpmcas-mg。
24、在一些实施方案中,喷雾干燥的分散体以第一组合物的约20%至约75%w/w的量存在。在一些实施方案中,喷雾干燥的分散体以第一组合物的约30%至约60%w/w的量存在。在一些实施方案中,喷雾干燥的分散体以第一组合物的约40%至约50%w/w的量存在。在一些实施方案中,喷雾干燥的分散体以第一组合物的约45%w/w的量存在。
25、在一些实施方案中,药物赋形剂选自:填料、润滑剂及其组合。
26、在一些实施方案中,填料以第一组合物的约25%至约80%w/w的量存在。在一些实施方案中,填料以第一组合物的约45%至约65%w/w的量存在。在一些实施方案中,填料以第一组合物的约55%w/w的量存在。
27、在一些实施方案中,所述填料选自:糖、明胶、合成聚合物或其组合。在一些实施方案中,填料选自:蔗糖、乳糖、微晶纤维素、甲基纤维素、乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、淀粉、木糖醇、山梨醇、甘露醇、聚乙烯吡咯烷酮、聚乙二醇、聚乙烯醇、聚甲基丙烯酸酯、泊洛沙姆、硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。
28、在一些实施方案中,填料是粘合剂、崩解剂或其组合。
29、在一些实施方案中,粘合剂以第一组合物的约30%至约80%w/w的量存在。在一些实施方案中,粘合剂以第一组合物的约40%至约60%w/w的量存在。在一些实施方案中,其中粘合剂以第一组合物的约52%w/w的量存在。
30、在一些实施方案中,粘合剂选自:微晶纤维素、纤维素醚、羟丙基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠、淀粉、甲基纤维素、乙基纤维素、羟丙基纤维素、甘露醇、木糖醇、山梨醇、乳糖、蔗糖、山梨醇、明胶、聚乙烯吡咯烷酮、聚乙二醇、聚乙烯醇、聚甲基丙烯酸酯及其组合。
31、在一些实施方案中,粘合剂是微晶纤维素、甘露醇或其组合。
32、在一些实施方案中,微晶纤维素以第一组合物的约5%至约55%w/w的量存在。在一些实施方案中,微晶纤维素以第一组合物的约10%至约40%w/w的量存在。在一些实施方案中,微晶纤维素以第一组合物的约20%至约30%w/w的量存在。在一些实施方案中,微晶纤维素以第一组合物的约30%至约60%w/w的量存在。在一些实施方案中,微晶纤维素以第一组合物的约26%w/w的量存在。
33、在一些实施方案中,甘露醇以第一组合物的约5%至约55%w/w的量存在。在一些实施方案中,甘露醇以第一组合物的约10%至约40%w/w的量存在。在一些实施方案中,甘露醇以第一组合物的约20%至约30%w/w的量存在。在一些实施方案中,甘露醇以第一组合物的约26%w/w的量存在。
34、在一些实施方案中,崩解剂以第一组合物的约0.5%至约5%w/w的量存在。在一些实施方案中,崩解剂以第一组合物的约1.5%至约3.5%w/w的量存在。在一些实施方案中,崩解剂以第一组合物的约2.5%w/w的量存在。
35、在一些实施方案中,崩解剂选自:羟基乙酸淀粉钠、海藻酸、海藻酸钠、交联羧甲基纤维素钠、阴离子交换树脂及其组合。在一些实施方案中,崩解剂是羟基乙酸淀粉钠。
36、在一些实施方案中,润滑剂以第一组合物的约0.05%至约2.5%w/w的量存在。在一些实施方案中,润滑剂以第一组合物的约0.1%至约1%w/w的量存在。在一些实施方案中,润滑剂以第一组合物的约0.25%w/w的量存在。
37、在一些实施方案中,润滑剂选自:硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、聚乙二醇、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。在一些实施方案中,润滑剂是硬脂酸镁。
38、在一些实施方案中,喷雾干燥的分散体以第一组合物的约20%至约75%w/w的量存在,填料以第一组合物的约25%至约80%w/w的量存在,并且润滑剂以第一组合物的约0.05%至约2%w/w的量存在。
39、在一些实施方案中,喷雾干燥的分散体以第一组合物的约45%w/w的量存在,填料以第一组合物的约55%w/w的量存在,并且润滑剂以第一组合物的约0.25%w/w的量存在。
40、在一些实施方案中,喷雾干燥的分散体以第一组合物的约40%至约50%w/w的量存在,微晶纤维素以第一组合物的约20%至约30%w/w的量存在,甘露醇以第一组合物的约20%至约30%w/w的量存在,羟基乙酸淀粉钠以第一组合物的约0.5%至约5%w/w的量存在,并且硬脂酸镁以第一组合物的约0.05%至约2%w/w的量存在。
41、在一些实施方案中,其中将喷雾干燥的分散体和药物赋形剂掺合。在一些实施方案中,将第一组合物造粒。在一些实施方案中,通过碾压将第一组合物造粒。
42、本文还提供了包含第一组合物和一种或多种药物赋形剂的药物组合物。
43、在一些实施方案中,第一组合物以总组合物的约15%至约99%w/w的量存在。
44、在一些实施方案中,所述一种或多种药物赋形剂选自:填料、润滑剂及其组合。
45、在一些实施方案中,润滑剂以总组合物的约0.05%至约2%w/w的量存在。在一些实施方案中,润滑剂以总组合物的约0.1%至约1.0%w/w的量存在。在其它实施方案中,润滑剂以总组合物的约0.1%至约0.8%w/w的量存在。在其它实施方案中,润滑剂以总组合物的约0.4%至约0.6%w/w的量存在。在另外的实施方案中,润滑剂以总组合物的约0.3%w/w的量存在。
46、在一些实施方案中,润滑剂选自:硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、聚乙二醇、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。在一些实施方案中,润滑剂是硬脂酸镁。
47、在一些实施方案中,填料以总组合物的约1%至约85%w/w的量存在。
48、在一些实施方案中,填料选自:蔗糖、乳糖、微晶纤维素、甲基纤维素、乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、淀粉、木糖醇、山梨醇、甘露醇、聚乙烯吡咯烷酮、聚乙二醇、聚乙烯醇、聚甲基丙烯酸酯、泊洛沙姆、硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。
49、在一些实施方案中,其中填料是粘合剂、崩解剂或其组合。
50、在一些实施方案中,崩解剂以总组合物的约0.5%至约5%w/w的量存在。在一些实施方案中,崩解剂以总组合物的约4%至约6%w/w的量存在。在一些实施方案中,崩解剂以总组合物的约2.5%w/w的量存在。
51、在一些实施方案中,崩解剂选自:羟基乙酸淀粉钠、海藻酸、海藻酸钠、交联羧甲基纤维素钠、阴离子交换树脂及其组合。在一些实施方案中,崩解剂是羟基乙酸淀粉钠。
52、在一些实施方案中,第一组合物以总组合物的约90%至约99%w/w的量存在。在一些实施方案中,第一组合物以总组合物的约97%w/w的量存在。
53、在一些实施方案中,第一组合物以总组合物的约15%至约60%w/w的量存在。在一些实施方案中,第一组合物以总组合物的约30%至约40%w/w的量存在。在一些实施方案中,第一组合物以总组合物的约35%w/w的量存在。
54、在一些实施方案中,粘合剂以总组合物的约40%至约85%w/w的量存在。在一些实施方案中,粘合剂以总组合物的约55%至约75%w/w的量存在。
55、在一些实施方案中,粘合剂选自:微晶纤维素、纤维素醚、羟丙基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠、淀粉、纤维素、甲基纤维素、乙基纤维素、羟丙基纤维素、甘露醇、木糖醇、山梨醇、乳糖、蔗糖、山梨醇、明胶、聚乙烯吡咯烷酮、聚乙二醇、聚乙烯醇、聚甲基丙烯酸酯及其组合。
56、在一些实施方案中,粘合剂是微晶纤维素、甘露醇或其组合。
57、在一些实施方案中,微晶纤维素以总组合物的约25%至约35%w/w的量存在。在一些实施方案中,微晶纤维素以总组合物的约31%w/w的量存在。
58、在一些实施方案中,甘露醇以总组合物的约25%至约35%w/w的量存在。在一些实施方案中,甘露醇以总组合物的约31%w/w的量存在。
59、在一些实施方案中,将第一组合物与药物赋形剂掺合。在一些实施方案中,将药物组合物共碾磨。
60、在一些实施方案中,药物组合物被配制成片剂。在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式以约10mg至约50mg的量存在。在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式以约25mg至约220mg的量,更优选约50mg至约150mg的量,还更优选约80mg至约120mg的量,在还更优选的实施方案中以约100mg的量存在。
61、本文还提供了药物组合物,其中所述药物组合物包含:
62、(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
63、hpmcas聚合物;和
64、一种或多种药物赋形剂。
65、在一些实施方案中,hpmcas聚合物是hpmcas-mg。
66、在一些实施方案中,一种或多种药物赋形剂选自:填料、润滑剂及其组合。
67、在一些实施方案中,填料选自:蔗糖、乳糖、微晶纤维素、甲基纤维素、乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、淀粉、木糖醇、山梨醇、甘露醇、聚乙烯吡咯烷酮、聚乙二醇、聚乙烯醇、聚甲基丙烯酸酯、硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。
68、在一些实施方案中,润滑剂选自:硬脂酸镁、硬脂酸钙、硬脂酸钠、硬脂酸、氢化植物油、矿物油、聚乙二醇、月桂基硫酸钠、月桂基硫酸镁、棕榈酸硬脂酸甘油酯、苯甲酸钠、硬脂富马酸钠、胶体二氧化硅、苯甲酸钠、油酸钠、乙酸钠及其组合。
69、在一些实施方案中,组合物包含:
70、(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
71、hpmcas聚合物;
72、微晶纤维素;
73、甘露醇;
74、羟基乙酸淀粉钠;和
75、硬脂酸镁。
76、在一些实施方案中,组合物包含:
77、以组合物的约5%至约30%w/w的量存在的(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
78、以组合物的约5%至约30%w/w的量存在的hpmcas聚合物;
79、以组合物的约30%至约60%w/w的量存在的微晶纤维素;
80、以组合物的约30%至约60%w/w的量存在的甘露醇;
81、以组合物的约0.5%至约5%w/w的量存在的羟基乙酸淀粉钠;和
82、以组合物的约0.05%至约2%w/w的量存在的硬脂酸镁。
83、在一些实施方案中,组合物包含:
84、以组合物的约8%w/w的量存在的(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
85、以组合物的约8%w/w的量存在的hpmcas聚合物;
86、以组合物的约40%w/w的量存在的微晶纤维素;
87、以组合物的约40%w/w的量存在的甘露醇;
88、以组合物的约3.5%w/w的量存在的羟基乙酸淀粉钠;和
89、以组合物的约0.3%w/w的量存在的硬脂酸镁。
90、在一些实施方案中,组合物包含:
91、以组合物的约10%至约30%w/w的量存在的(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
92、以组合物的约10%至约30%w/w的量存在的hpmcas聚合物;
93、以组合物的约20%至约30%w/w的量存在的微晶纤维素;
94、以组合物的约20%至约30%w/w的量存在的甘露醇;
95、以组合物的约2%至约8%w/w的量存在的羟基乙酸淀粉钠;和
96、以组合物的约0.05%至约2%w/w的量存在的硬脂酸镁。
97、在一些实施方案中,本文中的组合物包含:
98、以组合物的约22%w/w的量存在的(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺;
99、以组合物的约22%w/w的量存在的hpmcas聚合物;
100、以组合物的约25%w/w的量存在的微晶纤维素;
101、以组合物的约25%w/w的量存在的甘露醇;
102、以组合物的约5%w/w的量存在的羟基乙酸淀粉钠;和
103、以组合物的约0.5%w/w的量存在的硬脂酸镁。
104、在一些实施方案中,hpmcas聚合物是hpmcas-mg。
105、在一些实施方案中,药物组合物被配制成片剂。在一些实施方案中,将所述片剂包衣。
106、本文还提供了制备所述药物组合物的方法,包括:
107、将(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺、hpmcas聚合物和有机溶剂混合以形成混合物;
108、将所述混合物喷雾干燥以形成喷雾干燥的分散体;和
109、将所述喷雾干燥的分散体造粒以形成第一组合物。
110、在一些实施方案中,有机溶剂是二氯甲烷和甲醇的混合物。在一些实施方案中,有机溶剂是80:20二氯甲烷:甲醇。在一些实施方案中,在造粒之前,将喷雾干燥的分散体与一种或多种药物赋形剂掺合。在一些实施方案中,在造粒之前,将喷雾干燥的分散体在烘箱中干燥。在一些实施方案中,在造粒之前,将喷雾干燥的分散体与一种或多种药物赋形剂掺合。在一些实施方案中,通过碾压将喷雾干燥的分散体造粒。在一些实施方案中,其中第一组合物与一种或多种药物赋形剂掺合。在一些实施方案中,将第一组合物共碾磨。在一些实施方案中,将第一组合物压制成片剂。在一些实施方案中,将所述片剂包衣。在一些实施方案中,所述包衣包含聚合物、增塑剂、颜料或其组合。
111、在一些实施方案中,在喷雾干燥的分散体中(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺与hpmcas聚合物的比率为约1:4至约4:1。在一些实施方案中,在喷雾干燥的分散体中(s)-5-氨基-3-(4-((5-氟-2-甲氧基苯甲酰胺基)甲基)苯基)-1-(1,1,1-三氟丙-2-基)-1h-吡唑-4-甲酰胺与hpmcas聚合物的比率为约1:1。在一些实施方案中,hpmcas聚合物是hpmcas-mg。
112、本文还提供了具有下式的式i化合物的结晶形式
113、
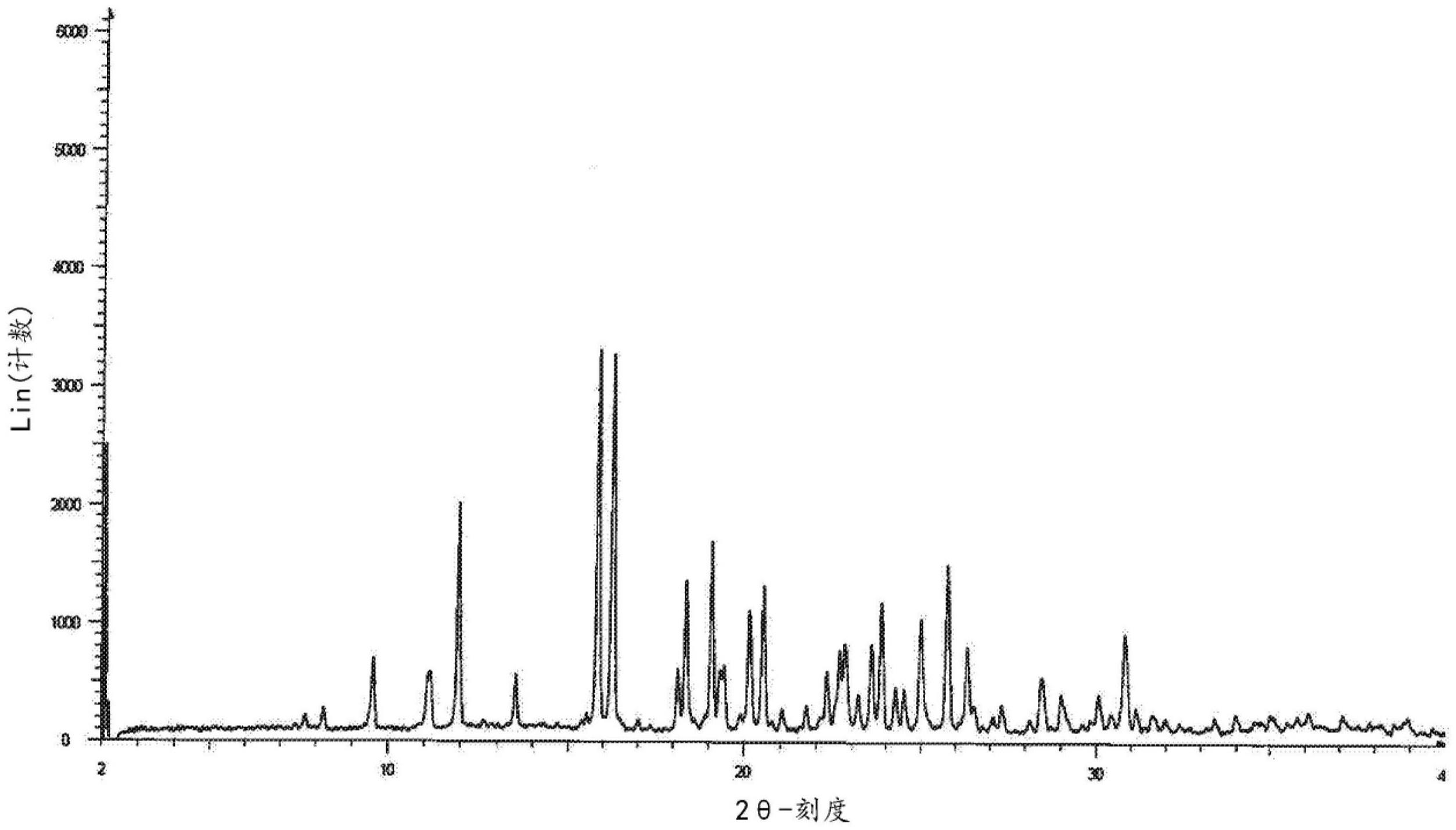
114、本文还提供了式i化合物的形式a,其特征在于具有包含在15.8±0.2、16.2±0.2和11.9±0.2的°2θ值处的峰的x射线粉末衍射(xrpd)图。
115、本文还提供了式i化合物的形式a,其特征在于具有包含在15.8±0.2、16.2±0.2、11.9±0.2、19.0±0.2和18.3±0.2的°2θ值处的峰的x射线粉末衍射(xrpd)图。
116、本文还提供了式i化合物的形式a,其特征在于具有包含在15.8±0.2、16.2±0.2、11.9±0.2、19.0±0.2、18.3±0.2、23.8±0.2和20.5±0.2的°2θ值处的峰的x射线粉末衍射(xrpd)图。
117、本文还提供了式i化合物的形式a,其特征在于具有包含在15.8±0.2、16.2±0.2、11.9±0.2、19.0±0.2、18.3±0.2、23.8±0.2、20.5±0.2、25.7±0.2、20.1±0.2和9.5±0.2的°2θ值处的峰的x射线粉末衍射(xrpd)图。
118、本文还提供了式i化合物的形式a,其特征在于具有包含在15.8±0.2、16.2±0.2、11.9±0.2、19.0±0.2、18.3±0.2、23.8±0.2、20.5±0.2、25.7±0.2、20.1±0.2、9.5±0.2、25.0±0.2和11.1±0.2的°2θ值处的峰的x射线粉末衍射(xrpd)图。
119、本文还提供了式i化合物的形式a,其具有基本上如图4a所示的xrpd图。
120、本文还提供了式i化合物的形式a,其具有包含起始约185℃的吸热的差示扫描量热法(dsc)曲线。
121、本文还提供了式i化合物的形式a,其具有基本上如图4c所示的dsc热谱图。
122、本文还提供了包含药物赋形剂和式i化合物的结晶形式的固体口服药物组合物。
123、本文还提供了通过将式i化合物的结晶形式与药物赋形剂混合而制备的固体口服药物组合物。
124、本文还提供了制备固体口服药物组合物的方法,包括将式i化合物的结晶形式和药物赋形剂混合。
125、本文还提供了治疗需要其的对象的癌症的方法,所述方法包括施用喷雾干燥的分散体、药物组合物或治疗有效量的式i化合物。在一些实施方案中,所述癌症是btk相关癌症。
126、本文还提供了治疗需要其的对象的癌症的方法,所述方法包括:
127、(a)检测btk基因、btk激酶或它们中任一种的表达或活性或水平的失调;以及
128、(b)向所述对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
129、本文还提供了治疗对象的btk相关癌症的方法,所述方法包括向被鉴定或诊断为具有btk相关癌症的对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
130、本文还提供了治疗对象的btk相关癌症的方法,所述方法包括:
131、检测btk基因、btk激酶或它们中任一种的表达或活性或水平的失调;以及
132、向确定具有btk相关癌症的对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
133、本文还提供了治疗对象的方法,所述方法包括向具有指示对象具有btk基因、btk激酶或它们中任一种的表达或活性或水平的失调的临床记录的对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
134、本文还提供了抑制需要其的对象的癌症转移的方法,所述方法包括向所述对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
135、在一些实施方案中,所述癌症是btk相关癌症。
136、在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物与另一化学治疗剂组合使用。
137、此处还提供了为对象选择治疗的方法,所述方法包括为被鉴定或诊断为具有btk相关癌症的对象选择治疗,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
138、本文还提供了为具有癌症的对象选择治疗的方法,所述方法包括:
139、检测对象中btk基因、btk激酶或它们中任一种的表达或活性或水平的失调;以及
140、为对象选择治疗,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
141、此处还提供了为治疗选择对象的方法,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物,所述方法包括:
142、鉴定具有btk相关癌症的对象;以及
143、为治疗选择对象,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
144、本文还提供了为治疗选择具有癌症的对象的方法,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物,所述方法包括:
145、检测对象中btk基因、btk激酶或它们中任一种的表达或活性或水平的失调;以及
146、为治疗选择对象,所述治疗包括施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
147、在一些实施方案中,确定对象中的癌症是否是btk相关癌症的步骤包括进行测定以检测来自对象的样品中btk基因、btk激酶蛋白或它们中任一种的表达或活性或水平的失调。在一些实施方案中,所述方法还包括从对象获得样品。在一些实施方案中,样品是活检样品。在一些实施方案中,所述测定选自测序、免疫组织化学、免疫印迹、酶联免疫吸附测定和荧光原位杂交(fish)。在一些实施方案中,fish是分离fish分析。在一些实施方案中,测序是焦磷酸测序或下一代测序。
148、在一些实施方案中,btk基因、btk激酶蛋白或它们中任一种的表达或活性或水平的失调是bcr信号传导通路基因、bcr(断裂点簇蛋白)信号传导通路蛋白或它们中任一种的表达或活性或水平的失调的结果。
149、在一些实施方案中,bcr信号传导通路基因或bcr信号传导通路蛋白选自:细胞周期蛋白-d1、card11、cd79b、cd79a、myd88及其组合。
150、在一些实施方案中,bcr信号传导通路基因、bcr信号传导通路蛋白或它们中的任一种的表达或活性或水平的失调是一个或多个遗传改变的结果。
151、在一些实施方案中,一个或多个遗传改变选自:染色体易位t(11;14)(q13;q32)、染色体区域17p13的缺失、染色体区域11q23的缺失、染色体区域13q14的缺失和12号染色体三体。
152、在一些实施方案中,一个或多个遗传改变是编码bcr信号传导通路蛋白的基因中的一个或多个点突变。
153、在一些实施方案中,编码bcr信号传导通路蛋白的基因中的一个或多个点突变导致具有一个或多个氨基酸取代的bcr信号传导通路蛋白的翻译,其中bcr信号传导通路蛋白选自:card11、cd79b、cd79a、myd88及其组合。在一些实施方案中,编码bcr信号传导通路蛋白的基因中的一个或多个点突变导致在一个或多个以下氨基酸位置具有一个或多个氨基酸取代的bcr信号传导通路蛋白的翻译:myd88l265。在一些实施方案中,氨基酸取代是myd88l265p。
154、在一些实施方案中,btk基因、btk激酶蛋白或它们中任一种的表达或活性或水平的失调是btk基因中的一个或多个点突变。在一些实施方案中,btk基因中的一个或多个点突变导致在一个或多个以下氨基酸位置具有一个或多个氨基酸取代的btk蛋白的翻译:117、316、474、481、528、560、562和601。在一些实施方案中,btk基因中的一个或多个点突变导致具有一个或多个以下氨基酸取代的btk蛋白的翻译:t117p、t316a、t474i、t474m、t474s、c481s、c481f、c481t、c481g、c481r、l528w、p560l、r562w、r562g和f601l。
155、本文还提供了治疗需要其的对象的癌症的方法,所述方法包括:
156、(a)检测bcr信号传导通路基因、bcr信号传导通路蛋白或它们中的任一种的表达或活性或水平的失调;和
157、(b)向所述对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
158、本文还提供了治疗对象的方法,所述方法包括向具有指示对象具有bcr信号传导通路基因、bcr信号传导通路蛋白或它们中的任一种的表达或活性或水平的失调的临床记录的对象施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
159、在一些实施方案中,btk相关癌症选自:霍奇金淋巴瘤、弥漫性大b细胞淋巴瘤(dlbcl)(例如激活的b细胞样dlbcl(abc-dlbcl))、滤泡性淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤(例如结外边缘区b细胞淋巴瘤、脾边缘区淋巴瘤)、伯基特淋巴瘤、瓦尔登斯特伦巨球蛋白血症(淋巴浆细胞性淋巴瘤(lpl))、原发性中枢神经系统淋巴瘤、小淋巴细胞性淋巴瘤、慢性淋巴细胞白血病(cll)、急性淋巴细胞白血病(all)、b细胞幼淋巴细胞白血病、前体b成淋巴细胞白血病、毛细胞白血病、急性髓样白血病(aml)、慢性髓样白血病、多发性骨髓瘤、浆细胞骨髓瘤、浆细胞瘤、骨癌、骨转移、乳腺癌、胃食管癌、胰腺癌、卵巢癌、前列腺癌、肺癌、结肠癌、子宫癌、肝细胞癌、头颈癌或神经胶质瘤。
160、在一些实施方案中,btk相关癌症是血液系统癌症。在一些实施方案中,血液系统癌症选自:白血病、淋巴瘤(非霍奇金淋巴瘤)、霍奇金病和骨髓瘤。
161、在一些实施方案中,血液系统癌症选自:急性淋巴细胞白血病(all)、急性髓样白血病(aml)、急性早幼粒细胞白血病(apl)、慢性淋巴细胞白血病(cll)、慢性髓样白血病(cml)、慢性粒单核细胞白血病(cmml)、慢性中性粒细胞白血病(cnl)、急性未分化白血病(aul)、间变性大细胞淋巴瘤(alcl)、幼淋巴细胞白血病(pml)、幼年型骨髓单核细胞白血病(jmml)、成人t细胞all、aml伴骨髓三系病态造血(aml/tmds)、混合谱系白血病(mll)、骨髓增生异常综合征(mdss)、骨髓增生性病症(mpd)、弥漫性大b细胞淋巴瘤(dlbcl)(例如激活的b细胞样dlbcl(abc-dlbcl))、滤泡性淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤(例如结外边缘区b细胞淋巴瘤、脾边缘区淋巴瘤)、伯基特淋巴瘤、瓦尔登斯特伦巨球蛋白血症(淋巴浆细胞性淋巴瘤(lpl))、原发性中枢神经系统淋巴瘤、小淋巴细胞性淋巴瘤、前体b成淋巴细胞白血病、毛细胞白血病、慢性髓样白血病、间变性大细胞淋巴瘤、malt淋巴瘤、浆细胞骨髓瘤、浆细胞瘤和多发性骨髓瘤(mm)。
162、在一些实施方案中,btk相关癌症是b细胞恶性肿瘤。在一些实施方案中,b细胞恶性肿瘤选自:霍奇金淋巴瘤、弥漫性大b细胞淋巴瘤(dlbcl)(例如激活的b细胞样dlbcl(abc-dlbcl))、滤泡性淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤(例如结外边缘区b细胞淋巴瘤、脾边缘区淋巴瘤)、伯基特淋巴瘤、瓦尔登斯特伦巨球蛋白血症(淋巴浆细胞性淋巴瘤(lpl))、原发性中枢神经系统淋巴瘤、小淋巴细胞性淋巴瘤、慢性淋巴细胞白血病、急性成淋巴细胞白血病(all)、b细胞幼淋巴细胞白血病、前体b成淋巴细胞白血病或毛细胞白血病。
163、在一些实施方案中,btk相关癌症选自:套细胞淋巴瘤、慢性淋巴细胞白血病、小淋巴细胞性淋巴瘤、瓦尔登斯特伦巨球蛋白血症和边缘区淋巴瘤。
164、在一些实施方案中,btk相关癌症未经历转化。btk相关癌症的转化的非限制性实例包括richter转化、幼淋巴细胞转化(例如cll的幼淋巴细胞转化)、转化的非霍奇金淋巴瘤和母细胞淋巴瘤(例如母细胞变体套细胞淋巴瘤)。
165、在一些实施方案中,btk相关癌症不是具有已知的淋巴瘤累及中枢神经系统的癌症。
166、在一些实施方案中,btk相关癌症是实体瘤。
167、在一些实施方案中,实体瘤选自:骨癌、骨转移、乳腺癌、胃食管癌、胰腺癌、卵巢癌、前列腺癌、肺癌、结肠癌、子宫癌、肝细胞癌、头颈癌和神经胶质瘤。
168、在一些实施方案中,口服施用式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
169、在一些实施方案中,该方法还包括向对象施用另外的疗法或治疗剂。
170、在一些实施方案中,另外的疗法或治疗剂选自:放射疗法、细胞毒性化学治疗剂、激酶靶向治疗剂、细胞凋亡调节剂、信号转导抑制剂、免疫靶向疗法、转录调节抑制剂和血管生成靶向疗法。在一些实施方案中,另外的治疗剂选自一种或多种激酶靶向治疗剂。在一些实施方案中,激酶靶向治疗剂靶向来自选自以下的激酶家族的激酶:jak、src、irak及其组合。
171、在一些实施方案中,另外的治疗剂选自一种或多种蛋白抑制剂。在一些实施方案中,一种或多种蛋白抑制剂抑制选自以下的蛋白:抗凋亡蛋白、热休克蛋白、核输出蛋白、激酶、组蛋白脱乙酰酶、e3泛素连接酶、组蛋白-赖氨酸n-甲基转移酶及其组合。在一些实施方案中,一种或多种蛋白抑制剂抑制选自以下的蛋白:pi3k、jak-2、irak1、irak4、bmx、tak1、src家族、hdac6、mdm2、bcl-2、ezh2、ehmt2、pim、jak3、mtor、ror-1、syk、pkc、hsp90、xpo1及其组合。在一些实施方案中,施用两种另外的治疗剂(例如,mtor的抑制剂和bcl-2的抑制剂)。
172、在一些实施方案中,另外的治疗剂抑制选自以下的蛋白:抗凋亡蛋白、热休克蛋白、核输出蛋白、激酶、组蛋白脱乙酰酶、e3泛素连接酶、组蛋白-赖氨酸n-甲基转移酶及其组合。
173、在一些实施方案中,另外的治疗剂抑制选自以下的蛋白:pi3k、jak-2、irak1、irak4、bmx、tak1、src家族、hdac6、mdm2、bcl-2、ezh2、ehmt2、pim、jak3、mtor、ror-1、syk、pkc、hsp90、xpo1及其组合。
174、在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体、或其药物组合物和另外的治疗剂以分开的剂量同时施用。
175、在一些实施方案中,式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体、或其药物组合物和另外的治疗剂以分开的剂量以任何顺序相继施用。
176、本文还提供了治疗具有癌症的对象的方法,其中所述方法包括:
177、(a)向对象施用一个或多个剂量的第一btk抑制剂一段时间;
178、(b)在(a)之后,确定获自对象的样品中的癌细胞是否具有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变;和
179、(c)如果对象具有有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用作为单一疗法或与另一种抗癌剂组合的式i化合物的喷雾干燥的分散体或药物组合物;或
180、(d)如果对象具有不具有赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用另外剂量的步骤(a)的第一btk抑制剂。
181、在一些实施方案中,步骤(c)中的抗癌剂是第二btk抑制剂、免疫疗法或其组合。
182、在一些实施方案中,步骤(c)中的抗癌剂是步骤(a)中施用的第一btk抑制剂。
183、在一些实施方案中,步骤(c)中的抗癌剂选自一种或多种激酶靶向治疗剂。在一些实施方案中,激酶靶向治疗剂靶向来自选自以下的激酶家族的激酶:jak、src、irak及其组合。
184、在一些实施方案中,步骤(c)中的抗癌剂是抑制选自以下的蛋白的蛋白抑制剂:抗凋亡蛋白、热休克蛋白、核输出蛋白、激酶、组蛋白脱乙酰酶、e3泛素连接酶、组蛋白-赖氨酸n-甲基转移酶及其组合。
185、在一些实施方案中,步骤(c)中的抗癌剂选自一种或多种蛋白抑制剂,其抑制选自以下的蛋白:抗凋亡蛋白、热休克蛋白、核输出蛋白、激酶、组蛋白脱乙酰酶、e3泛素连接酶、组蛋白-赖氨酸n-甲基转移酶及其组合。
186、在一些实施方案中,蛋白抑制剂抑制选自以下的蛋白:pi3k、jak-2、irak1、irak4、bmx、tak1、src家族、hdac6、mdm2、bcl-2、ezh2、ehmt2、pim、jak3、mtor、ror-1、syk、pkc、hsp90、xpo1及其组合。
187、在一些实施方案中,给对象施用另外剂量的步骤(a)的第一btk抑制剂,并且所述方法进一步包括(e)向所述对象施用另一种抗癌剂。
188、在一些实施方案中,其中步骤(e)的抗癌剂是第二btk抑制剂、免疫疗法或其组合。
189、在一些实施方案中,步骤(e)的抗癌剂是式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物。
190、本文还提供了治疗具有癌症的对象的方法,其中所述方法包括:
191、(a)向对象施用一个或多个剂量的第一btk抑制剂一段时间;
192、(b)在(a)之后,确定获自对象的样品中的癌细胞是否具有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变;
193、(c)如果对象具有有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用作为单一疗法或与另一种抗癌剂组合的第二btk抑制剂;或
194、(d)如果对象具有不具有赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用另外剂量的步骤(a)的第一btk抑制剂;其中该突变是在氨基酸位置481处的取代,例如c481s、c481f、c481t、c481g和c481r。
195、在一些实施方案中,步骤(c)的抗癌剂是在步骤(a)中施用的第一btk抑制剂。
196、在一些实施方案中,给对象施用另外剂量的步骤(a)的第一btk抑制剂,并且该方法进一步包括(e)施用另一种抗癌剂。
197、在一些实施方案中,步骤(e)的抗癌剂是第二btk抑制剂、免疫疗法或其组合。
198、在一些实施方案中,步骤(e)的抗癌剂是式i化合物或其药学上可接受的盐的药物组合物。
199、本文还提供了治疗具有癌症的对象的方法,其中所述方法包括:
200、(a)向对象施用一个或多个剂量的第一btk抑制剂一段时间;
201、(b)在(a)之后,确定获自对象的样品中的癌细胞是否具有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变;
202、(c)如果对象具有有至少一个赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用作为单一疗法或与另一种抗癌剂组合的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物;或
203、(d)如果对象具有不具有赋予癌细胞或肿瘤对采用步骤(a)的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用另外剂量的步骤(a)的第一btk抑制剂;其中该突变是在plcγ2的一个或多个氨基酸位置244、257、334、495、664、665、707、708、742、845、848、993、1140或1141处的取代。
204、本文还提供了治疗具有癌症的对象的方法,其中所述方法包括:
205、(a)确定获自具有癌症并先前施用了一个或多个剂量的第一btk抑制剂的对象的样品中的癌细胞是否具有一个或多个赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变;和
206、(b)如果对象具有有至少一个赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用作为单一疗法或与另一种抗癌剂组合的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物;或
207、(c)如果对象具有不具有赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用另外剂量的第一btk抑制剂。
208、本文还提供了治疗具有癌症的对象的方法,其中所述方法包括:
209、(a)确定获自具有癌症并先前施用了一个或多个剂量的第一btk抑制剂的对象的样品中的癌细胞是否具有一个或多个赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变;和
210、(b)如果对象具有有至少一个赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则向对象施用作为单一疗法或与另一种抗癌剂组合的第二btk抑制剂;或
211、(c)如果对象具有不具有赋予癌细胞或肿瘤对采用先前施用给对象的第一btk抑制剂的治疗增加的抗性的btk抑制剂抗性突变的癌细胞,则施用另外剂量的先前施用给对象的第一btk抑制剂。
212、本文还提供了治疗具有癌症的对象的方法,其中该方法包括:
213、(a)施用一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物一段时间;
214、(b)在(a)之后,确定获自对象的样品中的癌细胞是否具有一个或多个赋予癌细胞或肿瘤对采用步骤(a)的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗增加的抗性的btk抑制剂抗性突变;和
215、(c)向具有有一个或多个赋予癌细胞或肿瘤对采用步骤(a)的权利要求1-3中任一项的喷雾干燥的分散体或权利要求7-93中任一项的药物组合物的治疗增加的抗性的btk抑制剂抗性突变的癌细胞的对象施用作为单一疗法或与另一种抗癌剂组合的第二btk抑制剂;或
216、(d)向具有不具有赋予癌细胞或肿瘤对采用步骤(a)的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗增加的抗性的btk抑制剂抗性突变的癌细胞的对象施用另外剂量的步骤(a)的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物。
217、本文还提供了治疗具有癌症的对象的方法,其中该方法包括:
218、(a)确定获自具有癌症并先前施用了一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的对象的样品中的癌细胞是否具有一个或多个赋予癌细胞或肿瘤对采用先前施用给对象的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗增加的抗性的btk抑制剂抗性突变;
219、(b)向具有有一个或多个赋予癌细胞或肿瘤对采用先前施用给对象的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗增加的抗性的btk抑制剂抗性突变的癌细胞的对象施用作为单一疗法或与另一种抗癌剂组合的第二btk抑制剂;或
220、(c)向具有不具有赋予癌细胞或肿瘤对采用先前施用给对象的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗增加的抗性的btk抑制剂抗性突变的癌细胞的对象施用另外剂量的先前施用的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物。
221、本文还提供了治疗对象的btk相关癌症的方法,所述方法包括:
222、(a)向被鉴定或诊断为具有btk相关癌症的对象施用作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物;
223、(b)在步骤(a)后,确定获自对象的生物学样品中的循环肿瘤dna的水平;
224、(c)向被鉴定为与循环肿瘤dna的参考水平相比具有大约相同或升高水平的循环肿瘤dna的对象施用式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物和另外的治疗剂或治疗。
225、在一些实施方案中,另外的治疗剂是第二btk激酶抑制剂。在一些实施方案中,另外的治疗剂或治疗包括放射疗法、化学治疗剂、检查点抑制剂、手术和一种或多种第二激酶抑制剂中的一种或多种。
226、在一些实施方案中,循环肿瘤dna的参考水平是在步骤(a)之前获自对象的生物学样品中的循环肿瘤dna水平。
227、本文还提供了治疗对象的btk相关癌症的方法,所述方法包括:向(i)被鉴定或诊断为具有btk相关癌症,(ii)先前施用了作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物和(ii)在施用作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物之后,被鉴定为与循环肿瘤dna的参考水平相比具有大约相同或升高水平的循环肿瘤dna的对象施用治疗有效量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物和另外的治疗剂或治疗。
228、在一些实施方案中,循环肿瘤dna的参考水平为在施用作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物前获自对象的生物学样品中的循环肿瘤dna的水平。
229、在一些实施方案中,另外的治疗剂是第二btk激酶抑制剂。在一些实施方案中,另外的治疗剂或治疗包括放射疗法、化学治疗剂、检查点抑制剂、手术和一种或多种第二蛋白抑制剂中的一种或多种。
230、本文还提供了为对象选择治疗的方法,所述方法包括:为(i)被鉴定或诊断为具有btk相关癌症,(ii)先前施用了一个或多个剂量的第二btk激酶抑制剂,和(ii)在施用一个或多个剂量的第二btk激酶抑制剂后,被鉴定为与循环肿瘤dna的参考水平相比具有大约相同或升高水平的循环肿瘤dna的对象选择治疗有效量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物。
231、本文还提供了为对象选择治疗的方法,所述方法包括:为(i)被鉴定或诊断为具有btk相关癌症,(ii)先前施用了作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物,和(ii)在施用了一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物后,被鉴定为与循环肿瘤dna的参考水平相比具有大约相同或升高水平的循环肿瘤dna的对象选择治疗有效量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物和另外的治疗性治疗。
232、在一些实施方案中,循环肿瘤dna的参考水平为在施用作为单一疗法的一个或多个剂量的式i化合物或其药学上可接受的盐、无定形或多晶型物形式、其喷雾干燥的分散体或其药物组合物前获自对象的生物学样品中的循环肿瘤dna的水平。在一些实施方案中,另外的治疗性治疗为第二btk激酶抑制剂。在一些实施方案中,另外的治疗性治疗包括放射疗法、化学治疗剂、检查点抑制剂和一种或多种第二蛋白抑制剂中的一种或多种。
233、本文还提供了在对象中确定治疗功效的方法,所述方法包括:
234、(a)在第一时间点确定获自被鉴定或诊断为具有btk相关癌症的对象的生物学样品中的循环肿瘤dna的第一水平;
235、(b)在第一时间点之后和第二时间点之前,向对象施用包括一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗;
236、(c)在第二时间点确定获自对象的生物学样品中的循环肿瘤dna的第二水平;和
237、(d)鉴定治疗在被确定为与循环肿瘤dna的第一水平相比具有降低的循环肿瘤dna的第二水平的对象中有效;或
238、鉴定治疗在被确定为与循环肿瘤dna的第一水平相比具有大约相同或升高的循环肿瘤dna的第二水平的对象中无效。
239、本文还提供了确定对象是否对治疗发展抗性的方法,所述方法包括:
240、(a)在第一时间点确定获自被鉴定或诊断为具有btk相关癌症的对象的生物学样品中的循环肿瘤dna的第一水平;
241、(b)在第一时间点之后和第二时间点之前,向对象施用包括一个或多个剂量的式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物的治疗;
242、(c)在第二时间点确定获自对象的生物学样品中的循环肿瘤dna的第二水平;和
243、(d)确定与循环肿瘤dna的第一水平相比具有降低的循环肿瘤dna的第二水平的对象没有对治疗发展抗性;或
244、确定与循环肿瘤dna的第一水平相比具有大约相同或升高的循环肿瘤dna的第二水平的对象已经对治疗发展抗性。
245、在任何上述实施方案中的一些中,对象没有活跃的不受控制的自身免疫性血细胞减少症。在一些实施方案中,对象尚未被诊断为自身免疫性血细胞减少症。在一些实施方案中,对象在开始如本文所述的治疗的6个月内没有临床上显著的、不受控制的心脏、心血管疾病或心肌梗塞历史。在一些实施方案中,对象尚未被诊断为心脏或心血管疾病。在一些实施方案中,对象尚未具有心肌梗塞。在一些实施方案中,对象不具有临床上显著的活跃的吸收不良综合征。在一些实施方案中,对象尚未被诊断为吸收不良综合征。在一些实施方案中,在如本文所述的任何治疗期间,对象未用强细胞色素p4503a4(cyp3a4)抑制剂(例如,利托那韦、茚地那韦、奈非那韦、沙奎那韦、克拉霉素、泰利霉素、氯霉素、酮康唑、伊曲康唑、泊沙康唑、伏立康唑、奈法唑酮和可比司他)或诱导剂(例如,卡马西平、地塞米松、乙琥胺、糖皮质激素、灰黄霉素、苯妥英、扑米酮、孕酮、利福平、萘夫西林、奈非那韦、奈韦拉平、奥卡西平、苯巴比妥、苯基丁氮酮、罗非考昔(轻度)、金丝桃、磺胺二甲嘧啶、磺吡酮和曲格列酮)治疗。在一些实施方案中,在开始本文所述的任何治疗的7天内,对象未用质子泵抑制剂(例如,奥美拉唑、兰索拉唑、右兰索拉唑、艾美拉唑、泮托拉唑、雷贝拉唑、艾普拉唑)治疗。在一些实施方案中,对象不具有活跃的第二恶性肿瘤。在一些实施方案中,对象具有处于缓解期的活跃的第二恶性肿瘤,并且对象的预期寿命>2年。
246、本文还提供了用于抑制哺乳动物细胞中的btk激酶活性的方法,所述方法包括使所述哺乳动物细胞与式i化合物或其药学上可接受的盐的喷雾干燥的分散体、药物组合物或多晶型物形式接触。
247、本文还提供了治疗对象中的自身免疫性或炎性疾病的方法,所述方法包括向被鉴定或诊断为具有自身免疫性或炎性疾病的对象施用式i化合物或其药学上可接受的盐的喷雾干燥的分散体或药物组合物。
248、除非另有定义,否则本文中使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常所理解的含义相同的含义。本文描述了用于本发明的方法和物质;也可以使用本领域已知的其它合适的方法和物质。该物质、方法和实例仅是说明性的,并无意于限制。本文提及的所有出版物、专利申请、专利、序列、数据库条目和其它参考文献均通过引用以其整体并入。在发生冲突的情况下,以本说明书(包括定义)为准。
249、在附图和下面的描述中阐述了本发明的一个或多个实施方案的细节。本发明的其它特征、目的和优点将从说明书和附图以及权利要求书中显而易见。
- 还没有人留言评论。精彩留言会获得点赞!