一种苯乙烯与功能化苯乙烯的高间规共聚物及其制备方法与流程
本发明涉及聚合物制备技术领域,尤其涉及一种苯乙烯与功能化苯乙烯的高间规共聚物及其制备方法。
背景技术:
高间规聚苯乙烯(sPS)于1986年首次由日本Idemitsu Kosan公司通过使用钛的茂金属催化剂催化聚合实现。sPS由于具有高熔点、高结晶性、高弹性模量、低介电常数、低损耗因子以及优良的耐热耐溶剂等特性,在工业上成为一种非常有吸引力的材料。
然而,sPS的脆性较大,并且聚合物中缺少极性基团是其单独作为材料使用时致命的缺点,限制了sPS的应用领域。因此,改善sPS的脆性、提高其极性、合成功能化的sPS一直是广大科技工作者致力解决的课题。
但是,在对聚苯乙烯进行改性的过程中,会使得聚合物降解。将功能化的苯乙烯与苯乙烯进行高间规共聚合可以直接将功能化基团引入到高间规聚苯乙烯上,避免了由高间规聚苯乙烯后功能化带来的聚合物降解等问题。然而,含有功能化基团的苯乙烯很容易与催化剂配位后使其失去聚合活性,因此功能化苯乙烯与苯乙烯共聚合也非常困难。1990年,Kazuo Soga等人利用Ziegler-Natta催化剂研究了苯乙烯与对氯苯乙烯、间氯苯乙烯或对溴苯乙烯共聚合,结果表明所得共聚物为无规结构;后来,Jungahn Kim研究小组利用大位阻基团保护的功能化苯乙烯—4-叔丁基二甲基硅氧苯乙烯与苯乙烯共聚合,然而功能化苯乙烯单体在共聚物中的插入率仅为1.8%;在2002年,T.C.Chung教授利用单茂钛催化剂合成了对位硼烷功能化苯乙烯与苯乙烯的共聚物,功能化单体的插入率最高为32.2%。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种苯乙烯与功能化苯乙烯的高间规共聚物及其制备方法,可任意调节共聚物中功能化苯乙烯单体的插入率。
本发明提供了一种苯乙烯与功能化苯乙烯的高间规共聚物,具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元,
式(Ⅱ)中,
R独立的选自C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基;
m为取代基R的个数,独立的选自1~5的整数。
优选的,R独立的选自C2~10的烷氧基、C7~10的芳氧基、C2~10的烷硫基或C7~10的芳硫基。
优选的,所述苯乙烯与功能化苯乙烯的高间规共聚物的间规度不小于90%,式(Ⅱ)所示重复单元的摩尔分数w为0%﹤w﹤100%。
本发明还提供了一种苯乙烯与功能化苯乙烯的高间规共聚物的制备方法,包括:
将苯乙烯和功能化的苯乙烯在催化剂的作用下,反应得到苯乙烯与功能化苯乙烯的高间规共聚物,所述高间规共聚物具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元:
所述功能化的苯乙烯具有式(Ⅲ)所示结构:
式(Ⅱ)和式(Ⅲ)中,
R独立的选自C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基;
m为取代基R的个数,独立的选自1~5的整数;
所述催化剂包括稀土配合物、有机硼化合物和有机铝化合物。
优选的,所述稀土配合物具有式(Ⅳ)或式(Ⅴ)所示结构:
其中,R1选自环戊二烯基及其衍生物、茚基及其衍生物或芴基及其衍生物中的任意一种;
R2选自C1~10的烷基、C1~10的硅烷基、C6~10的胺基芳基、C1~10的硅胺基、C1~10烷胺基、C3~10的烯丙基或硼氢基;
L1为配体,选自四氢呋喃、乙醚、乙二醇二甲醚或甲苯;
p为L1的个数,0≤p≤2;
R3选自环戊二烯基及其衍生物、茚基及其衍生物或芴基及其衍生物中的任意一种;
R4选自亚甲基、乙撑基或二甲基硅基;
R5、R6、R7独立的选自氢、甲基、乙基、异丙基、叔丁基或苯基;
R8选自氢、甲基、乙基、异丙基、叔丁基、苯基、2,6-二甲基苯基、4-甲基苯基、均三甲基苯基、2,6-二异丙基苯基、2,4,6-三异丙基苯基或2,6-二叔丁基苯基;
R9选自C1~10的烷基、C1~10的硅烷基、C6~10的胺基芳基、C1~10的硅胺基、C1~10烷胺基、C3~10的烯丙基或硼氢基;
L2为配体,选自四氢呋喃、乙醚、乙二醇二甲醚或甲苯;
q为L2的个数,0≤q≤2;
Ln独立的选自Sc、Y、La、Ce、Pr、Nd、Pm、Sm、Eu、Gd、Tb、Dy、Ho、Er、Tm、Yb或Lu。
优选的,所述有机硼化合物选自[Ph3C][B(C6F5)4]、[PhNMe2H][BPh4]、[NEt3H][BPh4]、[PhNMe2H][B(C6F5)4]或B(C6F5)3。
优选的,所述有机铝化合物选自烷基铝、氢化烷基铝、卤代烷基铝或铝氧烷。
优选的,所述有机铝化合物选自三甲基铝、三乙基铝、三正丙基铝、三正丁基铝、三异丙基铝、三异丁基铝、三戊基铝、三己基铝、三环己基铝、三辛基铝、三苯基铝、三对甲苯基铝、三苄基铝、乙基二苄基铝、乙基二对甲苯基铝、二乙基苄基铝、二甲基氢化铝、二乙基氢化铝、二正丙基氢化铝、二正丁基氢化铝、二异丙基氢化铝、二异丁基氢化铝、二戊基氢化铝、二己基氢化铝、二环己基氢化铝、二辛基氢化铝、二苯基氢化铝、二对甲苯基氢化铝、二苄基氢化铝、乙基苄基氢化铝、乙基对甲苯基氢化铝、二甲基氯化铝、二乙基氯化铝、二正丙基氯化铝、二正丁基氯化铝、二异丙基氯化铝、二异丁基氯化铝、二戊基氯化铝、二己基氯化铝、二环己基氯化铝、二辛基氯化铝、二苯基氯化铝、二对甲苯基氯化铝、二苄基氯化铝、乙基苄基氯化铝、乙基对甲苯基氯化铝、甲基铝氧烷、乙基铝氧烷、正丙基铝氧烷和正丁基铝氧烷中的一种或多种。
优选的,所述稀土配合物、有机硼化合物和有机铝化合物的摩尔比为1:(0.5~2.0):(0.5~3000)。
优选的,所述功能化苯乙烯和稀土配合物的摩尔比为(50~10000):1,所述苯乙烯和稀土配合物的摩尔比为(50~10000):1。
优选的,所述反应的温度为-60℃~80℃;所述反应的时间为0.5小时~48小时。
与现有技术相比,本发明提供了一种苯乙烯与功能化苯乙烯的高间规共聚物,具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元。实验结果表明,本发明提供的高间规共聚物的间规选择性不小于90%,并且功能化苯乙烯的插入率可任意调节,并可高达99%以上。同时共聚物中含氧或硫基团,可以增加高间规聚苯乙烯的极性,从而增加高间规聚苯乙烯与其他聚合物的共混性能。
同时本发明还提供了一种苯乙烯与功能化苯乙烯的高间规共聚物的制备方法,包括:将苯乙烯和功能化的苯乙烯在催化剂的作用下,反应得到苯乙烯与功能化苯乙烯的高间规共聚物,所述高间规共聚物具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元。本发明通过采用稀土配合物、有机硼化合物和有机铝化合物作为催化剂,首次利用配位聚合的方法合成苯乙烯与功能化苯乙烯的高间规共聚物,并且功能化苯乙烯结构单元在共聚物中的插入率可任意调控,突破了以往功能化单体在共聚物中插入率低的限制。
附图说明
图1是本发明实施例45制备的苯乙烯与甲氧基功能化的苯乙烯的共聚物的核磁共振氢谱图;
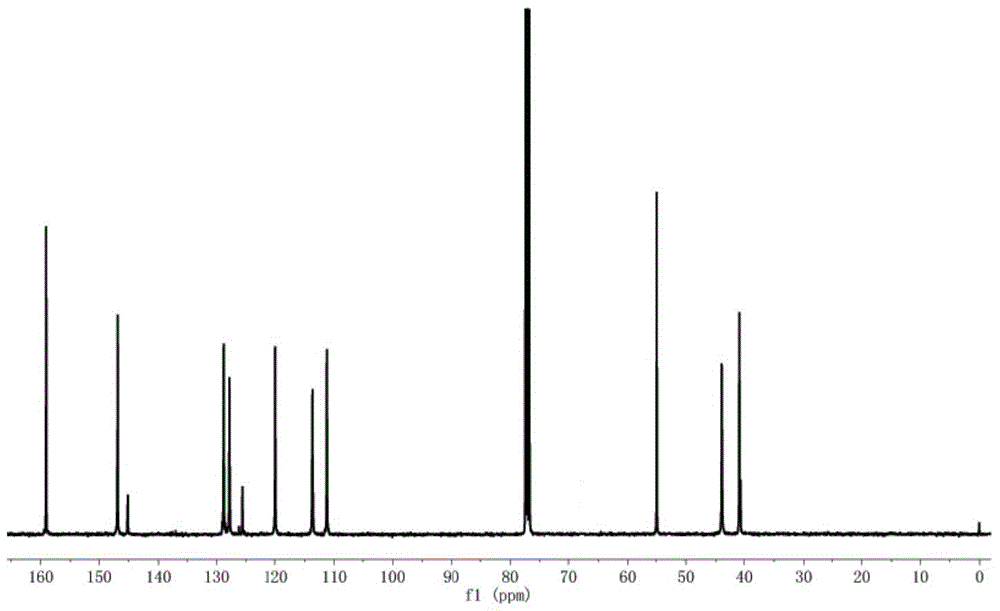
图2是本发明实施例45制备的苯乙烯与甲氧基功能化的苯乙烯的共聚物的核磁共振碳谱图;
图3是本发明实施例45制备的苯乙烯与甲氧基功能化的苯乙烯的共聚物的GPC曲线图;
图4是本发明实施例56制备的苯乙烯与甲氧基功能化的苯乙烯的共聚物的核磁共振氢谱图。
具体实施方式
本发明提供了一种苯乙烯与功能化苯乙烯的高间规共聚物,具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元,
式(Ⅱ)中,
R独立的选自C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基;
m为取代基R的个数,独立的选自1~5的整数。
本发明提供的高间规共聚物的间规选择性不小于90%,并且功能化苯乙烯的插入率可任意调节,并可以高达99%以上。同时共聚物中含氧或硫基团,可以增加高间规聚苯乙烯的极性,从而增加高间规聚苯乙烯与其他聚合物的共混性能。
本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物,具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元,且这两种重复单元在共聚物分子链上无规排列。
本发明提供的高间规共聚物中,R为苯环上的取代基,优选为C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基,更优选为C2~10的烷氧基、C7~10的芳氧基、C2~10的烷硫基或C7~10的芳硫基,更优选为C3~8的烷氧基、C8~9的芳氧基、C3~8的烷硫基或C8~9的芳硫基,最优选为C4~6的烷氧基、C8的芳氧基、C4~6的烷硫基或C8的芳硫基。本发明中,所述R可以为,但不限于,-O-CH3、-O-CH2CH3、-O-CH2CH2CH3、-O-CH2-Ph、-O-Ph、-S-Ph、-S-CH2-Ph、-C6H5或-S-CH3。本发明对所述R取代基的位置并无限定,可以在苯环上的任意位置进行取代。
本发明中,m为取代基R的个数,可以为1~5的任意整数,具体的,其可以为1、2、3、4或5,即本发明对所述取代基R的个数并无限定,可以为单取代或多取代。当m≥2时,所述式(Ⅱ)中同一苯环上的R可以为相同的取代基,也可以为不同的取代基。
本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物的数均分子量优选为1×104~250×104,更优选为2×104~200×104,最优选为10×104~150×104。所述高间规共聚物的间规度不小于90%,优选为90%~99%。式(Ⅱ)所示重复单元的摩尔分数w为0%﹤w﹤100%,更优选为1%﹤w﹤99%。所述w为式(Ⅱ)所示重复单元与所述高间规共聚物中重复单元总数的摩尔比。
本发明还提供了一种苯乙烯与功能化苯乙烯的高间规共聚物的制备方法,包括:
将苯乙烯和功能化的苯乙烯在催化剂的作用下,反应得到苯乙烯与功能化苯乙烯的高间规共聚物,所述高间规共聚物具有式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元:
所述功能化的苯乙烯具有式(Ⅲ)所示结构:
式(Ⅱ)和式(Ⅲ)中,
R独立的选自C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基;
m为取代基R的个数,独立的选自1~5的整数;
所述催化剂包括稀土配合物、有机硼化合物和有机铝化合物。
本发明通过采用稀土配合物、有机硼化合物和有机铝化合物作为催化剂,首次利用配位聚合的方法合成苯乙烯与功能化苯乙烯的高间规共聚物,并且功能化苯乙烯结构单元在共聚物中的插入率可任意调控,突破了以往功能化单体在共聚物中插入率低的限制,插入率可高达99%。
本发明在催化剂的作用下,将功能化苯乙烯与苯乙烯进行聚合,得到苯乙烯与功能化苯乙烯的高间规共聚物。在本发明中,所述催化剂包括稀土配合物、有机硼化合物和有机铝化合物。
在本发明中,所述稀土配合物优选为具有式(Ⅳ)所示结构的化合物或具有式(Ⅴ)所示结构的化合物:
式(Ⅳ)中:
R1优选为环戊二烯基及其衍生物、茚基及其衍生物或芴基及其衍生物中的任意一种;更优选为环戊二烯基、茚基或芴基。
R2优选为C1~10的烷基、C1~10的硅烷基、C6~10的胺基芳基、C1~10的硅胺基、C1~10烷胺基、C3~10的烯丙基或硼氢基;更优选为C2~8的烷基、C2~8的硅烷基、C7~9的胺基芳基、C2~8的硅胺基、C2~8烷胺基、C4~9的烯丙基或硼氢基;更优选为C3~6的烷基、C3~6的硅烷基、C8的胺基芳基、C3~6的硅胺基、C3~6烷胺基、C5~6的烯丙基或硼氢基;最优选为C3~6的硅烷基。本发明中,所述R2可以为,但不限于,-CH3、-CH2SiMe3、-CH(SiMe3)2、-O-NMe2-CH2C6H4、-N(SiMe3)2、-NH(SiMe3)、-1,3-C3H5或-BH4。
L1为配体,优选为四氢呋喃、乙醚、乙二醇二甲醚或甲苯;更优选为四氢呋喃、乙醚或甲苯。
p为L1的个数,0≤p≤2;其可以为0、1或2。当p为0时,所述式(Ⅳ)所示的稀土配合物没有配体。
Ln优选为Sc、Y、La、Ce、Pr、Nd、Pm、Sm、Eu、Gd、Tb、Dy、Ho、Er、Tm、Yb或Lu;更优选为Sc、Y、La、Lu、Ho、Gd、Nd或Er。
在本发明中,所述具有式Ⅳ所示结构的化合物优选为具有式1~式16所示结构化合物中的一种:
在本发明中,所述式1~式16中未给出的端基均为甲基。
本发明对所述具有式(Ⅳ)所示结构化合物的来源没有特殊限制,可以按照本领域技术人员熟知的制备具有式(Ⅳ)所示结构化合物的制备方法制备得到。优选的,可以按照文献(J.AM.CHEM.SOC.,2009,131,13870-13882)所公开的方法制备得到具有式1、式5和式8所示结构的化合物;按照文献(Chem.Eur.J.,2009,846-850)所公开的方法制备得到具有式10所示结构的化物;按照文献(Organometalics,2013,32,1445-1458)所公开的方法制备得到具有式11所示结构的化合物;按照文献(Angew.Chem.Int.Ed.2013,52,4418-4421)所述公开的方法制备得到具有式12所示结构的化合物;按照文献(Organometalics,2011,30,3270-3274)所公开的方法制备得到具有式13和式16所示结构的化合物;按照文献(Chem.Commun.,2009,3380-3382)所述公开的方法制备得到具有式14所示结构的化合物;按照文献(Chem.Asian J.2008,3,1406-1414)所述公开的方法制备得到具有式15所示结构的化合物。
式(Ⅴ)中:
R3优选为环戊二烯基及其衍生物、茚基及其衍生物或芴基及其衍生物中的任意一种;更优选为环戊二烯基、茚基或芴基。
R4优选为亚甲基、乙撑基或二甲基硅基;更优选为亚甲基或乙撑基;所述乙撑基为乙基失去两个氢原子的基团,所述二甲基硅基结构为
R5、R6、R7独立的优选为氢、甲基、乙基、异丙基、叔丁基或苯基;更优选为氢、甲基或乙基。
R8优选为氢、甲基、乙基、异丙基、叔丁基、苯基、2,6-二甲基苯基、4-甲基苯基、均三甲基苯基、2,6-二异丙基苯基、2,4,6-三异丙基苯基或2,6-二叔丁基苯基;更优选为氢、甲基、乙基、异丙基、叔丁基或均三甲基苯基。
R9优选为C1~10的烷基、C1~10的硅烷基、C6~10的胺基芳基、C1~10的硅胺基、C1~10烷胺基、C3~10的烯丙基或硼氢基;更优选为C2~8的烷基、C2~8的硅烷基、C7~9的胺基芳基、C2~8的硅胺基、C2~8烷胺基、C4~9的烯丙基或硼氢基;更优选为C3~6的烷基、C3~6的硅烷基、C8的胺基芳基、C3~6的硅胺基、C3~6烷胺基、C5~6的烯丙基或硼氢基;最优选为C3~6的硅烷基。本发明中,所述R9可以为,但不限于,-CH3、-CH2SiMe3、-CH(SiMe3)2、-O-NMe2-CH2C6H4、-N(SiMe3)2、-NH(SiMe3)、-1,3-C3H5或-BH4。
L2为配体,优选为四氢呋喃、乙醚、乙二醇二甲醚或甲苯;更优选为四氢呋喃、乙醚或甲苯。
q为L2的个数,0≤q≤2;其可以为0、1或2。当q为0时,所述式(Ⅴ)所示的稀土配合物没有配体。
Ln优选为Sc、Y、La、Ce、Pr、Nd、Pm、Sm、Eu、Gd、Tb、Dy、Ho、Er、Tm、Yb或Lu;更优选为Sc、Y、La、Lu、Ho、Gd、Nd或Er。
在本发明中,所述具有式Ⅴ示结构的化合物优选为具有式17~式28所示结构化合物中的一种:
在本发明中,所述式17~式28中未给出的端基均为甲基。
本发明对所述具有式(Ⅴ)所示结构化合物的来源没有特殊的限制,可按照本领域技术人员熟知的制备具有式(Ⅴ)所示结构化合物的制备方法制备得到。如可按照文献(Macromolecules,2012,45,1248-1253)所公开的方法,以及申请号为201210020478.1和201310750870.6的中国专利所公开的方法,制备得到具有式17~式28所示结构的化合物。
本发明中,所述有机硼化合物优选为[Ph3C][B(C6F5)4]、[PhNMe2H][BPh4]、[NEt3H][BPh4]、[PhNMe2H][B(C6F5)4]或B(C6F5)3;更优选为[Ph3C][B(C6F5)4]、[PhNMe2H][B(C6F5)4]或B(C6F5)3。本发明对所述有机硼化物的来源没有特殊的限制,采用本领域技术人员熟知的上述种类的有机硼化物即可,可由市场购买获得。
在本发明中,所述有机铝化合物优选为烷基铝、氢化烷基铝、卤代烷基铝和铝氧烷化合物中的一种或几种,更优选为三甲基铝、三乙基铝、三正丙基铝、三正丁基铝、三异丙基铝、三异丁基铝、三戊基铝、三己基铝、三环己基铝、三辛基铝、三苯基铝、三对甲苯基铝、三苄基铝、乙基二苄基铝、乙基二对甲苯基铝、二乙基苄基铝、二甲基氢化铝、二乙基氢化铝、二正丙基氢化铝、二正丁基氢化铝、二异丙基氢化铝、二异丁基氢化铝、二戊基氢化铝、二己基氢化铝、二环己基氢化铝、二辛基氢化铝、二苯基氢化铝、二对甲苯基氢化铝、二苄基氢化铝、乙基苄基氢化铝、乙基对甲苯基氢化铝、二甲基氯化铝、二乙基氯化铝、二正丙基氯化铝、二正丁基氯化铝、二异丙基氯化铝、二异丁基氯化铝、二戊基氯化铝、二己基氯化铝、二环己基氯化铝、二辛基氯化铝、二苯基氯化铝、二对甲苯基氯化铝、二苄基氯化铝、乙基苄基氯化铝、乙基对甲苯基氯化铝、甲基铝氧烷、乙基铝氧烷、正丙基铝氧烷和正丁基铝氧烷中的一种或几种;最优选为三异丁基铝、三乙基铝、三甲基铝、甲基铝氧烷和氢化二异丁基铝中的一种或几种。
本发明对所述有机铝化合物的来源没有特殊的限制,可以为一般市售。
本发明中,所述稀土配合物、有机硼化合物和有机铝化合物的摩尔比优选为1:(0.5~2.0):(0.5~3000),更优选为1:(0.8~1.5):(1~1000),最优选为1:(0.9~1.1):(2~500)。
在本发明中,所述催化剂的制备方法优选为:
将稀土配合物、有机硼化合物和有机铝化合物混合,得到催化剂。
在本发明中,所述混合的温度优选为-60℃~80℃,更优选为-20℃~60℃,最优选为0℃~60℃,最最优选为25℃~40℃。在本发明中,所述混合的时间优选为1分钟~4分钟,更优选为2分钟~3分钟。本发明优选在保护性气体的条件下进行混合。在本发明中,所述保护性气体优选为惰性气体,更优选为氮气或氩气。在本发明中,所述稀土配合物、有机硼化合物和有机铝化合物的种类、来源和摩尔比与上述技术方案所述的稀土配合物、有机硼化合物和有机铝化合物的种类、来源和摩尔比一致,在此不再赘述。
在本发明中,所述催化剂优选为催化剂溶液。在本发明中,所述催化剂溶液中的溶剂优选为烷烃、芳烃、卤代芳烃和环烷烃中的一种或几种,更优选为饱和烷烃、饱和芳烃、饱和卤代芳烃和饱和环烷烃中的一种或几种,最优选为正己烷、正庚烷、环己烷、苯、甲苯、二甲苯、氯苯、二氯苯和三氯苯中的一种或几种。本发明对所述催化剂溶液中溶剂的来源没有特殊的限制,可由市场购买获得。在本发明中,所述催化剂溶液中稀土配合物的摩尔浓度优选为0.1mmol/L~500mmol/L,更优选为0.2mmol/L~50mmol/L,最优选为0.3mmol/L~5mmol/L。
在本发明中,所述催化剂溶液的制备方法优选为:
将催化剂分散在溶剂中,得到催化剂溶液。
本发明更优选在保护性气体的条件下,将催化剂分散在有机溶剂中,得到催化剂溶液。在本发明中,所述保护性气体优选为惰性气体,更优选为氮气或氩气。本发明对所述分散的方法没有特殊的限制,采用本领域技术人员熟知的分散技术方案即可。
本发明对所述溶剂的用量并无特殊限定,优选使催化剂溶液中稀土配合物的摩尔浓度达到上述技术方案所述的催化剂溶液中稀土配合物的摩尔浓度。
在本发明中,所述功能化苯乙烯具有式(Ⅲ)所示的结构:
其中,R为苯环上的取代基,优选为C1~20的烷氧基、C6~20的芳氧基、C1~20的烷硫基或C6~20的芳硫基,更优选为C2~10的烷氧基、C7~10的芳氧基、C2~10的烷硫基或C7~10的芳硫基,更优选为C3~8的烷氧基、C8~9的芳氧基、C3~8的烷硫基或C8~9的芳硫基,最优选为C4~6的烷氧基、C8的芳氧基、C4~6的烷硫基或C8的芳硫基。本发明中,所述R可以为,但不限于,-O-CH3、-O-CH2CH3、-O-CH2CH2CH3、-O-CH2-Ph、-O-Ph、-S-Ph、-S-CH2-Ph、-C6H5或-S-CH3。本发明对所述R取代基的位置并无限定,可以在苯环上的任意位置进行取代。
m为取代基R的个数,可以为1~5的任意整数,具体的,其可以为1、2、3、4或5,即本发明对所述取代基R的个数并无限定,可以为单取代或多取代。当m≥2时,所述式(Ⅲ)中同一苯环上的R可以为相同的取代基,也可以为不同的取代基。
在本发明中,所述功能化苯乙烯优选为具有式A~式W所示结构的化合物中的任意一种:
本发明对所述功能化苯乙烯的来源没有特殊的限制,采用本领域技术人员熟知的上述种类的功能化苯乙烯即可,可由市场购买获得。
本发明中,所述功能化苯乙烯和稀土配合物的摩尔比优选为(50~10000):1,更优选为(100~8000):1,最优选为(200~6000):1。
所述苯乙烯和稀土配合物的摩尔比为((50~10000):1,更优选为(100~8000):1,最优选为(200~6000):1。
本发明对所述苯乙烯和功能化苯乙烯的摩尔比并无特殊限定,可以任意调节。
本发明将苯乙烯和功能化的苯乙烯在催化剂的作用下,进行反应,得到由式(Ⅰ)所示结构和式(Ⅱ)所示结构的重复单元无规共聚的高间规共聚物。优选将功能化的苯乙烯和苯乙烯加入到催化剂中进行聚合反应,得到高间规共聚物。
本发明优选在无水、无氧的条件下进行所述聚合反应。在本发明中,所述聚合反应的温度优选为-60℃~80℃,更优选为-30℃~60℃,最优选为0℃~50℃,最最优选为20℃~40℃。在本发明中,所述聚合反应的时间优选为0.5小时~48小时,更优选为1小时~35小时,最优选为2小时~24小时,最最优选为4小时~12小时。
在本发明中,所述聚合反应既可以在有溶剂的条件下进行溶液聚合,也可以在无溶剂的条件下进行本体聚合。当所述聚合反应在有溶剂的条件下进行时,所述溶剂优选为烷烃、芳烃、卤代芳烃和环烷烃中的一种或几种,更优选为饱和烷烃、饱和芳烃、饱和卤代芳烃和饱和环烷烃中的一种或几种,最优选为正己烷、正庚烷、环己烷、苯、甲苯、二甲苯、氯苯、二氯苯和三氯苯中的一种或几种。本发明对所述聚合反应溶剂的来源没有特殊的限制,可由市场购买获得。
在本发明中,当所述聚合反应在有溶剂的条件下进行聚合时,溶剂的用量优选使所述功能化的苯乙烯的质量浓度为1g/100mL~60g/100mL,更优选为2g/100mL~50g/100mL,最优选为3g/100mL~35g/100mL,最最优选为5g/100mL~20g/100mL。
所述聚合反应完成后,本发明优选采用盐酸乙醇溶液终止所述聚合反应;将得到的反应溶液进行沉降、干燥,得到功能化的高间规聚苯乙烯。在本发明中,所述盐酸乙醇溶液的体积浓度优选为5%~15%,更优选为8%~12%,最优选为10%。在本发明中,所述沉降采用的试剂优选为甲醇。本发明对所述干燥的方法并无限定,可以为本领域公知的干燥方法,本发明优选为真空干燥。在本发明中,所述干燥的时间优选为40小时~60小时,更优选为45小时~55小时,最优选为50小时。
将本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物进行核磁共振碳谱和氢谱检测,结果表明,本发明制备得到了式(I)结构所示的高间规共聚物,其间规选择性>90%,并且功能化苯乙烯的插入率可在0%~100%间任意调节。采用凝胶渗透色谱测试本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物的数均分子量,测试结果为,其数均分子量为1×104~250×104。采用接触角测量仪测试本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物的接触角,测试结果为,其接触角为85.4°~95.6°。
本发明提供了一种苯乙烯与功能化苯乙烯的高间规共聚物,实验结果表明,本发明提供的高间规共聚物的间规选择性不小于90%,并且功能化苯乙烯结构单元在共聚物中的插入率可任意调节。同时共聚物中含氧或硫基团,可以增加高间规聚苯乙烯的极性,从而增加高间规聚苯乙烯与其他聚合物的共混性能。
同时本发明还提供了一种苯乙烯与功能化苯乙烯的高间规共聚物的制备方法,包括:将苯乙烯和功能化的苯乙烯在催化剂的作用下,反应得到苯乙烯与功能化苯乙烯的高间规共聚物。本发明通过采用稀土配合物、有机硼化合物和有机铝化合物作为催化剂,首次利用配位聚合的方法合成苯乙烯与功能化苯乙烯的高间规共聚物,并且功能化苯乙烯结构单元在共聚物中的插入率可任意调控,突破了以往功能化单体在共聚物中插入率低的限制,插入率可高达99%。
为了进一步说明本发明,下面结合实施例对本发明提供的苯乙烯与功能化苯乙烯的高间规共聚物及其制备方法进行详细描述。
实施例1
在25℃下,向25mL经无水、无氧处理的聚合容器中加入10μmol具有式1所示结构的稀土配合物、10μmol[Ph3C][B(C6F5)4]、100μmol三异丁基铝以及甲苯溶剂5mL混合2分钟,得到稀土配合物的摩尔浓度为2.0mmol·L–1的催化剂甲苯溶液。
实施例2~41
按照实施例1所述的方法,采用表1中的原料配比及反应条件,分别制备得到催化剂溶液;表1为实施例2~41的原料配比及反应条件。所述反应容器的体积大小可以根据添加溶剂的体积自行决定。
表1实施例2~41的原料配比及反应条件
实施例42
取实施例1制备的催化剂溶液5mL,置于经过无水、无氧处理的聚合瓶中,再加入5.0mmol功能化苯乙烯单体A与5.0mmol苯乙烯单体,25℃下进行聚合反应4小时,然后加入2mL体积浓度为10%的盐酸乙醇溶液终止聚合反应,将反应溶液倒入100mL甲醇中沉降,得到苯乙烯与甲氧基功能化的苯乙烯的共聚物;再将得到的该聚合物置于真空干燥箱中干燥48小时,得到干燥恒重的苯乙烯与甲氧基功能化的苯乙烯的共聚物,净重1.19g。总转化率95%。接触角为92.1o。
用核磁共振氢谱(1H NMR)和核磁共振碳谱(13C NMR)分析得到的苯乙烯与甲氧基功能化的苯乙烯的共聚物,结果表明其间规度大于99%;共聚物中功能化苯乙烯单体的插入率为54%;用GPC分析得到其数均分子量(Mn)为23.6万,分子量分布(Mw/Mn)为1.19。
实施例43~102
按照实施例42所述的方法,采用表2中的原料配比及反应条件,分别制备得到苯乙烯与功能化苯乙烯的共聚物;表2为本发明实施例43~102的原料配比、反应条件,以及性能测试结果汇总。所述催化剂一列的数字表示选用所述实施例制备的催化剂。
表2本发明实施例43~102的原料配比、反应条件,以及性能测试结果汇总
注:表2中“n.d.”表示“未测试”
对本发明实施例45制备的苯乙烯与间甲氧基功能化的苯乙烯的共聚物进行核磁共振氢谱和碳谱检测,检测结果见图1和图2,其中图1是本发明实施例45制备的苯乙烯与间甲氧基功能化的苯乙烯的共聚物的核磁共振氢谱图,图2是本发明实施例45制备的苯乙烯与间甲氧基功能化的苯乙烯的共聚物的核磁共振碳谱图;由图1和图2可知,本发明制备得到了苯乙烯与间甲氧基功能化的苯乙烯的共聚物,其间规度大于99%;并且共聚物中间甲氧基功能化的苯乙烯单体的插入率为73%。
采用凝胶渗透色谱法(GPC)对本发明实施例45制备的苯乙烯与间甲氧基功能化的苯乙烯的高间规共聚物进行检测,结果见图3;由图3可知,所述苯乙烯与甲氧基功能化的苯乙烯的共聚物的数均分子量(Mn)为220.6万,分子量分布(Mw/Mn)为1.43。
对本发明实施例56制备的苯乙烯与对甲氧基功能化的苯乙烯的共聚物进行核磁共振氢谱检测,检测结果见图4;由图4可知,本发明制备得到了苯乙烯与对甲氧基功能化的苯乙烯的共聚物,其间规度大于99%;并且共聚物中间甲氧基功能化的苯乙烯单体的插入率为53%。
从以上实施例可以看出,本发明采用含稀土化合物的催化剂,通过配位聚合的方法,催化功能化苯乙烯与苯乙烯高间规共聚合反应,成功制备得到苯乙烯与功能化苯乙烯的高间规共聚物,具有71%~100%的较高转化率;且制备的功能化高间规共聚物的数均分子量为1×104~250×104,分子量分布为1.1~3.0,间规度均不小于90%,且通过调控原料配比,使得功能化苯乙烯结构单元在共聚物中的插入率可任意调控。
所获得的功能化苯乙烯与苯乙烯的共聚物虽然具有很高的间规选择性,但由于共聚物中功能化苯乙烯单体的插入不利于聚合物的结晶,从而使大部分共聚物没有熔点。
当共聚物中功能化苯乙烯结构单元的含量增大时,共聚物的接触角从95.6°降低到85.4°,表明共聚物的极性随着功能化苯乙烯结构单元含量的增大而明显提高。
以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!