高效乙醇发酵菌的制作方法
本发明涉及在使用木质纤维素类生物质生成生物乙醇的过程中用于发酵糖化溶液的微生物。
特别涉及在使用木质纤维素类生物质生成生物乙醇的过程中能够由五碳糖(下文中也称为c5)以及六碳糖(下文中也称为c6)有效地生成乙醇的微生物。
背景技术:
生物乙醇作为由生物质生成的不会发生枯竭的可再生资源而倍受期待。另外,由于燃烧生物乙醇而生成的二氧化碳为碳中性的,因而据信通过促进生物乙醇的利用可抑制作为地球温室化的主要原因的二氧化碳的增加。
生物乙醇是将生物质发酵并进行蒸馏提纯乙醇制得的。为了提高生物乙醇的收率,需要由糖化溶液中生成大多数的醇。在生物乙醇生成的过程中通常使用的酵母无法将木糖、阿拉伯糖等五碳糖转换为醇,因而作为发酵原料,仅使用了六碳糖。
尽管根据原料而不同,但在代表性的生物质中被认为含有35~45%的纤维素、25~40%的半纤维素、15~30%的木质素。因而,在不仅可利用六碳糖聚合而成的纤维素作为底物、而且还可利用主要含有作为五碳糖的木糖等的半纤维素作为底物时,可有效地产生乙醇。
木糖被认为是在生物质中大量含有的糖,其含量仅次于葡萄糖,有效地利用五碳糖是生物乙醇生产中的一大课题。
目前为止公开了少量利用木糖的技术,其是通过经基因重组而赋予木糖利用能力、或者利用木糖产生成乙醇的微生物的利用等而实现的。
在专利文献1中公开了下述发明:将具有木糖转运体活性的基因导入到宿主细胞中,从而将木糖(c5)转换为木酮糖,整合在糖酵解系统的戊糖磷酸途径中,在发酵中加以利用。
在专利文献2中公开了利用被赋予了阿拉伯糖转运体的酵母来生成醇的技术。与专利文献1同样地、将阿拉伯糖(c5糖)经阿拉伯糖醇、木酮糖而整合在糖酵解系统的戊糖磷酸途径中,在发酵中加以利用。
在非专利文献1中公开了通过将源自大肠杆菌的木糖同化基因重组到发酵单胞菌中而赋予木糖同化能力的内容。
在非专利文献2中记载了毕赤属酵母可利用木糖生产乙醇的内容。
现有技术文献
专利文献
专利文献1:日本特开2012-170422号公报
专利文献2:美国专利申请公开第2013/189788号说明书
非专利文献
非专利文献1:zhang,m.,etal.,science,1995.vol.267,pp.240-243.
非专利文献2:bicho,p.a.,etal.,appl.environ.microbiol.,1988,vol.54,pp.50-54.
技术实现要素:
发明所要解决的问题
但是,专利文献1的发明是将源自季也蒙假丝酵母(candidaguilliermondii)的具有木糖转运体活性的蛋白质导入到作为宿主的酿酒酵母(saccharomycescerevisiae)中。即导入了外来基因。
另外,专利文献2的发明,尽管转运基因不同,但也是向宿主中导入不同种基因的发明。
另外,非专利文献1所记载的技术是导入木糖同化基因的技术,与上述专利文献1和2的技术思想不同,但导入外来基因这一点不变。
因此,上述专利文献1和2、非专利文献1均需要采取用于实施联合国所采纳的“关于生物多样性公约的卡塔赫纳生物安全议定书”的封锁对策。从而需要用于保证生物安全的设施,因而利用该细菌生成乙醇从成本方面考虑是不利的。
另外,根据非专利文献2记载的技术,关于毕赤属酵母的利用,由于野生型的毕赤属酵母的木糖利用性低,因而乙醇产生效率并不那么高。
本发明的课题在于在不导入外来基因的情况下得到乙醇生成效率高的发酵菌。
用于解决课题的手段
本发明涉及一种由五碳糖和六碳糖有效地生成乙醇的季也蒙毕赤酵母(meyerozymaguilliermondii),其特征在于,通过在玉米秸秆糖液中对于2014年12月4日以保藏号nitebp-01976被保藏于专利微生物保藏中心(日本国〒292-0818千叶县木更津市上总镰足2-5-8122号室)的菌(下文也称作bp-01976菌株)进行育种,提高玉米秸秆糖液中乙醇的产生。
bp-01976菌株是在下述发酵菌中对转醛醇酶、醇脱氢酶基因进行自克隆从而进一步提高发酵收率的菌。上述发酵菌是通过在稻秆来源的糖液中进行育种并选择出发酵收率高的菌而得到的高效乙醇发酵菌。
但是,由于是利用稻秆进行育种并且从中进行了选择,所以在玉米秸秆来源的糖液中的发酵收率并不高。因此,通过用玉米秸秆进行育种,能够得到提高了发酵收率的菌。
并且,本发明的高效乙醇发酵菌是由五碳糖和六碳糖有效地生成乙醇的季也蒙毕赤酵母(meyerozymaguilliermondii),其特征在于,于2014年11月19日以保藏号nitebp-01966(下文也称作bp-01966菌株。)被保藏于专利微生物保藏中心(日本国〒292-0818千叶县木更津市上总镰足2-5-8122号室)。
通过在玉米秸秆来源的糖液中进行育种,在玉米秸秆糖液中进行驯化并提高了发酵收率的菌中的,将尤其是发酵收率高的菌保藏于专利微生物保藏中心中,得到保藏号nitebp-01966。
本发明的菌是通过育种和导入季也蒙毕赤酵母(meyerozymaguilliermondii)自身的酶基因的基因重组而得到的菌,不需要依据卡塔赫纳法的封锁对策。因而,不需要用于生物安全的特殊设施,能够使用现有的设备。
附图说明
图1是示出亲代菌株(n菌株)、bp-01964菌株、bp-01976菌株以及作为本发明的菌株的bp-01966菌株的发酵收率的图。
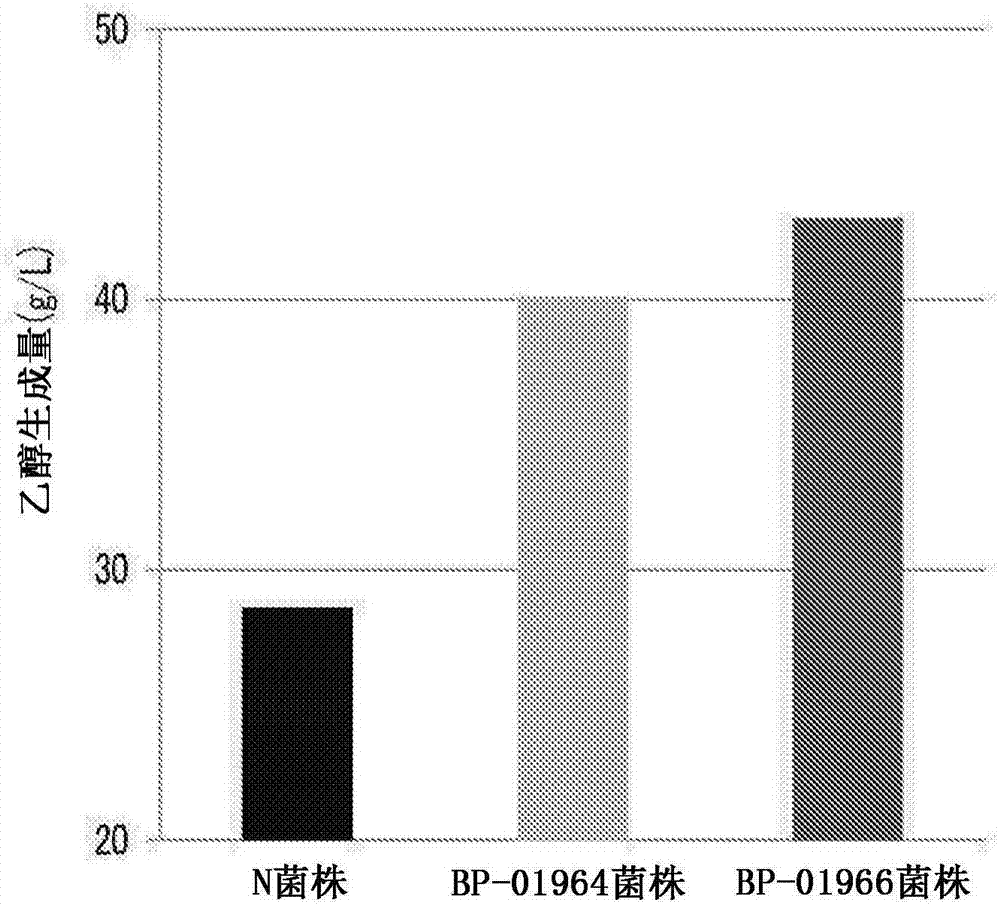
图2是示出亲代菌株(n菌株)、bp-01964菌株、bp-01966菌株的乙醇生成能力的图。
图3是示出浆液发酵中的葡萄糖、木糖同化能力的图。
图4是示出浆液发酵、澄清液发酵中的发酵收率的图。
具体实施方式
以下,对本发明的菌株进行说明。
实施例
1.菌株的分离
使用稻秆来源的糖液对季也蒙毕赤酵母(meyerozymaguilliermondii)的亲代菌株(n菌株)进行育种,选择出乙醇生成能力高的菌株。将日本熊谷产的稻秆浸入等量的25质量%氨水中,于80℃浸入3小时后,将氨解吸出。将处理后的生物质的ph调节至4后,添加支顶孢属纤维素酶(meijiseikapharma公司制),于50℃进行72小时酶糖化。将所制得的浆液通过压滤法进行固液分离回收液体。使用该液体(下文也称为澄清液),添加诱变剂进行19个月的驯化培养,分选出发酵性能提高的菌株。发酵性能提高的菌株的分选以规定时间后的生成乙醇量为基准来进行。将发酵性能高的菌株以保藏号nitebp-01964保藏于独立行政法人日本国家技术与评价研究所专利微生物保藏中心。
虽然在此未示出,bp-01964菌株是相对于野生型产生2倍以上乙醇的菌株,进一步确认到不仅作为c6的葡萄糖的同化能力提高,而且作为c5的木糖的同化能力也得到了提高。
接着,向bp-01964菌株中通过自克隆导入转醛醇酶、醇脱氢酶基因,进一步得到乙醇生成能力高的菌。
使用氨处理的稻秆液,通过糖化酶处理而得到糖液时,产生了作为副产物的有机酸、醛、酚等的发酵阻碍物质。特别是乙酸以约1000mg/l的浓度极大量存在,使发酵收率降低。因此,只要能够抑制由乙酸引起的对发酵菌的增殖阻碍,就能够进一步地提高乙醇的产生效率。
转醛醇酶是对由糖酵解系统分支出的戊糖磷酸途径中由景天庚酮糖-7-磷酸(s7p)和甘油醛3磷酸(gap)代谢为赤藓糖-4-磷酸(e4p)和果糖6磷酸(f6p)进行催化的酶。通过导入该酶,确认到在作为阻碍物质的乙酸存在的情况下乙醇收率得以提高的效果。
在转醛醇酶的上游连接有木糖还原酶的启动子。可以认为,通过使用木糖同化时发挥功能的木糖还原酶的启动子,使转醛醇酶有效地发挥作用。
另外,醇脱氢酶是能够使乙醛产生乙醇的酶,是能够将稻秆糖液中含有的作为阻碍物质的醛类转换、从而能够减弱毒性的酶。
醇脱氢酶的上流连接有gapdh的启动子。由于甘油醛-3-磷酸脱氢酶(gapdh)是存在于糖酵解系统中的强效的启动子,因此可以认为,将上述gapdh作为糖酵解系统的酶即醇脱氢酶的启动子来使用,能够有效地发挥作用。
因此,只要能够制作出通过基因导入而导入了2种酶的重组发酵菌,就可以期待得到乙醇产生能力更高的菌。
基因导入采取下述流程。将想要导入的基因和其终止子部(下文也称为基因+终止子部)进行pcr扩增。对想要用于导入的启动子部进行pcr扩增。这些均由本发明中使用的菌株即季也蒙毕赤酵母(candidaguilliermondii)的染色体进行pcr扩增。
使用融合(in-fusion)法,将经pcr扩增的dna片段以启动子、基因+终止子部分的顺序克隆到大肠杆菌用的市售载体中。将克隆后的载体转化到大肠杆菌中,进行载体的扩增。用限制酶从扩增后的载体切出启动子和基因+终止子部分,或者由扩增后的载体进行pcr扩增,从而得到用于同源重组的dna片段。
木糖还原酶的启动子具体使用下述序列编号1和序列编号2的引物进行扩增,转醛醇酶基因和终止子部分使用下述序列编号3和4的引物进行扩增。
序列编号1:aaggcttgggaactttcttt
序列编号2:agcaattgatgattaatttt
序列编号3:atgaccaattctcttgaaca
序列编号4:aaattgtgccgtgtcaaact
另外,gapdh的启动子具体使用下述序列编号5和序列编号6的引物进行扩增,醇脱氢酶基因和终止子部分使用下述序列编号7和8的引物进行扩增。
序列编号5:gttgtagcggaggctcaatt
序列编号6:tgtataatttaaatgtgggt
序列编号7:atgtcaattccagaatccat
序列编号8:caccttggctggaagtgctg
将所得的dna片段同源重组至菌株中,得到所希望的菌株。同源重组中使用电穿孔法。用于同源重组的dna片段呈以下顺序:木糖还原酶的启动子、转醛醇酶+终止子、gapdh的启动子、醇脱氢酶+终止子。另外,通过该方法得到的菌株尽管导入了基因,但由于为自克隆,因此依据卡塔赫纳法的规定,属于非重组菌的范畴。
由经基因导入的菌株中分离出乙醇产生能力高的菌,将其保藏于专利微生物保藏中心,得到保藏号nitebp-01976。
接着,在玉米秸秆来源的糖液中进行4个月的驯化培养,得到在玉米秸秆来源的糖液中发酵收率高的菌株,以保藏号bp-01966保藏于专利微生物保藏中心。以下,示出所得到的菌株的发酵收率等性质。
2.菌株的性质
2.1发酵收率
对亲代菌株、本发明的菌株进行了发酵试验。使用多种糖浓度不同的、将源自经稀硫酸处理的玉米秸秆的酶糖化溶液调节至ph6的溶液,添加上述菌株的培养液以使得培养基的od600达到2.0,在30℃温度下培养96小时,并通过由此得到的乙醇浓度和所投入糖化溶液的糖浓度计算得到的发酵收率进行描点。结果示于图1。
如图1所示,作为亲代菌株的n菌株的发酵收率约为48%,与此相对的,通过育种得到的高乙醇产生菌株bp-01964菌株的发酵收率为80%,通过基因重组导入转醛醇酶、醇脱氢酶而得到的bp-01976菌株的发酵收率为84%。而且,在玉米秸秆来源的糖液中进行了育种的本发明的保藏号bp-01966的菌株的发酵收率更高,约为86%。另外,图中△所示的是其他公司的发酵菌的发酵收率,与这些菌相比,本发明的菌也明显显示出更高的发酵收率。
进一步对乙醇产生能力进行比较。图2示出了本发明的菌株相比作为亲代菌株的n菌株(wt)、通过育种而提高了发酵收率的bp-01964菌株的乙醇的产生量。将玉米秸秆用稀硫酸处理后的糖化液的ph调节至6,利用该糖化液,添加菌株的培养液以使得培养基的od600达到2.0。示出于30℃培养96小时后的培养液中的乙醇量。糖化溶液的葡萄糖为63.2g/l、木糖为34.5g/l。使用gc-fid(glsciencesinc.公司制:gc390b)对乙醇进行测定。
从图2明确可知,本发明获得了一种产生了以下乙醇量的菌株:相比野生型的产生乙醇是2.5倍以上;相比通过育种提高了乙醇产生能力的菌株的产生乙醇也是约1.2倍。根据本发明的菌株相对于野生型菌株的乙醇产生量提高这一结果,可以认为作为c5的木糖的同化能力提高。因此确认到了该菌株的葡萄糖和木糖同化能力。
2.2木糖同化能力的研究
接着,用氨水对稻杆进行与上述氨处理同样的处理后,添加支顶孢属纤维素酶,于50℃进行72小时酶糖化,使用所制作的浆液进行发酵。
浆液发酵槽呈夹套结构,使温水在夹套部循环来进行温度调节。另外,在底部设置通气口,将规定量的通过了过滤器的空气持续由底部的通气口持续通入,在利用与马达联动的刮刀进行搅拌的同时进行发酵。
进行浆液中所含有的葡萄糖、木糖、乙醇的量的经时性变化的分析。关于葡萄糖、木糖,对浆液进行取样,对于通过离心得到的上清施以hpl(东曹公司制:lc-8020)测定木糖的浓度。与上述同样地使用gc-fid(glsciences公司制:gc390b)对乙醇进行了测定。将结果示于图3。
作为c6的葡萄糖先被消耗,其后,随着浆液中的葡萄糖减少,作为c5的木糖被消耗,产生乙醇。所得到的菌对c5、c6均具备同化能力,因而能够有效地产生乙醇。因此,上述得到的菌是在工业生产中也有用的菌株。
2.3浆液发酵能力、澄清液发酵能力
优选为在进行生物乙醇产生时不论使用浆液、澄清液中的任一种的情况下均可有效地发酵的菌。因此,使用浆液、澄清液对发酵收率进行比较。发酵收率通过下式计算。
发酵收率=所得到的乙醇量(g/l)/发酵开始时的糖液中含有的葡萄糖+木糖量(g/l)/0.5114
如图4所示,得到了不论在浆液发酵还是在澄清液发酵中均能够发挥出同等性能的菌株。
以保藏号bp-01966示出的菌,如上述所述,野生型季也蒙毕赤酵母(meyerozymaguilliermondii)的木糖同化能力通过育种得到强化,作为生物质不论使用稻秆、玉米秸秆中的任一种、均能够有效地产生乙醇。
如上述所示,野生型季也蒙毕赤酵母(meyerozymaguilliermondii)的木糖同化能力通过育种而得以强化,进一步地通过基因重组得到了乙醇产生能力高的菌株。而且,作为生物质不论使用稻秆、玉米秸秆中的任一种、均能有效地生成乙醇。
如上述所示,野生型季也蒙毕赤酵母(meyerozymaguilliermondii)的木糖同化能力通过育种而得以强化,进一步地通过基因重组得到了乙醇产生能力高的菌株。而且,不论使用稻秆、还是玉米秸秆作为生物质,均能有效地生成乙醇。
序列表
<110>本田技研工业株式会社(hondamotorco.,ltd.)
<120>高效乙醇发酵菌(highefficiencyethanol-zymocyte)
<130>pct140402
<160>8
<170>patentinversion3.5
<210>1
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>1
aaggcttgggaactttcttt20
<210>2
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>2
agcaattgatgattaatttt20
<210>3
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>3
atgaccaattctcttgaaca20
<210>4
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>4
aaattgtgccgtgtcaaact20
<210>5
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>5
gttgtagcggaggctcaatt20
<210>6
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>6
tgtataatttaaatgtgggt20
<210>7
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>7
atgtcaattccagaatccat20
<210>8
<211>20
<212>dna
<213>人工序列
<220>
<223>季也蒙毕赤酵母(meyerozymaguilliermondii)
<400>8
caccttggctggaagtgctg20
- 还没有人留言评论。精彩留言会获得点赞!