用于在治疗和诊断1型糖尿病中使用的肽的制作方法
相关申请的交叉引用
本申请根据35u.s.c.§119(e)要求2014年11月21日提交的美国临时申请号62/082,823的权益,将其内容通过引用以其全文并入本文。
背景技术:
1型糖尿病(t1d)是由胰腺中产生胰岛素的β细胞的破坏(归因于对β细胞的自身免疫应答)所致的一种糖尿病形式。全球约有3.5亿人患有糖尿病,其中约5%-10%患有t1d。目前t1d无法治愈,并且t1d管理需要终身使用胰岛素。
技术实现要素:
本披露涉及用于治疗患有自身免疫性糖尿病诸如t1d的受试者、评估治疗的疗效、诊断自身免疫性糖尿病诸如t1d、以及选择受试者进行治疗的组合物和方法。如本文所述,如通过与来自患有t1d和乳糜泻的受试者的全血接触时的ip-10分泌所测量的,将肽鉴定为诱导t细胞应答。不希望受理论束缚,这些t细胞被认为是对肽内含有的表位具有特异性的致病性cd4+t细胞。因此,含有这种表位的肽可用于例如诊断自身免疫性糖尿病诸如t1d、治疗自身免疫性糖尿病诸如t1d(例如,通过耐受对肽中的表位具有特异性的t细胞)、选择受试者进行治疗、以及评估治疗疗效。
本披露的方面涉及包含至少一种肽的组合物,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的组合物中任何一种的一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
在所提供的组合物中任何一种的一些实施例中,该组合物包含至少两种肽,其中第一肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位;并且第二肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的组合物中任何一种的一些实施例中,该第一或第二肽的至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
在所提供的组合物中任何一种的一些实施例中,该组合物包含至少三种肽,其中第一肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位;第二肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位;并且第三肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的组合物中任何一种的一些实施例中,该第一、第二或第三肽的至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
在所提供的组合物中任何一种的一些实施例中,这些肽中的至少一种包含在n-末端和/或c-末端的修饰。在所提供的组合物中任何一种的一些实施例中,这些肽中的至少一种包含n-末端焦谷氨酸酯或乙酰基基团和/或c-末端酰胺基团。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种都包含n-末端焦谷氨酸酯或乙酰基基团和/或c-末端酰胺基团。
在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地为8至50个氨基酸之间。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地为8至30个氨基酸之间。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地为8至20个氨基酸之间。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地为8至18个氨基酸之间。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地不超过20个氨基酸。在所提供的组合物中任何一种的一些实施例中,这些肽中的每种的长度都独立地不超过18个氨基酸。
在所提供的组合物中任何一种的一些实施例中,该至少一种、两种或三种肽,或该至少一种、两种或三种肽中的每种不是tpktrreaedlqvgqvel(seqidno:15)、tpktrreaedlqvgqvelgggp(seqidno:16)、malwmrllpllallalwgpdpaaa(seqidno:17)、mrllpllallalwgpdpaaa(seqidno:18)、gergffytpktrreaedlqv(seqidno:19)、tpktrreaedlqv(seqidno:20)、edlqvgqvelgggpga(seqidno:21)、eaedlqvgqvelgggpgagslqplalegslq(seqidno:22)、rreaedlqvgqvelgggpgagslqplalegslqkr(seqidno:23)、rreaedlqvgqvelgggpgagslqplalegslqar(seqidno:24)、hlcgshlvealylvcgergff(seqidno:25)、fvnqhlcgshlvealylvcgergffytpkt(seqidno:26)、fvnqhlcgshlvealylvcgergffytkpt(seqidno:27)、fvnqhlcgshlvealylvc(seqidno:28)、fvnqhlcgshlvealylvcgerg(seqidno:29)、fvnqhlcgshlvealylvcgergffp(seqidno:30)、fvnqhlcgshlvealylvcgergffytpk(seqidno:31)、fvnqhlcgshlvealylvcgergffytpkt(seqidno:26)、tnmftyeiapvfvlleyvtl(seqidno:32)或gergffytpktrreaedlqv(seqidno:19)。
在所提供的组合物中任何一种的一些实施例中,该组合物进一步包含药学上可接受的载体。在所提供的组合物中任何一种的一些实施例中,这些肽中的至少一种结合到a)hla分予,或b)能够结合该肽的hla分子的片段。
在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一个t细胞表位不是cd8+t细胞表位。在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一个t细胞表位不包含lpllallal(seqidno:76)。
本披露的其他方面涉及包含一种或多种多核苷酸的组合物,该一种或多种多核苷酸编码本文所述组合物中任何一种的肽。
本披露的又其他方面涉及包含本文所述的组合物中任何一种的分离的抗原呈递细胞。
本披露的其他方面涉及包含本文所述的组合物中的任何一种和检测组合物中的肽中的一种或多种与t细胞的结合的至少一种手段的试剂盒。在这些试剂盒中任何一种的一些实施例中,检测组合物中的肽中的一种或多种与t细胞的结合的至少一种手段是对细胞因子具有特异性的抗体。在这些试剂盒中任何一种的一些实施例中,该细胞因子选自ifn-γ、il-2或ip-10。在这些试剂盒中任何一种的一些实施例中,该细胞因子是il-2和ip-10。在这些试剂盒中任何一种的一些实施例中,该细胞因子是ifn-γ、il-2和ip-10。
本披露的另一个方面涉及用于治疗受试者的1型糖尿病(t1d)的方法,该方法包括向患有或怀疑患有t1d的受试者给予有效量的本文所述的组合物中的任何一种或本文所述的抗原呈递细胞中的任何一种。
本披露的其他方面涉及用于将受试者鉴定为患有t1d或有患t1d的风险的方法,该方法包括在包含来自该受试者的t细胞的样品中测定对本文所述的组合物中的任何一种或本文所述的抗原呈递细胞中的任何一种的t细胞应答;并评估该受试者是否患有t1d或是否有患t1d的风险。
在所提供的方法中任何一种的一些实施例中,该评估包括将受试者鉴定为(i)如果与对照t细胞应答相比,对组合物的t细胞应答升高,则患有t1d或有患t1d的风险,或(ii)如果对组合物的t细胞应答与对照t细胞应答相比降低或与对照t细胞应答相同,则未患t1d或没有患t1d的风险。
在所提供的方法中任何一种的一些实施例中,该测定步骤包括使样品与组合物接触并测量对该组合物的t细胞应答。在所提供的方法中任何一种的一些实施例中,使样品与包含0.4微克/ml、1微克/ml、4微克/ml、5微克/ml、10微克/ml、20微克/ml、25微克/ml或50微克/ml本文所述的至少一种肽的组合物接触。
在所提供的方法中任何一种的一些实施例中,测量对组合物的t细胞应答包括测量样品中至少一种细胞因子的水平。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2或ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是il-2和ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2和ip-10。
在所提供的方法中任何一种的一些实施例中,测量包括酶联免疫吸附测定(elisa)、酶联免疫吸附点(elispot)测定或多重珠基免疫测定。在所提供的方法中任何一种的一些实施例中,样品包含全血或外周血单核细胞。在所提供的方法中任何一种的一些实施例中,包含t细胞的样品包含来自受试者的新鲜血液。在所提供的方法中任何一种的一些实施例中,使样品与组合物接触约18至约30小时,例如约24小时。在所提供的方法中任何一种的一些实施例中,使样品在96孔板中与组合物接触。
在所提供的方法中任何一种的一些实施例中,该方法进一步包括如果被鉴定为患有t1d或有患t1d的风险则对受试者进行治疗,或者向受试者提供关于治疗的信息。在所提供的方法中任何一种的一些实施例中,受试者患有t1d和乳糜泻。
本披露的其他方面涉及用于评估受试者的i型糖尿病的治疗疗效的方法,该方法包括:(a)在来自已经给予致耐受性治疗的受试者的样品中测量对本文所述的组合物中的任何一种或本文所述的抗原呈递细胞中的任何一种的t细胞应答;并且(b)基于该测量来评估疗效。
在所提供的方法中任何一种的一些实施例中,该方法进一步包括(c)基于该评估来对受试者进行治疗或向受试者给出治疗建议。在所提供的方法中任何一种的一些实施例中,该方法进一步包括给予致耐受性治疗。在所提供的方法中任何一种的一些实施例中,致耐受性治疗是本文所述的组合物中的任何一种或本文所述的抗原呈递细胞中的任何一种。
在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估等于或高于对照t细胞应答,则该治疗包括继续治疗,或者该建议包括建议受试者继续治疗。在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估低于对照t细胞应答,则该治疗包括停止治疗,或者该建议包括建议受试者停止治疗。在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估低于对照t细胞应答,则该治疗包括给予不同的或另外的治疗,或者该建议包括建议受试者用另外的或不同的治疗来治疗。
在所提供的方法中任何一种的一些实施例中,通过测量在使来自受试者的样品与组合物或抗原呈递细胞接触后由该样品中的t细胞分泌的至少一种细胞因子的水平,来测量对组合物或抗原呈递细胞的t细胞应答。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2或ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是il-2和ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2和ip-10。
在所提供的方法中任何一种的一些实施例中,该样品包含来自受试者的新鲜血液。在所提供的方法中任何一种的一些实施例中,使样品与组合物接触约18至约30小时,例如约24小时。在所提供的方法中任何一种的一些实施例中,使样品在96孔板中与组合物接触。
在所提供的方法中任何一种的一些实施例中,受试者患有t1d和乳糜泻。
本披露的其他方面涉及用于选择患有i型糖尿病的受试者进行治疗的方法,该方法包括:(a)在来自患有i型糖尿病的受试者的样品中测量对本文所述的组合物中的任何一种或本文所述的抗原呈递细胞中的任何一种的t细胞应答;并且(b)如果t细胞应答等于或高于对照t细胞应答,则对受试者进行治疗或向受试者给出治疗建议。
在所提供的方法中任何一种的一些实施例中,该治疗是向受试者给予组合物或抗原呈递细胞。
在所提供的方法中任何一种的一些实施例中,通过测量在使来自受试者的样品与组合物或抗原呈递细胞接触后由该样品中的t细胞分泌的至少一种细胞因子的水平,来测量对组合物或抗原呈递细胞的t细胞应答。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2或ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是il-2和ip-10。在所提供的方法中任何一种的一些实施例中,该至少一种细胞因子是ifn-γ、il-2和ip-10。
在所提供的方法中任何一种的一些实施例中,该样品包含来自受试者的新鲜血液。在所提供的方法中任何一种的一些实施例中,使样品与组合物接触约18至约30小时,例如约24小时。在所提供的方法中任何一种的一些实施例中,使样品在96孔板中与组合物接触。
在所提供的方法中任何一种的一些实施例中,受试者患有t1d和乳糜泻。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,考虑使用实例或附图中的肽或表位中的任一种。
本披露的一个或多个实施例的细节在以下说明中阐述。本披露的其他特征或优点将从以下附图和若干实施例的详细描述并且还从所附权利要求中显而易见。
附图说明
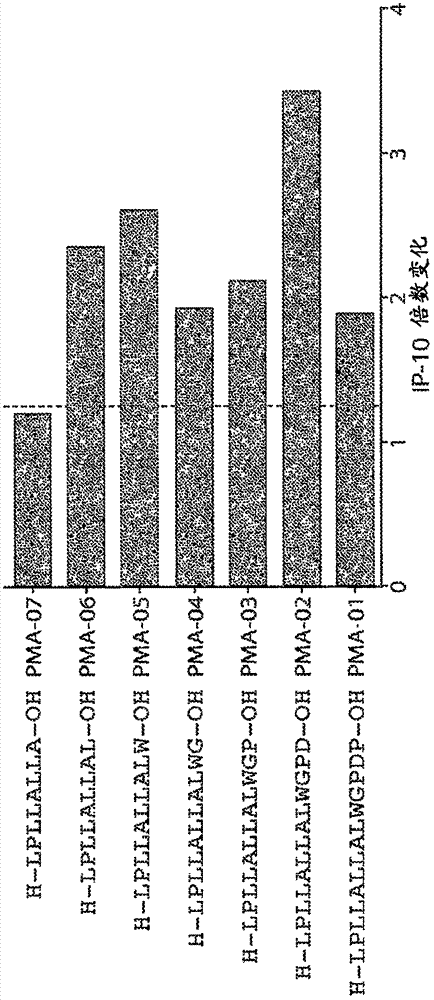
图1a-图1c是描绘针对前胰岛素原p10-20中的显性11聚体表位的精细表位作图,在患有t1d的4名受试者的全血ip-10释放测定中的长度和观察到的生物活性的图:llallalwgpd(seqidno:14)。数据是4名受试者全血ip-10释放的平均值,测量为相对于单独培养基(无肽)的倍数变化。seqidno:82-97分别从上到下出现在图1a中。seqidno:75-81分别从上到下出现在图1b中。seqidno:98-104和97分别从上到下出现在图1c中。
具体实施方式
1型糖尿病(t1d)是由胰腺中产生胰岛素的β细胞的破坏(归因于对β细胞的自身免疫应答)所致的一种糖尿病形式。患有t1d的受试者可能具有hla-dr3、hla-dr4、hla-dq2和/或hla-dq8易感性等位基因。不希望被理论束缚,据信这样的个体对自身抗原中存在的hla-dr3-、hla-dr4-、hla-dq2-和/或hla-dq8-限制性表位施加不适当的cd4+t细胞介导的免疫应答,导致β细胞的破坏。如本文所述,进行肽筛选以鉴定具有引起cd4+t细胞应答的表位的肽,例如在全血测定中通过ip-10分泌测量的。几种肽被鉴定为具有与从患有t1d和乳糜泻的受试者获得的全血接触时引起t细胞应答的表位。t细胞应答在谷蛋白激发前后没有变化,与相同受试者的谷蛋白肽的t细胞应答不同,表明这些肽也可用于治疗未患乳糜泻的受试者的自身免疫性糖尿病(例如,t1d)。
因此,本披露提供了与治疗自身免疫性糖尿病(例如,t1d)、诊断自身免疫性糖尿病(例如,t1d)、评估自身免疫性糖尿病(例如,t1d)的治疗疗效、以及选择受试者进行自身免疫性糖尿病(例如,t1d)的治疗相关的组合物、试剂盒和方法。
肽和含有肽的组合物
本披露的方面涉及肽和肽在组合物、方法、试剂盒等中的用途。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,提供了至少一种肽(例如,1、2、3种或更多种肽),该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。在一些实施例中,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13)。在一些实施例中,该至少一种肽中的每种的长度都独立地为至少8或9个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至50个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至18、8至17、8至16、8至15、8至14、8至13、8至12或8至11个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至18个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过18个氨基酸。
在本文所述的至少一个氨基酸序列内含有的至少一个t细胞表位可以通过本领域已知的或本文描述的任何方法来鉴定。例如,含有选自pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13)的氨基酸序列的肽的丙氨酸或赖氨酸扫描(例如,通过用丙氨酸或赖氨酸取代每个氨基酸位置,或者如果该位置的氨基酸已经是丙氨酸,则用非保守氨基酸进行取代)可被用于测定该肽内较短的氨基酸序列,其导致如本文所述的t细胞应答,例如在使t细胞与经丙氨酸或经赖氨酸取代的肽接触时导致ip-10释放。从免疫反应性序列的n-和c-末端的连续单氨基酸截短也可用于测定对于t细胞识别至关重要的表位的核心序列,典型地例如长度为9个氨基酸。可以使用从t1d患者血液募集的单独的t细胞克隆以进一步测定证实最小核心序列的单独表位的限制。
在一些实施例中,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13)。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一种肽包含选自实例或附图中提供的序列中任何一个的至少一个氨基酸序列。在一些实施例中,该至少一种肽中的每种的长度都独立地为至少8或9个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至50个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至18、8至17、8至16、8至15、8至14、8至13、8至12或8至11个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至18个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过18个氨基酸。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,提供了至少两种肽(例如,2、3种或更多种肽),其中第一肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位,并且第二肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位,其中该第一肽和该第二肽的序列有一个或多个氨基酸不同。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,提供了至少两种肽,第一肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位;第二肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位;并且第三肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位,其中该第一肽、该第二肽和该第三肽的序列彼此有一个或多个氨基酸不同。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,提供了至少两种肽(例如,2、3种或更多种肽),其中第一肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13),并且第二肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13),其中该第一肽和该第二肽的序列有一个或多个氨基酸不同。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。因此,本文所述的肽中的任何一种(例如,第一、第二或第三肽)可以包含氨基酸序列llallalwgpd(seqidno:14)。在一些实施例中,该至少两种肽中的每种的长度都独立地为至少8或9个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至50个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至30个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至19个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为8至18、8至17、8至16、8至15、8至14、8至13、8至12或8至11个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地为10至18个氨基酸之间。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过20个氨基酸。在一些实施例中,该至少一种肽中的每种的长度都独立地不超过18个氨基酸。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一种肽不是tpktrreaedlqvgqvel(seqidno:15)、tpktrreaedlqvgqvelgggp(seqidno:16)、malwmrllpllallalwgpdpaaa(seqidno:17)、mrllpllallalwgpdpaaa(seqidno:18)、gergffytpktrreaedlqv(seqidno:19)、tpktrreaedlqv(seqidno:20)、edlqvgqvelgggpga(seqidno:21)、eaedlqvgqvelgggpgagslqplalegslq(seqidno:22)、rreaedlqvgqvelgggpgagslqplalegslqkr(seqidno:23)、rreaedlqvgqvelgggpgagslqplalegslqar(seqidno:24)、hlcgshlvealylvcgergff(seqidno:25)、fvnqhlcgshlvealylvcgergffytpkt(seqidno:26)、fvnqhlcgshlvealylvcgergffytkpt(seqidno:27)、fvnqhlcgshlvealylvc(seqidno:28)、fvnqhlcgshlvealylvcgerg(seqidno:29)、fvnqhlcgshlvealylvcgergffp(seqidno:30)、fvnqhlcgshlvealylvcgergffytpk(seqidno:31)、fvnqhlcgshlvealylvcgergffytpkt(seqidno:26)、tnmftyeiapvfvlleyvtl(seqidno:32)或gergffytpktrreaedlqv(seqidno:19)。
在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一个t细胞表位不是cd8+t细胞表位。在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一个t细胞表位不包含lpllallal(seqidno:76)。
示例性肽和用于合成或获得这样的肽的方法是本领域已知的并且在本丈中进行了描述。肽可以重组地和/或合成地产生。在一些实施例中,肽是用化学方法合成的,例如使用本领域已知的方法。肽合成的非限制性实例包括液相合成和固相合成。在一些实施例中,通过酶消化产生肽,例如通过将较大的多肽酶消化成短肽。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的一个或多个谷氨酸残基可以通过组织型转谷氨酰胺酶(ttg)对该肽的一个或多个谷氨酸残基的脱酰胺活性来产生。这种谷氨酰胺至谷氨酸的脱酰胺可能导致产生可以高亲和力结合hla-dq2或hla-dq8分子的肽。这个反应可以通过使该肽与受试者体外的ttg接触而在体外发生或者在给药后通过体内的ttg脱酰胺而在体内发生。肽的脱酰胺也可以通过用谷氨酸残基代替一个或多个谷氨酰胺残基从头合成肽来实现,并且因此脱酰胺不一定需要使用ttg。例如,在一些实施例中,可以将包含氨基酸序列rreaedlqgsl(seqidno:3)的肽脱酰胺成rreaedlegsl(seqidno:4)和/或可以将包含氨基酸序列dlqvgqvelgggp(seqidno:5)的肽脱酰胺成dlqvgevelgggp(seqidno:6)。除了非脱酰胺形式之外或代替非脱酰胺形式,本文提供的组合物中的任何一种都可以包含脱酰胺形式。本文组合物、方法、试剂盒或抗原呈递细胞中任何一种中所述的肽中的任何一种都可以是脱酰胺形式,代替非脱酰胺形式。
在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,可以令人希望的是利用这样的肽的非脱酰胺形式,例如,如果这些肽包含在用于给予组织型转谷氨酰胺酶将原位发挥作用的受试者的组合物内的话(参见例如,
肽也可以是本文所述的肽中任何一种的类似物。优选地,在一些实施例中,识别本文所述的肽中的一种或多种的cd4+t细胞识别该类似物。示例性的类似物包含如下肽,该肽具有与本文列举的肽例如75%、80%、85%、90%、95%、96%、97%、98%或99%同源的序列。类似物也可以是所提供的肽中任何一种的变体,这样的变体可以包括保守的氨基酸取代。
肽的长度可以变化。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为例如8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50个或更多个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为例如8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、60、70、80、90或100个或更少个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为例如8-100、8-50、8-40、8-30或8-20个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为4-20、5-20、6-20、7-20、8-20、9-20、10-20、11-20、12-20、13-20、14-20或15-20个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为例如10-19、11-19、12-19或13-19个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,肽的长度为4-50、5-50、6-50、7-50、8-50、9-50、10-50、11-50、12-50、13-50、14-50或15-50个氨基酸。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,该至少一种肽中的每种的长度都独立地为8至50个氨基酸之间。
在所提供的组合物中任何一种的一些实施例中,考虑了包含一种或一种或多种肽的组合物。在一些实施例中,该组合物包含至少一种(例如,1、2、3种或更多种)肽,该至少一种肽包含选自如下项的至少一个(例如,1、2、3个或更多个)氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的t细胞表位。在一些实施例中,该组合物包含至少一种(例如,1、2、3种或更多种)肽,该至少一种肽包含选自如下项的至少一个(例如,1、2、3个或更多个)氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、或pkaarppvtpvllekks(seqidno:13)。在所提供的组合物中任何一种的一些实施例中,该至少一种(例如,1、2、3、3种或更多种)肽的至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
“第一”、“第二”、“第三”等并不意味着隐含使用或重要性顺序,除非另外明确说明。在一些实施例中,该组合物包含本文提供的任何肽中的至少一种、至少两种、至少三种、或更多种。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,这些肽中的至少一种包含n-末端修饰(例如,焦谷氨酸酯或乙酰基基团)和/或c-末端修饰(例如,酰胺基团)。在本文提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,这些肽中的每种都包含n-末端修饰(例如,焦谷氨酸酯或乙酰基基团)和/或c-末端修饰(例如,酰胺基团)。
在本文中也考虑了对肽的修饰。这种修饰可以在翻译或合成期间或之后发生(例如,通过法呢酰化、异戊二烯化、肉豆蔻酰化、糖基化、棕榈酰化、乙酰化、磷酸化(诸如磷酸酪氨酸、磷酸丝氨酸或磷酸苏氨酸)、酰胺化、热化(pyrolation)、通过已知的保护/封闭基团衍生化、蛋白水解切割、与抗体分子或其他细胞配体连接等)。可以利用本领域已知的许多化学修饰方法中的任一种,包括但不限于通过溴化氰、胰蛋白酶、糜蛋白酶、木瓜蛋白酶、v8蛋白酶、nabh4进行的特异性化学切割,乙酰化,甲酰化,氧化,还原,在衣霉素存在下的代谢合成等。
如本文所用的短语“保护基团”和“封闭基团”是指对肽的修饰,这些修饰保护其免受不希望的化学反应,特别是体内化学反应的影响。这样的保护基团的实例包括羧酸和硼酸的酯、醇和缩醛的醚、以及醛和酮的缩酮。合适的基团的实例包括酰基保护基团,例如像糠酰基、甲酰基、己二酰基、壬二酰基(azelayl)、环庚基、丹酰基、乙酰基、戊基(theyl)、苯甲酰基、三氟乙酰基、琥珀酰基和甲氧基琥珀酰基;芳香族聚氨酯保护基团,例如像苄氧基羰基(cbz);脂肪族聚氨酯保护基团,例如像叔丁氧基羰基(boc)或9-芴基甲氧基-羰基(fmoc);焦谷氨酸酯或乙酰化和酰胺化。提供增加的效力、延长时间的活性、易于纯化和/或增加的半衰期的许多其他修饰是本领域技术人员已知的。
这些肽中的任何一种或多种可以包含一种或多种修饰,其可以是天然的翻译后修饰或人为修饰。修饰可以提供化学部分(典型地通过氢的取代,例如c-h键的取代),诸如氨基、乙酰基、酰基、羧基、羟基或卤素(例如,氟)基团或碳水化合物基团。典型地,修饰存在于n-和/或c-末端。此外,这些肽中的任何一种或多种可以被聚乙二醇化,其中peg(聚乙烯氧基基团)提供在血流中增加的寿命。这些肽中的任何一种或多种也可以与其他蛋白质或与允许靶向靶细胞上的特定部分的特异性结合剂组合作为融合或嵌合蛋白。
也可以在氨基酸侧链、氨基酸手性和/或肽骨架的水平上对肽进行化学修饰。
可以对肽进行特殊的改变以与亲本肽相比改善降解抗性或优化溶解性,或者以另外的方式改善生物利用度,从而提供具有相似或改善的治疗、诊断和/或药代动力学特性的肽。优选的这种修饰包括使用n-末端乙酰基基团或焦谷氨酸酯和/或c-末端酰胺。与具有游离n-和c-末端的亲本肽相比,本领域已经显示出这样的修饰显著增加这些肽的半衰期和生物利用度(参见例如,pct公开号:wo/2010/060155)。在一些实施例中,这些肽中的任何一种或多种包含n-末端乙酰基基团或焦谷氨酸酯基团和/或c-末端酰胺基团。
肽生产
本文所述的肽能以任何合适的方式来制备。例如,这些肽可以是重组地和/或合成地产生的。
这些肽可以通过标准化学技术合成,包括使用可商购的肽合成仪通过自动化程序来合成。通常,肽可以通过固相肽合成方法来制备,其可以涉及通过用二环己基碳二亚胺活化来将每个受保护的氨基酸残基偶联到树脂支持体(优选4-甲基二苯甲基胺树脂)上,以产生具有c-末端酰胺的肽。可替代地,可以使用氯甲基树脂(merrifield树脂)产生在c-末端具有游离羧酸的肽。在最后一个残基附着后,用氟化氢处理受保护的肽-树脂,以从树脂中切割肽,并使侧链官能团脱保护。粗产物可以通过凝胶过滤、高压液相层析(hplc)、分配层析或离子交换层析进一步纯化。
如果需要,可以在合成期间或在表达期间将各个基团引入肽中,从而允许与其他分子或表面连接。例如,半胱氨酸可以用于制备硫醚、用于连接到金属离子络合物的组氨酸、用于形成酰胺或酯的羧基基团、用于形成酰胺的氨基基团等。
肽也可以使用无细胞翻译系统来生产。标准翻译系统诸如网织红细胞裂解物和小麦胚芽提取物使用rna作为模板;而“偶联”和“连接”系统则从dna模板开始,将所述模板转录成rna,然后进行翻译。
可替代地,可以通过用包含编码一种或多种肽的多核苷酸的表达载体转染宿主细胞来生产这些肽。
对于重组生产,将包含编码这些肽中一种或多种的序列的重组构建体通过常规方法诸如磷酸钙转染、deae-葡聚糖介导的转染、显微注射、阳离子脂质介导的转染、电穿孔、转导、划痕装载(scrapelading)、轰击引入或感染引入宿主细胞中。
这些肽中的一种或多种可以使用常规技术在合适的宿主细胞,例如像哺乳动物细胞(例如,cos、cho、bhk、293hek、vero、hela、hepg2、mdck、w138或nih3t3细胞)、酵母(例如,酵母属或毕赤酵母属)、细菌(例如,大肠杆菌、毕赤酵母或枯草芽孢杆菌)、昆虫细胞(例如,sf9细胞中的杆状病毒)或其他细胞中在适当启动子的控制下表达。在转化合适的宿主菌株并使该宿主菌株生长到适当的细胞密度后,通过离心收获细胞,通过物理或化学手段破坏,并保留所得粗提取物以进一步纯化肽或其变体。
合适的表达载体包括例如染色体的、非染色体的和合成的多核苷酸,例如sv40的衍生物,细菌质粒,噬菌体dna,酵母质粒,衍生自质粒和噬菌体dna的组合的载体,病毒dna诸如痘苗病毒、腺病毒、腺相关病毒、慢病毒、金丝雀痘病毒、禽痘病毒、伪狂犬病病毒、杆状病毒、疱疹病毒和逆转录病毒。可以通过本领域已知的常规程序将多核苷酸引入表达载体中。
编码一种或多种肽的多核苷酸可以被可操作地连接到指导mrna合成的表达控制序列,即启动子。这样的启动子的代表性实例包括ltr或sv40启动子、大肠杆菌lac或trp、噬菌体λpl启动子和已知控制原核或真核细胞中或病毒中基因表达的其他启动子。表达载体还可以含有用于翻译起始的核糖体结合位点和转录终止子。表达载体还可以包括复制起点和选择性标记,诸如大肠杆菌的氨苄青霉素抗性基因,以允许选择经转化的细胞,即表达异源多核苷酸的细胞。编码这些肽中一种或多种的核酸分子可以与翻译起始和终止序列同框并入载体中。
可以通过公知的方法从重组细胞培养物中(即,从细胞或培养基中)回收和纯化这些肽中的一种或多种,这些方法包括硫酸铵或乙醇沉淀、酸提取、阴离子或阳离子交换层析、磷酸纤维素层析、疏水相互作用层析、亲和层析、羟基磷灰石层析、凝集素层析和hplc。当在分离和/或纯化期间该肽被变性时,用于重折叠蛋白质的公知技术可用于再生活性构象。
为了生产糖基化肽,优选的是使用重组技术。为了生产糖基化肽,优选的是在重组技术中使用哺乳动物细胞诸如cos-7和hep-g2细胞。
肽也可以通过切割更长的肽(尤其是来自食物提取物)来制备。
肽的药学上可接受的盐可以通过常规的化学方法由含有碱性或酸性部分的肽合成。通常,通过使游离碱或酸与化学计量量的或与过量的所需的成盐无机酸或有机酸或者无机碱或有机碱在合适的溶剂中反应来制备盐。
在一些实施例中,本文所述的组合物中的任何一种进一步包含药学上可接受的载体。术语“药学上可接受的载体”是指当给予受试者,特别是哺乳动物,并且更特别是人时,不产生过敏反应、毒性反应或其他不良反应的分子实体和组合物。药学上可接受的载体可以是固体或液体。药学上可接受的载体的有用实例包括但不限于稀释剂、赋形剂、溶剂、表面活性剂、悬浮剂、缓冲剂、润滑剂、佐剂、运载体、乳化剂、吸收剂、分散介质、涂料、稳定剂、保护胶体、粘合剂、增稠剂、触变剂、渗透剂、螯合剂、等渗剂和吸收延迟剂,它们不影响药物组合物的活性剂的活性。该载体可以是常规使用的那些中的任何一种,并且仅受化学-物理考虑因素(诸如可溶性和缺乏与活性剂的反应性)以及受给药途径的限制。该药物组合物的合适载体包括常规使用的那些,例如水、盐水、右旋糖水溶液、乳糖、林格氏溶液、缓冲溶液、透明质酸、二醇、淀粉、纤维素、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸镁、硬脂酸钠、单硬脂酸甘油酯、氯化钠、甘油、丙二醇、水、乙醇等。脂质体也可以用作载体。其他载体是本领域公知的(参见例如,remington:thescienceandpracticeofpharmacy,21sted.lippincottwilliams&wilkins,2005[雷明顿:药物科学与实践,第21版,利平科特·威廉姆斯&威尔金斯出版公司,2005])。
评估治疗疗效和选择受试者进行治疗
本披露的方面涉及评估受试者的自身免疫性糖尿病(例如,t1d)的治疗疗效的方法。在所提供的方法中任何一种的一些实施例中,受试者患有t1d或t1d和乳糜泻。
在所提供的方法中任何一种的一些实施例中,该方法包括:
(a)在来自已经给予致耐受性治疗(诸如肽组合物或包含肽的抗原呈递细胞)的受试者的样品中测量对包含本文所述的至少一种肽或本文所述的抗原呈递细胞的组合物的t细胞应答;
(b)基于该测量来评估疗效。
在所提供的方法中任何一种的一些实施例中,该方法包括:
(a)在来自已经给予组合物或抗原呈递细胞的受试者的样品中测量对包含本文所述的至少一种肽或本文所述的抗原呈递细胞的组合物的t细胞应答;并且
(b)基于该测量来评估疗效。该组合物可以是本文提供的组合物中的任何一种。
在所提供的方法中任何一种的一些实施例中,该方法进一步包括(c)基于该评估来对受试者进行治疗或向受试者给出治疗建议。在所提供的方法中任何一种的一些实施例中,该方法进一步包括给予致耐受性治疗。在所提供的方法中任何一种的一些实施例中,该方法进一步包括向受试者给予组合物或抗原呈递细胞。在一些实施例中,该组合物包含至少一种肽,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的组合物中任何一种的一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估等于或高于对照t细胞应答,则该治疗包括继续治疗,或者该建议包括建议受试者继续治疗。在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估低于对照t细胞应答,则该治疗包括停止治疗,或者该建议包括建议受试者停止治疗。在所提供的方法中任何一种的一些实施例中,基于评估,如果指示t细胞应答的评估低于对照t细胞应答,则该治疗包括给予不同的或另外的治疗,或者该建议包括建议受试者用另外的或不同的治疗来治疗。
在所提供的方法中任何一种的一些实施例中,通过测量在使来自受试者的样品与组合物或抗原呈递细胞接触后由该样品中的t细胞分泌的细胞因子的水平,来测量对组合物或抗原呈递细胞的t细胞应答。在一些实施例中,已经使样品与包含0.4微克/ml、1微克/ml、4微克/ml、5微克/ml、10微克/ml、20微克/ml、25微克/ml或50微克/ml本文所述的至少一种肽的组合物接触。在一些实施例中,该细胞因子是ifn-γ、il-2或ip-10中的一种或多种。在一些实施例中,该细胞因子是ip-10。
在一些实施例中,样品包含来自受试者的新鲜血液。在一些实施例中,使样品与组合物接触约18至约30小时,例如约24小时。在一些实施例中,使样品在96孔板中与组合物接触。
本披露的其他方面涉及选择患有自身免疫性糖尿病(例如,t1d)的受试者进行治疗的方法。在这些方法中任何一种的一些实施例中,受试者患有t1d或t1d和乳糜泻。在所提供的方法中任何一种的一些实施例中,该方法包括(a)在来自患有自身免疫性糖尿病(例如,t1d)的受试者的样品中测量对包含本文所述的至少一种肽或本文所述的抗原呈递细胞的组合物的t细胞应答;并且(b)如果t细胞应答等于或高于对照t细胞应答,则对受试者进行治疗或向受试者给出治疗建议。该组合物可以是本文提供的组合物中的任何一种。在一些实施例中,该组合物包含至少一种肽,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的方法中任何一种的一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。
在所提供的方法中任何一种的一些实施例中,该治疗包括向受试者给予组合物或抗原呈递细胞。
在所提供的方法中任何一种的一些实施例中,通过测量在使来自受试者的样品与组合物或抗原呈递细胞接触后由该样品中的t细胞分泌的细胞因子的水平,来测量对组合物或抗原呈递细胞的t细胞应答。在一些实施例中,该细胞因子是ifn-γ、il-2或ip-10中的一种或多种。在一些实施例中,该细胞因子是ip-10。
在一些实施例中,样品包含来自受试者的新鲜血液。在一些实施例中,使样品与抗原呈递细胞接触约18至约30小时,例如约24小时。在一些实施例中,使样品在96孔板中与抗原呈递细胞接触。
t细胞应答及其测量
本披露的方面涉及包含来自受试者的t细胞的样品中的t细胞应答的确定或测量。可以例如通过测量包含来自受试者的t细胞的样品中的t细胞应答来离体地测量这样的t细胞应答。
如本文所述,与对照t细胞应答相比,包含来自受试者的t细胞的样品中升高的t细胞应答(诸如升高的cd4+t细胞应答)可能与自身免疫性糖尿病(例如,t1d)的存在相关。因此,本披露的方面涉及包括确定或测量包含来自受试者(例如,患有或怀疑患有自身免疫性糖尿病(例如,t1d))的t细胞的样品中的t细胞应答的方法。在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,升高的t细胞应答是cd4+t细胞应答。在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,升高的t细胞应答是cd8+t细胞应答。在所提供的组合物、肽、方法、试剂盒或抗原呈递细胞中任何一种的一些实施例中,升高的t细胞应答是cd4+而不是cd8+t细胞应答。
在所提供的方法中任何一种的一些实施例中,测量包含来自受试者的t细胞的样品中的t细胞应答包括使样品与包含本文所述的至少一种肽的组合物接触。该组合物可以是本文提供的组合物中的任何一种。例如,从受试者获得的全血或pbmc可以与包含肽的组合物接触,以刺激全血样品或pbmc中的t细胞。
可以使用本领域已知的任何测定来测量t细胞应答(参见例如,molecularcloning:alaboratorymanual,m.greenandj.sambrook,fourthedition,coldspringharborlaboratorypress,coldspringharbor,newyork,2012[分子克隆:实验室手册,m.green和j.sambrook,第四版,冷泉港实验室出版社,冷泉港,纽约,2012];currentprotocolsinmolecularbiology,f.m.ausubel,etal.,currentedition,johnwiley&sons,inc.,newyork[分子生物学实验指南,f.m.ausubel等人,现行版,约翰威利父子公司,纽约])。在一些实施例中,测量t细胞应答包括mhcii类四聚体测定,诸如进行mhcii类四聚体染色的流式细胞术(参见例如,rakim,fallangle,brottveitm,bergsenge,quarstenh,lundinke,sollidlm:tetramervisualizationofgut-hominggluten-specifictcellsintheperipheralbloodofceliacdiseasepatients.proceedingsofthenationalacademyofsciencesoftheunitedstatesofamerica2007[rakim、fallangle、brottveitm、bergsenge、quarstenh、lundinke、sollidlm:在乳糜泻患者的外周血中肠道归巢谷蛋白特异性t细胞的四聚体可视化,美国国家科学院院刊,2007];andersonrp,vanheelda,tye-dinja,barnardom,saliom,jewelldp,hillav:tcellsinperipheralbloodafterglutenchallengeincoeliacdisease.gut2005,54(9):1217-1223[andersonrp、vanheelda、tye-dinja、barnardom、saliom、jewelldp、hillav:乳糜泻中谷蛋白激发后外周血中的t细胞,肠道,2005,54(9):1217-1223];brottveitm,rakim,bergsenge,fallangle,simonsenb,lovika,larsens,lobergem,jahnsenfl,sollidlmetal:assessingpossibleceliacdiseasebyanhla-dq2-gliadintetramertest.theamericanjournalofgastroenterology2011,106(7):1318-1324[brottveitm、rakim、bergsenge、fallangle、simonsenb、lovika、larsens、lobergem、jahnsenfl、sollidlm等人:通过hla-dq2-醇溶蛋白四聚物测试评估可能的乳糜泻,美国胃肠病学杂志,2011,106(7):1318-1324];以及andersonrp,deganop,godkinaj,jewelldp,hillav:invivoantigenchallengeinceliacdiseaseidentifiesasingletransglutaminase-modifiedpeptideasthedominanta-gliadintcellepitope.naturemedicine2000,6(3):337-342[andersonrp、deganop、godkinaj、jewelldp、hillav:乳糜泻中的体内抗原激发将单一转谷氨酰胺酶修饰肽鉴定为显性的a-醇溶蛋白t细胞抗原,自然医学,2000,6(3):337-342])。
在这些方法中任何一种的一些实施例中,测量包含来自受试者的t细胞的样品中的t细胞应答包括测量样品中至少一种细胞因子的水平。在这些方法中任何一种的一些实施例中,测量包含来自受试者的t细胞的样品中的t细胞应答包括使样品与包含本文所述的至少一种肽的组合物接触,并测量样品中至少一种细胞因子的水平。在这些方法中任何一种的一些实施例中,该至少一种细胞因子是il-2、ifn-γ或ip-10。在这些方法中任何一种的一些实施例中,该至少一种细胞因子包括il-2、ifn-γ和ip-10的全部三种。在这些方法中任何一种的一些实施例中,该至少一种细胞因子是ip-10。在这些方法中任何一种的一些实施例中,该至少一种细胞因子是ip-10、il-2和ifn-γ。
干扰素-γ(ifn-γ,也称为ifng、ifg和ifi)是ii类干扰素类型的二聚可溶性细胞因子。ifn-γ典型地与由干扰素γ受体1(ifngr1)和干扰素γ受体2(ifngr2)组成的异源二聚受体结合。ifn-γ也可以与糖胺聚糖硫酸乙酰肝素(hs)结合。ifn-γ主要由天然杀伤细胞(nk)和天然杀伤t(nkt)细胞产生,作为先天免疫应答的一部分,并且一旦抗原特异性免疫在受试者体内发展,由cd4th1和cd8细胞毒性t淋巴细胞(ctl)效应t细胞产生。在人类中,ifn-γ蛋白由ifng基因编码。人类ifng基因的genbank号为3458。ifn-γ的示例性genbankmrna转录物id和蛋白质id分别为nm_000619.2和np_000610.2。下文提供了ifn-γ的示例性rna和蛋白质序列。
>gi|56786137|ref|nm_000619.2|智人干扰素,γ(ifng),mrna
cacattgttctgatcatctgaagatcagctattagaagagaaagatcagttaagtcctttggacctgatcagcttgatacaagaactactgatttcaacttctttggcttaattctctcggaaacgatgaaatatacaagttatatcttggcttttcagctctgcatcgttttgggttctcttggctgttactgccaggacccatatgtaaaagaagcagaaaaccttaagaaatattttaatgcaggtcattcagatgtagcggataatggaactcttttcttaggcattttgaagaattggaaagaggagagtgacagaaaaataatgcagagccaaattgtctccttttacttcaaactttttaaaaactttaaagatgaccagagcatccaaaagagtgtggagaccatcaaggaagacatgaatgtcaagtttttcaatagcaacaaaaagaaacgagatgacttcgaaaagctgactaattattcggtaactgacttgaatgtccaacgcaaagcaatacatgaactcatccaagtgatggctgaactgtcgccagcagctaaaacagggaagcgaaaaaggagtcagatgctgtttcgaggtcgaagagcatcccagtaatggttgtcctgcctgcaatatttgaattttaaatctaaatctatttattaatatttaacattatttatatggggaatatatttttagactcatcaatcaaataagtatttataatagcaacttttgtgtaatgaaaatgaatatctattaatatatgtattatttataattcctatatcctgtgactgtctcacttaatcctttgttttctgactaattaggcaaggctatgtgattacaaggctttatctcaggggccaactaggcagccaacctaagcaagatcccatgggttgtgtgtttatttcacttgatgatacaatgaacacttataagtgaagtgatactatccagttactgccggtttgaaaatatgcctgcaatctgagccagtgctttaatggcatgtcagacagaacttgaatgtgtcaggtgaccctgatgaaaacatagcatctcaggagatttcatgcctggtgcttccaaatattgttgacaactgtgactgtacccaaatggaaagtaactcatttgttaaaattatcaatatctaatatatatgaataaagtgtaagttcacaacaaaaaaaaaaaaaaaaaaaaaaaaaaaaaa(seqidno:33)
>gi|56786138|ref|np_000610.2|干扰素γ前体[智人]
mkytsyilafqlcivlgslgcycqdpyvkeaenlkkyfnaghsdvadngtlflgilknwkeesdrkimqsqivsfyfklfknfkddqsiqksvetikedmnvkffnsnkkkrddfekltnysvtdlnvqrkaiheliqvmaelspaaktgkrkrsqmlfrgrrasq(seqidno:34)
>gi|56786138:24-166干扰素γ成熟蛋白[智人]
qdpyvkeaenlkkyfnaghsdvadngtlflgilknwkeesdrkimqsqivsfyfklfknfkddqsiqksvetikedmnvkffnsnkkkrddfekltnysvtdlnvqrkaiheliqvmaelspaaktgkrkrsqmlfrgrrasq(seqidno:35)
ifn-γ诱导型蛋白-10(ip-10,也称为c-x-c基序趋化因子10、cxcl10、小诱导型细胞因子b10、scyb10、c7、ifi10、crg-2、gip-10或mob-1)是在人类中由cxcl10基因编码的蛋白质。ip-10是属于cxc趋化因子家族的小细胞因子,并结合趋化因子受体cxcr3。人类cxcl10基因的genbankid号为3627。ip-10的示例性genbankmrna转录物id和蛋白质id分别为nm_001565.3和np_001556.2。下文提供了ip-10的示例性序列。
>gi|323422857|ref|nm_001565.3|智人趋化因子(c-x-c基序)配体10(cxcl10),mrna
ctttgcagataaatatggcacactagccccacgttttctgagacattcctcaattgcttagacatattctgagcctacagcagaggaacctccagtctcagcaccatgaatcaaactgccattctgatttgctgccttatctttctgactctaagtggcattcaaggagtacctctctctagaactgtacgctgtacctgcatcagcattagtaatcaacctgttaatccaaggtctttagaaaaacttgaaattattcctgcaagccaattttgtccacgtgttgagatcattgctacaatgaaaaagaagggtgagaagagatgtctgaatccagaatcgaaggccatcaagaatttactgaaagcagttagcaaggaaaggtctaaaagatctccttaaaaccagaggggagcaaaatcgatgcagtgcttccaaggatggaccacacagaggctgcctctcccatcacttccctacatggagtatatgtcaagccataattgttcttagtttgcagttacactaaaaggtgaccaatgatggtcaccaaatcagctgctactactcctgtaggaaggttaatgttcatcatcctaagctattcagtaataactctaccctggcactataatgtaagctctactgaggtgctatgttcttagtggatgttctgaccctgcttcaaatatttccctcacctttcccatcttccaagggtactaaggaatctttctgctttggggtttatcagaattctcagaatctcaaataactaaaaggtatgcaatcaaatctgctttttaaagaatgctctttacttcatggacttccactgccatcctcccaaggggcccaaattctttcagtggctacctacatacaattccaaacacatacaggaaggtagaaatatctgaaaatgtatgtgtaagtattcttatttaatgaaagactgtacaaagtagaagtcttagatgtatatatttcctatattgttttcagtgtacatggaataacatgtaattaagtactatgtatcaatgagtaacaggaaaattttaaaaatacagatagatatatgctctgcatgttacataagataaatgtgctgaatggttttcaaaataaaaatgaggtactctcctggaaatattaagaaagactatctaaatgttgaaagatcaaaaggttaataaagtaattataactaagaaaaaaaaaaaa(seqidno:36)
>gi|149999382|ref|np_001556.2|c-x-c基序趋化因子10前体[智人]
mnqtailicclifltlsgiqgvplsrtvrctcisisnqpvnprslekleiipasqfcprveiiatmkkkgekrclnpeskaiknllkavskerskrsp(seqidno:37)
>gi|149999382:22-98c-x-c基序趋化因子10成熟蛋白[智人]
vplsrtvrctcisisnqpvnprslekleiipasqfcprveiiatmkkkgekrclnpeskaiknllkavskerskrsp(seqidno:38)
白细胞介素-2(il-2)是在人类中由il2基因编码的蛋白质。il-2是分泌型细胞因子并结合到例如异源三聚蛋白受体白细胞介素-2受体(il-2r)。人类il2基因的genbankid号为3558。下文示出了il-2的示例性mrna序列和蛋白质序列。
>gi|125661059|ref|nm_000586.3|智人白细胞介素2(il2),mrna
agttccctatcactctctttaatcactactcacagtaacctcaactcctgccacaatgtacaggatgcaactcctgtcttgcattgcactaagtcttgcacttgtcacaaacagtgcacctacttcaagttctacaaagaaaacacagctacaactggagcatttactgctggatttacagatgattttgaatggaattaataattacaagaatcccaaactcaccaggatgctcacatttaagttttacatgcccaagaaggccacagaactgaaacatcttcagtgtctagaagaagaactcaaacctctggaggaagtgctaaatttagctcaaagcaaaaactttcacttaagacccagggacttaatcagcaatatcaacgtaatagttctggaactaaagggatctgaaacaacattcatgtgtgaatatgctgatgagacagcaaccattgtagaatttctgaacagatggattaccttttgtcaaagcatcatctcaacactgacttgataattaagtgcttcccacttaaaacatatcaggccttctatttatttaaatatttaaattttatatttattgttgaatgtatggtttgctacctattgtaactattattcttaatcttaaaactataaatatggatcttttatgattctttttgtaagccctaggggctctaaaatggtttcacttatttatcccaaaatatttattattatgttgaatgttaaatatagtatctatgtagattggttagtaaaactatttaataaatttgataaatataaaaaaaaaaaaaaaaaaaaaaaaaa(seqidno:39)
>gi|28178861|ref|np_000577.2|白细胞介素-2前体[智人]
myrmqllscialslalvtnsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfcqsiistlt(seqidno:40)
>gi|28178861|ref|np_000577.2|白细胞介素-2成熟蛋白[智人]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfcqsiistlt(seqidno:41)
在这些方法中任何一种的一些实施例中,测量t细胞应答包括测量至少一种细胞因子的水平。至少一种细胞因子的水平包括细胞因子rna(例如,mrna)的水平和/或细胞因子蛋白的水平。在优选的实施例中,该至少一种细胞因子的水平是蛋白质水平。
用于检测细胞因子rna的测定包括但不限于northern印迹分析、rt-pcr、测序技术、rna原位杂交(使用例如dna或rna探针来杂交样品中存在的rna分子)、原位rt-pcr(例如,如在以下文献中所述:nuovogj,eta1.amjsurgpatho1.1993,17:683-90[nuovogj等人,美国外科病理学杂志,1993,17:683-90];komminothp,etal.patholrespract.1994,190:1017-25[komminothp等人,病理研究与实践,1994,190:1017-25])和寡核苷酸微阵列(例如,通过将衍生自样品的多核苷酸序列与附着于固体表面(例如,具有可寻址位置的玻璃晶片,诸如affymetrix微阵列(
用于检测蛋白质水平的测定包括但不限于免疫测定(本文也称为基于免疫的或者基于免疫学的测定,例如western印迹、elisa和elispot测定)、质谱法和多重珠基测定。用于蛋白质检测的结合配偶体可以使用本领域已知的方法并如本文所述的来设计。在一些实施例中,蛋白质结合配偶体(例如,抗体)与至少一种细胞因子(例如,ifn-γ、il-2或ip-10)的部分或整个氨基酸序列结合。蛋白质检测和定量方法的其他实例包括例如在美国专利号6939720和8148171以及公开的美国专利申请号2008/0255766中所述的多重免疫测定,和例如在公开的美国专利申请号2009/0088329中所述的蛋白质微阵列。
本文考虑了任何合适的结合配偶体。在一些实施例中,结合配偶体是与本文提供的细胞因子特异性结合的任何分子。如果与替代靶标相比,分子与特定靶标更频繁地、更快速地、以更大的持续时间和/或以更大的亲和力反应或相关联,则其被称为展示出“特异性结合”。如本文所述,“特异性结合”,当提及蛋白质时,表示该分子更可能与待测量的蛋白质的部分或整体结合,而不是与另一种蛋白质的部分或整体结合。在一些实施例中,结合配偶体是抗体或其抗原结合片段,诸如fab、f(ab)2、fv、单链抗体、fab和sfab片段、f(ab′)2、fd片段、scfv、或dab片段。本领域公知用于生产抗体及其抗原结合片段的方法(参见例如,sambrooketal,″molecularcloning:alaboratorymanual″(2nded.),coldspringharborlaboratorypress(1989)[sambrook等人,“分子克隆:实验室手册”(第2版),冷泉港实验室出版社(1989)];lewin,″genesiv″,oxforduniversitypress,newyork,(1990)[lewin,“基因iv”,牛津大学出版社,纽约,(1990)],和roittetal.,”immunology″(2nded.),gowermedicalpublishing,london,newyork(1989)[roitt等人,“免疫学”(第2版),高尔医学出版社,伦敦,纽约(1989)],wo2006/040153,wo2006/122786,以及wo2003/002609)。结合配偶体还包括特异性结合的其他肽分子和适体。用于生产肽分子和适体的方法在本领域是公知的(参见例如,公开的美国专利申请号2009/0075834,美国专利号7435542、7807351和7239742)。在一些实施例中,结合配偶体是与mrna(例如,ifn-γ或ip-10mrna)特异性结合的任何分子。如本文所述,“与mrna特异性结合”意指分子更可能与待测量的mrna的部分或整体结合(例如,通过互补碱基配对)而不是与另一种mrna或其他核酸的部分或整体结合。在一些实施例中,与mrna特异性结合的结合配偶体是核酸,例如探针。
在这些方法中任何一种的一些实施例中,测量至少一种细胞因子的水平包括多重珠基测定。示例性的多重珠基测定涉及使用以荧光染料内部染色的磁珠以产生特定光谱地址。将结合配偶体(例如,抗体)与珠的表面轭合以捕获至少一种细胞因子。将样品加载到含有珠的96孔板中,并将样品进行孵育以允许该至少一种细胞因子与珠结合。在该至少一种细胞因子结合珠之后,加入该至少一种细胞因子的第二生物素化结合配偶体。然后将链霉亲和素轭合的可检测标签与该生物素结合。使用发光二极管来照射样品,导致珠中的荧光染料发荧光,并且可检测标签发荧光。然后基于荧光水平确定该至少一种细胞因子的浓度。用于运行多重珠基测定的示例性系统是可从
在这些方法中任何一种的一些实施例中,测量至少一种细胞因子的水平包括酶联免疫吸附测定(elisa)或酶联免疫吸附点(elispot)测定。elisa和elispot测定在本领域是公知的(参见例如,美国专利号5,939,281、6,410,252和7,575,870;czerkinskyc,nilssonl,nygrenh,ouchterlonyo,tarkowskia(1983)″asolid-phaseenzyme-linkedimmunospot(elispot)assayforenumerationofspecificantibody-secretingcells″.jimmunolmethods65(1-2):109-121[czerkinskyc、nilssobl、nygrenh、ouchterlonyo、tarkowskia(1983)“用于枚举特定的抗体分泌细胞的固相酶联免疫点(elispot)测定”,免疫学方法杂志,65(1-2):109-121]和lequinr(2005).″enzymeimmunoassay(eia)/enzyme-linkedimmunosorbentassay(elisa)″.clin.chem.51(12):2415-8[lequinr(2005)“酶免疫测定(eia)/酶联免疫吸附测定(elisa)”,临床化学,51(12):2415-8])。
示例性的elisa涉及对至少一种细胞因子(例如,ifn-γ、il-2或ip-10)具有特异性的至少一种结合配偶体,例如抗体或其抗原结合片段。具有未知量的至少一种细胞因子的样品可以非特异性地(通过吸附到表面)或特异性地(通过由对相同的至少一种细胞因子具有特异性的另一种结合配偶体捕获,如在“夹心”elisa中)而固定在固体支持体(例如,聚苯乙烯微量滴定板)上。在抗原被固定后,加入该至少一种细胞因子的结合配偶体,与固定化的至少一种细胞因子形成复合物。结合配偶体可以附着到如本文所述的可检测标签(例如,荧光体或酶),或者本身可以由识别附着到如本文所述的可检测标签(例如,荧光体或酶)的至少一种细胞因子结合配偶体的试剂检测到。如果可检测标签是酶,则加入酶的底物,并且该酶通过作用在底物上引发显色或荧光信号。然后可以使用适当的机器,例如荧光计或分光光度计,或通过眼睛,来检测可检测标签。
示例性elispot测定涉及针对该至少一种细胞因子的结合剂(例如,抗ifn-γ抗体),其被无菌地涂覆在pvdf(聚偏二氟乙烯)背衬微量培养板上。将感兴趣的细胞(例如,外周血单核细胞)以不同密度连同本文所述的一种或多种肽铺板开,并允许孵育一段时间(例如,约24小时)。由活化细胞分泌的该至少一种细胞因子被高表面积pvdf膜上的该至少一种细胞因子的结合配偶体局部捕获。在该至少一种细胞因子被固定后,加入该至少一种细胞因子的第二结合配偶体,与固定化的至少一种细胞因子形成复合物。结合配偶体可以连接到可检测标签(例如,荧光体或酶)上,或者本身可以由识别连接到可检测标签(例如,荧光体或酶)的至少一种细胞因子的结合配偶体(例如,第二抗体)的试剂检测到。如果可检测标签是酶,则加入酶的底物,并且该酶通过作用在底物上引发显色或荧光信号。然后可以使用适当的机器,例如荧光计或分光光度计,或通过眼睛,来检测可检测标签。
在这些方法中任何一种的一些实施例中,使用elisa测量至少一种细胞因子的水平。作为示例性方法,将包含如本文所述的至少一种肽的组合物干燥到采血管的内壁上。提供不含抗原的阴性对照管。还提供了含有丝裂原的阳性对照管。将来自受试者的血液抽入三个管中的每一个中。搅拌每个管以确保混合。然后将管在37摄氏度下孵育,优选在抽血之后立即或至少在收集约16小时内孵育。孵育后,通过离心从血浆中分离细胞。然后将血浆加载到elisa板中以检测血浆中存在的至少一种细胞因子(例如,ifn-γ、il-2或ip-10)的水平。然后可以使用如上所述的标准elisa测定来检测存在于每个血浆样品中的至少一种细胞因子的水平。
在这些方法中任何一种的一些实施例中,使用上述方法中的任何一种或任何其他适当的方法检测在本文所述的激发之后从受试者获得的样品中的t细胞应答测量,并且然后与对照t细胞应答进行比较。示例性的对照t细胞应答包括但不限于从患病受试者(例如,患有t1d的受试者)、健康受试者(例如,未患t1d的受试者)获得的样品中的t细胞应答。在这些方法中任何一种的一些实施例中,使用上述方法中的任何一种或任何其他适当的方法测量对照t细胞应答。在这些方法中任何一种的一些实施例中,使用相同的方法来测量受试者的样品和对照样品中的t细胞应答。
在这些方法中任何一种的一些实施例中,将t细胞应答与对照t细胞应答进行比较。在这些方法中任何一种的一些实施例中,如果对照t细胞应答是来自一名或多名健康对照受试者的样品中的t细胞应答,则与对照t细胞应答相比升高的t细胞应答指示受试者患有t1d或有患t1d的风险,而与对照t细胞应答相比降低或相等的t细胞应答指示受试者未患t1d或没有患t1d的风险。
升高的t细胞应答包括高于对照t细胞应答例如1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%、150%、200%、300%、400%、500%或更多的应答。在所提供的方法中任何一种的一些实施例中,升高的t细胞应答是高于对照t细胞应答至少两倍的应答。在所提供的方法中任何一种的一些实施例中,对照t细胞应答是已经与包含磷酸盐缓冲盐水和/或二甲亚砜的组合物接触的样品中的t细胞应答。降低的t细胞应答包括低于对照t细胞应答例如1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%、150%、200%、300%、400%、500%或更多的应答。
在这些方法中任何一种的一些实施例中,考虑了第二对照t细胞应答。在这些方法中任何一种的一些实施例中,第二对照t细胞应答是阴性对照t细胞应答。示例性的阴性对照包括但不限于已经与非t细胞活化肽(例如,未被来自受试者的样品中存在的t细胞识别的肽)(诸如非cd4+-t细胞活化肽)接触的样品中的t细胞应答,或尚未与t细胞活化肽(诸如cd4+t细胞活化肽)接触的样品(例如,使样品与不含肽的盐溶液接触)中的t细胞应答。这样的第二对照t细胞应答可以使用上述方法中的任何一种或任何其他适当的方法来测量。在这些方法中任何一种的一些实施例中,第二对照t细胞应答是阳性对照t细胞应答。示例性的阳性对照包括但不限于已经与丝裂原(例如,植物血凝素、伴刀豆球蛋白a、脂多糖或商陆丝裂原)接触的样品中的t细胞应答。在所提供的方法中任何一种的一些实施例中,阳性对照t细胞应答是已经与病原体衍生的回忆抗原肽混合物(例如,cef;由来自人巨细胞病毒、eb病毒和流感病毒的mhci类限制性t-细胞表位组成的23种肽的混池(pool),可从mabtech(#3615-1;nackastrand,瑞典)获得,或者ceft,由来自破伤风梭菌、eb病毒、人巨细胞病毒、甲型流感病毒的mhci类和ii类限制性t-细胞表位组成的27种肽的混池,可从creativepeptides(#ppo-h107)获得)接触的样品中的t细胞响应。可以使用阳性和/或阴性对照来确定测定(诸如elisa或elispot测定)没有缺陷或被污染。
治疗
本披露的其他方面涉及患有自身免疫性糖尿病(例如,t1d)的受试者的治疗。
在这些方法中任何一种的一些实施例中,待治疗的受试者是通过本文所述的方法中任何一种选择的受试者,例如通过评估t细胞应答以选择患有自身免疫性糖尿病(例如,t1d)的受试者进行治疗。在这些方法中任何一种的一些实施例中,治疗方法包括向患有自身免疫性糖尿病(例如,t1d)的受试者给予有效量的包含本文所述的至少一种肽的组合物。这些组合物可以是本文提供的组合物中的任何一种。在这些方法中任何一种的一些实施例中,该组合物包含至少一种肽,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的方法中任何一种的一些实施例中,该至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。在所提供的方法中任何一种的一些实施例中,该至少一个t细胞表位不是cd8+t细胞表位。
本文考虑并描述了对这样的肽的修饰,例如n-末端乙酰化或n-末端焦谷氨酸酯和/或c-末端酰胺。可以使用本领域已知的任何方法给予治疗。适用于每种给药途径的药物组合物在本领域是公知的(参见例如,remington:thescienceandpracticeofpharmacy,22nded.pharmaceuticalpress,2012[雷明顿:药物科学与实践,第22版,医药出版社,2012])。在这些方法中任何一种的一些实施例中,通过皮内注射给予治疗,例如本文所述的组合物。
肽可以是盐形式,优选药学上可接受的盐形式。“药学上可接受的盐形式”包括肽的常规无毒盐或季铵盐,例如来自无毒的有机酸或无机酸。常规的无毒盐包括例如源自无机酸诸如盐酸、氢溴酸、硫酸、磺酸、磷酸、硝酸等的那些;以及制备自有机酸诸如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、棕榈酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、对氨基苯磺酸、2-乙酰氧基苯甲酸、富马酸、甲苯磺酸、甲磺酸、乙二磺酸、草酸、异硫羰酸(isothionic)等的盐。
所提供的组合物中的任何一种都可以包括药学上可接受的载体。术语“药学上可接受的载体”是指当给予受试者,特别是哺乳动物,并且更特别是人时,不产生过敏反应、毒性反应或其他不良反应的分子实体和组合物。药学上可接受的载体可以是固体或液体。药学上可接受的载体的有用实例包括但不限于稀释剂、赋形剂、溶剂、表面活性剂、悬浮剂、缓冲剂、润滑剂、佐剂、运载体、乳化剂、吸收剂、分散介质、涂料、稳定剂、保护胶体、粘合剂、增稠剂、触变剂、渗透剂、螯合剂、等渗剂和吸收延迟剂,它们不影响药物组合物的活性剂的活性。该载体可以是常规使用的那些中的任何一种,并且仅受化学-物理考虑因素(诸如可溶性和缺乏与活性剂的反应性)以及受给药途径的限制。所提供的组合物中任何一种的合适载体包括常规使用的那些,例如水、盐水、右旋糖水溶液、乳糖、林格氏溶液、缓冲溶液、透明质酸、二醇、淀粉、纤维素、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸镁、硬脂酸钠、单硬脂酸甘油酯、氯化钠、甘油、丙二醇、水、乙醇等。脂质体也可以用作载体。其他载体是本领域公知的(参见例如,remington:thescienceandpracticeofpharmacy,22nded.pharmaceuticalpress,2012[雷明顿:药物科学与实践,第22版,医药出版社,2012])。
所提供的组合物中的任何一种都可以处于无菌可注射水性或油性悬浮液的形式。在这些组合物中任何一种的一些实施例中,将组合物配制成无菌可注射溶液。这种悬浮液或溶液可以根据已知的方法使用上面已经提及的那些适合的分散剂或润湿剂以及悬浮剂来配制。无菌可注射制剂可以是在非毒性的、胃肠外可接受的稀释剂或溶剂中的悬浮液,例如作为在1.3-丁二醇中的溶液。可以采用的可接受的载体是水、林格氏溶液以及等渗氯化钠溶液。在这些组合物中任何一种的一些实施例中,将组合物配制成无菌可注射溶液,其中该溶液是氯化钠溶液(例如,氯化钠0.9%usp)。在这些组合物中任何一种的一些实施例中,将组合物配制为用于皮内注射的推注。用于皮内给药的适当的递送机制的实例包括但不限于植入物、贮藏库(depot)、注射器、针、胶囊和渗透泵。
以易于给药和实现剂量均匀性的剂量单位形式配制活性剂可以是有利的。如本文所用的“剂量单位形式”是指作为针对待治疗受试者的单一剂量适合的物理上离散的单位;每个单位含有预定量的经计算产生与所需药用载体相关的所希望的治疗效果的活性剂。这些剂量单位形式的规格由以下因素支配且直接取决于以下因素:活性剂的独特特征和待实现的特定治疗效果,以及调配这种活性剂以用于治疗受试者的领域中固有的限制。可替代地,这些组合物能以多剂量形式存在。剂量单位的实例包括密封的安瓿和小瓶,并且可以在冷冻干燥状态下储存,只需要在使用前立即加入无菌液体载体。
给予的实际量(或者剂或剂量)以及给予的速率和时程将取决于正治疗的病症的性质和严重性以及待治疗受试者的特征(体重、年龄等)。治疗处方(例如,关于剂量、时机、频率等的决定)是在全科医生或专科医生(包括人类医师、兽医或医学科学家)的责任之内,并且典型地要考虑待治疗的障碍、受试者的状况、递送部位、给药方法、以及执业医生已知的其他因素。技术和方案的实例可见于例如以下文献中:remington:thescienceandpracticeofpharmacy,22nded.pharmaceuticalpress,2012[雷明顿:药物科学与实践,第22版,医药出版社,2012]。有效量可以从ng/kg体重到g/kg体重每分钟、小时、日、周或月测量。取决于给药途径,剂量可以例如每天从10ng/kg到高达100mg/kg哺乳动物体重或更多而变化,优选约1μg/kg/天至10mg/kg/天。
如本文所用,术语“治疗(treat、treating和treatment)”包括消除、抑制、减缓或逆转疾病或病症的进展,或者改善或预防疾病(例如,t1d)的临床症状。治疗可以包括诱导免疫耐受性(例如,针对胰岛细胞)、修饰受试者的细胞因子分泌谱和/或诱导抑制性t细胞亚群以分泌细胞因子。在这些方法中任何一种的一些实施例中,给予有效量的治疗。术语“有效量”意指在适当或足够的条件下给药时足以提供所希望的治疗或生理效果的治疗量。
可以在细胞培养物或实验动物中,通过标准制药程序,通过确定ic50和最大耐受剂量,确定试剂的毒性和治疗疗效。从这些细胞培养测定和动物研究获得的数据可用于制定适合于人的范围。
受试者
受试者可以包括怀疑患有或患有自身免疫性糖尿病(包括t1d、成人隐匿性自身免疫性糖尿病(lada)),或被认为处于升高的患上t1d的风险(前期糖尿病)的任何受试者。在一些实施例中,这样的受试者具有与t1d相关的mhc-ii类基因(hla-dr3、dr4、dq2或和dq8),并且还具有与t1d相关的可检测水平的血清igg特异性自身抗原(例如抗胰岛素、抗gad、抗ia-2和/或抗锌转运蛋白-8)。在本文提供的方法中任何一种的一些实施例中,受试者可以包括患有或怀疑患有t1d和乳糜泻的任何受试者。优选地,受试者是人。在一些实施例中,受试者具有编码hla-dr3、hla-dr4、hla-dq2.5(dqa1*05和dqbl*02)或hla-dq8(dqa1*03和dqb1*0302)的一个或多个hla-drb、hla-dqa和hla-dqb易感性等位基因。在一些实施例中,受试者可以具有如下家族成员,其具有hla-dq8(dqa1*03和dqb1*0302)。可以通过本领域已知的任何核酸检测方法检测易感性等位基因的存在,例如通过聚合酶链式反应(pcr)扩增从患者提取的dna,随后与序列特异性寡核苷酸探针杂交。可以使用本领域已知的和/或本文所述的诊断方法(例如,针对t1d的诊断测定和针对乳糜泻的诊断测定),将受试者鉴定为患有或怀疑患有t1d或t1d和乳糜泻。
t1d的示例性诊断测定包括但不限于糖化血红蛋白测试、葡萄糖耐量测试、空腹血糖测试和/或自身抗体测定。在一些实施例中,等于或高于6.5的糖化血红蛋白水平、等于或高于11.1mmol/l(200mg/dl)的血浆葡萄糖、等于或高于7.0mmol/l的空腹血浆葡萄糖水平、存在自身抗体或其组合指示受试者患有t1d。
可以使用高效液相层析(hplc)、免疫测定、酶测定、毛细管电泳或硼酸盐亲和层析来检测糖化血红蛋白。
葡萄糖耐量测试可以包括向受试者给予葡萄糖并在葡萄糖给予后从受试者获得血液以确定葡萄糖从血液中清除多快。在一些实施例中,使用口服葡萄糖耐量测试(ogtt),并通过口服摄取标准剂量的葡萄糖,并从两小时后收集的样品测量血液水平。可以使用本领域已知的任何方法测量葡萄糖。
空腹血糖测试可以包括在受试者未摄食至少8小时后测量血糖水平。可以使用本领域已知的任何方法测量葡萄糖。
可以使用本领域已知的任何方法,例如通过elisa、组织学、细胞学、免疫荧光或免疫印迹,来检测自身抗体。在一些实施例中,使用免疫测定来检测自身抗体。在一些实施例中,自身抗体包括胰岛细胞自身抗体、胰岛素自身抗体、谷氨酸脱羧酶的65-kda同种型(gad65)自身抗体、胰岛抗原-2(ia-2)自身抗体和锌转运蛋白(znt8)自身抗体中的一种或多种。胰岛细胞自身抗体可以通过间接免疫荧光检测。可以使用放射免疫测定或elisa检测gad65、ia-2和/或znt8自身抗体。
也考虑了遗传测试(基因分型)。可以针对编码例如hla-dr3(drb1*03)或hla-dr4(drb1*04)、hla-dq2.5(dqa1*05和dqb1*02)、dq2.2(dqa1*02和dqb1*02)或dq8(dqa1*03和dqb1*0302)的hla-drb、hla-dqa和hla-dqb易感性等位基因的存在来测试受试者。编码dqa和dqb易感性等位基因的示例性序列包括hla-dqa1*0501(genbank登录号:af515813.1)、hla-dqa1*0505(ah013295.2)、hla-dqb1*0201(ay375842.1)或hla-dqb1*0202(ay375844.1)。遗传测试的方法在本领域是公知的(参见例如,nguyenetal.definitionofhigh-risktype1diabeteshla-drandhla-dqtypesusingonlythreesinglenucleotidepolymorphisms.diabetes2013.62:2135-2140[nguyen等人,仅使用三种单核苷酸多态性定义高风险1型糖尿病hla-dr和hla-dq类型,糖尿病,2013,62:2135-2140];morahaneta1.thegeneticsoftype1diabetes.inthehlacomplexinbiologgyandmedicine:aresourcebook.mehrank,ed.,newdelhi,jaypeebrotherspublishing,2010,p.205-218[morahan等人,1型糖尿病的遗传学,生物学和医学中的hia复合体:资源书,mehrank编辑,新德里,捷彼兄弟出版社,2010,第205-218页];leslieetal.astatisticalmethodforpredictingclassicalhlaallelesfromsnpdata.amjhumgenet2008;82:48-56[leslie等人,从snp数据预测经典hla等位基因的统计方法,美国人类遗传学杂志,2008,82:48-56];diltheyetal.hla*imp-anintegratedframeworkforimputingclassicalhlaallelesfromsnpgenotypes.bioinformatics2011;27:968-972[dilthey等人,hla*imp用于输入来自snp基因型的经典hla等位基因的集成框架,生物信息学,2011,27:968-972];ferreiraetal.high-densitysnpmappingofthehlaregionidentifiesmultipleindependentsusceptibilitylociassociatedwithselectiveigadeficiency.plosgenet2012;8:e1002476[ferreira等人,hla区的高密度snp基因作图鉴定与选择性iga缺陷关联的多个独立易感性基因座,plos遗传学,2012,8:e1002476];barkeretal.twosinglenucleotidepolymorphismsidentifythehighest-riskdiabeteshlagenotype:potentialforrapidscreening.diabetes2008;57:3152-3155[barker等人,两种单核苷酸多态性鉴定最高风险糖尿病hla基因型:快速筛选的可能性,糖尿病,2008,57:3152-3155];29.sanjeevietal.dr4subtypesandtheirmolecularpropertiesinapopulation-basedstudyofswedishchildhooddiabetes.tissueantigens1996;47:275-283[sanjeevi等人,在瑞典儿童糖尿病的基于群体的研究中的dr4亚型及其分子特性,组织与抗原,1996,47:275-283];alyetal.extremegeneticriskfortype1adiabetes.procnatlacadsciusa2006;103∶14074-14079[aly等人,1a型糖尿病的极端遗传风险,美国国家科学院院刊,2006,103:14074-14079])。
具有易感性等位基因的一个或多个拷贝的受试者被认为是该等位基因阳性的。可以通过本领域已知的任何核酸测定完成对易感性等位基因的存在的检测,例如通过聚合酶链式反应(pcr)扩增从患者提取的dna,随后与序列特异性寡核苷酸探针杂交,或使用白细胞衍生的dna。
也考虑了t细胞应答测试作为对自身免疫性糖尿病(例如,t1d)的诊断并且在本文中进行提供。在一些实施例中,t细胞应答测试包括使包含t细胞的样品与本文所述的肽接触并测量样品中的t细胞应答。在一些实施例中,通过测量如本文所述的细胞因子(例如,ip-10、il-2和/或ifn-γ)的水平来测量t细胞应答,其中与对照水平(例如,未与本文所述的肽接触的样品中的细胞因子的水平)相比增加的细胞因子水平可以将受试者鉴定为患有自身免疫性糖尿病诸如t1d。示例性t细胞应答测试是本领域已知的(参见例如,pct公开号:wo/2001/025793、wo/2003/104273、wo/2005/105129、以及wo/2010/060155)。
在这些方法中任何一种的一些实施例中,受试者具有t1d的一种或多种症状。t1d的示例性症状包括但不限于多尿(频尿)、多饮(口渴增加)、多食(饥饿增加)或体重减轻。在一些实施例中,受试者可患有糖尿病酮症酸中毒。糖尿病酮症酸中毒症状包括皮肤干燥(干性皮肤)、呼吸急促、困倦、腹痛和呕吐。t1d的其他症状是本领域已知的,并且在本领域技术人员的知识内。
在这些方法中任何一种的一些实施例中,受试者处于无谷蛋白饮食。
样品
如本文所用的样品是指取自或源自受试者的生物样品,例如患有或怀疑患有自身免疫性糖尿病(例如,t1d)的受试者。样品的实例包括组织样品或流体样品。流体样品的实例是包含t细胞的全血、血浆、血清和其他体液。在本文提供的方法或试剂盒中任何一种的一些实施例中,样品包含t细胞。在本文提供的方法或试剂盒中任何一种的一些实施例中,样品包含t细胞和单核细胞和/或粒细胞。在本文提供的方法或试剂盒中任何一种的一些实施例中,包含t细胞的样品包含全血或外周血单核细胞(pbmc)。t细胞可以是cd4+t细胞,例如胰岛细胞反应性cd4+t细胞。在本文提供的方法中任何一种的一些实施例中,该方法包括获得或提供样品。在这些方法中任何一种的一些实施例中,考虑了第一样品和第二样品。如果需要t细胞应答的附加测量,也考虑另外的样品,例如第三、第四、第五等。这样的附加样品可以随时从受试者获得。
对照和对照受试者
在这些方法中任何一种的一些实施例中,本文提供的方法包括测量或使用对照t细胞应答。在这些方法中任何一种的一些实施例中,对照t细胞应答是来自受试者的样品中的t细胞应答。
在这些方法中任何一种的一些实施例中,对照t细胞应答是从对照受试者(名或多名)获得的样品中的t细胞应答。在一些实施例中,对照受试者例如具有编码例如本文所述的hla-dr3(drb1*03)、hla-dr4(drb1*04)、hla-dq2.5(dqa1*05和dqb1*02)或dq8(dqa1*03和dqb1*0302)的一个或多个hla-dr3、hla-dr4、hla-dq4和hla-dqb易感性等位基因,但未患t1d或未患t1d和乳糜泻。在一些实施例中,对照受试者不具有hla-dr3、hla-dr4、hla-dqa和hla-dqb易感性等位基因中的任一个。在一些实施例中,对照受试者是未患或怀疑患有t1d或者t1d和乳糜泻的健康个体。在这些方法或试剂盒中任何一种的一些实施例中,对照水平是来自一名或多名对照受试者的预定值,使得每当执行本文所述的方法时,不需要测量对照水平。
在一些实施例中,对照水平是来自与包含磷酸盐缓冲盐水或者磷酸盐缓冲盐水和二甲亚砜的组合物接触的样品的水平。
多核苷酸、抗原呈递细胞和hla分子
本文所述的至少一种肽可以由一种或多种多核苷酸编码。在本文提供的组合物、方法或试剂盒中任何一种的一些实施例中,组合物可以包含肽和编码这些肽的多核苷酸的混合物。
每个构成多核苷酸的总长度可以是例如21至150个核苷酸,诸如21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、50、60、70、80、90、100、110、120、130、140或150个核苷酸。
也考虑了多核苷酸的类似物。类似物包括从参考多核苷酸变化一个或多个核苷酸的多核苷酸。例如,类似物可以包含用以下项进行的一个或多个天然存在的核苷酸的取代:核苷酸类似物(诸如吗啉环),甲基化核苷酸,核苷酸间修饰诸如不带电荷的连接(例如,膦酸甲酯、磷酸三酯、磷酰胺化物、氨基甲酸酯等),带电荷的连接(例如,硫代磷酸酯、二硫代磷酸酯等),悬垂部分(例如,多肽),嵌入剂(例如,吖啶、补骨脂素等),螯合剂,烷基化剂和修饰的连接(例如,α-异头核酸等)。可以在载体中提供编码这些肽中一种或多种的多核苷酸。
编码本文定义的肽中一种或多种的多核苷酸可用于使用本领域公知的技术重组生产肽。本披露的多核苷酸可以包括可衍生自这些肽中一种或多种的dna序列,考虑到密码子使用的简并性。这一点为本领域所熟知,在不同表达宿主中密码子使用的知识也是本领域所熟知的,其有助于优化肽的重组表达。
在将多核苷酸用于这些肽中一种或多种的重组生产时,多核苷酸可以包括单独的肽的编码序列或者与其他编码序列在阅读框中的肽的编码序列,这些其他编码序列是诸如编码前导序列或分泌序列、前蛋白序列、或原蛋白序列或前原蛋白序列、接头肽序列或其他融合肽部分的编码序列。例如,可编码有助于融合肽纯化的标记序列。在某些实施例中,标记序列是如在pqe载体(凯杰公司(qiagen,inc.))中提供的六组氨酸肽,或是ha标签,或是谷胱甘肽-s-转移酶。多核苷酸还可含有非编码的5′和3′序列,诸如转录的非翻译序列、剪接和多腺苷酸化信号、核糖体结合位点和稳定mrna的序列。
本文中也考虑了抗原呈递细胞(apc)。在一些实施例中,考虑了包含如本文所述的组合物、肽或多核苷酸的抗原呈递细胞。本文定义的组合物、肽或多核苷酸可以通过用例如本文所述的至少一种肽和/或编码其中一种或多种的多核苷酸加载apc来递送。
在一些实施例中,apc选自下组,该组由以下各项组成:树突状细胞、巨噬细胞、b淋巴细胞和肝窦内皮细胞,它们表达与受试者的mhc表型共享的mhcii类分子。例如,apc可以表达hladq8。为这个目的使用的apc可以从加载后将要递送的受试者分离,或者可以从同种异体匹配(allo-matched)的受试者获得。
“加载”apc意指将apc用一种或多种肽或编码其中一种或多种的多核苷酸进行孵育或转染。通过使用常规的核酸转染方法,诸如脂质介导的转染、电穿孔或磷酸钙转染,可以实现加载apc。
在一些实施例中,本文所述的一种或多种肽结合到a)hla分子,或b)能够结合该肽的hla分子的片段。在一些实施例中,hla分子是以下项的异源二聚体:hla-dr3分子,hla-dr4分子,或由hla-dqa1*05、dqa1*02、或dqa1*03编码的hla-dqa蛋白以及由hla-dqb1*02或dqb1*0302编码的hla-dqb蛋白。在一些实施例中,hla分子的片段是这样的以下项的异源二聚体的片段:hla-dr3分子,hla-dr4分子,或由hla-dqa1*05、dqa1*02、或dqa1*03编码的hla-dqa蛋白以及由hla-dqb1*02或dqb1*0302编码的hla-dqb蛋白。
试剂盒
本披露的其他方面涉及试剂盒。在这些试剂盒中任何一种的一些实施例中,试剂盒包含本文所述的组合物中的任何一种。
在一些实施例中,该组合物包含至少一种(例如,1、2、3种或更多种)肽,该至少一种肽包含选自如下项的至少一个氨基酸序列:pllallalwgpdp(seqidno:1)、pktrreaevgq(seqidno:2)、rreaedlqgsl(seqidno:3)、rreaedlegsl(seqidno:4)、dlqvgqvelgggp(seqidno:5)、dlqvgevelgggp(seqidno:6)、cgshlvealylvc(seqidno:7)、mnilleyvvks(seqidno:8)、nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)、fnqlstgldmvglaadw(seqidno:11)、grtgtyilidmvlnrma(seqidno:12)、pkaarppvtpvllekks(seqidno:13),或该至少一个氨基酸序列内含有的至少一个t细胞表位。在所提供的试剂盒中任何一种的一些实施例中,该至少一种肽(例如,1、2、3种或更多种)的至少一个氨基酸序列内含有的至少一个t细胞表位包含氨基酸序列llallalwgpd(seqidno:14)。在所提供的试剂盒中任何一种的一些实施例中,该至少一种肽(例如,1、2、3种或更多种)的至少一个t细胞表位不是cd8+t细胞表位。在所提供的试剂盒中任何一种的一些实施例中,该至少一个t细胞表位不包含lpllallal(seqidno:76)。
在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含用以检测组合物中的肽中的一种或多种与t细胞的结合的手段。在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含用于将组合物给予受试者的装置,例如针。
在这些试剂盒中任何一种的一些实施例中,检测组合物中的肽中的一种或多种与t细胞的结合的手段是对细胞因子(例如,ifn-γ、il-2或ip-10)具有特异性的结合配偶体(例如,抗体)。本文描述了结合配偶体。在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含识别结合配偶体的试剂。在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含血液的容器。在这些试剂盒中任何一种的一些实施例中,组合物包含在容器内(例如,干燥到容器的壁上)。
在这些试剂盒中任何一种的一些实施例中,试剂盒包含细胞因子的第一和第二结合配偶体。本文描述了结合配偶体。在这些试剂盒中任何一种的一些实施例中,第一和第二结合配偶体是抗体或其抗原结合片段。在这些试剂盒中任何一种的一些实施例中,第二结合配偶体与表面结合。第二结合配偶体可以共价地或非共价地结合表面。第二结合配偶体可以直接结合到表面,或者可以间接地结合,例如通过接头。接头的实例包括但不限于含碳链、聚乙二醇(peg)、核酸、单糖单元和肽。表面可以由任何材料制成,例如金属、塑料、纸或任何其他聚合物,或其任何组合。在这些试剂盒中任何一种的一些实施例中,使细胞因子的第一结合配偶体冲洗结合到第二结合配偶体的细胞因子(例如,如在夹心elisa中)。第一结合配偶体可以包含可检测标签,或识别细胞因子的第一结合配偶体(例如,第二抗体)的试剂可以包含可检测标签。
考虑了识别细胞因子的结合配偶体的任何合适的试剂。在这些试剂盒中任何一种的一些实施例中,结合配偶体是与细胞因子的结合配偶体特异性结合的任何分子。在这些试剂盒中任何一种的一些实施例中,试剂是抗体(例如,第二抗体)或其抗原结合片段,诸如fab、f(ab)2、fv、单链抗体、fab和sfab片段、f(ab′)2、fd片段、scfv、或dab片段。试剂还包括与细胞因子的结合配偶体特异性结合的其他肽分子和适体。在这些试剂盒中任何一种的一些实施例中,细胞因子的结合配偶体包含生物素部分,并且该试剂是结合生物素部分(例如,抗生物素蛋白或链霉亲和素)的组合物。
在这些试剂盒中任何一种的一些实施例中,细胞因子的结合配偶体包含可检测标签。考虑了任何合适的可检测标签。可检测标签包括可通过光谱学、光化学、生物化学、免疫化学、化学或其他物理手段检测的任何组合物,例如酶、放射性标签、荧光团、电子致密试剂、生物素、地高辛或半抗原。本领域公知的这样的可检测标签是可以通过使用例如酶测定、显色测定、发光测定、荧光测定或放射免疫测定来检测的。进行可检测标签检测的反应条件取决于所选择的检测方法。
在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含阴性对照,例如不包含本文所述的肽的组合物,例如盐溶液或细胞培养基。在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含阳性对照,例如包含预定浓度的细胞因子的组合物。
在这些试剂盒中任何一种的一些实施例中,试剂盒包含上述组分的任何组合。
在这些试剂盒中任何一种的一些实施例中,试剂盒进一步包含使用该组合物的说明书。在这些试剂盒中任何一种的一些实施例中,说明书包括如本文所述的方法。说明书可以处于任何合适的形式,例如印刷的插页或标签。
通用技术和定义
除非确切地另外定义,在此使用的所有技术和科学术语应视为具有与本领域(例如,细胞培养、分子遗传学、免疫学、免疫组织化学、蛋白质化学、以及生物化学)普通技术人员通常理解的相同的含义。
除非另外指明,本披露中所使用的技术是标准程序,对于本领域的普通技术人员而言是熟知的。这样的技术在例如以下来源的文献中被描述和解释:j.sambrooketal.,molecularcloning:alaboratorymanual,coldspringharbourlaboratorypress(2012)[j.sambrook等人,分子克隆:实验室手册,冷泉港实验室出版社(2012)];t.a.brown(editor),essentialmolecularbiology:apracticalapproach,volumes1and2,irlpress(2000and2002)[t.a.brown(编辑),基本分子生物学:实用方法,卷1和2,irl出版社(2000和2002)];d.m.gloverandb.d.hames(editors),currentprotocolsinmolecularbiology,greenepub.associatesandwiley-interscience(1988,includingallupdatesuntilpresent)[d.m.glover和b.d.hames(编辑),分子生物学实验指南,格林出版联营公司和威利国际科学公司(1988,包括直至现在的所有更新)];edwarda.greenfield(editor)antibodies:alaboratorymanual,coldspringharbourlaboratory,(2013)[edwarda.greenfield(编辑),抗体:实验室手册,冷泉港实验室,(2013)];以及j.e.coliganetal.(editors),currentprotocolsinimmunology,johnwiley&sons(includingallupdatesuntilpresent)[j.e.coligan等人(编辑),免疫学实验指南,约翰威利父子公司(包括直至现在的所有更新)]。
不需要进一步详细阐述,相信本领域的技术人员可以根据上述描述最大程度地利用本披露。因此,以下具体实施例被解释为仅是说明性的,而不是以任何方式对其余的公开内容进行限制。出于本文参考的目的或主题,本文引用的所有出版物都通过引用并入。
实例
实例1.t1d中的胰岛自身免疫
该研究的目的是量化并比较在患有1型糖尿病(t1d)和乳糜泻两者的患者中口服谷蛋白激发前后对胰岛自身抗原、免疫显性谷蛋白肽和病原体衍生的回忆抗原的t细胞应答。
背景
膳食谷蛋白可能在引起或增强胰岛自身免疫中起作用,但机制尚不明了。在过去14年的基于患者的研究中,短期“谷蛋白激发”已经提供了乳糜泻下的免疫应答的详细了解。在本研究中,首先使用谷蛋白激发来研究受乳糜泻以及t1d影响的患者,以检测对牵涉在t1d中的自身抗原具有特异性的cd4+t细胞,并测试胰岛自身免疫是否受到谷蛋白免疫力的再活化的影响。
在乳糜泻中,最流行的遗传相关性是与编码hla-dq2.5的mhc-ii类等位基因,并且由乳糜泻特异性cd4+t细胞识别的谷蛋白衍生表位优先由hla-dq2.5呈递。10%的患有乳糜泻的hla-dqa1*05和dqb1*02(其编码hla-dq2.5)阴性的患者大多数具有编码hla-dq8的hla-dqa1*03和dqb1*0302等位基因,并且在这些患者中,与众不同的谷蛋白特异性表位受hla-dq8的限制。已经描述了谷蛋白衍生的hla-dq2.5-和dq8-限制性表位的氨基酸序列(sollidlmetal.immunogenetics.2012[sollidlm等人,免疫遗传学,2012])。通常排除膳食谷蛋白的乳糜泻患者开始口服谷蛋白激发后6天,某些谷蛋白肽在用外周血单核细胞(pbmc)或全血孵育时会刺激干扰素(ifn)-γ分泌(ontiverosnetal.clinexpimmunol2014[ontiverosn等人,临床与实验免疫学,2014])。谷蛋白肽引起的ifn-γ分泌可以通过elispot测定检测到,并且是归因于活化的cd4+t细胞(andersonrpeta1.,naturemed2000[andersonrp等人,自然医学,2000]),其已经通过流式细胞术使用mhc-ii类多聚体进一步表征(rakimetal.,pnasusa2007[rakim等人,pnasusa2007])。在常规消耗谷蛋白的hla-dq2.5+乳糜泻患者(未治疗)中,用对两种显性小麦谷蛋白表位具有特异性的hla-dq2.5多聚体染色的循环cd4+t细胞的中值频率为大约16/百万cd4+t细胞;而在排除膳食谷蛋白的hla-dq2.5+乳糜泻患者中,中值频率为5/百万(christophersena.etal.,uegwj2014[christophersena等人,uegwj2014])。口服谷蛋白激发暂时将对显性谷蛋白表位具有特异性的cd4+t细胞的频率增加10-100倍(andersonrpetal.gut2005[andersonrp等人,肠道,2005];rakimetal.pnasusa2007[rakim等人,pnasusa2007]),从而允许以其他方式不可检测的谷蛋白表位特异性t细胞通过离体ifn-γ分泌测定诸如elispot使用pbmc或elisa使用来自用谷蛋白肽孵育的全血的血浆来定量和表征。
在使用于hla-dq2.5+乳糜泻患者中口服谷蛋白激发之前和之后6天收集的血液的最近研究中,发现ifn-γ诱导型蛋白(ip)-10和白细胞介素(il)-2在来自用显性谷蛋白肽孵育的全血的血浆中更一致地增加并到相对更高的浓度。在大多数患者中,在用谷蛋白肽进行的口服谷蛋白激发之前收集的全血的孵育刺激ip-10和(有时)il-2水平,其显著高于用单独的培养基孵育的全血。在口服谷蛋白激发后,ip-10和il-2以及ifn-γ在用谷蛋白肽孵育的全血中升高。
这个观察结果表明,在测量来自用包含同源表位的候选肽孵育的全血的血浆中的ip-10的细胞因子释放测定中,可以检测到罕见的抗原特异性cd4+i细胞。
在还患有乳糜泻的1型糖尿病(t1d)患者中测试了用以对稀有抗原特异性cd4+t细胞的表位进行作图的这种新颖方法。t1d也是t细胞介导的疾病,但由致病性cd4+t细胞识别的表位尚不清楚。hla-dr3-dq2.5和hla-dr4-dq8单型与t1d强烈相关,并且已经报道了在t1d中由igg识别的自身抗原衍生的t细胞表位。然而,尚没有单个hla-dr或dq限制性表位与t1d一致地相关,并且最彻底研究的胰岛自身抗原(前胰岛素原、谷氨酸脱羧酶(gad)-65和胰岛瘤相关抗原(ia)-2)的许多区域能够被mhcii类转基因小鼠、健康人和/或t1d患者中的cd4+t细胞识别(dilorenzotpetal.,clinexpimmunol2007[dilorenzotp等人,临床与实验免疫学,2007])。
在患有t1d和乳糜泻的患者中,口服谷蛋白激发将允许对良好表征的谷蛋白衍生表位的cd4+t细胞应答用作由衍生自牵涉在t1d中的自身抗体的肽引起的全血ifn-γ、il-2和ip-10应答的阳性对照。对与t1d相关的表位作图可能是在隔夜测定中首次使用新鲜血液。在当前的研究中,在谷蛋白排除饮食后患乳糜泻的t1d患者中的口服谷蛋白激发前后,评估对包括t1d自身抗原、前胰岛素原、gad65和ia-2中所有独特的12聚体的混池和各肽的细胞因子应答。
方法
如果是18-55岁的成年人,在过去3个月内没有接受免疫抑制药物治疗,并且坚持无谷蛋白饮食,则受试者符合条件。所有受试者都患有活检证实的乳糜泻,并且也是胰岛素治疗的1型糖尿病患者。评估与t1d和乳糜泻相关的自身抗体(芭芭拉·戴维斯中心(barbaradaviscenter),丹佛,科罗拉多州);和奎斯特诊断公司(questdiagnostics))。四名受试者中的每名都显示升高的胰岛素自身抗体,但是没有检测到对谷氨酸脱羧酶(gad)、胰岛瘤相关抗原(ia)-2或锌转运蛋白-8具有特异性的自身抗体(表1)。测定了mhcii类等位基因(芭芭拉·戴维斯中心,佛,科罗拉多州丹),并且显示四名受试者中的每名都具有编码hla-dr3和hla-dq2.5的等位基因,并且三名还具有编码hla-dr4和dq8的等位基因(表2)。所有受试者都严格坚持无谷蛋白饮食,直到经历3天口服食物激发。激发期间消耗的食物由从小麦谷蛋白、大麦和黑麦面粉制成的饼干组成。估计每天消耗的三块饼干总共提供4.5g小麦谷蛋白、3g大麦醇溶蛋白和1.5g黑麦醇溶蛋白。在开始口服食物激发之前和之后6天收集肝素化血液。
表1.受试者人口统计学和血清学
表2.受试者的mhcii类等位基因
进行ifn-γelispot和全血细胞因子释放测定以评估对17聚体肽混池的t细胞应答,所述混池包括衍生自通常被t1d中的自身抗体识别的胰岛抗原的所有独特的12聚体氨基酸序列:胰岛素、谷氨酸脱羧酶-65(gad65)、和胰岛瘤相关抗原(ia)-2(通过hplc测得纯度为70%,通过lc-ms证实一致性;由德国jpt肽技术股份有限公司(jptpeptidetechnologiesgmbh,germany)合成)(表3)。使用源自公共ncbigenbank数据库(ncbi.nlm.nih.gov/protein)的蛋白质序列,根据beissbarth等人(bioninformaticst.etal.suppl1:i29-37[bioninformaticst.等人,增刊1:i29-37])设计文库。表3总结了所得肽文库。表3.胰岛自身抗原肽文库
1如果一级序列中的谷氨酰胺残基符合针对转谷氨酰胺酶-2定义的脱酰胺基序(qx1px3,或qx1x2[f,y,w,i,l,v],其中x1和x3不是脯氨酸),则由谷氨酸酯替代谷氨酰胺产生第二一级序列。这个脱酰胺一级序列包括在用以产生肽文库的那些中。
此外,还评估了由免疫显性hla-dq2.5限制性t细胞表位组成的3种谷蛋白肽的混池(通过hplc测得的纯度为95%,通过lc-ms证实一致性;由加利福尼亚州csbio公司合成),具有由免疫显性hla-dq2.5、hla-dq8以及hla-dq2.2限制性t细胞表位组成的10种另外的谷蛋白肽的混池(通过hplc测得的纯度为90%,通过lc-ms证实一致性;由荷兰pepscan公司合成),由来自这两个较小的混池的11种组成的14种谷蛋白肽的混池(通过hplc测得的纯度为90%,通过lc-ms证实一致性;由荷兰pepscan公司合成),由以下项组成的71种谷蛋白衍生肽的混池:三个较小混池中所有的肽连同由牵涉在hla-dq2.5相关乳糜泻中的序列组成的55种另外的肽(通过hplc测得的纯度为70%,通过lc-ms证实一致性;jpt肽技术公司(jptpeptidetechnologies))(tye-dineta1.scitranslmed2010[tye-din等人,科学转化医学,2010]),以及23个mhci类(cef)(产品号3615-1,mabtechag,瑞典)和源自于回忆病毒抗原的14个mhcii类限制性表位(pm-ceft-mhc-ii,德国jpt肽技术股份有限公司)的混池。使用在开始口服谷蛋白激发后6天收集的血液,在全血细胞因子释放测定中评估来自前胰岛素原、gad、ia-2和谷蛋白混池的各构成肽。
在全血测定中,在96孔圆底板中,将225μl体积的新鲜肝素化血液用在具有二甲亚砜(dmso)的磷酸盐缓冲盐水(pbs)中的25μll肽孵育至终浓度为0.05%或0.1%。在全血测定中,胰岛自身抗原混池中构成肽的浓度是0.4、1或4μg/ml;对于cef是0.1μg/ml;ceft1是μg/ml;3-谷蛋白-肽混池是10、20或50μg/ml,13-谷蛋白-肽混池是5、10、或25μg/ml;14-谷蛋白-肽混池是5、10、或25μg/ml;71-谷蛋白-肽混池是1、5或10μg/ml。用10%pbs在全血中孵育的各肽的最终浓度为20μg/ml,含有0.0.5%dmso。将全血测定在37℃下在5%co2中孵育24小时。在孵育期结束时,在离心各板后将大约120μl的血浆从血液中分离,并且然后转移到“镜像”无菌96孔板的相对应孔中。将含有血浆的各板用胶塑料盖玻片密封并在-80℃下冷冻。在解冻同时在室温下离心10分钟的血浆上进行多重珠基细胞因子测定
在elispot测定中,将重悬浮于50μl
结果
谷蛋白肽混池应答:在口服谷蛋白激发后,对混池和各谷蛋白衍生肽的细胞因子释放应答没有变化或显著增加(表4和表5a-5c)。在全血细胞因子释放测定中,对谷蛋白肽的应答在全血ifn-γ释放测定中最不常见且最弱,而在口服谷蛋白激发后在ip-10测定中最一致且显著。然而,在所有四名受试者中口服谷蛋白激发前后收集的血液中,对这两个较大的谷蛋白肽混池的ip-10应答是仅用培养基的那些的超过两倍。在三名受试者中口服谷蛋白激发之前收集的血液中,对最高浓度(10-50μg/ml)的谷蛋白肽混池的il-2应答也是仅用培养基的应答的超过两倍。在口服谷蛋白激发前,全血ifn-γ释放和对谷蛋白肽混池的ifn-γelispot应答没有升高。
表4.对肽混池2的ifngelispot应答1
1点形成单位(3个孔的总和,40万pbmc/孔)
2具有以0.5%dmso的最终浓度指示的浓度的各肽的混池
表5a.针对谷蛋白肽混池的全血ifng释放
表5a(续).
表5b.针对谷蛋白肽混池的全血il-2释放
表5b(续)
表5c.针对谷蛋白肽混池的全血ip-10释放
表5c(续).
t1d自身抗原肽混池应答:在细胞因子释放测定中特别是全血ip-10释放,对t1d自身抗原肽混池的应答经常升高(表4和表6a-6c)。经测试的肽混池的最高浓度(4μg/ml)几乎总是刺激比最低浓度(0.4μg/ml)更强的应答。除了1名患者中gad65的混池1外,8个t1d自身抗原肽混池中的每个都引起为所有四名受试者中仅用培养基的超过两倍的全血ip-10应答。前胰岛素原混池和ia-2混池2经常刺激最强的细胞因子释放应答,特别是在ifn-γelispot中。t1d自身抗原肽混池刺激的细胞因子释放的一致性和幅度在口服谷蛋白激发后没有一致地变化。
表6a.针对胰岛自身抗原肽混池的全血ifng释放
表6a(续)
表6b.针对胰岛自身抗原肽混池的全血il-2释放
表6b(续)
表6c.针对胰岛自身抗原肽混池的全血ip-10释放
表6c(续)
t1d自身抗原肽特异性应答:将440种单独的t1d自身抗原衍生的17聚体肽中的每种(20μg/ml)在单孔中用在开始口服谷蛋白激发后6天收集的全血孵育。前胰岛素原衍生肽的数据提供于表7a和7b中。在34种前胰岛素原衍生肽中,一种在所有四名受试者中都引起比仅用培养基高2倍的ip-10应答。该17聚体衍生自前胰岛素原信号序列(pllallalwgpdpaaaf,seqidno:45),并与三名受试者更弱地识别的另一17聚体(mrllpllallalwgpdp,seqidno:47)重叠。具有对应于pllallalw(seqidno:105)的重叠序列的另一17聚体(malwmrllpllallalw,seqidno:54)也在对cgshlvealylvcgerg(seqidno:53)的最强应答者中刺激ip-10释放。这些发现一起表明,t1d患者经常具有对重叠序列(pllallalwgpdp,seqidno:1)具有特异性的t细胞,其可能拥有一个或多个mhc-ii类表位。前胰岛素原中的三个其他区域也是免疫原性的:(1)在三名受试者中肽fytpktrreaedlqgsl(seqidno:46)刺激升高的ip-10释放,并且在这些受试者之一中il-2和ifn-γ释放也增加。重叠序列也是免疫原性的,从而支持以下项的重要性:序列pktrreaevgq(seqidno:2)和rreaedlegsl(seqidno:4),(2)reaedlqvgqvelgggp(seqidno:48)并且具体而言重叠序列dlqvgqvelgggp(seqidno:5),并且(3)ip-10释放在对nqhlcgshlvealylvc(seqidno:51)hla-dr3+dr4-和hladq2.5+dq8-的一名受试者中是明显的并且针对共享序列cgshlvealylvc(seqidno:7)的重叠肽cgshlvealylvcgerg(seqidno:53)更弱,从而表明表位含在这个序列中。由于前胰岛素原混池仅由34种肽组成,并且持续刺激强的ip-10释放和ifn-γelispot应答,这些发现表明前胰岛素原中的表位,特别是在包括序列pllallalw(seqidno:105)的信号序列中,在t1d的免疫发病机制中经常起重要作用。
表7a.刺激全血ip-10、il-2或ifn-g释放>2倍增加的前胰岛素原肽
表7a(续)
表7a(续)
表7b.刺激全血ip-10、il-2或ifn-g释放>2倍增加的前胰岛素原肽的比对
表7b(续)
表7b(续)
155个成员的gad65肽文库中的三种17聚体在所有四名受试者中都引起增加的ip-10释放:nmftyeiapvfvlleyv(seqidno:9)、nvcfwyippslrtledn(seqidno:10)和fnqlstgldmvglaadw(seqidno:11)(表8)。三名受试者针对以下两个另外的序列显示升高的ip-10释放:rptlaflqdvmnillqy(seqidno:59)和kykiwmhvdaawgggll(seqidno:60),并且两名受试者对以下重叠序列有应答:aflqdvmnilleyvvks(seqidno:63)和mnilleyvvksfdrstk(seqidno:64),这表明重叠序列mnilleyvvks(seqidno:8)具有在t1d患者中通常识别的表位。一名受试者以升高的ip-10、il-2和ifn-γ对肽fdrstkvidfhypnell(seqidno:61)有应答。
表8.在2名或更多名受试者中刺激全血ip-10、il-2或ifn-g释放>2倍增加的gad65肽
表8(续)
表8(续)
ia-2文库中255个17聚体中的一种肽一致地刺激ip-10和il-2的释放,并且在两名受试者中还刺激ifn-γ的释放,这表明它是ia-2中的免疫显性肽(grtgtyilidmvlnrma(seqidno:12),表9))。第二肽pkaarppvtpvllekks(seqidno:13)在所有四名受试者中都引起ip-10而非il-2或ifn-γ的释放。应答于肽ctvivmltplvedgvkq(seqidno:66),三名受试者显示出ip-10释放。两名受试者各自以ip-10释放应答于以下两种肽:ahstspmrsvlltlval(seqidno:70)和splqaellppllehlll(seqidno:71)。只有受试者7应答于以下三种肽:wesgctvivmltplved(seqidno:67)、ssevqqvpspvsseppk(seqidno:68)和nvgadikktmegpvegr(seqidno:69),但ip-10、il-2和ifn-γ释放全部升高。
表9.在2名或更多名受试者中刺激全血ip-10、il-2或ifn-g释放>2倍增加的ia-2肽
表9(续)
表9(续)
结论
口服谷蛋白激发不会增强应答于t1d自身抗原衍生肽的全血细胞因子释放,就如它对乳糜泻中的谷蛋白衍生肽所表现的那样。然而,在全血细胞因子释放测定中针对乳糜泻中的谷蛋白反应性t细胞,ip-10和il-2都比ifn-γ提供更高的灵敏度,并且当应用于筛选衍生自患有t1d和乳糜泻的患者中的t1d自身抗原的肽时,鉴定一致地免疫显性的氨基酸序列。来自前胰岛素原的一种17聚体肽、来自gad65的三种17聚体肽和来自ia-2的两种17聚体肽在四名t1d受试者的四名中刺激升高的全血ip-10释放。在此研究中评估的t1d受试者中,其他一些序列通常但不太一致地且较不有效地刺激ip-10释放。因此,将多重细胞因子和趋化因子测量应用于t1d中的表位作图揭示了经典的t1d相关自身抗原前胰岛素原、gad65和ia-2中以前不显而易见的表位层级。
实例2.1型糖尿病中的谷蛋白免疫和胰岛自身免疫
此研究的目的是量化并比较在患有1型糖尿病(t1d)和乳糜泻两者的患者中口服谷蛋白激发前后对胰岛自身抗原、免疫显性谷蛋白肽和病原体衍生的回忆抗原的t细胞应答。执行全血样品的cd4+和cd8+t细胞耗尽,以便确定对正在分析的t1d肽抗原的t细胞细胞因子应答的特异性细胞群。
根据制造商的方案直接从全血耗尽人cd4+和cd8+t细胞,分别使用cd4和cd8dynabeads(dynabeadshumancd4,生命技术公司(lifetechnologies),#11145d;dynabeadshumancd8,生命技术公司,#11145d)。简言之,将dynabeads重悬浮并将所需体积转移至15ml管中。添加到全血中的珠的体积的计算是每m1全血2x106个cd4珠(25μl)和4x106个cd8珠(50μl)。将各珠首先用3m1pbs洗涤,涡旋并置于磁体上1分钟。弃去上清液,并将各珠从磁体中去除。然后将全血以针对管中珠浓度计算的体积加入珠中。然后将含有全血和dynabeads的管在4℃下在连续摇床上孵育45分钟。
然后将管放入磁体中2分钟。然后将全血上清液转移到新管中以用于24小时全血测定或流式细胞术分析。丢弃磁珠。
首先通过聚蔗糖密度梯度离心纯化来自全血、cd4+t细胞耗尽血液和cd8+t细胞耗尽血液的pbmc。将ficoll-paque(15m1)加入到sepmate管的底室中。将全血(6m1)或耗尽血液(4m1)用等体积的d-pbs+2%fbs稀释并分层在聚蔗糖垫的顶部。然后在室温下将各管在吊桶式转头中以500xg离心10分钟。然后将顶层转移到新的50ml管中,并通过用d-pbs+2%fbs将总体积调节至50ml来洗涤细胞。将细胞在室温下以300xg离心10分钟。弃去上清液并且将耗尽细胞悬浮于2mld-pbs+2%fbs中。将来自全血的细胞重悬浮于6mld-pbs+2%fbs中。将细胞转移到1.0m1微量离心机卡帽管(1m1/管)中,并在室温下以300xg离心5分钟。弃去上清液并且将细胞重悬浮于100μd-pbs+2%fbs中。相应地,向每个管中加入荧光标计的抗体(10μg/ml)(表10)。
将细胞在黑暗中于4℃下孵育45分钟。用d-pbs+2%fbs将体积调节至1ml,并将细胞在室温下以300xg离心5分钟。弃去上清液,并将细胞重悬浮于100μld-pbs+2%fbs中。用amnisflowcyte流式细胞仪收集的数据来分析细胞。使用来自全血的单抗体染色细胞(管2-5;表10)进行荧光补偿调节。使用amnisideasapplication进行分析。
使用dynabeads磁珠针对cd4+和cd8+t细胞耗尽处理来自受试者的全血样品(表11)。
耗尽样品的流式细胞术分析表明,cd4+和cd8+t细胞的耗尽近乎完全(表12)。对存于活淋巴细胞群体(门控r1)中的cd3+t细胞进行分析。针对六名受试者,正常pbmc群体中的cd3+/cd4+t细胞的百分比范围为56.9%-66.9%。pbmc的活淋巴细胞门控中的cd3+/cd8+t细胞的百分比为28.2%-34-9%。通过磁珠分离除去细胞,cd3+/cd4+t细胞的百分比下降到0.04%-0.5%。耗尽样品中cd3+/cd8+t细胞的检测范围为0%-1.29%。
在所有受试者中,cd4+和cd8+t细胞近乎完全耗尽发生为>99%的cd4+t细胞耗尽和>98%的cd8+t细胞耗尽。
然后将耗尽血液以及剩余的未耗尽全血用于全血细胞因子释放测定。针对对包括以下项的17聚体肽的混池的反应性评估t细胞细胞因子应答:衍生自通常被t1d中的自身抗体识别的胰岛抗原的所有独特的12聚体氨基酸序列:胰岛素、谷氨酸脱羧酶-65(gad65)、和胰岛瘤相关抗原(ia)-2,如表13a和表13b中所提供的。
表13b.
将新鲜肝素化血液用肽孵育。各胰岛自身抗原肽的浓度为20μg/ml,并且胰岛自身抗原混池中的构成肽为4μg/ml。以1μg/ml使用对照mhcii类肽混合物ceft。将醇溶蛋白肽混池以25μm加入到全血测定中。将全血测定在37℃下在5%co2中孵育24小时。在室温下以500xg离心10分钟后将血浆从血液中分离,并且然后转移到“镜像”无菌96孔板中的相对应孔中,并在-80℃下冷冻直至使用。根据制造商的说明对解冻血浆进行多重珠基细胞因子测定(magpix)。干扰素(ifn)-γ诱导型蛋白-10(ip-10)、白细胞介素(il)-2和ifn-γ的浓度。表14是全血细胞因子测定的结果的概述,其表达了在对相对于仅用培养基孵育的细胞(背景)的≥1.25倍细胞因子生产阳性的受试者的数目中的数据。
表14.
t1d
六名t1d受试者显示出对正在分析的肽的清晰反应性,具有相对于背景大于1.25的细胞因子倍数变化(表14)。在所测试的21种肽中的15种和对照肽中,大多数应答以至少1名受试者中的ip-10生产呈现。所测试的受试者超过50%显示出对20150-01、20150-05-w1、20150-24、l2p1-051、l3p2-076、l1p1-胰岛素原混池、l2p1-gad65混池、l2p2-gad65混池、l3p1-ia2混池、l3p2-ia2混池、l3p3-ia2混池和nexgen混池以及ceft对照的显著ip-10应答。
所测试的受试者超过50%还显示出显著的ifng和il-2应答。这些应答包括肽20150-24、l3p2-076、l1p1-胰岛素原混池、l2p2-gad65混池和l3p2-ia2混池。
健康受试者
将这些应答与正常健康受试者进行比较,在ifng和il-2应答上存在显著降低。没有肽使>50%的健康受试者表现出>1.25倍的ifng或il-2应答。至少1名t1d受试者中从15种反应性肽看到略微增加,对比至少1名健康受试者中18种反应性肽的略微增加。总共有13种反应性肽对于>50%的t1d受试者是刺激性的而12种反应性肽对于>50%的健康受试者是刺激性的。
cd4+t细胞耗尽的pbmc
当cd4+t细胞从pbmc中耗尽,并且然后在相同条件下测试时,所有细胞因子倍数变化应答减弱。对于所有t1d受试者和所有测试的肽,il-2应答完全消除。尽管ifng应答在反应性肽的数目上略有增加,但总体而言,在>50%的所测试的t1d受试者中,没有肽刺激与pbmc相比>1.25倍的ifng应答。在引起ip-10应答的反应性肽的数目上(12种肽而不是15种)观察到略微减少。此外,与pbmc相比,没有肽在>50%的所测试的受试者中刺激ip-10应答。对于ip-10,cd4+t细胞耗尽导致更高的背景水平(仅培养基)。
cd8+t细胞耗尽的pbmc
cd8+t细胞耗尽的pbmc表现出ifng、il-2的细胞因子产生增加,但ip-10应答略有下降。
在刺激性肽的数目上也观察到具有>1.25倍变化的ifng应答,而且在表现出>1.25倍变化的受试者的数目上也观察到。在所测试的21种肽中,16种肽刺激了ifng产生,相比针对全pbmc的8种肽。9种肽使>50%的t1d受试者中观察到显著的ifng倍数变化,相比针对全pbmc的4种肽。
il-2产生的分析显示出相似的结果。在所测试的21种肽中,16种肽刺激了il-2产生,相比针对全pbmc的12种肽。此外,对8种肽的反应性使>50%的t1d受试者中观察到显著的il-2倍数变化,相比针对全pbmc的5种肽。
cd8+t细胞耗尽的pbmc中的ip-10应答显示反应性肽上仅有略微增加(16种肽,相比针对pbmc的15种反应性肽)。以>1.25倍变化刺激来自>50%的受试者的ip-10反应性的肽的数目从正常pbmc中的13种减少到cd8+t细胞耗尽的pbmc中的8种。对于ip-10,cd8+t细胞耗尽也导致更高的背景水平(仅培养基)。
实例3.前胰岛素原表位的精细作图
将前胰岛素原表位的前导序列以赖氨酸取代的肽以及c-和n-末端截短精细作图。图1a-1c显示了前胰岛素原p10-20中的显性11聚体表位的图:llallalwgpd(seqidno:14)。在患有t1d的4名受试者中,全血ip-10释放测定中的长度和观察到的生物活性与cd4t细胞的表位兼容。然而,9聚体p8-16:lpllallal(seqidno:76)的活性表明,这是cd8t细胞的表位并与cd4表位重叠。不希望受任何理论束缚,可以选择根据本披露的治疗性肽和/或诊断性肽以避免cd8活性,但确保靶向cd4t细胞。数据是4名受试者全血ip-10释放的平均值,测量为相对于单独培养基(无肽)的倍数变化。
从年龄在29与45岁之间的患有1型糖尿病的4名受试者收集全血。三名受试者为hla-dr3,4和dq2,8,并且一名为hla-dr4,13dq6,8。在全血测定中,在96孔圆底板中,使用新鲜肝素化血液用磷酸盐缓冲盐水(pbs)和dmso中的肽(最终浓度10μm)孵育。肽(通过lc-ms测得的纯度>80%)是前胰岛素原中的序列的截短或经赖氨酸取代的变体,其在以前的比较跨越这种多肽的肽的研究中显示是免疫原性的。在37℃下在5%co2中24小时之后,将血浆分离并在-80℃下冷冻。根据制造商的说明(hcytomag-60k,end密理博公司(endmilliporecorp),比勒利卡,马萨诸塞州),对解冻的血浆进行多重磁珠基细胞因子免疫测定,以测量干扰素(ifn)-γ诱导型蛋白-10(ip-10)、白细胞介素(il)-2和ifn-γ的浓度。将测定板在luminexmagpix磁性酶标仪上运行。定量上限为10,000pg/ml,并且检测下限为3.2pg/ml。通过将来自各肽孵育物的细胞因子浓度除以在相同的测定板上pbs和dmso(nil)孵育物的细胞因子浓度,计算来自各肽孵育物的细胞因子浓度的倍数变化。数据表示4名供体的平均倍数变化。
等效形式
尽管已经在本文描述并展示了几个发明实施例,但本领域普通技术人员应容易想象用于执行功能和/或获得结果和/或在本文描述的优点中的一个或多个的多种其他装置和/或结构,并且此类变型和/或修改中的每者都被视为是在本文描述的发明实施例的范围内。更一般地说,本领域的普通技术人员应容易理解,在本文描述的所有参数、尺寸、材料以及配置意味着为示例性的,并且实际参数、尺寸、材料和/或配置将取决于发明传授内容所用于的一种或多种具体应用。本领域的普通技术人员仅仅使用常规实验便认识到或能够确认在本文描述的具体发明实施例的许多等效形式。因此,应理解的是,前述实施例是仅藉助于实例来呈现,并且在所附权利要求书及其等效形式的范围内,发明实施例可以按与具体地描述和要求不同的方式来实践。本披露的发明实施例涉及在本文描述的每个单独特征、系统、物品、材料、试剂盒和/或方法。另外,如果此类特征、系统、物品、材料、试剂盒和/或方法不是相互矛盾的,则两个或更多个此类特征、系统、物品、材料、试剂盒和/或方法的任何组合也被包括在本披露的创造性范围之内。
如在本文限定并使用的所有定义应当被理解成凌驾于所限定术语的字典定义、通过引用而结合的文件中的定义和/或一般含义。
在本文披露的所有参考文献、专利和专利申请都相对于每个被引用的主题通过引用而并入,这在一些情况下可以包括文件的全部内容。
如本文在说明书和权利要求书中使用的,不定冠词“一种/一个(a和an)”除非明确作出相反指示,否则应当理解为意味着“至少一种/一个”。
如本文在说明书和权利要求书中使用的,短语“和/或(and/or)”应当理解为意味着元素中的“任一者或两者(eitherorboth)”如此联合,即,多个元素在一些情况下联合地存在并且在其他情况下分离地存在。用“和/或(and/or)”列出的多个元素应以相同的方式理解,即,如此联合的元素中的“一个或多个(oneormore)”。除了通过“和/或(and/or)”项具体指明的元素之外还可以任选地存在其他元素,而无论与具体指明的那些元素相关还是无关。因此,作为非限制性实例,当结合例如“包含(comprising)”等开放式语言使用时,在一个实施例中对“a和/或b(aand/orb)”的提及可以指代仅有a(任选地包括除了b之外的元件),在另一个实施例中可以指代仅有b(任选地包括除了a之外的元件),在又另一个实施例中可以指代有a和b两者(任选地包括其他元件)等等。
如本文在说明书和权利要求书中使用的,“或(or)”应当理解为具有与如上文定义的“和/或(and/or)”相同的含义。举例来说,当在列表中划分多个项目时,“或(or)”或“和/或(and/or)”应当解释为包括性的,即包括若干元素或元素列表中的至少一个元素,但也包括一个以上的元素,并且任选地包括另外的未列出的项目。只有清楚地作出相反指示的术语,诸如“仅一种/一个(onlyoneof)”或“确切一种/一个(exactlyoneof)”或当在权利要求书中使用时,“由……组成(consistingof)“将指代若干元素或元素列表的确切一种/一个元素。总体上,如本文使用的术语“或(or)”在前面带有诸如“任一种/一个(either)”、“一种/一个(oneof)”、“仅一种/一个(onlyoneof)”或“确切一种/一个(exactlyoneof)”等排他性术语时应当仅解释为指示排他性替代例(即,“一者或另一者但并非两者(oneortheotherbutnotboth)”)。“基本上由……组成(consistingessentiallyof)”当在权利要求书中使用时,应具有如在专利法范围内使用的普通含义。
如本文在说明书和权利要求书中使用的,参考一个或多个元素的列表的短语“至少一个(atleastone)”应当理解为意味着选自该元素列表中的任意一个或多个元素中的至少一个元素,但不一定包括该元素列表内具体列出的每个元素中的至少一个,并且不排除该元素列表中的元素的任何组合。这一定义还允许,可以任选地存在除短语“至少一个”所指元素列表内具体指明的元素外的元素,而无论与具体指明的那些元素相关还是无关。因此,作为非限制性实例,“a和b中的至少一个(atleastoneofaandb)”(或,相当地,“a或b中的至少一个(atleastoneofaorb)”,或相当地“a和/或b中的至少一个(atleastoneofaand/orb)”)可以在一个实施例中指代至少一个,任选地包括一个以上,即a,不存在b(并且任选地包括除b外的元素);在另一个实施例中,指代至少一个,任选地包括一个以上,即b,不存在a(并且任选地包括除a外的元素);在又另一个实施例中,指代至少一个,任选地包括一个以上,即a,以及至少一个,任选地包括一个以上,即b(并且任选地包括其他元素)等等。
还应当理解的是,除非明确作出相反指示,否则在包括多于一个步骤或动作的在本文所要求保护的任何方法中,方法的步骤或动作的顺序不一定限于方法的步骤或动作被列举的顺序。
在权利要求书中,以及在以上说明书中,所有过渡性短语,诸如“包含(comprising)”、“包括(including)”、“携带(carrying)”、“具有(having)”、“含有(containing)”、“涉及(involving)”、“持有(holding)”、“由……构成(composedof)”等应理解为开放性的,即,意味着包括但不限于。仅过渡短语“由……组成(consistingof)”和”基本上由……组成(consistingessentiallyof)”应分别是封闭的或者半封闭的短语,如在美国专利局专利审查程序手册(unitedstatespatentofficemanualofpatentexaminingprocedures)2111.03部分中列举的。
- 还没有人留言评论。精彩留言会获得点赞!