CD317单链抗体317scFv、其编码序列及制备方法和应用与流程
本发明涉及肿瘤治疗技术领域,具体涉及cd317单链抗体317scfv、其编码序列及制备方法和应用。
背景技术:
肿瘤尤其是实体瘤治疗是一个世界性难题,现今临床采用的常规治疗方法如手术、放疗、化疗都无法完全切除或彻底杀灭肿瘤细胞,肿瘤转移或复发时有发生,临床效果差;另外,常规放/化疗的特异性极差,在杀伤肿瘤细胞的同时也给正常细胞带来很大的损伤,有较严重的不良反应,癌症患者常因不能耐受而被迫停止接受治疗;另一方面放化疗尤其容易损伤在抗肿瘤机制中占重要地位的免疫系统,往往导致残留肿瘤细胞的免疫逃逸,导致复发、转移等恶性转变。肿瘤三大常规治疗方法的局限性促使人们去寻找新的治疗手段,肿瘤的免疫治疗因其安全、有效、不良反应低等特点逐渐脱颖而出,成为继手术、放疗、化疗之后肿瘤治疗的第四种模式(中国肿瘤编辑部.点评肿瘤生物治疗研究专题[j].中国肿瘤,2011,20(2):80-81)。尤其是利用基因工程技术生产的小分子单链抗体免疫治疗因其具有较高的安全性和有效性已成为肿瘤治疗的新热点。
目前已有人源单克隆抗体抗双唾液酸神经节苷酯的免疫细胞因子hu14.18-il2用于治疗复发或难治的成神经细胞瘤(aldersonk,sondelp.clinicalcancertherapybynkcellsviaantibody-dependentcell-mediatedcytotoxicity[j].jbiomedbiotechnol,2011,2011:379123);美罗华(一种嵌合型的抗cd20单克隆抗体),用于治疗复发的或难治的低度恶性的或滤泡型的非霍奇金淋巴瘤;赫赛汀(一种与原癌基因产物her2/neu结合的单克隆抗体),用于治疗转移性乳腺癌(hamiltone,blackwellk,hobeikaac,etal.phaseⅰclinicaltrialofher2-specificimmunotherapywithconcomitanther2kinaseinhibition[j].jtranslmed,2012,10:28);以及细胞毒性抗生素calicheamicin结合的人源化抗cd33抗体,用于治疗急性髓样白血病等。
基于抗体的肿瘤免疫治疗的关键限制因素在于靶点选择。不同靶点的抗体的作用和适应症不同,因此,每个靶点的抗体都具有独特的意义。
cd317,又名bst-2、hm1.24或tetherin,是骨髓瘤免疫疗法的靶向抗原(ohtomo,t.,etal.,molecularcloningandcharacterizationofasurfaceantigenpreferentiallyoverexpressedonmultiplemyelomacells.biochembiophysrescommun,1999.258(3):p.583-91;rew,s.b.,etal.,generationofpotentantitumorctlfrompatientswithmultiplemyelomadirectedagainsthm1.24.clinicalcancerresearch,2005.11(9):p.3377-3384.)。研究发现,cd317在多发性骨髓瘤、b淋巴瘤、肺癌、头颈鳞状细胞癌、子宫内膜癌、脑癌及骨转移的乳腺癌等均有cd317表达上调的现象(wang,w.,etal.,chimericandhumanizedanti-hm1.24antibodiesmediateantibody-dependentcellularcytotoxicityagainstlungcancercells.lungcancer,2009.63(1):p.23-31.;schliemann,c.,etal.,invivobiotinylationofthevasculatureinb-celllymphomaidentifiesbst-2asatargetforantibody-basedtherapy.blood,2010.115(3):p.736-744.;wainwright,d.a.,etal.,theexpressionofbst2inhumanandexperimentalmousebraintumors.experimentalandmolecularpathology,2011.91(1):p.440-446.),提示其可能是一个肿瘤相关抗原和潜在的免疫治疗靶点。
目前有不少癌症领域的专家正在开展靶向cd317的抗肿瘤治疗的研究,在细胞水平、小鼠模型上均取得了初步的成果。研究表明,cd317特异性的ctl细胞对骨髓瘤具有明显的抑制作用,而cd317单克隆抗体也可以通过adcc效应抑制多发性骨髓瘤、肾细胞肾癌、子宫内膜癌等的发展(kawai,s.,etal.,interferon-alphaenhancescd317expressionandtheantitumoractivityofanti-cd317monoclonalantibodyinrenalcellcarcinomaxenograftmodels.cancerscience,2008.99(12):p.2461-2466.;yokoyama,t.,etal.,plasmamembraneproteomicsidentifiesbonemarrowstromalantigen2asapotentialtherapeutictargetinendometrialcancer.internationaljournalofcancer,2013.132(2):p.472-484.;harada,t.,etal.,combinationwithadefucosylatedanti-hm1.24monoclonalantibodypluslenalidomideinducesmarkedadccagainstmyelomacellsandtheirprogenitors.plosone,2013.8(12):p.e83905.)。
现有的靶向cd317的抗体的抗肿瘤机制都是通过抗体依赖性的细胞介导的细胞毒作用(antibody-dependentcell-mediatedcytotoxicity,adcc)发挥作用,但是肿瘤病人,尤其是经历过放化疗之后的肿瘤病人大量免疫细胞死亡,因此adcc作用大打折扣,也无法与放化疗联用。另外,传统的抗体分子量较大,穿透性差,在实体瘤治疗过程中很难在肿瘤内部富集足够浓度的抗体,因此对实体瘤治疗效果比较有限。
技术实现要素:
本发明提供一种cd317单链抗体317scfv、其编码序列及制备方法和应用,该单链抗体317scfv不依赖于adcc,直接作用于肿瘤细胞抑制其生长,能够与放化疗等联合使用,其不含fc段,分子量小,穿透效果也更好。
根据第一方面,一种实施例中提供一种cd317单链抗体317scfv,其编码序列包括如seqidno:9所示的核苷酸序列,或其编码序列包括与seqidno:9编码相同氨基酸序列的核苷酸序列;上述cd317单链抗体317scfv不含fc段。
根据第二方面,一种实施例中提供一种编码cd317单链抗体317scfv的核苷酸序列,包括如seqidno:9所示的序列,或与seqidno:9编码相同氨基酸序列的序列。
根据第三方面,一种实施例中提供一种cd317单链抗体317scfv的制备方法,包括:
(1)制备cd317单链抗体317scfv的重组表达载体,上述重组表达载体包含如seqidno:9所示的核苷酸序列,或与seqidno:9编码相同氨基酸序列的核苷酸序列;
(2)将上述重组表达载体转入宿主细胞中表达出上述cd317单链抗体317scfv。
进一步地,上述表达载体是真核表达载体。
进一步地,上述真核表达载体是pcdna3.1(+)。
进一步地,上述宿主细胞是真核细胞。
进一步地,上述真核细胞是hek293f细胞。
进一步地,上述核苷酸序列通过抗体的重链和轻链简并引物组,以从杂交瘤细胞中提取的rna作为模板,经反转录和扩增得到。
进一步地,上述简并引物组包括如seqidno:1-8所示的序列。
根据第四方面,一种实施例中提供一种第一方面的cd317单链抗体317scfv或第二方面的核苷酸序列在制备治疗和/或预防肿瘤的药物中的应用。
本发明借助基因工程手段,将编码cd317抗体的重、轻链可变区基因重组到真核表达载体上进行表达,制备的单链抗体317scfv不受动物品系和抗体类型的限制,可以减少潜在的抗原表位,增强抗体的疗效。传统方法制备的抗体,一般只能治疗一种类型的肿瘤,而本发明的单链抗体317scfv可以有效地抑制cd317高表达的一系列肿瘤细胞的生长,因此其抗肿瘤的临床应用将更加广泛。与其他cd317抗体相比,本发明的小片段抗体不依赖于adcc发挥功能,对放化疗后免疫力差的病人可能具有更好的疗效,也能够与放化疗等方法联合使用。此外,本发明的小片段抗体分子量小,对实体瘤具有更好的穿透效果。
附图说明
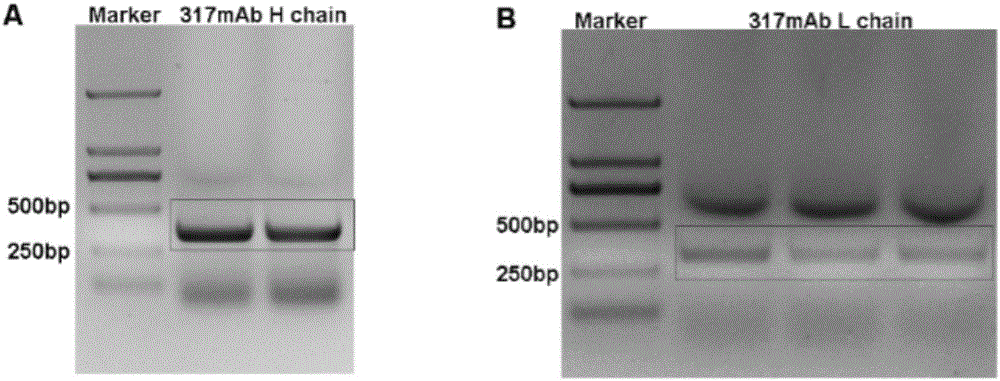
图1示出了单链抗体317scfv重链和轻链可变区基因的pcr扩增产物。
图2示出了单链抗体317scfv合成序列片段结构示意图。
图3示出了pcdna3.1(+)-317scfv重组质粒中317scfv表达序列测序结果,其中箭头指示为起始密码子atg。
图4示出了dotblot检测单链抗体317scfv在真核细胞中的表达情况。
图5示出了单链抗体317scfv抑制多种肿瘤细胞的生长。
图6示出了单链抗体317scfv对肿瘤细胞的杀伤实验。
具体实施方式
下面通过具体实施方式结合附图对本发明作进一步详细说明。在以下的实施方式中,很多细节描述是为了使得本发明能被更好的理解。然而,本领域技术人员可以毫不费力的认识到,其中部分特征在不同情况下是可以省略的,或者可以由其他元件、材料、方法所替代。在某些情况下,本发明相关的一些操作并没有在说明书中显示或者描述,这是为了避免本发明的核心部分被过多的描述所淹没,而对于本领域技术人员而言,详细描述这些相关操作并不是必要的,他们根据说明书中的描述以及本领域的一般技术知识即可完整了解相关操作。
针对现有肿瘤治疗手段的局限性,尤其是靶向cd317抗肿瘤策略的局限性,本发明利用小鼠抗体简并引物组从杂交瘤细胞株(1c12c6)中通过pcr扩增获得cd317抗体的重链、轻链可变区序列,构建表达载体pcdna3.1(+)-317scfv,并在哺乳动物细胞hek293f中表达。本发明首次制备出了单链抗体317scfv,通过对其活性的检测,发现单链抗体317scfv在体外可以抑制多种肿瘤细胞的生长。
以下通过实施例详细说明本发明的技术方案,应当理解实施例仅是示例性的,不能理解为对本发明保护范围的限制。
实施例1单链抗体317scfv基因的pcr扩增、克隆鉴定和表达载体的构建
(1)单链抗体317scfv基因的pcr扩增:收集杂交瘤细胞株(1c12c6),提取细胞rna,具体步骤如下:
①取处理好的细胞,去除培养基,加入1mltrizol将细胞溶解。
②将用trizol溶解的细胞加入ep管中,加入200μl氯仿,混匀后12000rpm,4℃离心15min。
③吸取500μl上清,加入500μl预冷的异丙醇,混匀后12000rpm,4℃离心15min。
④去除上清,用75%的乙醇清洗沉淀物,12000rpm,4℃离心8min。
⑤超净台上,吹干沉淀后,加入20μldepc水。
⑥检测rna浓度和纯度。
用反转录试剂盒反转录成cdna,以此cdna为模板,利用英潍捷基公司合成抗体的重链和轻链简并引物组(序列如下表1所示),分别进行pcr反应扩增。pcr条件为:95℃预变性3min,95℃变性30s,58℃退火30s,72℃延伸30s,循环35次,72℃延伸5min至10℃。如图1所示,扩增产物片段317scfv重链(hchain)和轻链(lchain)dna长度为300bp左右。
表1抗体的重链和轻链简并引物组
(2)t克隆和鉴定:分别回收重链和轻链pcr产物并与pmd19t(takara)连接,通过热激法转入trans5α感受态细菌,在氨苄青霉素抗性平板上进行筛选。各挑取至少10个阳性菌落,扩大培养并抽提质粒,测序。测序结果在imgt数据库(http://www.imgt.org/imgt_vquest/share/textes/imgtvquest.html)进行比对,挑取出现频率最高的抗体序列。重链(vh)与轻链(vl)之间通过(g4s)3连接序列进行连接,拼接成317scfv表达序列,如下seqidno:9所示,其合成序列结构示意图如图2所示。
317scfv序列:
atgggctggtcctgcatcatcctgttcctggtggccaccgccaccggcgaggtgcagctggtggagtctgggggaggcttagtgcagcctggagggtccctgaaactctcctgtgcagcctctggattcactttcagtagttatggcatgtcttgggttcgccagactccagacaagaggctggagtgggtcgcaaccattaatagtaatggtgctaacacctattatccagacagtgtgaagggccgattcaccatctccagagacaatgccaagaacaccctgtacctgcaaatgagcagtctgaagtctgaggacacagccatgtattactgtgcaaggatctatgatgcttactcctcctggtttacttactggggtgaaggaacttttgtcacagtcaatctcggtggcggtggctcgggcggtggtgggtcgggtggcggcggatctgatattgttctgacacagactacatcctccctgtctgcctctctgggagacagagtcaccatcagttgcagtgcaagtcaggggattaaaaattatttaaactggtatcagcagaaaccagatggaactgttaaactcctgatctattacacatcaagtttacactcaggagtcccatcaaggttcagtggcagtgggtctgggacagattattctctcaccatcagcaacctggaacctgaagatattgccacttactattgtcagcagtatagtaagcttccgtacacgttcggcgcaggcacaaaattggaaatcaatgattacaaggatgacgacgataagcaccaccaccaccaccactga(seqidno:9)。
(3)pcdna3.1(+)-317scfv表达载体的构建和鉴定:将pmd19t-317scfv和pcdna3.1(+)质粒分别用ecorⅰ、xholⅰ双酶切,分别回收317scfv和线性化pcdna3.1(+)载体片段;将317scfv与线性化载体pcdna3.1(+)进行连接,转入trans5α感受态细菌,挑取阳性克隆进行酶切和测序鉴定,图3示出了pcdna3.1(+)-317scfv重组质粒中317scfv表达序列测序结果,其中箭头指示为起始密码子atg。
实施例2单链抗体317scfv在真核细胞hek293f中的表达
(1)单链抗体317scfv在真核细胞hek293f中的表达:利用pei25000转染试剂将pcdna3.1(+)对照质粒和pcdna3.1(+)-317scfv重组质粒分别转染到真核细胞hek293f中,于8%co2、37℃恒温培养箱震荡培养(120rpm)72h;收集细胞表达上清,3000g离心5min,小心吸取上清,0.45μm滤膜过滤。
(2)通过dotblot检测317scfv的表达情况:各取50μl上述步骤(1)中收集的对照组和pcdna3.1(+)-317scfv组的细胞表达上清液,均匀地滴加于无水甲醇活化过的pvdf膜上,5%的脱脂奶粉室温封闭1h,加入sigma公司带hrp的抗his标签抗体(稀释浓度为1:5000),室温孵育45min,pbst洗膜3次,每次6min,ecl显色,观察结果如图4所示。
实施例3单链抗体317scfv抑制肿瘤细胞生长的作用
(1)单链抗体317scfv抑制肿瘤细胞生长的作用:肝癌细胞株hepg2、乳腺癌细胞株mcf-7严格计数(tc20tmautomatedcellcounter)后,以每孔1×105个细胞接种于12孔板;子宫颈癌细胞株hela以每孔2×105个细胞接种于12孔板;过夜后每孔去掉500μldmem培养基,并加入500μl实施例2中收集的无菌hek293f表达上清液(pcdna3.1(+)对照组,以下简称ctrl组)或pcdna3.1(+)-317scfv上清(以下简称317scfv组),轻轻混匀后于5%co2、37℃恒温培养箱继续培养48h后(各实验组分别设置3个复孔),显微镜下拍照,并收集细胞计数(tc20tmautomatedcellcounter),结果如图5所示,表明单链抗体317scfv抑制肿瘤细胞生长。
(2)单链抗体317scfv抑制肿瘤细胞活性:子宫颈癌细胞株hela细胞严格计数后,接种于96孔板,每孔200μl培养基,1×104个细胞,过夜后分别加入不同体积(0μl,5μl,10μl,20μl,50μl,100μl)单链抗体317scfv上清液继续培养48h(每种浓度设置5个复孔),48h后每孔加入10μl的mtt工作液并于37℃恒温箱中孵育2h,酶标仪上机检测od490,结果如图6所示,表明单链抗体317scfv抑制肿瘤细胞活性,并且随浓度增加抑制能力也增加。
以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。例如,单链抗体317scfv的组装方式并不限于本发明披露的vh-vl连接的方式,其他通过简单修改连接片段、突变个别氨基酸或者改成vl-vh等的修改方式,均属于本发明保护范围。
sequencelisting
<110>中国科学院深圳先进技术研究院
<120>cd317单链抗体317scfv、其编码序列及制备方法和应用
<130>17i25047
<160>9
<170>patentinversion3.3
<210>1
<211>14
<212>dna
<213>人工序列
<400>1
gaggtgmwgcttrt14
<210>2
<211>24
<212>dna
<213>人工序列
<400>2
gaggtgmwgctkvwgsagtctgga24
<210>3
<211>17
<212>dna
<213>人工序列
<400>3
gacdgtgashgwrgtyc17
<210>4
<211>27
<212>dna
<213>人工序列
<400>4
gacdgtgashrdrgtbcctksrcccca27
<210>5
<211>14
<212>dna
<213>人工序列
<400>5
gahrtygtkmtsac14
<210>6
<211>24
<212>dna
<213>人工序列
<400>6
gahrtygtkmtsacmcarwctmca24
<210>7
<211>15
<212>dna
<213>人工序列
<400>7
katytccaryytkgt15
<210>8
<211>27
<212>dna
<213>人工序列
<400>8
katytccaryytkgtscchbcdccgaa27
<210>9
<211>819
<212>dna
<213>人工序列
<400>9
atgggctggtcctgcatcatcctgttcctggtggccaccgccaccggcgaggtgcagctg60
gtggagtctgggggaggcttagtgcagcctggagggtccctgaaactctcctgtgcagcc120
tctggattcactttcagtagttatggcatgtcttgggttcgccagactccagacaagagg180
ctggagtgggtcgcaaccattaatagtaatggtgctaacacctattatccagacagtgtg240
aagggccgattcaccatctccagagacaatgccaagaacaccctgtacctgcaaatgagc300
agtctgaagtctgaggacacagccatgtattactgtgcaaggatctatgatgcttactcc360
tcctggtttacttactggggtgaaggaacttttgtcacagtcaatctcggtggcggtggc420
tcgggcggtggtgggtcgggtggcggcggatctgatattgttctgacacagactacatcc480
tccctgtctgcctctctgggagacagagtcaccatcagttgcagtgcaagtcaggggatt540
aaaaattatttaaactggtatcagcagaaaccagatggaactgttaaactcctgatctat600
tacacatcaagtttacactcaggagtcccatcaaggttcagtggcagtgggtctgggaca660
gattattctctcaccatcagcaacctggaacctgaagatattgccacttactattgtcag720
cagtatagtaagcttccgtacacgttcggcgcaggcacaaaattggaaatcaatgattac780
aaggatgacgacgataagcaccaccaccaccaccactga819
- 还没有人留言评论。精彩留言会获得点赞!