银杏内酯B氮杂环衍生物及其盐的制备及药用用途的制作方法
本发明属医药技术领域,涉及银杏内酯b氮杂环衍生物及其盐及其制备方法和药用用途。本发明以银杏内酯b为母体,经结构修饰,引入含氮杂环结构,制成银杏内酯b氮杂环衍生物,以及银杏内酯b氮杂环衍生物相应的盐,达到改善水溶性,增强疗效的目的。
背景技术:
银杏作为药用植物由来已久,早在公元1000年左右,我国民间就使用银杏叶治疗哮喘与支气管炎。随着药物提取工艺标准化和药理作用活性研究的深入,世界各国,特别是德国、法国等欧洲国家已将银杏提取物(gbe)广泛用于治疗呼吸系统、心脑血管系统等疾病。
银杏内酯b(ginkgolideb,gb)是从银杏叶中提取的一种六环笼状结构的二萜化合物,是迄今发现的最强的血小板活化因子(paf)拮抗剂,研究显示,它直接参与血栓形成,可刺激冠状动脉和脑动脉,引起它们的收缩、痉挛,导致心肌和脑组织缺血。近年研究还发现,银杏内酯b有较强的抗炎作用,在炎症反应中,中性白细胞膜磷脂经活化磷脂酶a2作用,水解成花生四烯酸(aa)。花生四烯酸在5-脂氧酶(5-lo)的作用下进一步代谢为白三烯(lts)和羟基二十碳四烯酸(hetes)等与炎症介质相关的重要产物,同时,磷脂酶a2的活化需要细胞内钙参与,银杏内酯b具有影响大鼠中性白细胞花生四烯酸代谢酶及细胞内游离钙的作用,其抗炎作用可能与其抑制中性白细胞溶酶体酶的释放、超氧阴离子的产生以及细胞内钙水平的升高有关。但实践显示,作为天然产物,银杏内酯b的结构刚性较强,存在水溶性和生物利用度均较差的缺陷,致使其药效的充分发挥受到限制,影响了临床应用效果。
基于现有技术的现状,本申请的发明人通过对银杏内酯b的结构进行化学修饰,在10-位羟基上引入水溶性的含氮杂环基团,获得一类新的银杏内酯b含氮杂环衍生物及其相应的盐类化合物,其能提高药物水溶性,克服银杏内酯b水溶性差的不利因素。
技术实现要素:
本发明的目的是基于现有技术的现状,提供一类银杏内酯b氮杂环衍生物及其盐及其制备方法和药用用途。本发明在银杏内酯b结构中引入氮杂环的衍生物,其结构特征为,式1所示的在银杏内酯b的10位羟基上连接有含氮杂环的衍生物,
其中y为ch或者n,即杂环为三氮唑环或者四氮唑环;连接10位氧原子和氮杂环碳原子之间的l为含0-10个碳原子的各种连接链,包括烃基连接链,或者链中插入氮、氧等原子的连接链;g为h,1-4个碳原子的烃基,氰基,羧基,烷氧酰基,或者氨酰基以及烷基取代的氨酰基。
本发明的进一步目的是提供银杏内酯b氮杂环衍生物与各种有机碱或者无机碱形成的盐,即式1所示化合物中氮杂环上的-nh-,可与各种无机碱或者有机碱制备成盐;无机碱盐可选自各类钠,钾,钙和镁盐,但不局限于这些盐;有机碱盐选自各类胺盐以及碱性氨基酸盐,但不局限于这些盐;
本发明的再一个目的是同时提供式1所示化合物的制备方法,其可以通过式2所示方法制备获得:
式2中,i是指在合适的溶剂中,碱性催化条件下,各类含有炔基(y为ch),或者氰基(y为n)的卤代烃,与银杏内酯b通过醚键缩合,获得式2中所示的中间体;
其中,卤代烃包括氯代、溴代和碘代烃,l为含0-10个碳原子的各种连接链,包括烃基连接链,或者链中插入氮、氧等原子的连接链;
y为ch或者n原子;
g为h,1-4个碳原子的烃基,氰基,羧基,烷氧酰基,或者氨酰基以及烷基取代的氨酰基;
溶剂选自二氯甲烷,氯仿,thf,丙酮,乙腈,dmf等;
碱性催化剂选自碳酸氢钠,碳酸钠,碳酸钾,碳酸铯等无机碱,以及三乙胺,吡咯烷,哌嗪等有机碱;
反应温度控制在25-110度之间;
ii是指式2中所示中间体,在适当的溶剂中,有催化剂或者无催化剂条件下,与叠氮化合物发生1,3-偶极环加成反应,生成含氮杂环,获得式1化合物,即含有氮杂环的银杏内酯b衍生物;
其中,催化剂选自氯化锌,氯化铁,氯化铝,氯化锡等,且不限于以上试剂;
溶剂选自水,甲醇,乙醇,正丁醇,乙二醇,或者乙二醇单甲醚等,且不限于以上溶剂。
本发明提供了式1所示化合物及其盐的药用用途,经实验证实,式1化合物及其盐具有显著的血小板活化因子(paf)拮抗作用,可用于制备预防及治疗缺血性中风、心绞痛、心肺梗塞、脑血栓形成、以及炎症、哮喘等与血小板活化因子相关的疾病的预防及临床治疗的药物,能达到改善水溶性,增强疗效的目的。
附图说明
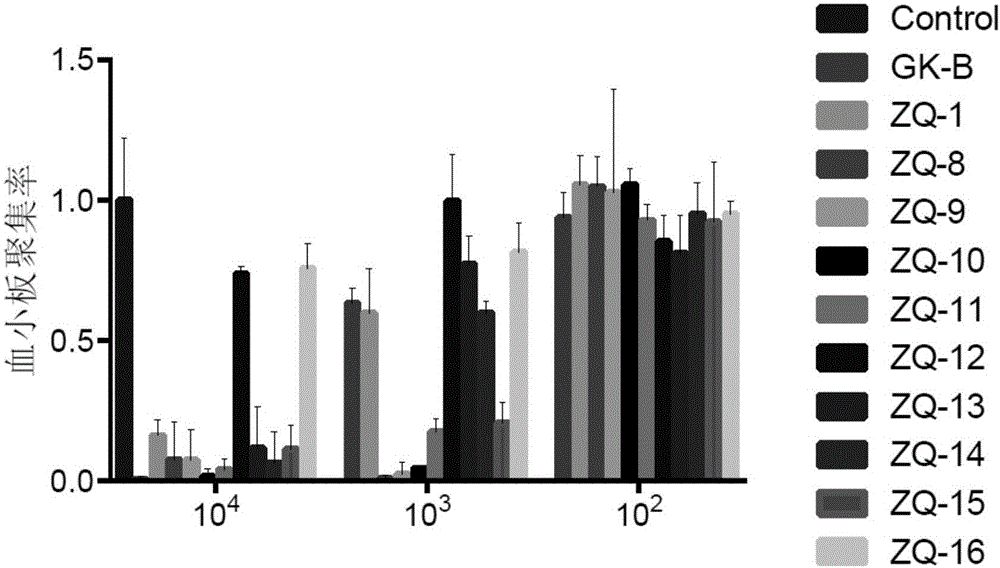
图1显示了实施例1,实施例8-16不同浓度(102,103和104nm)对血小板聚集的抑制活性。
图2显示了化合物实施例15的1h-nmr谱(400mhz,dmso-d6)。
图3显示了化合物实施例15的质谱esi-ms(m/e):505(m-na+)。
具体实施方式
实施例1、10-o-(氰基甲基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入溴代乙腈240mg(2.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流2小时后,结束反应。后处理,母液浓缩,残留物柱层析,分得淡黄色固体240mg,收率52%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),4.02(m,1h,1-h),4.57(d,1h,2-h),4.82(d,1h,j=16hz,10-ch2-),4.91(d,1h,j=16hz,10-ch2-),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lcms(m/z):464(m+h+)。
实施例2、10-o-(1-氰基乙基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入1-溴代丙腈266mg(2.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至结束反应。后处理,母液浓缩,残留物柱层析,分得黄色固体340mg,收率71%。1h-nmr(dmso-d6,400mhz):1.05(s,9h,t-bu),1.13(d,j=8hz,3h,14-me),1.72(dd,1h,8-h),1.81(ddd,1h,7α-h),1.91(d,3h,j=5hz,10-chch3),2.10(dd,1h,7β-h),2.82(q,j=8hz,1h,14-h),4.04(m,1h,1-h),4.58(d,1h,2-h),4.83(q,1h,j=5hz,10-ch-),5.29(s,1h,10-h),5.30(d,1h,1-oh),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lc-ms(m/z):478(m+h+)。
实施例3、10-o-(3-氰基烯丙基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入4-溴代-2-丁烯腈290mg(2.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至结束反应。后处理,母液浓缩,残留物柱层析,分得淡黄色固体368mg,收率75%。1h-nmr(dmso-d6,400mhz):1.04(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),4.02(m,1h,1-h),4.57(d,1h,2-h),4.78(m,2h,10-ch2-),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.51(d,j=16hz,1h,10-ch=),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh),6.64(d,j=16hz,1h,10-ch=).lc-ms(m/z):490(m+h+)。
实施例4、10-o-(氰基甲氧基乙基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入2-溴乙氧基乙腈326mg(2.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至结束反应。后处理,母液浓缩,残留物柱层析,分得淡黄色固体238mg,收率47%。1h-nmr(dmso-d6,400mhz):1.06(s,9h,t-bu),1.10(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.55(m,4h,-ch2ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),4.84(d,1h,j=16hz,10-ch2-),4.90(d,1h,j=16hz,10-ch2-),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lc-ms(m/z):508(m+h+)。
实施例5、10-o-(炔丙基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入氯代丙炔222mg(3.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至反应结束。后处理,母液浓缩,残留物柱层析,分得淡黄色固体210mg,收率45%。1h-nmr(dmso-d6,400mhz):1.04(s,9h,t-bu),1.12(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.28(s,1h,≡ch),3.91(m,2h,10-ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),,5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lc-ms(m/z):463(m+h+)。
实施例6、10-o-(4-炔-2-烯戊基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入氯代乙腈戊-3-烯-1-炔300mg(3.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至结束反应。后处理,母液浓缩,残留物柱层析,分得黄色固体188mg,收率38%。1h-nmr(dmso-d6,400mhz):1.02(s,9h,t-bu),1.10(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.25(s,1h,≡ch),3.94(m,2h,10-ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.64(m,1h,10-ch=),5.77(d,1h,6-h),6.15(s,1h,12-h),6.19(d,j=15hz,10-ch=),6.43(s,1h,3-oh).lcms(m/z):489(m+h+)。
实施例7、10-o-(炔丙氧基乙基)银杏内酯b
银杏内酯b424mg(1.0mmol)溶于30ml氯仿中,依次加入溴乙氧基丙炔324mg(2.0mmol),ki332mg(2.0mmol),三乙胺1ml,加热回流至结束反应。后处理,母液浓缩,残留物柱层析,分得黄色固体212mg,收率42%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.28(s,1h,≡ch),3.54(m,4h,10-ch2ch2-),3.91(m,2h,10-ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),,5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lcms(m/z):507(m+h+)。
实施例8、10-o-[5-(1h-四氮唑)甲基]银杏内酯b
取实施例1化合物50mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化锡21mg(0.11mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体46mg,收率82%。1h-nmr(dmso-d6,400mhz):1.01(s,9h,t-bu),1.12(d,j=8hz,3h,14-me),1.74(dd,1h,8-h),1.90(ddd,1h,7α-h),2.13(dd,1h,7β-h),2.85(q,j=8hz,1h,14-h),4.15(d,1h,1-h),4.64(d,1h,2-h),5.14(d,1h,j=16hz,10-ch2-),5.36(d,1h,1-oh),5.41(s,1h,10-h),5.56(d,1h,j=16hz,10-ch2-),5.78(d,1h,6-h),6.22(s,1h,12-h),6.48(s,1h,3-oh).lc-ms(m/z):507(m+h+)。
实施例9、10-o-{1-[5-(1h-四氮唑)]乙基}银杏内酯b
取实施例2化合物53mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化锡21mg(0.11mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体43mg,收率75%。1h-nmr(dmso-d6,400mhz):1.02(s,9h,t-bu),1.10(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.03(d,3h,j=5hz,10-chch3),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),4.02(m,1h,1-h),4.57(d,1h,2-h),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.58(q,1h,j=5hz,10-ch-),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lc-ms(m/z):521(m+h+)。
实施例10、10-o-{3-[5-(1h-四氮唑)]烯丙基}银杏内酯b
取实施例3化合物54mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化锡21mg(0.11mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体36mg,收率62%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),4.02(m,1h,1-h),4.57(d,1h,2-h),4.61(m,2h,10-ch2-),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),5.91(m,j=16hz,1h,10-ch=),6.15(s,1h,12-h),6.43(s,1h,3-oh),6.73(d,j=16hz,1h,10-ch=).lc-ms(m/z):533(m+h+)。
实施例11、10-o-{2-[5-(1h-四氮唑)甲氧基]乙基}银杏内酯b
取实施例4化合物56mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化锡21mg(0.11mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体40mg,收率66%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.55(m,4h,-ch2ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.34(d,1h,j=16hz,10-ch2-),5.56(d,1h,j=16hz,10-ch2-),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh).lc-ms(m/z):551(m+h+)。
实施例12、10-o-[5-(1h-三氮唑)甲基]银杏内酯b
取实施例5化合物51mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化亚铜15mg(0.15mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体48mg,收率86%。1h-nmr(dmso-d6,400mhz):1.01(s,9h,t-bu),1.12(d,j=8hz,3h,14-me),1.74(dd,1h,8-h),1.90(ddd,1h,7α-h),2.13(dd,1h,7β-h),2.85(q,j=8hz,1h,14-h),4.15(d,1h,1-h),4.64(d,1h,2-h),5.10(d,1h,j=16hz,10-ch2-),5.36(d,1h,1-oh),5.41(s,1h,10-h),5.46(d,1h,j=16hz,10-ch2-),5.78(d,1h,6-h),6.22(s,1h,12-h),6.48(s,1h,3-oh),7.41(s,1h,唑环-h).lc-ms(m/z):506(m+h+)。
实施例13、10-o-{3-[5-(1h-三氮唑)]烯丙基}银杏内酯b
取实施例6化合物54mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化亚铜15mg(0.15mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体44mg,收率75%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),4.02(m,1h,1-h),4.57(d,1h,2-h),4.61(m,2h,10-ch2-),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.77(d,1h,6-h),5.86(m,j=16hz,1h,10-ch=),6.15(s,1h,12-h),6.43(s,1h,3-oh),6.65(d,j=16hz,1h,10-ch=),7.28(s,1h,唑环-h).lc-ms(m/z):532(m+h+)。
实施例14、10-o-{2-[5-(1h-三氮唑)甲氧基]乙基}银杏内酯b
取实施例7化合物56mg(0.11mmol)于10ml水中,加入2ml乙二醇溶清,依次加入叠氮化钠10mg(0.15mmol),氯化亚铜15mg(0.15mmol),加热搅拌48小时后,加入2滴浓盐酸,减压蒸除溶剂,残留物水洗,过滤得白色固体47mg,收率78%。1h-nmr(dmso-d6,400mhz):1.03(s,9h,t-bu),1.11(d,j=8hz,3h,14-me),1.70(dd,1h,8-h),1.81(ddd,1h,7α-h),2.12(dd,1h,7β-h),2.81(q,j=8hz,1h,14-h),3.55(m,4h,-ch2ch2-),4.02(m,1h,1-h),4.57(d,1h,2-h),5.28(s,1h,10-h),5.31(d,1h,1-oh),5.35(d,1h,j=16hz,10-ch2-),5.51(d,1h,j=16hz,10-ch2-),5.77(d,1h,6-h),6.15(s,1h,12-h),6.43(s,1h,3-oh),7.34(s,1h,唑环-h).lc-ms(m/z):550(m+h+)。
实施例15、10-o-[5-(1h-四氮唑)甲基]银杏内酯b钠盐
10-o-[5-(1h-四氮唑)甲基]银杏内酯b(实施例8)200mg(0.40mmol)溶于2ml无水乙醇中,滴加等摩尔量的na2co3的甲醇溶液(46mg于5ml),室温搅拌1小时后,加入等体积的无水乙醚,放置过夜,析出固体,得产物175mg,收率83%。
实施例16、10-o-[5-(1h-四氮唑)甲基]银杏内酯b赖氨酸盐
10-o-[5-(1h-四氮唑)甲基]银杏内酯b(实施例8)200mg(0.40mmol)溶于2ml无水乙醇中,滴加等摩尔量的赖氨酸的甲醇溶液,室温搅拌2小时后,减压蒸除溶剂,加入10ml乙醚洗涤,过滤得淡黄色固体245mg,收率93%。
实施例17、体外活性测试
实验方法:新西兰白兔戊巴比妥钠(2%,2ml/kg)麻醉,腹主动脉穿刺取血约40ml。离心1000rpm/min×10min取上清为prp,剩余血液离心4000rpm/min×10min取上清为ppp;空白对照组:100ulprp+100ul生理盐水;药物组:100ulprp+100ul0.05%dmso溶解的不同浓度的药物(102,103和104nm),银杏内酯b为阳性对照组,温育5min后,加入2ulpaf(10×终浓度为145nm);血小板聚集仪测试聚集率,每个样品重复三组,得到的聚集率除以空白对照组的平均值,得到校正值,进行比较;
结果显示:各组均表现出血小板聚集抑制活性,抑制程度并随着药物浓度的增加而增强(如图1所示)。
实施例18、化合物体内活性测试实验
实验方法:sd大鼠用水合氯醛以400mg/kg的剂量麻醉后,于正中切开腹壁,分离下腔静脉,并于左肾静脉下方预置缝合线以备结扎用,各药物组由尾静脉注射,以等容量生理盐水为阴性对照,阿司匹林为阳性对照(给药量均为20mg/kg)。给药10分钟后结扎下腔静脉,关闭腹腔;
结扎后4h重新打开腹腔,于结扎处下方2cm处夹闭血管,同时夹闭该部分的主要静脉侧枝并用注射器吸尽静脉内残余血液,纵剖血管,观察是否有无血栓形成;若有血栓形成,则于烤箱内60℃烘20分钟称其干重,记录血栓形成动物数及血栓干重,结果如表1所示;
表1.化合物实施例15sd大鼠体内的抗血栓活性
- 还没有人留言评论。精彩留言会获得点赞!