一种N-(6-羟基己基)咔唑衍生物及N-(6-羟基己基)咔唑及其衍生物的合成方法与流程
本发明涉及含氮芳杂环化合物合成技术领域,具体涉及一种n-(6-羟基己基)咔唑衍生物及n-(6-羟基己基)咔唑及其衍生物的合成方法。
背景技术:
n-(6-羟基己基)咔唑及其衍生物是一类重要的含氮芳杂环化合物,分子内含有较大的共轭体系和较强的分子内电子转移,这种特殊的刚性稠环结构使咔唑类化合物具有优良的化学稳定性和电子流动性能。富电子结构使得n-(6-羟基己基)咔唑及其衍生物很容易在咔唑环上发生亲核取代反应方便地引入各种功能基团从而调节分子的光电性能。更为重要的是由于羟基位点的存在,使得n-(6-羟基己基)咔唑及其衍生物很容易通过接枝的方法在不影响分子本身光电性能的情况下连接到聚合物主链上,便于做成光电性能优良的器件满足应用的需求。
随着对n-(6-羟基己基)咔唑及其衍生物研究地不断深入,科研工作者发现现有的合成方法已不能满足于n-(6-羟基己基)咔唑及其衍生物需求量不断增加的趋势。因此,开发一种快速、高效的合成方法迫在眉睫。目前n-(6-羟基己基)咔唑及其衍生物合成方法主要是通过咔唑及其衍生物、1,6-二溴己烷在碱性条件下反应生成n-(6-溴代己基)咔唑及其衍生物,n-(6-溴代己基)咔唑及其衍生物在催化剂作用下与乙酸钠反应生成n-(6-乙酰氧基己基)咔唑及其衍生物,产物在强碱溶液中发生水解最终得到n-(6-羟基己基)咔唑及其衍生物。该合成方法步骤繁琐需要长的反应时间,同时三步合成大大降低了最终产物的产率导致合成成本的增加。
技术实现要素:
为解决以上技术问题,本发明提供一种n-(6-羟基己基)咔唑衍生物及n-(6-羟基己基)咔唑及其衍生物的合成方法,该合成方法快速高效。
技术方案如下:
一种n-(6-羟基己基)咔唑衍生物,其关键在于其通式如下:
其中r为烷氧基。
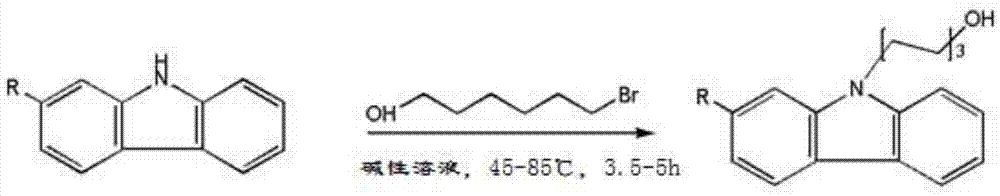
一种n-(6-羟基己基)咔唑及其衍生物的合成方法,其关键在于按以下步骤进行:取咔唑或其衍生物和相转移催化剂加入有机溶剂中,搅拌使咔唑或其衍生物溶解于有机溶剂,再加入饱和碱性溶液以及6-溴正己醇,其中咔唑或其衍生物与6-溴正己醇的摩尔比为1:1.02-1.5,在45-85℃下剧烈搅拌使咔唑或其衍生物与6-溴正己醇充分反应,然后分离得到n-(6-羟基己基)咔唑或其衍生物。
上述合成方法的反应过程如图1所示,该方法一步即合成了n-(6-羟基己基)咔唑及其衍生物,反应效率高,反应成本低,底物适性高等,非常适用于工业化大规模生产。与现有合成方法相比,本合成方法具有以下优势:所涉及的反应对官能团具有非常好的容忍性和普适性,可用于制备各种n-(6-羟基己基)咔唑的医药、农药、光电材料和高分子功能材料等;本方法所涉及的反应环境友好,底物无需预官能团化、无需官能团保护且反应不需要无水无氧条件,操作非常简单;产物单一,分离提纯非常便捷,产物纯度高。
相转移催化剂用量为咔唑或其衍生物用量的5-10%,每1mol咔唑或其衍生物需加入1.5-2.5l有机溶剂、1.0-1.5l强碱溶液。
上述反应时间为3.5-5h。
上述咔唑衍生物的通式如下:
其中r选自氢或者烷氧基。其中烷氧基可以是甲氧基(-o-ch3)等。上述相转移催化剂为季铵盐相转移催化剂;
所述有机溶剂为二甲基亚砜、n,n-二甲基甲酰胺或1,3-二甲基-3,4,5,6-四氢-2-嘧啶酮;
所述碱性溶液为氢氧化钠溶液、氢氧化钾溶液或强氧化钙溶液。本合成反应对碱溶液的纯度没有特别的要求。反应的最佳有机溶剂是二甲基亚砜,dmf在强碱条件性不稳定,尤其是高温时易分解,会降低最终产物的产率。
上述反应温度为65℃,反应时间为4h,咔唑或其衍生物与6-溴正己醇的摩尔比为1:1.2。6-溴正己醇的用量略大于于咔唑或其衍生物,有利于保证反应完全,若6-溴正己醇过多又会造成产物与和6-溴正己醇进一步反应,二者的比例为1:1.2时反应产率最高,反应四小时产量可达90%以上。
上述季铵盐为苄基三乙基氯化铵、苄基三乙基溴化铵、四丁基溴化铵、四丁基氯化铵、三辛基甲基氯化铵、十二烷基三甲基氯化铵或十四烷基三甲基氯化铵。
有益效果:采用本发明的有益效果是一步即合成了n-(6-羟基己基)咔唑及其衍生物,反应效率高,反应成本低,底物适性高等,非常适用于工业化大规模生产。与现有合成方法相比,本合成方法所涉及的反应对官能团具有非常好的容忍性和普适性,可用于制备各种n-(6-羟基己基)咔唑的医药、农药、光电材料和高分子功能材料等;本方法所涉及的反应环境友好,底物无需预官能团化、无需官能团保护且反应不需要无水无氧条件,操作非常简单;产物单一,分离提纯非常便捷,产物纯度高。
附图说明
图1为本发明的反应过程示意图;
图2为实施例1的合成路线图;
图3为n-(6-羟基己基)咔唑的红外图谱;
图4为实施例3的合成路线图;
图5为衍生物n-(6-羟基己基)甲氧基咔唑的红外图谱。
具体实施方式
下面结合实施例和附图对本发明作进一步说明。
实施例1,一种n-(6-羟基己基)咔唑的合成方法,按以下步骤进行:在单口烧瓶中依次加入咔唑1.67g(10mmol),苄基三乙基氯化铵150mg,二甲基亚砜20ml,饱和氢氧化钠15ml,6-溴正己醇1.57ml(12mmol),磁力搅拌下于65℃反应4h。加入去离子水100ml,乙酸乙酯100ml,分液,有机相用水洗涤多次直到溶液呈中性(一般3次),分离有机相加入无水硫酸钠干燥,过滤,减压旋蒸除去乙酸乙酯,残留物经硅胶柱层析(洗脱剂:二氯甲烷)分离得白色固体n-(6-羟基己基)咔唑2.54g,产率95%。合成路线如图2所示。
产物n-(6-羟基己基)咔唑表征数据包括:
(1)红外图谱如图3所示,ir(kbr,cm-1):3306(-oh);3050,1625,1594,1484,1465(carbazole);2926(alkyl-h);2858(methylene-h)。
(2)核磁氢谱:
1hnmr(300mhz,cdcl3):δ8.10(d,2h),7.45(t,2h),7.39(d,2h),7.23(q,2h),4.29(t,2h),3.58(t,2h),1.88(m,2h),1.52(m,2h),1.39(m,4h)。
(3)核磁碳谱:
13cnmr(300mhz,cdcl3):δ140.43,125,62,122.85,120.39,118.77,108.65,62.79,42.98,32.59,28.97,27.11,25.57。
实施例2,一种n-(6-羟基己基)咔唑的合成方法,按以下步骤进行:在单口烧瓶中依次加入咔唑1.67g(10mmol),四丁基溴化铵75mg,n,n-二甲基甲酰胺15ml,饱和氢氧化钾10ml,6-溴正己醇10.02mmol,磁力搅拌下于45℃反应3.5h。加入去离子水100ml,乙酸乙酯100ml,分液,有机相用水洗涤多次直到溶液呈中性(一般3次),分离有机相加入无水硫酸钠干燥,过滤,减压旋蒸除去乙酸乙酯,残留物经硅胶柱层析(洗脱剂:二氯甲烷)分离得白色固体n-(6-羟基己基)咔唑2.14g,产率50%。
实施例3,一种n-(6-羟基己基)甲氧基咔唑的合成方法,按以下步骤进行:
在单口烧瓶中依次加入甲氧基咔唑1.97g(10mmol),苄基三乙基氯化铵150mg,二甲基亚砜20ml,饱和氢氧化钠15ml,6-溴正己醇1.57ml(12mmol),磁力搅拌下于65℃反应4h。加入去离子水100ml,乙酸乙酯100ml,分液,有机相用水洗涤多次直到溶液呈中性(一般3次),分离有机相加入无水硫酸钠干燥,过滤,减压旋蒸除去乙酸乙酯,残留物经硅胶柱层析(洗脱剂:二氯甲烷)分离得白色固体n-(6-羟基己基)甲氧基咔唑2.7g,产率90%。合成路线如图4所示。
产物n-(6-羟基己基)甲氧基咔唑表征数据包括:
(1)红外图谱如图5所示:
ir(kbr,cm-1):3389(-oh);3049,1630,1601,1498,1463(carbazole);2933(alkyl-h);
2857(methylene-h)。
(2)核磁氢谱:
1hnmr(300mhz,(cd3)2so):δ8.00(dd,2h),7.59(d,1h),7.35(t,1h),7.14(t,1h),7.10(d,1h),6.80(dd,1h),4.38(t,1h),4.33(t,2h),3.88(s,3h),3.34(q,2h),1.75(m,2h),1.36(m,2h),1.30(m,4h)。
(3)核磁碳谱:
13cnmr(300mhz,cdcl3):δ158.97,141.73,140.54,124.31,122.98,121.02,119.45,118.85,116.80,108.38,106.86,93.28,62.62,55.68,42.83,32.48,28.74,26.99,25.49。
实施例4,一种n-(6-羟基己基)甲氧基咔唑的合成方法,按以下步骤进行:
在单口烧瓶中依次加入甲氧基咔唑1.97g(10mmol),十二烷基三甲基氯化铵90mg,1,3-二甲基-3,4,5,6-四氢-2-嘧啶酮25ml,饱和氢氧化钠12ml,6-溴正己醇15mmol,磁力搅拌下于85℃反应5h。加入去离子水100ml,乙酸乙酯100ml,分液,有机相用水洗涤多次直到溶液呈中性(一般3次),分离有机相加入无水硫酸钠干燥,过滤,减压旋蒸除去乙酸乙酯,残留物经硅胶柱层析(洗脱剂:二氯甲烷)分离得白色固体n-(6-羟基己基)甲氧基咔唑2.79g,产率75%。
最后需要说明的是,上述描述仅仅为本发明的优选实施例,本领域的普通技术人员在本发明的启示下,在不违背本发明宗旨及权利要求的前提下,可以做出多种类似的表示,这样的变换均落入本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!