羰基合钴配合物及其制备方法与流程
本发明属于有机金属配合物领域,涉及一种羰基合钴配合物及其制备方法,具体涉及一种二水高氯酸双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺·羰基合钴(ⅲ)配合物及其制备方法。
背景技术:
三足配体具有半刚性的结构特征,其三条侧链可自由翻转形成空腔,加之丰富多变的侧链取代基类型,使得它与金属离子配位时表现出特有的选择性配位能力及多变的配位模式。三足配体化合物及其配合物在光学、电学、磁学等方面均表现出良好的应用前景。近年来,对于新型三足配体及其配合物的结构设计与制备研究,已成为有机化学、配位化学以及超分子化学等领域的热门研究课题之一。
以三足羰基钴配合物的制备与酸解特性为例,由于四元碳酸根螯合环在质子化的过程中变得紧张,即使螯合金属配合物也不能保护碳酸酯免受酸水解,导致大部分配位碳酸盐在酸性水溶液中发生开环反应而水解。allanblackman课题组及其导师一直在研究三足羰基钴(iii)配合物以及三足羰基铜(ⅱ)配合物,曾在inorganicchemistry发表一篇“在酸性水溶液中配位羰基化合物的稳定性:空间阻力对含有螯合羰基钴(iii)配合物中的质子化的影响”,设计构造并合成了[co(tpa)(o2co)]clo4·h2o、[co(me-tpa)(o2co)]clo4·0.5h2o、[co(me3-tpa)(o2co)]clo4共3种三足羰基钴配合物,并对配合物的酸解速率进行研究后发现:在相同条件下,含有甲基化配体的配合物酸解速率比[co(tpa)(o2co)]+慢25到90倍,且很大的原因是空间因素引起的;并且提出其酸解的可能性:即在酸性条件下,引入的6-甲基吡啶基环导致三足配体的扭曲,c=o断裂,生成羟基。
三足配体的化学结构与空间排列的不同,三足配体与羰基上氧原子形成分子内氢键的强弱,均可能导致酸解过程中质子的传递机理与质子化速率发生改变,从而改变其酸解机理。可见,构建和制备新型模型三足羰基钴配位化合物,在有机金属配合物学科的制备及其反应性等基础研究中占有重要的学术地位。因此,在三足配体中设计不同取代数目、不同空间取代位置、不同类型的取代基,分别可以构造出多种三足配体,而不同三足配体上的取代基在空间位置上可能与羰基氧形成强度与数目不同的分子内氢键,对三足钴配合物的酸解研究具有非常重要的意义,但是由于三足配体及其配合物化学结构的特殊性、以及其制备路线的复杂性,制备和研究具有不同空间构型的新型有机金属配合物是一直是基础学科研究领域的一个难点和热点方向。
技术实现要素:
本发明要解决的技术问题是克服现有技术的不足,提供一种羰基合钴配合物及其制备方法,为配位化学等基础学科领域提供新的结构模型。
为解决上述技术问题,本发明采用的技术方案为:
一种羰基合钴配合物,所述羰基合钴配合物的分子式为[co(bapa)(o2co)]clo4·2h2o,其中bapa表示双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。
上述的羰基合钴配合物,进一步改进的,所述羰基合钴配合物的结构式如式(ⅰ)或式(ⅱ)所示:
上述的羰基合钴配合物,进一步改进的,所述羰基合钴配合物属三斜晶系,空间点群为p-1,晶胞参数为:
作为一个总的技术构思,本发明还提供了一种上述的羰基合钴配合物的制备方法,包括以下步骤:
(1)将[co(h2o)6](clo4)2、双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺、nahco3和h2o/甲醇混合溶剂混合,得到混合溶液;
(2)将空气通入到步骤(1)得到的混合溶液中进行鼓泡,搅拌,使混合溶液发生反应,所得反应产物经后处理,得到羰基合钴配合物。
上述的制备方法,进一步改进的,所述双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺的制备方法,包括以下步骤:
(a)将2-氨基-6-甲基吡啶溶于ch2cl2/三乙胺混合溶剂中,滴加特戊酰氯进行反应,所得反应产物经后处理,得到2-特戊酰氨基-6-甲基吡啶;
(b)将步骤(a)得到的2-特戊酰氨基-6-甲基吡啶溶于除去空气的四氯化碳中,加入n-溴代丁二酰亚胺和偶氮二异丁腈,在氮气保护下进行反应,所得反应产物经后处理,得到2-特戊酰氨基-6-溴甲基吡啶;
(c)将步骤(b)得到的2-特戊酰氨基-6-溴甲基吡啶和2-吡啶甲基胺溶于1,4-二氧六环/h2o混合溶剂中,加入koh进行反应,所得反应产物经后处理,得到双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺;
(d)将步骤(c)得到的双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶于乙醇中,加入koh进行反应,所得反应产物经后处理,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。
上述的制备方法,进一步改进的,所述步骤(a)中:所述2-氨基-6-甲基吡啶与ch2cl2/三乙胺混合溶剂的比例为0.07mmol~0.08mmol∶100ml;所述特戊酰氯与ch2cl2/三乙胺混合溶剂比例为0.10mmol~0.12mmol∶100ml;所述ch2cl2/三乙胺混合溶剂中ch2cl2和三乙胺的比例为6ml~8ml∶1g。
上述的制备方法,进一步改进的,所述步骤(b)中:所述2-特戊酰氨基-6-甲基吡啶、n-溴代丁二酰亚胺、偶氮二异丁腈的摩尔比为1∶1∶0.05。
上述的制备方法,进一步改进的,所述步骤(c)中:所述2-吡啶甲基胺、2-特戊酰氨基-6-溴甲基吡啶、koh的摩尔比为3.25∶7.50∶13.00;所述1,4-二氧六环/h2o混合溶剂中1,4-二氧六环和h2o的体积比为4∶1。
上述的制备方法,进一步改进的,所述步骤(d)中:所述双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺、乙醇、koh的比例为3.25mmol∶163ml∶160mmol。
上述的制备方法,进一步改进的,所述步骤(a)中:所述反应在搅拌条件下进行;所述反应的时间为12h~24h;所述后处理包括以下步骤:将反应产物过滤,除去沉淀,除去所得滤液中的溶剂,得到2-特戊酰氨基-6-甲基吡啶粗品;采用乙醚对2-特戊酰氨基-6-甲基吡啶粗品进行重结晶,洗涤,干燥,得到2-特戊酰氨基-6-甲基吡啶。
上述的制备方法,进一步改进的,所述步骤(b)中:所述反应的时间为6h~12h;所述后处理包括以下步骤:除去反应产物中的溶剂,得到2-特戊酰氨基-6-溴甲基吡啶粗品;以石油醚/乙酸乙酯为淋洗剂,采用二氧化硅柱对2-特戊酰氨基-6-溴甲基吡啶粗品进行层析分离,得到2-特戊酰氨基-6-溴甲基吡啶;所述淋洗剂中石油醚/乙酸乙酯的体积比为8∶1。
上述的制备方法,进一步改进的,所述步骤(c)中:所述反应在搅拌条件下进行;所述反应的时间为2天~4天;所述后处理包括以下步骤:采用浓度为1mol/l的hcl溶液中和反应产物,在真空条件下对反应产物进行蒸发,得到双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品;采用乙醚对双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品进行重结晶,得到双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。
上述的制备方法,进一步改进的,所述步骤(d)中:所述反应在搅拌条件下进行;所述反应的温度为60℃;所述反应的时间为4天~7天;所述后处理包括以下步骤:除去反应产物中的溶剂,所得固体物质溶于水中,采用ch2cl2萃取至少5次;萃取完成后,除去萃取所得固体物质中的ch2cl2,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品;将双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶于甲醇中,加入活性炭除杂,过滤,蒸发,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。
上述的制备方法,进一步改进的,所述步骤(1)中,包括以下步骤:
(1.1)将[co(h2o)6](clo4)2溶解于h2o/甲醇混合溶剂中,得到[co(h2o)6](clo4)2溶液;将双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶解于h2o/甲醇混合溶剂中,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶液;
(1.2)将[co(h2o)6](clo4)2溶液加入到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶液中,加入nahco3,搅拌,得到混合溶液。
上述的制备方法,进一步改进的,所述[co(h2o)6](clo4)2、双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺和nahco3的摩尔比为1~1.03∶1∶1;所述[co(h2o)6](clo4)2与h2o/甲醇混合溶剂的比例为4.06mmol∶24ml;所述双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺与h2o/甲醇混合溶剂的比例为3.96mmol∶72ml;所述h2o/甲醇混合溶剂中h2o和甲醇的体积比为1∶1。
上述的制备方法,进一步改进的,所述步骤(2)中,所述鼓泡过程中空气的发泡速率控制在每秒发出1到2个气泡;所述搅拌的时间为36h~144h;所述后处理包括以下步骤:将反应产物过滤,采用真空旋转干燥法除去过滤所得滤液中的溶剂,得到羰基合钴配合物粗品;将羰基合钴配合物粗品溶于去离子水中,采用sp-c25型阳离子交换树脂对羰基合钴配合物进行提纯,除去溶剂,结晶,干燥,得到羰基合钴配合物。
本发明中,双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)的结构式如式(ⅲ)所示:
本发明中,羰基合钴配合物的空间结构是以co为中心,co离子的配位数是6,来自bapa上的4个n以及羰基上的两个o,形成八面体空间构型,两个取代氨基位于轴方向或径向的吡啶环上。
本发明的制备方法中,双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)与钴离子形成配合物时,在空间构型上能形成轴向和面向两种异构体,也就是说,反应结束后,所得反应产物是由含有两种不同空间构型的羰基合钴配合物组成。
本发明的制备方法中,羰基合钴配合物[co(bapa)(o2co)]clo4·2h2o的制备原理如下:
本发明的制备方法中,双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)的制备原理如下:
与现有技术相比,本发明的优点在于:
(1)本发明提供了一种羰基合钴配合物,分子式为[co(bapa)(o2co)]clo4·2h2o,其中bapa表示双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。本发明中,双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺是一种多齿、多点配位的三足有机配体,能够与过渡金属钴形成稳定的配合物,带有bapa的羟基合钴配合物具有2个取代氨基,取代氨基在合适的空间位置上可以与羰基上的氧形成分子内氢键,由于分子内氢键的形成会影响质子的传递过程,从而影响其酸解速率与酸解机理,配合物上取代氨基的空间位置与数目在研究三足羰基钴配合物在酸解开环过程中具有重要的作用。本发明羰基合钴配合物是一种全新的带有三足配体的羰基合钴(ⅲ)配合物,作为一种新颖的结构模型,其为配位化学的研究提供了一种重要的研究对象,具有极高的学术价值。
(2)本发明提供了一种羰基合钴配合物的制备方法,将[co(h2o)6](clo4)2、双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺、nahco3和h2o/甲醇混合溶剂混合,在室温条件下,在空气发泡作用下搅拌反应得到羰基合钴配合物,反应条件温和,能耗低。本发明中,还采用了sp-c25型阳离子交换树脂对羰基合钴配合物进行提纯,提纯效率高。本发明羰基合钴配合物的制备方法具有反应条件温和、低能耗、提纯效率高等优点,对制备羰基合钴配合物具有十分重要的意义。
(3)本发明制备方法中,所用双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺,是以2-氨基-6-甲基吡啶、2-吡啶甲基胺为原料,通过四步反应及分离提纯得到。在双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺的制备过程中,采用了工艺流程短的制备步骤,优选价格低且易与产物分离的试剂作为制备所用试剂,有利于降低制备成本和提高产率。如,在制备中间产物2-特戊酰氨基-6-溴甲基吡啶的步骤中,采用二氧化硅柱对2-特戊酰氨基-6-溴甲基吡啶粗品进行层析分离,优选了石油醚/乙酸乙酯(8∶1)作洗脱剂,代替价格较高的己烷/乙酸乙酯(6∶1),进一步降低了制备成本。
附图说明
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整的描述。
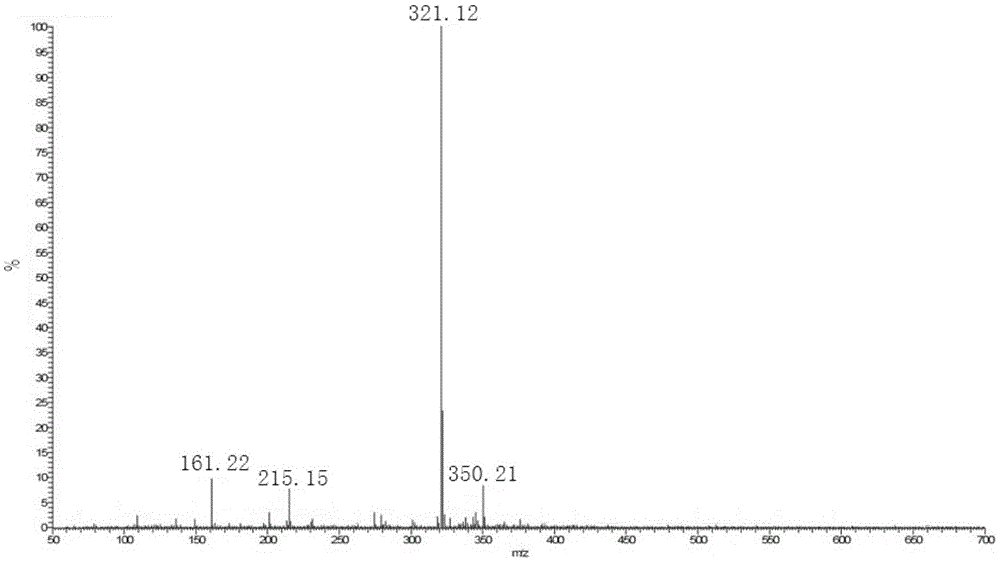
图1为本发明实施例1制得的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺的高分辨质谱图。
图2为本发明实施例1制得的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺的核磁共振1hnmr谱图。
图3为本发明实施例1中制得的羰基合钴配合物的高分辨质谱图。
图4为本发明实施例1中利用x-ray单晶衍射测试数据绘制的羰基合钴配合物的不对称结构图。
图5为本发明实施例1中利用x-ray单晶衍射测试数据绘制的羰基合钴配合物中[co(bapa)(o2co)]+阳离子的晶体堆积图。
图6为本发明实施例1中制得的羰基合钴配合物的核磁共振1hnmr谱图。
图7为本发明实施例1中制得备的羰基合钴配合物的紫外-可见光谱图。
具体实施方式
以下结合说明书附图和具体优选的实施例对本发明作进一步描述,但并不因此而限制本发明的保护范围。
实施例1:
一种羰基合钴配合物,分子式为[co(bapa)(o2co)]clo4·2h2o,其中bapa表示双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺。
本实施例中,羰基合钴配合物的结构式如式(ⅰ)或式(ⅱ)所示,这说明本发明羰基合钴配合物含有两种结构异构体,即可以是轴向异构体,也可以是面向异构体。
本实施例中,羰基合钴配合物属三斜晶系,空间点群为p-1,晶胞参数为:
一种上述本实施例的羰基合钴配合物的制备方法,包括以下步骤:
(1)制备双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa):
(1.1)将250mlch2cl2和32.8868g三乙胺(0.17mmol)混合制成ch2cl2/三乙胺混合溶剂,加入27.2242g(0.19mmol)2-氨基-6-甲基吡啶,搅拌至溶解,然后逐滴加入33.1595g(0.275mmol)特戊酰氯,在室温、搅拌条件下进行反应12h;反应完成后,将得到的反应产物进行过滤,除去沉淀,所得滤液采用真空旋转干燥法除去溶剂,得到淡黄色的2-特戊酰氨基-6-甲基吡啶粗品;用乙醚对2-特戊酰氨基-6-甲基吡啶粗品进行重结晶,所得晶体采用正已烷洗涤,干燥,得到28.6307g白色针状晶体,即2-特戊酰氨基-6-甲基吡啶,产率为59.14%。
(1.2)取15.3832g(0.08mmol)步骤(1.1)得到的2-特戊酰氨基-6-甲基吡啶,溶于200ml已经除去空气的四氯化碳中,加入14.2384g(0.08mmol)n-溴代丁二酰亚胺(nbs)和0.6568g(0.004mmol)偶氮二异丁腈,在氮气的保护下回流反应6h;反应完成后,将反应产物冷却至室温,用真空旋转干燥法除去溶剂,得到棕色油状混合物(2-特戊酰氨基-6-溴甲基吡啶粗品);以8∶1的石油醚/乙酸乙酯为淋洗剂,采用二氧化硅柱对2-特戊酰氨基-6-溴甲基吡啶粗品进行层析分离,得到4.9723g黄色结晶状的2-特戊酰氨基-6-溴甲基吡啶,产率为22.99%。
(1.3)将0.3514g(3.25mmol)2-吡啶甲基胺和步骤(1.2)得到的2.0336g(7.5mmol)2-特戊酰氨基-6-溴甲基吡啶,溶于75ml1,4-二氧六环/h2o混合溶剂(该混合溶剂中1,4-二氧六环和h2o的体积比4∶1)中,加入0.7294g(13mmol)koh,所得混合溶液在室温、搅拌条件下反应2天;反应完成后,用1mol·l-1hcl溶液将所得反应产物溶液进行中和,然后在在真空条件下进行蒸发,除去溶剂,得到褐色油状粗产物(即为双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品);采用乙醚对双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品进行重结晶,得到2.1539g无色针状晶体状的目标产物,即双(6-特戊酰氨基-2-吡啶基甲基)(2-吡啶基甲基)胺,缩写为bppa。
(1.4)取2.1539g(3.25mmol)步骤(1.3)得到的bppa溶于163ml乙醇中,加入koh溶液(该溶液由koh溶于少量水中制得,且该溶液中含有8.9776gkoh(160mmol)),所得混合溶液在温度为60℃的搅拌条件下反应4天。反应过程中,用薄层色谱(chcl3/meoh=7/1,rf=0.05)对反应产物进行检测。反应完成后,将所得反应液进行减压蒸发,除去溶剂,所得固体物质溶于4ml水中;采用40mlch2cl2对水中的目标产物进行萃取至少5次;萃取完成后,合并ch2cl2相,减压旋转蒸发将ch2cl2蒸发干,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品;将双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺粗品溶于4ml甲醇溶液中,加入活性炭除杂,过滤除去活性炭,将过滤所得的滤液中的溶剂蒸发,得到0.8384g红棕色粘稠状的目标产物,即双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺,缩写为bapa,产率80.51%。
(2)制备[co(h2o)6](clo4)2和bapa的混合溶液:
(2.1)称取1.519g(4.06mmol)[co(h2o)6](clo4)2溶解于24mlh2o/甲醇混合溶剂中,得到[co(h2o)6](clo4)2溶液;称取1.270g(3.96mmol)步骤(1)中制得的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa),溶于72mlh2o/甲醇混合溶剂中,得到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶液。该步骤中,所用h2o/甲醇混合溶剂中h2o和甲醇的体积比为1∶1。
(2.2)将步骤(2.1)中的[co(h2o)6](clo4)2溶液加入到双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺溶液中,加入0.333g(3.96mmol)nahco3,搅拌,混合均匀,得到混合溶液。
(3)制备羰基合钴配合物:采用市售的低功率小型气泵向步骤(2)得到的混合溶液中通入空气鼓泡,其中鼓泡过程中空气的发泡速率控制在每秒发出1到2个气泡,在室温下对混合溶液搅拌6天,使混合溶液发生反应生成羰基合钴配合物(即为二水高氯酸双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺·羰基合钴(ⅲ)配合物)。反应停止后,将反应后的反应产物过滤,得到红色滤液和棕色滤渣;将红色滤液真空旋转干燥得到1.9568g粗产物(即为羰基合钴配合物粗品);将粗产物溶于去离子水中,得到淡红色溶液;以sephadexsp-c25型阳离子交换柱对淡红色溶液进行分离提纯,重结晶,干燥,得到羰基合钴配合物。
通过高分辨质谱、1hnmr对上述本实施例制备的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)进行结构表征,结果如图1和图2所示。
图1为本发明实施例1制得的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)的高分辨质谱图。双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)的分子式为:c18h20n6,分子量320.17,结合一个质子所形成的[bapah]+的理论荷质比m/z为321.18。由图1可知,本发明实施例1制备的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)样品的质谱测试图中最大m/z峰为321.21,对应[bapah]+的荷质比,表明产物为双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)。
图2为本发明实施例1制得的双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)的核磁共振1hnmr谱图。图2中:1hnmr(400mhz,dmso)δ(ppm):8.49(d,j=4.4hz,1h),7.78(t,j=7.6hz,1h),7.60(d,j=7.8hz,1h),7.34(t,j=7.7hz,2h),7.27-7.23(m,1h),6.72(d,j=7.2hz,2h),6.29(d,j=8.1hz,2h),3.71(s,2h),3.49(s,4h)。由图2可知,与氨基吡啶环相连的亚甲基氢化学位移对应3.49ppm,这两个氨基取代吡啶环上的氢化学位移依次为6.29ppm、6.72ppm和7.34ppm;与吡啶环相连的亚甲基氢的化学位移为3.71ppm,该吡啶环上的氢化学位移分别对应7.27-7.23、7.60ppm、7.78ppm和8.49ppm;-nh2在极性dmso中未出峰。3.31ppm和2.51ppm为dmso中水的溶剂峰,1.20和0.96为残留的少量溶剂乙醇和二氯乙烷的溶剂峰。1hnmr图谱所示的h峰的化学位移和峰面积比,均与双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)分子的结构特征相符。
由以上结果可知,本发明中已成功合成双(6-氨基-2-吡啶基甲基)(2-吡啶基甲基)胺(bapa)。
通过高分辨质谱、x-ray单晶衍射、1hnmr、紫外-可见光谱和元素分析对上述本实施例制备的羰基合钴配合物进行结构和成分测定,结果如图3至图7所示。
采用watersxevog2-xsqtof高分辨质谱测试仪对本发明实施例1中制得的羰基合钴配合物进行测试,结果如图3所示。图3为本发明实施例1制得的羰基合钴配合物的高分辨质谱图。本发明实施例1中制得的羰基合钴配合物的分子式为[co(bapa)(o2co)]clo4·2h2o,其中阳离子[co(bapa)(o2coo)]+的组成式为:c19h20con6o3,[co(bapa)(o2coo)]+的理论荷质比m/z为439.09。由图3可知,该羰基合钴配合物晶体样品的质谱测试图中最大m/z峰为439.09,对应阳离子[co(bapa)(o2coo)]+的荷质比,表明产物为目标产物。
本发明实施例1中采用挥发溶剂法制备的羰基合钴配合物晶体,其晶体结构测定采用brukerkappaapex-ⅱx-射线衍射仪,使用经过石墨单色化的mokα射线为入射辐射,以ω-2θ扫描方式收集衍射点。利用helxl-97经过最小二乘法修正得到晶胞参数,利用wingxv1.80解得晶体结构。所有的h原子由差值fourier合成并经理想位置计算。详细的晶体学测定数据如表1所示:
表1本发明实施例1制得的[co(bapa)(o2co)]clo4·2h2o的x-ray单晶衍射测试晶体学数据表
图4为本发明实施例1中利用x-ray单晶衍射测试数据绘制的羰基合钴配合物的化合物不对称结构图。从羰基合钴配合物样品单晶测试结果显示:羰基合钴配合物的两个取代氨基,在图4中所示的编号为6n和6n′的位置的机率各为50%。
图5为本发明实施例1中利用x-ray单晶衍射测试数据绘制的羰基合钴配合物的晶体堆积图。由图5可知,羰基合钴配合物的晶体存在无序结构。
在25℃下,采用400mhz核磁共振仪对本发明实施例1中制得的羰基合钴配合物进行测试,结果如图6所示。图6为本发明实施例1制备的羰基合钴配合物的核磁共振1hnmr谱图。图6中:1hnmr(400mhz,dmso)δ9.61(s,1h),8.59(s,1h),8.16–8.06(m,1h),8.06–7.96(m,1h),7.74–7.33(m,6h),7.24(s,1h),6.81–6.34(m,6h),5.33(d,j=17.0hz,1h),4.96(ddd,j=72.6,41.7,17.0hz,5h),4.59(dd,j=31.4,19.1hz,3h)。由图6测试结果所示的分子中氢的类型和数据表明,该晶体组成中应包含两种异构体。同时,结合表1和图6中的结果可知,在所测试的温度下,核磁和单晶衍射测试结果表明,本发明制备方法制得的羰基合钴配合物中两种异构体的含量各为50%。
在25℃下,采用北京莱伯泰科仪器股份有限公司的bluestara紫外仪对本发明实施例1中制得的羰基合钴配合物进行测试,结果如图7所示。图7为本发明实施例1中制得的羰基合钴配合物的紫外-可见光谱图。由图7可知,配位中心原子co的最大吸收波长λmax有两个,分别是516nm和517nm,其对应吸光度的值都为0.3024,表明产物中确实形成了配位键。
本发明制备的羰基合钴配合物的化学式为[co(bapa)(o2co)]clo4·2h2o或c19h24clcon6o9,其中各元素含量的理论计算值为:c,39.70;h,4.21;cl,6.17;co,10.25;n,14.62;o,25.05;本发明制备的羰基合钴配合物晶体的元素分析测定结果为c,39.33;h,4.247;n,14.88,与理论值相符。
由以上检测结果可知,本发明制备方法已成功制备得到羰基合钴配合物,且该制备方法制得的产品中包含轴向异构体和面向异构体两种异构体分子的羰基合钴配合物,同时这两种异构体的含量各为50%。经过多次对产物在不同温度条件、在层析柱分离过程中,对不同析出顺序进行1hnmr测试,经过与图6所示的谱图对比,谱图所示的h的类型与数据均无变化,表示构成产物晶体及相应溶液中,两个异构体的成份不会随温度发生变化,也无法通过层析柱法进行分离。
以上所述仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例。凡属于本发明思路下的技术方案均属于本发明的保护范围。应该指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下的改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!