包含植物来源的脂肪酸氧化抑制剂的食品稳定组合物的制作方法
本发明涉及包含至少一种植物来源的脂肪酸氧化抑制剂的食品稳定组合物、用于提供这类组合物的方法和所述组合物和包含这类组合物的食品的方法和用途。
稳定化合物和组合物、例如抗氧化剂和螯合剂广泛应用于易发生氧化变性、例如油氧化的食品。
抗氧化剂广泛应用于易发生氧化变性的食品中。食品药品监督管理局(foodanddrugadministration)(21cfr170.3)将抗氧化剂定义为“一种用于通过延缓由于氧化引起的变质、酸败或变色来保存食物的物质”。
典型地,氧化变性、例如油氧化由游离金属离子例如铁和铜离子催化。传统上,乙二胺四乙酸(edta)由于其螯合金属的能力已被用于食品中,以防止食品的氧化变性以及所导致的腐败。
然而,edta是一种合成或人造成分,近年来,由于它们可能对消费者的健康产生负面影响,因此在食品中使用合成或人造成分已成为人们关注的问题。
这导致公众对人造食品成分的天然替代品的需求增加。
为此,香料或植物汁液或植物提取物或植物产品可在食品中用作抗氧化剂,并赋予食品基质香味或颜色或其它感官特征。这类提取物的一个优点在于,与edta和其它抗氧化剂例如丁羟茴醚(bha)和丁羟甲苯(bht)相比,它们被视为天然成分。然而,香料和或植物汁液或植物提取物或植物产品可以包含可能使掺入它们的食品变色或着色的成分,这可以证实对消费者而言是不期望的。
已经研究了几种不同的植物材料,例如水果,蔬菜,农作物,药草和香料作为抗氧化剂化合物的潜在来源。抗氧化剂化合物通常存在于植物材料中,因为它们在帮助植物生长和发育方面很重要。
然而,天然植物材料的抗氧化功效差异很大。鉴于此,要预测哪种植物材料或植物提取物将提供足够的稳定/抗氧化活性或者在食品中需要多少量的某种提取物并不是一件容易的事情。
另外,在某些情况下,提供足够的稳定/抗氧化活性所需的提取或表达的植物材料或植物的量可以证实并不经济,或者为不可接受的水平,这归因于法规和立法限制,或者可能以消费者不期望的方式使它们掺入的食品变色或影响它们掺入的食品的味道。
本发明人令人惊奇地发现,包含至少一种植物来源的脂肪酸氧化抑制剂的组合物在稳定易发生氧化变性的食品方面是高度有效的。例如,通过减少/防止氧化变性。
如本文所用,术语“植物来源的脂肪酸氧化抑制剂”是指来自植物来源的提取物或汁液或产品,它们减少、抑制或防止脂肪酸(例如存在于食品中的那些)被氧化。例如,植物来源的脂肪酸氧化抑制剂可以作为螯合化合物起作用。
特别地,相对于在没有稳定组合物存在下发生的氧化的量,“植物来源的脂肪酸氧化抑制剂”可以在给定期限内起到减少、抑制或防止氧化的作用。例如,存在于本发明的食品稳定组合物中的“植物来源的脂肪酸氧化抑制剂”可以通过螯合过渡金属例如cu2+和fe2+来减少、抑制或防止氧化,和/或可以提供自由基清除活性。
本发明人已经发现,包含至少一种植物来源的脂肪酸氧化抑制剂的组合物特别有效,其中所述至少一种植物来源的抑制剂为提取物或汁液或产品,其得自或可得自选自谷物、假谷物、豆科(fabaceaefamily)、唇形科(lamiaceaefamily)、金虎尾科(malpighiaceae)、苋科(amaranthaceaefamily)和千屈菜科(lythraceaefamily)及其组合的植物。
稳定组合物
本发明提供了包含至少一种植物来源的脂肪酸氧化抑制剂的食品稳定组合物,其在下文中可以称作“本发明的组合物”。例如,本发明的食品稳定组合物可以例如通过抑制或防止多不饱和脂肪酸(pufa)油转化为2,4-庚二烯醛和/或2,4-癸二烯醛来抑制或防止食品的氧化变性。
所述至少一种植物来源的脂肪酸氧化抑制剂,可替代地在本文中被称作所述至少一种植物来源的抑制剂,可以为使用如本文所述的方法得自或可得自所述至少一种植物种类的提取物或汁液或产品。
在本发明的组合物中,所述至少一种植物来源的脂肪酸氧化抑制剂可以为提取物或汁液或产品或可以形成提取物或汁液或产品的一部分,所述提取物或汁液或产品得自或可得自单一植物种类,或可以得自或可得自两种、三种或四种或更多种的植物种类。
例如,所述至少一种植物来源的抑制剂可以为提取物或汁液或产品或可以形成提取物或汁液或产品的一部分,所述提取物或汁液或产品得自或可得自至少一种植物,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,优选地,所述至少一种植物来源的抑制剂可以为提取物或汁液或产品或可以形成提取物或汁液或产品的一部分,所述提取物或汁液或产品得自或可得自至少一种植物,所述至少一种植物选自豆科、唇形科、苋科和千屈菜科及其组合和混合物,例如(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。
在本发明的一个方面,当所述至少一种植物来源的抑制剂为得自或可得自唇形科的提取物或汁液或产品时,所述至少一种植物来源的抑制剂必须包含得自或可得自至少一种选自豆科、苋科和千屈菜科及其组合和混合物的植物的提取物或汁液或产品,即得自或可得自唇形科的提取物或汁液或产品从来不是食品稳定组合物中存在的唯一的至少一种植物来源的抑制剂。
典型地,所述当至少一种植物为谷物或假谷物时,所述至少一种植物来源的抑制剂可以提取自植物的种子,例如提取自植物的种子的外壳。当所述至少一种植物为豆科、唇形科、金虎尾科、苋科和千屈菜科植物时,所述至少一种植物来源的抑制剂可以提取自植物的叶子和/或果实,例如提取自植物的果实。
特别地,所述至少一种植物来源的抑制剂可以为提取物或汁液或产品或可以形成提取物或汁液或产品的一部分,所述提取物或汁液或产品得自或可得自至少一种植物,所述至少一种植物选自豆科、唇形科、金虎尾科、苋科和千屈菜科及其混合物,即得自或可得自菠菜、豌豆、石榴、针叶樱桃(acerola)和迷迭香及其组合的提取物或汁液,优选地,所述至少一种植物来源的抑制剂可以为提取物或汁液,其得自或可得自至少一种植物,所述至少一种植物选自豆科、唇形科、苋科和千屈菜科及其组合和混合物,即得自或可得自菠菜、豌豆、石榴和迷迭香及其组合,例如(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴的提取物或汁液。
当所述至少一种植物来源的抑制剂为得自或可得自一种、两种、三种或四种或更多种植物种类的提取物时,所述提取物可以在单一提取中共同得到,或可以单独得到并且单独得到的提取物被合并在一起以提供所述至少一种植物来源的抑制剂。如果所用的不同植物种类需要不同的提取技术,则这可能特别有利。
干燥的汁液可以从补充了碳酸盐和/或不同盐的羟基化合物的浓缩的果实汁液中得到。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自至少一种谷物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自至少一种假谷物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自豆科植物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物。
例如,本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自豆科植物的提取物;和任选的得自或可得自唇形科植物的提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自唇形科植物的提取物;和任选的
(b)(i)得自或可得自金虎尾科植物的提取物(即汁液);和/或
(ii)得自或可得自苋科植物的提取物。
例如,本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自唇形科植物的提取物;和
(b)(i)得自或可得自豆科植物的提取物;和/或
(ii)得自或可得自苋科植物的提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自千屈菜科植物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自苋科植物的提取物。
例如,本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂,其中所述至少一种植物来源的抑制剂包含得自或可得自千屈菜科植物的提取物。
食品稳定组合可以包含按组合物的重量计约1%至约100%的如上述所定义的所述至少一种植物来源的抑制剂,例如约20%至约80%或约40%至约60%。
在某些方面,本发明的食品稳定组合物可以由如上述所定义的所述至少一种植物来源的抑制剂组成或主要由其组成。
例如,组合物可以由至少一种植物来源的抑制剂组成或主要由其组成,所述至少一种植物来源的抑制剂得自或可得自至少一种谷物、至少一种假谷物、豆科植物、唇形科植物、金虎尾科植物、苋科植物或千屈菜科植物或其组合,或者本发明的食品稳定组合物可以由至少一种植物来源的抑制剂组成或主要由其组成,所述至少一种植物来源的抑制剂得自或可得自:
(a)得自或可得自至少一种谷物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物;
或
(a)得自或可得自至少一种假谷物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物;
或
(a)得自或可得自豆科植物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物;
例如,得自或可得自豆科植物的提取物;和任选的得自或可得自唇形科植物的提取物。
或
(a)得自或可得自唇形科植物的提取物;和任选的
(b)(i)得自或可得自金虎尾科植物的提取物;和/或
(ii)得自或可得自苋科植物的提取物。
例如,得自或可得自唇形科植物的提取物;和
(i)得自或可得自豆科植物的提取物;和/或
(ii)得自或可得自苋科植物的提取物。
或
(a)得自或可得自千屈菜科植物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自苋科植物的提取物。
例如,得自或可得自千屈菜科植物的提取物。
在本发明的一个方面,食品稳定组合物可以包含至少一种植物来源的抑制剂,其包含得自或可得自如下的提取物、多种提取物或汁液:(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。
如本文所用,术语“稳定”是指相对于没有稳定组合物存在下发生的氧化量,在给定期限内减少、抑制或防止降解,尤其是减少、抑制或防止氧化。例如,“稳定组合物”可以通过螯合过渡金属例如cu2+和fe2+来减少、抑制或防止氧化,和/或可以提供自由基清除活性。
如本文所用,术语“谷物”是指因其可食用种子生长的单子叶植物或双子叶(eudicotyledonous)植物。如本文所用,谷物包括选自属于禾本科(familyofpoaceae)的稻属(oryza)、小麦属(triticum)及其组合的属的植物。例如,大米、小麦和玉米/甜玉米。
所有本文涉及的得自或可得自至少一种谷物的提取物典型地是指得自或可得自所述至少一种谷物的种子或汁液的提取物。例如,得自至少一种谷物的种子的外壳或得自所述至少一种谷物的完全去壳的种子的提取物。种子可以是发芽的或未发芽的。
如本文所用,术语“假谷物”是指因其可食用种子生长的的双子叶植物。如本文所用,假谷物包括选自蓼科(polygonaceae)、藜科(chenopodiceae)和大麻科(cannabaceae)及其组合的植物。例如,荞麦、藜麦(quinoa)、奇亚(chia)、苜蓿和大麻及其组合。
所有本文涉及的得自或可得自至少一种假谷物的提取物典型地是指得自或可得自所述至少一种假谷物的种子或汁液的提取物。例如,得自所述至少一种假谷物的种子的外壳的提取物。种子可以是发芽的或未发芽的。
得自至少一种谷物或假谷物的提取物可以得自如上述所定义的植物的干燥和/或研磨的部分。例如,来自谷物或假谷物的干燥和/或研磨的种子可以用于得到提取物。
所有本文涉及的得自或可得自豆科植物例如豌豆的提取物典型地是指得自或可得自豆科植物的果实、种子或汁液的提取物。例如,得自种子的提取物。种子可以是发芽的或未发芽的。
所有本文涉及的得自或可得自唇形科植物(例如迷迭香)的提取物典型地是指得自或可得自唇形科植物的叶子的提取物。唇形科提取物可以是已除臭和/或脱色的。例如,唇形科提取物可能已除去所有挥发油化合物。
所有本文涉及的得自或可得自金虎尾科植物例如针叶樱桃的提取物典型地是指得自或可得自植物的汁液的提取物。例如,得自植物的果实汁液的提取物。
所有本文涉及的得自或可得自苋科植物例如菠菜的提取物典型地是指得自或可得自植物的地上部分的提取物。例如,得自植物叶子或茎的提取物。
所有本文涉及的得自或可得自千屈菜科植物例如石榴的提取物典型地是指得自或可得自植物果实或种子的外皮、例如来自种子的外壳的提取物。例如,得自果实外皮的提取物。如果提取物得自种子,则该种子可以是发芽的或未发芽的。
在一些方面,仅使用水从相应的植物中提取所述至少一种植物来源的抑制剂。例如,可以仅使用水提取得自或可得自至少一种植物的所述至少一种植物来源的抑制剂,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,例如豆科、唇形科、苋科和千屈菜科及其组合,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。这种提取物可以称作水提取物。
在某些方面,用于提供提取物的水可以为酸性的。例如,用于提供提取物的水的ph可以为约1至约6或约2至约4,例如ph3。这种提取物可以称作酸性水提取物。
在其它方面,使用醇例如乙醇从相应的植物提取所述至少一种植物来源的抑制剂。例如,可以仅使用醇,例如仅使用乙醇提取得自或可得自至少一种植物的所述至少一种植物来源的抑制剂,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,例如豆科、唇形科、苋科和千屈菜科及其组合,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。这种提取物可以称作醇提取物,例如乙醇提取物。
在其它方面,使用醇和水例如乙醇和水的混合物从相应的植物提取所述至少一种植物来源的抑制剂。例如,可以使用醇和水例如乙醇和水的混合物提取得自或可得自至少一种植物的所述至少一种植物来源的抑制剂,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,例如豆科、唇形科、苋科和千屈菜科及其组合,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。这种提取物可以称作水-醇、例如水-乙醇提取物。
在其它方面,使用不为醇的有机溶剂例如丙酮从相应的植物提取所述至少一种植物来源的抑制剂。例如,可以使用有机溶剂例如丙酮提取得自或可得自至少一种植物的所述至少一种植物来源的抑制剂,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,例如豆科、唇形科、苋科和千屈菜科及其组合,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。这种提取物可以称作有机提取物或丙酮提取物。
典型地,当所述至少一种植物为谷物或假谷物时,所述至少一种植物来源的抑制剂可以提取自植物的种子,例如提取自植物的种子的外壳。当所述至少一种植物为豆科、唇形科、金虎尾科、苋科和千屈菜科植物时,所述至少一种植物来源的抑制剂可以提取自植物的叶子和/或果实和/或植物的种子,例如提取自植物的果实或种子。
因此,本发明提供了包含水、酸性水、水-醇、醇或有机植物来源的抑制剂的组合物,所述植物来源的抑制剂得自或可得自至少一种植物,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合,例如豆科、唇形科、苋科和千屈菜科及其组合,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自至少一种谷物的水、酸性水、水-醇、醇或有机提取物;和任选的(b)(i)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自千屈菜科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(iii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自至少一种假谷物的水、酸性水、水-醇、醇或有机提取物;和任选的(b)(i)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自千屈菜科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(iii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自豆科植物的水、酸性水、水-醇、醇或有机提取物;和任选的
(b)(i)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自千屈菜科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(iii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
例如,本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自豆科植物的水、酸性水、水-醇、醇或有机提取物;和任选的得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和任选的
(b)(i)得自或可得自金虎尾科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和
(b)(i)得自或可得自豆科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含:
(a)得自或可得自千屈菜科植物的水、酸性水、水-醇、醇或有机提取物;和任选的
(b)(i)得自或可得自唇形科植物的水、酸性水、水-醇、醇或有机提取物;和/或
(ii)得自或可得自苋科植物的水、酸性水、水-醇、醇或有机提取物。
例如,本发明的食品稳定组合物可以包含至少一种植物来源的抑制剂、由其组成或主要由其组成,其中所述至少一种植物来源的抑制剂包含得自或可得自千屈菜科植物的水、酸性水、水-醇、醇或有机提取物。
任选地,本发明的组合物可以包含以上定义的提取物组合和载体、由其组成或主要由其组成。
适合的载体包括惰性固体稀释剂或填充剂、无菌水溶液和各种有机溶剂。固体载体的实例为乳糖,石膏粉,蔗糖,环糊精,麦芽糖糊精,糊精,滑石粉,明胶,琼脂,果胶,金合欢胶(acacia),硬脂酸镁,氢氧化镁;硬脂酸,阿拉伯树胶(arabicgum),改性淀粉和纤维素的低级烷基醚,蔗糖,二氧化硅。液体载体的实例为糖浆,植物油,磷脂,脂肪酸,脂肪酸胺,聚氧乙烯和水。此外,载体或稀释剂可包括本领域已知的任何缓释材料,例如单独的或与蜡混合的单硬脂酸甘油酯或二硬脂酸甘油酯。
如本文所用,术语“载体”可以指天然产物或源自自然的产品,该产品已经过转化或修饰,因此与其所来源的天然产物不同。
优选的载体为麦芽糖糊精。
当我们使用“主要由......组成”或“基本上由......组成”时,是指所描述的组合物或提取物或汁液必须包含所列成分,并且还可能包含小量(例如至多2%重量或至多1%或至多0.1%或0.01%重量)的其它成分,前提是任何另外的成分均不影响所述组合物或提取物的基本特性。当我们使用“由……组成”时,我们是指所描述的组合物必须仅包含所列成分。这些术语可以类似的方式应用于过程、方法和用途中。
如本领域技术人员将理解的,如本文所用,术语“可得自”是指提取物可以得自植物或可以分离自植物,或者可以得自可替代来源,例如通过化学合成或酶促生产。而如本文所用,术语“得到”是指该提取物直接来源于植物来源。
如本文所用,术语“谷物”是指因其可食用种子生长的单子叶植物或双子叶植物。如本文所用,谷物包括属于禾本科的植物,包括选自稻属、小麦属及其组合的那些。例如,大米、小麦和玉米/甜玉米及其组合。
典型地,在本发明的组合物中,所述至少一种假谷物选自蓼科、藜科和大麻科。例如,荞麦、藜麦、奇亚、苜蓿和大麻及其组合。
典型地,在本发明的组合物中,所述至少一种唇形科植物典型地为迷迭香和/或所述至少一种千屈菜科植物典型地为石榴和/或所述至少一种苋科植物为菠菜。
典型地,在本发明的组合物中,所述至少一种金虎尾科植物为针叶樱桃。
典型地,在本发明的组合物中,所述至少一种豆科植物为豌豆。
本发明的食品稳定组合物可以包含至少一种植物来源的脂肪酸氧化抑制剂,其中所述至少一种植物来源的抑制剂为得自或可得自如下的一种提取物或多种提取物:
-大米;
-大米和迷迭香;
-大米和石榴;
-大米和菠菜;
-荞麦;
-荞麦和迷迭香;
-荞麦和石榴;
-荞麦和菠菜;
-藜麦;
-藜麦和迷迭香;
-藜麦和石榴;
-藜麦和菠菜;
-藜麦和荞麦;
-苜蓿;
-苜蓿和迷迭香;
-苜蓿和石榴;
-苜蓿和菠菜;
-大麻;
-大麻和迷迭香;
-大麻和石榴;
-大麻和菠菜;
-针叶樱桃;
-针叶樱桃和迷迭香;
-针叶樱桃和石榴;
-针叶樱桃和菠菜;
-针叶樱桃和豌豆;
-石榴;
-石榴和迷迭香;
-石榴和菠菜;
-石榴和豌豆;
-菠菜;
-菠菜和迷迭香;
-豌豆;
-豌豆和迷迭香;
-豌豆和菠菜。
优选地,本发明的食品稳定组合物可以包含至少一种植物来源的脂肪酸氧化抑制剂,其中所述至少一种植物来源的抑制剂为得自或可得自如下的一种提取物或多种提取物
-迷迭香和菠菜;
-迷迭香和豌豆;
-豌豆;或
-石榴。
为避免疑问,除非上下文另有指示,否则应将本发明的给定方面,特征或参数所指示的偏好、选项、特定特征等视为已与如针对本发明的相同或其它方面、特征和参数所指示的任何和所有其它偏好、选择、特定特征等组合公开。
得自或可得自所述至少一种谷物的提取物可以包含按提取物的重量计约0.1%至约10%的有机酸,例如约0.5%至约5%的有机酸。典型地,有机酸可以为植酸,其可以以按提取物的重量计约0.5%至约5%的量存在。
得自或可得自所述至少一种假谷物的提取物可以包含按提取物的重量计至少约0.1%的多酚化合物(由folinciocalteu测定)。例如,按提取物的重量计约0.1%至约30%或约0.5%至约20%或约1%至约10%的多酚化合物,和/或得自或可得自所述至少一种假谷物的提取物可以包含按提取物的重量计小于约5%的柠檬酸。例如,按提取物的重量计约0.01%至约5%或约1%至约3%的柠檬酸。
其它化合物也可以存在于得自或可得自所述至少一种假谷物的提取物中。可能存在的其它化合物包括、但不限于草酸、植酸、类黄酮、皂苷、原花色素(proanthcyanidins)(pac)和黄烷-3-醇。
例如,包含得自或可得自至少一种假谷物的提取物的组合物可以包含按提取物的重量计约0.01%至约5%的草酸、约0.1%至约5%的柠檬酸、约0.1%至约10%的多酚、约0.01%至约1%的类黄酮、约0.1%至约5%的pac。
得自或可得自唇形科植物的提取物可以包含按提取物的重量计至少1%的量的酚二萜。例如,得自或可得自唇形科植物的提取物可以包含约1%至约95%重量、例如约2.5%至约90%重量、约5%至约85%重量、约10%至约80%重量、约15%至约60%重量、约20%至约50%重量、约25%至约40%重量、例如约1%至约30%重量、约5%至约20%重量、约10%至约15%重量或约1%至约5%重量的量的酚二萜。
得自或可得自唇形科植物的提取物可以为酚二萜,例如鼠尾草酸(carnosicacid)。例如,得自或可得自唇形科植物的提取物可以包含按提取物的重量计至少1%的量的鼠尾草酸。例如,得自或可得自唇形科植物的提取物可以包含按提取物的重量计约1%至约95%重量、例如约2.5%至约90%重量、约5%至约85%重量、约10%至约80%重量、约15%至约60%重量、约20%至约50%重量、约25%至约40%重量、例如约1%至约30%重量、约5%至约20%重量、约10%至约15%重量、或约1%至约5%重量、例如约15%至约30%或约40%至约65%的量的鼠尾草酸。
当所述至少一种植物来源的抑制剂与载体合并时,组分的相对比例由此将减少。例如,在一些方面,鼠尾草酸的量可以为提取物重量的约1%至约10%、例如约2%至约6%或5%。
得自或可得自唇形科植物的提取物还可以包含鼠尾草酚和12-o-甲基鼠尾草酸。例如,得自或可得自唇形科植物的提取物可以包含或含有约15%至约30%重量的鼠尾草酸和约1%至约3%重量的鼠尾草酚,或得自或可得自唇形科植物的提取物可以包含或含有约40%至约65%重量的鼠尾草酸、约2%至约10%的鼠尾草酚和约2%至约10%重量的12-o-甲基鼠尾草酸。
得自或可得自苋科植物例如菠菜的提取物可以包含按提取物的重量计至少约0.1%的多酚化合物(由folinciocalteu测定)。例如,按提取物的重量计约0.1%至约20%或约0.5%至约10%多酚化合物,和/或得自或可得自苋科植物的提取物可以包含按提取物的重量计小于约5%的柠檬酸。例如,按提取物的重量计约0.01%至约5%或约1%至约3%的柠檬酸。
其它化合物也可以存在于得自或可得自苋科植物的提取物中。可能存在的其它化合物包括、但不限于草酸、植酸、蛋白质和糖。
例如,包含得自或可得自苋科植物的提取物的组合物可以包含按提取物的重量计约0.01%至约10%的草酸、约0.1%至约5%的柠檬酸、约0.1%至约10%的多酚、约1%至约25%的蛋白质(通过kjeldahl方法测定)和约5%至约35%的糖(通过ridcq-mo-286与离子型比较测得)。
得自或可得自豆科植物例如豌豆的提取物可以包含按提取物的重量计至少约0.1%的多酚化合物(由folinciocalteu测定)。例如,按提取物的重量计约0.1%至约10%或约0.2%至约5%的多酚化合物,和/或得自或可得自豆科植物的提取物可以包含按提取物的重量计小于约10%的柠檬酸。例如,按提取物的重量计约0.01%至约10%或约1%至约8%的柠檬酸。
其它化合物也可以存在于得自或可得自豆科植物的提取物中。可能存在的其它化合物包括、但不限于植酸、蛋白质和糖。
例如,包含得自或可得自豆科植物的提取物的组合物可以包含按提取物的重量计约0.1%至约10%的柠檬酸、约0.1%至约5%的多酚、约1%至约15%的蛋白质(通过kjeldahl方法测定)和约10%至约60%的糖(通过ridcq-mo-286与离子型比较测得)。
得自或可得自千屈菜科植物例如石榴的提取物可以包含鞣花酸和安石榴苷(punicalagin)。鞣花酸的量可以为提取物重量的约0.5%至约20%,例如提取物重量的约1%至约15%。安石榴苷的量可以为提取物重量的约0.5%至约15%。例如提取物重量的约1%至约10%。根据所述提取物是固体还是液体形式的不同,鞣花酸和安石榴苷的量可能不同。在液体形式中,鞣花酸的量可以为提取物重量的约5%至约15%,而安石榴苷的量可以为提取物重量的约2.5%至约10%。在固体形式例如粉末中,鞣花酸的量可以为提取物重量的约0.5%至约5%,而安石榴苷的量可以为提取物重量的约0.5%至约10%。
得自或可得自金虎尾科植物例如针叶樱桃的提取物可以包含抗坏血酸。抗坏血酸的量可以为提取物重量的约5%至约50%。当提取物得自或可得自干燥的汁液时,该提取物可以包含按提取物的重量计约15%至约35%的抗坏血酸。
除非本文另有说明,否则所列的重量百分比基于提取物的总重,例如干燥提取物的总重。
如本文所用,例如,术语“约”在涉及可测量的数值(例如组合物或反应混合物中特定组分的重量)时是指指定量的±20%、±10%、±5%、±1%、±0.5%或特别是±0.1%的变化。
在本发明的食品稳定组合物中,其中所述至少一种植物来源的抑制剂为一种以上的植物提取物、汁液或产品例如两种不同的植物提取物的组合,两种提取物的重量百分比之比(weightpercentageratio)可以为约1:99至约99:1,例如约50:1至约1:50,或约25:1至约1:25,或约5:1至约1:5,例如1:1。
例如,在本发明的食品稳定组合物中,所述至少一种植物来源的抑制剂可以为得自或可得自两种不同植物的提取物、汁液或产品的组合,所述两种不同植物选自豆科、唇形科、苋科和千屈菜科,其中每种提取物、汁液或产品的重量比可以为约1:99至约99:1,例如约50:1至约1:50,或约25:1至约1:25,或约5:1至约1:5,例如1:1。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂为得自或可得自至少一种假谷物的提取物和得自或可得自唇形科植物的提取物,两种提取物的重量百分比之比可以为约10:1至约1:10,例如约5:1至约1:5。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂为得自或可得自金虎尾科植物的干燥的汁液和得自或可得自唇形科植物的提取物,两种提取物的重量百分比之比可以为约5:1至约1:5,例如约2.5:1至约1:2.5。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂为得自或可得自豆科植物的提取物和得自或可得自唇形科植物的提取物,两种提取物的重量百分比之比可以为约5:1至约1:5,例如约2.5:1至约1:2.5或1:1。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂为得自或可得自千屈菜科植物的提取物和得自或可得自唇形科植物的提取物,两种提取物的重量百分比之比可以为约30:1至约1:30,例如约20:1至约1:20。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂为得自或可得自苋科植物的提取物和得自或可得自唇形科植物的提取物,两种提取物的重量百分比之比可以为约10:1至约1:10,例如约5:1至约1:5。
在本发明的食品稳定组合物中,其中所述植物来源的抑制剂得自或可得自苋科植物的提取物和得自或可得自千屈菜科植物的提取物,两种提取物的重量百分比之比可以为约30:1至约1:30,例如约20:1至约1:20。
本发明的食品稳定组合物可以用于抑制或防止多不饱和脂肪酸(pufa)油转化为2,4-庚二烯醛和/或2,4-癸二烯醛。例如,在50℃加速老化15或20天后,本发明的组合物可以在食品例如蛋黄酱中抑制2,4-庚二烯醛的形成至小于15,000ppb,例如,小于10,000ppb。
本领域技术人员将理解,本发明的组合物可以典型地以固体形式提供,但是也可以以液体形式提供,这取决于植物的类型或用于获得提取物的提取方法的类型。所谓固体形式应包括该组合物可以以粉末、无定形固体或作为结晶或部分结晶固体的形式提供。
干燥的提取物可以与液体载体混合,然后使用。
如上所述,本发明的食品稳定组合物可以包含载体,例如麦芽糖糊精。典型地,如果载体存在于本发明的组合物中,则载体可以以组合物或提取物重量的约1%至约50%、例如约10%至约30%或25%的量存在。
用于得到稳定组合物的方法
包含至少一种植物来源的脂肪酸氧化抑制剂的本发明的食品稳定组合物可以通过如本文一般性描述的或其常规改进的提取、汁液表达(juiceexpression)和分离方法得到或可通过上述方法得到。
包含至少一种植物来源的脂肪酸氧化抑制剂的本发明的食品稳定组合物可以通过一种方法得到或可通过该方法得到,该方法包括下列步骤:
(i)使选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合的至少一种植物(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴)的至少部分与溶剂接触,即用溶剂研磨相应植物的完整种子或种子的外壳或研磨植物自身,例如植物的叶子和/或茎;和
(ii)除去溶剂。
任选地,可以将植物研磨,然后使其与溶剂接触。
其中,所述至少一种植物来源的抑制剂得自干燥的汁液,所述干燥的汁液得自浓缩的果实汁液。例如,补充了碳酸盐和/或不同盐的羟基化合物的浓缩的果实汁液。
例如,包含至少一种植物来源的脂肪酸氧化抑制剂的本发明的食品稳定组合物还可以通过一种方法得到或可通过该方法得到,所述方法包括下列步骤:
a.压碎所述至少一种植物或所述至少一种植物的果实,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科或其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴),得到汁液;和
b.在碳酸盐/和或羟基化合物及其相应盐的存在下从汁液中蒸发液体或对汁液进行浓缩。
典型地,该方法可以用于提供本发明的食品稳定组合物,所述食品稳定组合物包含至少一种植物来源的抑制剂,该抑制剂得自或可得自至少一种金虎尾科植物例如针叶樱桃的果实。
应当理解,如果本发明的稳定组合物包含来自两种或更多种如先前定义的植物种类的提取物,则可以使用上述方法一起制备提取物,或者可以分别使用上述方法独立地制备提取物,然后与任何其它任选的成分例如载体(即麦芽糖糊精)以所需比例组合使用,形成本发明的食品稳定组合物。
因此,本发明的方法包括任选地合并得到的提取物与另一种提取物的步骤。
当在步骤(i)之前研磨至少一种植物时,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴),可以将植物例如植物的种子、外皮或外壳或种子研磨成具有约0.1mm至约20mm,例如约0.5mm至约10mm,或约1mm至5mm,例如2mm粒度的颗粒。任选地,在研磨前可以干燥植物。可以使用本领域公知的方法进行研磨,例如研磨(milling)或使用研钵和研杵。
可以在步骤(i)中使用的溶剂包括醇(例如甲醇和乙醇)、水(包括已经酸化的水)、醇/水混合物(例如乙醇和水的混合物)和丙酮。例如,提取溶剂可以为丙酮、水、酸化水、水-醇混合物(水中约1%至约99%的醇,例如水中约10%至约50%的醇,例如水中约30%的醇)或醇。可以举出的具体的醇包括甲醇和乙醇。
典型地,在本发明的方法中,水(存在时)为酸性ph。例如,水为约1至约5的ph,例如约ph3。可以通过本领域已知的技术酸化水。例如,可以用20%硝酸、磷酸或柠檬酸酸化水。
典型地,在本发明的方法中,当本发明的稳定组合物包含得自或可得自唇形科植物的提取物时,提取溶剂为丙酮。
典型地,在本发明的方法中,当本发明的稳定组合物包含得自或可得自千屈菜科植物的提取物时,提取溶剂为乙醇或含水乙醇。
典型地,在本发明的方法中,当本发明的稳定组合物包含得自或可得自金虎尾科植物的提取物时,提取物通过从植物(例如从果实)得到汁液并且从汁液中除去液体或任选地在碳酸盐或羟基化合物存在下干燥来提供。
典型地,在本发明的方法中,当本发明的稳定组合物包含得自或可得自苋科植物的提取物时,提取溶剂为酸性水。
典型地,在本发明的方法中,当本发明的稳定组合物包含得自或可得自至少一种谷物或假谷物的提取物时,提取溶剂为水、酸性水、乙醇或水-乙醇溶剂。
步骤(ii)可以在约20℃至约200℃范围内的温度下进行。例如,步骤(ii)的温度可以在约40℃至约100℃范围内,例如50℃、55℃、60℃、65℃或70℃。
可替代地,步骤(ii)可以在溶剂回流的温度下进行。
可以使用任何适合的提取装置。例如,可以使用索氏提取器提取所述至少一种植物,其选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴)。
典型地,用于提取方法的植物材料与溶剂混合物之比在约1:1至约1:10之间改变,以克-毫升为基础,例如约1:3至约1:8。例如,可以使用10m比例。
典型地,温育期(即植物材料与溶剂接触(步骤(ii)和(v))的期限)为约2小时至约24小时。任何未溶解的植物材料可以例如通过过滤从溶剂中除去,并重新溶解在溶剂中。然后可以重复温育期。
在将植物材料和溶剂在步骤(ii)中温育后,将溶剂与任何未溶解的植物材料分离,并将提取的组合物浓缩(即除去溶剂),直到提取组合物具有固体组分。例如,直到所有溶剂都被除去,只剩下固体提取物。
步骤b中使用类似的过程,其中将汁液从固体植物原料中分离出来,然后浓缩(即除去汁液中的液体),直到有了固体组分。例如,仅保留固体提取物。
典型地,在本发明的方法中,除去至少50%、例如60%、70%、80%、90%、95%或100%的溶剂和/或液体。
典型地,在得到本发明的食品稳定组合物的方法(即如上文所述的步骤(i)-(iii))中:将所述至少一种植物研磨成具有约0.1mm至30mm直径的颗粒,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴);与溶剂(水,约ph3的水,70%的约ph3的水在/30%乙醇96°或丙酮)接触,并且在约20℃至约100℃的温度下温育约2小时至约24小时;然后除去溶剂,得到固体提取物。
例如,本发明的食品稳定组合物可以通过如下方法得到或可通过如下方法得到:
-将所述至少一种植物研磨成约2mm的颗粒,所述至少一种植物选自谷物、假谷物、豆科、唇形科、金虎尾科、苋科和千屈菜科及其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴);
-使研磨的颗粒与溶剂(水、酸性ph的水、70%水30%乙醇96°、无水乙醇或丙酮)接触;
-将任何未溶解的材料从溶剂中过滤并重新溶解在溶剂(水、酸性ph的水、70%水30%乙醇96°、无水乙醇或丙酮)中;
-将任何未溶解的材料从溶剂中过滤,并合并两种溶剂级分,并且蒸发溶剂;
-然后将干燥固体研磨以形成细颗粒固体。
如前所述,如果本发明的稳定组合物包含来自两种或更多种如前所定义的植物种类的提取物,则该提取物可以使用上述方法一起制备,或者可以各自使用上述方法独立地制备,然后再以所需比例与任何另外的任选成分例如载体(即麦芽糖糊精)合并,形成本发明的食品稳定组合物。
例如,所述至少一种谷物或所述至少一种假谷物或所述至少一种豆科植物或所述至少一种唇形科植物或所述至少一种金虎尾科植物或所述至少一种苋科植物或所述至少一种千屈菜科植物可以分别提取,然后合并,得到本发明的稳定组合物。
在提取过程完成后,可以使用色谱方法纯化该提取物(如果需要)。
得自这类方法的提取物可以基本上不含其它植物材料(例如不含植物纤维素)。
如本文所用,所涉及的“基本上”不含另一种材料的材料可以指包含小于1%重量(例如小于0.1%,例如小于0.01%或小于0.001%重量)另一种材料的材料。
如本文所述的本发明的组合物可以包含得自(或可得自)如本文所述的方法的一种提取物或多种提取物。
应用
本发明的食品稳定组合物可以用于需要氧化、抑制或防止氧化的任何应用中。
已经发现本发明的组合物在食品、营养和健康基质/产品或化妆品基质/产品中的用途是特别有利的。
通过相对于在没有稳定组合物存在下氧化过程中会发生的氧化的量在给定期限内减少、抑制或防止氧化量,本发明的组合物可以稳定易发生氧化变性的食品、营养和健康基质/产品或化妆品基质/产品。
因此,根据本发明,提供了稳定食品、营养和健康基质/产品或化妆品基质/产品的方法,其中该方法包括使食品与本文所述的食品稳定组合物接触的步骤。在上下文中,“接触”包括将本发明的组合物掺入食品中。
还提供了本文所定义的食品稳定组合物在稳定食品、营养和健康基质/产品或化妆品基质/产品中的用途。
“稳定食品、营养和健康基质/产品或化妆品基质/产品”包括减少、抑制或防止食品、营养和健康基质/产品或化妆品基质/产品的氧化。例如,稳定食品可能意味着可以通过螯合过渡金属例如cu2+和fe2+和/或提供自由基清除活性来减少、抑制或防止食品的氧化。
本发明的食品稳定组合物可以用于抑制或防止多不饱和脂肪酸(pufa)油转化为2,4-庚二烯醛和/或2,4-癸二烯醛。例如,在50℃下加速老化15或20天后,本发明的组合物可以在食品例如蛋黄酱中抑制2,4-庚二烯醛的形成至小于15,000ppb,例如,小于10,000ppb。
本发明的组合物特别适用于食品,其包含水包油型乳状液或为水包油型乳状液,例如基于鸡蛋和油的调味品,例如蛋黄酱、荷兰酱(hollandaise)或贝亚恩酱(béarnaise)。
典型地,所述食品基本上不含任何edta。例如,所述食品可以包含小于约5%edta或小于约2.5%edta或小于约75ppmedta或不含edta。
食品
本发明进一步提供了包含本文所定义的食品稳定组合物的食品。
本发明的组合适用于广泛的食品。这类食品包括、但不限于生肉,熟肉,生禽产品,熟禽产品,生海鲜产品,熟海鲜产品,即食餐,烹调酱,例如意大利面酱和番茄酱,调味酱,巴氏消毒和非巴氏消毒汤,沙拉酱和其它水包油型乳状液,例如蛋黄酱,油包水型乳状液,乳制品,烘焙食品,糖食产品,水果产品和具有脂肪基或含水馅的食品(foodswithfatbasedorwatercontainingfilings)。优选地,食品包含水包油型乳状液或为水包油型乳状液。例如,食品可以为调味酱,例如基于鸡蛋和油的调味品,例如蛋黄酱、荷兰酱或贝亚恩酱,或包含调味酱的食品,例如基于鸡蛋和油的调味品,例如蛋黄酱、荷兰酱或贝亚恩酱。
典型地,所述食品基本上不含任何edta。例如,所述食品可以含有不小于约5%的edta或小于约2.5%的edta或不含edta。
食品典型地包含本发明的组合物,其用量足以稳定该食品,例如,减少、抑制或防止氧化。典型地,稳定组合物以按食品的重量计约0.01%至约10%的量存在于食品中。例如约0.025%至约5%或约0.05%至约2.5%。例如,本发明的组合物可以以约5ppm至约20pmm、例如约10ppm的量存在于食品中。
本发明提供了用于稳定食品的试剂盒(kit)。所述试剂盒包含:
得自或可得自至少一种植物的提取物,所述至少一种植物选自谷物、假谷物、豆科、唇形科和金虎尾科、苋科和千屈菜科或其组合(例如豆科、唇形科、苋科和千屈菜科及其组合和混合物,即(i)迷迭香和菠菜;(ii)迷迭香和豌豆;(iii)豌豆;或(iv)石榴。)。
例如,所述试剂盒可以包含:
(a)得自或可得自至少一种谷物的提取物;和任选的(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物,
或
(a)得自或可得自至少一种假谷物的提取物;和任选的
(b)得自或可得自唇形科植物的提取物;和/或
(c)得自或可得自千屈菜科植物的提取物,
或
(a)得自或可得自豆科植物的提取物;和任选的
(b)(i)得自或可得自唇形科植物的提取物;和/或
(ii)得自或可得自千屈菜科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物。
例如,得自或可得自豆科植物的提取物;和任选的得自或可得自唇形科植物的提取物,
或
(a)得自或可得自唇形科植物的提取物;和任选的
(b)(i)得自或可得自金虎尾科植物的提取物;和/或
(iii)得自或可得自苋科植物的提取物。
例如,得自或可得自唇形科植物的提取物;和得自或可得自豆科植物的提取物或汁液;和/或得自或可得自苋科植物的提取物,
或
(a)得自或可得自千屈菜科植物的提取物;和任选的
(b)得自或可得自唇形科植物的提取物。
例如,得自或可得自千屈菜科植物的提取物。
在所述试剂盒中,提取物(a)和任选地(b)和/或(c)可以在相同或单独的容器中提供,任选地还有用于混合和/或接触和/或使用的说明书。
当将本发明的食品稳定组合物掺入食品,例如基于鸡蛋和油的调味品,例如蛋黄酱、荷兰酱或贝亚恩酱中,并且相对于在没有稳定组合物存在下发生的氧化的量通过在给定期限内减少、抑制或防止氧化的量来提供稳定作用时,本发明的组合物不应对其所掺入的食品的颜色产生不良影响。
因此,本发明的目的在于提供一种稳定组合物,该稳定组合物实现了期望的稳定作用,并且还可以掺入食品,例如基于鸡蛋和油的调味品,例如蛋黄酱、荷兰酱或贝亚恩酱,其中在食品颜色或口味上没有可辨认的或最小的改变,而这种改变对于消费者而言是无法接受的。
食品的制备
(i)本发明提供了制备水包油型乳状液食品的方法,所述食品包含本发明的食品稳定组合物,该方法包括下列步骤:混合第一水相,任选地与本发明的食品稳定组合物一起混合;
(ii)将油添加到步骤(i)中得到的产品中,任选地与本发明的食品稳定组合物一起添加;和
(iii)将至少一种另外的水相添加到步骤(ii)中得到的产品中。
典型地,第一水相可以包含水和蛋黄。
典型地,所述至少一种另外的水相可以包含醋。
典型地,如果在步骤(i)中添加本发明的食品稳定组合物,则在步骤(ii)中不添加本发明的食品稳定组合物,且反之亦然。然而,在某些方面,可以在步骤(i)和(ii)中均添加本发明的食品稳定组合物。
例如,水包油型乳状液,例如蛋黄酱可以通过下列步骤制备:
(a)彼此混合水、蛋黄、山梨酸盐和本发明的食品稳定组合物(其可以预先溶于水);
(b)将水相添加至如下混合物中:(cemtex12688+lygommekct58)/油,比例为1/3,并且混合1分钟,直至它变成粘性的;
(c)在剧烈搅拌下将油缓慢地添加至水相,并且在添加2/3的油时,添加醋和盐,然后添加其余的油并且混合1分钟;
(d)给43ml玻璃罐填充10g水包油型乳状液(蛋黄酱)。
附图简述
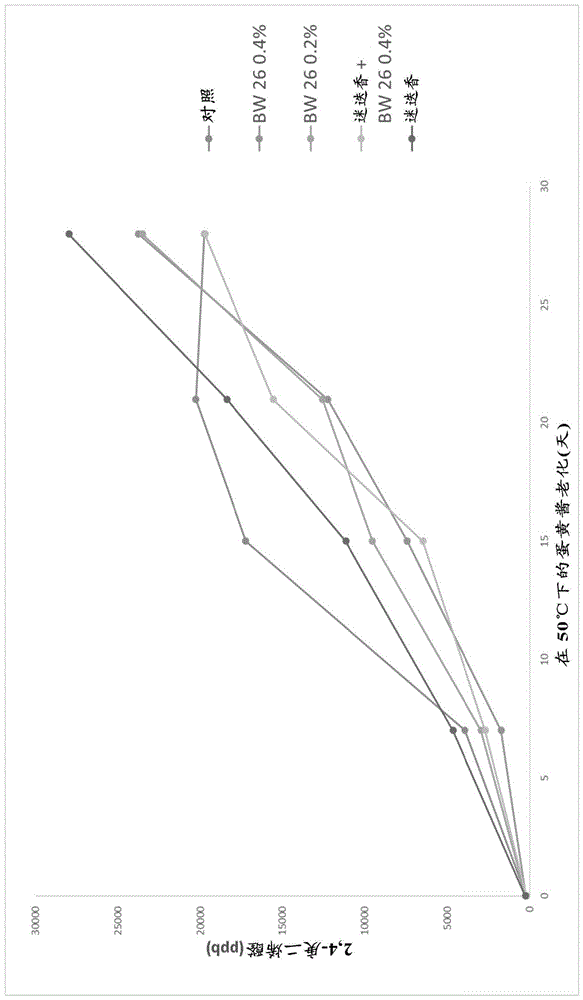
图1描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例1中制备的蛋黄酱的氧化稳定性。
图2描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例2中制备的蛋黄酱的氧化稳定性。
图3描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例3中制备的蛋黄酱的氧化稳定性。
图4描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例4中制备的蛋黄酱的氧化稳定性。
图5描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例5中制备的蛋黄酱的氧化稳定性。
图6描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例6中制备的蛋黄酱的氧化稳定性。
图7描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例7中制备的蛋黄酱的氧化稳定性。
图8描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例8中制备的蛋黄酱的氧化稳定性。
图9描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例9中制备的蛋黄酱的氧化稳定性。
图10描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例10中制备的蛋黄酱的氧化稳定性。
图11描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例11中制备的蛋黄酱的氧化稳定性。
图12描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的实施例12中制备的蛋黄酱的氧化稳定性。
图13描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.035%迷迭香提取物和0.05%针叶樱桃提取物的蛋黄酱的氧化稳定性。
图14描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.4%荞麦25d提取物和1%迷迭香(mpg/p80)提取物的蛋黄酱的氧化稳定性。
图15描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含1%荞麦提取物的蛋黄酱的氧化稳定性。
图16描绘了在室温下在60天老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.047%迷迭香提取物和0.066%豌豆提取物的蛋黄酱的氧化稳定性。
图17描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含的蛋黄酱的氧化稳定性1%迷迭香提取物和1%豌豆提取物。
图18描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.06%豌豆提取物的蛋黄酱的氧化稳定性。
图19描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含1%迷迭香(mpg/p80)提取物和0.05%石榴提取物的蛋黄酱的氧化稳定性。
图20描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.05%石榴提取物和1%菠菜提取物的蛋黄酱的氧化稳定性。
图21描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.05%石榴提取物的蛋黄酱的氧化稳定性。
图22描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含1%迷迭香(mpg/p80)提取物和1%藜麦提取物的蛋黄酱的氧化稳定性。
图23描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含1%藜麦提取物的蛋黄酱的氧化稳定性。
图24描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含1%大米外壳提取物的蛋黄酱的氧化稳定性。
图25描绘了在室温下在60天老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.124%菠菜提取物和0.047%迷迭香提取物的蛋黄酱的氧化稳定性。
图26描绘了在50天加速老化测试中通过测定2,4-庚二烯醛(ppb)的形成得到的包含0.124%菠菜提取物和0.035%迷迭香提取物的蛋黄酱的氧化稳定性。
图27描绘了奇亚提取物和藜麦之间的协同螯合作用。
图28描绘了在植物提取物的各种组合之间看到的协同螯合作用。
实施例
参照以下非限制性实施例进一步描述本发明。
通用方法
使用菲洛嗪(ferrozine)测试和光谱法的螯合活性的体外筛选
试剂的制备
1)ph4.5的缓冲溶液
在1l烧瓶中将乙酸溶液(250ml,0.1m)缓慢地添加到乙酸钠溶液(500ml,0.1m)中,直至ph达到4.5。
2)0.4mm/l的fecl2溶液
将fecl2,4h2o(75.5mg)置于100ml容量瓶中。将足量的蒸馏水添加到烧瓶中,使得蒸馏水的水平达到100ml刻度。然后使用该溶液制备1/10的稀释液。
3)0.5mm/l的菲洛嗪
将菲洛嗪(246.3mg)置于100ml容量瓶中。将足量的蒸馏水添加到烧瓶中,使得蒸馏水的水平达到100ml刻度。然后使用该溶液制备1/10的稀释液。
样品的制备
将植物材料提取物(120mg)放入20ml的容量瓶中。然后将缓冲溶液(6ml,ph4.5)添加到烧瓶中。然后将小瓶放入超声浴中以使溶液均化。
然后将所得溶液(smother)用于制备以下样品:
1)1.125mlsmother+0.375mlph4.5的缓冲溶液,得到15mg/ml溶液;
2)0.75mlsmother+0.75mlph4.5的缓冲溶液,得到10mg/ml溶液;
3)0.375mlsmother+1.125mlph4.5的缓冲溶液,得到5mg/ml溶液;
4)0.187mlsmother+1.310mlph4.5的缓冲溶液,得到2.5mg/ml溶液;
5)0.094mlsmother+1.406mlph4.5的缓冲溶液,得到1.25mg/ml溶液;
制备每种浓度的两个样品,总计十个样品。
每种浓度的样品之一用作空白。通过取1.5ml样品并加入0.15mlfecl2和0.3mlph4.5的缓冲溶液来制备每种空白。
每种浓度的剩余样品用作测试样品。通过取0.5ml样品并添加0.15mlfecl2和0.3ml菲洛嗪来制备测试样品。
通过将0.5mlph4.5的缓冲溶液添加到0.15mlfecl2和0.3ml菲洛嗪中制备对照品。
使用分光光度计shimadzu1700uvprobe的分光光度分析
25分钟后,将每个样品离心2分钟30秒。然后滗析液体并确定液体的吸光度。
数据处理
结合的feii(即螯合的%fe)的百分比如下计算:
螯合的%fe=(对照品的吸光度-样品的吸光度-空白的吸光度)/对照品的吸光度)x100
然后绘制浓度对螯合的%fe(ii)的回归曲线,以能够确定回归斜率。
使用与hptlc指纹结合的dpph方法的体外自由基清除活性分析
样品的制备
将植物材料提取物溶于水中直至浓度达到20mg/ml。然后将该溶液在65℃加热,使用4.5μm过滤器过滤,然后将4μl提取物溶液置于hptlc机器(camagautomatictlcsampler4ats4)中的平板上。
用1-丁醇:水:甲酸(8:3:2)使植物材料提取物迁移穿过平板,然后用在甲醇中稀释的dpph溶液(0.05%)显示。
数据处理
用密度仪观察迁移的结果,以便以负信号模式定量在518nm处的提取物的dpph清除(通过减少(remission)和模式荧光的lampd2&w/measurement类型)。
然后通过camag可视化仪获取平板的图像。
通过将相应的标准分子负载在平板上来研究典型植物抗氧化剂的存在。
然后用密度仪通过绘制rf值与吸光度的关系图获得色谱图。
然后计算相对于每种提取物的活性值的所有峰的面积的总和,得到总自由基清除活性。
实施例1-荞麦提取物26(bw26)
提取物的制备
将荞麦外壳研磨成约2mm的颗粒。然后在65℃下用ph3的70%水(用20%的硝酸酸化)/30%乙醇96°的混合物将研磨的样品提取2次,历时2小时,其代表了大规模工厂的10m比例。然后将该混合物过滤。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表1中所示。
表1:对bw26的菲洛嗪和dpph测试结果
正如可以从表1中看到的,bw26对菲洛嗪测试的反应为阳性螯合活性,其中斜率为11且1%时螯合的%fe(ii)等于81.8%。bw26的自由基清除活性也为阳性,面积为42803.9。
荞麦外壳也使用相同的方法提取,但只用自来水。该提取物具有的斜率为11且1%时螯合的%fe(ii)等于83%。因此,它具有与bw26相同的螯合活性。
使用自来水的提取物的自由基清除活性也为阳性,面积为18597。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将bw26提取物与相i混合。将水相ii(0.2%(w/w)的lygommekct58(包含三种类型的淀粉、胶凝剂、半乳甘露聚糖(e410,e412,e417)和卡拉胶(e407))、0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋(spiritvinegar)和0.5%(w/w)的盐),然后将剩余的油倾入混合物中。
使用上述技术制备了五种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.4%重量的bw26提取物的蛋黄酱;
3)包含0.2%重量的bw26提取物的蛋黄酱;
4)包含0.4%重量的bw26和迷迭香提取物的蛋黄酱;和
5)包含1%迷迭香提取物的蛋黄酱。
每种蛋黄酱在50℃的烘箱中经过5周加速老化。每周使用偶联至gc/ms的hs-spme对每种蛋黄酱测试挥发性化合物的形成。该过程由将样品放入小瓶中、然后用隔片型盖或miniert阀将其密封组成。然后将spme针刺穿隔片,并且将一根纤维穿过该针伸入样品中。然后允许在样品基质与固定相之间进行分配。达到平衡时,样品中的分析物就会吸收到纤维上。然后将纤维转移到气相色谱仪的进样口,在此使分析物热解吸。
通过测定2,4-庚二烯醛(ppb)评价蛋黄酱的氧化稳定性,且结果如图1中所示。
正如可以从图1中看到的,当蛋黄酱包含bw26提取物时,减少形成2,4-庚二烯醛25天。
颜色
该提取物具有dl(1%)=-65
由于dl为-65,所以bw26将蛋黄酱着色为具有浅灰色。
实施例2-荞麦蛋黄酱(mayo)1(bw蛋黄酱1)
提取物的制备
将荞麦外壳研磨成约2mm的颗粒。然后用ph3的水(用20%的硝酸酸化)将研磨的样品在回流下提取2次,历时2小时,其代表了大规模工厂的10m比例。然后过滤该混合物。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到研磨的bw蛋黄酱1提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表2中所示。
表2:对bw蛋黄酱1的菲洛嗪和dpph测试结果
正如可以从表2中看到的,bw蛋黄酱1对菲洛嗪测试的反应为螯合活性阳性,斜率为13且1%时螯合的%fe(ii)等于83.2%。bw蛋黄酱1的自由基清除活性也为阳性,面积为20099。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将bw蛋黄酱1提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
使用上述技术制备了四种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.4%重量的bw蛋黄酱1提取物的蛋黄酱;
3)包含0.2%重量的bw蛋黄酱1提取物的蛋黄酱;和
4)包含1%重量的bw蛋黄酱1提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图2中所示。
正如可以从图2中看出的,bw蛋黄酱1在加速老化的整个过程中都会减少蛋黄酱的氧化。当以1%重量包括在蛋黄酱中时,在50℃加速老化28天后2,4-庚二烯醛的比例不超过5000ppb。
颜色
该提取物具有dl(1%)=-74.76
由于dl为-74.76,所以bw蛋黄酱1将蛋黄酱着色为具有灰褐色。
实施例3-荞麦25d(bw25d)
提取物的制备
将荞麦外壳研磨成约2mm的颗粒。然后用70%的ph3的水(用20%硝酸酸化)/30%乙醇96°的混合物将研磨的样品在65℃提取2次,历时2小时,其代表了大规模工厂的10m比例。然后过滤该混合物。然后将该混合物用木炭脱色。将脱色的液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到研磨的荞麦25d提取物(bw25d)。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表3中所示。
表3:对bw25d的菲洛嗪和dpph测试结果
正如可以从表3中看到的,bw25d对菲洛嗪测试的反应为螯合活性阳性,斜率为17且1%时螯合的%fe(ii)等于85.5%。bw25d的自由基清除活性也为阳性,面积为9336。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将bw25d提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
使用上述技术制备了五种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.4%重量的bw25d提取物的蛋黄酱;
3)包含0.2%重量的bw25d提取物的蛋黄酱;
4)包含0.4%重量的bw25d和0.5%重量的迷迭香提取物的蛋黄酱;和
5)包含0.5%重量的迷迭香提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图3中所示。
正如可以从图3中看到的,包含0.5%鼠尾草酸和鼠尾草酚(osr0.5)+bw25d0.4%的1%迷迭香提取物与0.4%和0.2%剂量的bw25d的两种组合都防止了蛋黄酱氧化。有趣的是,迷迭香本身并没有显著减少氧化。
颜色
该提取物具有dl(1%)=-35
由于dl为-35,所以bw25d将蛋黄酱着色为具有浅灰色,但对蛋黄酱的着色低于bw26。
实施例4-藜麦c
提取物的制备
将藜麦c外壳研磨成约2mm的颗粒。然后用70%的ph3的水(用20%硝酸酸化)/30%乙醇96°的混合物将研磨的样品提取2次,其代表了大规模工厂的10m比例。然后过滤该混合物。然后将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到研磨的藜麦c提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表4中所示。
表4:对藜麦c的菲洛嗪和dpph测试结果
正如可以从表4中看到的,藜麦c对菲洛嗪测试的反应为螯合活性阳性,斜率为10且1%时螯合的%fe(ii)等于77.7%。藜麦c的自由基清除活性也为阳性,面积为7320。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将藜麦c提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
使用上述技术制备了五种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.4%重量的藜麦c提取物的蛋黄酱;
3)包含0.2%重量的藜麦c提取物的蛋黄酱;
4)包含0.4%重量的藜麦c和0.5%重量的迷迭香提取物的蛋黄酱;和
5)包含0.5%重量的迷迭香提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图4中所示。
颜色
该提取物具有dl(1%)=-11
该提取物不影响蛋黄酱的颜色。
实施例5-藜麦a
提取物的制备
将藜麦a外壳研磨成约2mm的颗粒。然后用70%的ph3的水(用20%硝酸酸化)/30%乙醇96°的混合物将研磨的样品在回流下提取2次,历时2小时,其代表了大规模工厂的10m比例。然后过滤该混合物。然后将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到研磨的藜麦a提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表5中所示。
表5:对藜麦a的菲洛嗪和dpph测试结果
正如可以从表5中看到的,藜麦a外壳提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为17且1%时螯合的%fe(ii)等于100%。用70%水ph3/30%乙醇96°提取的藜麦a具有自由基清除活性,面积为7366。
藜麦a外壳也用相同的方法提取,但仅用ph3下的水提取。该提取物具有斜率为16,且1%时螯合的%fe(ii)等于98%。因此,它具有与藜麦a外壳水/etoh25°相同的螯合活性。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将藜麦a提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
使用上述技术制备了七种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.5%重量的迷迭香提取物的蛋黄酱;
3)包含0.4%重量的藜麦a提取物的蛋黄酱;
4)包含0.2%重量的藜麦a提取物的蛋黄酱;
5)包含0.4%重量的藜麦a和0.5%重量的迷迭香提取物的蛋黄酱;
6)包含1%重量的藜麦a提取物的蛋黄酱;和
7)包含1%重量的藜麦a提取物(水ph3)的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图5中所示。
颜色
该提取物具有dl(1%)=-22
该提取物不影响蛋黄酱的颜色。
实施例6-藜麦b
提取物的制备
将藜麦b外壳研磨成约2mm的颗粒。然后用ph3的水(用20%硝酸酸化)将研磨的样品在回流下提取2次,历时2小时,其代表了大规模工厂的10m比例。然后过滤该混合物。然后将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到31.32%的研磨的藜麦b提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表6中所示。
表6:对藜麦b的菲洛嗪和dpph测试结果
正如可以从表6中看到的,藜麦b外壳提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为10且1%时螯合的%fe(ii)等于95.6%。
蛋黄酱的制备
用stephan混合水相i(19.7%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将藜麦b提取物和/或迷迭香提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58、0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则加入67.9%(w/w)的菜籽油。最终,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐)。
使用上述技术制备了六种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含1%重量的迷迭香提取物(rews(水溶性))的蛋黄酱;
3)包含1%重量的迷迭香提取物(reos(油溶性))的蛋黄酱;
4)包含0.4%重量的藜麦b提取物的蛋黄酱;
5)包含0.4%重量的藜麦b和1%重量的迷迭香提取物(reos)的蛋黄酱;和
6)包含0.4%重量的藜麦b和1%重量的迷迭香提取物(rews)的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图6中所示。
正如可以从图6中看到的,rews和藜麦b外壳的组合在28天期间防止了蛋黄酱氧化。
颜色
该提取物不影响蛋黄酱的颜色。
实施例7-藜麦红色外壳
提取物的制备
将藜麦红色外壳研磨成约2mm的颗粒。然后用ph3的水(用20%硝酸酸化)将研磨的样品在回流下提取2次,历时2小时,其代表了大规模工厂的10m比例。然后在25℃下用厚度滤纸fibratixaf6+af31h过滤该混合物。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到44.88%的研磨的藜麦红色外壳提取物。
将使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表7中所示。
表7:对藜麦红色外壳的菲洛嗪和dpph测试结果
将正如可以从表7中看到的,藜麦红色外壳提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为6且1%时螯合的%fe(ii)等于86.6%。
蛋黄酱的制备
用stephan混合水相i(19.7%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将藜麦红色外壳提取物和/或迷迭香提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则加入67.9%(w/w)的菜籽油。最终,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐)。
使用上述技术制备了六种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含1%重量的迷迭香提取物(rews)的蛋黄酱;
3)包含1%重量的迷迭香提取物(reos)的蛋黄酱;
4)包含0.4%重量的藜麦红色外壳提取物的蛋黄酱;
5)包含0.4%重量的藜麦红色外壳和1%重量的迷迭香提取物(reos)的蛋黄酱;和
6)包含0.4%重量的藜麦红色外壳和1%重量的迷迭香提取物(rews)的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图7中所示。
颜色
该提取物不影响蛋黄酱的颜色。
实施例8-完整藜麦c(乙醇提取物)
提取物的制备
将藜麦c完整种子研磨成约2mm的颗粒。然后通过索氏提取器用水(ph3)/etoh30/70将研磨的样品提取,其代表了大规模工厂的10m比例。然后过滤该混合物。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到完整藜麦c。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表8中所示。
表8:对完整藜麦c的菲洛嗪和dpph测试结果
正如可以从表8中看到的,完整藜麦c提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为10.34且1%时螯合的%fe(ii)等于81.11%。
蛋黄酱的制备
用stephan混合水相i(19.7%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将1%(w/w)藜麦c提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则加入67.9%(w/w)的菜籽油。最终,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐)。
使用上述技术制备了两种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含1%重量的完整藜麦c提取物(etoh)的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图8中所示。
正如可以从图8中看到的,完整藜麦c提取物在50℃(28天)加速老化的整个过程中防止蛋黄酱氧化。
颜色
该提取物不影响蛋黄酱的颜色。
实施例9-藜麦a(水提取物)
提取物的制备
将藜麦a外壳研磨成约2mm的颗粒。然后用ph3的水(用20%硝酸酸化)将研磨的样品在回流下提取2次,历时2小时,其代表了大规模工厂的10m比例。然后过滤该混合物。然后将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。然后研磨干燥的提取物,得到研磨的藜麦a提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表9中所示。
表9:对藜麦a(水提取物)的菲洛嗪和dpph测试结果
正如可以从表9中看到的,藜麦a外壳提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为19且1%时螯合的%fe(ii)等于104.1%。藜麦a外壳提取物具有自由基清除活性,面积为2478。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将藜麦a提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
使用上述技术制备了三种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含1%重量的藜麦a提取物的蛋黄酱;和
3)包含0.6%重量的藜麦a提取物的蛋黄酱
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图9中所示。
正如可以从图9中看到的,藜麦a外壳提取物在50℃(28天)加速老化的整个过程中防止蛋黄酱氧化。
颜色
该提取物具有dl(1%)=-11
该提取物不影响蛋黄酱的颜色。
实施例10-奇亚汁液
提取物的制备
使奇亚种子发芽11天。每天用水喷洒种子。在第11天,用水冲洗发芽的种子,然后用汁液离心机(hurom)离心。将液体混合物以4000rpm再离心2次20min。然后收集液体并且用旋转蒸发器(heidolph)蒸发至干。最终研磨干燥的提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表10中所示。
表10:奇亚汁液提取物的菲洛嗪和dpph测试结果
正如可以从表10中看到的,奇亚汁液对菲洛嗪测试的反应为螯合活性阳性,斜率为11且1%时螯合的%fe(ii)等于86.9%。奇亚汁液具有自由基清除活性,面积为709。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将奇亚提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58、0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
制备了三种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.5%重量的迷迭香os提取物的蛋黄酱;和
3)包含0.5%重量的迷迭香os提取物和1%重量的奇亚汁液提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图10中所示。
颜色
奇亚汁液将蛋黄酱着色为较深的颜色,轻微地变成蓝色/绿色。
实施例11-苜蓿发芽种子
使苜蓿种子发芽8天。每天用水喷洒种子。在第11天,用水冲洗发芽的种子,然后用索氏提取器和70%水/30%乙醇96°在回流下提取8小时。用于提取的溶剂代表了大规模工厂的10m比例。一旦冷却后,则过滤该混合物。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。最终研磨干燥的提取物。
然后对研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表11中所示。
表11:对苜蓿发芽种子提取物的菲洛嗪和dpph测试结果
正如可以从表11中看到的,苜蓿发芽种子提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为13.1且1%时螯合的%fe(ii)等于80.3%。然而,苜蓿发芽种子仅具有自由基清除活性,面积为1795。
苜蓿发芽种子也用相同的方法提取,但用ph3水提取。这种提取物具有斜率5.8,且1%时螯合的%fe(ii)等于48.1%。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将苜蓿提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
制备了三种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.5%重量的迷迭香os提取物的蛋黄酱;和
3)包含0.5%重量的迷迭香os提取物和1%重量的苜蓿发芽种子提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图11中所示。
颜色
苜蓿发芽种子提取物将蛋黄酱着色为较深的颜色,轻微地变成蓝色/绿色。
实施例12-大麻籽提取物
将不去壳的大麻籽用索氏提取器和ph3的水(用20%的硝酸酸化)在回流下提取8h。用于提取的溶剂代表了大规模工厂的10m比例。一旦冷却,则过滤该混合物。将液体提取物用旋转蒸发器(heidolph)与25%的麦芽糖糊精一起蒸发至干。最终研磨干燥的提取物。
使研磨的提取物进行如上所述的螯合活性和体外自由基清除活性测试的体外筛选。这些测试结果如表12中所示。
表12:对大麻籽提取物的菲洛嗪和dpph测试结果
正如可以从表12中看到的,大麻籽提取物对菲洛嗪测试的反应为螯合活性阳性,斜率为8.2且1%时螯合的%fe(ii)等于68.3%。
大麻籽也用相同的方法提取,但用水/etoh70/30提取。这种提取物具有斜率4.9,且1%时螯合的%fe(ii)等于38.9%。
蛋黄酱的制备
用ultraturax混合水相i(20.69%(w/w)的水、5%(w/w)的巴氏杀菌蛋黄和0.1%(w/w)的山梨酸钾)。接下来,如果包括,则将大麻籽提取物与相i混合。然后将水相ii(0.2%(w/w)的lygommekct58,0.5%(w/w)的cemtex12688和2.1%(w/w)的菜籽油)添加到混合物中。一旦该混合物均化,则在剧烈搅拌下靠着turax杆缓慢添加67.9%(w/w)的菜籽油。在添加油的2/3时,添加水相iii(3%(w/w)的酒精醋和0.5%(w/w)的盐),然后将剩余的油倾入。
制备了三种不同的蛋黄酱。
1)对照蛋黄酱,其中不添加提取物;
2)包含0.5%重量的迷迭香os提取物的蛋黄酱;和
3)包含0.5%重量的迷迭香os提取物和1%重量的大麻籽提取物的蛋黄酱。
如实施例1中所述,使每种蛋黄酱在50℃下在烘箱中进行5周的加速老化。结果如图12中所示。
颜色
该提取物不影响蛋黄酱的颜色。
实施例13-豌豆的提取
用ph3的水(具有硝酸或磷酸或柠檬酸)、70%乙醇提取豌豆。
将豌豆原料(压碎的)和溶剂放入圆底烧瓶(或对于更大量的圆形反应容器)中,比例为每克原料10ml溶剂。然后将混合物机械震荡,提取,然后离心。在相同条件下,将原料回收用于第二次提取。将两种液体提取物过滤,然后汇集在一起进行真空蒸发,添加25%(的干燥提取物)的载体,然后将提取物蒸发至干。然后将得到的提取物在-18℃下冷冻并冻干,然后在研钵中手动研磨,随后保存在干燥器中。
当使用上述通用方法测试时,豌豆提取物具有高于100的螯合活性斜率。
实施例14-菠菜的提取
使菠菜原料接受干燥和压碎,并在未改变的情况下用于提取。
用水提取菠菜原料。
将原料和溶剂放入带夹套的反应器容器中,比例为每克原料15ml溶剂,并进行机械振荡。然后将提取物离心、过滤并再次过滤。将液体提取物真空蒸发。添25%(的干燥提取物)麦芽糖糊精,并将提取物蒸发至干。然后将其在-18℃下冷冻,并冻干,然后在研钵中手动压碎。随后将提取物保存在干燥器中。
当使用上述通用方法测试时,菠菜提取物具有高于25的螯合活性斜率,并且通过hptlc-dpph方法得到的菠菜提取物的清除活性为dpph的39000表面积。
实施例15-包含菠菜和/或豌豆的蛋黄酱的制备
将菠菜和/或豌豆提取物单独或与其它提取物组合添加到蛋黄酱(所实施例1-12中所制备)中,并且分别在室温、40℃或50℃下老化2或1个月,且如图16、17、18、25和26所示,防止了在蛋黄酱中生成2,4-庚二烯醛。
实施例16-螯合活性:协同作用
通过菲洛嗪测试单独或组合地测试不同的提取物的螯合活性。总结每种提取物的螯合活性,并将这些总结与相应提取物组合的螯合活性进行比较。如果发现提取物组合的螯合活性高于单个提取物的螯合活性之和,则为协同作用。结果如图27和28中所示。
- 还没有人留言评论。精彩留言会获得点赞!