用于检测和/或治疗NAFLD/NASH以及肝脏中未治疗进展的后续并发症的抗体的制作方法
相关申请的交叉引用
本申请要求2018年5月8日提交的临时申请ussn62/668,637的优先权的益处,所述临时申请的公开内容通过引用并入,如同以其整体在本文中完全阐述一样。
电子提交的序列表的引用
本申请含有已经以ascii形式电子提交且在此以其整体通过引用并入的序列表。所述ascii拷贝,在2018年4月30日创建,名为“seqencelisting_st25”,并且大小为16kb字节。
本公开总体涉及结合人几丁质酶-3-样蛋白1(chi3l1)的抗体及其用途。在几个方面,所述抗体可用于检测和/或治疗主体中的非酒精性脂肪肝病(nafld)或非酒精性脂肪性肝炎(nash)以及主体肝脏中未治疗进展的后续并发症、诸如肝硬化和肝细胞癌(hcc)的组合物和方法中。
背景技术:
nafld与其严重和进行性形式(称为nash)相结合,是世界上慢性肝病的最常见原因,并且通常与肥胖、ii型糖尿病、高血压、血液的高脂质含量和不健康高脂饮食有关。据估计,在美国以及亚洲和欧洲的一些国家中,nafld的发病率高达人口的25%。nafld的进行性形式由nash代表,其发生在那些个体的近似20%中。在大多数情况下,nafld通常被认为是良性和可逆的,而nash的特征在于进行性肝脏炎症、脂肪变性、肝细胞变性、纤维化、进展至肝硬化,且甚至在一定比例的个体中发展hcc。nash的严重程度也反映在估计在美国nafld发病率为近似10-12%的儿童中,同时一些儿童将进展至终末期肝病。nafld/nash的主要预后指标是肝纤维化的存在,因为许多此类个体可能最终发展肝硬化和甚至hcc,并且因此成为肝移植的候选者。最近的研究证实,与肝脏中的任何其他病理特征无关,纤维化的程度可能决定nafld/nash的死亡率。因为nafld/nash在世界各国的流行率高,所以预计对患者和健康护理系统将存在巨大的医疗经济负担。
用于评价nafld/nash的程度和严重性的金标准需要评估肝脏活检,其是侵入性的,疼痛的,昂贵的并且与出血并发症和很少死亡相关。肝脏活检的评估可以确定脂肪变性(脂肪沉积)的程度,炎症的严重程度,肝细胞变性(由慢性损伤引起)的存在,以及纤维化/肝硬化的存在或不存在。因此,存在对生物标志物的替代测试(诸如简单且准确的血液测试)的持续需求,所述生物标志物与nafld/nash的进展以及在主体肝脏中未治疗进展的后续并发症(诸如肝硬化和hcc)相关。
技术实现要素:
因此,本公开的主题涉及结合人chi3l1的抗体及其用途。根据本公开的各个实施方案,所述抗体可用于检测和/或治疗主体中的nafld或nash以及主体肝脏中未治疗进展的后续并发症、诸如肝硬化和/或hcc的组合物和方法中。
在各个实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且所述hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1是seqidno:6,lcdr2是seqidno:7,lcdr3是seqidno:8,hcdr1是seqidno:3,hcdr2是seqidno:4且hcdr3是seqidno:5。
在一些实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含lcvr且所述重链包含hcvr,其中所述lcvr包含氨基酸序列seqidno:10且所述hcvr包含氨基酸序列seqidno:9。
在一些实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含氨基酸序列seqidno:12,且所述重链包含氨基酸序列seqidno:11。
在一些实施方案中,提供了结合人chi3l1的抗体,包含两条轻链和两条重链的抗体,其中每条轻链包含氨基酸序列seqidno:12,且每条重链包含seqidno:11。
在一些实施方案中,提供了dna分子,所述dna分子包含编码具有氨基酸序列seqidno:12的轻链多肽的多核苷酸序列。
在一些实施方案中,提供了dna分子,所述dna分子包含编码具有氨基酸序列seqidno:11的重链多肽的多核苷酸序列。
在一些实施方案中,提供了重组宿主细胞,所述重组宿主细胞包含两个前述实施方案的dna分子,所述细胞能够表达包含重链和轻链的抗体,其中所述重链的氨基酸序列是seqidno:11,且所述轻链的氨基酸序列是seqidno:12。
在一些实施方案中,提供了用于生产包含重链和轻链的结合人chi3l1的抗体的方法,其中所述重链包含氨基酸序列seqidno:11,且所述轻链包含seqidno:12的氨基酸序列,所述方法包括以下步骤:(a)在使得表达所述抗体的条件下培养前述实施方案的重组宿主细胞;和(b)从所述宿主细胞回收表达的抗体。在一些实施方案中,提供了通过所述方法生产的抗体。
在各个实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且所述hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1是seqidno:16,lcdr2是seqidno:17,lcdr3是seqidno:18,hcdr1是seqidno:13,hcdr2是seqidno:14且hcdr3是seqidno:15。
在一些实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含lcvr且所述重链包含hcvr,其中所述lcvr包含氨基酸序列seqidno:20且所述hcvr包含氨基酸序列seqidno:19。
在一些实施方案中,提供了结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含氨基酸序列seqidno:22,且所述重链包含氨基酸序列seqidno:21。
在一些实施方案中,提供了结合人chi3l1的抗体,包含两条轻链和两条重链的抗体,其中每条轻链包含氨基酸序列seqidno:22,且每条重链包含seqidno:21。
在一些实施方案中,提供了dna分子,所述dna分子包含编码具有氨基酸序列seqidno:22的轻链多肽的多核苷酸序列。
在一些实施方案中,提供了dna分子,所述dna分子包含编码具有氨基酸序列seqidno:21的重链多肽的多核苷酸序列。
在一些实施方案中,提供了重组宿主细胞,所述重组宿主细胞包含两个前述实施方案的dna分子,所述细胞能够表达包含重链和轻链的抗体,其中所述重链的氨基酸序列是seqidno:21,且所述轻链的氨基酸序列是seqidno:22。
在一些实施方案中,提供了用于生产包含重链和轻链的结合人chi3l1的抗体的方法,其中所述重链包含氨基酸序列seqidno:21,且所述轻链包含seqidno:22的氨基酸序列,所述方法包括以下步骤:(a)在使得表达所述抗体的条件下培养前述实施方案的重组宿主细胞;和(b)从所述宿主细胞回收表达的抗体。在一些实施方案中,提供了通过所述方法生产的抗体。
在一些实施方案中,提供了药物组合物,其包含至少一种本公开的抗体和一种或多种药学上可接受的载体、稀释剂或赋形剂。
在各个实施方案中,提供了测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与权利要求11-14中任一项的抗体在具有固定化的权利要求1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将所述主体鉴定为具有nafld或nash;或(b)如果chi3l1的水平等于或低于参考水平,则将所述主体鉴定为不具有nafld或nash。在一些方面,所述参考水平是约2.0ng/30μl血清。在一些方面,当chi3l1的水平高于参考水平时,所述测定法进一步包括提供适于治疗nafld或nash的治疗。在一些方面,所述治疗包括施用chi3l1抑制剂。在一些方面,所述chi3l1抑制剂包含至少一种本公开的结合人chi3l1的抗体。
在各个实施方案中,提供了测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与权利要求11-14中任一项的抗体在具有固定化的权利要求1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将所述主体鉴定为具有肝硬化;或(b)如果chi3l1的水平等于或低于参考水平,则将所述主体鉴定为不具有肝硬化。在一些方面,所述参考水平是约2.0ng/30μl血清。在一些方面,当chi3l1的水平高于参考水平时,所述测定法进一步包括提供适于治疗肝硬化的治疗。在一些方面,所述治疗包括施用chi3l1抑制剂。在一些方面,所述chi3l1抑制剂包含至少一种本公开的结合人chi3l1的抗体。
在一些实施方案中,提供了测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与权利要求11-14中任一项的抗体在具有固定化的权利要求1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将所述主体鉴定为具有hcc;或(b)如果chi3l1的水平等于或低于参考水平,则将所述主体鉴定为不具有hcc。在一些方面,所述参考水平是约2.0ng/30μl血清。在一些方面,当chi3l1的水平高于参考水平时,所述测定法进一步包括提供适于治疗hcc的治疗。在一些方面,所述治疗包括施用chi3l1抑制剂。在一些方面,所述chi3l1抑制剂包含至少一种本公开的结合人chi3l1的抗体。
在一些实施方案中,提供了监测具有nafld或nash的主体中的治疗功效的方法,所述方法包括:(i)在第一时间点测量从主体获得的第一样品中的chi3l1的第一水平,其中所述测量包括将所述样品与权利要求11-14中任一项的抗体在具有固定化的权利要求1-4中任一项的抗体的物品中一起孵育;(ii)向所述主体施用用于治疗nafld或nash的治疗剂;和(iii)在第二时间点测量从主体获得的第二样品中的chi3l1的第二水平,其中所述测量包括将所述样品与权利要求11-14中任一项的抗体在具有固定化的权利要求1-4中任一项的抗体的物品中一起孵育,其中所述第二时间点晚于所述第一时间点并且在所述施用之后,且其中如果所述第二水平显著低于所述第一水平,则认为所述治疗是有效的。在一些方面,所述治疗剂是chi3l1抑制剂。在一些方面,所述chi3l1抑制剂包含至少一种本公开的结合人chi3l1的抗体。
在一些实施方案中,提供了治疗主体中的nafld或nash的方法,所述方法包括将治疗有效量的至少一种本公开的结合人chi3l1的抗体施用于所述主体。
在一些方面,提供了治疗主体中的肝硬化的方法,所述方法包括将治疗有效量的至少一种本公开的结合人chi3l1的抗体施用于所述主体。
在一些方面,提供了治疗主体中的hcc的方法,所述方法包括将治疗有效量的至少一种本公开的结合人chi3l1的抗体施用于所述主体。
本公开的主题的额外特征和优点将在下面的详述中阐述,并且部分地对于本领域技术人员而言从该描述中是显而易见的,或者通过实施如本文所述的本公开(包括下面的详述、权利要求以及附图)的主题而被认识到。
应理解,前面的一般描述和以下的详述都呈现了本公开的主题的实施方案,并且旨在提供用于理解如请求保护的本公开的主题的性质和特征的概述或框架。包括附图以提供对本公开的主题的进一步理解,并且附图被并入并构成本说明书的一部分。附图举例说明本公开的主题的各个实施方案,并且与说明书一起用于解释本公开的主题的原理和操作。另外,附图和描述仅仅是说明性的,并且不旨在以任何方式限制权利要求的范围。
附图说明
当结合以下附图阅读时,可以最好地理解本公开的具体实施方案的以下详述,其中相似的结构用相似的附图标记表示,并且其中:
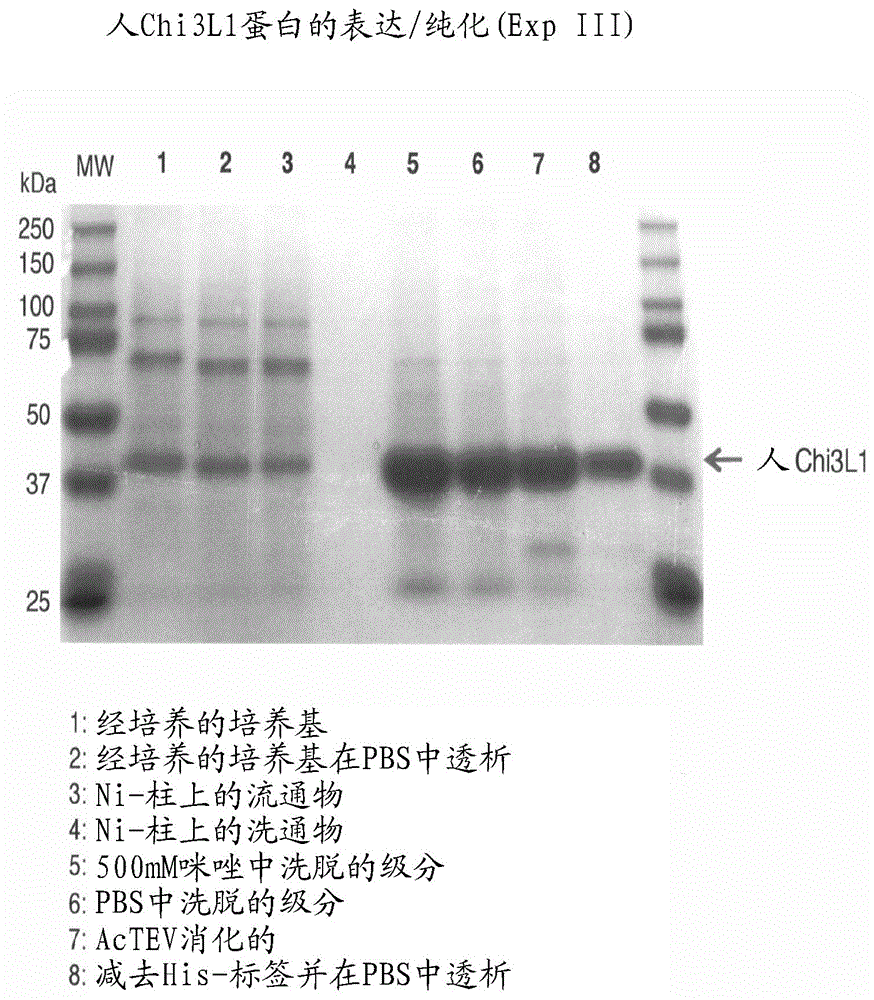
图1描绘人chi3l1蛋白的表达和纯化。通过针对chi3l1蛋白的商业抗体证实重组chi3l1蛋白的免疫原性。
图2证实,当包被在平板上时,单克隆ab1(ch568)结合chi3l1蛋白,其可以以约2ng/ml的浓度被检测到。
图3证实,在标准曲线中,就与重组chi3l1蛋白的结合而言,使用本文公开的抗体的基于双位点单克隆抗体的elisa的性能。注意,结合活性在2-50ng/30μl的chi3l1蛋白的宽浓度范围是线性的。该标准曲线用于测定具有nafld/nash的个体(如表5中所示)和正常对照(如表6中所示)的血液中chi3l1蛋白的水平。
图4描绘源自正常对照(nc)、非酒精性脂肪肝病/非酒精性脂肪性肝炎(nafld/nash)、肝硬化(lc)和肝细胞癌(hcc)的各个组的血液中的chi3l1蛋白水平,如使用基于双位点单克隆抗体的elisa使用本文公开的抗体所测定。注意,nafld/nash群组中超高值的组。
图5描绘如使用基于双位点单克隆抗体的elisa使用本文公开的抗体所测定的,各个临床组之间的阳性率的比较,其中nc代表正常对照,bc代表乳腺癌,nafld/nash代表非酒精性脂肪肝病/非酒精性脂肪性肝炎,lc代表肝硬化,且hcc代表肝细胞癌。
具体实施方式
以下具体实施方案的描述本质上仅仅是示例性的,并且决不旨在限制本发明、其应用或用途的范围,所述范围当然可以变化。本发明的描述涉及本文包括的非限制性定义和术语。这些定义和术语并不设计用于对本发明的范围或实践的限制,而是仅出于说明性和描述性目的而呈现。除非另有定义,否则本文使用的所有术语(包括技术和科学术语)具有与本公开所属领域的普通技术人员通常理解的相同含义。应进一步理解,术语,诸如常用字典中定义的那些,应当被理解为具有与它们在相关领域和本公开的背景下的含义一致的含义,并且不应以理想化或过于正式的含义进行解释,除非本文中明确如此定义。尽管所述方法和组合物被描述为使用特定顺序的单个步骤或特定材料,但应理解,步骤或材料可以是可互换的,使得本发明的描述可以包括以多种方式排列的多个步骤或部分,如本领域技术人员所容易理解的。
定义
如本文所用,单数形式“一(a)”、“一(an)”和“该(the)”包括复数对象,除非上下文另有清楚指出。因此,例如,对“结构化底部表面”的提及包括具有两个或更多个此类“结构化底部表面”的实例,除非上下文另有清楚指出。
如本文所用,术语“或”意指“和/或”。如在本文中的短语诸如“a和/或b”中使用的术语“和/或”旨在包括a和b两者;a或b;a(单独);和b(单独)。同样地,如短语诸如“a、b和/或c”中使用的术语“和/或”旨在涵盖以下实施方案中的每一个:a、b和c;a、b或c;a或c;a或b;b或c;a和c;a和b;b和c;a(单独);b(单独);和c(单独)。
如本文所用,关于值或参数的术语“近似”或“约”通常被认为包括在任一方向(大于或小于)上落入数字的5%、10%、15%或20%的范围内的数字,除非另有说明或从上下文中显而易见(除非此数字小于可能值的0%或超过可能值的100%)。如本文所用,对“近似”或“约”值或参数的提及包括(并描述)涉及该值或参数的实施方案。例如,涉及“约x”的描述包括“x”的描述。
如本文所用,“具有(have)”、“具有(has)”、“具有(having)”、“包括(include)”、“包括(includes)”、“包括(including)”、“包含(comprise)”、“包含(comprises)”、“包含(comprising)”等在它们的开放式包括性含义上使用,并且通常意指“包括,但不限于(include,butnotlimitedto)”、“包括,但不限于(includes,butnotlimitedto)”或“包括,但不限于(including,butnotlimitedto)”。
“任选的”或“任选地”意指随后描述的事件、情况或组分可以发生或可以不发生,并且该描述包括该事件、情况或组分发生的情况和其不发生的情况。
词语“优选的”和“优选地”是指在某些情况下可以提供某些益处的本公开的实施方案。然而,在相同或其他情况下,其他实施方案也可以是优选的。此外,对一个或多个优选实施方案的描述并不意味着其他实施方案不是有用的,并且不旨在从本发明技术的范围排除其他实施方案。
范围在本文中可以表示为从“约”一个特定值,和/或至“约”另一个特定值。当表达此范围时,实例包括从一个特定值和/或至另一个特定值。类似地,当通过使用先行词“约”将值表示为近似值时,应理解特定值形成另一个方面。还应进一步理解,每个范围的端点相对于另一个端点以及独立于另一个端点都是显著的。
应理解,在本文中使用语言“包含”来描述实施方案的任何地方,还提供了以“由......组成”和/或“基本上由......组成”描述的另外类似的实施方案。还应理解,在本文中使用语言“基本上由......组成”的描述实施方案的任何地方,还提供了以“由......组成”描述的另外类似实施方案。
此外,本文中,通过端点记载数值范围包括该范围内包含的所有数字(例如,1至5包括1、1.5、2、2.75、3、3.80、4、5等)。应进一步理解,本说明书中给出的每个数值范围将包括落入此较宽的数值范围内的每个较窄的数值范围,如同此类较窄的数值范围都在本文中明确写出一样。在一系列值“大于”、“小于”等特定值的情况下,该值包括在该范围内。
如本文所用,术语“疾病”、“病症”或“病况”在本文中可互换使用,是指身体或一些器官的状态的任何改变,中断或干扰功能的表现和/或引起受困扰的人或与人接触的那些的症状诸如不适、功能障碍、痛苦或甚至死亡。疾病或病症也可以与瘟热、生病、病恙、痼疾、病症、疾病、病、病苦或病痛相关。
如本文所用,“非酒精性脂肪肝病”或“nafld”是指良性和非进展性疾病或病症,其特征在于肝脏中不是由于过量饮酒导致的异常脂肪沉积(即,脂肪变性)。
如本文所用,“非酒精性脂肪性肝炎”或“nash”是指进行性疾病或病症,其特征在于与脂肪肝组合的肝脏炎症。其类似于酒精性肝病,但发生在少喝酒或不喝酒的人中。nash可以导致纤维化、肝硬化、终末期肝病、肝衰竭和肝细胞癌。
如本文所用,术语“长期”施用意指治疗剂或药物施用至少12周的时段。这包括施用治疗剂或药物,使得其经至少12周的时段或持续至少12周的时段是有效的,并且不一定意味着施用本身发生12周,例如,如果使用持续释放组合物或长效治疗剂或药物。因此,所述主体被治疗至少12周的时段。在许多情况下,长期施用持续至少4、5、6、7、8、9个月或更长,或至少1、2、3、5、7或10年或更长。
如本文所用,“chi3l1”、“几丁质酶-3-样蛋白1”或“ykl-40”是指由至少巨噬细胞、软骨细胞、中性粒细胞、滑膜细胞和一些癌细胞分泌的~40kda糖蛋白。chi3l1不具有几丁质酶活性,是th2促进细胞因子,已经与akt抗细胞凋亡信号传导途径相关并诱导星形胶质细胞的迁移。chi3l1表达产物的序列对于许多物种是已知的,例如人chi3l1(ncbi基因idno:1116)mrna(seqidno:2;ncbirefseq:nm001276)和多肽(seqidno:1;ncbirefseq:np001267)。chi3l1的活性可以通过例如测量chi3l1的抗细胞凋亡作用,或通过测定th2细胞因子产生的促进来测量。
如本文所用,术语“抑制剂”是指可以使靶向表达产物(例如,编码靶标或靶多肽的mrna)的表达和/或活性降低例如至少10%或更多、例如10%或更多、50%或更多、70%或更多、80%或更多、90%或更多、95%或更多或98%或更多的试剂。例如,可以通过测量chi3l1的表达产物的水平和/或chi3l1的活性,确定例如chi3l1的抑制剂的功效,例如其降低chi3l1的水平和/或活性的能力。用于测量给定mrna和/或多肽的水平的方法是本领域技术人员已知的,例如,rt-pcr可用于测定rna的水平,并且用抗体(例如,抗chi3l1抗体)的western印迹或免疫测定可用于测定多肽的水平。可以使用本领域已知的方法测定例如chi3l1的活性。在一些实施方案中,所述抑制剂可以是抑制性核酸;适体;抗体试剂;抗体;或小分子。
如本文所用,术语“物品”、“细胞培养物品”等意指可用于用细胞(包括培养细胞)的体外实验的任何容器,并且包括平板、孔,烧瓶、多孔板、多层烧瓶和灌注系统,其为细胞培养提供环境。
术语“减少(decrease)”,“降低(reduced、reduction)”或“抑制(inhibit)”在本文中均用于表示统计学上显著的量的减少。在一些实施方案中,“降低”或“减少”或“抑制”通常表示相较于参考水平(例如,在没有给定治疗的情况下)减少至少10%,并且可以包括例如减少至少约10%、至少约20%、至少约25%、至少约30%、至少约35%、至少约40%、至少约45%、至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约98%、至少约99%,或更多。本文所使用的“降低”或“抑制”不包括相较于参考水平的完全抑制或降低。“完全抑制”是相较于参考水平100%抑制。减少可以优选下降至无给定病症的个体的正常范围内接受的水平。
术语“增加(increased、increase)”、“增强”或“活化”在本文中均用于表示统计学上显著的量的增加。在一些实施方案中,术语“增加”、“增强”或“活化”可以表示相较于参考水平增加至少10%,例如相较于参考水平增加至少约20%、或至少约30%、或至少约40%、或至少约50%、或至少约60%、或至少约70%、或至少约80%、或至少约90%、或最高达并包括100%的增加,或者在10%-100%之间的任意增加,或相较于参考水平的至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍、或至少约10倍的增加,或2倍-10倍之间或更多的任意增加。在标志物或症状的上下文中,“增加”是以这种水平的统计学上显著的增加。
如本文所用的“主体”表示人或动物。通常,动物是脊椎动物,例如灵长类动物、啮齿动物、家畜或狩猎动物。灵长类动物包括黑猩猩、食蟹猴、蜘蛛猴和猕猴,例如恒河猴。啮齿动物包括小鼠、大鼠、土拨鼠、雪貂、兔和仓鼠。家畜和狩猎动物包括牛、马、猪、鹿、野牛、水牛、猫科动物物种(例如家猫)、犬科动物物种(例如狗、狐狸、狼)、禽类物种(例如鸡、鸸鹋、鸵鸟),以及鱼(例如鳟鱼、鲶鱼和鲑鱼)。在一些实施方案中,主体是哺乳动物,例如灵长类动物,例如人。术语“个体”、“患者”和“主体”在本文中可互换使用。优选地,主体是哺乳动物。哺乳动物可以是人、非人灵长类动物、小鼠、大鼠、狗、猫、马或牛,但不限于这些实例。有利地,可以使用非人哺乳动物作为代表nash的动物模型的主体。主体可以是雄性或雌性的。
主体可以是先前已被诊断患有或被鉴定为患有或具有需要治疗的病况(例如,nafld和/或nash)或与这种病况相关的一种或多种并发症的主体,并且任选地,已经经历过针对nafld和/或nash或与nafld和/或nash相关的一种或多种并发症(例如,肝硬化和/或肝细胞癌)的治疗。或者,主体也可以是先前未被诊断为患有例如nafld和/或nash或与nafld和/或nash相关的一种或多种并发症的主体。例如,主体可以是表现出nafld和/或nash或与nafld和/或nash相关的一种或多种并发症的一种或多种风险因素的主体,或未表现出风险因素的主体。
“需要针对特定病况的治疗的主体”可以是患有该病况、被诊断为患有该病况、或处于发展出该病况的升高风险的主体。
如本文所用的术语“样品”、“生物样品”或“测试样品”表示从生物有机体获取或分离的样品,例如来自主体的血液或血浆样品。示例性生物样品包括但不限于生物流体样品;血清;血浆;尿;唾液;和/或组织样品等。该术语还包括上述样品的混合物。术语“测试样品”还包括未处理或预处理(或预加工)的生物样品。在一些实施方案中,测试样品可包含来自主体的细胞。在一些实施方案中,测试样品可以是血液样品。在一些实施方案中,测试样品可以是血浆样品。在一些实施方案中,测试样品可以是血清样品。
可以通过从主体取出样品来获得测试样品,但也可以通过使用先前的样品(例如,在先前时间点分离的,以及由相同或另一个人分离的)来完成。此外,测试样品可以是新鲜收集的或先前收集的样品。
如本文所用,术语“分离的”是指不含或基本上不含见于细胞环境中的任何其他大分子物质的蛋白、肽或核酸。如本文所用的“基本上不含”表示目标蛋白、肽或核酸占存在的大分子物质的大于80%(以摩尔计),大于90%,大于95%,或大于99%。
在一些实施方案中,测试样品可以是未处理的测试样品。如本文所用,短语“未处理的测试样品”是指除了在溶液中稀释和/或悬浮之外没有任何先前样品预处理的测试样品。用于处理测试样品的示例性方法包括但不限于离心、过滤、超声处理、均质化、加热、冷冻和解冻,及其组合。在一些实施方案中,测试样品可以是冷冻的测试样品,例如冷冻的组织。在采用本文所述的方法、测定和系统之前,可以将冷冻的样品解冻。解冻后,可以将冷冻的样品离心,然后进行本文所述的方法、测定和系统。在一些实施方案中,测试样品是澄清的测试样品,例如,通过离心和收集包含澄清的测试样品的上清液。在一些实施方案中,测试样品可以是预加工的测试样品,例如,由选自离心、过滤、解冻、纯化及其任何组合的处理产生的上清液或滤液。在一些实施方案中,可以用化学和/或生物试剂处理测试样品。化学和/或生物试剂可用于在加工过程中保护和/或维持样品(包括其中的生物分子(例如,核酸和蛋白质))的稳定性。一种示例性试剂是蛋白酶抑制剂,其通常用于在加工过程中保护或维持蛋白质的稳定性。技术人员充分了解适合于预加工测定如本文所述的表达产物的水平所需的生物样品的方法和过程。
如本文所用,术语“核酸”或“核酸序列”是指并入核糖核酸、脱氧核糖核酸或其类似物的单元的任何分子,优选聚合物分子。核酸可以是单链或双链的。单链核酸可以是变性双链dna的一条核酸链。或者,它可以是不衍生自任何双链dna的单链核酸。在一个方面,核酸可以是dna。在另一方面,核酸可以是rna。合适的核酸分子是dna,包括基因组dna或cdna。其他合适的核酸分子是rna,包括mrna。
如本文所用,术语“蛋白质”和“多肽”在本文中可互换使用,表示通过相邻残基的α-氨基和羧基之间的肽键彼此连接的一系列氨基酸残基。术语“蛋白质”和“多肽”是指氨基酸的聚合物,所述氨基酸包括修饰的氨基酸(例如,磷酸化的,糖化的,糖基化的等)和氨基酸类似物,无论其大小或功能如何。“蛋白质”和“多肽”通常用于指相对大的多肽,而术语“肽”通常用于指小的多肽,但本领域中这些术语的使用重叠。当提及基因产物及其片段时,术语“蛋白质”和“多肽”在本文中可互换使用。因此,示例性多肽或蛋白质包括基因产物、天然存在的蛋白质、同源物、直系同源物、旁系同源物、片段和前述的其他等同物、变体、片段和类似物。
如本文所用,“表达水平”是指存在于细胞或样品中的由给定基因编码的mrna分子和/或多肽分子的数量。表达水平可以相对于参考水平增加或减少。
如本文所用,术语“治疗(treat,treatment,treating)”或“改善”是指治疗性治疗,其中目标是逆转、减轻、改善、抑制、减缓或停止与疾病或病症(例如nafld,nash,以及主体肝脏中未治疗进展的后续并发症,例如肝硬化和/或hcc)相关的病况的进展或严重性。术语“治疗”包括减少或减轻病况、疾病或病症(例如nafld,nash,以及主体肝脏中未治疗进展的后续并发症,例如肝硬化和/或hcc)的至少一种不良作用或症状。如果一种或多种症状或临床标志物减少,治疗通常是“有效的”。或者,如果疾病的进展减少或停止,则治疗是“有效的”。也即,“治疗”不仅包括症状或标志物的改善,还包括与对于没有治疗的情况的预期相比,症状的进展或恶化的停止或至少减缓。有益或期望的临床结果包括但不限于减轻一种或多种症状,减轻疾病程度,稳定(即,不恶化)疾病状态,延迟或减缓疾病进展,改善或缓解疾病状态,缓解(无论是部分的还是全部的)和/或降低的死亡率,无论是可检测的还是不可检测的。术语疾病的“治疗”还包括提供疾病的症状或副作用的缓解(包括姑息治疗)。
如本文所用,术语“药物组合物”是指活性剂与药学上可接受的载体(例如通常用于制药工业的载体)的组合。
本文采用短语“药学上可接受的”指在合理的医学判断范围内,适合与人类和动物的组织接触使用而无过度毒性、刺激、过敏反应或其他问题或并发症,与合理的效益/风险比率相称的那些化合物、材料、组合物和/或剂型。
如本文所用,术语“施用”是指通过方法或途径将如本文公开的化合物置于主体中,其导致在所需部位至少部分递送所述药剂。可以通过任何合适的途径施用包含本文公开的化合物的药物组合物,其导致在主体中的有效治疗。
如本文所用的术语“有效量”是指减轻疾病或病况(例如,nafld,nash,以及主体肝脏中未治疗进展的后续并发症,例如肝硬化和/或hcc)的至少一种或多种症状所需的治疗量,并且涉及提供所需效果的药物组合物的足够量。因此,术语“治疗有效量”是指当施用于典型主体时,足以引起特定效果的治疗量。在各种背景下,如本文所用的有效量还包括足以延迟疾病况状的发展,改变疾病况状的过程(例如但不限于,减缓疾病况状的进展),或逆转疾病况状的量。应当理解,本领域已知有许多方式来确定用于给定应用的有效量。例如,用于剂量确定的药理学方法可用于治疗背景中。在治疗性或预防性应用的背景下,施用于主体的组合物的量将取决于疾病的类型和严重性以及个体的特征,例如总体健康状况、年龄、性别、体重和对药物的耐受性。它还取决于疾病的程度、严重性和类型。技术人员将能够根据这些和其他因素来确定合适的剂量。组合物还可以与一种或多种另外的治疗化合物组合施用。
示例性施用模式包括但不限于注射、输注、滴注、吸入或摄取。“注射”包括但不限于静脉内、肌肉、动脉内、鞘内、心室内、囊内、眶内、心内、皮内、肝内、腹膜内、经气管、皮下、表皮下、关节内、囊膜下、蛛网膜下腔、脊柱内、脑脊髓内和胸骨内注射和输注。施用可以是全身或局部的。
术语“统计学上显著的”或“显著的”是指统计学显著性,其在某些方面可以表示两个标准偏差(2sd)或更大的差异。
如本文所用,术语“显著”应解释为如同用术语“统计学上”修饰的。
细胞生物学和分子生物学中常见术语的定义可见于:“themerckmanualofdiagnosisandtherapy”,第19版,merckresearchlaboratories出版,2006(isbn0-911910-19-0);roberts.porter等人(编),theencyclopediaofmolecularbiology,blackwellscienceltd.出版,1994(isbn0-632-02182-9);benjaminlewin,genesx,jones&bartlettpublishing出版,2009(isbn-10:0763766321);kendrew等人(编),molecularbiologyandbiotechnology:acomprehensivedeskreference,vchpublishers,inc.出版,1995(isbn1-56081-569-8)和currentprotocolsinproteinsciences2009,wileyintersciences,coligan等人编辑。
除非另有明确说明,否则绝无意将本文所述的任何方法解释为要求以特定顺序执行其步骤。因此,在方法权利要求实际上没有记载其步骤所遵循的顺序或者在权利要求或说明书中没有特别说明步骤将限于特定顺序的情况下,无意推断任何特定的顺序。任何一个权利要求中任何所述的单个或多个特征或方面可以与任何其他一个或多个权利要求中的任何其他所述的特征或方面组合或交换。
虽然可以使用连接词“包含”来公开具体实施方案的各种特征、要素或步骤,但是应该理解隐含替代实施方案,包括可以使用连接词“由……组成”或“基本上由……组成”来描述的那些。
药物组合物
本发明的组合物和方法可以被用于治疗有此需要的个体。在某些实施方案中,个体是哺乳动物,诸如人或非人哺乳动物。当施用至动物(如人)时,组合物或化合物优选地作为药物组合物施用,所述药物组合物包含例如本发明的化合物和药学上可接受的载体。药学上可接受的载体是本领域周知的,并且包括例如水性溶液(如水或生理缓冲盐水)或其他溶剂或媒介物(如二醇类、甘油、油(如橄榄油)或可注射的有机酯)。在优选的实施方案中,当这样的药物组合物用于人类施用,特别是用于侵入性施用途径(即,规避通过上皮屏障的运输或扩散的途径(如注射或植入))时,水性溶液是无热原的或基本上无热原的。可以选择赋形剂,例如,以实现药剂的延迟释放或以选择性地靶向一种或多种细胞、组织或器官。药物组合物可以呈剂量单位形式,如片剂、胶囊剂(包含分散型胶囊和明胶胶囊)、颗粒剂、用于重构的亲液物(lyophile)、粉剂、溶液、糖浆剂、栓剂、注射剂等。组合物也可以存在于透皮递送系统(例如,皮肤贴剂)中。组合物也可以存在于适合于局部施用的溶液(例如洗液、乳霜或软膏剂)中。
药学上可接受的载体可以含有生理学上可接受的试剂,其起作用以例如稳定化合物(诸如本发明的化合物)、增加其溶解度或增加其吸收。这样的生理学上可接受的试剂包括例如,碳水化合物(诸如葡萄糖、蔗糖或葡聚糖)、抗氧化剂(诸如抗坏血酸或谷胱甘肽)、螯合剂、低分子量蛋白质或其他稳定剂或赋形剂。药学上可接受的载体(包括生理学上可接受的试剂)的选择取决于例如组合物的施用途径。制剂或药物组合物可以是自乳化药物递送系统或自微乳化药物递送系统。药物组合物(制剂)也可以是其中可并入例如本发明的化合物的脂质体或其他聚合物基质。例如,包含磷脂或其他脂质的脂质体是制造和施用相对简单的、无毒的、生理学上可接受的和可代谢的载体。
本文中采用短语“药学上可接受的”是指在合理的医学判断范围内,适合与人类和动物的组织接触使用而无过度毒性、刺激、过敏反应或其他问题或并发症,与合理的效益/风险比率相称的那些化合物、材料、组合物和/或剂型。
如本文所用的短语“药学上可接受的载体”表示药学上可接受的材料、组合物或媒介物(如液体或固体填充剂、稀释剂、赋形剂、溶剂或包封材料)。每种载体在与制剂的其他成分相容并且对患者无害的意义上必须是“可接受的”。可以用作药学上可接受的载体的材料的一些实例包括:(1)糖(诸如乳糖、葡萄糖和蔗糖);(2)淀粉(诸如玉米淀粉和马铃薯淀粉);(3)纤维素及其衍生物(诸如羧甲基纤维素钠、乙基纤维素和乙酸纤维素);(4)粉状黄蓍胶;(5)麦芽;(6)明胶;(7)滑石;(8)赋形剂(诸如可可脂和栓剂蜡);(9)油类(诸如花生油、棉籽油、红花子油、芝麻油、橄榄油、玉米油和大豆油);(10)二醇类(如丙二醇);(11)多元醇(如甘油、山梨糖醇、甘露糖醇和聚乙二醇);(12)酯类(诸如油酸乙酯和月桂酸乙酯);(13)琼脂;(14)缓冲剂(诸如氢氧化镁和氢氧化铝);(15)海藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)磷酸盐缓冲溶液;以及(21)药物制剂中采用的其他无毒相容物质。
可以通过很多施用途径中的任何一种将药物组合物(制剂)施用至主体,所述施用途径包括例如,口服(例如,作为在水性溶液或非水性溶液或悬浮液中的灌服剂、片剂、胶囊剂(包括分散型胶囊和明胶胶囊)、大丸剂、粉剂、颗粒剂、用于应用至舌的糊剂);通过口腔粘膜吸收(例如,舌下地);皮下;经皮(例如作为应用至皮肤的贴剂);以及局部(例如,作为应用至皮肤的乳霜、软膏或喷雾剂)。化合物也可以经配制用于吸入。在某些实施方案中,化合物可以简单地被溶解或被悬浮在无菌水中。适当的施用途径和适用于所述施用途径的组合物的细节可以见于例如美国专利号6,110,973、5,763,493、5,731,000、5,541,231、5,427,798、5,358,970和4,172,896以及其中引用的专利中。
所述制剂可以方便地以单位剂型呈现,并且可以通过药学领域中众所周知的任何方法制备。可以与载体材料组合以产生单一剂型的活性成分的量将根据所治疗的宿主、特定的施用模式而变化。可以与载体材料组合以产生单一剂型的活性成分的量将通常是产生治疗效果的化合物的量。通常,在百分之百中,此量将范围为约1%至约99%的活性成分,优选地约5%至约70%,最优选地约10%至约30%。
制备这些制剂或组合物的方法包括使活性化合物(诸如本发明的化合物)与载体以及任选一种或多种辅助成分结合的步骤。通常,通过将本发明的化合物与液体载体或精细粉碎的固体载体或两者均匀地且密切地结合,并且然后使产品成型(如果必要的话),而制备制剂。
适合于口服施用的本发明的制剂可以是下列形式:胶囊剂(包括分散型胶囊和明胶胶囊)、扁囊剂、丸剂、片剂、糖锭(使用调味基底,通常是蔗糖和阿拉伯胶或黄蓍胶)、亲液物、粉剂、颗粒剂、或作为水性或非水性液体中的溶液或混悬液、或作为水包油或油包水液体乳剂、或作为酏剂或糖浆剂、或作为软锭剂(使用惰性基质(如明胶和甘油、或蔗糖和阿拉伯胶))和/或作为漱口剂等,每种含有预定量的本发明化合物作为活性成分。组合物或化合物也可以作为大丸剂、药糖剂或糊剂施用。
为了制备用于口服施用的固体剂型(胶囊剂(包括分散型胶囊和明胶胶囊)、片剂、丸剂、糖衣丸、粉剂、颗粒剂等),将活性成分与一种或多种药学上可接受的载体(如柠檬酸钠或磷酸二钙)和/或下列中的任何混合:(1)填充剂或增量剂(诸如淀粉、乳糖、蔗糖、葡萄糖、甘露糖醇和/或硅酸);(2)粘合剂(诸如例如,羧甲基纤维素、海藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和/或阿拉伯胶);(3)湿润剂(诸如甘油);(4)崩解剂(诸如琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、海藻酸、某些硅酸盐以及碳酸钠);(5)溶液阻滞剂(诸如石蜡);(6)吸收加速剂(诸如季铵化合物);(7)润湿剂(诸如例如,鲸蜡醇和单硬脂酸甘油酯);(8)吸收剂(诸如高岭土和膨润土);(9)润滑剂(诸如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、硫酸月桂酸钠及其混合物);(10)络合剂(诸如改性的或未改性的环糊精);以及(11)着色剂。在胶囊剂(包括分散型胶囊和明胶胶囊)、片剂和丸剂情况下,药物组合物也可以包含缓冲剂。相似类型的固体组合物也可以用作软填充的和硬填充的明胶胶囊中的填充剂,其使用此类赋形剂,如乳糖(lactose或milksugar)以及高分子量聚乙二醇等。
可以通过压缩或模塑制造片剂,任选地使用一种或多种辅助成分。可以使用粘合剂(例如,明胶或羟丙基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如,乙醇酸淀粉钠,或交联羧甲基纤维素钠)、表面活性剂或分散剂,制备压制片剂。可以通过在适合的机器中模塑用惰性液体稀释剂润湿的粉状化合物的混合物制造模制片剂。
药物组合物的片剂以及其他固体剂型(如糖衣丸、胶囊剂(包括分散型胶囊和明胶胶囊)、丸剂和颗粒剂)可以任选地被刻痕,或制备有包衣和壳(如肠溶包衣以及其他药物配制领域中众所周知的包衣)。它们也可以经配制以提供其中活性成分的缓慢释放或控制释放,其使用例如不同比例的羟丙基甲基纤维素以提供期望的释放曲线,其他聚合物基质、脂质体和/或微球体。可以通过例如通过截留细菌的过滤器过滤,或通过并入无菌固体组合物形式的灭菌剂对它们灭菌,所述无菌固体组合物可以在临使用前溶解在无菌水或一些其他无菌可注射介质中。这些组合物也可以任选地含有乳浊剂,并且可以是仅在或优先地在胃肠道的某个部分(任选地,以延迟方式)释放一种或多种活性成分的组合物。可以被使用的包埋组合物的实例包含聚合物质和蜡。活性成分也可以是微囊化的形式,其在适当时具有上述赋形剂中的一种或多种。
可用于口服施用的液体剂型包括药学上可接受的乳剂、用于重构的亲液物、微乳剂、溶液、混悬液、糖浆剂和酏剂。除活性成分之外,液体剂型可以含有本领域中通常使用的惰性稀释剂(诸如例如,水或其他溶剂、环糊精及其衍生物)、增溶剂和乳化剂(诸如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油类(特别地,棉籽油、落花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢呋喃醇、聚乙二醇和失水山梨糖醇的脂肪酸酯,及其混合物)。
除惰性稀释剂之外,口服组合物也可以包含助剂(如润湿剂、乳化剂和悬浮剂、甜味剂、风味剂、着色剂、芳香剂和防腐剂)。
除活性化合物之外,混悬液可以含有悬浮剂(诸如例如,乙氧基化异硬脂醇、聚氧乙烯山梨糖醇和失水山梨糖醇酯、微晶纤维素、偏氢氧化铝、膨润土、琼脂和黄蓍胶,及其混合物)。
用于局部施用或经皮施用的剂型包括粉剂、喷雾剂、软膏、糊剂、乳霜、洗液、凝胶剂、溶液、贴剂和吸入剂。活性化合物可以在无菌条件下与药学上可接受的载体、以及与可能需要的任何防腐剂、缓冲剂或推进剂混合。
除活性化合物之外,软膏、糊剂、乳霜和凝胶剂可以含有赋形剂(如动物脂肪和植物脂肪、油类、蜡、石蜡、淀粉、黄蓍胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、硅酸、滑石和氧化锌,或其混合物)。
除活性化合物之外,粉剂和喷雾剂可以含有赋形剂(如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末,或这些物质的混合物)。喷雾剂可以额外含有通常的推进剂(如氯氟代烃和挥发性的未被取代的烃类(如丁烷和丙烷))。
经皮贴剂具有提供将本发明的化合物至身体的受控递送的额外优势。这样的剂型可以通过将活性化合物溶解或分散在适当的介质中而制造。吸收增强剂也可以被用于增加化合物穿过皮肤的通量。这样的通量的速率可以通过提供速率控制膜或将化合物分散在聚合物基质或凝胶中被控制。
如本文所用,短语“肠胃外施用”和“肠胃外地施用”表示除肠和局部施用以外的施用模式,通常通过注射并且包括但不限于静脉内、眼内(如玻璃体内)、肌内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊膜下、蛛网膜下腔、脊柱内和胸骨内注射和输注。适合于肠胃外施用的药物组合物包含与一种或多种药学上可接受的无菌等渗水性或非水性溶液、分散体、混悬液或乳剂、或无菌粉剂(其可以在临使用前被重构为无菌可注射溶液或分散体)组合的一种或多种活性化合物,其可以含有抗氧化剂、缓冲剂、抑菌剂、溶质或悬浮剂或增稠剂,所述溶质使制剂与预期接受者的血液等渗。
可以被用在本发明的药物组合物中的适合的水性载体和非水性载体的实例包括水、乙醇、多元醇(如甘油、丙二醇、聚乙二醇等)及其适合的混合物、植物油(如橄榄油)和可注射的有机酯(如油酸乙酯)。可以被用在本发明的药物组合物中的适合的水性载体和非水性载体的实例包括水、乙醇、多元醇(如甘油、丙二醇、聚乙二醇等)及其适合的混合物、植物油(如橄榄油)和可注射的有机酯(如油酸乙酯)。例如,可以通过使用包衣材料(如卵磷脂)、在分散体的情况下通过保持所需的颗粒尺寸,以及通过使用表面活性剂,保持适当的流动性。例如,可以通过使用包衣材料(如卵磷脂)、在分散体的情况下通过保持所需的颗粒尺寸,以及通过使用表面活性剂,保持适当的流动性。
这些组合物还可以含有助剂(如防腐剂、润湿剂、乳化剂和分散剂)。可以通过包括各种抗细菌剂和抗真菌剂(例如,对羟苯甲酸甲酯、氯丁醇、苯酚山梨酸等),确保预防微生物的作用。将等渗剂(如糖、氯化钠等)包括在组合物内也可以是期望的。此外,可以通过包括延迟吸收的试剂(如单硬脂酸铝和明胶)引起可注射药物形式的延长吸收。
在一些情况下,为了延长药物的效果,期望的是减缓来自皮下注射或肌内注射的药物的吸收。这可以通过使用具有不良水溶性的结晶材料或无定形材料的液体悬浮液实现。药物的吸收速率则取决于其溶解速率,所述溶解速率进而可以取决于晶体尺寸和结晶形式。或者,肠胃外施用的药物形式的延迟的吸收通过将药物溶解或悬浮在油媒介物中实现。
通过在可生物降解的聚合物(如聚交酯-聚乙交酯)中形成主题化合物的微囊化的基质而制造可注射储库形式。根据药物与聚合物的比例以及采用的特定聚合物的性质,可以控制药物释放速率。其他可生物降解的聚合物的实例包括聚(原酸酯)和聚(酸酐)。也通过将药物截留在与身体组织相容的脂质体或微乳中制备储库可注射制剂。
为了用于本发明的方法中,可以给予活性化合物本身与或将其作为药物组合物给予,所述药物组合物含有例如0.1%至99.5%(更优选地,0.5%至90%)的活性成分与药学上可接受的载体的组合。
也可以通过可再充填的或可生物降解的装置提供引入方法。近年来,已经开发和体内测试了各种缓慢释放聚合物装置,以用于药物(包括蛋白质生物药剂)的控制递送。各种生物相容的聚合物(包括水凝胶)(包括可生物降解的聚合物和不可降解的聚合物两者)可以用于形成用于在特定靶标位点的化合物持续释放的植入物。
药物组合物中的活性成分的实际剂量水平可以变化,以获得活性成分的量,所述活性成分的量对实现对于特定患者、组合物和施用模式的期望的治疗响应是有效的,而对患者无毒。
选择的剂量水平将取决于各种因素,包括采用的特定化合物或化合物的组合、或其酯、盐或酰胺的活性,施用途径,施用时间,所采用的一种或多种特定化合物的排泄率,治疗持续时间,与所采用的一种或多种特定化合物组合使用的其他药物、化合物和/或材料,所治疗的患者的年龄、性别、体重、病况、总体健康状况和在先病史,以及医学领域中众所周知的类似因素。
本领域中具有普通技术的医师或兽医可以容易地确定和开具所需要的药物组合物的治疗有效的量。例如,医师或兽医可以起始于处于低于为实现期望的治疗效果所需要的水平的药物组合物或化合物的剂量,并且逐渐增加剂量直至实现期望的效果。“治疗有效的量”表示足以引起期望的治疗效果的化合物的浓度。通常理解,化合物的有效的量将根据主体的重量、性别、年龄和病史变化。影响有效的量的其他因素可以包括但不限于,患者病况的严重程度、所治疗的病症、化合物的稳定性、以及(如果需要)与本发明的化合物一起施用的另一类型的治疗剂。可以通过药剂的多次施用递送较大的总剂量。确定功效和剂量的方法是本领域技术人员已知的。参见例如isselbacher等人,(1996)harrison'sprinciplesofinternalmedicine,第13版,1814-1882。
通常,本发明的组合物和方法中使用的活性化合物的适合的日剂量将是对产生治疗效果有效的最低剂量的化合物的量。这样的有效剂量将通常取决于如上所述的因素。
如果需要,活性化合物的有效日剂量可以作为分开施用的一、二、三、四、五、六或更多的亚剂量,任选地以单位剂量形式,在全天以适当的时间间隔施用。在本发明的某些实施方案中,活性化合物可以每天施用两次或三次。在其他实施方案中,活性化合物将每天施用一次。
接受此治疗的患者是任何有需要的动物,包括灵长类动物(特别是人);和其他哺乳动物(如马、牛、猪、羊、猫和狗);家禽;以及通常的宠物。
在某些实施方案中,本发明的化合物可以单独使用或与另一类型的治疗剂联合施用。
本发明包括本发明的化合物的药学上可接受的盐在本发明的组合物和方法中的用途。在某些实施方案中,本发明的预期的盐包括但不限于烷基、二烷基、三烷基或四烷基铵盐。在某些实施方案中,本发明的预期的盐包括但不限于l-精氨酸、苯乙苄胺(benethamine)、苄星、甜菜碱、氢氧化钙、胆碱、二甲基乙醇胺、二乙醇胺、二乙胺、2-(二乙基氨基)乙醇、乙醇胺、乙二胺、n-甲葡糖胺、哈胺、1h-咪唑、锂、l-赖氨酸、镁、4-(2-羟乙基)吗啉、哌嗪、钾、1-(2-羟乙基)吡咯烷、钠、三乙醇胺、氨丁三醇和锌盐。在某些实施方案中,本发明的预期的盐包括但不限于na、ca、k、mg、zn或其他金属盐。在某些实施方案中,本发明的预期的盐包括但不限于1-羟基-2-萘甲酸、2,2-二氯乙酸、2-羟乙基磺酸、2-酮戊二酸、4-乙酰氨基苯甲酸、4-氨基水杨酸、乙酸、己二酸、l-抗坏血酸、l-天冬氨酸、苯磺酸、苯甲酸、(+)-樟脑酸、(+)-樟脑-10-磺酸、羊蜡酸(癸酸)、羊油酸(己酸)、羊脂酸(辛酸)、碳酸、肉桂酸、柠檬酸、环拉酸、十二烷基硫酸、乙烷-1,2-二磺酸、乙磺酸、甲酸、富马酸、半乳糖二酸、龙胆酸、d-葡庚糖酸、d-葡萄糖酸、d-葡萄糖醛酸、谷氨酸、戊二酸、甘油磷酸、乙醇酸、马尿酸、氢溴酸、盐酸、异丁酸、乳酸、乳糖酸、月桂酸、马来酸、l-苹果酸、丙二酸、扁桃酸、甲磺酸、萘-1,5-二磺酸、萘-2-磺酸、烟酸、硝酸、油酸、草酸、棕榈酸、双羟萘酸、磷酸、丙酸、l-焦谷氨酸、水杨酸、癸二酸、硬脂酸、琥珀酸、硫酸、l-酒石酸、硫氰酸、对甲苯磺酸、三氟乙酸和十一碳烯酸盐。
药学上可接受的酸加成盐也可以作为各种溶剂化物(如与水、甲醇、乙醇、二甲基甲酰胺等的溶剂化物)存在。也可以制备这样的溶剂化物的混合物。这样的溶剂化物的来源可以是来自结晶的溶剂、制备或结晶的溶剂中固有的或对于这样的溶剂是外来的。
润湿剂、乳化剂和润滑剂(如十二烷基硫酸钠和硬脂酸镁),以及着色剂、释放剂、包衣剂、甜味剂、风味剂和芳香剂、防腐剂和抗氧化剂也可以存在于组合物中。
药学上可接受的抗氧化剂的实例包括:(1)水溶性抗氧化剂(如抗坏血酸、盐酸半胱氨酸、硫酸氢钠、焦亚硫酸钠、亚硫酸钠等);(2)油溶性抗氧化剂(如抗坏血酸棕榈酸酯、叔丁基羟基茴香醚(bha)、丁基化羟基甲苯(bht)、卵磷脂、没食子酸丙酯、α-生育酚等);以及(3)金属-螯合剂(如柠檬酸、乙二胺四乙酸(edta)、山梨糖醇、酒石酸、磷酸等)。
chi3l1抗体
目前公开的数据表明,本发明的与人chi3l1结合的抗体可在用于检测主体中nafld或nash以及在主体肝脏中未治疗进展的后续并发症(例如肝硬化和/或hcc)的组合物和方法中使用。与结合人chi3l1的一些现有技术抗体不同,本发明的抗体可用于清楚地区分健康主体和患病主体,例如患有nafld/nash以及肝硬化和/或hcc的主体。在本发明之前,没有可靠的方法来准确地确定该蛋白质在具有nafld/nash的个体的血液中的存在。目前针对nafld/nash的唯一fda批准的治疗是改变生活方式,包括减重和运动。减肥手术是另一种激烈的减重方法,其也可用于治疗这种疾病,但他是侵入性的并且具有严重的并发症。很有可能在未来开发出更新的药物疗法。因此,本发明对于鉴定患有nafld/nash的个体并监测其对治疗的反应将是有价值的。他可能有助于预测长期结果,并作为衡量新药剂的治疗效果的有希望的终点。
因此,本发明提供了与人chi3l1结合的抗体(本文中为“ab1”或“ch568”),该抗体包含轻链和重链,其中轻链包含lcvr,且重链包含hcvr,其中lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1是seqidno:6,lcdr2是seqidno:7,lcdr3是seqidno:8,hcdr1是seqidno:3,hcdr2是seqidno:4,且hcdr3是seqidno:5。
在前一实施方案的一些方面,所述抗体包含轻链和重链,其中所述轻链包含lcvr且所述重链包含hcvr,其中所述lcvr包含氨基酸序列seqidno:10且所述hcvr包含氨基酸序列seqidno:9。
在前述实施方案的其他方面,抗体包含轻链和重链,其中轻链包含氨基酸序列seqidno:12且重链包含氨基酸序列seqidno:11。
在前述实施方案的更进一步的方面,抗体包含两条轻链和两条重链,其中每条轻链包含氨基酸序列seqidno:12且每条重链包含seqidno:11。
在前述实施方案的方面,抗体是igg型抗体。在其他方面,抗体包含κ轻链。在更进一步的方面,抗体是鼠抗体。
表1显示了ab1(ch568)的氨基酸序列。
表1
本发明进一步提供结合人chi3l1的抗体(本文中为“ab2”或“chxi3b6-6”),所述抗体包含轻链和重链,其中轻链包含lcvr且重链包含hcvr,其中lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1是seqidno:16,lcdr2是seqidno:17,lcdr3是seqidno:18,hcdr1是seqidno:13,hcdr2是seqidno:14,且hcdr3是seqidno:15。
在前述实施方案的一些方面,所述抗体包含轻链和重链,其中所述轻链包含lcvr且所述重链包含hcvr,其中所述lcvr包含氨基酸序列seqidno:20且所述hcvr包含氨基酸序列seqidno:19。
在前述实施方案的其他方面,抗体包含轻链和重链,其中轻链包含氨基酸序列seqidno:22,且重链包含氨基酸序列seqidno:21。
在前述实施方案的更进一步的方面,抗体包含两条轻链和两条重链,其中每条轻链包含氨基酸序列seqidno:22,并且每条重链包含seqidno:21。
在前述实施方案的方面,抗体是igg型抗体。在其他方面,抗体包含κ轻链。在更进一步的方面,抗体是鼠抗体。
表2显示了ab2(chxi3b6-6)的氨基酸序列。
表2
本发明还涉及编码本发明的上述抗体(例如,ab1和ab2)的多核苷酸。
在一些实施方案中,本发明提供了dna分子,其包含编码具有氨基酸序列seqidno:12的轻链多肽的多核苷酸序列。在一些实施方案中,提供dna分子,所述dna分子包含编码具有氨基酸序列seqidno:11的重链多肽的多核苷酸序列。
在一些实施方案中,本发明提供了编码本发明的抗体的多核苷酸,其中lcvr由seqidno:24编码且hcvr由seqidno:23编码。
在进一步的实施方案中,本发明提供了编码本发明的抗体的多核苷酸,其中轻链由seqidno:26编码且重链由seqidno:25编码。
表3显示了用于表达ab1(ch568)的dna序列。
表3
在一些实施方案中,本发明提供了dna分子,其包含编码具有氨基酸序列seqidno:22的轻链多肽的多核苷酸序列。在一些实施方案中,提供dna分子,所述dna分子包含编码具有氨基酸序列seqidno:21的重链多肽的多核苷酸序列。
在一些实施方案中,本发明提供了编码本发明的抗体的多核苷酸,其中lcvr由seqidno:28编码且hcvr由seqidno:27编码。
在进一步的实施方案中,本发明提供了编码本发明的抗体的多核苷酸,其中轻链由seqidno:30编码且重链由seqidno:29编码。
表4显示了表达ab2(chxi3b6-6)的dna序列。
表4
本发明的多核苷酸可以以rna的形式或以dna的形式,其中dna包括cdna和合成dna。dna可以是双链的或单链的。作为遗传密码冗余性或简并性的结果,编码本发明的抗体的编码序列可以变化。
编码本发明抗体的多核苷酸可包括以下:仅抗体的编码序列,抗体的编码序列和额外的编码序列例如前导序列或分泌序列或前蛋白序列;抗体的编码序列和非编码序列,例如内含子或蛋白质的编码序列的5'和/或3'的非编码序列。因此,术语"编码抗体的多核苷酸"涵盖这样的多核苷酸,其可包括不仅蛋白质的编码序列,还有包括额外的编码和/或非编码序列的多核苷酸。
在序列已可操作连接至表达控制序列之后,可以在宿主细胞中表达本发明的多核苷酸。表达载体通常可在宿主生物体中作为附加体或作为宿主染色体dna的整合部分而复制。通常,表达载体将含有选择标记物(例如四环素、新霉素和二氢叶酸还原酶),以允许检测用期望dna序列转化的那些细胞。
本发明还提供了包含dna分子的重组宿主细胞,所述dna分子包含编码或含有编码本发明抗体的多核苷酸序列的多核苷酸序列。
在一些实施方案中,重组宿主细胞包含dna分子,所述dna分子包含编码具有氨基酸序列seqidno:12的轻链多肽的多核苷酸序列且包含编码具有氨基酸序列seqidno:11的重链多肽的多核苷酸序列,所述细胞能够表达包含重链和轻链的抗体,其中重链的氨基酸序列是seqidno:11并且轻链的氨基酸序列是seqidno:12。
在其他实施方案中,重组宿主细胞包含dna分子,所述dna分子包含编码具有氨基酸序列seqidno:22的轻链多肽的多核苷酸序列且包含编码具有氨基酸序列seqidno:21的重链多肽的多核苷酸序列,所述细胞能够表达包含重链和轻链的抗体,其中重链的氨基酸序列是seqidno:21并且轻链的氨基酸序列是seqidno:22。
本发明的抗体可以容易地在以下中产生:哺乳动物细胞,例如但不限于cho、ns0、hek293或cos细胞;细菌细胞,例如但不限于大肠杆菌、枯草芽孢杆菌(bacillussubtilis)或荧光假单胞菌(pseudomonasfluorescence);或真菌或酵母细胞。使用本领域众所周知的技术培养宿主细胞。
可通过众所周知方法将含有目标多核苷酸序列(例如,编码抗体的多肽的多核苷酸和表达控制序列)的载体转移至宿主细胞中,所述方法根据细胞宿主的类型而变化。例如,氯化钙转化通常用于原核细胞,而磷酸钙处理或电穿孔可用于其他细胞宿主。
可以使用各种蛋白质纯化方法,且这些方法是本领域已知的,并描述于例如deutscher,methodsinenzymology182:83-89(1990)andscopes,proteinpurification:principlesandpractice,第三版,springer,ny(1994)。
本发明还提供了产生本发明的抗体的方法。
在一些实施方案中,提供了产生包含重链和轻链的与人chi3l1结合的抗体的方法,其中重链包含氨基酸序列seqidno:11,且轻链包含seqidno:12的氨基酸序列,所述方法包括以下步骤:(a)在使得表达所述抗体的条件下培养重组宿主细胞,所述重组宿主细胞包含编码由seqidno:11给出的多肽序列的第一多核苷酸序列和编码由seqidno:12给出的多肽序列的第二多核苷酸序列;和(b)从所述宿主细胞中回收表达的抗体。在一些实施方案中,提供了通过该方法产生的抗体。
在上文描述的方法的一个实施方案中,编码由seqidno:11给出的多肽序列的第一多核苷酸序列和编码由seqidno:12给出的多肽序列的第二多核苷酸序列是相同核酸分子的部分。
在一个实施方案中,本发明提供了通过前文提及的方法生产的抗体。
在进一步的实施方案中,通过前文提及的方法生产的抗体具有两条重链和两条轻链,其中每条重链的多肽序列是由seqidno:11给出,并且每条轻链的多肽序列是由seqidno:12给出。
在一些实施方案中,提供了产生包含重链和轻链的与人chi3l1结合的抗体的方法,其中重链包含氨基酸序列seqidno:21,且轻链包含seqidno:22的氨基酸序列,所述方法包括以下步骤:a)在使得表达所述抗体的条件下培养重组宿主细胞,所述重组宿主细胞包含编码由seqidno:21给出的多肽序列的第一多核苷酸序列和编码由seqidno:22给出的多肽序列的第二多核苷酸序列;和b)从所述宿主细胞中回收表达的抗体。在一些实施方案中,提供了通过该方法产生的抗体。
在上文描述的方法的一个实施方案中,编码由seqidno:21给出的多肽序列的第一多核苷酸序列和编码由seqidno:22给出的多肽序列的第二多核苷酸序列是相同核酸分子的部分。
在一个实施方案中,本发明提供了通过前文提及的方法生产的抗体。
在进一步的实施方案中,通过前文提及的方法生产的抗体具有两条重链和两条轻链,其中每条重链的多肽序列是由seqidno:21给出,并且每条轻链的多肽序列是由seqidno:22给出。
在本发明的一个实施方案中,以分离形式提供本文所公开的抗体或编码其的核酸。
在一些方面中,本发明的抗体是单克隆抗体。如本文所用,"单克隆抗体"或"mab"指来源于包括例如任何真核生物、原核生物或噬菌体克隆的单一拷贝或克隆的抗体,而不指其产生的方法。其单克隆抗体可以例如通过杂交瘤技术、重组技术、噬菌体展示技术、合成技术(例如cdr移植)或此类技术或本领域已知的其他技术的组合产生。
本发明的抗体(例如,如本文所述的ab1和ab2)的不同抗体和抗体片段(例如,单链抗体、fab和sfab片段、f(ab')2、fd片段、fv片段、scfv和结构域抗体(dab)片段)以及抗体模拟物,可以通过在可变区和恒定区序列内突变、缺失和/或插入而容易地产生,所述可变区和恒定区序列侧接本发明的抗体(例如,如本文所述的ab1和ab2)的特定cdr组。因此,例如,通过取代不同的重链,对于给定的一组cdr(例如,如本文所述的ab1和ab2的cdr),不同类别的本发明的抗体(例如,如本文所述的ab1和ab2)是可能的,由此,例如,可以产生igg1-4、igm、iga1-2、igd、ige抗体类型和同种型。类似地,本发明范围内的本发明的抗体(例如,如本文所述的ab1和ab2)的人工抗体可以通过在完整的合成框架内嵌入给定的一组cdr(例如,如本文所述的ab1和ab2的cdr)来产生。如本领域所知,术语“可变”在本文中用于描述抗体之间序列不同并用于每种特定抗体对其抗原的结合和特异性的可变结构域的某些部分。然而,如本领域已知的,可变性通常不均匀地分布在抗体的可变结构域中。他通常集中在轻链和重链可变结构域中称为互补决定区(“cdr”)或高变区的三个区段中。可变结构域的更高度保守的部分被称为框架(fr)。重链和轻链的可变结构域各自包含通过三个cdr连接的大多采用β-折叠构型的四个框架区,其形成连接并在一些情况下形成β-折叠结构的部分的环。每个链中的cdr通过fr区紧密靠近地保持在一起,并且来自另一条链的cdr有助于抗体的抗原结合位点的形成(eakabat等人,sequencesofproteinsofimmunologicalinterest,第五版,1991,nih)。恒定结构域不直接参与抗体结合抗原,但展示各种效应子功能,例如抗体参与抗体依赖性细胞毒性。
本发明还包括本说明书中描述的抗体(例如,如本文所述的ab1和ab2)的功能等同物。功能等同物具有与抗体的那些相当的结合特征,并且包括例如嵌合、人源化和单链抗体及其片段。产生这种功能等同物的方法公开在pct申请wo93/21319、欧洲专利申请号239,400;pct申请wo89/09622;欧洲专利申请338,745;和欧洲专利申请ep332,424,他们通过引用以其各自整体并入。在一些方面,功能等同物还包括具有与本发明抗体的可变区或高变区(称为“互补决定区”(“cdr”))的氨基酸序列基本上相同的氨基酸序列的多肽。如应用于氨基酸序列的“基本上相同”在本文中定义为与另一氨基酸序列具有至少约90%、91%、92%、94%、95%、96%、97%、98%、99%或其间的任何值或范围的序列同一性的序列,如通过例如根据pearson和lipman,proc.natl.acad.sci.usa85,2444-2448(1988)的fasta搜索方法所测定的。
嵌合抗体是免疫球蛋白分子,其特征在于来自不同动物物种的两个或更多个区段或部分。本发明的抗体(例如,如本文所述的ab1和ab2)的嵌合抗体优选具有基本上或完全源自人抗体恒定区的恒定区和基本上或完全源自本发明的抗体(例如,如本文所述的ab1和ab2)的可变区序列的可变区。通过将例如本发明的抗体(例如,如本文所述的ab1和ab2)的互补决定区取代到人框架结构域中来制备人源化形式的抗体,例如参见pct公开号w092/22653。除了基本上或完全源自相应的人抗体区的互补决定区(cdr)和基本上或完全源自除人以外的哺乳动物的cdr,人源化抗体优选具有恒定区和可变区。
本文公开的抗体(例如,如本文所述的ab1和ab2)的人源化抗体可以使用几种技术产生,例如表面重修和cdr移植。在表面重修技术中,组合分子建模、统计分析和诱变以调节可变区的非cdr表面以类似于靶宿主的已知抗体的表面。用于抗体的表面重修的策略和方法以及用于降低不同宿主内抗体的免疫原性的其他方法是本领域已知的,并且公开于例如美国专利号5,639,641,其以其整体通过引用并入本文。在cdr移植技术中,将鼠重链和轻链cdr(例如,如本文所述的ab1和ab2的重链和轻链cdr)移植到完全人框架序列中。
功能等同物还包括单链抗体片段,也称为单链抗体(scfv)。这些片段含有具有或不具有一个或多个互连接头的与抗体可变轻链序列(vl)的至少一个片段拴系的抗体可变重链氨基酸序列(vh)的至少一个片段。这样的接头可以是短的、柔性肽,其被选择以确保一旦(vl)和(vh)结构域连接,其正确的三维折叠就发生,从而保持整个抗体的靶分子结合特异性,从中衍生出单链抗体片段。通常,(vl)或(vh)序列的羧基末端可以通过这种肽接头共价连接到互补(vl)和(vh)序列的氨基酸末端。可以通过分子克隆、抗体噬菌体展示文库或类似技术产生单链抗体片段。这些蛋白质可以在真核细胞或原核细胞(包括细菌)中产生。
单链抗体片段含有具有本说明书中描述的完整抗体的至少一个可变区或互补决定区(cdr)的氨基酸序列,但缺少那些抗体的一些或所有恒定结构域。这些恒定结构域对于抗原结合不是必需的,但是构成完整抗体结构的主要部分。因此,单链抗体片段可以克服与使用含有部分或全部恒定结构域的抗体相关的一些问题。例如,单链抗体片段倾向于在生物分子和重链恒定区之间没有不希望的相互作用、或其他不想要的生物活性。另外,单链抗体片段比完整抗体小得多,因此可以具有比完整抗体更大的毛细管通透性,允许单链抗体片段更有效地定位和结合靶抗原结合位点。而且,抗体片段可以在原核细胞中以相对大的规模产生,从而促进他们的产生。此外,相对小尺寸的单链抗体片段使得他们在受体中引起免疫应答的可能性比完整抗体更低。
功能等同物还包括具有与完整抗体的那些相同或相当的结合特征的抗体的片段。此类片段可含有一个或两个fab片段或f(ab')2片段,并可进一步包括sfab片段、fd片段、fv片段和结构域抗体(dab)片段。在一些方面,抗体片段含有完整抗体的所有六个互补决定区,尽管含有少于所有这些区域(例如三个、四个或五个cdr)的片段也是有功能的。此外,功能等同物可以是或可以组合以下免疫球蛋白类别中的任何一种的成员:igg、igm、iga、igd或ige及其亚类。
在一些方面,本发明进一步提供本文公开的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)的缀合物。例如,抗体可以直接或通过可切割或不可切割的接头与治疗剂(例如但不限于细胞毒性药物、抗肿瘤剂或免疫肿瘤剂)共价连接,共价连接至本发明的抗体或功能等同物。细胞毒性药物的非限制性实例包括甲氨蝶呤、柔红霉素、多柔比星、长春新碱、长春碱、美法仑、丝裂霉素c、苯丁酸氮芥和卡利奇霉素。抗肿瘤剂的非限制性实例包括雷莫芦单抗、耐昔妥珠单抗、奥拉单抗(olaratumab)、galunisertib、abemaciclib、顺铂、卡铂、达卡巴嗪、脂质体多柔比星、多西他赛、环磷酰胺和多柔比星、诺维本、艾瑞布林、紫杉醇、用于可注射悬浮液的紫杉醇蛋白结合的颗粒、伊沙匹隆、卡培他滨、folfox(甲酰四氢叶酸、氟尿嘧啶和奥沙利铂)、folfiri(甲酰四氢叶酸、氟尿嘧啶和伊立替康)和西妥昔单抗。免疫肿瘤剂的非限制性实例包括纳武单抗、易普利姆玛、pidilizumab、帕博利珠单抗(pembrolizumab)、tremelimumab、乌瑞鲁单抗(urelumab)、利丽单抗(lirilumab)、阿特珠单抗(atezolizumab)和度伐单抗(durvalumab)。
在一些实施方案中,本文公开的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)被可检测地标记或能够产生可检测信号。本发明的此类抗体特别适合用于诊断应用和体内成像。可检测标记可包括例如光吸收染料、荧光染料或放射性标记。可检测标记、检测他们的方法以及将他们掺入试剂(例如,抗体和核酸探针)的方法是本领域熟知的。
在一些实施方案中,可检测标记可以包括可通过如下检测的标记:光谱方法、光化学方法、生物化学方法、免疫化学方法、电磁方法、放射化学方法或化学方法,例如荧光、化学荧光、或化学发光、或任何其他适当的方法。本文所述的方法中使用的可检测标记可以是一级标记(其中,标记包含可被直接检测的部分或产生可被直接检测部分的部分)或二级标记(其中,可检测标记结合至另一部分以产生可测定的信号,例如,如同在免疫标记中使用二抗和三抗一样常见)。可检测标记可通过共价或非共价的方法连接至本文公开的抗体。可选地,可检测标记可以例如通过直接标记这样的分子(所述分子通过配体-受体结合对布置(ligand-receptorbindingpairarrangement)来实现与本文公开的抗体的结合)或其他此类特异性识别分子而得以连接。可检测标记可以包括但不限于:放射性同位素、生物发光化合物、发色团、抗体、化学发光化合物、荧光化合物、金属螯合物和酶。
在其他实施方案中,将检测试剂用荧光化合物进行标记。当荧光标记的试剂暴露至适当波长的光时,其存在由于荧光随后可以被检测。在一些实施方案中,可检测标记可以是荧光染料分子或荧光团,其包括但不限于:荧光素、藻红蛋白、藻蓝蛋白、邻苯二醛、荧光胺、cy3tm、cy5tm、别藻蓝蛋白(allophycocyanine)、德克萨斯红、多甲藻黄素叶绿素(perideninchlorophyll)、青色素、串联缀合物如藻红蛋白-cy5tm、绿色荧光蛋白、罗丹明、异硫氰酸荧光素(fitc)和oregongreentm、罗丹明及衍生物(例如,德克萨斯红和四罗丹明异硫氰酸酯(tetrarhodimineisothiocynate,tritc))、生物素、藻红蛋白、amca、cydyestm、6-羧基荧光素(6-carboxyfhiorescein;通常已知缩写为fam和f)、6-羧基-2′,4′,7′,4,7-六氯荧光素(hex)、6-羧基-4′,5′-二氯-2′,7′-二甲氧基荧光素(joe或j)、n,n,n′,n′-四甲基-6羧基罗丹明(tamra或t)、6-羧基-x-罗丹明(rox或r)、5-羧基罗丹明-6g(r6g5或g5)、6-羧基罗丹明-6g(r6g6或g6)和罗丹明110;青色素染料,例如cy3、cy5和cy7染料;香豆素,例如伞形酮;苯甲亚胺染料,例如hoechst33258;菲啶染料,例如德克萨斯红;乙锭染料;吖啶染料;咔唑染料;吩噁嗪染料;卟啉染料;聚甲炔染料,例如青色素染料如cy3、cy5等;bodipy染料和喹啉染料。在一些实施方案中,可测定标记可以是放射性标记,包括但不限于:3h、125i、35s、14c、32p和33p。在一些实施方案中,可检测标记可以是酶,其包括但不限于:辣根过氧化物酶和碱性磷酸酶。酶标记可以产生例如化学发光信号、有色信号或荧光信号。考虑用于可检测地标记本文公开的抗体的酶包括但不限于:苹果酸脱氢酶、葡萄球菌核酸酶、δ-v-类固醇异构酶、酵母醇脱氢酶、α-甘油磷酸脱氢酶、磷酸丙糖异构酶、辣根过氧化物酶、碱性磷酸酶、天冬酰胺酶、葡萄糖氧化酶、β-半乳糖苷酶、核糖核酸酶、脲酶、过氧化氢酶、葡萄糖-vi-磷酸脱氢酶、葡萄糖淀粉酶和乙酰胆碱酯酶。在一些实施方案中,可检测标记是化学发光标记物,其包括但不限于:光泽精、鲁米诺、荧光素、异鲁米诺、theromatic吖啶酯、咪唑、吖啶盐和草酸酯。在一些实施方案中,可检测标记可以是光谱比色标记,其包括但不限于:胶体金或者有色玻璃或塑料(例如,聚苯乙烯、聚丙烯和乳胶)珠。
在一些实施方案中,本文公开的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)还可用可检测标签(例如c-myc、ha、vsv-g、hsv、flag、v5、his或生物素)进行标记。还可使用其他的检测系统,例如,生物素-链霉抗生物素蛋白系统。在这一系统中,本文公开的抗体可以是生物素化的。结合至生物标记物的生物素化的抗体的量使用链霉抗生物素蛋白-过氧化物酶缀合物和显色底物加以确定。此类链霉抗生物素蛋白过氧化物酶检测试剂盒是可商购得到的,例如,来自dako;carpinteria,calif。本文公开的抗体还可以使用荧光发射金属(例如152eu或镧系的其他金属)进行可检测地标记。可以使用金属螯合基团将这些金属连接至本文公开的抗体,所述金属螯合基团如二乙烯三胺五乙酸(dtpa)或乙二胺四乙酸(edta)。
本发明进一步提供药物组合物,其包含至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)和一种或多种药学上可接受的载体和/或稀释剂。可用作药学上可接受的载体的材料的一些实例包括:(1)糖,例如乳糖、葡萄糖和蔗糖;(2)淀粉,例如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,例如羧甲基纤维素钠、甲基纤维素、乙基纤维素、微晶纤维素和醋酸纤维素;(4)粉末黄蓍胶;(5)麦芽;(6)明胶;(7)润滑剂,例如硬脂酸镁、十二烷基硫酸钠和滑石;(8)赋形剂,例如可可脂和栓剂蜡;(9)油,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和豆油;(10)二醇类,例如丙二醇;(11)多元醇,例如甘油、山梨糖醇、甘露醇和聚乙二醇;(12)酯类,例如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,例如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)ph缓冲溶液;(21)聚酯类、聚碳酸酯类和/或聚酸酐类;(22)填充剂,例如多肽和氨基酸;(23)血清组分,例如血清白蛋白、hdl和ldl;(22)c2-c12醇类,例如乙醇;和(23)药物制剂中使用的其他无毒的相容物质。润湿剂、着色剂、脱模剂、包衣剂、甜味剂、增味剂、芳香剂、防腐剂和抗氧化剂也可以存在于制剂中。术语例如“赋形剂”、“载体”、“药学上可接受的载体”等在本文中可互换使用。
药物组合物可以特别配制成以固体、液体或凝胶形式施用,其包括适合于以下的那些:(1)口服施用,例如,灌液(drenches)(水性或非水性溶液或悬浮液)、锭剂、糖衣丸、胶囊、丸剂、片剂(例如,用于口腔、舌下和全身吸收的那些)、大丸剂、散剂、颗粒剂、施加于舌头的糊剂;(2)肠胃外施用,例如,通过皮下、肌内、静脉内或硬膜外注射,例如作为无菌溶液或悬浮液或缓释制剂;(3)局部应用,例如,作为霜剂、软膏剂或施用于皮肤的控释贴剂或喷雾剂;(4)阴道内或直肠内,例如,作为阴道药栓、霜剂或泡沫剂;(5)舌下;(6)眼部;(7)经皮;(8)经粘膜;或(9)经鼻。另外,可将本文所述的化合物植入患者体内或使用药物递送系统注射。参见,例如,urquhart等人,ann.rev.pharmacol.toxicol.24:199-236(1984);lewis,编辑“controlledreleaseofpesticidesandpharmaceuticals”(plenumpress,newyork,1981);美国专利号3,773,919;和美国专利号353,270,960。剂型的实例包括但不限于:片剂;囊片;胶囊,例如硬明胶胶囊和软弹性明胶胶囊;扁囊剂(cachets);糖锭;锭剂;分散剂;栓剂;软膏剂;泥罨剂(cataplasms)(泥敷剂);糊剂;散剂;敷料;霜剂;膏药;溶液;贴剂;气溶胶(例如鼻喷雾剂或吸入器);凝胶;液体如悬浮液(例如水性或非水性液体悬浮液、水包油乳液或油包水液体乳液)、溶液和酏剂;和无菌固体(例如,结晶或无定形固体),其可以重构以提供液体剂型。
肠胃外剂型可以通过各种途径施用于患者,其包括但不限于皮下、静脉内(包括推注)、肌内和动脉内。由于肠胃外剂型的施用通常绕过患者对污染物的天然防御,因此胃肠外剂型优选是无菌的或能够在施用于患者之前进行灭菌。肠胃外剂型的实例包括但不限于注射即用型溶液、准备溶解或悬浮于药学上可接受的注射用媒介物中的干燥产品、注射即用型悬浮液、以及乳液。此外,可以制备控释胃肠外剂型用于施用于患者,其包括但不限于施用duros®型剂型和剂量倾卸(dose-dumping)。
可用于提供本发明抗体的肠胃外剂型的合适的媒介物是本领域技术人员熟知的。实例包括但不限于:无菌水;注射用水usp;生理盐水;葡萄糖溶液;水性媒介物,例如但不限于氯化钠注射液、林格氏注射液、右旋糖注射液、右旋糖和氯化钠注射液、以及乳酸林格氏注射液(lactatedringer'sinjection);水溶性的媒介物,例如但不限于乙醇、聚乙二醇和丙二醇;和非水性媒介物,例如但不限于玉米油、棉籽油、花生油、芝麻油、油酸乙酯、肉豆蔻酸异丙酯和苯甲酸苄酯。
药物组合物可以任何剂量或给药方案施用。关于本发明的治疗方法,并不旨在施用限于特定的施用方式、剂量或给药频率。
本发明的药物组合物可以通过本领域已知的任何适当途径施用,其包括但不限于口服或肠胃外途径,包括静脉内、肌内、皮下、透皮、气道(气溶胶)、肺、鼻、直肠和局部(包括口腔和舌下)施用。
在一个实施方案中,可能期望将药物组合物局部施用于需要治疗的区域;这可以通过以下实现,例如但不限于手术期间的局部输注、局部施用,例如通过注射,借助于导管(例如,心导管、肾导管、肝内导管等),或者借助于植入物,所述植入物是多孔的、无孔的或凝胶状的材料,包括膜,例如硅橡胶膜、纤维或商业皮肤替代物。在一些实施方案中,对于可通过注射接近的某些软组织钙化部位,可能期望注射至钙化部位中或其附近。
在一些实施方案中,药物组合物可以口服施用至主体(例如,在胶囊、悬浮液或片剂中)或通过肠胃外施用。口服施用的常规方法包括以下任何一种;片剂、悬浮液、溶液、乳液、胶囊、散剂、糖浆剂等是可用的。肠胃外施用可包括例如肌内、静脉内、关节内、动脉内、鞘内、皮下或腹膜内施用。药物组合物还可以口服、经皮、局部、通过吸入(例如,支气管内、鼻内、经口吸入或鼻内滴剂)或直肠施用。
当肠胃外施用药物组合物时,通常将其配制成单位剂量可注射形式(例如,溶液、悬浮液、乳液)。适合用于注射的药物制剂包括无菌水溶液或分散液和用于重构为无菌可注射溶液或分散液的无菌粉末。所述载体可以是溶剂或分散介质,其含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇)、其合适的混合物和植物油。如本文所用的术语“剂量单位”形式是指适合作为待治疗主体的单位剂量的物理离散单位;每个单位含有预定量的活性化合物,其经计算以产生与所需药物载体相关的期望的治疗效果。
可以以单剂量或多剂量向患者施用有效量、例如治疗有效剂量的本文公开的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)。当施用多剂量时,剂量可以彼此分开例如,1小时、3小时、6小时、8小时、1天、2天、1周、2周或1个月。例如,包含本文公开的化合物的组合物可以施用例如2、3、4、5、6、7、8、10、15、20或更多周。要理解的是,对于任何具体主体,应当根据个体需要以及施用组合物或监督施用组合物的人员的专业判断来随时间调整具体的剂量方案。例如,如果较低剂量不能提供足够的治疗活性,可以增加治疗剂的剂量。
在一些实施方案中,本文公开的药物组合物的有效量可以是使chi3l1表达水平降低、稳定或至少以比预期在没有接受所述药物组合物的主体中的增加更低的速率增加的量。在一些实施方案中,有效量可以是使主体中存在的chi3l1多肽的量降低统计学显著的量的量。在一些实施方案中,本文公开的药物组合物的有效量可以是降低chi3l1多肽活性的量。在一些实施方案中,chi3l1抑制剂的有效量可以是使nai降低至少5%、至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%或至少90%的量。
例如,医生可以首先开具相对低的剂量,随后增加剂量直至获得适当的反应。施用于患者的剂量足以随时间影响患者的有益治疗反应,或者例如,取决于应用,足以减轻症状或其他适当的活性。剂量取决于具体制剂的功效,所施用组合物的活性、稳定性或血清半衰期,和患者的病况,待治疗的软组织钙化的具体状况,以及体重或体表面积。剂量的大小还取决于具体主体中伴随具体制剂的施用的任何不良副作用的存在、性质和程度等。根据本领域众所周知的方法,任选地在一种或多种适当的体外和/或体内疾病动物模型中测试治疗组合物,并且为本领域普通技术人员所知,以确认功效、组织代谢并估计剂量。具体地,在相关测定中,剂量最初可以通过活性、稳定性或治疗与未治疗的其他合适的量度(例如,比较治疗的与未治疗的细胞或动物模型)来确定。将制剂以由相关制剂的ld50和/或药物组合物在各种浓度下的任何副作用的观察结果来确定的速率(例如,当应用于患者的质量和总体健康时)施用。
剂量可以由本领域技术人员确定,并且在任何并发症的情况下也可以由个别医师调整。通常,包含本文公开的抗体的组合物的剂量范围可以为0.001mg/kg体重至5g/kg体重。在一些实施方案中,剂量范围为0.001mg/kg体重至1g/kg体重、0.001mg/kg体重至0.5g/kg体重、0.001mg/kg体重至0.1g/kg体重、0.001mg/kg体重至50mg/kg体重、0.001mg/kg体重至25mg/kg体重、0.001mg/kg体重至10mg/kg体重、0.001mg/kg体重至5mg/kg体重、0.001mg/kg体重至1mg/kg体重、0.001mg/kg体重至0.1mg/kg体重、或0.001mg/kg体重至0.005mg/kg体重。可选地,在一些实施方案中,剂量范围为0.1g/kg体重至5g/kg体重、0.5g/kg体重至5g/kg体重、1g/kg体重至5g/kg体重、1.5g/kg体重到5g/kg体重、2g/kg体重到5g/kg体重、2.5g/kg体重到5g/kg体重、3g/kg体重至5g/kg体重、3.5g/kg体重至5g/kg体重、4g/kg体重至5g/kg体重、或4.5g/kg体重至5g/kg体重。可以从衍生自体外或动物模型测试生物测定或系统的剂量-反应曲线推算有效剂量。剂量不应太大以至于引起不可接受的不良副作用。
在一些实施方案中,提供了治疗主体中nafld和/或nash的方法,所述方法包括向主体施用治疗有效量的至少一种本发明的结合人chi3l1的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)。在一些方面,提供了治疗主体中肝硬化的方法,所述方法包括向主体施用治疗有效量的至少一种本发明的结合人chi3l1的抗体。在一些方面,提供了治疗主体中的hcc的方法,所述方法包括向主体施用治疗有效量的至少一种本发明的结合人chi3l1的抗体。
在用于治疗nafld和/或nash、肝硬化和/或hcc的方法的另一个实施方案中,所述方法包括如先前所述,与一种或多种细胞毒性剂、抗肿瘤剂或免疫肿瘤剂同时、分开或顺序组合地施用有效量的至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)。
在一些实施方案中,本文公开的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)可以用于各种测定和技术,包括免疫测定。此类测定和技术包括但不限于使用技术诸如蛋白质印迹、放射免疫测定(ria)、elisa(酶联免疫吸附测定)、“夹心”免疫测定、免疫沉淀测定、免疫扩散测定、凝集测定(例如胶乳凝集)、补体固定测定、免疫放射测定、荧光免疫测定、例如fia(荧光连接免疫测定)、化学发光免疫测定(clia)、电化学发光免疫测定(eclia)、计数免疫测定(cia)、侧向流动测试或免疫测定(lfia)、磁免疫测定(mia)、蛋白a免疫测定、免疫组织化学技术、免疫细胞化学技术、电泳技术(包括sds-page电泳、2dsds-page电泳)的竞争性和非竞争性测定系统。进行此类测定的方法是本领域已知的。在一些实施方案中,免疫测定可以是定量或半定量免疫测定、免疫组织化学技术、免疫细胞化学技术、电泳技术(包括sds-page电泳、2dsds-page电泳)。
在各种实施方案中,使用本发明的抗体(例如,如本文所公开的ab1和ab2,包括其功能等同物),公开了高度特异性的基于单克隆的双位点免疫测定,其可以清楚地区分健康主体和患病主体,诸如患有nafld/nash以及肝硬化和/或hcc的那些主体。
在各种实施方案中,提供了测定,该测定包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将样品与至少一种本发明的抗体(例如,如本文所公开的ab1和ab2,包括其功能等同物)孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将主体鉴定为具有nafld或nash;或(b)如果chi3l1的水平等于或低于参考水平,则将主体鉴定为不具有nafld或nash。在一些方面,将样品与本发明的至少一种抗体孵育包括在具有权利要求1-4中任一项的固定化抗体的制品中将样品与权利要求11-14中任一项的抗体孵育。在一些方面,参考水平为约2.0ng/30μl血清。在一些方面,当chi3l1的水平高于参考水平时,所述测定还包括提供适于治疗nafld或nash的治疗。在一些方面,治疗包括施用chi3l1抑制剂。在一些方面,chi3l1抑制剂包含至少一种本发明的结合人chi3l1的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)。
在各种实施方案中,提供测定,所述测定包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与至少一种本发明的抗体(例如,如本文所公开的ab1和ab2,包括其功能等同物)孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将主体鉴定为具有肝硬化;或(b)如果chi3l1的水平等于或低于参考水平,则将主体鉴定为不具有肝硬化。在一些方面,将样品与本发明的至少一种抗体孵育包括在具有权利要求1-4中任一项的固定化抗体的制品中将样品与权利要求11-14中任一项的抗体孵育。在一些方面,参考水平为约60ng/ml、约61ng/ml、约62ng/ml、约63ng/ml、约64ng/ml、约65ng/ml、约66ng/ml、约67ng/ml、约68ng/ml、约69ng/ml、约70ng/ml、约71ng/ml、约72ng/ml、约73ng/ml、约74ng/ml、约75ng/ml、或其间的任何值或范围。在一些方面,参考水平为约2.0ng/30μl。在一些方面,当chi3l1的水平高于参考水平时,该测定还包括提供适合于治疗肝硬化的治疗。在一些方面,治疗包括施用chi3l1抑制剂。在一些方面,chi3l1抑制剂包含至少一种本发明的结合人chi3l1的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)。
在一些实施方案中,提供测定,所述测定包括:(i)在从主体获得的样品中测量chi3l1水平,其中所述测量包括将所述样品与至少一种本发明的抗体(例如,如本文所公开的ab1和ab2,包括其功能等同物)孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于参考水平,则将主体鉴定为具有hcc;或(b)如果chi3l1的水平等于或低于参考水平,则将主体鉴定为不具有hcc。在一些方面,将样品与本发明的至少一种抗体孵育包括在具有权利要求1-4中任一项的固定化抗体的制品中将样品与权利要求11-14中任一项的抗体孵育。在一些方面,参考水平为约2ng/30μl。在一些方面,当chi3l1的水平高于参考水平时,该测定还包括提供适合于治疗hcc的治疗。在一些方面,治疗包括施用chi3l1抑制剂。在一些方面,chi3l1抑制剂包含至少一种本发明的结合人chi3l1的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)。
在一些实施方案中,提供了监测患有nafld或nash的主体中的治疗进展的方法,该方法包括:(i)在第一时间点测量从主体获得的第一样品中的chi3l1的第一水平,其中所述测量包括将样品与至少一种本发明的抗体(例如,如本文所公开的ab1和ab2,包括其功能等同物)孵育;(ii)给主体施用用于治疗nafld或nash的治疗剂;和(iii)在第二时间点测量从主体获得的第二样品中的chi3l1的第二水平,其中所述测量包括将所述样品与至少一种本发明的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)孵育/在具有权利要求1-4中任一项的固定化抗体的制品中将样品与权利要求11-14中任一项的抗体孵育,其中第二时间点晚于第一时间点并且在所述施用之后,且其中如果第二水平显着低于第一水平,则认为治疗有效。在一些方面,在第一时间点测量chi3l1的第一水平和/或在第二时间点测量chi3l1的第二水平包括在具有权利要求1-4中任一项的固定化抗体的制品中将样品与权利要求11-14中任一项的抗体孵育。在一些方面,治疗剂是chi3l1抑制剂。在一些方面,chi3l1抑制剂包含至少一种本发明的结合人chi3l1的抗体(例如,如本文中公开的ab1和ab2,包括其功能等同物)。应当理解,上述方法还可以用于不仅监测主体中具有nafld和/或nash的主体中的治疗进展,还监测主体肝脏中未治疗进展的后续并发症,诸如肝硬化和/或hcc。
本发明进一步提供了用于执行本文所述的任何方法和/或测定的试剂盒,包括nafld和/或nash的诊断和/或治疗(以及主体肝脏中未治疗进展的后续并发症,例如肝硬化和/或hcc)。在一些实施方案中,试剂盒可包含至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)。试剂盒是包含至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)的任何制品(例如,包装或容器),其用于特异性检测例如chi3l1表达产物或其片段,所述制品作为用于执行本文所述方法或测定的单元被推销,分发或出售。
在一些实施方案中,本文描述了用于检测样品中chi3l1表达产物的试剂盒,所述试剂盒包含至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物),其在固体支持物上特异性结合chi3l1表达产物。至少一种本发明的抗体可任选地包含可检测标记。本文描述的试剂盒包括允许测定从主体获得的样品(例如,从主体获得的生物样品)中chi3l1表达产物水平的试剂和/或组分。本文描述的试剂盒可任选地包含可用于执行本文所述方法和测定的额外组分。
试剂盒可以进一步包含用于浓缩样品(例如血清样品)中的表达产物(例如,多肽)的装置和/或试剂。因此,也可以包括允许例如蛋白质浓缩的超滤装置作为试剂盒组分。
优选地,与本文公开的方法和测定一起使用的诊断或预后试剂盒含有chi3l1表达产物的检测试剂。除了至少一种本发明的抗体(例如,如本文公开的ab1和ab2,包括其功能等同物)和可能的其他chi3l1特异性试剂,此类检测试剂还包含例如,缓冲溶液、标记物或洗涤液等。此外,试剂盒可包含一定量的已知核酸和/或多肽,其可用于校准试剂盒或作为内部对照。用于检测表达产物的诊断试剂盒还可以包含辅助成分,如第二亲和配体,例如第二抗体、检测染料和执行本领域技术人员已知的表达产物检测方法所需的任何其他合适的化合物或液体。这些成分是本领域技术人员已知的,并且可以根据所进行的检测方法而变化。另外,试剂盒可以包含说明书散页和/或可以提供关于所获得的结果的相关性的信息。
本公开的主题的另外的特征和优点将在下文的详细描述中阐述,并且其在一定程度上对于本领域技术人员而言通过所述描述而容易得以明确,或通过实施包括下文的详细描述、权利要求以及附图的如本文描述的本公开的主题而被认识到。
应当理解前述的一般性描述和随后的详细描述呈现了本公开的主题的实施方案,并且意在提供用于理解要求保护的本公开的主题的性质和特征的概述或框架。包括附图以提供对本公开的主题的进一步的理解,并且附图被并入本说明书并构成本说明书的一部分。附图示出了本发明主题的各种实施方案,并且与说明书一起用于解释本公开的主题的原理和操作。另外,附图和说明书仅仅是说明性的,并且不意图以任何方式限制权利要求的范围。
此外,本发明还涉及以下方案:
方案1.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且所述hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1由氨基酸序列seqidno:6组成,lcdr2由氨基酸序列seqidno:7组成,lcdr3由氨基酸序列seqidno:8组成,hcdr1由氨基酸序列seqidno:3组成,hcdr2由氨基酸序列seqidno:4组成,且hcdr3由氨基酸序列seqidno:5组成。
方案2.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含氨基酸序列seqidno:10,且所述hcvr包含氨基酸序列seqidno:9。
方案3.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含氨基酸序列seqidno:12,且所述重链包含氨基酸序列seqidno:11。
方案4.结合人chi3l1的抗体,所述抗体包含两条轻链和两条重链,其中每条轻链包含氨基酸序列seqidno:12,且每条重链包含seqidno:11。
方案5.dna分子,所述dna分子包含编码具有氨基酸序列seqidno:12的轻链多肽的多核苷酸序列。
方案6.dna分子,所述dna分子包含编码具有氨基酸序列seqidno:11的重链多肽的多核苷酸序列。
方案7.重组宿主细胞,所述重组宿主细胞包含方案5的dna分子和方案6的dna分子,所述细胞能够表达包含重链和轻链的抗体,其中所述重链的氨基酸序列是seqidno:11,且所述轻链的氨基酸序列是seqidno:12。
方案8.用于生产包含重链和轻链的结合人chi3l1的抗体的方法,其中所述重链包含氨基酸序列seqidno:11,且所述轻链包含seqidno:12的氨基酸序列,所述方法包括以下步骤:a)在使得表达所述抗体的条件下培养方案7的重组宿主细胞;和b)从所述宿主细胞回收表达的抗体。
方案9.通过方案8的方法生产的抗体。
方案10.药物组合物,所述药物组合物包含方案1-4中任一项的抗体和一种或多种药学上可接受的载体、稀释剂或赋形剂。
方案11.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含互补决定区lcdr1、lcdr2和lcdr3,且所述hcvr包含互补决定区hcdr1、hcdr2和hcdr3,其中lcdr1由氨基酸序列seqidno:16组成,lcdr2由氨基酸序列seqidno:17组成,lcdr3由氨基酸序列seqidno:18组成,hcdr1由氨基酸序列seqidno:13组成,hcdr2由氨基酸序列seqidno:14组成,且hcdr3由氨基酸序列seqidno:15组成。
方案12.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含轻链可变区(lcvr),且所述重链包含重链可变区(hcvr),其中所述lcvr包含氨基酸序列seqidno:20,且所述hcvr包含氨基酸序列seqidno:19。
方案13.结合人chi3l1的抗体,所述抗体包含轻链和重链,其中所述轻链包含氨基酸序列seqidno:22,且所述重链包含氨基酸序列seqidno:21。
方案14.结合人chi3l1的抗体,所述抗体包含两条轻链和两条重链,其中每条轻链包含氨基酸序列seqidno:22,且每条重链包含seqidno:21。
方案15.dna分子,所述dna分子包含编码具有氨基酸序列seqidno:22的轻链多肽的多核苷酸序列。
方案16.dna分子,所述dna分子包含编码具有氨基酸序列seqidno:21的重链多肽的多核苷酸序列。
方案17.重组宿主细胞,所述重组宿主细胞包含方案15的dna分子和方案16的dna分子,所述细胞能够表达包含重链和轻链的抗体,其中所述重链的氨基酸序列是seqidno:21,且所述轻链的氨基酸序列是seqidno:22。
方案18.用于生产包含重链和轻链的结合人chi3l1的抗体的方法,其中所述重链包含氨基酸序列seqidno:21,且所述轻链包含seqidno:22的氨基酸序列,所述方法包括以下步骤:a)在使得表达所述抗体的条件下培养方案7的重组宿主细胞;和b)从所述宿主细胞回收表达的抗体。
方案19.通过方案18的方法生产的抗体。
方案20.药物组合物,所述药物组合物包含方案11-14中任一项的抗体和一种或多种药学上可接受的载体、稀释剂或赋形剂。
方案21.测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与方案11-14中任一项的抗体在具有固定化的方案1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于所述参考水平,则将所述主体鉴定为具有nafld(非酒精性脂肪肝病)或nash(非酒精性脂肪性肝炎);或(b)如果chi3l1的水平等于或低于所述参考水平,则将所述主体鉴定为不具有nafld或nash。
方案22.方案21的测定法,其中所述生物样品是血清,且所述参考水平是约2.0ngchi3l1/30μl血清。
方案23.方案21-22中任一项的测定法,其中当chi3l1的水平高于所述参考水平时,所述测定法进一步包括提供适于治疗nafld或nash的治疗。
方案24.方案23的测定法,其中所述治疗包括施用chi3l1抑制剂。
方案25.方案24的测定法,其中所述chi3l1抑制剂包含方案1-4、11-14中任一项的抗体。
方案26.测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与方案11-14中任一项的抗体在具有固定化的方案1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于所述参考水平,则将所述主体鉴定为具有肝硬化;或(b)如果chi3l1的水平等于或低于所述参考水平,则将所述主体鉴定为不具有肝硬化。
方案27.方案25的测定法,其中所述生物样品是血清,且所述参考水平是约2.0ngchi3l1/30μl血清。
方案28.方案25-26中任一项的测定法,其中当chi3l1的水平高于所述参考水平时,所述测定法进一步包括提供适于治疗肝硬化的治疗。
方案29.方案28的测定法,其中所述治疗包括施用chi3l1抑制剂。
方案30.方案29的测定法,其中所述chi3l1抑制剂包含方案1-4、11-14中任一项的抗体。
方案31.测定法,所述测定法包括:(i)在从主体获得的样品中测量chi3l1的水平,其中所述测量包括将所述样品与方案11-14中任一项的抗体在具有固定化的方案1-4中任一项的抗体的物品中一起孵育;(ii)将chi3l1的水平与参考水平进行比较;和(iii)(a)如果chi3l1的水平高于所述参考水平,则将所述主体鉴定为具有肝细胞癌(hcc);或(b)如果chi3l1的水平等于或低于所述参考水平,则将所述主体鉴定为不具有hcc。
方案32.方案31的测定法,其中所述生物样品是血清,且所述参考水平是约2.0ngchi3l1/30μl血清。
方案33.方案31-32中任一项的测定法,其中当chi3l1的水平高于所述参考水平时,所述测定法进一步包括提供适于治疗hcc的治疗。
方案34.方案33的测定法,其中所述治疗包括施用chi3l1抑制剂。
方案35.方案34的测定法,其中所述chi3l1抑制剂包含方案1-4、11-14中任一项的抗体。
方案36.监测具有nafld或nash的主体中的治疗进展的方法,所述方法包括:(i)在第一时间点测量从主体获得的第一样品中的chi3l1的第一水平,其中所述测量包括将所述样品与方案11-14中任一项的抗体在具有固定化的方案1-4中任一项的抗体的物品中一起孵育;(ii)向所述主体施用用于治疗nafld或nash的治疗剂;和(iii)在第二时间点测量从主体获得的第二样品中的chi3l1的第二水平,其中所述测量包括将所述样品与方案11-14中任一项的抗体在具有固定化的方案1-4中任一项的抗体的物品中一起孵育,其中所述第二时间点晚于所述第一时间点并且在所述施用之后,且其中如果所述第二水平显著低于所述第一水平,则认为所述治疗是有效的。
方案37.方案36的方法,其中所述治疗剂是chi3l1抑制剂。
方案38.方案37的方法,其中所述chi3l1抑制剂包含方案1-4、11-14中任一项的抗体。
方案39.治疗主体中的nafld或nash的方法,所述方法包括将治疗有效量的方案1-4、11-14中任一项的抗体施用于所述主体。
方案40.治疗主体中的肝硬化的方法,所述方法包括将治疗有效量的方案1-4、11-14中任一项的抗体施用于所述主体。
方案41.治疗主体中的hcc的方法,所述方法包括将治疗有效量的方案1-4、11-14中任一项的抗体施用于所述主体。
实施例
现在对本发明进行了一般描述,其通过参考以下的实施例将更容易理解,包括所述实施例仅仅是为了举例说明本发明的某些方面和实施方案的目的,并且不意图限制本发明。
实施例1ch3l1单克隆抗体的产生
将编码chi3l1蛋白的cdna克隆到具有his-标签的表达载体中并转染到细菌中。制备细胞裂解物,澄清并如图1所示在镍(ni)柱上纯化人chi3l1蛋白。用pbs洗脱后纯化chi3l1蛋白,并通过酶消化除去his-标签。最终纯化的chi3l1蛋白用于免疫小鼠。该蛋白质不具有免疫原性,并且需要在不同浓度下用完全和不完全弗氏佐剂进行多次免疫,以产生几种igg和igm抗chi3l1单克隆抗体。优选的免疫方法是首先用50%生理盐水和50%完全弗氏佐剂中的10μg重组chi3l1蛋白腹膜内(ip)免疫小鼠,总注射体积为0.5ml。至少六周后,小鼠接受在50%盐水和50%不完全弗氏佐剂中的10μgchi3l1蛋白的ip加强免疫,总体积为250μl。在融合程序前三天,小鼠接受在生理盐水中的10μgchi3l1蛋白的另外的静脉内加强,总体积为100μl。优选的融合程序如下:使小鼠安乐死并移除脾。将脾用针解离到dulbecco氏改良的eagle培养基(dmem)中,并收集悬浮的细胞。第二细胞系是在含有20%胎牛血清的dmem中悬浮生长的sp2/0-ag14小鼠骨髓瘤细胞。收获在20mm×10cm培养皿中生长的完全汇合细胞。在三次单独洗涤后,将两种细胞悬浮液合并。在室温下以1000rpm离心5分钟后,将沉淀细胞与1ml60%聚乙二醇在37℃下融合6分钟。融合后,将细胞铺板,并且随后用hat(次黄嘌呤、氨基蝶呤和胸苷)培养基选择。使用elisa测定测试在选择中存活的细胞是否存在抗体,所述elisa测定使用包被有chi3l1蛋白的96孔板。维持该抗体阳性的克隆并进行稀释克隆。克隆后,维持、表征阳性细胞系/杂交瘤,并最终保存在液氮中。将杂交瘤克隆×2(两次)并注射至未引发(pristineprimed)的balb-c小鼠中以产生腹水(腹腔中的异常积聚液),如之前所述(nambotin,s.b.,等人functionalconsequencesofwnt3/frizzled7-mediatedsignalinginnon-transformedhepaticcells.oncogenesis1,e31(2012),通过引用整体并入本文)。
抗体的生长和纯化如下:将确定分泌目标抗体的细胞系扩增,并通过腹水法产生相应的抗体。向小鼠腹膜内注射0.5ml的姥鲛烷。7天后,腹膜内注射0.5mldmem中的400万个杂交瘤细胞。约10天后,使小鼠安乐死并从腹部收集腹水,在室温下以1000rpm离心5分钟,并收集含有抗体的上清液。使用商业试剂盒对抗体进行同种型分型。使用hitrap蛋白g柱从腹水中纯化目标igg。腹水在上样缓冲液中以1:20稀释,用0.45μmmce(混合纤维素酯)膜过滤,并且随后在中性ph下上样到柱上。在酸性ph下洗脱抗体,立即中和,然后用2×生理盐水透析。通过bca测定确定蛋白质浓度,通过page凝胶电泳确定纯度水平。
实施例2针对ch3l1的单克隆抗体的测序
按照trizol®reagent(ambion,目录号:15596-026)的技术手册从杂交瘤细胞(实施例1中描述)中分离总rna。随后按照primescripttm1ststrandcdnasynthesiskit(takara,目录号:6110a)的技术手册,使用同种型特异性反义引物或通用引物将总rna反转录为cdna。根据genscript的cdna末端快速扩增(race)的标准操作程序(sop)扩增vh、vl、ch和cl的抗体片段。将扩增的抗体片段分别克隆到标准克隆载体中。执行菌落pcr以筛选具有正确大小的插入物的克隆。对于每个片段,对不少于5个具有正确大小的插入物的菌落进行测序。比对不同克隆的序列并提供共有序列。
实施例3血清检测的elisa测定的建立
如图2所示,在elisa测定形式中表征其对chi3l1蛋白的免疫反应性之后,将纯化的免疫球蛋白在任何应用之前储存在-80℃。在2位点测定中测试igg和igm抗体的性能。将ab1(也称为“ch568”)与固相支持物(96孔聚苯乙烯板)结合,并且将检测抗体ab2(也称为“chxi3b-6”)使用标准和完善的程序进行生物素标记,这使得6个分子的生物素与一个分子的ab2相连。这种基于mab的2位点测定(每种抗体识别chi3l1蛋白上的不同且分开的表位)的操作特征以测定样品之间的系数变量小于10%来确定。如图3中所示,由该测定构建的标准曲线显示出在2-50ng/30μl血清的浓度范围内的线性关系,且r2值为0.99387。测定设计和性能的详细方法如下:
chi3l1的基于单克隆抗体的双位点测定
1.使用来自corning或nunc的标准高结合免疫测定板,将ab1(ch568)以在0.2m碳酸钠-碳酸氢钠缓冲液(ph9.4)中3μg/ml的浓度包被在板上。然后每孔施加100μl抗体溶液并使其在室温(rt)下静置过夜。
2.包被后,将板用tris缓冲盐水(tbs)+0.05%tween20洗涤两次。
3.将板在37℃用315μl封闭缓冲液tbs+2%w/v牛血清白蛋白(bsa)孵育2小时。
4.封闭后,将板洗涤五次,并且随后装载样品。测定缓冲液是tbs(ph7.2)+1%bsa。将标准曲线在测定缓冲液+30%胎牛血清中孵育。将含有样品的平板在37℃孵育2小时。
5.随后将板用洗涤缓冲液洗涤5次,并将3μg/ml生物素化的ab2(chxi3b6-6)溶液在37℃孵育1.5小时。
6.洗涤板,并且随后用1:5000稀释的tbs/1%bsa中的链霉抗生物素蛋白-过氧化物酶在37℃下孵育45分钟。
7.将孔洗涤5次并用tmb底物显色。
在30分钟后用2.0nh2so4终止反应,并在分光光度计上在450nm下读板。
实施例4elisa测定
执行基于单克隆抗体的双位点elisa测定以检测来源自正常和nafld/nash个体的血清样品中的chi3l1蛋白,并评估与nash患者中的血清中肝酶水平、肝组织学以及纤维化的存在和程度的相关性。
在个体签署知情同意书后,分析他们的血液和肝脏活检材料的丙氨酸转氨酶(alt)和天冬氨酸转氨酶(ast)水平以检测肝损伤。肝脏活检组织用于确定nash活动评分(nas),如通过脂肪变性程度、炎症等级、肝细胞中气球样变性的存在以及肝纤维化的存在和程度测量的,如之前所述(promrat,k.,等人randomizedcontrolledtrialtestingtheeffectsofweightlossonnonalcoholicsteatohepatitis.hepatology51,121-129(2010),以其整体通过引用并入本文)。
表5表明男性和女性都受这种疾病影响,并且几乎所有个体都超重或肥胖,如分别通过bmi大于25或30所定义的。如在27名患有nafld/nash的个体中测量的,血清中chi3l1的水平范围为2.2至58.6ng/30μl血清样品。此外,如通过血液中alt和ast水平升高所测量的,93%的患者(23/25)表现出肝脏损害的迹象。如通过肝脏病理学所确定的,nash活动评分(nas)范围为中度至重度。更重要的是,该elisa测定中的大多数阳性个体具有晚期纤维化和甚至肝硬化,如通过纤维化评分为4或更高所确定的。因此,这种基于单克隆抗体的双位点测定能够通过定量血液中的chi3l1蛋白来鉴定肝脏中的中度至重度nash疾病。与之相比,如表6所示,研究的大多数正常个体在他们的血液中没有可检测的chi3l1蛋白,除了值得注意的一个个体(#18)。可以预料,由于美国一般人群中nafld的高患病率,以前被认为是“正常”的一些个体可能具有nash并且在该测定中变得具有反应性。
表5显示来源自患有nafld/nash的个体的血清中的chi3l1水平。
表5
表6显示来源自正常献血者和志愿者的血清中的chi3l1水平。
表6
实施例5临床样品中测量的chi3l1蛋白水平。
在来源自正常对照(nc)、乳腺癌(bc)、非酒精性脂肪肝病/非酒精性脂肪性肝炎(nafld/nash)、肝硬化(lc)和肝细胞癌(hcc)的临床样本中测试了用于检测chi3l1蛋白的基于单克隆抗体的双位点elisa测定。众所周知,患有nash的个体可能发展为lc和hcc,这是这种进行性肝病的可怕的并发症。出乎意料的是,基于单克隆抗体的双位点测定也检测出患有lc和hcc的患者,这表明独特的三重测定不仅可以检测原发性疾病nafld和/或nash,还可以检测后续并发症诸如lc和hcc。先前未在任何基于单克隆抗体的双位点测定中观察到该发现。在该背景下,图4证实了这些研究的结果并详述了以ng/孔(100μl)测量的chi3l1蛋白的绝对浓度。注意,与其他组相比,患有nash的个体中该蛋白质的值非常高,这可能表明该疾病在这些个体中发展迅速。在“正常”献血者群体中,阳性率仅为4.55%;并且乳腺癌的阳性率相似,为4.76%,这可能表明nafld/nash在一般人群中的背景患病率。与之相比,来源自nash个体的20.5%的血清样品对该蛋白是高度阳性的,并且25%的lc个体在该测定中也是反应性的。最后,在hcc中存在极高的阳性率,其为70.83%(图5)。因此,该测定具有检测原发性疾病(nafld/nash)和肝脏中未治疗进展的后续并发症(lc和hcc)的独特特征。
上文说明书中提及的所有出版物和专利通过引用并入本文。对于本领域技术人员显而易见的是,在不脱离本发明的精神和范围的情况下可以对本发明的技术进行各种修改和变化。虽然本发明已结合具体的优选实施方案进行描述,但应当理解,所要求保护的本发明不应被不适当地限于这些具体实施方案。由于本领域技术人员可以想到并入本发明的技术的精神和实质的所公开的实施方案的修改、组合、子组合和变化,因此本发明的技术应该被解释为包括所附权利要求范围内的所有内容及其等同方案。
序列表
<110>rhodeislandhospital
wands,jackr.
carlson,rolfi.
<120>用于检测和/或治疗nafld/nash以及肝脏中未治疗进展的后续并发症的抗chi3l1抗体
<130>405002-502p01us
<160>30
<170>patentinversion3.5
<210>1
<211>383
<212>prt
<213>智人
<400>1
metglyvallysalaserglnthrglyphevalvalleuvalleuleu
151015
glncyscysseralatyrlysleuvalcystyrtyrthrsertrpser
202530
glntyrarggluglyaspglysercyspheproaspalaleuasparg
354045
pheleucysthrhisileiletyrserphealaasnileserasnasp
505560
hisileaspthrtrpglutrpasnaspvalthrleutyrglymetleu
65707580
asnthrleulysasnargasnproasnleulysthrleuleuserval
859095
glyglytrpasnpheglyserglnargpheserlysilealaserasn
100105110
thrglnserargargthrpheilelysservalpropropheleuarg
115120125
thrhisglypheaspglyleuaspleualatrpleutyrproglyarg
130135140
argasplysglnhisphethrthrleuilelysglumetlysalaglu
145150155160
pheilelysglualaglnproglylyslysglnleuleuleuserala
165170175
alaleuseralaglylysvalthrileaspsersertyraspileala
180185190
lysileserglnhisleuasppheileserilemetthrtyraspphe
195200205
hisglyalatrpargglythrthrglyhishisserproleuphearg
210215220
glyglngluaspalaserproaspargpheserasnthrasptyrala
225230235240
valglytyrmetleuargleuglyalaproalaserlysleuvalmet
245250255
glyileprothrpheglyargserphethrleualasersergluthr
260265270
glyvalglyalaproileserglyproglyileproglyargphethr
275280285
lysglualaglythrleualatyrtyrgluilecysasppheleuarg
290295300
glyalathrvalhisargileleuglyglnglnvalprotyralathr
305310315320
lysglyasnglntrpvalglytyraspaspglngluservallysser
325330335
lysvalglntyrleulysaspargglnleualaglyalametvaltrp
340345350
alaleuaspleuaspasppheglnglyserphecysglyglnaspleu
355360365
argpheproleuthrasnalailelysaspalaleualaalathr
370375380
<210>2
<211>1867
<212>dna
<213>智人
<400>2
cacatagctcagttcccataaaagggctggtttgccgcgtcggggagtggagtgggacag60
gtatataaaggaagtacagggcctggggaagaggccctgtctaggtagctggcaccagga120
gccgtgggcaagggaagaggccacaccctgccctgctctgctgcagccagaatgggtgtg180
aaggcgtctcaaacaggctttgtggtcctggtgctgctccagtgctgctctgcatacaaa240
ctggtctgctactacaccagctggtcccagtaccgggaaggcgatgggagctgcttccca300
gatgcccttgaccgcttcctctgtacccacatcatctacagctttgccaatataagcaac360
gatcacatcgacacctgggagtggaatgatgtgacgctctacggcatgctcaacacactc420
aagaacaggaaccccaacctgaagactctcttgtctgtcggaggatggaactttgggtct480
caaagattttccaagatagcctccaacacccagagtcgccggactttcatcaagtcagta540
ccgccatttctgcgcacccatggctttgatgggctggaccttgcctggctctaccctgga600
cggagagacaaacagcattttaccaccctaatcaaggaaatgaaggccgaatttataaag660
gaagcccagccagggaaaaagcagctcctgctcagcgcagcactgtctgcggggaaggtc720
accattgacagcagctatgacattgccaagatatcccaacacctggatttcattagcatc780
atgacctacgattttcatggagcctggcgtgggaccacaggccatcacagtcccctgttc840
cgaggtcaggaggatgcaagtcctgacagattcagcaacactgactatgctgtggggtac900
atgttgaggctgggggctcctgccagtaagctggtgatgggcatccccaccttcgggagg960
agcttcactctggcttcttctgagactggtgttggagccccaatctcaggaccgggaatt1020
ccaggccggttcaccaaggaggcagggacccttgcctactatgagatctgtgacttcctc1080
cgcggagccacagtccatagaatcctcggccagcaggtcccctatgccaccaagggcaac1140
cagtgggtaggatacgacgaccaggaaagcgtcaaaagcaaggtgcagtacctgaaggac1200
aggcagctggcgggcgccatggtatgggccctggacctggatgacttccagggctccttc1260
tgcggccaggatctgcgcttccctctcaccaatgccatcaaggatgcactcgctgcaacg1320
tagccctctgttctgcacacagcacgggggccaaggatgccccgtccccctctggctcca1380
gctggccgggagcctgatcacctgccctgctgagtcccaggctgagcctcagtctccctc1440
ccttggggcctatgcagaggtccacaacacacagatttgagctcagccctggtgggcaga1500
gaggtagggatggggctgtggggatagtgaggcatcgcaatgtaagactcgggattagta1560
cacacttgttgattaatggaaatgtttacagatccccaagcctggcaagggaatttcttc1620
aactccctgccccccagccctccttatcaaaggacaccattttggcaagctctatcacca1680
aggagccaaacatcctacaagacacagtgaccatactaattataccccctgcaaagccca1740
gcttgaaaccttcacttaggaacgtaatcgtgtcccctatcctacttccccttcctaatt1800
ccacagctgctcaataaagtacaagagcttaacagtgaaaaaaaaaaaaaaaaaaaaaaa1860
aaaaaaa1867
<210>3
<211>5
<212>prt
<213>小家鼠
<400>3
sertyrasnmethis
15
<210>4
<211>17
<212>prt
<213>小家鼠
<400>4
leuileserproglyasnglyaspthrsertyrasnglnlysphelys
151015
gly
<210>5
<211>14
<212>prt
<213>小家鼠
<400>5
glyglyprothrvalvalalahistyrtyralametasptyr
1510
<210>6
<211>10
<212>prt
<213>小家鼠
<400>6
seralaserserargvalsertyrmethis
1510
<210>7
<211>7
<212>prt
<213>小家鼠
<400>7
aspthrserasnleualaser
15
<210>8
<211>9
<212>prt
<213>小家鼠
<400>8
glnglntrpserserasnproleuthr
15
<210>9
<211>123
<212>prt
<213>小家鼠
<400>9
glnvalglnleuglnglnthrglyalagluleuvallysproglyala
151015
servallysmetsercyslysalaserglytyrthrphethrsertyr
202530
asnmethistrpleulysglnthrproglyglnglyleuglutrpile
354045
glyleuileserproglyasnglyaspthrsertyrasnglnlysphe
505560
lysglylysalathrleuthralaasplysserserasnthralatyr
65707580
metglnleuserserleuthrsergluaspseralavaltyrphecys
859095
alaargglyglyprothrvalvalalahistyrtyralametasptyr
100105110
trpglyglnglythrservalthrvalserser
115120
<210>10
<211>106
<212>prt
<213>小家鼠
<400>10
glnilevalleuthrglnserproalailemetseralaserprogly
151015
gluargvalthrmetthrcysseralaserserargvalsertyrmet
202530
histrptyrglnglnlysserglythrserprolysargtrpiletyr
354045
aspthrserasnleualaserglyvalproalaargpheserglyser
505560
glyserglythrsertyrserleuthrileserthrmetglualaglu
65707580
aspalaalathrtyrtyrcysglnglntrpserserasnproleuthr
859095
pheglyalaglythrlysleugluleulys
100105
<210>11
<211>447
<212>prt
<213>小家鼠
<400>11
glnvalglnleuglnglnthrglyalagluleuvallysproglyala
151015
servallysmetsercyslysalaserglytyrthrphethrsertyr
202530
asnmethistrpleulysglnthrproglyglnglyleuglutrpile
354045
glyleuileserproglyasnglyaspthrsertyrasnglnlysphe
505560
lysglylysalathrleuthralaasplysserserasnthralatyr
65707580
metglnleuserserleuthrsergluaspseralavaltyrphecys
859095
alaargglyglyprothrvalvalalahistyrtyralametasptyr
100105110
trpglyglnglythrservalthrvalserseralalysthrthrpro
115120125
proservaltyrproleualaproglyseralaalaglnthrasnser
130135140
metvalthrleuglycysleuvallysglytyrpheprogluproval
145150155160
thrvalthrtrpasnserglyserleuserserglyvalhisthrphe
165170175
proalavalleuglnseraspleutyrthrleuserserservalthr
180185190
valproserserthrtrpprosergluthrvalthrcysasnvalala
195200205
hisproalaserserthrlysvalasplyslysilevalproargasp
210215220
cysglycyslysprocysilecysthrvalprogluvalserserval
225230235240
pheilepheproprolysprolysaspvalleuthrilethrleuthr
245250255
prolysvalthrcysvalvalvalaspileserlysaspaspproglu
260265270
valglnphesertrpphevalaspaspvalgluvalhisthralagln
275280285
thrglnproargglugluglnpheasnserthrpheargservalser
290295300
gluleuproilemethisglnasptrpleuasnglylysgluphelys
305310315320
cysargvalasnseralaalapheproalaproileglulysthrile
325330335
serlysthrlysglyargprolysalaproglnvaltyrthrilepro
340345350
proprolysgluglnmetalalysasplysvalserleuthrcysmet
355360365
ilethraspphepheprogluaspilethrvalglutrpglntrpasn
370375380
glyglnproalagluasntyrlysasnthrglnproilemetaspthr
385390395400
aspglysertyrphevaltyrserlysleuasnvalglnlysserasn
405410415
trpglualaglyasnthrphethrcysservalleuhisgluglyleu
420425430
hisasnhishisthrglulysserleuserhisserproglylys
435440445
<210>12
<211>213
<212>prt
<213>小家鼠
<400>12
glnilevalleuthrglnserproalailemetseralaserprogly
151015
gluargvalthrmetthrcysseralaserserargvalsertyrmet
202530
histrptyrglnglnlysserglythrserprolysargtrpiletyr
354045
aspthrserasnleualaserglyvalproalaargpheserglyser
505560
glyserglythrsertyrserleuthrileserthrmetglualaglu
65707580
aspalaalathrtyrtyrcysglnglntrpserserasnproleuthr
859095
pheglyalaglythrlysleugluleulysargalaaspalaalapro
100105110
thrvalserilepheproprosersergluglnleuthrserglygly
115120125
alaservalvalcyspheleuasnasnphetyrprolysaspileasn
130135140
vallystrplysileaspglysergluargglnasnglyvalleuasn
145150155160
sertrpthraspglnaspserlysaspserthrtyrsermetserser
165170175
thrleuthrleuthrlysaspglutyrgluarghisasnsertyrthr
180185190
cysglualathrhislysthrserthrserproilevallysserphe
195200205
asnargasnglucys
210
<210>13
<211>5
<212>prt
<213>小家鼠
<400>13
asptyrsermethis
15
<210>14
<211>17
<212>prt
<213>小家鼠
<400>14
trpileasnthrgluthrglygluprothrtyralaaspaspphelys
151015
gly
<210>15
<211>10
<212>prt
<213>小家鼠
<400>15
glutyrglyasntyrgluglyphevaltyr
1510
<210>16
<211>15
<212>prt
<213>小家鼠
<400>16
argalaserlysservalserthrserglytyrsertyrmethis
151015
<210>17
<211>7
<212>prt
<213>小家鼠
<400>17
leualaserasnleugluser
15
<210>18
<211>9
<212>prt
<213>小家鼠
<400>18
glnhisserarggluleuprotrpthr
15
<210>19
<211>119
<212>prt
<213>小家鼠
<400>19
glnileglnleuvalglnserglyprogluleulyslysproglyglu
151015
thrvallysilesercyslysalaserglytyrthrphethrasptyr
202530
sermethistrpvallysglnthrproglylysglyleulystrpmet
354045
valtrpileasnthrgluthrglygluprothrtyralaaspaspphe
505560
lysglyargphealapheserleugluthrseralaserthralatyr
65707580
leuglnileasnasnleulysasngluaspthralathrtyrphecys
859095
alaargglutyrglyasntyrgluglyphevaltyrtrpglyglngly
100105110
thrleuvalthrvalserala
115
<210>20
<211>111
<212>prt
<213>小家鼠
<400>20
aspilevalleuthrglnserproalaserleualavalserleugly
151015
glnargalathrilesercysargalaserlysservalserthrser
202530
glytyrsertyrmethistrptyrglnglnlysproglyglnpropro
354045
lysleuleuiletyrleualaserasnleugluserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuasnilehis
65707580
provalgluglugluaspalaalathrtyrtyrcysglnhisserarg
859095
gluleuprotrpthrpheglyglyglythrlysleugluilelys
100105110
<210>21
<211>443
<212>prt
<213>小家鼠
<400>21
glnileglnleuvalglnserglyprogluleulyslysproglyglu
151015
thrvallysilesercyslysalaserglytyrthrphethrasptyr
202530
sermethistrpvallysglnthrproglylysglyleulystrpmet
354045
valtrpileasnthrgluthrglygluprothrtyralaaspaspphe
505560
lysglyargphealapheserleugluthrseralaserthralatyr
65707580
leuglnileasnasnleulysasngluaspthralathrtyrphecys
859095
alaargglutyrglyasntyrgluglyphevaltyrtrpglyglngly
100105110
thrleuvalthrvalseralaalalysthrthrproproservaltyr
115120125
proleualaproglyseralaalaglnthrasnsermetvalthrleu
130135140
glycysleuvallysglytyrpheprogluprovalthrvalthrtrp
145150155160
asnserglyserleuserserglyvalhisthrpheproalavalleu
165170175
glnseraspleutyrthrleuserserservalthrvalproserser
180185190
thrtrpprosergluthrvalthrcysasnvalalahisproalaser
195200205
serthrlysvalasplyslysilevalproargaspcysglycyslys
210215220
procysilecysthrvalprogluvalserservalpheilephepro
225230235240
prolysprolysaspvalleuthrilethrleuthrprolysvalthr
245250255
cysvalvalvalaspileserlysaspaspprogluvalglnpheser
260265270
trpphevalaspaspvalgluvalhisthralaglnthrglnproarg
275280285
glugluglnpheasnserthrpheargservalsergluleuproile
290295300
methisglnasptrpleuasnglylysgluphelyscysargvalasn
305310315320
seralaalapheproalaproileglulysthrileserlysthrlys
325330335
glyargprolysalaproglnvaltyrthrileproproprolysglu
340345350
glnmetalalysasplysvalserleuthrcysmetilethraspphe
355360365
pheprogluaspilethrvalglutrpglntrpasnglyglnproala
370375380
gluasntyrlysasnthrglnproilemetaspthraspglysertyr
385390395400
phevaltyrserlysleuasnvalglnlysserasntrpglualagly
405410415
asnthrphethrcysservalleuhisgluglyleuhisasnhishis
420425430
thrglulysserleuserhisserproglylys
435440
<210>22
<211>218
<212>prt
<213>小家鼠
<400>22
aspilevalleuthrglnserproalaserleualavalserleugly
151015
glnargalathrilesercysargalaserlysservalserthrser
202530
glytyrsertyrmethistrptyrglnglnlysproglyglnpropro
354045
lysleuleuiletyrleualaserasnleugluserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuasnilehis
65707580
provalgluglugluaspalaalathrtyrtyrcysglnhisserarg
859095
gluleuprotrpthrpheglyglyglythrlysleugluilelysarg
100105110
alaaspalaalaprothrvalserilepheproproserserglugln
115120125
leuthrserglyglyalaservalvalcyspheleuasnasnphetyr
130135140
prolysaspileasnvallystrplysileaspglysergluarggln
145150155160
asnglyvalleuasnsertrpthraspglnaspserlysaspserthr
165170175
tyrsermetserserthrleuthrleuthrlysaspglutyrgluarg
180185190
hisasnsertyrthrcysglualathrhislysthrserthrserpro
195200205
ilevallysserpheasnargasnglucys
210215
<210>23
<211>369
<212>dna
<213>小家鼠
<400>23
caggtgcaactgcagcagactggggctgagctggtgaagcctggggcctcagtgaagatg60
tcctgcaaggcttctggctacacatttaccagttacaatatgcactggctaaagcagaca120
cctggacagggcctggaatggattggacttatttctccaggaaatggtgatacttcctac180
aatcagaagttcaaaggcaaggccacattgactgcagacaaatcctccaacacagcctac240
atgcagctcagtagcctgacatctgaggactctgcggtctatttctgtgcaagagggggg300
cctacggtagtagcccattactatgctatggactactggggtcagggaacctcagtcacc360
gtctcctca369
<210>24
<211>318
<212>dna
<213>小家鼠
<400>24
caaattgttctcacccagtctccagcaatcatgtctgcatctccaggggagagggtcacc60
atgacctgcagtgccagctcacgtgtaagttacatgcactggtaccagcagaagtcaggc120
acctcccccaaaagatggatttatgacacatccaacctggcttctggagtccctgctcgc180
ttcagtggcagtgggtctgggacctcttactctctcacaatcagcaccatggaggctgaa240
gatgctgccacttattactgccagcagtggagtagtaacccgctcacgttcggtgctggg300
accaagctggagctgaaa318
<210>25
<211>1341
<212>dna
<213>小家鼠
<400>25
caggtgcaactgcagcagactggggctgagctggtgaagcctggggcctcagtgaagatg60
tcctgcaaggcttctggctacacatttaccagttacaatatgcactggctaaagcagaca120
cctggacagggcctggaatggattggacttatttctccaggaaatggtgatacttcctac180
aatcagaagttcaaaggcaaggccacattgactgcagacaaatcctccaacacagcctac240
atgcagctcagtagcctgacatctgaggactctgcggtctatttctgtgcaagagggggg300
cctacggtagtagcccattactatgctatggactactggggtcagggaacctcagtcacc360
gtctcctcagccaaaacgacacccccatctgtctatccactggcccctggatctgctgcc420
caaactaactccatggtgaccctgggatgcctggtcaagggctatttccctgagccagtg480
acagtgacctggaactctggatccctgtccagcggtgtgcacaccttcccagctgtcctg540
cagtctgacctctacactctgagcagctcagtgactgtcccctccagcacctggcccagc600
gagaccgtcacctgcaacgttgcccacccggccagcagcaccaaggtggacaagaaaatt660
gtgcccagggattgtggttgtaagccttgcatatgtacagtcccagaagtatcatctgtc720
ttcatcttccccccaaagcccaaggatgtgctcaccattactctgactcctaaggtcacg780
tgtgttgtggtagacatcagcaaggatgatcccgaggtccagttcagctggtttgtagat840
gatgtggaggtgcacacagctcagacgcaaccccgggaggagcagttcaacagcactttc900
cgctcagtcagtgaacttcccatcatgcaccaggactggctcaatggcaaggagttcaaa960
tgcagggtcaacagtgcagctttccctgcccccatcgagaaaaccatctccaaaaccaaa1020
ggcagaccgaaggctccacaggtgtacaccattccacctcccaaggagcagatggccaag1080
gataaagtcagtctgacctgcatgataacagacttcttccctgaagacattactgtggag1140
tggcagtggaatgggcagccagcggagaactacaagaacactcagcccatcatggacaca1200
gatggctcttacttcgtctacagcaagctcaatgtgcagaagagcaactgggaggcagga1260
aatactttcacctgctctgtgttacatgagggcctgcacaaccaccatactgagaagagc1320
ctctcccactctcctggtaaa1341
<210>26
<211>639
<212>dna
<213>小家鼠
<400>26
caaattgttctcacccagtctccagcaatcatgtctgcatctccaggggagagggtcacc60
atgacctgcagtgccagctcacgtgtaagttacatgcactggtaccagcagaagtcaggc120
acctcccccaaaagatggatttatgacacatccaacctggcttctggagtccctgctcgc180
ttcagtggcagtgggtctgggacctcttactctctcacaatcagcaccatggaggctgaa240
gatgctgccacttattactgccagcagtggagtagtaacccgctcacgttcggtgctggg300
accaagctggagctgaaacgggctgatgctgcaccaactgtatccatcttcccaccatcc360
agtgagcagttaacatctggaggtgcctcagtcgtgtgcttcttgaacaacttctacccc420
aaagacatcaatgtcaagtggaagattgatggcagtgaacgacaaaatggcgtcctgaac480
agttggactgatcaggacagcaaagacagcacctacagcatgagcagcaccctcacgttg540
accaaggacgagtatgaacgacataacagctatacctgtgaggccactcacaagacatca600
acttcacccattgtcaagagcttcaacaggaatgagtgt639
<210>27
<211>357
<212>dna
<213>小家鼠
<400>27
cagatccagttggtgcagtctggacctgagctgaagaagcctggagagacagtcaagatc60
tcctgcaaggcttctggttataccttcacagactattcaatgcactgggtgaaacagact120
ccaggaaagggtttaaagtggatggtctggataaacactgagactggtgagccaacatat180
gcagatgacttcaagggacggtttgccttctctttggaaacctctgccagcaccgcctat240
ttgcagatcaacaacctcaaaaatgaggacacggctacatatttctgtgctagagagtat300
ggaaactacgaggggtttgtttactggggccaagggactctggtcactgtctctgca357
<210>28
<211>333
<212>dna
<213>小家鼠
<400>28
gacattgtgctgacacagtctcctgcttccttagctgtatctctggggcagagggccacc60
atctcatgcagggccagcaaaagtgtcagtacatctggctatagttatatgcactggtac120
caacagaaaccaggacagccacccaaactcctcatctatcttgcatccaacctagaatct180
ggggtccctgccaggttcagtggcagtgggtctgggacagacttcaccctcaacatccat240
cctgtggaggaggaggatgctgcaacctattactgtcagcacagtagggagcttccgtgg300
acgttcggtggaggcaccaagctggaaatcaaa333
<210>29
<211>1329
<212>dna
<213>小家鼠
<400>29
cagatccagttggtgcagtctggacctgagctgaagaagcctggagagacagtcaagatc60
tcctgcaaggcttctggttataccttcacagactattcaatgcactgggtgaaacagact120
ccaggaaagggtttaaagtggatggtctggataaacactgagactggtgagccaacatat180
gcagatgacttcaagggacggtttgccttctctttggaaacctctgccagcaccgcctat240
ttgcagatcaacaacctcaaaaatgaggacacggctacatatttctgtgctagagagtat300
ggaaactacgaggggtttgtttactggggccaagggactctggtcactgtctctgcagcc360
aaaacgacacccccatctgtctatccactggcccctggatctgctgcccaaactaactcc420
atggtgaccctgggatgcctggtcaagggctatttccctgagccagtgacagtgacctgg480
aactctggatccctgtccagcggtgtgcacaccttcccagctgtcctgcagtctgacctc540
tacactctgagcagctcagtgactgtcccctccagcacctggcccagcgagaccgtcacc600
tgcaacgttgcccacccggccagcagcaccaaggtggacaagaaaattgtgcccagggat660
tgtggttgtaagccttgcatatgtacagtcccagaagtatcatctgtcttcatcttcccc720
ccaaagcccaaggatgtgctcaccattactctgactcctaaggtcacgtgtgttgtggta780
gacatcagcaaggatgatcccgaggtccagttcagctggtttgtagatgatgtggaggtg840
cacacagctcagacgcaaccccgggaggagcagttcaacagcactttccgctcagtcagt900
gaacttcccatcatgcaccaggactggctcaatggcaaggagttcaaatgcagggtcaac960
agtgcagctttccctgcccccatcgagaaaaccatctccaaaaccaaaggcagaccgaag1020
gctccacaggtgtacaccattccacctcccaaggagcagatggccaaggataaagtcagt1080
ctgacctgcatgataacagacttcttccctgaagacattactgtggagtggcagtggaat1140
gggcagccagcggagaactacaagaacactcagcccatcatggacacagatggctcttac1200
ttcgtctacagcaagctcaatgtgcagaagagcaactgggaggcaggaaatactttcacc1260
tgctctgtgttacatgagggcctgcacaaccaccatactgagaagagcctctcccactct1320
cctggtaaa1329
<210>30
<211>654
<212>dna
<213>小家鼠
<400>30
gacattgtgctgacacagtctcctgcttccttagctgtatctctggggcagagggccacc60
atctcatgcagggccagcaaaagtgtcagtacatctggctatagttatatgcactggtac120
caacagaaaccaggacagccacccaaactcctcatctatcttgcatccaacctagaatct180
ggggtccctgccaggttcagtggcagtgggtctgggacagacttcaccctcaacatccat240
cctgtggaggaggaggatgctgcaacctattactgtcagcacagtagggagcttccgtgg300
acgttcggtggaggcaccaagctggaaatcaaacgggctgatgctgcaccaactgtatcc360
atcttcccaccatccagtgagcagttaacatctggaggtgcctcagtcgtgtgcttcttg420
aacaacttctaccccaaagacatcaatgtcaagtggaagattgatggcagtgaacgacaa480
aatggcgtcctgaacagttggactgatcaggacagcaaagacagcacctacagcatgagc540
agcaccctcacgttgaccaaggacgagtatgaacgacataacagctatacctgtgaggcc600
actcacaagacatcaacttcacccattgtcaagagcttcaacaggaatgagtgt654
- 还没有人留言评论。精彩留言会获得点赞!